1.本发明涉及药品、保健食品和食品领域,具体的,涉及一种化合物在用于制备具有改善脉络丛作用的药物的应用。
背景技术:
2.脑室系统的脉络丛最外层被一层室管膜上皮所覆盖,称之为脉络丛上皮,具有物质转运和分泌功能,中心部位是一组毛细血管网组织结构,在其周围被疏松的结缔组织所包绕着。侧脑室脉络丛,是产生脑脊液的主要场所,约占其总量的80%
‑
85%;脉络丛也是血
‑
脑脊液屏障的主要部位;亦是许多脑脊液中生物活性成分(甚至免疫细胞)合成和运输的重要脑室结构。脉络丛可分泌多种生长因子、神经营养因子和酶,进入脑脊液参与神经活动的调节:包括通过积极调节脑脊液和脑实质间的化学物质交换,维持大脑的细胞外环境、检测大脑的化学和免疫状态、使大脑解毒、分泌多肽的营养池、参与创伤后的修复过程。脉络丛在中枢神经系统的生长和发育、维持脑内环境的相对稳定、神经再生和修复中,可能发挥重要作用。
3.脉络丛结构和功能发生病理改变,会直接影响脑脊液的产生,进而造成脑脊液循环障碍,进一步导致颅内高压、脑内积水、脑组织萎缩、海马组织受损等疾患,与阿尔兹海默病、血管性痴呆、脑卒中后脑水肿等中枢神经系统疾病的发生和发展有关。
4.目前未发现本发明的化合物在脉络丛结构的改善方面的应用。
技术实现要素:
5.本发明为了解决上述背景技术中没有前未发现本发明的化合物在脉络丛结构的改善方面的应用,提供了一种化合物在用于制备具有改善脉络丛作用的药物的应用。
6.本发明采用的技术方案如下:
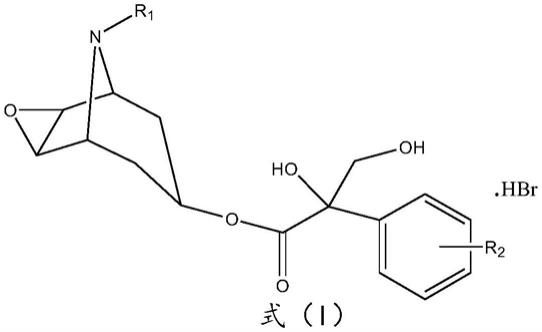
7.一种化合物在用于制备具有改善脉络丛作用的药物的应用,所述化合物如式(i)所示,
[0008][0009]
其中:
[0010]
r1选自c1‑
c6的烷基、c1‑
c6的杂烷基和c3‑
c6环烷基中的一种;
[0011]
r2选自羟基、甲基、乙基和氢原子中的一种。
[0012]
在上述技术方案的基础上,本发明还可以做如下改进。
[0013]
进一步,所述脉络丛是指侧脑室脉络丛;优选地,所述脉络丛是指第三脑室脉络丛、第四脑室脉络丛和部分侧脑室脉络丛;更优选地,所述脉络丛是指第三脑室脉络丛。
[0014]
进一步,所述具有改善脉络丛作用是指恢复和保护脉络丛的形态;优选地,所述恢复和保护脉络丛的形态是指恢复脉络丛正常的组织结构和生理功能。
[0015]
进一步,所述具有改善脉络丛作用是指调节脑脊液的分泌。
[0016]
进一步,所述化合物可以促进脉络丛上皮细胞的增殖。
[0017]
进一步,所述化合物可以抑制脉络丛上皮细胞的增殖。
[0018]
进一步,所述保护侧脑室脉络丛的结构和功能、和/或促进或抑制脉络丛上皮细胞的增殖是在内源或外源刺激物质的作用下发挥;优选地,所述内源或外源刺激物质是指脑缺血再灌注损伤;更优选地,所述内源或外源刺激物质是指c9h
15
alo9,其结构式如式(ii)所示,
[0019][0020]
进一步,所述药物还包括药学上可接受的辅料或辅助性成分。
[0021]
进一步,所述药学上可接受的辅料或辅助性成分为注射液水、淀粉、糊精、蔗糖、硬脂酸镁和蒸馏酒精中的至少一种。
[0022]
进一步,所述r1选自甲基,所述r2选自氢原子。
[0023]
本发明的有益效果是:本发明发现本发明化合物式(i)可以有效治疗和保护脉络丛,对脉络丛的组织结构和生理功能有较好的疗效。本发明发现25μg/ml的本发明化合物式(i)能够显著促进脉络丛上皮细胞的增殖,65~80μg/mlμg/ml的本发明化合物式(i)均能够显著抑制脉络丛上皮细胞的增殖。故本发明化合物式(i)可以实现对脉络丛上皮细胞的双向调节,显示了本发明化合物式(i)恢复了脉络丛上皮细胞的正常增殖的能力。从而很好的保护血-脑脊液屏障(blood
‑
cerebrospinal fluidbarrier,bcb),实现保护脑部和脊髓的作用。从而应用了本发明的化合物式(1)的药物能够有效的治疗脉络丛,从而能够治疗痴呆。能够恢复脉络丛正常的组织结构和生理功能。药物有效成分为25μg/ml的本发明的化合物式(1)时能够显著促进脉络丛上皮细胞的增殖,有效成分为65~80μg/ml的本发明的化合物式(1)均能够显著抑制脉络丛上皮细胞的增殖。
附图说明
[0024]
图1为本发明假手术模型组大鼠的第三脑室脉络丛he染色图;
[0025]
图2为本发明mcao实验组大鼠的第三脑室脉络丛he染色图;
[0026]
图3为本发明mcao低剂量组大鼠的第三脑室脉络丛he染色图;
[0027]
图4为本发明mcao中剂量组大鼠的第三脑室脉络丛he染色图;
[0028]
图5为本发明mcao高剂量组大鼠的第三脑室脉络丛he染色图;
[0029]
图6为本发明dapi热细胞核图;
[0030]
图7为本发明特异表达蛋白荧光染色图;
[0031]
图8为本发明相差显微镜下图;
[0032]
图9为本发明图6、图7和图8叠加图;
[0033]
图10为本发明实验化合物1对c9h
15
alo9诱导的原代脉络丛上皮细胞增殖的影响,*p<0.05与0μg/ml实验化合物1比较。
具体实施方式
[0034]ⅰ.定义
[0035]
脑室脉络丛的结构和功能
[0036]
脉络丛(choroid plexus)见于第ⅲ、ⅳ脑室顶和部分侧脑室壁,它是由富含血管的软膜与室管膜直接相贴并突入脑室而成的皱襞状结构,室管膜则成为有分泌功能的脉络丛上皮。脉络丛上皮由一层立方形或矮柱形细胞组成,细胞表面有许多微绒毛,细胞核大而圆,胞质内线粒体很多。细胞侧面之间靠近游离面处有连接复合体。上皮下是基膜,基膜深部是结缔组织。结缔组织内含丰富血管和巨噬细胞。毛细血管属有孔型,内皮细胞上的小孔有薄隔膜封闭。
[0037]
脉络丛的主要功能是产生脑脊液(cerebrospinal fluid),脑脊液是由脉络丛上皮细胞分泌的,为无色透明的液体,含蛋白质很少,但有较高浓度的na
、k
和cl
-
,并有少许脱落细胞和淋巴细胞。成年男性约有100ml脑脊液,在脑室、脊髓中央管、蛛网膜下隙和血管周隙。脑脊液通过蛛网膜粒(蛛网膜突入颅静脉窦内的绒毛状突起)吸收入血。脉络丛上皮不断分泌脑脊液,又不断回流入血液,形成脑脊液循环。脉络丛上皮和脉络丛毛细血管内皮共同构成血-脑脊液屏障(blood
‑
cerebrospinal fluidbarrier,bcb),使脑脊液保持稳定的成分而不同于血液。脑脊液有营养和保护脑与脊髓的作用。
[0038]
药物或药物组合物
[0039]
本公开所述化合物式(i),与一种或多种辅料如佐剂、载体或稀释剂一起,可以置入药物组合物、单位剂量(unit dosages)或剂型(dosage forms)的形式中。所述药物组合物可以固体剂型(如粉剂、颗粒剂、丸粒剂、包衣或未包衣的片剂或经填充的胶囊)或液体的剂型(如溶液、混悬液、乳液或填充其的胶囊)或半固体剂型(如凝胶、霜剂和软膏)采用。药物剂型的一种或多种活性成分的溶解和释放特性可以在数秒至数月的范围内变化。
[0040]
所述“药物”被设计用于在动物和人中的用途并可以经所有给药途径施用。优选的给药途径是注射途径、口服途径、肺途径、鼻途径、直肠途径、肠胃外途径。此种药物及其单位剂型可以常规或特别的比例包含常规的或新的成分,具有或不具有另外的活性化合物或成分,并且此种单位剂型可包含与目的日剂量范围相称的待采用的任何适宜有效量的活性成分。
[0041]
应用于本公开的药物组合物的术语“载体”涉及与活性化合物一起施用的稀释剂、辅料或赋形剂。
[0042]
治疗方法和药物配制剂
[0043]
无论通过口服、注射、直肠或肠胃外(包括静脉内的和皮下)或在某些情况下甚至局部途径,可以将本公开的式i活性成分或与一种或多种药物
‑
可接受的辅料、载体或稀释剂,特别是和优选地以它们的药物的形式,以有效量施用给需要其的对象,例如活动物(包括人)体,用于治疗、减轻或改善、缓解或消除对其敏感的适应症或病症或者阐述于本技术其它处的适应症或病症。
[0044]
本文中使用的术语“保护”、“治疗”意味减轻或缓解对象中的疾病的至少一种症状,在本公开的含义范围内,术语“保护”、“治疗”还指抑制、延迟发作(即,疾病临床表现的前期)和/或减小发展或恶化疾病的风险。
[0045]
本文中使用的术语“恢复”意味在某些内源或外源性刺激物质,如缺血缺氧,再灌注损伤的作用下,脉络丛的功能和/或结构会发生改变,出现结构和/或功能异常,“恢复”指将该异常状态回复到正常状态。“保护”意味着减少或避免所述内源或外源性刺激物质对脉络丛结构和/或功能的进一步改变或损伤。
[0046]
本公开的药物可以经口地、局部地(侧脑室)、肠胃外地或粘膜地(例如,含服地、通过吸入或直肠地)以包含常规的非
‑
毒性药学可接受的载体的剂量单位配制剂施用。通常希望使用注射途径。所述活性试剂可以经口地以胶囊、片剂等形式(参见remington:the science and practice of pharmacy,20th edition)施用。
[0047]
对于以片剂或胶囊形式的口服给药,活性药物组分可以与非
‑
毒性的、药学可接受的辅料如粘结剂(例如,预胶化的玉米淀粉、聚乙烯吡咯烷酮或羟丙基甲基纤维素);填料(例如,乳糖、蔗糖、葡萄糖、甘露糖醇、山梨糖醇和其它还原性和非
‑
还原性糖类、微晶纤维素、硫酸钙或磷酸氢钙);润滑剂(例如,硬脂酸镁、滑石粉或硅土、硬脂酸、硬脂基富马酸酯钠、甘油二十二烷酸酯、硬脂酸钙等);崩解剂(例如,马铃薯淀粉或羟乙酸淀粉钠);或润湿剂(例如,月桂基硫酸钠)、着色剂和调味剂、明胶、甜味剂、天然和合成的胶(如阿拉伯胶、黄蓍胶或藻朊酸盐)、缓冲盐、羧甲纤维素、聚乙二醇、蜡、等。对于以液体形式的口服给药,所述药物组分可以与非
‑
毒性、药学可接受的惰性载体(例如,乙醇、甘油、水)、防沉降剂(例如,山梨糖醇糖浆、纤维素衍生物或氢化的可食用脂肪)、乳化剂(例如,卵磷脂或阿拉伯胶)、非
‑
水性载体(例如,扁桃油、油酯类、乙醇或经分馏的植物油)、保藏剂(例如,p
‑
羟基苯甲酸甲酯或p
‑
羟基苯甲酸丙酯或山梨酸)等组合。还可以加入稳定剂如抗氧化剂(bha、bht、桔酸丙酯、抗坏血酸钠、柠檬酸)以稳定所述剂型。
[0048]
包含作为活性化合物的片剂可以通过本领域熟知的方法包衣。包含作为活性化合物式(1)的化合物的本公开的所述药物还可以引入小珠、微球或微胶囊,例如由聚乙醇酸/乳酸(pgla)构建的。用于口服给药的液体的制剂可以采取例如溶液,糖浆剂,乳液或混悬液的形式或者它们可以呈现为在使用前用水或其它适宜的辅料重构的干产品。用于口服给药的制剂可以适宜地配制以使活性化合物受控或延迟地释放。
[0049]
本公开的药物可以经肠胃外递送,即,通过静脉内(i.v.)、脑室内(i.c.v.)、皮下(s.c.)、腹膜内(i.p.)、肌内(i.m.)、皮下(s.d.)或皮内(i.d.)施用,通过直接注射,经例如快速浓注或连续输液。用于注射的配制剂可以单位剂型呈现,例如在具有添加的保藏剂的安瓿瓶或多
‑
剂量容器中。所述组合物可以采用赋形剂(excipient)的形状,在油或水性载体中的混悬液、溶液或乳液的形式,并可以包含配制试剂如防沉降剂、稳定剂和/或分散剂。
备选地,所述活性成分可以以粉末形式在使用前用适宜的载体(例如无菌无热原水)重构。
[0050]
本公开的药物还可以配制用于直肠给药,例如呈栓剂或保留灌肠(例如,包含常规栓剂基质如可可油或其它甘油酯)。
[0051]
以下结合附图对本发明的原理和特征进行描述,所举实例只用于解释本发明,并非用于限定本发明的范围。
[0052]
本公开的一个方面,涉及一种化合物在用于制备具有改善脉络丛作用的药物的应用,所述化合物如式(i)所示,
[0053][0054]
其中:
[0055]
r1选自c1‑
c6的烷基、c1‑
c6的杂烷基和c3‑
c6环烷基中的一种;
[0056]
r2选自羟基、甲基、乙基和氢原子中的一种。
[0057]
可选的,所述脉络丛是指侧脑室脉络丛;优选地,所述脉络丛是指第三脑室脉络丛、第四脑室脉络丛和部分侧脑室脉络丛;更优选地,所述脉络丛是指第三脑室脉络丛。
[0058]
可选的,所述具有改善脉络丛作用是指恢复和保护脉络丛的形态;优选地,所述恢复和保护脉络丛的形态是指恢复脉络丛正常的组织结构和生理功能。
[0059]
可选的,所述具有改善脉络丛作用是指调节脑脊液的分泌。
[0060]
可选的,所述化合物可以促进脉络丛上皮细胞的增殖。
[0061]
可选的,所述化合物可以抑制脉络丛上皮细胞的增殖。
[0062]
可选的,所述保护侧脑室脉络丛的结构和功能、和/或促进或抑制脉络丛上皮细胞的增殖是在内源或外源刺激物质的作用下发挥;优选地,所述内源或外源刺激物质是指脑缺血再灌注损伤;更优选地,所述内源或外源刺激物质是指c9h
15
alo9,其结构式如式(ii)所示,
[0063][0064]
可选的,所述药物还包括药学上可接受的辅料或辅助性成分。
[0065]
可选的,所述药学上可接受的辅料或辅助性成分为注射液水、淀粉、糊精、蔗糖、硬脂酸镁和蒸馏酒精中的至少一种。
[0066]
可选的,所述r1选自甲基,所述r2选自氢原子。
[0067]
取化合物式(i),且r1为甲基,所述r2为氢原子,得到实验化合物式1。所述实验化合物1来自中国大陆地区成都第一制药有限公司。
[0068]
实施例1、实验化合物式1对缺血再灌注损伤大鼠模型脉络丛的保护作用。
[0069]
1.1缺血再灌注模型大鼠的复制
[0070]
a、药物与试剂
[0071]
实验化合物式1(来自成都第一制药有限公司)。水合氯醛,生理盐水
[0072]
b、动物
[0073]
清洁级健康wistar大鼠30只,雌雄各半,体重(200
±
20)g,由山西省中医院实验动物中心提供。
[0074]
c、模型制备与处理
[0075]
mcao模型组的制备:采用线栓法制备大鼠大脑中动脉栓塞模型制备(以下简称mcao模型组),取24只雌雄各半的大鼠,分别用10%水合氯醛(35mg/kg)腹腔注射麻醉大鼠后,仰卧位固定,颈部备皮,消毒铺巾,颈部前正中线切口,沿胸锁乳突肌内缘分离肌肉和筋膜,将左侧颈总动脉、颈内动脉和颈外动脉分离,距离颈总动脉分叉4mm处结扎颈总动脉近心端,在颈外动脉穿入另一根丝线,在靠近颈总动脉分叉处结扎,动脉夹夹闭颈内动脉,并在距离颈总动脉分叉处3mm处的颈总动脉上剪一小口,将一根头端处理过的0.33mm直径的尼龙线从小口中插入,进入颈内动脉并向内插入大脑中动脉,尼龙线的插入深度距离颈总动脉分叉处约16mm,缺血2小时后拔掉线栓,缝合颈部伤口。
[0076]
假手术模型组制备:取剩余的6只雌雄各半的大鼠,与mcao模型组的区别在于假手术模型组的6只大鼠不插入线栓,其他操作同mcao模型组。
[0077]
d、药物作用剂量筛选
[0078]
在术后,将mcao模型组的大鼠均分为4组,雌雄各半。将3组分别给予相应低(2.5mg/kg)、中(5mg/kg)、高浓度(10mg/kg)的实验化合物式1的注射液,得到mcao低剂量组、mcao中剂量组和mcao高剂量组,剩余的1组不作任何处理,得到mcao实验组;
[0079]
假手术模型组内的6只大鼠均分为3个类别,雌雄各半,并且分别给予相应低(2.5mg/kg)、中(5mg/kg)、高浓度(10mg/kg)的生理盐水进行注射。
[0080]
mcao模型组和假手术模型组均注射3天,每天1次。收集各组大鼠脑组织,制备组织切片,进行he染色,得到图示如图1至图5所示。分析脑组织脉络丛的损伤情况。
[0081]
1.2结果
[0082]
如图1所示,假手术模型组大鼠的第三脑室脉络丛形态完整,无淤血和血栓。
[0083]
如图2所示,mcao实验组大鼠的第三脑室脉络丛明显萎缩或消失,缺乏完整形态,明显可见血栓。
[0084]
如图3所示,mcao低剂量组大鼠的第三脑室脉络可见清晰的脉络丛,但形态欠完整。
[0085]
如图4和图5所示,mcao中剂量组大鼠的第三脑室脉络和mcao高剂量组的大鼠第三脑室脉络丛形态明显有改善。mcao高剂量组的效果最优。
[0086]
实施例2、实验化合物式1对c9h
15
alo9诱导脉络丛上皮细胞的增殖的影响
[0087]
实验操作方法:
[0088]
2.1、实验动物
[0089]
出生16d的清洁级健康wistar大鼠28只,雌雄各半,体重(200
±
20)g,由山西省中医院实验动物中心提供。
[0090]
2.2、实验材料
[0091]
超净工作台(苏州净化设备有限责任公司),co2培养箱(美国thermo electron corporation公司),ix71型倒置显微镜(日本olympus公司),激光共聚焦显微镜(日本olympus公司),酶标仪(美国md公司),流式细胞仪(美国millipore公司)。dmem培养基(武汉博士德生物工程有限公司),d
‑
hanks缓冲液(武汉博士德生物工程有限公司),c9h
15
alo9(美国sigma公司)等。
[0092]
2.3、大鼠原代脉络丛上皮细胞的培养
[0093]
无菌环境中,将大鼠乙醚麻醉,浸75%冰乙醇中处死,取脑,并放人d
‑
hanks缓冲液中,洗去残留的血液,沿冠状面切开大脑,使切面向上,用一只镊子轻轻压住中脑组织,另一只镊子将脑灰质剥离,完全暴露海马和丘脑附近的脉络丛组织,用镊子轻轻取出脉络丛组织,置于预先装有少量d
‑
hanks缓冲液的1.5ml的ep管中,将组织剪碎,移入15ml离心管中,加人2ml的0.25%的胰酶,混匀后放入37℃培养箱中消化酶解20min,加入等量含血清培养液终止消化,1000r/min离心5min,留沉淀层,加入细胞培养液,吹打均匀,制成细胞悬液。将悬液移入预先铺有多聚赖氨酸的细胞培养瓶中,将培养瓶放入37℃,5%co2的培养箱中。第2天清除未贴壁的细胞,加人新培养液,以后每隔2d换液。得到大鼠原代脉络丛上皮细胞。期间注意用倒置显微镜观察细胞形态变化。
[0094]
2.4、大鼠原代脉络丛上皮细胞纯度的鉴定
[0095]
将细胞悬液接种在铺有多聚赖氨酸的盖玻片上5d,用d
‑
hanks缓冲液洗3次,每次5min;4%多聚甲醛固定30min,洗3次,每次5min;0.3%tritonx
‑
100室温孵育30min,洗3次,每次5min;5%bsa 37℃孵育30min,弃bsa,不洗;孵育一抗(anti
‑
ttr,1:300),4℃过夜;第2天洗去一抗(3次,每次5min),37℃孵育二抗(山羊抗兔igg.fitc,1:1000)2h,洗3次,每次5min;dapi(1:1000)孵育10min,洗3次,每次5min。新鲜配制的缓冲甘油(甘油:pbs=1:1)封片。激光共聚焦显微镜下观察,对脉络丛上皮细胞特异表达蛋白ttr做免疫组化检测。得到如图6至图9所示,根据脉络丛上皮细胞纯度=脉络丛上皮细胞/总细胞数
×
100%,本发明得到的同一视野下脉络丛上皮细胞纯度大于96%。
[0096]
2.5、大鼠原代脉络丛上皮细胞存活率的测定:
[0097]
将细胞悬浮液接种于96孔板上,隔天换液,5d后用c9h
15
alo9染毒,分为4个组:空白组、对照低剂量组、对照中剂量组、对照高剂量组。具体为:
[0098]
空白组:不添加任何成份。
[0099]
对照低剂量组:添加100μmol的c9h
15
alo9;
[0100]
对照中剂量组:添加400μmol的c9h
15
alo9;
[0101]
对照高剂量组:添加1600μmol的c9h
15
alo9;
[0102]
每组设5个复孔平行样,48h后换液,每个孔加人20ul的cck
‑
8溶液,2h后用酶标仪在450nm处测定吸光度(a)值。细胞存活率=a
染毒组
/a
对照组
×
100%。根据预实验结果,细胞半数
致死浓度(lc
50
)约为6400μmol/l,本研究所设剂量分别为lc
50
的0、1/64、1/16、1/4,即对照组、低剂量组、中剂量组和高剂量组。得到的结果如下表1:
[0103]
表1
[0104]
组别细胞存活率空白组100%对照低剂量组92.95%
±
8.80%对照中剂量组86.89%
±
4.06%对照高剂量组80.93%
±
9.14%
[0105]
随着染毒剂量增加,大鼠脉络丛上皮细胞存活率明显下降,差异有统计学意义(f=6.897,p<0.01):与对照组比较。中剂量组、高剂量组细胞存活率明显下降,差异有统计学意义(p<0.o1);与低剂量组比较,高剂量组细胞存活率有所下降,差异有统计学意义(p<0.o1)。所有数据均采用spss18.0进行分析。采用单因素方差分析(anova)进行数据分析,两两比较采用最小显著差(lsd)法进行比较。以p<0.05为差异有统计学意义。故采用添加400μmol的c9h
15
alo9的细胞悬浮液进行下面实验。
[0106]
2.6、实验化合物式1对c9h
15
alo9感染的大鼠原代脉络丛上皮细胞增殖的影响:
[0107]
将细胞悬浮液接种于6孔板中,待生长状态良好时,用添加400μmol的c9h
15
alo9染毒,接着分别添加10、20、25、30、40、65、70和80μg/ml的实验化合物式1,48h时,用cck
‑
8法检测实验化合物式1对c9h
15
alo9感染的大鼠原代脉络丛上皮细胞增殖的影响。得到如图10所示,25μg/ml的实验化合物式1能够显著促进原代脉络丛上皮细胞的增殖,65、70和80μg/ml的实验化合物式1均能够显著抑制原代脉络丛上皮细胞的增殖。说明实验化合物式1能够双向调节原代脉络丛上皮细胞的增殖。25μg/ml的实验化合物式1作用48h可以保护原代脉络丛上皮细胞的增殖。
[0108]
在本说明书的描述中,术语“一个实施例”、“一些实施例”、“具体实施例”等的描述意指结合该实施例或示例描述的具体特征、结构、材料或特点包含于本发明的至少一个实施例或示例中。在本说明书中,对上述术语的示意性表述不一定指的是相同的实施例或实例。而且,描述的具体特征、结构、材料或特点可以在任何的一个或多个实施例或示例中以合适的方式结合。
[0109]
以上所述仅为本发明的较佳实施例,并不用以限制本发明,凡在本发明的精神和原则之内,所作的任何修改、等同替换、改进等,均应包含在本发明的保护范围之内。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。