嘧啶并吲哚二酮类化合物在制备治疗pde5障碍疾病药物中应用
技术领域
1.本发明涉及医药技术领域,具体涉及嘧啶并吲哚二酮类化合物在制备治疗pde5障碍疾病药物中的应用。
背景技术:
2.环磷酸腺苷(camp)和环磷酸鸟苷(cgmp)作为重要的细胞内第二信使得到了越来越多人的关注。它们在体内广泛参与到多种生理功能的实现,例如:细胞周期调控、细胞分化、增殖、炎症过程、平滑肌收缩放松、视觉信号转导、学习记忆和代谢功能等,还涉及到类固醇合成、胰岛素分泌、糖原合成和脂肪生成等。腺苷酸环化酶(ac)可以活化三磷酸腺苷(atp)为camp,鸟苷酸环化酶(gc)可以活化三磷酸鸟苷(gtp)为cgmp。磷酸二酯酶(pdes)通过水解camp和cgmp为无活性的5
’‑
amp和5
’‑
gmp,从而降低camp和cgmp在细胞内的浓度,维持camp和cgmp在细胞内保持动态平衡,发挥正常的生理功能。
3.pdes家族包含11种亚型,其中pde4、pde7、pde8是camp特异性水解酶;pde5、pde6、pde9是cgmp特异性水解酶,pde1、pde2、pde3、pde10、pde11能同时水解camp和cgmp。体内高浓度的pdes将导致视觉退化、充血性心衰、忧郁、哮喘、勃起障碍和炎症等。
4.磷酸二酯酶pde5(phosphodiesterase 5)是首个被确定为以cgmp为特异性底物的磷酸二酯酶,目前被确证的有3个异构体pde5a1、pde5a2、pde5a3,它们在人体内均有表达,虽然3个异构体在人体内催化活性相同,但组织分布不同。pde5广泛分布于血管和内脏平滑肌细胞、血小板、肺、肾脏、前列腺、海绵体组织、脑、骨骼肌和心肌等。其中pde5a1、pde5a2几乎遍布上述所有组织,而pde5a3分布限于平滑肌中。pde5参与平滑肌伸缩、细胞凋亡、抑制和激活血小板的聚集、purkinje细胞的神经兴奋性、记忆形成的调节等重要生理作用。
5.目前,pde5抑制剂已经有多个上市药物,主要用于治疗男性勃起功能障碍(ed),通过抑制pde5活性,可以增加平滑肌细胞内的cgmp浓度,使平滑肌舒张,增加海绵体充血来治疗ed。sildenafil、vardenafil、tadalafil先后被fda批准,udenafil、mirodenafil在韩国获得批准,lodenafil在巴西批准用于ed治疗。但这些药物对pdes家族其他酶选择性不够高,容易造成视觉异常、听觉障碍等副作用。因此,发现具有新颖化学结构、良好特异性和高活性的pde5抑制剂具有重要的意义,本发明希望能设计开发新的pde5抑制剂为后续药物研发提供相应帮助。
技术实现要素:
6.为了治疗pde5障碍疾病的技术问题,而提供嘧啶并吲哚二酮类化合物在制备治疗pde5障碍疾病药物中的应用。本发明的嘧啶并吲哚二酮类化合物作为pde5活性抑制剂能够在体外有效抑制磷酸二酯酶的活性,具有潜在的治疗pde5障碍疾病的作用。
7.为了达到以上目的,本发明通过以下技术方案实现:
8.嘧啶并吲哚二酮类化合物在制备治疗pde5障碍疾病药物中的应用,所述嘧啶并吲
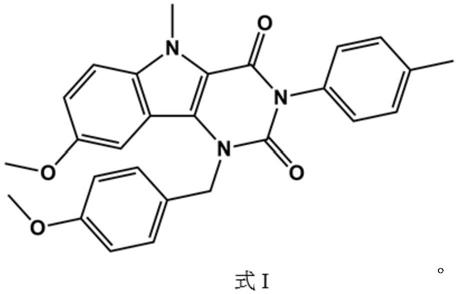
哚二酮类化合物通过抑制pde5活性来治疗pde5障碍疾病,所述嘧啶并吲哚二酮类化合物为如下结构的式i化合物或者其药学上可接受的盐,
[0009][0010]
进一步地,所述pde5障碍包括男性性功能障碍,前列腺增生,膀胱过度活动症,肺动脉高压,肺纤维化,肿瘤耐药疾病。
[0011]
进一步地,所述药物的成分包括所述嘧啶并吲哚二酮类化合物或者其药学上可接受的盐,以及药学上可接受的载体。所述的载体包括药学领域常规的稀释剂、赋形剂、填充剂、粘合剂、湿润剂、崩解剂、吸收促进剂、表面活性剂、吸附载体、润滑剂等。
[0012]
再进一步地,所述药物的剂型为注射液、片剂、粉剂、颗粒剂、丸剂、胶囊、口服液、膏剂、霜剂中的任意一种。上述各种剂型的药物均可以按照药学领域的常规方法制备。不同剂型的药物均是通过抑制pde5活性来治疗pde5障碍疾病,通过注射、喷射、滴鼻、滴眼、渗透、吸收、物理或化学介导的方法导入机体如肌肉、皮内、皮下、静脉、粘膜组织,或是被其他物质混合或包裹后导入机体。
[0013]
有益技术效果:
[0014]
本发明采用计算虚拟筛选与生物活性实验测定的方法从chemdiv数据库中寻找相关潜在能够治疗pde5障碍的药物分子结构,通过对药物分子的有效性进行先期计算评估,获得式i的嘧啶并吲哚二酮类化合物(8
‑
甲氧基
‑1‑
(4
‑
甲氧苄基)
‑5‑
甲基
‑3‑
(p
‑
甲苯基)
‑
1氢
‑
嘧啶并[5,4
‑
b]吲哚
‑
2,4(3h,5h)
‑
二酮)(下文中出现的该化合物以编号e737
‑
0759表示)具有潜在的pde5抑制活性,接着采用生物学实验方法检测并验证活性,采用pde
‑
glo
tm
phosphodiesterase assay测得其酶学水平为ic
50
值3.04μm,具有较好的pde5酶活性抑制的效果。实验证实e737
‑
0759化合物对pde5具有较好的抑制pde5活性的作用。虽然关于pde5抑制剂e737
‑
0759的研究还未成熟到进入临床阶段,但这些研究对于最终研制出治疗pde5障碍药物至关重要,具有重要的应用前景。
附图说明
[0015]
图1为pde
‑
glo
tm
phosphodiesterase assay测得e737
‑
0759在pde5蛋白水平上的ic
50
值图。
具体实施方式
[0016]
下面将结合本发明的实施例和附图,对本发明实施例中的技术方案进行清楚、完整地描述,显然,所描述的实施例仅仅是本发明一部分实施例,而不是全部的实施例。以下对至少一个示例性实施例的描述实际上仅仅是说明性的,决不作为对本发明及其应用或使
用的任何限制。基于本发明中的实施例,本领域普通技术人员在没有作出创造性劳动前提下所获得的所有其他实施例,都属于本发明保护的范围。
[0017]
除非另外具体说明,否则在这些实施例中阐述的数值不限制本发明的范围。对于相关领域普通技术人员已知的技术、方法可能不作详细讨论,但在适当情况下,所述技术、方法应当被视为说明书的一部分。在这里示出和讨论的所有示例中,任何具体值应被解释为仅仅是示例性的,而不是作为限制。因此,示例性实施例的其它示例可以具有不同的值。
[0018]
实施例1
[0019]
1.实验方法
[0020]
1.1基于受体的虚拟筛选
[0021]
采用分子模拟软件包中的蛋白准备模块protein preparation wizard对pde5的晶体结构(pdb:1xoz)进行预处理,包括修正键级,添加氢原子及部分电荷。接着采用中的配体准备模块ligprep对chemdiv化合物库(https://www.chemdiv.com/)进行化合物的预处理,包括去重、去除盐离子和无机物,在ph=7.4条件下产生化合物的可能离子化状态和互变异构体,以及产生环构象等。采用中的glide对接方法,选择1xoz晶体结构中配体分子tadalafil为质心的正方体区域,定义为pde5的活性位点,将该晶体结构中的配体分子重新用ligprep软件进行预处理,接着采用glide软件的sp(standard precision)打分方法重新对接到pde5活性位点,发现glide可以较好的重现晶体结构中配体的结合构象,从而证实了glide对接方法的有效性。采用上述的glide sp方法将ligprep预处理后的chemdiv化合物,对接到1xoz晶体结构的pde5活性位点,保留打分靠前的2000个化合物。采用中的canvas模块中reos方法对上述化合物进行成药性分析,除去可能具有毒性、反应活性或其他不理想组分的化合物,得到1691个化合物。
[0022]
提取pde5的5个晶体结构(pdb:2h42、2h44、1uho、4g2w、5zz2)进行预处理,包括修正键级,添加氢原子及部分电荷。然后提取pde5上述5个晶体结构以及1xoz晶体结构中的配体活性构象,采用discovery studio分子模拟软件包中的common feature pharmacophore generation模块构建了基于pde5已知抑制剂配体结构的药效团模型,得到fit value打分最高的药效团,通过该药效团对上面的1691个化合物进行基于配体药效团模型的虚拟筛选,得到符合要求的1124个化合物。为了充分考虑筛选化合物的结构多样性,采用discovery studio中的find diverse molecules模块进行基于分子指纹的聚类分析,经过人工挑选最终获得了41个化合物,委托chemdiv公司在国内代理商上海陶素公司购买了化合物实体,并且进行了pde5酶活性测定。
[0023]
1.2 pde5体外酶活性初筛实验步骤
[0024]
(1)pde5蛋白的表达纯化:pet15b
‑
pde5a(139
‑
875)野生型及截短体质粒由美国北卡大学柯衡明教授实验室赠予。经测序鉴定后,转化于大肠杆菌bl21 (codon plus)中诱导表达(用0.1mm iptg诱导后,在15℃持续培养24小时),用ni柱进行纯化,获得his标签的pde5蛋白。
[0025]
(2)pde5体外酶活性检测步骤,使用pde
‑
glo
tm
phosphodiesterase assay测定化合物对pde5的抑制效果:
[0026]
①
每个孔加入1μl待筛化合物(每个化合物测定7个浓度,3组平行实验),1.5μl pde5,室温孵育30分钟;
[0027]
②
继续加入2.5μl 2μm cgmp,室温孵育90分钟;
[0028]
③
每孔加入2.5μl pde
‑
glo
tm
termination buffer,2.5μl pde
‑
glo
tm
detection solution,室温孵育20分钟;
[0029]
④
最后加入10μl含有底物的缓冲液,室温孵育10分钟;
[0030]
⑤
用多功能酶标仪读取微孔板信号值。
[0031]
每组实验设置阴性和阳性对照,阴性对照:加入cgmp和无pde蛋白。没有加入pde蛋白,则cgmp含量最高,pka活性也最高,磷酸化底物消耗的atp最多,因此发光信号最弱,这一组读板值最小。阳性对照:加入cgmp和pde蛋白。pde水解大部分cgmp,pka的活性有所下降,磷酸化底物消耗的atp减少,剩余的atp增加,发光信号最强,这一组读板值最大。
[0032]
2.实验结果
[0033]
测定了人工挑选最终获得了41个化合物在蛋白水平上针对磷酸二酯酶pde5的活性抑制作用,其中具有式i结构的嘧啶并吲哚二酮类化合物(以编号e737
‑
0759表示)具有较好的pde5酶抑制活性,
[0034][0035]
采用pde
‑
glo
tm
phosphodiesterase assay测得e737
‑
0759化合物在pde5酶蛋白水平上的ic
50
值图如图1和表1所示。
[0036]
表1对应图1中的点值
[0037][0038]
由图1和表1可知,经pde
‑
glo
tm
phosphodiesterase assay检测,当cgmp终浓度为20μm,e737
‑
0759化合物终浓度为50μm时,e737
‑
0759化合物在体外蛋白酶学水平上具有较好的pde5抑制效果,对图1和表1中的数据进行计算得到ic
50
值为3.04μm。
[0039]
对比例1
[0040]
与e737
‑
0759化合物具有相似结构的含有氮杂环的化合物对pde5的抑制率见表2。
[0041]
表2相似结构化合物对pde5的抑制率
[0042]
[0043][0044]
由表2可知,与e737
‑
0759化合物具有相似结构的含有氮杂环的化合物对pde5的抑制率均未超过60%,效果不佳。
[0045]
综上,本发明e737
‑
0759化合物为有效的pde5活性抑制剂,在体外可有效抑制其酶活性。由于pde5在调节cgmp中的重要作用,本发明e737
‑
0759化合物作为pde5活性抑制剂,具有潜在的治疗pde5障碍疾病的作用,可望作为活性成分用于制备治疗pde5障碍疾病的药物,尤其可望用于治疗男性性功能障碍,前列腺增生,膀胱过度活动症,肺动脉高压,肺纤维化,肿瘤耐药疾病。本发明e737
‑
0759化合物具有药用前景。
[0046]
以上所述,仅为本发明较佳的具体实施方式,但本发明的保护范围并不局限于此,任何熟悉本技术领域的技术人员在本发明揭露的技术范围内,根据本发明的技术方案及其发明构思加以等同替换或改变,都应涵盖在本发明的保护范围之内。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。