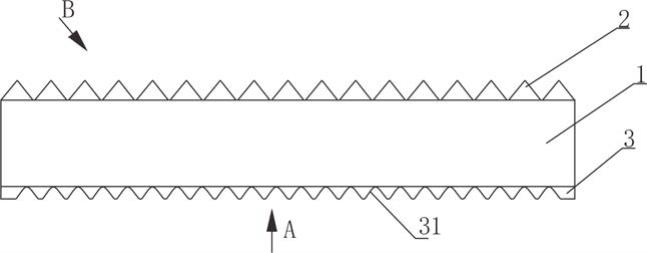
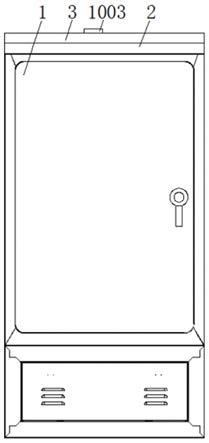
1.本发明涉及医药生物技术领域,具体为一种能预防食物过敏和感染的功能性食品益生菌凝胶的制备方法。
背景技术:
2.医学研究表明,过敏体质的根源在于体内肠道系统菌群失调。初生宝宝因免疫系统发育不成熟,从而易发生感染和过敏,某些过敏反应的发生是由于肠粘膜屏障功能的朋溃,致使大量抗原侵袭所造成的。各种过敏原因中以皮肤病过敏如湿疹、荨麻疹等最为明显,而其他过敏原因也持续的居高,过敏的症状也因人而异。
3.目前,抗过敏治疗药物主要是类固醇、抗组织胺等,而此类激素类药物主要是通过抑制组织胺来抑制过敏的症状,并非治疗过敏的根源,且易引起副作用,导致体重增加、骨质疏松等症状.益生菌具有调节过敏反应的功效,加快免疫系统的成熟,从而预防过敏。
4.而γ
‑
聚谷氨酸[poly
‑
γ
‑
glutamic acid,(γ
‑
pga)]是一种典型的聚电解质,与其他聚合高分子化合物相比,γ
‑
pga在体内能降解为谷氨酸单体,为人体所必需,生物相容性优良,低免疫原性,无毒副作用,这是其它材料所不可比拟的。壳寡糖[chitosan oligosaccharide,(co)]又称壳聚寡糖、低聚壳聚糖,是水溶性较好、功能作用大、生物活性高的低分子量产品。
技术实现要素:
5.针对现有技术中存在的问题,本发明提供一种能预防食物过敏和感染的功能性食品益生菌凝胶,该凝胶将壳聚糖加入,同时提高了益生菌的抗敏作用,而且由于聚γ
‑
谷氨酸的存在因此具有良好的生物相容性、分散性,使益生菌更好的发挥其作用。
6.本发明还提供了上述功能性食品益生菌凝胶的制备方法。
7.为实现上述目的,本发明涉及的具体技术方案如下:本发明提供了一种能预防食物过敏和感染的功能性食品益生菌凝胶的制备方法,包括以下步骤:(1)取γ
‑
pga溶于超纯水中,得γ
‑
pga预混液,利用mes buffer将ph调至5
‑
6,加入edc和nhs,然后超声10 min,封口,置于摇床反应,得γ
‑
pga溶液;(2)取co溶于pbs buffer中,超声,得co溶液,将co溶液加入到活化好的γ
‑
pga溶液中,利用pbs buffer将混合液调至7.2
‑
7.5,超声,封口,置于摇床反应,反应后离心洗涤,透析,冷冻干燥得到co
‑
γ
‑
pga粉末;(3)将干酪乳杆菌在mrs培养基中活化培养,收集纯化菌体,调节菌体的ph值为5.5
‑
6.5;冷冻干燥,得到的纯化菌体经冷冻干燥机进行冷冻干燥处理后,粉碎、过筛,得到益生菌菌粉;(4)制备益生菌凝胶,将co
‑
γ
‑
pga粉末、益生菌菌粉混合后与海藻酸丙二醇酯、丙
三醇充分搅拌乳化,静置至达到体系平衡状态,制成益生菌凝胶。
8.进一步的,步骤(1)中,所述γ
‑
pga预混液的浓度为2 mg/ml;所述γ
‑
pga和nhs的质量比为1:6;所述edc和nhs的质量比为8 :5;所述摇床反应为在37℃下反应15min。
9.进一步的,步骤(2)中,所述co溶液的浓度为10
‑
20mg/ml;所述co和γ
‑
pga的质量比为10
‑
20:1;所述反应为在37℃下反应10min;所述pbs buffer的浓度为0.1 mol/l。
10.本发明所使用的mrs培养基配方为蛋白胨10.0g、牛肉浸取物10.0g、酵母提取液5.0g、葡萄糖20.0g、乙酸钠5.0g、柠檬酸二胺2.0g、吐温
‑
80 1.0g、磷酸氢二钾0.4g、硫酸镁0.58g、硫酸锰0.29g、碳酸钙20.0g、蒸馏水补充到1000ml,ph 6.3,搅拌后加热,煮沸2min,在121℃、0.1mpa下灭菌30min。
11.进一步的,步骤(4)中,所述co
‑
γ
‑
pga 粉末和益生菌菌粉的质量比为100:1;所述丙三醇在总体系中的质量分数为40%;所述海藻酸丙二醇酯和丙三醇的质量比为1:30。
12.本发明还提供了一种利用上述制备方法制备得到的功能性食品益生菌凝胶。
13.本发明的有益效果为1、本发明中壳寡糖与益生菌联合,在预防食物过敏和感染方面具有协同作用,能够更好的促进胃肠对营养物质的吸收,最终制得的益生菌凝胶具有更好的预防食物过敏和感染性能,稳定性好,且制备方法简单,原料成本较低。
14.2、本发明制备的益生菌凝胶安全可靠,可有效定植,起效迅速,作用更直接有效,降低了生产成本,且可生物降解,对环境无污染,可应用于多个领域。
具体实施方式
15.以下通过具体实施方式对本发明作进一步的详细说明,但不应将此理解为本发明的范围仅限于以下的实例。在不脱离本发明上述方法思想的情况下,根据本领域普通技术知识和惯用手段做出的各种替换或变更,均应包含在本发明的范围内。
16.本发明所使用的γ
‑
聚谷氨酸分子量大小为40 kd;co分子量大小为800
‑
1000 d。
17.实施例1(1)取10 mg γ
‑
pga溶于10 ml超纯水中,利用mes buffer将ph调至5
‑
6,加入192 mg edc和120 mg nhs,然后超声10 min,封口,置于摇床,37℃,反应15 min。
18.(2)取200mg co溶于20 ml pbs buffer中,超声10 min。将co溶液加入到活化好的γ
‑
pga溶液中,利用pbs buffer将混合液调至7.2
‑
7.5,超声10 min,封口,置于摇床,37℃,反应10 h,反应后离心洗涤,透析2天,冷冻干燥得到co
‑
γ
‑
pga粉末。
19.(3)所选益生菌为干酪乳杆菌,将干酪乳杆菌在mrs培养基中活化培养,接种量为8%,收集菌体,纯化菌体,调节菌体的ph值为5.5
‑
6.5;冷冻干燥,得到的纯化菌体经冷冻干燥机进行冷冻干燥处理后,粉碎、过筛,得到益生菌菌粉;(4)制备益生菌凝胶:将co
‑
γ
‑
pga粉末、益生菌菌粉以质量比80:1混合与海藻酸丙二醇酯、丙三醇充分搅拌乳化,静置至达到体系平衡状态,制成益生菌凝胶。
20.实施例2(1)取10 mg γ
‑
pga溶于10 ml超纯水中,利用mes buffer将ph调至5
‑
6,加入192 mg edc和120 mg nhs,然后超声10 min,封口,置于摇床,37℃,反应15 min。
21.(2)取200 mg co溶于20 ml pbs buffer中,超声10 min。将co溶液加入到活化好
的γ
‑
pga溶液中,利用pbs buffer将混合液调至7.2
‑
7.5,超声10 min,封口,置于摇床,37℃,反应10 h,反应后离心洗涤,透析2天,冷冻干燥得到co
‑
γ
‑
pga粉末。
22.(3)所选益生菌为干酪乳杆菌,将干酪乳杆菌在mrs培养基中活化培养,收集菌体,纯化菌体,调节菌体的ph值为5.5
‑
6.5;冷冻干燥,得到的纯化菌体经冷冻干燥机进行冷冻干燥处理后,粉碎、过筛,得到益生菌菌粉;(4)制备益生菌凝胶,将co
‑
γ
‑
pg粉末、益生菌菌粉以质量比100:1混合与海藻酸丙二醇酯、丙三醇充分搅拌乳化,静置至达到体系平衡状态,制成益生菌凝胶。
23.实施例3(1)取20 mg γ
‑
pga溶于10 ml超纯水中,利用mes buffer将ph调至5
‑
6,加入192 mg edc和120 mg nhs,然后超声10 min,封口,置于摇床,37℃,反应15 min。
24.(2)取300mg co溶于20 ml pbs buffer中,超声10 min。将co溶液加入到活化好的γ
‑
pga溶液中,利用pbs buffer将混合液调至7.2
‑
7.5,超声10 min,封口,置于摇床,37℃,反应10 h,反应后离心洗涤,透析2天,冷冻干燥得到co
‑
γ
‑
pga粉末。
25.(3)所选益生菌为干酪乳杆菌,将干酪乳杆菌在mrs培养基中活化培养,收集菌体,纯化菌体,调节菌体的ph值为5.5
‑
6.5;冷冻干燥,得到的纯化菌体经冷冻干燥机进行冷冻干燥处理后,粉碎、过筛,得到益生菌菌粉;(4)制备益生菌凝胶,将co
‑
γ
‑
pga粉末、益生菌菌粉以质量比100:1混合与海藻酸丙二醇酯、丙三醇充分搅拌乳化,静置至达到体系平衡状态,制成益生菌凝胶。
26.实施例4(1)取20 mg γ
‑
pga溶于10 ml超纯水中,利用mes buffer将ph调至5
‑
6,加入192 mg edc和120 mg nhs,然后超声10 min,封口,置于摇床,37℃,反应15 min。
27.(2)取400 mg co溶于20 ml pbs buffer中,超声10 min。将co溶液加入到活化好的γ
‑
pga溶液中,利用pbs buffer将混合液调至7.2
‑
7.5,超声10 min,封口,置于摇床,37℃,反应10 h,反应后离心洗涤,透析2天,冷冻干燥得到co
‑
γ
‑
pga粉末。
28.(3)所选益生菌为干酪乳杆菌,将干酪乳杆菌在mrs培养基中活化培养,收集菌体,纯化菌体,调节菌体的ph值为5.5
‑
6.5;冷冻干燥,得到的纯化菌体经冷冻干燥机进行冷冻干燥处理后,粉碎、过筛,得到益生菌菌粉;(4)制备益生菌凝胶,将co
‑
γ
‑
pga粉末、益生菌菌粉以质量比100:1混合与海藻酸丙二醇酯、丙三醇充分搅拌乳化,静置至达到体系平衡状态,制成益生菌凝胶。
29.对比例1只使用壳寡糖和益生菌制备凝胶,其他制备条件与实施例4一致。
30.该对比例中,制备的凝胶稳定性较差,同时,少了聚γ
‑
谷氨酸,该凝胶的生物相容性较差。
31.对比例2(1)取20 mg γ
‑
pga溶于10 ml超纯水中,利用mes buffer将ph调至5
‑
6,加入192 mg edc和120 mg nhs,然后超声10 min,封口,置于摇床,37℃,反应15 min。
32.(2)取400 mg co溶于20 ml pbs buffer中,超声10 min。将co溶液加入到活化好的γ
‑
pga溶液中,利用pbs buffer将混合液调至7.2
‑
7.5,超声10 min,封口,置于摇床,37℃,反应10 h,反应后离心洗涤,透析2天,冷冻干燥得到co
‑
γ
‑
pga粉末。
33.(3)所选益生菌为干酪乳杆菌,将干酪乳杆菌在mrs培养基中活化培养,收集菌体,纯化菌体,调节菌体的ph值为5.5
‑
6.5;冷冻干燥,得到的纯化菌体经冷冻干燥机进行冷冻干燥处理后,粉碎、过筛,得到益生菌菌粉;(4)制备益生菌凝胶,将co
‑
γ
‑
pga粉末、益生菌菌粉以质量比100:1混合与丙三醇充分搅拌乳化,静置至达到体系平衡状态,制成益生菌凝胶。
34.效果实施例将40只km雌性小鼠,体质量18~22 g,随机分为4组(每组10只),各组之间小鼠体重无统计学差异。4组分别为空白对照组、阳性对照组、益生菌@co干预组、益生菌@co
‑
γ
‑
pga干预组。具体处理如下:空白对照组:对小鼠不加任何干预手段;阳性对照组:马来酸氯苯那敏软膏(每日剂量为10 mg/kg)涂抹全身;益生菌@co干预组:每只小鼠每次分别用10 mg/kg的co益生菌凝胶涂抹全身;益生菌@co
‑
γ
‑
pga干预组(实施例4):每只小鼠每次分别用10 mg/kg的co
‑
γ
‑
pga益生菌凝胶涂抹全身。
35.益生菌@co
‑
γ
‑
pga干预组(对比例2)每天涂抹1次连续10天,第10天涂抹后1 h,各组动物尾iv 40 mg/kg右旋糖酐40注射液。即刻观察并记录各组小鼠30 min 内出现的瘙痒次数及首次开始瘙痒时间,即瘙痒阈值。具体结果见表1。
36.表1 右旋糖酐致不同组别小鼠全身皮肤瘙痒的影响注:t检验,l:p<0.05 (与空白组比较);2:p<0.05 (和阳性对照组比较)观察瘙痒次数和瘙痒阈值发现,益生菌@co干预组对于空白组无明显统计学差异,而相对于阳性对照组有明显统计学差异(p<0.05),而益生菌@co
‑
γ
‑
pga干预组(实施例4)相对于益生菌@co和空白组均有统计学差异(p<0.05)。说明益生菌@co
‑
γ
‑
pga有拮抗右旋糖酐致不同组别小鼠全身皮肤瘙痒的作用,而单独使用效果欠佳。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。