用于癌细胞鉴别和监测的聚集诱导发光的荧光剂
1.相关申请的交叉引用
2.本技术要求于2020年4月21日提交的美国临时申请第63/101,200号的优先权,特此通过引用将其全部内容并入。
技术领域
3.本公开大体上涉及用于癌细胞检测、鉴别和/或动态监测的荧光染料。
背景技术:
4.癌症是人类最大的敌人之一。癌症转移前的早期检测对提高癌症患者的存活率非常重要。与正常细胞不同,癌细胞过度表达一些受体,这些受体可以用作鉴定癌细胞的靶生物标志物。目前,免疫荧光和基于适体的荧光系统是癌症检测的常用工具。在免疫荧光癌症检测中,对过度表达的受体高度特异的抗体与荧光染料缀合。
5.然而,在癌症的早期,受体的表达水平较低,这增加了早期癌症检测的难度。此外,制备针对癌细胞受体的特异性识别元件复杂且昂贵,且荧光染料与抗体的缀合可能影响抗体的结合和选择性。
6.在基于适体的荧光系统的癌症检测中,筛选对癌细胞特异的适体以及荧光染料与已鉴定到的适体的缀合也是复杂的过程。尽管这些特异性配体能有效地鉴定癌细胞的类型,但它们受到可利用的肿瘤细胞种类的限制,特别是来源于未知癌症的限制,难以实现癌症的广谱筛查。因此,免疫荧光癌症检测仍有很大的改进空间。广谱癌细胞检测迫切需要一种通用且方便的方法。
7.自体细胞的活力与人体健康密切相关。监测细胞活力对人类健康、亚健康和疾病检测很重要。特别是在药物筛选(包括药物开发和功效评价)方面,细胞活力监测也发挥重要作用。常用的检测细胞活力的标准方法是mtt测定。通过被线粒体的还原酶还原,黄色的mtt变成深紫色的甲瓒。然后通过在570nm处测量甲瓒的吸光度,可获得细胞活力。然而,mtt测定非常耗时,且详细的信息诸如细胞形态无法可视化。
8.荧光显微镜是在体内原位实时检测并监测生物样品的有力工具。研究人员已经开发出用于细胞活力检测的荧光探针。例如,钙黄绿素am在死细胞中无荧光,但在活细胞中显示强荧光。荧光素标记的膜联蛋白v被用于检测早期凋亡细胞上磷脂酰丝氨酸的表达。碘化丙啶(pi)只能对晚期凋亡细胞和死细胞染色,但不能进入活细胞。然而,使用这些探针实时监测细胞活力是困难的。快速和原位实时监测细胞活力的新系统是非常希望的。
9.响应于这些挑战,已经开发了各种各样的有机荧光团以用于生物样品成像。传统的芳香族和平面型荧光团(planar fluorophore)在水性条件中具有差的溶解性。增加溶液中此类荧光团的数量将导致聚集引起的猝灭(acq)。而在非常稀的溶液中,荧光过弱以致无法被检测到,且容易被照射漂白。
10.通常,物理效应往往与添加的物质的量呈正相关。由于癌细胞的膜通透性和线粒体膜电位(δψm)高于正常细胞的膜通透性和线粒体膜电位(δψm),因此理论上进入癌细
胞的荧光分子比正常细胞多,为癌细胞的鉴别提供了机会。对于具有acq效应的传统荧光团,进入正常细胞的分子较少,导致相对弱的荧光信号。然而,更多的进入癌细胞的分子由于acq继而导致荧光减少,从而减弱了癌细胞与正常细胞之间的荧光信号差异。因此,由于癌细胞与正常细胞的对比度低,传统荧光团实际上难以区分癌细胞与正常细胞。
11.因此,需要改进的用于对细胞(例如癌症细胞)成像、检测样本中的癌细胞以及监测癌细胞活力的化合物和方法。
技术实现要素:
12.本公开提供了用于癌细胞鉴别和/或细胞活力监测的独特的聚集诱导发光的荧光剂(aiegen)家族。本文描述的aiegen在高浓度下具有高发射性。由于癌细胞具有比正常细胞更高的膜通透性和δψm,因此较多的aiegen进入癌细胞,而较少的aiegen进入正常细胞。因此,aiegen在癌细胞中发出比在正常细胞中更强的荧光,允许对癌细胞的鉴别。
13.在第一方面,本文提供了一种用于对样品中的细胞成像的方法,所述方法包括:使所述样品与式1的聚集诱导发光的荧光剂(aiegen)接触:
[0014][0015]
其中x是阴离子;
[0016]
r1和r3中的每一个独立地为氢、卤化物、烷基、or、cn、no2或nr2;
[0017]
r2是氢或烷基;
[0018]
r4是烷基;并且
[0019]
对于每次出现,r独立地为氢或烷基;
[0020]
用光照射所述细胞;和
[0021]
检测所述化合物的荧光。
[0022]
在某些实施方案中,所述细胞是癌细胞。
[0023]
在某些实施方案中,r1和r3中的每一个都是氢。
[0024]
在某些实施方案中,r2是氢或c1‑
c5烷基。
[0025]
在某些实施方案中,r4是c1‑
c5烷基。
[0026]
在某些实施方案中,aiegen具有式2:
[0027][0028][0029]
其中x是阴离子;
[0030]
r2是氢或c1‑
c5烷基;并且
[0031]
r4是c1‑
c5烷基。
[0032]
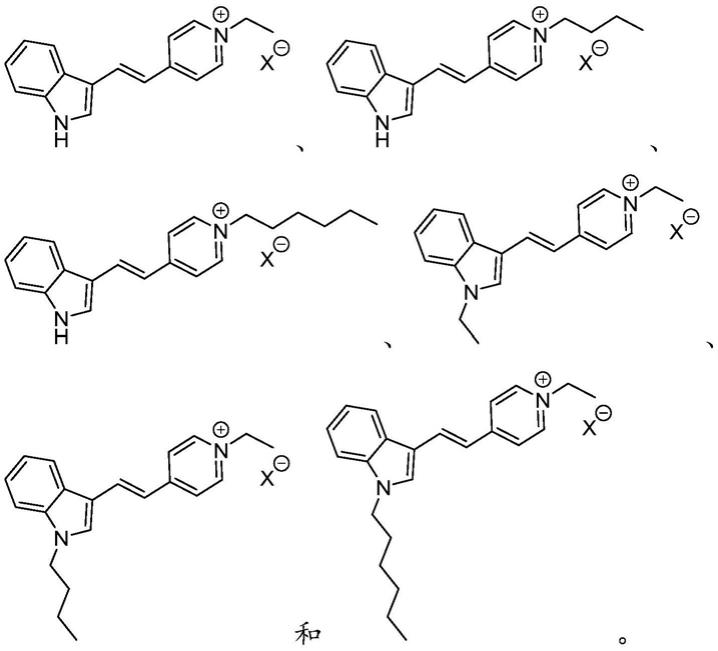
在某些实施方式中,aiegen选自由以下组成的组:
[0033][0034]
在某些实施方案中,x是pf6‑
。
[0035]
在某些实施方案中,检测aiegen的荧光的步骤包括监测aiegen从癌细胞的线粒体到核仁的迁移。
[0036]
在某些实施方案中,所述方法还包括基于aiegen从线粒体到核仁的迁移确定癌细胞的活力。
[0037]
在某些实施方案中,癌细胞的活力是在癌细胞处于抗癌剂存在下时确定的。
[0038]
在某些实施方案中,r2是氢或c2‑
c4烷基;r4是c2‑
c4烷基。
[0039]
在某些实施方案中,用波长在350至550nm之间的光照射所述细胞;并检测波长在450至650nm之间的荧光。
[0040]
在第二方面,本文提供了一种用于检测疑似包含癌细胞的样品中的癌细胞的方法,所述方法包括:使所述样品与式1的aiegen接触:
[0041][0042]
其中x是阴离子;
[0043]
r1和r3中的每一个独立地为氢、卤化物、烷基、or、cn、no2或nr2;
[0044]
r2是氢或烷基;
[0045]
r4是烷基;并且
[0046]
对于每次出现,r独立地为氢或烷基;
[0047]
用光照射所述样品;
[0048]
检测所述aiegen的荧光;和
[0049]
基于检测到的荧光来确定所述样品是否包含癌细胞。
[0050]
在某些实施方案中,r2是c1‑
c4烷基;且r4是c1‑
c4烷基;或r2是氢且r4是乙基。
[0051]
在某些实施方案中,aiegen选自由以下组成的组:
[0052][0053][0054]
在某些实施方案中,所述癌细胞是肺癌细胞或宫颈癌细胞。
[0055]
在第三方面,本文提供了一种式3的aiegen:
[0056][0057]
其中x是阴离子;
[0058]
r1和r3中的每一个独立地为氢、卤化物、烷基、or、cn、no2或nr2;
[0059]
r2和r4中的每一个独立地为烷基;并且
[0060]
对于每次出现,r独立地为氢或烷基。
[0061]
在某些实施方案中,r1和r3中的每一个都是氢;且r2和r4独立地为c1‑
c6烷基。
[0062]
在某些实施方案中,aiegen选自由以下组成的组:
[0063][0064]
众所周知,一些重要的位置或分子在细胞内是带负电的,例如细胞核内的线粒体和核酸。亲脂性阳离子倾向于通过静电相互作用靶向这些带负电荷的位置或分子。优化aiegens的电荷和亲脂性可以根据细胞活力的变化实现染色位置的改变。在这里,我们设计并合成了一系列aiegen,它们不但能够选择性地对癌细胞染色,而且能够通过线粒体
‑
核仁迁移来监测细胞活力。
[0065]
本主题大体上涉及一系列具有不同长度烷基链的aiegen分子。一方面,ivp
‑
02、ivp
‑
22、ivp
‑
42、ivp
‑
62能够区分癌细胞和正常细胞,因为癌细胞的膜通透性和线粒体膜电位高于正常细胞的膜通透性和线粒体膜电位。与ivp
‑
02、ivp
‑
22、ivp
‑
42和ivp
‑
62相比,更多的ivp
‑
04和ivp
‑
06分子进入正常细胞。ivp
‑
02、ivp
‑
22、ivp
‑
42、ivp
‑
62与ivp
‑
04、ivp
‑
06之间的明显区别在于吡啶鎓盐侧的烷基链的长度。吡啶鎓盐侧的烷基链的长度决定了离子半径。不希望受理论束缚,认为烷基链越长,离子半径越大,这使得aiegen更容易进入细胞。ivp
‑
04和ivp
‑
06可同时对癌细胞和正常细胞染色。癌细胞中的亮度高于正常细胞的亮度,因为癌细胞的线粒体膜电位高于正常细胞的线粒体膜电位。
[0066]
另一方面是细胞活力监测。ivp
‑
02、ivp
‑
04、ivp
‑
22和ivp
‑
42可以通过线粒体
‑
核仁迁移来监测癌细胞的活力,而ivp
‑
06和ivp
‑
62则不能,因为ivp
‑
06、ivp
‑
62与磷脂之间的疏水性相互作用较强并且对rna的亲和力较低。最后,ivp
‑
02具有良好的双光子特性和较低的细胞毒性。这些ivp分子在癌细胞检测、癌细胞转移监测方面表现出优异的性能,并且在评价癌症治疗药物的活性和功效方面表现出巨大的潜力。这项工作为实现癌细胞鉴别和动态活力监测的其他荧光探针的设计提供了理论和实验依据。
附图说明
[0067]
当结合所附附图理解本公开的以下描述时,本公开的上述和其它目的以及特征将变得明显。
[0068]
图1ivp
‑
02的化学结构及其在单晶胞中的单分子构型。
[0069]
图2(a)ivp
‑
02在不同溶剂中的归一化uv(虚线)和fl(实线)光谱。(b)ivp
‑
02在h2o中和具有不同甘油百分比(f
gly
)的h2o/甘油混合物中的fl光谱。(c)ivp
‑
02溶液的fl峰强度(i)随h2o/甘油混合物中甘油含量的变化。i0是在纯h2o中的强度。(d)ivp
‑
02在25℃和
‑
20℃的含90%甘油的h2o/甘油混合物中的fl光谱。(e)呈固态的ivp
‑
02的fl光谱。λ
ex
=440nm。插图:来自手持式紫外线灯的在365nmuv照射下拍摄的ivp
‑
02固体的荧光照片。(f)在dmso中的ivp
‑
02分别被780nm、800nm、820nm、840nm、860nm、880nm和900nm激发的tpef光谱。浓度:10μm。ivp
‑
02晶体结构的顶视图(g)和侧视图(h)。
[0070]
图3(a)ivp
‑
02在meoh中和具有不同甘油百分比(f
gly
)的meoh/甘油混合物中的fl
光谱。(b)ivp
‑
02溶液的fl峰强度(i)随meoh/甘油混合物中甘油含量的变化。i0是在纯meoh中的强度。(c)ivp
‑
02在25℃和
‑
20℃的含90%甘油的meoh/甘油混合物中的fl光谱。浓度:10μm。(d)ivp
‑
02(5μm)在具有不同rna浓度的pbs中的fl光谱。
[0071]
图4活的癌细胞(a549和hela)和正常细胞(cos7和hlf)分别用2μm ivp
‑
02染色30分钟的clsm图像。λ
ex
=488nm,λ
em
=500
‑
650nm。比例尺=20μm。
[0072]
图5分别用2μm ivp
‑
02染色30分钟的与正常细胞(cos7和hlf)共培养的活的癌细胞(a549和hela)的clsm图像(比例尺=50μm)(a)以及接种在不同盖玻片上的a549和hlf细胞的图像(比例尺=20μm)(b)。λ
ex
=488nm,λ
em
=500
‑
650nm。
[0073]
图6分别用2μm ivp
‑
02和0.2μm mtdr染色的活hela和a549细胞的clsm图像。ivp
‑
02:λ
ex
=488nm,λ
em
=500
‑
650nm;mtdr:λ
ex
=640nm,λ
em
=650
‑
700nm。比例尺=20μm。
[0074]
图7(a)ivp
‑
02、ivp
‑
04、ivp
‑
06、ivp
‑
22、ivp
‑
42和ivp
‑
62的化学结构。(b)分别用2μm ivp
‑
04、ivp
‑
06、ivp
‑
22、ivp
‑
42和ivp
‑
62染色30分钟的活a549细胞的clsm图像。λ
ex
=488nm,λ
em
=500
‑
650nm。(c)分别用2μm ivp
‑
04、ivp
‑
06、ivp
‑
22、ivp
‑
42、ivp
‑
62和0.2μm mtdr染色的a549细胞的clsm图像。ivp
‑
04、ivp
‑
06、ivp
‑
22、ivp
‑
42和ivp
‑
62:λ
ex
=488nm,λ
em
=500
‑
650nm;mtdr:λ
ex
=640nm,λ
em
=650
‑
700nm。比例尺=20μm。
[0075]
图8分别用2μm ivp
‑
04、ivp
‑
06、ivp
‑
22、ivp
‑
42和ivp
‑
62染色30分钟的活hela细胞的clsm图像。λ
ex
=488nm,λ
em
=500
‑
650nm。比例尺=20μm。
[0076]
图9分别用2μm ivp
‑
04、ivp
‑
06、ivp
‑
22、ivp
‑
42、ivp
‑
62和0.2μm mtdr染色的hela细胞的clsm图像。ivp
‑
04、ivp
‑
06、ivp
‑
22、ivp
‑
42和ivp
‑
62:λ
ex
=488nm,λ
em
=500
‑
650nm;mtdr:λ
ex
=640nm,λ
em
=650
‑
700nm。比例尺=20μm。
[0077]
图10分别用2μm ivp
‑
02、ivp
‑
04、ivp
‑
06、ivp
‑
22、ivp
‑
42和ivp
‑
62染色30分钟的与正常细胞(cos7)共培养的活的癌细胞(a549)的clsm图像(比例尺=50μm)(a),以及接种在不同盖玻片上的a549和hlf细胞的图像(比例尺=20μm)(b)。(b中的第一列与图3b相同)λ
ex
=488nm,λ
em
=500
‑
650nm。
[0078]
图11分别用2μm ivp
‑
02、ivp
‑
04、ivp
‑
06、ivp
‑
22、ivp
‑
42和ivp
‑
62染色30分钟的与正常细胞(cos7)共培养的活的癌细胞(hela)的clsm图像。λ
ex
=488nm,λ
em
=500
‑
650nm。比例尺=20μm。
[0079]
图12分别用2μm ivp
‑
02、ivp
‑
04、ivp
‑
06、ivp
‑
22、ivp
‑
42和ivp
‑
62染色30分钟的与正常细胞(hlf)共培养的活的癌细胞(a549)的clsm图像。λ
ex
=488nm,λ
em
=500
‑
650nm。比例尺=20μm。
[0080]
图13分别用2μm ivp
‑
02、ivp
‑
04、ivp
‑
06、ivp
‑
22、ivp
‑
42和ivp
‑
62在4℃染色20分钟的活a549细胞的clsm图像。λ
ex
=488nm,λ
em
=500
‑
650nm。比例尺=20μm。
[0081]
图14(a)波恩能量方程。(b)亲脂性阳离子通过膜的示意图。
[0082]
图15活a549细胞(a)和与cos7细胞共培养的活a549细胞、与cos7细胞共培养的活hela细胞(b)用2μm ivp
‑
02预染30分钟并用20μm cccp处理5分钟。然后移除cccp,并加入新鲜培养基,持续另外的5分钟。λ
ex
=488nm,λ
em
=500
‑
650nm。比例尺=20μm。
[0083]
图16活hela细胞用2μm ivp
‑
02预染30分钟,并用20μm cccp处理5分钟。然后移除cccp,并加入新鲜培养基,持续另外的5分钟。λ
ex
=488nm,λ
em
=500
‑
650nm。比例尺=20μm。
[0084]
图17活a549和hela细胞用2μm ivp
‑
02预染30分钟,并用10mm h2o2处理10分钟。λ
ex
=488nm,λ
em
=500
‑
650nm。比例尺=20μm。
[0085]
图18活a549细胞用2μm ivp
‑
04、ivp
‑
22、ivp
‑
42、ivp
‑
06、ivp
‑
62预染30分钟,并用20μm cccp处理5分钟。然后移除cccp,并分别加入新鲜培养基,持续另外的5分钟。λ
ex
=488nm,λ
em
=500
‑
650nm。比例尺=20μm。
[0086]
图19活hela细胞用2μm ivp
‑
04、ivp
‑
22、ivp
‑
42、ivp
‑
06、ivp
‑
62预染30分钟,并用20μm cccp处理5分钟。然后移除cccp,并分别加入新鲜培养基,持续另外的5分钟。λ
ex
=488nm,λ
em
=500
‑
650nm。比例尺=20μm。
[0087]
图20(a)用rna对ivp
‑
02进行荧光滴定(左),以及按照斯卡查德(scatchard)方程的拟合曲线(右)。(b)ivp
‑
02与rna的结合方式。(c)ivp分子与rna的结合常数(k)和结合能(e)。
[0088]
图21用rna对ivp
‑
04、ivp
‑
22、ivp
‑
42、ivp
‑
06和ivp
‑
62进行荧光滴定(左)和按照斯卡查德方程的拟合曲线(中)以及它们与rna的结合方式(右)。
[0089]
图22(a)用2μm ivp
‑
02染色30分钟的活hela细胞的双光子显微镜图像。λ
ex
=800nm,λ
em
=495
‑
540nm。比例尺=20μm。(b)a549细胞与不同浓度的ivp
‑
02、ivp
‑
04、ivp
‑
06、ivp
‑
22、ivp
‑
42和ivp
‑
62孵育24小时后的活力。
具体实施方案
[0090]
定义
[0091]
在整个申请中,在组合物被描述为具有、包括或包含特定组分的情况下,或者在方法被描述为具有、包括或包含特定处理步骤的情况下,预期本技术教导的组合物也可以主要由所述及的组分组成或由所述组分组成,并且本技术教导的方法也可以主要由所述及的处理步骤组成或由所述及的处理步骤组成。
[0092]
在本技术中,如果一种要素或组分被表述为被包括在具有所述及的要素或组分的列表中和/或选自具有所述及的要素或组分的列表,则应理解所述要素或组分可以是被述及的多个要素或组分中的任何一个,或者所述要素或组分可以选自由被述及的多个要素或组分中的两个或更多个组成的组。此外,应当理解,本文描述的组合物或方法的要素和/或特征可以以各种方式组合,而不脱离本技术教导的精神和范围,无论本技术的教导是明确的还是隐含的。
[0093]
应当理解,只要本技术教导保持可操作,步骤的顺序或执行某些动作的顺序是无关紧要的。此外,两个或更多个步骤或动作可以同时进行。
[0094]
除非另有特别说明,否则本文中单数的使用包括复数(反之亦然)。另外,如果术语“约”用在数值之前,除非另有特别说明,否则本技术的教导还包括具体的数值本身。如本文所用,除非另有指示或推断,否则术语“约”是指距标称值的变化为
±
10%、
±
7%、
±
5%、
±
3%、
±
1%或
±
0%。
[0095]
术语“组合物”意图包括含有指定量的指定成分的产品,以及直接或间接由指定量的指定成分的组合所产生的任何产品。
[0096]
如本文所用,除非另有说明,否则术语“卤代(halo)”或“卤化物”包括氟代、氯代、溴代或碘代。
[0097]
如本文所用,“烷基”指直链或支链的饱和烃基团。烷基基团的实例包括甲基、乙
基、丙基(例如,正丙基和异丙基)、丁基(例如,正丁基、异丁基、仲丁基、叔丁基)、戊基基团(例如,1
‑
甲基丁基、2
‑
甲基丁基、异戊基、叔戊基、1,2
‑
二甲基丙基、新戊基和1
‑
乙基丙基)、己基基团等。在多种实施方案中,烷基基团可具有1到40个碳原子(即,c1‑
40
烷基基团),例如,1
‑
30个碳原子(即,c1‑
30
烷基基团)。在某些实施方案中,烷基基团可具有1到6个碳原子,并且可称为“低级烷基基团”。低级烷基基团的实例包括甲基、乙基、丙基(例如,正丙基和异丙基)和丁基(例如,正丁基、异丁基、仲丁基、叔丁基)基团。在某些实施方案中,烷基基团可任选地如本文所述地被取代。烷基基团通常不被另一烷基基团、烯基基团或炔基基团取代。
[0098]
如本文所使用的,术语“药学上可接受的阴离子”是指那些在合理的医学判断范围内,适合于与受试者的组织接触而没有过度毒性、刺激性、过敏反应等,并且与合理的益处/风险比率相称的阴离子。药学上可接受的阴离子在本领域是众所周知的。例如,berge等人在j.pharmaceutical sciences(1977)66:1
‑
19中详细描述了药学上可接受的阴离子。本文提供的化合物中包含的药学上可接受的阴离子包括合适的无机阴离子和有机阴离子。药学上可接受的无毒无机阴离子的实例,例如氯离子、溴离子、磷酸根、硫酸根、六氟磷酸根和高氯酸根,或有机阴离子的实例,例如乙酸根、草酸根、马来酸根、酒石酸根、柠檬酸根、琥珀酸根或丙二酸根。其他药学上可接受的阴离子包括己二酸根、海藻酸根、抗坏血酸根、天冬氨酸根、苯磺酸根(benzenesulfonate)、苯磺酸根(besylate)、苯甲酸根、硫酸氢根、硼酸根、丁酸根、樟脑酸根、樟脑磺酸根、柠檬酸根、环戊烷丙酸根、二葡萄糖酸根、十二烷基硫酸根、乙磺酸根、甲酸根、富马酸根、葡庚糖酸根、甘油磷酸根、葡萄糖酸根、半硫酸根(hemisulfate)、庚酸根、己酸根、碘离子、2
‑
羟基乙磺酸根、乳糖酸根、乳酸根、月桂酸根、十二烷基硫酸根、苹果酸根、丙二酸根、甲磺酸根、2
‑
萘磺酸根、烟酸根、硝酸根、油酸根、草酸根、棕榈酸根、双羟萘酸根、果胶酸根、过硫酸根、3
‑
苯基丙酸根、磷酸根、苦味酸根、新戊酸根、丙酸根、硬脂酸根、琥珀酸根、硫酸根、酒石酸根、硫氰酸根、对甲苯磺酸根、十一酸根、戊酸根等。
[0099]
本文所使用的措辞“聚集诱导发光”或“aie”是指在荧光化合物在以该荧光化合物的无定形状态或结晶(固态)状态聚集后光发射增强,而该荧光化合物在稀溶液中表现出弱的发射或基本上不发射。
[0100]
如本文中使用的术语“λ
ex”是指激发波长。
[0101]
如本文中使用的术语“λ
em”是指发射波长。
[0102]
如本文中使用的术语“样品”涉及怀疑含有一个或更多个癌细胞的材料或材料混合物,所述材料或材料混合物通常不需要呈流体形式,而是也可以呈固体形式。在某些实施方案中,所述样品来源于生物样品例如体液、来自组织或器官的样品、或自身体外表面或内表面的洗涤/冲洗液或拭子或涂片获得的样品。在某些实施方案中,粪便、尿液、唾液、脑脊液、血液、血清、血浆或泪液的样品作为本文描述的方法的样品被包括。
[0103]
本公开提供了用于对细胞(例如癌症细胞)成像、检测样本中的癌细胞以及监测癌细胞的活力的aiegen和方法。在某些实施方案中,所述aiegen具有式1:
[0104][0105]
其中x是阴离子;
[0106]
r1和r3中的每一个独立地为氢、卤化物、烷基、or、cn、no2或nr2;
[0107]
r2是氢或烷基;
[0108]
r4是烷基;并且
[0109]
对于每次出现,r独立地为氢或烷基。
[0110]
式1的aiegen中存在的双键可以是顺式双键或反式双键。在某些实施方案中,式1的aiegen中的双键是反式双键。
[0111]
在某些实施方案中,r1和r3中的每一个独立地为氢、氟化物、氯化物、溴化物、烷基、or、cn、no2或nr2,其中r为氢、c1‑
c
12
烷基、c1‑
c
10
烷基、c1‑
c8烷基、c1‑
c6烷基、c1‑
c4烷基或c1‑
c2烷基。在某些实施方案中,r1和r3中的每一个都是氢。
[0112]
在某些实施方案中,r2是氢、c1‑
c
12
烷基、c1‑
c
10
烷基、c1‑
c8烷基、c1‑
c6烷基、c2‑
c6烷基、c1‑
c5烷基、c2‑
c5烷基、c1‑
c4烷基或c2‑
c4烷基。在某些实施方案中,r2是氢、c1‑
c5烷基、c2‑
c5烷基、c1‑
c4烷基或c2‑
c4烷基。在某些实施方案中,r2是氢或c2‑
c4烷基。
[0113]
在某些实施方案中,r4是c1‑
c
12
烷基、c1‑
c
10
烷基、c1‑
c8烷基、c1‑
c6烷基、c2‑
c6烷基、c1‑
c5烷基、c2‑
c5烷基、c1‑
c4烷基或c2‑
c4烷基。在某些实施方案中,r4是c1‑
c5烷基、c2‑
c5烷基、c1‑
c4烷基或c2‑
c4烷基。在某些实施方案中,r4是c2‑
c4烷基。
[0114]
x可以是一种或更多种药学上可接受的阴离子,包括但不限于氯离子、溴离子、磷酸根、硫酸根、六氟磷酸根、四氟硼酸根、高氯酸根、乙酸根、草酸根、马来酸根、酒石酸根、柠檬酸根、琥珀酸根、丙二酸根、己二酸根、海藻酸根、抗坏血酸根、天冬氨酸根、苯磺酸根(benzenesulfonate)、苯磺酸根(besylate)、苯甲酸根、硫酸氢根、硼酸根、丁酸根、樟脑酸根、樟脑磺酸根、柠檬酸根、环戊烷丙酸根、二葡萄糖酸根、十二烷基硫酸根、乙磺酸根、甲酸根、富马酸根、葡庚糖酸根、甘油磷酸根、葡萄糖酸根、半硫酸根(hemisulfate)、庚酸根、己酸根、碘离子、2
‑
羟基乙磺酸根、乳糖酸根(lactobionate)、乳酸根、月桂酸根、十二烷基硫酸根、苹果酸根、丙二酸根、甲磺酸根、2
‑
萘磺酸根、烟酸根、硝酸根、油酸根、草酸根、棕榈酸根、双羟萘酸根、果胶酸根、过硫酸根、3
‑
苯基丙酸根、磷酸根、苦味酸根、新戊酸根、丙酸根、硬脂酸根、琥珀酸根、硫酸根、酒石酸根、硫氰酸根、对甲苯磺酸根、十一酸根、戊酸根等。在某些实施方案中,x是六氟磷酸根。
[0115]
在某些实施方案中,r2是氢、c1‑
c5烷基、c2‑
c5烷基、c1‑
c4烷基或c2‑
c4烷基;r4是c1‑
c5烷基、c2‑
c5烷基、c1‑
c4烷基或c2‑
c4烷基。在某些实施方案中,r2是氢或c2‑
c4烷基;r4是c2‑
c4烷基。
[0116]
在某些实施方案中,aiegen具有式2:
[0117][0118]
其中x是阴离子;
[0119]
r2是氢或c1‑
c5烷基;并且
[0120]
r4是c1‑
c5烷基。
[0121]
在某些实施方案中,aiegen选自由以下组成的组:
[0122][0123]
本领域普通技术人员使用已知方法能够容易地制备本文描述的aiegen。例如,aiegen可通过缩合反应或金属偶联反应制备。在以下实例中,通过将适当改性的吲哚
‑3‑
甲醛与1
‑
烷基
‑4‑
甲基吡啶鎓盐缩合而形成aiegen。
[0124]
本文还提供了一种制备式2的aiegen的方法,所述方法包括:使式4的化合物:
[0125][0126]
(其中r2是c1‑
c5烷基)与式5的化合物:
[0127][0128]
(其中x是阴离子;且r4是c1‑
c5烷基)以及布朗斯特碱接触,从而形成式2的化合物。
[0129]
具有合适pkb的任何碱可用于本文描述的方法中,包括但不限于naoh、koh、lioh、三乙胺、n,n
‑
二异丙基乙胺、吡咯烷、吗啉、吡啶、咪唑等。
[0130]
反应可在任何极性质子或极性非质子溶剂中进行。示例性溶剂包括但不限于醇类、醚类、甲酰胺类、亚砜类、芳香族溶剂、卤化溶剂及其组合。在某些实施方案中,反应在甲醇、乙醇、异丙醇、二甲基甲酰胺、二甲基亚砜、四氢呋喃、四氢吡喃、二氧杂环己烷、苯、甲苯、吡啶、二氯甲烷、二氯乙烷及其混合物中进行。
[0131]
在可选择的实施方案中,使式4的化合物与式5的化合物的共轭碱接触,从而形成式2的aiegen。式5的化合物的共轭碱可通过式5的化合物与布朗斯特碱的反应制备。
[0132]
本公开还提供了一种用于对样品中的细胞成像的方法,所述方法包括:使样品与本文描述的aiegen接触;用光照射细胞;以及检测aiegen的荧光。
[0133]
样本可以是已知可能包括癌细胞的任何合适类型。合适样品的实例包括但不一定局限于活检材料、切除材料、尿液、膀胱冲洗物、膀胱擦洗物、血液、痰、脑脊液、胸腔积液、腹水、肝脏、甲状腺、卵巢、淋巴结、乳腺、宫颈、肺、胆管树、胰、肺和结肠。在某些实施方案中,样品为流体样品。
[0134]
在某些实施方案中,细胞来源于动物(例如哺乳动物),包括但不限于人类、非人灵长类、犬科动物、牛科动物、猫科动物和啮齿动物。在某些实施方案中,细胞来自人类细胞。
[0135]
在某些实施方案中,细胞是癌细胞。在某些实施方案中,癌细胞是头、颈、眼、口、咽喉、食道、支气管、喉、咽、胸、骨、肺、结肠、直肠、胃、前列腺、膀胱、子宫、宫颈、乳腺、卵巢、睾丸或其他生殖器官、皮肤、甲状腺、血液、淋巴结、肾、肝、胰腺和脑或中枢神经系统的癌症的癌细胞。在某些实施方案中,癌症是肺癌或乳腺癌。
[0136]
用于照射细胞的光可具有350
‑
600nm、350
‑
550nm、350
‑
500nm、400
‑
500nm、375
‑
475nm或400
‑
450nm之间的激发波长λ
ex
。
[0137]
能够发射350
‑
600nm之间的光的可用光来照射细胞的任何仪器能够结合本文描述的方法使用。在某些实施方案中,仪器是激光器。在某些实施方案中,采用共聚焦激光扫描显微镜照射细胞并检测aiegen的荧光。
[0138]
荧光可具有450
‑
700nm、450
‑
650nm、450
‑
600nm、475
‑
575nm、500
‑
600nm或500
‑
550nm之间的发射波长λ
em
。
[0139]
可通过目视检查和/或使用光谱仪来检测样品中是否存在发光。任何能够测量样品吸光度(在约450到700nm之间)的常规光谱仪可结合本文所述的方法使用。在某些实施方案中,所述光谱仪是可见光光谱仪或紫外
‑
可见光光谱仪,其能够测量受试样品在450
‑
700nm、450
‑
650nm、450
‑
600nm、475
‑
575nm、500
‑
600nm或500
‑
550nm之间的吸光度。
[0140]
检测aiegen的荧光的步骤还可以包括监测aiegen从细胞的线粒体到核仁的迁移;以及任选地,基于aiegen从线粒体到核仁的迁移确定细胞的活力。在某些实施方案中,细胞
是癌细胞。
[0141]
本文描述的方法可用于监测癌细胞在测试试剂存在下的活力。测试试剂可以是怀疑对细胞具有生物学影响(例如,细胞生长或细胞周期)的任何试剂,包括但不限于小分子、抗体、蛋白质、干扰性核酸等。在某些实施方案中,测试试剂是怀疑具有或已知具有抗癌性质的试剂。本文描述的方法可用于监测抗癌试剂对癌细胞活力的影响。
[0142]
本公开还提供了一种检测疑似含有癌细胞的样品中的癌细胞的方法,所述方法包括:使样品与本文描述的aiegen接触;用光照射样品;检测aiegen的荧光;以及基于检测到的荧光确定样品是否包含癌细胞。
[0143]
ivpi
‑
2能够对健康的活的癌细胞中的线粒体染色。然而,当δψm减小时,ivpi
‑
2迁移到核仁中。由于ivpi
‑
2根据线粒体生理学性质的变化是可改变靶的(target
‑
changeable),因此,对ivpi
‑
2的化学结构进行了修饰以增强线粒体向核仁的迁移。由于其重原子效应,碘离子是众所周知的有效荧光猝灭剂。因此,使碘离子被六氟磷酸根取代并获得如图1所示的ivp
‑
02。呈固态的ivp
‑
02的量子产率为4.3%,是ivpi
‑
02(1.3%)的约3倍。方案1中描绘了得到本文描述的化合物的某些实施方案的示例性合成路线。
[0144]
方案1.ivp
‑
02、ivp
‑
04、ivp
‑
06、ivp
‑
22、ivp
‑
42和ivp
‑
62的合成路线。
[0145][0146]
ivp
‑
02的化学结构通过1h nmr、
13
c nmr、
19
f nmr和hrms充分表征。另外,单晶x射线衍射分析进一步证实了ivp
‑
02的结构(ccdc1986367,图1)。
[0147]
图2a中显示了ivp
‑
02在不同溶剂中的吸收光谱和单光子激发的荧光(fl)光谱。ivp
‑
02显示出从400nm到450nm的强吸收以及从500nm到550nm的强发射。ivp
‑
02具有明显的供体
‑
π
‑
受体结构。表明由于分子内电荷转移效应,fl光谱随着溶剂极性的增加发生了红移。在ivp
‑
02的水溶液中加入thf和etoh无法使染料分子聚集,这可能是由于染料分子的两亲性所致。其他人也报告了类似的结果。然后对ivp
‑
02在粘性增加环境和固态下的发射进行了仔细的测量以研究ivp
‑
02是否具有aie活性。在图2b和2c中,ivp
‑
02在纯水溶液中表现出弱的发射。随着与粘度增加相伴的甘油体积含量的增加,fl强度逐渐增加。除了水/甘油体系外,图3a和3b在meoh/甘油体系中进行了类似的实验。结果也表明,ivp
‑
02在高粘度环境中具有高度发射。此外,在图2d和3c中,当溶液温度从25℃降至
‑
20℃时,fl强度也明显增强。这些现象之所以发生是因为高粘度和低温会阻碍分子内运动,导致非辐射衰减通道关闭,从而增强fl发射。此外,我们在ivp
‑
02的pbs溶液中加入了一些rna。在图3d中,ivp
‑
02在pbs溶液中表现出弱的发射,但随着rna浓度的增加,fl强度明显增强。根据图20的计算结果,ivp
‑
02位于rna的小凹槽中,在此处ivp
‑
02的分子内运动也受到阻碍。这些结果表明,分子内运动受限(rim)是导致染料高发射的主要原因,这也是aiegen的发光机制。ivp
‑
02在固态下也表现出575nm左右的强荧光,且其粉末发出明亮的黄光(图2e)。因此,基于以上结果,ivp
‑
02具有aie活性。
[0148]
ivp
‑
02在水溶液中表现出弱的发射,但在高粘度条件下则发射强荧光,因此非常有利于免洗生物成像。另外,ivp
‑
02在固态下比在溶液中发出更红的荧光。为了验证ivp
‑
02
固态红移的机理,在图2g和2h中对其晶体进行了分析。ivp
‑
02的分子是反平行堆积的,并在结晶状态形成多聚体。多聚体分子间的短堆积距离为结晶状态形成多聚体。多聚体分子间的短堆积距离为和表明多聚体内部的强分子间相互作用。因此,固态时的红移发射应归因于分子间的短接触引起的分子间π
‑
π相互作用。一般来说,具有供体
‑
受体结构的有机染料表现出良好的双光子吸收(tpa)和双光子激发荧光(tpef)。在图2f中,在dmso中测量了在不同脉冲波长(780
‑
900nm)被激发的ivp
‑
02的tpef光谱。使用荧光素做为标准,计算了ivp
‑
02的双光子吸收截面(δ)并显示在表1中。在800nm激发时,最大δ为287gm。如此高的δ值有利于活细胞和深层组织中的双光子成像。
[0149]
表1.ivp
‑
02在dmso中的双光子吸收截面(δ)
[0150][0151]
通过共聚焦激光扫描显微镜(clsm)研究了ivp
‑
02在活细胞中的生物成像性质。将癌细胞(a549和hela)和正常细胞(cos7和hlf)分别用ivp
‑
02染色。在图4中,在相同的染色和成像条件下,正常细胞的荧光强度比癌细胞的荧光强度弱得多。因此ivp
‑
02具有区分癌细胞和正常细胞的高潜力。为了验证该推测,将癌细胞和正常细胞共培养并用ivp
‑
02染色。在图5a中,可以看出只有癌细胞(a549和hela)被高度照亮,而正常细胞(cos7和hlf)几乎不显示荧光。为准确证实ivp
‑
02对癌细胞的选择性,将癌细胞a549和正常细胞hlf(a549和hlf均为人肺细胞)分别接种在不同的盖玻片上。然后将两个盖玻片放入同一个培养皿,并同时进行ivp
‑
02染色。在图5b中,只有上玻片上的a549细胞被照亮,而下玻片上的hlf细胞未被照亮。成像结果表明,ivp
‑
02可以选择性地区分癌细胞与正常细胞。
[0152]
在以上图片中,观察到癌细胞的胞质内的丝状结构,这些丝状结构是线粒体的典型形态。然后用商购线粒体探针mitotracker
tm deep red fm(mtdr)进行共染色实验(图6)。ivp
‑
02与mtdr的共定位系数为约0.9,表明ivp
‑
02在癌细胞线粒体中的定位。
[0153]
不希望受理论束缚,认为ivp
‑
02能够相对于正常细胞选择性地对癌细胞染色,所基于的部分原因是癌细胞与正常细胞相比更高的δψm。然而,某些对δψm也很敏感的商购线粒体探针却可以对癌细胞和正常细胞都进行染色。因此,δψm可能不是允许本文描述的化合物区分癌细胞与正常细胞的唯一参数。染料本身的化学结构可能也起重要作用。
[0154]
据推测,探针的膜通透性是其对癌细胞的选择性的关键因素,因为据报道,癌细胞的质膜比正常细胞更易渗透。因此,通过分别延长吡啶鎓盐侧和吲哚侧的烷基链来修饰ivp
‑
02以调节膜通透性。如图7a所示,获得了五个新的分子ivp
‑
04、ivp
‑
06、ivp
‑
22、ivp
‑
42和ivp
‑
62。方案1中描绘了这些新ivp分子的合成路线。它们的化学结构通过1h nmr、
13
c nmr和
19
f nmr充分表征。然后分别用这5种新分子对癌细胞a549染色。在图7b中,荧光图谱显示所有这些分子都对线粒体染色。在图7c中,与mtdr的共染色实验也证实了它们在a549细胞的线粒体中的位置。除了a549细胞外,对hela细胞也进行了同样的实验(图8和9)。结果与a549细胞相似,这表明ivp
‑
04、ivp
‑
06、ivp
‑
22、ivp
‑
42和ivp
‑
62能选择性地对癌细胞中的线粒体染色。
[0155]
分别用这些分子对与正常细胞cos7共培养的a549癌细胞进行染色。在图10a中,ivp
‑
02、ivp
‑
22、ivp
‑
42和ivp
‑
62仅对a549细胞染色,表明它们能够明显地区分癌细胞与正常细胞。有趣的是,ivp
‑
04和ivp
‑
06可以对a549和cos7细胞都染色,这意味着它们不能区分癌细胞与正常细胞。然后还用这些分子对与cos7细胞共培养的hela细胞(图11)、与hlf细胞共培养的a549细胞(图12)进行了染色,结果与同cos7细胞共培养的a549细胞的结果相似。除共培养外,还将a549细胞和hlf细胞接种在不同的盖玻片上,并用这些分子染色。成像结果(图10b)也与共培养结果相似,ivp
‑
04和ivp
‑
06可对a549和hlf细胞都染色,而其他四种分子仅对a549细胞染色。基于以上成像结果,可以得出结论,这些ivp分子对癌细胞的选择性也是基于吡啶鎓盐侧烷基链的长度。延长吡啶鎓盐侧的烷基链将消除对癌细胞的选择性。
[0156]
探讨了ivp分子进入细胞的机制。将癌细胞a549与ivp分子在4℃孵育20分钟。在图13中,在低温时,细胞内仍可观察到明显的荧光信号。该结果表明ivp分子通过扩散进入细胞。在一些已报道的工作中,研究人员发现,尽管亲脂性阳离子带有净正电荷,但它们具有呈相对脂溶性的不寻常性质。将亲脂性阳离子从水性环境移动到膜的非极性脂质内部所需的能量远远低于移动亲水阳离子所需的能量。从水性介质向膜的疏水核移动的活化能主要来自静电相互作用。主要的静电能组成部分波恩能(w
b
,图14a)是由在从水环境转移到膜的脂质核后除去阳离子中的水分子所需的焓输入所致。因w
b
较低,亲脂性阳离子能够容易地通过膜。图14a中的方程给出了波恩能,其中z是阳离子电荷,且r是离子半径。根据该方程,w
b
与离子半径成反比。对于这些ivp分子,离子半径是从分子电荷到周围水分子的平均距离。图14b是通过膜的亲脂性阳离子的示意图。除去亲脂性阳离子周围的水分子是第一步。对于亲脂性阳离子,离子半径越大,阳离子与水分子之间的相互作用越弱,w
b
越低;因此,分子更容易通过膜。
[0157]
回到这些ivp分子的化学结构,所有这些分子的吡啶鎓侧都带正电荷。这一侧更亲水,意味着更多的水分子在这一侧富集,因此这一侧决定了离子半径。此外,ivp
‑
02、ivp
‑
22、ivp
‑
42、ivp
‑
62在吡啶鎓侧的相似部分为2
‑
碳烷基链。ivp
‑
02、ivp
‑
22、ivp
‑
42、ivp
‑
62与ivp
‑
04、ivp
‑
06之间在吡啶鎓侧的区别在于烷基链的长度。ivp
‑
04和ivp
‑
06在吡啶鎓侧具有较长的烷基链,使得其离子半径大于ivp
‑
02、ivp
‑
22、ivp
‑
42、ivp
‑
62,意味着ivp
‑
04、ivp
‑
06与水分子之间的相互作用较弱。因此ivp
‑
04、ivp
‑
06的波恩能值低于ivp
‑
02、ivp
‑
22、ivp
‑
42、ivp
‑
62的波恩能值。如此一来,它们更容易通过膜。当对正常细胞染色时,ivp
‑
04、ivp
‑
06比ivp
‑
02、ivp
‑
22、ivp
‑
42、ivp
‑
62更易穿透细胞膜。
[0158]
监测细胞活力是生物学、病理学和医学的基础研究中非常有价值的任务。于是我们研究了ivp
‑
02是否能够监测细胞活力。δψm是表征细胞活力的非常重要的指标。随着细胞活力的损失,δψm将降低,而随着细胞活力的恢复,δψm也恢复到正常水平。因此,观察δψm的变化是监测细胞活力的有效方法。羰基氰化物间氯苯腙(cccp)是一种类型的质子载体,并且可通过缩减(collapsing)δψm引起线粒体的快速酸化。将癌细胞a549用ivp
‑
02预染色30分钟。在图15a中,开始时,ivp
‑
02对线粒体清晰地染色。随着cccp的加入,线粒体内的荧光强度降低,而核仁的荧光强度增加,说明ivp
‑
02从线粒体释放并迁移至核仁。然后,去除cccp后随着δψm的恢复,核仁中的荧光消失,而线粒体中的荧光逐渐恢复,说明ivp
‑
02迁回线粒体。除了a549细胞外,在hela细胞中也观察到类似的结果,在图16示出。过氧化氢
(h2o2)能抑制将导致细胞活力丧失的呼吸链的氧化。然后,将活a549和hela细胞用ivp
‑
02预染色,并用10mm h2o2处理。在图17中,可以看到,加入h2o2后,随着细胞活力下降,在核仁中观察到强荧光。这些结果表明ivp
‑
02可以通过线粒体
‑
核仁的迁移来监测癌细胞的活力。
[0159]
为了检测ivp
‑
02是否能选择性地对癌细胞染色并监测其活力,将癌细胞与正常细胞共培养并用ivp
‑
02染色。正如我们所预测的,图15b中仅清楚地显示了a549细胞中的线粒体形态。加入cccp后,ivp
‑
02从线粒体释放并迁移至核仁。除去cccp后,核仁中的荧光消失,而线粒体中的荧光逐渐恢复。在整个过程中,正常细胞cos7中观察到很少的荧光。也在与cos7细胞共培养的hela细胞中进行了同样的实验,在图15b中示出,并观察到类似的现象。这些结果表明,ivp
‑
02可以选择性地对癌细胞进行染色,并通过在共存的癌细胞和正常细胞中的线粒体
‑
核仁迁移来监测癌细胞的活力。
[0160]
除ivp
‑
02外,我们还进一步研究了其他ivp分子是否可以通过线粒体
‑
核仁迁移来监测癌细胞的活力。a549细胞分别用ivp
‑
04、ivp
‑
22、ivp
‑
42、ivp
‑
06和ivp
‑
62预染色,然后加入cccp。在图18中,在加入cccp后,随着δψm降低,只有ivp
‑
04、ivp
‑
22和ivp
‑
42能进入细胞核并对核仁染色,而ivp
‑
06和ivp
‑
62在很大程度上不能进入细胞核。除去cccp后,随着δψm的恢复,ivp
‑
04、ivp
‑
22和ivp
‑
42可迁回线粒体中。为了消除细胞干扰,对hela细胞进行了相同的实验,在图19中示出。与a549细胞一致,ivp
‑
02、ivp
‑
04、ivp
‑
22和ivp
‑
42能对核仁染色,而ivp
‑
06和ivp
‑
62则不能。基于这些结果可以得出结论,ivp
‑
02、ivp
‑
04、ivp
‑
22、ivp
‑
42可通过线粒体
‑
核仁迁移来监测癌细胞的活力。
[0161]
为什么ivp
‑
06和ivp
‑
62不能以显著的程度对癌细胞的核仁染色?一方面,当ivp分子位于线粒体内时,除了阳离子与线粒体内膜负电荷之间的静电相互作用外,还存在烷基链与磷脂之间的疏水相互作用。当δψm降低时,虽然静电相互作用减弱,但疏水相互作用仍然存在。ivp
‑
06和ivp
‑
62具有比其他四个ivp分子更长的烷基链,因此ivp
‑
06和ivp
‑
62与磷脂之间的疏水作用比其他四个ivp分子强。因此,ivp
‑
06和ivp
‑
62更倾向于留在线粒体,而ivp
‑
02、ivp
‑
04、ivp
‑
22和ivp
‑
42更容易从线粒体中逸出。另一方面,由于核仁富含rna,因此也应考虑到ivp分子对rna的亲和力。然后先进行rna滴定实验。在图20a和图21中,随着rna浓度的增加,所有分子的荧光强度都增加。基于斯卡查德方程,计算并归纳了这些分子与rna的结合常数(k),并归纳在图20c中。可以看出ivp
‑
06和ivp
‑
62的结合常数低于ivp
‑
02、ivp
‑
04、ivp
‑
22和ivp
‑
42。此外,还进行了基于ivp分子和rna结构的分子对接计算。在图20b和图21中,ivp分子结合至rna的小凹槽,计算结合能(e)并总结在图20c中。计算的ivp
‑
02、ivp
‑
04、ivp
‑
22和ivp
‑
42的结合能也高于ivp
‑
06和ivp
‑
62,表明ivp
‑
02、ivp
‑
04、ivp
‑
22和ivp
‑
42对rna的亲和力比ivp
‑
06和ivp
‑
62更强。
[0162]
考虑到800nm激发的ivp
‑
02的高双光子吸收截面值,我们在活hela细胞中进行了ivp
‑
02的体外双光子成像。如图22a所示,从细胞质中线粒体的丝状结构可以清楚地收集到具有高保真度的明亮双光子荧光,表明ivp
‑
02在双光子成像方面具有巨大的潜力。
[0163]
对于活细胞成像,应认真考虑生物探针的潜在长期细胞毒性。然后我们通过标准mtt测定研究了这些ivp分子对活a549细胞的细胞毒性。在图22b中,可以清楚地看到,在与浓度小于5μm的ivp分子孵育24h后,a549细胞的活力高于80%,显示出极低的细胞毒性。当孵育浓度为10μm时,细胞活力在60%至80%之间,显示出一定的细胞毒性。不过,本研究中的所有细胞成像实验均在2μm的低浓度下进行,这是合理和可接受的。
[0164]
实施例
[0165]
由于ivp分子的合成路线和实验程序非常相似,这里我们以ivp
‑
02为例。
[0166]
合成ivp
‑
02:先合成化合物1
‑
乙基
‑4‑
甲基吡啶
‑1‑
鎓碘。将4
‑
甲基吡啶(1ml,10mmol)溶解于乙醇(5ml)中并加入碘乙烷(1ml,12mmol)。使混合物在78℃搅拌过夜。然后将反应混合物倒入石油醚中,并过滤浅黄色固体。重结晶后,得到浅黄色固体化合物1
‑
乙基
‑4‑
甲基吡啶
‑1‑
鎓碘(2.24g,90%)。然后合成ivpi
‑
2。向溶于甲醇(5ml)中的1h
‑
吲哚
‑3‑
甲醛(0.15g,1mmol)和化合物1
‑
乙基
‑4‑
甲基吡啶
‑1‑
鎓碘(0.25g,1mmol)的溶液中加入吡咯烷(200μl)。将混合物在室温搅拌5h。然后将反应混合物倒入石油醚中,并过滤橙色固体。重结晶后,获得橙色固体(0.26g,65%)ivpi
‑
12。最后,合成ivp
‑
02。将ivpi
‑
2(0.11g,0.3mmol)溶解于丙酮(10ml)中,并加入kpf6(0.55g,3mmol)溶液。将混合物在室温搅拌24小时。在减压下除去丙酮,并使用ch2cl2/meoh混合物(8:1,v/v)作为洗脱剂通过硅胶色谱法纯化残余物,得到橙红色固体(66mg,56%)。
[0167]1h nmr(400mhz,dmso
‑
d6),δ(ppm):11.92(s,1h),8.77(d,j=6.60hz,2h),8.25(d,j=16.20hz,1h),8.15(dd,j=11.70hz,6.80hz,3h),7.97(s,1h),7.51(dd,j=6.90hz,1.90hz,1h),7.34
‑
7.19(m,3h),4.44(q,j=7.30hz,2h),1.51(t,j=7.30hz,3h).
13
c nmr(100mhz,meod
‑
d4),δ(ppm):155.14,141.82,137.43,136.53,131.42,127.88,124.43,122.33,121.28,120.65,119.31,115.68,113.49,111.38,54.41,14.56.
19
f nmr(376mhz,meod
‑
d4),δ(ppm):(
‑
73.73,3f),(
‑
75.61,3f).hrms m/z:c
17
h
17
n
2
的计算值为249.1386,实测值为49.1375([m]
)。
[0168]
对于ivp
‑
04,1h nmr(400mhz,dmso
‑
d6),δ(ppm):11.95(s,1h),8.76(d,j=6.60hz,2h),8.25(d,j=16.20hz,1h),8.14(dd,j=11.80hz,7.50hz,3h),7.97(s,1h),7.52(dd,j=7.00hz,1.90hz,1h),7.35
‑
7.21(m,3h),4.41(t,j=7.3hz,2h),1.86(q,j=7.40hz,2h),1.29(m,2h),0.93(t,j=7.40hz,3h).
13
c nmr(100mhz,dmso
‑
d6),δ(ppm):154.34,143.09,137.36,136.30,132.27,124.66,122.82,121.71,120.05,116.60,113.41,112.45,58.69,32.25,18.62,13.16.
19
f nmr(376mhz,dmso
‑
d6)δ(ppm):
‑
69.18(s,3f),
‑
71.07(s,3f).
[0169]
对于ivp
‑
06,1h nmr(400mhz,丙酮
‑
d6),δ(ppm):11.12(s,1h),8.87
‑
8.81(m,2h),8.35(d,j=16.20hz,1h),8.24(d,j=6.60hz,2h),8.17(d,j=7.60hz,1h),8.02(d,j=2.60hz,1h),7.60(d,j=7.80hz,1h),7.45(d,j=16.20hz,1h),7.37
‑
7.22(m,2h),4.67(t,j=7.50hz,2h),1.47
‑
1.30(m,6h),0.90(t,j=6.90hz,3h).
13
c nmr(100mhz,丙酮
‑
d6),δ(ppm):154.88,142.59,137.40,136.32,131.79,124.60,122.59,121.61,120.89,120.85,119.74,116.36,113.62,111.93,59.44,30.33,30.29,24.88,21.51,12.65.
19
f nmr(376mhz,丙酮
‑
d6),δ(ppm):
‑
71.62(s,3f),
‑
73.50(s,3f).
[0170]
对于ivp
‑
22,1h nmr(400mhz,meod
‑
d4),δ(ppm):8.55(d,j=5.60hz,2h),8.15(d,j=16.10hz,1h),8.07(dd,j=7.30hz,1.50hz,1h),8.00(d,j=7.00hz,2h),7.87(s,1h),7.53(d,j=7.90hz,1h),7.34
‑
7.17(m,3h),4.45(q,j=7.30hz,2h),4.29(q,j=7.30hz,2h),1.59(m,3h),1.49(m,3h).
13
c nmr(100mhz,dmso
‑
d6),δ(ppm):154.21,142.94,136.86,135.59,133.89,125.38,122.81,121.75,121.22,120.48,116.64,112.62,110.84,54.37,40.76,15.98,15.00.
19
f nmr(376mhz,meod
‑
d4)δ(ppm):
‑
73.84(s,3f),
‑
75.72(s,3f)。
[0171]
对于ivp
‑
42,1h nmr(400mhz,dmso
‑
d6),δ(ppm):8.77(d,j=6.60hz,2h),8.26
‑
8.15(m,2h),8.13(d,j=6.60hz,2h),8.01(s,1h),7.63(d,j=8.00hz,1h),7.36
‑
7.24(m,3h),4.44(q,j=7.40hz,2h),4.27(t,j=7.00hz,2h),1.78(t,j=7.50hz,2h),1.51(t,j=7.20hz,3h),1.25(dd,j=14.30hz,6.90hz,2h),0.90(t,j=7.30hz,3h).
13
c nmr(100mhz,dmso
‑
d6),δ(ppm):154.20,142.94,137.15,135.57,134.52,125.31,122.81,121.76,121.18,120.46,116.71,112.52,110.95,54.37,45.54,31.39,19.25,15.97,13.34.
19
f nmr(376mhz),δ(ppm):
‑
69.17(s,3f),
‑
71.05(s,3f).
[0172]
对于ivp
‑
62,1h nmr(400mhz,meod
‑
d4),δ(ppm):8.49(d,j=6.70hz,2h),8.14
‑
8.01(m,2h),7.94(d,j=6.90hz,2h),7.83(s,1h),7.50(dd,j=7.60hz,1.40hz,1h),7.34
‑
7.24(m,2h),7.17(d,j=16.10hz,1h),4.42(q,j=7.40hz,2h),4.22(t,j=7.10hz,2h),1.86(t,j=7.20hz,2h),1.58(t,j=7.30hz,3h),1.35
‑
1.26(m,6h),0.92
‑
0.80(m,3h).
13
c nmr(100mhz,dmso
‑
d6),δ(ppm):154.21,143.25,142.93,137.15,135.59,134.53,125.54,125.30,122.81,121.77,121.19,120.46,119.10,116.70,112.52,110.94,54.37,45.82,30.60,29.26,25.65,21.82,15.96,13.69.
19
f nmr(376mhz,meod
‑
d4),δ(ppm):
‑
73.45(s,3f),
‑
75.33(s,3f).
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。

