ehdv
‑
2型单克隆抗体、制备源细胞株、产物应用及试剂盒
技术领域
1.本发明涉及病毒抗体检测领域,尤其涉及流行性出血病病毒2型单克隆抗体、制备源细胞株及其试剂盒。
背景技术:
2.流行性出血病病毒2型简写ehdv
‑
2型。ehd
‑
2型属于ehd九种血清型中的一种。ehd不同的血清型毒株对牛的致病性差异较大。现有的研究认为仅ehdv
‑
2型的其中1个毒株
‑
茨城病病毒(ibaraki virus,ibav)对牛有较强致病性,其引起牛的突发高热、咽喉麻痹、关节疼痛性肿胀等症状。我国每年从国外进口10万
‑
20万头种牛,加强ehdv
‑
2型病毒抗体的监测,是保障我国种牛健康养殖的措施之一。
3.ehd抗体检测方法,现有中和试验(vn)、琼扩试验和elisa检测方法,其中中和试验实验环境要求高,需要生物安全一定级别实验室进行,试验周期长3
‑
5天;琼扩试验需要有经验的实验员观察判定,不能数字显示检测结果;elisa方法,通过酶联免疫分析仪读取,结果以数字化形式判定,客观、准确,具有较强的使用优势。本专利研制的ehd
‑
2型b
‑
elisa抗体检测方法,主要针对ehd感染牛致病性的毒株产生的抗体检测而设计,具有显著的针对性,对于ehd感染牛的防控意义较大,同时研制的试剂盒其检测灵敏性、特异性等指标均与oie推荐的类似方法相近。
技术实现要素:
4.本发明要解决的技术问题在于,利用制备的ehd
‑
2型单克隆抗体、ehd
‑
2型病毒包被的elisa板,组装试剂盒,试剂盒检测指标达到国际认可的检测值。
5.本发明解决上述技术问题的技术方案是,一种制备流行性出血病病毒2型单克隆抗体的细胞株,该细胞株:杂交瘤细胞株ehd e2c5,保藏时间:2021年8月12日,保藏编号:cctcc no:c2021180,保藏单位:中国典型培养物保藏中心,地点:中华人民共和国湖北省武汉市武汉大学保藏中心。
6.使用上述的细胞株制备流行性出血病病毒2型单克隆抗体的方法,该方法包括以下步骤:在杂交瘤细胞株ehd e2c5中提取流行性出血病病毒2型单克隆抗体,注射小鼠腹腔,取腹水纯化制备而得。
7.上述的方法,包括以下步骤:
8.(1)用纯化的ehdv
‑
2型灭活病毒,分别加等体积弗氏完全佐剂(fca)乳化和弗氏不完全佐剂(fia)乳化,先后免疫balb/c小鼠(balb/c小鼠)三次;
9.(2)取免疫小鼠的脾细胞与sp2/0骨髓瘤细胞在50%聚乙二醇(mw1500)融合剂下融合,hat培养基筛选杂交瘤细胞,用间接elisa方法检测分泌抗ehdv
‑
2病毒的阳性孔;用有限稀释法进行细胞克隆,经间接elisa筛选阳性克隆,获得能稳定传代并分泌抗ehdv
‑
2病毒蛋白的特异性单克隆抗体的杂交瘤细胞株ehd e2c5。
10.上述方法制备产物的应用,所述的流行性出血病病毒2型单克隆抗体针对口蹄疫a
型或asia i型或蓝舌病或赤羽病或病毒性腹泻无任何免疫反应。
11.上述方法制备产物的应用,所述的流行性出血病病毒2型单克隆抗体仅针对ehdv
‑
2病毒的抗原决定簇
12.上述方法制备产物的应用,所述的流行性出血病病毒2型单克隆抗体仅与ehdv
‑
2病毒及ehd抗原有特异性免疫反应。
13.一种抗体试剂盒,所述的试剂盒包括如上述的流行性出血病病毒2型单克隆抗体。
14.上述述的抗体试剂盒,所述的试剂盒还包括流行性出血病病毒2型抗原预包被板、强阳性对照、弱阳性对照、阴性对照、hrp羊抗鼠二抗、20倍浓缩洗涤液、稀释液、底物液以及终止液。
15.上述20倍浓缩洗涤液为20倍浓缩的含0.05%~0.5%tween
‑
20的0.01mol/lph7.4 pbst;稀释液为含1%~10%bsa、0.05%~0.5%tween
‑
20ph7.4的pbs;底物液为可溶性tmb;终止液为1
‑
2mol/l h2so4溶液。
16.上述的抗体试剂盒各组成部分的体积或数量如下:流行性出血病病毒2型抗原预包被板2块;ehd
‑
2型单克隆抗体0.3ml;强阳性对照0.6ml;弱阳性对照0.6ml;阴性对照0.6ml;hrp标记羊抗鼠二抗0.3ml;20倍浓缩洗涤液50ml;稀释液60ml;底物液25ml;终止液25ml;封板纸6张;说明书1份。
17.所述ehdv
‑
2型病毒包被板通过以下方法制备:
18.ehdv
‑
2病毒接种于长成单层的bhk21细胞,5%co
2 37℃培养3d
‑
5d,细胞出现缩圆脱落后,
‑
20℃冻融细胞3次,收集病毒液。用ph4.0柠檬酸缓冲液透析24h,再用ph7.0 pbs透析24h,收集病毒液。病毒液中加入等体积饱和硫酸铵,沉淀2h,离心弃上清,取沉淀,用pbs溶解,作为包被用抗原。ehdv
‑
2型病毒抗原按照1:500~1:1000比列,用ph9.0
‑
10.0碳酸盐缓冲液稀释,每孔100ul加入康宁公司高吸附可拆酶标板,4℃放置18~24h,洗板3次,用含1%~10%bsa pbs缓冲液封闭1h,pbst洗板,干燥1h~3h制得。
19.一种如上所述的试剂盒的制备方法,包括:
20.(1)使用ehdv
‑
2型抗原预包被板;
21.(2)使用纯化的灭活ehdv
‑
2病毒免疫balb/c小鼠,取免疫小鼠的脾细胞,将所述脾细胞与sp2/0骨髓瘤细胞在融合剂下融合后筛选获得杂交瘤细胞株ehd e2c5,取杂交瘤细胞上清,利用proteing柱纯化的ehdv
‑
2型单克隆抗体。
22.在本发明所述的试剂盒的制备方法中,还包括强阳性对照、弱阳性对照、阴性对照、hrp标记羊抗鼠二抗、20倍浓缩洗涤液、稀释液、底物液以及终止液,并将所述液体和ehdv
‑
2型抗原预包被板、ehdv
‑
2单克隆抗体分开放置。
23.本发明的试剂盒采用阻断elisa检测牛、羊和鹿等动物血清ehdv
‑
2病毒抗体,可用于ehdv
‑
2及ehd其它血清型病毒血清抗体的快速检测和流行病学调查。
24.本发明有益效果为,试剂盒中ehdv
‑
2型病毒单克隆抗体通过ehdv
‑
2型灭活病毒免疫balbc小鼠,取其脾细胞与骨髓瘤细胞融合而制得;通过单克隆抗体与ehd
‑
2灭活病毒,优化反应条件制备的ehdv
‑
2型病毒阻断elisa抗体检测试剂盒,操作程序简单,检测结果、技术性能指标均等同于世界动物卫生组织(oie)推荐的ehd elisa抗体检测方法。
具体实施方式
25.本发明提供一种制备流行性出血病病毒2型单克隆抗体的细胞株,该细胞株:杂交瘤细胞株ehd e2c5,保藏时间:2021年8月12日,保藏编号:cctcc no:c2021180,保藏单位:中国典型培养物保藏中心,地点:中华人民共和国湖北省武汉市武汉大学保藏中心。
26.使用上述的细胞株制备流行性出血病病毒2型单克隆抗体的方法,该方法包括以下步骤:在杂交瘤细胞株ehd e2c5中提取流行性出血病病毒2型单克隆抗体,注射小鼠腹腔,取腹水纯化制备而得。
27.上述的方法,包括以下步骤:
28.(1)用纯化的ehdv
‑
2型灭活病毒,分别加等体积弗氏完全佐剂(fca)乳化和弗氏不完全佐剂(fia)乳化,先后免疫balb/c小鼠(balb/c小鼠)三次;
29.(2)取免疫小鼠的脾细胞与sp2/0骨髓瘤细胞在50%聚乙二醇(mw1500)融合剂下融合,hat培养基筛选杂交瘤细胞,用间接elisa方法检测分泌抗ehdv
‑
2病毒的阳性孔;用有限稀释法进行细胞克隆,经间接elisa筛选阳性克隆,获得能稳定传代并分泌抗ehdv
‑
2病毒蛋白的特异性单克隆抗体的杂交瘤细胞株ehd e2c5。
30.上述方法制备产物的应用,所述的流行性出血病病毒2型单克隆抗体针对口蹄疫a型或asia i型或蓝舌病或赤羽病或病毒性腹泻无任何免疫反应。
31.上述方法制备产物的应用,所述的流行性出血病病毒2型单克隆抗体仅针对ehdv
‑
2病毒的抗原决定簇
32.上述方法制备产物的应用,所述的流行性出血病病毒2型单克隆抗体仅与ehdv
‑
2病毒及ehd抗原有特异性免疫反应。
33.一种抗体试剂盒,所述的试剂盒包括如上述的流行性出血病病毒2型单克隆抗体。
34.上述述的抗体试剂盒,所述的试剂盒还包括流行性出血病病毒2型抗原预包被板、强阳性对照、弱阳性对照、阴性对照、hrp羊抗鼠二抗、20倍浓缩洗涤液、稀释液、底物液以及终止液。
35.上述20倍浓缩洗涤液为20倍浓缩的含0.05%~0.5%tween
‑
20的0.01mol/l ph7.4 pbst;稀释液为含1%~10%bsa、0.05%~0.5%tween
‑
20ph7.4的pbs;底物液为可溶性tmb;终止液为1
‑
2mol/l h2so4溶液。
36.上述的抗体试剂盒各组成部分的体积或数量如下:ehdv
‑
2抗原预包被板2块;ehd
‑
2型单克隆抗体0.3ml;强阳性对照0.6ml;弱阳性对照0.6ml;阴性对照0.6ml;hrp标记羊抗鼠二抗0.3ml;20倍浓缩洗涤液50ml;稀释液60ml;底物液25ml;终止液25ml;封板纸6张;说明书1份。
37.一种ehdv
‑
2病毒单克隆抗体的制备和相应的elisa抗体检测试剂盒,该试剂盒包括分别放置的ehdv
‑
2抗原预包被板,ehdv
‑
2病毒特异性单克隆抗体。
38.此外,在上述试剂盒中,还包括分别放置的强阳性对照、弱阳性对照、阴性对照、hrp标记羊抗鼠二抗、20倍浓缩洗涤液、稀释液、底物液以及终止液。其中所述20倍浓缩洗涤液为20倍浓缩的含0.05%~0.1%tween
‑
20的0.01mol/l ph 7.4pbst;稀释液为含1%~10%bsa、0.05%~0.1%tween
‑
20ph7.4的pbs;底物液为可溶性tmb;终止液为1mol/l h2so4溶液。
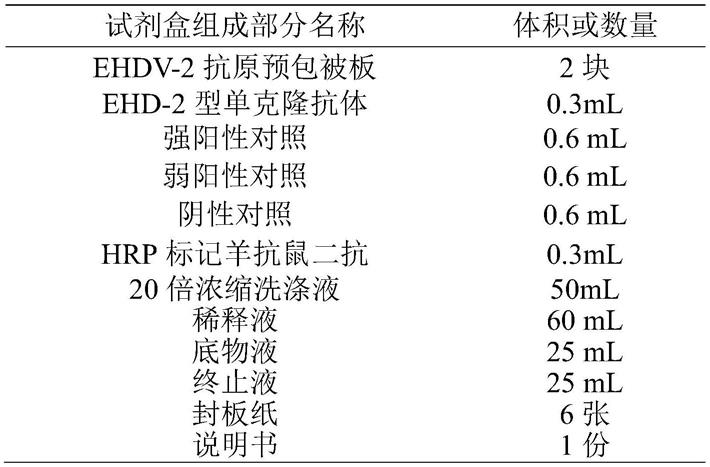
39.为了便于使用,上述试剂盒的各组成部分的体积或数量如下:
[0040][0041]
以下提供制备上述试剂盒的具体实例:
[0042]
1.制备ehdv
‑
2抗原预包被板:ehdv
‑
2病毒接种于长成单层的bhk21细胞,5%co
2 37℃培养3天,细胞出现缩圆,脱落后,
‑
20℃冻融细胞3次,收集病毒液。用ph4.0柠檬酸缓冲液透析24h,再用ph7.0 pbs透析24h,收集病毒液。病毒液中加入等体积饱和硫酸铵,沉淀2h,离心弃上清,取沉淀,用pbs溶解,作为包被用抗原。ehdv
‑
2型病毒抗原按照1:500~1:1000比列,用ph9.0
‑
10.0碳酸盐缓冲液稀释,每孔100ul加入康宁公司高吸附可拆酶标板,4℃放置18~24h,洗板3次,用含1%~10%bsa pbs缓冲液封闭1h,pbst洗板,干燥1h~3h制得。
[0043]
2、制备抗ehdv
‑
2型病毒单克隆抗体:用纯化的ehdv
‑
2型灭活病毒,分别加等体积弗氏完全佐剂(fca)乳化和弗氏不完全佐剂(fia)乳化,先后免疫balb/c小鼠(balb/c小鼠)三次;取免疫小鼠的脾细胞与sp2/0骨髓瘤细胞在50%聚乙二醇(mw1500)融合剂下融合,hat培养基筛选杂交瘤细胞,用间接elisa方法检测分泌抗ehdv
‑
2病毒的阳性孔;用有限稀释法进行细胞克隆,经间接elisa筛选阳性克隆,获得能稳定传代并分泌抗ehdv
‑
2病毒蛋白的特异性单克隆抗体的杂交瘤细胞株ehd e2c5;用间接elisa方法鉴定制备的单克隆抗体仅与ehdv
‑
2病毒蛋白抗原有特异性免疫反应,而与其它相关病毒(如口蹄疫a型、asia i型,蓝舌病、赤羽病、病毒性腹泻等)没有任何免疫反应。
[0044]
3、制备强阳性对照:挑选体格健壮的16个月以上的山羊2~3只,将灭活的ehdv
‑
2病毒经背部皮下注射,5ml/只;首免后第2周和第4周分别用ehdv
‑
2病毒进行二免和三免;待山羊血清中抗ehdv
‑
2病毒抗体,酶联免疫吸附试验效价达1:100以上,无菌采血分离血清,离心或过滤除去沉淀,抽滤除菌,3ml/管分装,贴上标签,
‑
80℃保存。
[0045]
4、阴性对照的制备:选择体格健壮的18个月以上的山羊,采血用oie(2010)《ehdv病毒中和试验》检测方法确认血清中是否有ehdv
‑
2病毒抗体,证实无ehdv
‑
2病毒抗体的山羊,无菌采血分离血清。3ml/管分装,贴上标签,
‑
80℃保存。
[0046]
5、制备弱阳性对照:利用阴性对照,倍比稀释ehdv
‑
2病毒强阳性对照,采用oie推荐的elisa方法进行效价测定,与国际标准阳性血清进行比较,制备ehdv
‑
2病毒弱阳性对照。
[0047]
6、包被缓冲液:0.05mol/lph9.6碳酸盐缓冲液(nahco31.465g、na2co30.795g或na2co3.10h2o 1.2g、水500ml)。溶解后过滤除菌,置于4℃冰箱,一周内使用。
[0048]
7、单克隆抗体制备:取5d3杂交瘤细胞株,利用20%胎牛血清的imdm培养基进行培养,收集细胞上清,8000rpm离心,取上清利用proteing柱进行纯化,纯化后,稀释成0.48mg/ml进行保存。
[0049]
8、底物液:tiangen(中国),可溶性单组份tmb(货号:pa107
‑
01)。
[0050]
9、20倍浓缩洗涤液、稀释液、底物液、终止液的优选:本发明通过试验,选定如下最佳的洗涤液、稀释液,终止液配方。
[0051]
20倍浓缩洗涤液配方:nacl160g,kh2po
4 4.8g,na2hpo429g,kcl4g,tween
‑
20 10ml,蒸馏水1000ml,充分溶解,过滤除菌后分装。用时作20倍稀释。
[0052]
稀释液配方:nacl8g,kh2po
4 0.24g,na2hpo41.44g,kcl 0.2g,蒸馏水1000ml,充分溶解,加入3%bsa,过滤除菌后分装。
[0053]
终止液:将10.87ml初始浓度为95%~98%的硫酸缓慢加入到89.13ml的去离子水中混匀,即为终止液。
[0054]
10、羊抗鼠二抗:采用商品化的辣根过氧化物酶标记的羊抗鼠抗体(usa,kpl公司,货号074
‑
1806,1.0mg),作1:50稀释。
[0055]
11、试剂盒的组装:将按上述方法制备好的ehdv
‑
2抗原预包被板、单克隆抗体、hrp羊抗鼠二抗、稀释液、20倍浓缩洗涤液、底物液、终止液、强阳性对照、弱阳性对照、阴性对照定量分装,分别贴上标签与说明。1份详细的试剂盒使用操作说明书。6张贴板纸。装入专用的试剂盒外壳内,外壳上贴上试剂盒标签。
[0056]
12、试剂盒中各种试液的配制与分装
[0057]
试剂盒中试液的配制分装表
[0058][0059]
使用上述试剂盒进行检测操作的程序如下:
[0060]
1.试剂工作液的配置
[0061]
pbst洗液:利用试剂盒提供的20
×
洗液(洗液中如出现沉淀,请37℃加热使其溶解),用去离子水或蒸馏水进行20倍稀释,即为pbst洗液
[0062]
ehdv
‑
2单克隆抗体工作液:用试剂盒提供的稀释液按1:50稀释ehdv单克隆抗体
(如:10μl单克隆抗体 490μl试剂盒提供稀释液),即为ehdv单克隆抗体工作液。
[0063]
hrp羊抗鼠二抗工作液:用试剂盒提供的稀释液进行1:100稀释hrp羊抗鼠二抗(如:10μlhrp羊抗鼠二抗 990μl稀释液),即为hrp羊抗鼠二抗工作液。
[0064]
2.操作步骤:
[0065]
计算测试样品数量,取所需测试elisa板条,进行试验。
[0066]
(1)每孔加入30μl稀释液,然后分别加入:
[0067]
a:加20μl稀释液到a1,a2孔;
[0068]
b:加20μl待检血清样品到测试孔中,每孔加一份样品;
[0069]
c:加20μl强阳性对照到b1,b2,c1,c2孔;
[0070]
d:加20μl弱阳性对照到d1,d2,e1,e2孔;
[0071]
e:加20μl阴性对照到f1,f2,g1,g2孔;
[0072]
37℃连续震荡反应1h;
[0073]
(2)不要洗板。
[0074]
a1,a2孔加50μl稀释液,其余每孔加入50μlehdv
‑
2型单克隆抗体工作液。
[0075]
(3)37℃连续震荡反应45min。
[0076]
(4)用pbst洗液,每孔加250μl,洗板3次,甩干。
[0077]
(5)每孔加入hrp羊抗鼠二抗工作液100μl,37℃连续震荡反应30min。
[0078]
(6)用pbst洗液,每孔加250μl,洗板3次,甩干。
[0079]
(7)每孔加入底物液100μl,37℃避光静置10min~15min。
[0080]
(8)每孔加终止液100μl
[0081]
(9)用elisa仪,在450nm波长下读数。
[0082]
3.结果判定:
[0083]
①
计算公式:
[0084]
s/m=100
‑
血清样本平均od值/m孔平均od值*100
[0085]
②
判定标准:
[0086]
pi结果≤50阳性>50阴性
[0087]
注:若每份样品做双孔,在结果判定时如出现1孔s/m值小于等于50,1孔pi值大于50时,需重新检测。
[0088]
注:1.试剂盒置4℃保存。
[0089]
2.可疑样品,需用其它方法进行检测。
[0090]
试剂盒阳性判定值的确定:按照上述试剂盒的检测程序,采用oie(2010)《ehd病毒中和试验》检测方法确认的30份阴性对照和120份阳性血清,进行b
‑
elisa试验后,结果所有阳性血清的s/m≤50%,所有阴性s/m>50。因此,获得belisa阴性判定值(cut
‑
off value)为:s/m≤50被检血清ehdv
‑
2型抗体阳性;反之阴性。
[0091]
试剂盒的临床样品检测与应用以及试剂盒敏感性、特异性的评价:按照上述试剂盒的检测程序,用oie(2010)《ehd病毒中和试验》检测方法确认的30份阴性对照和30份阳性血清,进行belisa试验。统计获得试剂盒的特异性为97%(阴性结果数/阴性样品总数=29/
30),敏感性为90%(阳性结果数/阳性样品总数=27/30),本试剂盒的特异性、敏感性为良好。
[0092]
上述具体实施例的实验数据表明,本发明的ehdv
‑
2型病毒抗体阻断酶联免疫吸附试验(b
‑
elisa)试剂盒特异性强,敏感性高,适用于鹿流行性出血病病毒的快速诊断、检测、检疫和流行病学调查。
[0093]
以上所述,仅为本发明较佳的具体实施方式,但本发明的保护范围并不局限于此,任何熟悉本技术领域的技术人员在本发明揭露的技术范围内,可轻易想到的变化或替换,都应涵盖在本发明的保护范围之内。因此,本发明的保护范围应该以权利要求的保护。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。

