一种扩增抗感染用药基因snp位点用引物组、检测引物组及其应用
技术领域
1.本发明属于基因检测技术领域,具体涉及一种扩增抗感染用药基因snp位点用引物组、检测引物组及其应用。
背景技术:
2.抗感染药物是指用于治疗病原体(细菌、病毒、真菌、衣原体、支原体、螺旋体等)所致感染的各种药物。在使用抗感染药物的时,相同的药物剂量用于不同的个体产生的药物反应有很大差异,造成这种差异的原因包括内在因素和外在因素,其中内在因素的主要因素是个体的遗传物质,即基因型的差异。
3.常用的抗感染用药包括伏立康唑、红霉素、利福平、异烟肼、奥司他韦、利巴韦林等。伏立康唑大部分个体差异可由其cyp2c19基因多态性来解释,cyp2c19是细胞色素p450家族成员,cyp2c19基因存在多种等位基因,其中等位基因*1为正常代谢型,*2,*3,*4,*5,*6,*8为慢代谢型,*17为超快代谢型。因此,不同基因型的患者应采用不同剂量的伏立康唑治疗。红霉素是大环内酯类抗生素的一种,抗菌谱和青霉素相似,对革兰阳性菌如金葡菌、溶血性链球菌等均有强大的抗菌作用,对革兰氏阴性菌也有一定的作用。临床研究表明,葡萄糖
‑6‑
磷酸脱氢酶缺乏症患者(g6pd基因突变),使用红霉素会造成溶血等恶性毒副作用。药物基因组学研究还表明,abcc2基因多态与红霉素代谢速度相关。利福平主要用于布鲁氏菌病及敏感分支杆菌属感染的治疗性用药。可致恶心、呕吐、食欲不振、腹泻、胃痛、腹胀等胃肠道反应,还可引起多种过敏反应。临床研究提示,nat1/nat2基因的遗传多态性会影响异烟肼在体内的代谢,从而引起毒副作用。异烟肼主要用于各型肺结核的进展期、溶解播散期、吸收好转期,还可用于结核性脑膜炎和其他肺外结核。此外,异烟肼对痢疾、百日咳、麦粒肿等也有一定疗效。不良反应有胃肠道症状(如食欲不振、恶心、呕吐、腹痛、便秘等)、血液系统症状(贫血、白细胞减少、嗜酸细胞增多,引起血痰、咯血、鼻出血、眼底出血等)、肝损害;过敏(皮疹或其他)、内分泌失调(男子女性化乳房、泌乳、月经不调、阳萎等)。临床研究提示,大剂量或长期应用异烟肼时,慢乙酰化者较易引起血液系统、内分泌系统和神经及精神系统的反应;快乙酰化者则较易引起肝脏损害,而nat1/nat2基因的表达产物能够参与体内异烟肼的乙酰化过程。奥司他韦(商品名“达菲”)是一种抑制神经氨酸酶的抗病毒药物,可以用于甲型与乙型流感的治疗;同时,对于流感并发症高风险的人群,如孕妇、小于5岁的儿童、大于65岁的老人、慢性病患者、重度肥胖者等,也可作为预防用药。有相关药物代谢动力学研究显示,ces1基因中rs200707504位点多态性能够影响奥司他韦在体内的代谢速率,从而影响治疗效果。利巴韦林具广谱抗病毒作用,对多种病毒,如丙型肝炎、呼吸道合胞病毒、流感病毒、单纯疱疹病毒等有抑制作用;对流感(流感病毒a和b引起)、腺病毒肺炎、甲型肝炎、疱疹、麻疹等有防治作用。大剂量应用(包括滴鼻)可致心脏损害,对有呼吸道疾病者,如慢性阻塞性肺病或哮喘,可致呼吸困难、胸痛等。有临床研究表明,ifnl3/ifnl4基因中多个基因位点多态性对丙型肝炎的治疗效果有影响。
buffer、0.6μl 25mm mg
2
、0.2μl 10mm dntp、0.15μl 1u hotstartaqpolymerase、1μl dna模板和1μl多重pcr引物混合液,用超纯水补足10μl;所述多重pcr引物混合液包含所述扩增抗感染用药基因snp位点用引物组,所述引物组中每条引物的浓度为1~3μm;
20.步骤2)中所述多重pcr扩增的反应程序:95℃5min;94℃20s,65℃40s,72℃1.5min,11个循环;94℃20s,59℃30s,72℃1.5min,20个循环;72℃2min。
21.优选的,步骤3)中所述多重延伸反应的反应体系为10μl:5μl snapshot multiplex kit、2μl纯化后多重pcr扩增产物、1μl延伸引物混合物和2μl超纯水;所述延伸引物混合物中各条单碱基延伸引物的浓度为1~3μm;
22.步骤3)中所述多重延伸反应的反应程序:96℃1min;96℃10s,55℃5s,60℃30s,28个循环。
23.本发明提供的扩增抗感染用药基因snp位点用引物组包括核苷酸序列如序列表seq id no:1~seq id no:28所示的引物。所述引物组可同时扩增涉及13种药物、6种药物有效成分的8个用药相关基因的14个snp位点的dna片段,实现多种抗感染用药基因snp位点的多重pcr扩增。本发明提供的引物组不仅能有效提高检测效率,而且还能大大降低检测成本。
24.本发明提供的检测抗感染用药基因snp位点多态性用引物组,包括所述扩增抗感染用药基因snp位点用引物组和核苷酸序列如序列表seq id no:29~seq id no:42所示的单碱基延伸引物。所述引物组具有以下优点:1)涵盖常用抗感染用药种类、药品有效成分多,包括13种药物、6种药物有效成分的用药;2)涵盖的基因、snp位点数量多,包括8个基因、14个snp位点;3)基因位点的置信等级高,依据遗传药理学知识库(pharmgkb)数据,本检测方法中涉及的14个snp位点,置信等级1级的有9个,2级的有2个,3级的有2个,4级的有1个;4)针对中国人自己的基因数据库进行基因位点设计和优化,有效性高;5)该方法灵敏度高,仅需1ng dna即可实现,广泛适用于血卡、口腔试子等微量dna样本;6)检测效率高,一次实验可检测384个样本,全部实验流程6小时内完成;7)通量高,通过snapshot snp分型技术,仅需一次可实现多个位点的检测。
附图说明
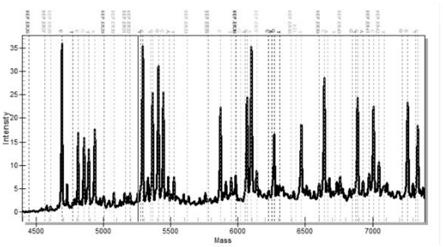
25.图1为本发明实施例中一个样本的所有目标snp位点检测结果图谱。
具体实施方式
26.本发明提供了一种扩增抗感染用药基因snp位点用引物组,包括核苷酸序列如序列表seq id no:1~seq id no:28所示的引物。本发明还提供了一种检测抗感染用药基因snp位点多态性用引物组,包括所述扩增抗感染用药基因snp位点用引物组和核苷酸序列如序列表seq id no:29~seq id no:42所示的单碱基延伸引物。snp位点的pcr扩增引物组和单碱基延伸引物的序列如表1所示。
27.表1本发明目标snp位点的pcr扩增引物序列和单碱基延伸引物序列
[0028][0029][0030]
本发明提供了所述引物组或所述引物组在检测抗感染用药基因snp位点多态性中的应用。
[0031]
在本发明中,所述抗感染用药的种类、药物有效成分、药物靶向基因及所述基因中snp位点的关系见表2。
[0032]
表2抗感染用药相关基因与snp位点对应关系
[0033][0034]
本发明提供了一种抗感染用药基因snp位点多态性的检测方法,包括以下步骤:
[0035]
1)提取待测样本的基因组dna;
[0036]
2)以提取的dna为模板,用所述引物组进行多重pcr扩增,得到多重pcr扩增产物;
[0037]
3)所述多重pcr扩增产物经纯化后在所述引物组中单碱基延伸引物的作用下进行多重延伸反应,得到延伸产物;
[0038]
4)将所述延伸产物进行测序,得到抗感染用药基因snp位点的基因型。
[0039]
本发明提取待测样本的基因组dna。
[0040]
本发明对所述提取dna的方法没有特殊限制,采用本领域所熟知的提取dna的方法即可,例如试剂盒法。所述待测样本优选为唾液。所述唾液优选以口腔咽拭子形式进行采集。
[0041]
提取得到dna后,本发明以提取的dna为模板,用所述引物组进行多重pcr扩增,得到多重pcr扩增产物。
[0042]
在本发明中,所述多重pcr扩增的反应体系优选为10μl:1μl 1
×
hotstartaq buffer、0.6μl 25mm mg
2
、0.2μl 10mm dntp、0.15μl 1u hotstartaqpolymerase、1μl dna模板和1μl多重pcr引物混合液,用超纯水补足10μl;所述多重pcr引物混合液包含所述引物组,所述引物组中每条引物的浓度为1~3μm,各snp位点对应的扩增引物浓度见表3。
[0043]
表3本发明各snp位点对应的扩增引物浓度
[0044]
snp_idrs200707504rs4986893rs1801280rs8099917rs1799930单条引物浓度(μm)1~21~22~31~31~2snp_idrs72554664rs4244285rs5030869rs12979860rs717620单条引物浓度(μm)2~31~31~31~21~2snp_idrs2228570rs12248560rs72554665rs137852327
‑
单条引物浓度(μm)1~21~31~21~2
‑
[0045]
所述多重pcr扩增的反应程序优选如下:95℃5min;94℃20s,65℃40s,72℃1.5min,11个循环;94℃20s,59℃30s,72℃1.5min,20个循环;72℃2min。本发明对所述多重pcr扩增反应用仪器没有特殊限制,采用本领域所熟知的pcr仪即可。
[0046]
得到多重pcr扩增产物后,所述多重pcr扩增产物经纯化后在所述引物组中单碱基延伸引物的作用下进行多重延伸反应,得到延伸产物。
[0047]
在本发明中,所述纯化的方法优选每10μl多重pcr扩增产物的体系添加5u sap酶和2u exonuclease i酶进行孵育。所述孵育的条件优选为在36~38℃下温育30min。所述孵育后还优选包括灭活酶;所述灭活酶的条件优选在72~78℃下灭活12~17min,更优选为在75℃下灭活15min。
[0048]
在本发明中,所述多重延伸反应的反应体系为10μl:5μl snapshot multiplex kit、2μl纯化后多重pcr扩增产物、1μl延伸引物混合物和2μl超纯水;所述延伸引物混合物中各条单碱基延伸引物的浓度为1~3μm,不同snp位点对应的引物浓度优选如表4所示。
[0049]
表4延伸引物混合物中各snp位点对应的各条延伸引物的浓度
[0050][0051]
所述多重延伸反应的反应程序:96℃1min;96℃10s,55℃5s,60℃30s,28个循环。
[0052]
在本发明中,所述延伸产物还优选包括纯化。所述纯化采用sap酶处理。所述纯化的体系优选为每10μl延伸产物中加入1u sap酶。所述纯化的条件优选为在37℃下温浴30min,然后75℃灭活15min。
[0053]
得到纯化后的延伸产物,本发明将所述纯化后的延伸产物进行测序,得到抗感染用药基因snp位点的基因型。
[0054]
在本发明中,将所述纯化后的延伸产物配制成测序溶液;所述测序溶液优选每1μl纯化后的延伸产物与0.3μl liz120 size standard和9μl hi
‑
di混合制备得到。所述测序溶液在上机测序前优选在95℃下变性5min。所述测序优选采用abi3730xl测序仪进行测序。测序后,优选用genemapper4.1(appliedbiosystems co.,ltd.,usa)分析测序结果,得到各snp位点的基因型。
[0055]
在本发明中,得到各基因snp基因型为后续进一步根据具体基因型指导用抗感染药物奠定基础。
[0056]
下面结合实施例对本发明提供的一种扩增抗感染用药基因snp位点用引物组、检测引物组及其应用进行详细的说明,但是不能把它们理解为对本发明保护范围的限定。
[0057]
实施例1
[0058]
1.唾液/咽拭子等dna提取
[0059]
将采集不同患者的唾液或在面颊内擦拭过的棉签10支分别转置于2ml离心管中,用剪刀将棉签部分从起杆上剪下,加入40μl缓冲液ga。加入20μl proteinase k溶液,涡旋30s混匀,56℃放置60min,其间每15min涡旋混匀数次。加入400μl缓冲液gb,充分颠倒混匀,70℃放置10min,此时溶液应变清亮,简短离心以去除管盖内壁的液滴,然后挤压去除拭子,将尽可能多的裂解液转移至新的离心管中。加入200μl无水乙醇,充分颠倒混匀,简短离心以去除管盖内壁的液滴。将上一步所得溶液和絮状沉淀都加入一个吸附柱cr2中(吸附柱cr2放入收集管中),在12000rpm下离心30s,倒掉收集管中的废液,将吸附柱cr2放回收集管中。向吸附柱cr2中加入500μl缓冲液gd,12000rpm离心30s,倒掉收集管中的废液,将吸附柱cr2放回收集管中。向吸附柱cr2中加入600μl漂洗液pw,12000rpm离心30s,倒掉收集管中的废液,将吸附柱cr2放回收集管。重复上一步操作。12000rpm离心2min,倒掉废液。将吸附柱cr2室温放置数分钟,以彻底晾干吸附材料中残余的漂洗液。将吸附柱cr2转入一个干净的离心管中,向吸附膜中间位置悬空滴加30μl洗脱缓冲液tb,室温放置3min,在12000rpm下离心2min,收集dna溶液,质检,4℃保存。
[0060]
2.多重pcr扩增反应
[0061]
2.1pcr反应体系的配制
[0062]
10μl反应体系包含1
×
hotstartaqbuffer、3.0mm mg
2
、0.3mm dntp、1u hotstartaqpolymerase(qiagen inc.)、1μl样本dna和1μl多重pcr扩增引物混合液,用超纯水补充至10μl。
[0063]
2.2多重pcr扩增引物混合液中各条引物序列见seq id no:1~seq id no:28,各条引物多重pcr扩增引物混合液中的浓度见表3。
[0064]
表3各snp位点对应的扩增引物浓度
[0065][0066][0067]
注:每种引物(上下游引物)稀释至100μm,按照表3中数量添加至终体积100μl的primermix,上下游引物都混在一起。
[0068]
2.3多重pcr扩增反应程序
[0069][0070]
3.多重pcr扩增产物纯化
[0071]
在10μl多重pcr扩增产物中加入5u sap酶和2u exonuclease i酶,37℃温浴30分钟,然后75℃灭活15分钟。
[0072]
其中sap和exonuclease i两种酶购自neb(new england biolabs(beijing)ltd.),sap浓度为1u/μl,exonuclease i为20u/μl,添加量为sap 5μl,exon i 0.1μl。
[0073]
4.snapshot多重单碱基延伸反应
[0074]
4.1延伸反应
[0075]
10μl的延伸反应体系包括5μl snapshot multiplex kit(abi)、2μl纯化后多重pcr产物、1μl延伸引物混合物和2μl超纯水。
[0076]
4.2延伸引物混合物中各条延伸引物如seq id no:29~seq id no:42|所示,各条延伸引物的浓度见表4。
[0077]
表4不同snp位点对应的延伸引物浓度
[0078]
snp_idrs200707504rs4986893rs1801280rs8099917rs1799930单条引物浓度(μm)11211snp_idrs72554664rs4244285rs5030869rs12979860rs717620单条引物浓度(μm)21311snp_idrs2228570rs12248560rs72554665rs137852327
‑
单条引物浓度(μm)1111
‑
[0079]
注:每种延伸引物稀释至100μm,按照表中数量添加至终体积100μl的primer mix,上下游引物都混在一起。
[0080]
4.3反应程序
[0081][0082]
5.延伸产物纯化
[0083]
在10μl延伸产物中加入1u sap酶,37℃温浴30分钟,然后75℃灭活15分钟。
[0084]
6.延伸产物上abi3730xl测序仪
[0085]
取1μl纯化后的延伸产物,与0.3μl liz120 size standard、9μl hi
‑
di混匀,95℃变性5分钟后上abi3730xl测序仪。
[0086]
7.用genemapper4.1(appliedbiosystems co.,ltd.,usa)分析abi3730xl测序仪上收集的原始数据,得到目标snp位点的具体基因型信息。
[0087]
同时本实验还将相同样本进行sanger测序,得到目标snp位点的基因型。
[0088]
本发明检测方法与sanger测序的测序结果见表5。
[0089]
表5两种检测方法得到的基因snp分型结果
[0090][0091][0092]
表5两种检测方法得到的基因snp分型结果(续)
[0093][0094][0095]
结果显示,10例随机样本检测结果与sanger测序法结果完全一致,显示本发明所述的检测体系结果准确性为100%。图1为一个样本中所有目标snp位点检测结果图谱。由图1可以看出,每个基因型的结果峰高比例清晰,彼此分离,互相无相交,表明本发明的引物特异性和重复性良好。
[0096]
以上所述仅是本发明的优选实施方式,应当指出,对于本技术领域的普通技术人员来说,在不脱离本发明原理的前提下,还可以做出若干改进和润饰,这些改进和润饰也应视为本发明的保护范围。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。

