1.本发明属于病毒性抗原及该抗原的医药配制品。具体地,本发明涉及一种口蹄疫病毒样颗粒抗原、其制备的疫苗组合物及其制备方法和应用。
背景技术:
2.口蹄疫(foot-and-mouth disease,fmd)为一种急性、高度接触传染性和可快速远距离传播的动物疾病,是哺乳类动物中感染性最强的疾病,其中偶蹄类动物染病更会造成全球重大的经济损失。遭受口蹄疫危害的动物包括牛、羊和猪。致病因子为口蹄疫病毒(fmdv),是小核糖核酸病毒属家族的一种口疮病毒。该病毒分为7个血清型(a、o、c、asia1、sat1、sat2和sat3型),其中我国主要流行o型口蹄疫病毒和a型口蹄疫病毒。疫苗免疫是控制此病、保护家畜免受危害的有效措施。
3.随着a型口蹄疫的不断传播,我国流行的a型口蹄疫病毒发生了极大的变化,与以往不同的是,在自然流行的过程中,a型口蹄疫病毒主要引起牛、羊感染和发病,猪的病例较少;然而目前流行的a型口蹄疫对牛、猪都有致病性,且毒力高于之前a型病毒10倍之多。市场上缺少一种生物安全性及免疫效果均有优势的疫苗。
4.病毒样颗粒(vlps)是一种在体外和/或体内表达时能够自主包装成病毒外壳结构的类病毒粒子,它们是具有病毒的相似外壳结构但不具有病毒复制能力的假病毒。vlps疫苗能有效地激发机体产生抗感染,抗肿瘤免疫,基于病毒样颗粒设计的疫苗是一种较为理想的疫苗形式。因此,筛选理想的口蹄疫毒株序列制备病毒样颗粒是当务之急,也符合国家提出的有效防控重大动物疫病,保障畜牧业健康可持续发展的需要。
技术实现要素:
5.为解决现有技术中a型口蹄疫病毒流行株的问题,本发明提供了a型口蹄疫病毒样颗粒抗原,其中,所述a型口蹄疫病毒样颗粒抗原由a型口蹄疫病毒流行株vp2、vp3、vp1抗原蛋白组装而成,所述a型口蹄疫病毒vp2抗原蛋白如seq id no.1所示核苷酸序列或其简并序列编码,所述a型口蹄疫病毒vp3抗原蛋白如seq id no.2所示核苷酸序列或其简并序列编码,所述a型口蹄疫病毒vp1抗原蛋白如seq id no.3所示核苷酸序列或其简并序列编码。
6.所述口蹄疫病毒样颗粒抗原具有良好的免疫原性,其制备的疫苗组合物仅一次免疫就能提供对a型口蹄疫病毒流行株的完全保护。同时所述口蹄疫病毒样颗粒抗原具有良好的稳定性,在4℃下放置3个月,再通过磷钨酸负染及电镜观察仍可见病毒样颗粒依旧饱满,无聚集现象。
7.所述a型口蹄疫病毒样颗粒抗原来源于现在的流行株,能针对现在的流行野毒株产生完全保护。
8.本发明还提供一种疫苗组合物,其中,所述疫苗组合物包括免疫量的所述的a型口蹄疫病毒样颗粒抗原和药学上可接受的载体。
9.本发明的a型流行株口蹄疫病毒样颗粒疫苗在抗原含量仅为160μg/ml时,免疫后
第14日也能达到1:128以上的抗体效价,且能维持长时期高滴度抗体效价,能针对整个育肥期产生保护;显示了良好的免疫原性。
10.作为本发明的一种实施方式,本发明所述的疫苗组合物中,所述a型口蹄疫病毒样颗粒抗原含量为160~240μg/ml。
11.a型流行株口蹄疫病毒样颗粒抗原含量可选自160μg/ml、170μg/ml、180μg/ml、190μg/ml、200μg/ml、210μg/ml、220μg/ml、230μg/ml、240μg/ml。
12.即使当a型流行株口蹄疫病毒样颗粒抗原含量仅为160μg/ml,免疫后第14日也能达到1:128以上的抗体效价,即能产生免疫保护,且能维持长时期的高滴度的抗体效价。
13.作为本发明的一种优选实施方式,本发明所述的疫苗组合物中,所述a型口蹄疫病毒样颗粒抗原含量为160μg/ml、或200μg/ml、或240μg/ml。
14.作为本发明的一种实施方式,本发明所述的疫苗组合物中,所述药学上可接受的载体包括佐剂,所述佐剂选自:(1)矿物油、铝胶佐剂、皂苷、阿夫立定、dda;(2)油包水乳剂、水包油乳剂、水包油包水乳剂;或(3)丙烯酸或甲基丙烯酸的聚合物、顺丁烯二酸酐和链烯基衍生物的共聚物;以及ribi佐剂系统、block co-polymer、saf-m、单磷酰脂质a、avridine脂质-胺佐剂、大肠杆菌不耐热肠毒素、霍乱毒素、ims 1314、胞壁酰二肽、montanide isa 206、gel佐剂中的一种或几种;优选地,皂苷为quil a、qs-21、gpi-0100;优选地,所述佐剂为isa 206佐剂。
15.所述佐剂含量为5%-60%v/v,优选从30%-60%v/v,更优选50%v/v。
16.作为本发明的一种实施方式,本发明所述的疫苗组合物中,所述疫苗组合物还包括免疫量的o型口蹄疫sea拓扑型病毒样颗粒抗原和/或免疫量的o型口蹄疫cathay拓扑型病毒样颗粒抗原;其中,所述o型口蹄疫sea拓扑型病毒样颗粒抗原由o型口蹄疫sea拓扑型病毒流行株vp4、vp2、vp3、vp1抗原蛋白组装而成,其中,所述o型口蹄疫sea拓扑型病毒vp4抗原蛋白如seq id no.4所示核苷酸序列或其简并序列编码,所述o型口蹄疫sea拓扑型病毒vp2抗原蛋白如seq id no.5所示核苷酸序列或其简并序列编码,所述o型口蹄疫sea拓扑型病毒vp3抗原蛋白如seq id no.6所示核苷酸序列或其简并序列编码,所述o型口蹄疫sea拓扑型病毒vp1抗原蛋白如seq id no.7所示核苷酸序列或其简并序列编码;以及所述o型口蹄疫cathay拓扑型病毒样颗粒抗原由o型口蹄疫cathay拓扑型病毒流行株vp0、vp3、vp1抗原蛋白组装而成,其中,所述o型口蹄疫cathay拓扑型病毒vp0抗原蛋白如seq id no.8所示核苷酸序列或其简并序列编码,所述o型口蹄疫cathay拓扑型病毒vp3抗原蛋白如seq id no.9所示核苷酸序列或其简并序列编码,所述o型口蹄疫cathay拓扑型病毒vp1抗原蛋白如seq id no.10所示核苷酸序列或其简并序列编码。
17.本发明的o型口蹄疫sea拓扑型病毒样颗粒抗原具有良好的免疫原性,疫苗免疫后第14日即能达到1:128以上的o型口蹄疫sea拓扑型抗体效价。所述o型口蹄疫sea拓扑型病毒样颗粒抗原具有良好的稳定性,在4℃下放置3个月,再通过磷钨酸负染及电镜观察仍可见病毒样颗粒依旧饱满,无聚集现象。
18.本发明的o型口蹄疫cathay拓扑型病毒样颗粒抗原具有良好的免疫原性,疫苗免疫后第14日即能达到1:128以上的o型口蹄疫cathay拓扑型抗体效价。所述o型口蹄疫cathay拓扑型病毒样颗粒抗原具有良好的稳定性,在4℃下放置3个月,再通过磷钨酸负染及电镜观察仍可见病毒样颗粒依旧饱满,无聚集现象。
19.作为本发明的一种优选实施方式,本发明所述的疫苗组合物中,所述o型口蹄疫sea拓扑型病毒样颗粒抗原含量为100~200μg/ml;所述o型口蹄疫cathay拓扑型病毒样颗粒抗原含量为100~200μg/ml。
20.o型口蹄疫sea拓扑型病毒样颗粒抗原含量可选自100μg/ml、110μg/ml、120μg/ml、130μg/ml、140μg/ml、150μg/ml、160μg/ml、170μg/ml、180μg/ml、190μg/ml、200μg/ml。
21.即使当o型口蹄疫sea拓扑型病毒样颗粒抗原含量仅为100μg/ml,免疫后第14日也能达到1:128以上的抗体效价,即能产生免疫保护,且能维持长时期的高滴度的抗体效价,显示了良好的免疫原性。
22.o型口蹄疫cathay拓扑型病毒样颗粒抗原含量可选自100μg/ml、110μg/ml、120μg/ml、130μg/ml、140μg/ml、150μg/ml、160μg/ml、170μg/ml、180μg/ml、190μg/ml、200μg/ml。
23.即使当o型口蹄疫cathay拓扑型病毒样颗粒抗原含量仅为100μg/ml,免疫后第14日也能达到1:128以上的抗体效价,即能产生免疫保护,且能维持长时期的高滴度的抗体效价,显示了良好的免疫原性。
24.本发明含有a型口蹄疫病毒样颗粒抗原、o型口蹄疫sea拓扑型病毒样颗粒抗原和o型口蹄疫cathay拓扑型病毒样颗粒抗原的疫苗组合物,两种o型口蹄疫病毒样颗粒抗原协同增效,即使抗原含量减半也能发挥各组分单苗的免疫效果。
25.作为本发明的一种更优选实施方式,本发明所述的疫苗组合物中,所述o型口蹄疫sea拓扑型病毒样颗粒抗原含量为100μg/ml、或150μg/ml、或200μg/ml;以及所述o型cathay拓扑型口蹄疫病毒样颗粒抗原含量为100μg/ml、或150μg/ml、或200μg/ml。
26.作为本发明的一种实施方式,所述的药学上可接受的载体包括药物、免疫刺激剂、抗氧化剂、表面活性剂、着色剂、挥发性油、缓冲剂、分散剂、推进剂和防腐剂;所述免疫刺激剂包括α-干扰素、β-干扰素、γ-干扰素、粒细胞巨噬细胞集落刺激因子(gm-csf)、巨噬细胞集落刺激因子(m-csf)和白介素2(il2)。
27.为了制备这样的组合物,可以使用本领域公知的方法。
28.本发明还涉及一种制备所述疫苗组合物的方法,其中,所述方法包括:步骤(1)分别克隆、重组所述a型口蹄疫病毒vp2抗原蛋白的基因、所述a型口蹄疫病毒vp3抗原蛋白的基因和所述a型口蹄疫病毒vp1抗原蛋白的基因到同一串联表达载体;步骤(2)转化或转导所述步骤(1)的重组表达载体到宿主,可溶性表达a型口蹄疫病毒重组sumo-vp2抗原蛋白、重组sumo-vp3抗原蛋白和重组sumo-vp1抗原蛋白,表达的a型口蹄疫病毒重组sumo-vp2抗原蛋白、重组sumo-vp3抗原蛋白和重组sumo-vp1抗原蛋白能够自我组装为病毒样颗粒抗原;步骤(3)分离、纯化所述步骤(2)的a型口蹄疫病毒的重组抗原,酶切、纯化去除sumo融合标签;以及步骤(4)自我组装病毒样颗粒抗原,加入佐剂,得到所述的疫苗组合物。本发明通过表达a型流行株口蹄疫病毒vp2、vp3、vp1抗原蛋白,能够得到稳定的自我组装的病毒样颗粒;通过串联表达a型流行株口蹄疫病毒vp2、vp3、vp1抗原蛋白,利于后续的抗原纯化和分离。表达纯化的活性蛋白能高效自我组装成a型流行株口蹄疫病毒样颗粒抗原。
29.作为本发明的一种实施方式,本发明所述的方法中,所述步骤(1)的串联表达载体为pet28a、pet28b、pet32a;所述步骤(2)的宿主为e.coli bl21(de3)、origami b(de3)plyss、rosetta-gami b(de3)。
30.本发明通过选择串联表达载体和宿主菌,对vp2、vp3、vp1抗原蛋白进行串联表达,
利于后续的抗原分离、纯化,简化了程序。表达、纯化和自我组装成为病毒样颗粒的可溶性蛋白具有生物活性。
31.作为本发明的一种优选实施方式,本发明所述的方法中,所述步骤(2)中在宿主细胞扩增后,加入iptg,诱导所述蛋白表达。
32.作为本发明的一种优选实施方式,本发明所述的方法中,所述步骤(3)的分离、纯化工序为破碎所述菌体后,取上清,采用硫酸铵分级沉淀法和色谱纯化所述病毒样颗粒抗原。
33.本发明首次采用a型口蹄疫病毒三个结构蛋白vp2、vp3、vp1,即可生产口蹄疫病毒样颗粒,具有免疫原性好、无生物安全风险等优点。本发明制备的病毒样颗粒疫苗组合物不仅能对a型流行株口蹄疫提供保护活性,并且抗体产生快,抗体产生水平高,免疫持续期长,能维持长时间的免疫保护。
34.本发明还涉及所述疫苗组合物在制备预防和/或治疗a型口蹄疫的药物中的应用。
35.本发明所述的制备预防和/或治疗口蹄疫病毒感染的药物的施用对象包括猪。
36.本发明的疫苗组合物在一次免疫后,长达133天的时间里维持1:128以上的抗体效价,对猪体产生完全保护,该时长能涵盖整个育肥期。
具体实施方式
37.以下,对本发明的实施方式进行说明。
38.定义
[0039]“口蹄疫病毒”属于小rna病毒科,口疮病毒属,该病毒有o、a、c、sat1、sat2、sat3(即南非口蹄疫病毒1、2、3型)和asia1(亚洲1型)7个血清型,各型之间无交叉保护反应,每个类型内又有多个亚型。在病毒的中心为一条单链的正链rna,由大约8000个碱基组成,是感染和遗传的基础;周围包裹着的蛋白质决定了病毒的抗原性、免疫性和血清学反应能力;病毒外壳为对称的20面体。口蹄疫病毒是偶蹄类动物高度传染性疾病——口蹄疫的病原,国际兽疫局将口蹄疫列为“a类动物传染病名单”中的首位,中国把它列为“进境动物检疫一类传染病”,我国对口蹄疫的防治,预防主要通过疫苗注射接种,发生口蹄疫的动物则捕杀。
[0040]“抗原(antigen)”是指能诱导机体发生免疫应答的物质,即能被t/b淋巴细胞表面的抗原受体(tcr/bcr)特异性识别与结合,活化t/b细胞,使之增殖分化,产生免疫应答产物(致敏淋巴细胞或抗体),并能与相应产物在体内外发生特异性结合的物质。
[0041]“病毒样颗粒(virus-like particles,vlps)”是由一种或多种病毒结构蛋白组装成的颗粒,具有与病毒颗粒相似的外部结构和抗原性,但不含病毒基因。
[0042]“口蹄疫病毒vp2、vp3、vp1抗原蛋白”:fmdv结构蛋白前体蛋白p1被蛋白酶3c催化加工成vp0、vp3和vp1,这3种蛋白质能够自我组装成二十面体的病毒衣壳。vp0蛋白是p1经蛋白酶3c裂解后的中间体,在病毒粒子形成的最后阶段,vp0成熟裂解为vp4和vp2。
[0043]
本发明所用术语“疫苗”、“疫苗组合物”指含有口蹄疫病毒样颗粒抗原的药物组合物,该药物组合物可诱发、刺激或增强猪只针对口蹄疫的免疫反应。
[0044]
术语“免疫量”应当理解为“免疫有效量”,又称免疫保护量或产生免疫应答的有效量,为可在接受者体内有效诱导免疫应答的抗原量,该量足以预防或改善疾病的体征或症状,包括不利的健康影响或其并发症。所述免疫应答可能足以用于诊断目的或其它试验,或
胺佐剂、大肠杆菌不耐热肠毒素(重组或其它)、霍乱毒素、ims 1314、胞壁酰二肽、gel佐剂等。优选地,所述佐剂包括白油、铝胶佐剂、皂苷、油包水乳剂、水包油乳剂、水包油包水乳剂、丙烯酸或甲基丙烯酸的聚合物、顺丁烯二酸酐和链烯基(alkenyl)衍生物的共聚物、ribi佐剂系统、block co-polymer、saf-m、单磷酰脂质a、avridine脂质-胺佐剂、大肠杆菌不耐热肠毒素、霍乱毒素、ims 1314、胞壁酰二肽、montanide isa 206或gel佐剂中的一种或几种。
[0046]“简并序列”:在分子生物学中,同一种氨基酸具有两个或更多个密码子的现象称为密码子的简并性(degeneracy),这样的序列就叫简并序列。
[0047]“基因重组”:是指控制不同性状的基因重新组合。现代基因工程技术在试管内按人为的设计实施基因重组,也称为重组dna,目的是将一个个体细胞内的遗传基因转移到另一个不同性状的个体细胞内dna分子上,使之发生遗传变异。来自供体的目的基因被转入受体细菌后,可进行基因产物的表达,从而获得用一般方法难以获得的产品。
[0048]“转化(transformation)”是指通过自动获取或人为地供给外源dna,使细胞或培养的受体细胞获得新的遗传表型。
[0049]“转导(transduction)”是指当病毒从被感染的(供体)细胞释放出来、再次感染另一(受体)细胞时,发生在供体细胞与受体细胞之间的dna转移及基因重组即为转导。
[0050]
术语“预防和/或治疗”在涉及口蹄疫病毒感染时是指抑制口蹄疫病毒的复制、抑制口蹄疫病毒的传播或防止口蹄疫病毒在其宿主体内定居,以及减轻口蹄疫病毒感染的疾病或病症的症状。若病毒荷载量减少、病症减轻和/或摄食量和/或生长增加,那么就可以认为所述治疗达到了治疗效果。
[0051]
下面结合具体实施例来进一步描述本发明,本发明的优点和特点将会随着描述更为清楚。但这些实施例仅是范例性的,并不对本发明的范围构成任何限制。本领域技术人员应该理解的是,在不偏离本发明的精神和范围下可以对本发明技术方案的细节和形式进行修改或替换,但这些修改和替换均落入本发明的保护范围内。
[0052]
本发明实施例中所用到的化学试剂均为分析纯,购自国药集团。本发明所述的实验方法,若无特殊说明,均为常规方法;所述的生物材料,若无特殊说明,均可从商业途径获得。
[0053]
实施例
[0054]
材料及方法
[0055]
载体的构建和转化
[0056]
含有a型口蹄疫病毒vp2、vp3、vp1基因的重组载体pet28a-sumovp2-sumovp3-sumovp1
[0057]
由苏州金唯智生物科技有限公司合成序列表seq id no.1所示的a型口蹄疫病毒vp2基因片段、序列表seq id no.2所示的a型口蹄疫病毒vp3基因片段、序列表seq id no.3所示的a型口蹄疫病毒vp1基因片段,分别与petsumo载体连接。然后分别以连接成功的重组质粒为模板,扩增含有rbs-sumo-vp2、t7-rbs-sumo-vp3和t7-rbs-sumo-vp1的片段。分别经xba i/bamh i、sac i/sal i、not i/xho i酶切消化后得到的片段,然后依次克隆入pet28a载体。
[0058]
将连接产物转化到用cacl2制备的dh5α感受态细胞中,涂布于卡那霉素抗性的固
体lb培养基上,等单克隆菌落清晰可见时,挑取单克隆至含有卡那霉素的lb液体培养基中,37℃230转/分钟,培养12小时过夜,提取重组质粒pet28a-sumovp2-sumovp3-sumovp1。
[0059]
将上述的插入a型口蹄疫病毒vp2、vp3、vp1基因的重组质粒pet28a-sumovp2-sumovp3-sumovp1转化40μl以氯化钙法制备的感受态大肠杆菌bl21(de3),涂布于卡那霉素抗性的固体lb培养基,37℃静置培养10-12小时至单菌落清晰可见时,挑取单克隆至含4ml卡那霉素抗性的液体lb培养基的试管,37℃,230转/分振荡培养12小时,从中取1ml菌液于-80℃冻干保存。
[0060]
含有o型口蹄疫sea拓扑型病毒vp4、vp2、vp3、vp1基因的重组载体
[0061]
由苏州金唯智生物科技有限公司合成序列表seq id no.4所示的o型sea拓扑型vp4基因片段、序列表seq id no.5所示的o型sea拓扑型vp2基因片段、序列表seq id no.6所示的o型sea拓扑型vp3基因片段、序列表seq id no.7所示的o型sea拓扑型vp1基因片段,构建带有重组质粒pet28a-sumovp4-sumovp2-sumovp3-sumovp1、能串联表达o型口蹄疫sea拓扑型病毒vp4、vp2、vp3、vp1基因的大肠杆菌表达菌株,于-80℃冻干保存。
[0062]
含有o型口蹄疫cathay拓扑型病毒vp0、vp3、vp1基因的重组载体
[0063]
由苏州金唯智生物科技有限公司合成序列表seq id no.8所示的o型cathay拓扑型vp0基因片段、序列表seq id no.9所示的o型cathay拓扑型vp3基因片段、序列表seq id no.10所示的o型cathay拓扑型vp1基因片段,构建带有重组质粒pet28a-sumovp0-sumovp3-sumovp1、能串联表达o型口蹄疫cathay拓扑型病毒vp0、vp3、vp1基因的大肠杆菌表达菌株,于-80℃冻干保存。
[0064]
抗原蛋白的表达、纯化、组装及口蹄疫病毒样颗粒粒子的鉴定
[0065]
a型口蹄疫病毒抗原和病毒样颗粒粒子
[0066]
从-80℃中取出带有重组质粒pet28a-sumovp2-sumovp3-sumovp1的大肠杆菌菌种接种卡那霉素抗性的50ml lb液体培养基,37℃,230转/分振荡培养12小时后,转接入1l lb液体培养基中,37℃培养,制备发酵用种子液。
[0067]
使用发酵罐为上海保兴生物公司50l发酵罐,配制30l培养基装入发酵罐,121℃灭菌30分钟。第二天将3l种子液接入发酵罐,培养菌液浓度达到od600值大约10左右时将培养温度降至25℃,加入iptg至终浓度为0.5mm诱导培养12小时。发酵密度大约为40左右(od600)停止培养,离心收集菌体。
[0068]
重悬菌体,采用均质机以800bar压力破碎菌体4次。13500rpm,离心40min,留取上清,通过15%sds-page电泳检测。采用硫酸铵分级沉淀法进行蛋白粗纯,随后进行色谱纯化、酶切、色谱纯化去除sumo融合标签和a型口蹄疫病毒样颗粒的组装。纯化后的蛋白经sds-page电泳检测。
[0069]
通过磷钨酸负染及电镜观察a型口蹄疫病毒样颗粒。
[0070]
o型口蹄疫sea拓扑型病毒样颗粒抗原和病毒样颗粒粒子
[0071]
从-80℃中取出带有重组质粒pet28a-sumovp4-sumovp2-sumovp3-sumovp1的大肠杆菌菌种接种卡那霉素抗性的50ml lb液体培养基,按上述制备a型口蹄疫病毒抗原相似的制备条件培养菌种,再转接入1l lb液体培养基中,37℃培养。
[0072]
使用50l发酵罐,按上述a型口蹄疫病毒抗原相似的制备条件大规模发酵、表达o型口蹄疫sea拓扑型病毒抗原。
[0073]
按上述a型口蹄疫病毒抗原相似的制备条件分离、纯化和鉴定菌体中的串联表达的四个o型口蹄疫sea拓扑型病毒抗原。
[0074]
通过磷钨酸负染及电镜观察o型口蹄疫sea拓扑型病毒样颗粒。
[0075]
o型口蹄疫cathay拓扑型病毒样颗粒抗原和病毒样颗粒粒子
[0076]
从-80℃中取出带有重组质粒pet28a-sumovp0-sumovp3-sumovp1的大肠杆菌菌种接种卡那霉素抗性的50ml lb液体培养基,按上述制备a型口蹄疫病毒抗原相似的制备条件培养菌种,再转接入1l lb液体培养基中,37℃培养。
[0077]
使用50l发酵罐,按上述a型口蹄疫病毒抗原相似的制备条件大规模发酵、表达o型口蹄疫cathay拓扑型病毒抗原。
[0078]
按上述a型口蹄疫病毒抗原相似的制备条件分离、纯化和鉴定菌体中的串联表达的三个o型口蹄疫cathay拓扑型病毒抗原。
[0079]
通过磷钨酸负染及电镜观察o型口蹄疫cathay拓扑型病毒样颗粒。
[0080]
口蹄疫病毒样颗粒疫苗组合物的制备
[0081]
含a型口蹄疫病毒样颗粒抗原疫苗组合物
[0082]
取制备的a型口蹄疫病毒样颗粒抗原缓缓加入到佐剂中,加的过程不断用转速为800rpm乳化机搅拌12min,混匀,4℃保存,即为含a型口蹄疫病毒样颗粒抗原的疫苗组合物。适用于本发明的佐剂可以为本领域技术人员公知的佐剂。在本发明中,选用佐剂为双相佐剂(水包油包水乳剂),例如可以是佐剂isa 206(法国赛比克公司)。
[0083]
含a型口蹄疫病毒样颗粒抗原和o型口蹄疫sea拓扑型病毒样颗粒抗原的疫苗组合物
[0084]
取制备的a型口蹄疫病毒样颗粒抗原、o型口蹄疫sea拓扑型病毒样颗粒抗原,按上述制备含a型口蹄疫病毒样颗粒抗原疫苗组合物的方法,制备疫苗组合物。适用于本发明的佐剂可以为本领域技术人员公知的佐剂。在本发明中,选用佐剂为双相佐剂(水包油包水乳剂),例如可以是佐剂isa 206(法国赛比克公司)。
[0085]
含a型口蹄疫病毒样颗粒抗原、o型口蹄疫sea拓扑型病毒样颗粒抗原和o型口蹄疫cathay拓扑型病毒样颗粒抗原的疫苗组合物
[0086]
取制备的a型口蹄疫病毒样颗粒抗原、o型口蹄疫sea拓扑型病毒样颗粒抗原、o型口蹄疫cathay拓扑型病毒样颗粒抗原,按上述制备含a型口蹄疫病毒样颗粒抗原疫苗组合物的方法,制备疫苗组合物。适用于本发明的佐剂可以为本领域技术人员公知的佐剂。在本发明中,选用佐剂为双相佐剂(水包油包水乳剂),例如可以是佐剂isa 206(法国赛比克公司)。
[0087]
a型口蹄疫病毒样颗粒疫苗组合物的免疫原性分析
[0088]
a型口蹄疫病毒样颗粒疫苗组合物的免疫原性
[0089]
采用免疫后猪血清中抗体的elisa抗体水平检测疫苗组合物中抗原的免疫原性。
[0090]
选取a型口蹄疫病毒抗原、抗体均为阴性的体重40kg左右的健康易感架子猪,免疫制备的含a型口蹄疫病毒样颗粒抗原的疫苗组合物,免疫途径为颈部肌肉注射2ml,空白对照组免疫等量的pbs。疫苗免疫前每头猪采血,免疫后分别于第7日、14日、21日、28日采血。对采集的血清使用a型口蹄疫抗体elisa检测试剂盒进行抗体的检测。
[0091]
a型口蹄疫病毒样颗粒疫苗组合物的免疫持续期实验
[0092]
采用免疫后猪血清中抗体的elisa抗体水平检测疫苗组合物中抗原的免疫持续期。
[0093]
选取a型口蹄疫病毒抗原、抗体均为阴性的体重40kg左右的健康易感架子猪,免疫制备的含a型口蹄疫病毒样颗粒抗原的疫苗组合物,免疫途径为颈部肌肉注射2ml,空白对照组免疫等量的pbs,均一次免疫,疫苗免疫前每头猪采血,免疫后21日、28日、35日、77日、105日、133日采血。
[0094]
商品化灭活苗(re-o/mya98/jscz/2013株 re-a/wh/09株)免疫组作为对照组,免疫途径为颈部肌肉注射2ml,其空白对照组免疫等量的pbs,疫苗免疫前每头猪采血,免疫后第21日采血并进行第2次免疫,2次免疫后分别于第7日、14日、56日、84日、112日采血。
[0095]
含a型口蹄疫病毒样颗粒抗原和o型口蹄疫sea拓扑型病毒样颗粒抗原的疫苗组合物中抗原免疫原性
[0096]
采用免疫后猪血清中抗体的elisa抗体水平检测疫苗组合物中抗原的免疫原性。
[0097]
选取a型、o型口蹄疫病毒抗原、抗体均为阴性的体重40kg左右的健康易感架子猪,免疫制备的含a型口蹄疫病毒样颗粒抗原和o型口蹄疫sea拓扑型病毒样颗粒抗原的疫苗组合物,免疫途径为颈部肌肉注射2ml,空白对照组免疫2ml的pbs。疫苗免疫前每头猪采血,免疫后分别于第7日、14日、21日、28日采血。
[0098]
含a型口蹄疫病毒样颗粒抗原、o型口蹄疫sea拓扑型病毒样颗粒抗原和o型口蹄疫cathay拓扑型病毒样颗粒抗原的疫苗组合物中抗原免疫原性
[0099]
采用免疫后猪血清中抗体的elisa抗体水平检测疫苗组合物中抗原的免疫原性。
[0100]
选取a型、o型口蹄疫病毒抗原、抗体均为阴性的体重40kg左右的健康易感架子猪,免疫制备的含a型口蹄疫病毒样颗粒抗原、o型口蹄疫sea拓扑型病毒样颗粒抗原和o型口蹄疫cathay拓扑型病毒样颗粒抗原的疫苗组合物,免疫途径为颈部肌肉注射2ml,对照组免疫含o型口蹄疫sea拓扑型病毒样颗粒抗原的疫苗组合物,或免疫含o型口蹄疫cathay拓扑型病毒样颗粒抗原的疫苗组合物,免疫途径为颈部肌肉注射2ml,空白对照组免疫2ml的pbs。疫苗免疫前每头猪采血,免疫后分别于第7日、14日、21日、28日采血。
[0101]
实施例1 a型口蹄疫病毒样颗粒
[0102]
重悬表达a型口蹄疫病毒抗原蛋白的菌体,通过sds-page电泳检测,显示此时上清中三个串联表达的目的蛋白得到表达。纯化后的蛋白经sds-page电泳检测,显示目的蛋白均得到了纯化和富集。
[0103]
通过磷钨酸负染及电镜观察可见a型口蹄疫蛋白形成了病毒样颗粒,并且形成的病毒样颗粒饱满,组装效率高,没有聚集。通过将口蹄疫病毒样颗粒置于4℃下放置3个月,再通过磷钨酸负染及电镜观察可见病毒样颗粒依旧颗粒饱满,无聚集现象。说明本发明筛选的序列制备的口蹄疫蛋白形成了稳定的病毒样颗粒。
[0104]
实施例2 a型口蹄疫病毒样颗粒疫苗组合物的制备
[0105]
制备的疫苗中各组分的具体配比见表1。
[0106]
表1 a型口蹄疫病毒样颗粒疫苗组合物成分配比
[0107]
组分疫苗1疫苗2疫苗3口蹄疫抗原(μg/ml)160200240双相佐剂(v/v%)50%50%50%
[0108]
实施例3含a型口蹄疫病毒样颗粒抗原的疫苗组合物的免疫原性试验
[0109]
选取a型口蹄疫病毒抗原、抗体均为阴性的体重40kg左右的健康易感架子猪20头,随机分为4组,每组5头。1-3组分别为本发明实施例2制备的疫苗1、疫苗2、疫苗3免疫组,第4组为空白对照组。免疫组免疫途径为颈部肌肉注射2ml,对照组免疫等量的pbs。
[0110]
抗体效价结果显示,疫苗免疫前所有猪只的抗体均为阴性,1次免疫后第14日均能达到1:128以上。空白对照组猪只抗体为阴性,无变化。具体结果见表2。
[0111]
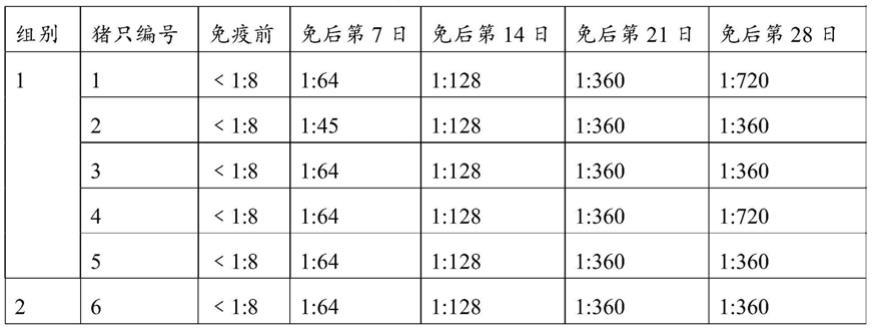
表2 a型口蹄疫elisa抗体水平
[0112][0113][0114]
表明本发明制备的病毒样颗粒能快速形成高水平的特异性抗体,即便抗原含量仅为160μg/ml,在免疫后第14天也能对a型口蹄疫起到很好的免疫保护作用。
[0115]
实施例4含a型口蹄疫病毒样颗粒抗原的疫苗组合物的免疫持续期对比试验
[0116]
选取a型口蹄疫病毒抗原、抗体均为阴性的体重40kg左右的健康易感架子猪20头,随机分为4组,每组5头。第5组为本发明实施例2制备的疫苗2免疫组,第7组为商品化灭活苗
(re-o/mya98/jscz/2013株 re-a/wh/09株)免疫组,第6组、第8组为对照组。第5组免疫组免疫途径为颈部肌肉注射2ml,第6组对照组免疫等量的pbs,均一次免疫,疫苗免疫前每头猪采血,免疫后21日、28日、35日、77日、105日、133日采血;第7组免疫组免疫途径为颈部肌肉注射2ml,第8组对照组免疫等量的pbs,疫苗免疫前每头猪采血,第7组、第8组免疫后第21日采血并进行第2次免疫,2次免疫后分别于第7日、14日、56日、84日、112日采血。
[0117]
结果显示,疫苗免疫前所有猪只的抗体均为阴性,1次免疫后第21日疫苗2免疫组能达到1:128以上,商品苗免疫组不能达到1:128,商品苗免疫组2次免疫后第7日才能达到1:128;疫苗2免疫组1次免疫133日,依然维持较高的抗体水平,elisa抗体可达1:180及以上,而商品苗免疫组2次免疫后第112日,部分猪只抗体水平接近1:128免疫保护临界值。对照组猪只抗体为阴性,无变化。具体结果见表3。
[0118]
表3 a型口蹄疫elisa抗体水平比较结果
[0119]
[0120][0121]
上述实验表明本发明制备的病毒样颗粒疫苗组合物与商品化全病毒灭活苗相比,对a型口蹄疫病毒样颗粒抗原不仅抗体产生快,抗体水平高,仅一次免疫就能起到很好的免疫保护作用,而且免疫持续期显著增长,能维持更长时间的免疫保护。
[0122]
实施例5 o型口蹄疫sea拓扑型病毒样颗粒
[0123]
重悬表达o型口蹄疫sea拓扑型病毒蛋白抗原的菌体,通过sds-page电泳检测,显示此时上清中四个串联表达的目的蛋白得到表达。纯化后的蛋白经sds-page电泳检测,显示目的蛋白均得到了纯化和富集。
[0124]
通过磷钨酸负染及电镜观察可见o型口蹄疫sea拓扑型蛋白形成了病毒样颗粒,并且形成的病毒样颗粒饱满,组装效率高,没有聚集。通过将口蹄疫病毒样颗粒置于4℃下放置3个月,再通过磷钨酸负染及电镜观察可见病毒样颗粒依旧颗粒饱满,无聚集现象。说明本发明筛选的序列制备的口蹄疫蛋白形成了稳定的病毒样颗粒。
[0125]
实施例6 o型sea拓扑型、a型二价口蹄疫病毒样颗粒疫苗组合物的制备
[0126]
制备的疫苗中各组分的具体配比见表4。
[0127]
表4 o型sea拓扑型、a型二价口蹄疫病毒样颗粒疫苗组合物成分配比
[0128]
组分疫苗4疫苗5疫苗6a型口蹄疫抗原(μg/ml)160200240o型口蹄疫sea拓扑型抗原(μg/ml)100150200双相佐剂(v/v%)50%50%50%
[0129]
实施例7 o型sea拓扑型、a型二价口蹄疫病毒样颗粒疫苗组合物的免疫原性试验
[0130]
选取a型、o型口蹄疫病毒抗原、抗体均为阴性的体重40kg左右的健康易感架子猪20头,随机分为4组,每组5头。9-11组分别为本发明实施例6制备的疫苗4、疫苗5、疫苗6免疫组,第12组为空白对照组。免疫途径为颈部肌肉注射2ml,对照组免疫2ml的pbs。疫苗免疫前每头猪采血,免疫后分别于第7日、14日、21日、28日采血。
[0131]
对采集的血清使用a型口蹄疫抗体elisa检测试剂盒进行相关抗体的检测。结果显示,疫苗免疫前所有猪只的抗体均为阴性,1次免疫后第14日均能达到1:128以上;空白对照组猪只抗体为阴性,无变化。具体结果见表5。
[0132]
表5 a型口蹄疫elisa抗体水平
[0133][0134][0135]
对采集的血清使用o型口蹄疫sea拓扑型抗体elisa检测试剂盒进行相关抗体的检测。结果显示,疫苗免疫前各免疫组所有猪只的抗体均为阴性,1次免疫后第14日均能达到1:128以上;空白对照组猪只抗体为阴性,无变化。具体结果见表6。
[0136]
表6 o型口蹄疫sea拓扑型elisa抗体水平
[0137][0138][0139]
上述试验表明本发明制备的a型、o型口蹄疫sea拓扑型病毒样颗粒疫苗组合物能快速形成高水平的特异性抗体,能对a型口蹄疫和o型口蹄疫sea拓扑型起到很好的免疫保护作用。
[0140]
实施例8 o型口蹄疫cathay拓扑型病毒样颗粒
[0141]
重悬表达o型口蹄疫cathay拓扑型病毒蛋白抗原的菌体,通过sds-page电泳检测,显示此时上清中三个串联表达的目的蛋白得到表达。纯化后的蛋白经sds-page电泳检测,显示目的蛋白均得到了纯化和富集。
[0142]
通过磷钨酸负染及电镜观察可见o型口蹄疫cathay拓扑型蛋白形成了病毒样颗粒,并且形成的病毒样颗粒饱满,组装效率高,没有聚集。通过将口蹄疫病毒样颗粒置于4℃下放置3个月,再通过磷钨酸负染及电镜观察可见病毒样颗粒依旧颗粒饱满,无聚集现象。说明本发明筛选的序列制备的口蹄疫蛋白形成了稳定的病毒样颗粒。
[0143]
实施例9 o型(sea拓扑型、cathay拓扑型)、a型二价口蹄疫病毒样颗粒疫苗组合物的制备
[0144]
制备的疫苗中各组分的具体配比见表7。
[0145]
表7 o型(sea拓扑型、cathay拓扑型)、a型二价口蹄疫病毒样颗粒疫苗组合物成分配比
[0146]
组分疫苗7疫苗8疫苗9疫苗10疫苗11a型口蹄疫抗原(μg/ml)160200240
--
sea拓扑型口蹄疫抗原(μg/ml)100150200200-cathay拓扑型口蹄疫抗原(μg/ml)100150200-200双相佐剂(v/v%)50%50%50%50%50%
[0147]
实施例10 o型(sea拓扑型、cathay拓扑型)、a型二价口蹄疫病毒样颗粒疫苗组合物的免疫原性试验
[0148]
选取a型、o型口蹄疫病毒抗原、抗体均为阴性的体重40kg左右的健康易感架子猪30头,随机分为6组,每组5头。13-15组分别为本发明实施例9制备的疫苗7、疫苗8、疫苗9免疫组,免疫途径为颈部肌肉注射2ml;16-17组分别为本发明实施例9制备的疫苗10、疫苗11免疫组,免疫途径为颈部肌肉注射2ml;第18组为空白对照组,免疫途径为颈部肌肉注射2ml的pbs。疫苗免疫前每头猪采血,免疫后分别于第7日、14日、21日、28日采血。
[0149]
对采集的血清使用a型口蹄疫抗体elisa检测试剂盒进行相关抗体的检测。结果显示,疫苗免疫前所有猪只的抗体均为阴性,第13组、第14组、第15组1次免疫后第14日均能达到1:128以上;第16组、第17组和空白对照组猪只抗体为阴性,无变化。具体结果见表8。
[0150]
表8 a型口蹄疫elisa抗体水平
[0151]
[0152][0153]
对采集的血清使用o型口蹄疫sea拓扑型抗体elisa检测试剂盒进行相关抗体的检测。结果显示,疫苗免疫前所有猪只的抗体均为阴性,第13组、第14组、第15组、第16组1次免疫后第14日均能达到1:128以上;二价(三组份)口蹄疫病毒样颗粒疫苗组合物低含量免疫组抗体水平依然达到或超过单价o型口蹄疫sea拓扑型病毒样颗粒疫苗组合物高含量免疫组抗体水平;第17组和空白对照组猪只抗体为阴性,无变化。具体结果见表9;第13组、第14组、第15组与第16组中o型口蹄疫sea拓扑型抗体elisa检测结果相比,在本发明o型(sea型、cathay型)、a型二价口蹄疫病毒样颗粒疫苗组合物中,两种o型抗原之间产生了协同增效作
用,使得o型口蹄疫sea拓扑型病毒样颗粒抗原含量减半仍能保证免疫效果。
[0154]
表9 o型口蹄疫sea拓扑型elisa抗体水平
[0155]
[0156][0157]
对采集的血清使用o型口蹄疫cathay拓扑型抗体elisa检测试剂盒进行相关抗体的检测。结果显示,疫苗免疫前所有猪只的抗体均为阴性,第13组、第14组、第15组、第17组1次免疫后第14日均能达到1:128以上;二价(三组份)口蹄疫病毒样颗粒疫苗组合物低含量免疫组抗体水平依然达到或超过单价o型口蹄疫cathay拓扑型病毒样颗粒疫苗组合物高含量免疫组抗体水平;第16组和空白对照组猪只抗体为阴性,无变化。具体结果见表10;第13组、第14组、第15组与第17组中o型口蹄疫cathay拓扑型抗体elisa检测结果相比,在本发明o型(sea拓扑型、cathay拓扑型)、a型二价口蹄疫病毒样颗粒疫苗组合物中,两种o型抗原之间产生了协同增效作用,使得o型口蹄疫cathay拓扑型病毒样颗粒抗原含量减半仍能保证免疫效果。
[0158]
表10 o型口蹄疫cathay拓扑型elisa抗体水平
[0159]
[0160][0161][0162]
上述实验表明本发明制备的二价(三组份)口蹄疫病毒样颗粒能快速形成高水平的特异性抗体,两种o型抗原之间相互协同增效,抗原含量减半时也能对o型口蹄疫sea拓扑
型和o型口蹄疫cathay拓扑型起到很好的免疫保护作用;同时,也表明单价o型口蹄疫cathay拓扑型病毒样颗粒能起很好的免疫反应,实现对猪的完全保护。
[0163]
实施例11 o型(sea拓扑型、cathay拓扑型)、a型二价口蹄疫病毒样颗粒疫苗组合物的攻毒保护试验
[0164]
选取a型、o型口蹄疫病毒抗原、抗体均为阴性的体重40kg左右的健康易感架子猪34头,随机分为8组,第19-23组每组5头,第24-26组每组3头。第19-21组为本发明实施例9制备的疫苗8免疫组,免疫途径为颈部肌肉注射2ml;第22-23组为商品化灭活苗(re-o/mya98/jscz/2013株 re-a/wh/09株)免疫组,免疫途径为颈部肌肉注射2ml;第24-26组为对照组,免疫途径为颈部肌肉注射2ml的pbs。免疫后观察各组临床症状。免后28天,每头用1000id50强毒肌肉注射,第19组、第22组、第24组攻毒毒株为cathay拓扑型毒株o/0718株,第20组、第23组、第25组攻毒毒株为sea拓扑型o/mya98/by/2010株,第21组、第26组攻毒毒株为a型a/gdmm/2013株。观察10天,猪至少有1蹄出现水疱或者溃疡即判为发病。发病情况及pd50值见表11、12、13。
[0165]
表11 o/0718株攻毒保护情况
[0166][0167][0168]
表12 o/mya98/by/2010株攻毒保护情况
[0169][0170]
表13 a/gdmm/2013株攻毒保护情况
[0171][0172][0173]
结果显示,本发明的o型(sea拓扑型、cathay拓扑型)、a型二价口蹄疫病毒样颗粒疫苗组合物针对口蹄疫o型sea拓扑型、o型cathay拓扑型、a型流行株攻击均具有良好的免疫保护效果,pd50在13.59-15.59;商品化灭活疫苗针对口蹄疫o型sea拓扑型流行株攻击不能完全保护,pd50为7.19;商品化灭活疫苗针对口蹄疫o型cathay拓扑型流行株攻击不能有效保护,pd50为2.01。
[0174]
表明,本发明的o型(sea拓扑型、cathay拓扑型)、a型二价口蹄疫病毒样颗粒疫苗
组合物具有良好的免疫原性,能抵抗流行株的攻击,解决了现有灭活疫苗不能有效针对流行株保护的问题,且生物安全性也好。
[0175]
以上所述仅是本发明的优选实施例而已,并非对本发明做任何形式上的限制,虽然本发明已以优选实施例揭露如上,然而并非用以限定本发明,任何熟悉本专业的技术人员,在不脱离本发明技术方案的范围内,当可利用上述揭示的技术内容作出些许更动或修饰为等同变化的等效实施例,但凡是未脱离本发明技术方案的内容,依据本发明的技术实质对以上实施例所作的任何简单修改、等同变化与修饰,均仍属于本发明技术方案的范围内。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。