一种特异性结合蛋白激酶p38
γ
的纳米抗体、核酸、表达载体、宿主细胞及其应用
技术领域
1.本发明涉及生物技术领域,且特别涉及一种特异性结合蛋白激酶p38γ的纳米抗体、核酸、表达载体、宿主细胞及其应用。
背景技术:
2.p38γ是p38 mapk家族中的一种丝氨酸/苏氨酸特异性蛋白激酶,主要参与调控细胞外刺激与细胞内应答之间的信号转导。p38 mapk家族共有四个成员,即p38α、p38β、p38γ以及p38δ。虽然所有的p38 mapks在序列及结构上都高度保守,但是他们在生理和病理环境中的功能却不尽相同。其中,p38α和 p38β广泛表达于各种细胞和组织,调控细胞的基本生命活动。例如:p38α在白细胞、肝、脾、小脑、骨髓、甲状腺及胎盘中具有较高的表达水平;p38β主要在脑和心脏中进行表达。而p38γ和p38δ的表达具有组织细胞特异性,并受严格的调控,p38γ主要在骨骼肌中表达;p38δ的表达主要在肺、肾、肠、唾液腺的表皮细胞及睾丸、卵巢、肾上腺和垂体。近年来研究揭示,p38γ在多种肿瘤疾病的发生发展中发挥中的调控功能,如肝癌、肠癌、乳腺癌等。p38γ作为一种类似cdk的激酶,其与cdk蛋白(与调控细胞周期有关)在结构和功能上相似性很高,p38γ能够诱使细胞进入分裂周期,因此,p38γ可以作用一种肿瘤诊断生物标志物及治疗靶点。
3.纳米抗体是源于重链抗体可变区域的小分子抗体,其分子量约为15kda,具有亲和力高、稳定性强、组织相容性好以及易筛选、易制备等特点,近年来在治疗型药物抗体、临床检测型抗体、科研运用型抗体等方面得到了广泛的研究与发展。纳米抗体主要是由4个保守的骨架区(fr)和3个抗原互补决定区 (cdr)依次交叉串联形成,其中,抗原互补决定区(cdr)是抗原识别及抗原结合的主要执行部位。所以纳米抗体的筛选关键在于获得可以介导与抗原特异性结合的互补决定区。纳米抗体中的互补决定区根据其在整个抗体中的位置不同,可以依次分为三个独立区域,即互补决定区1(cdr1)、互补决定区2 (cdr2)和互补决定区3(cdr3)。与传统抗体相比,纳米抗体互补决定区的氨基酸序列较长,使得其可以深入抗原较为隐匿的结构中与其相互作用。纳米抗体还具有良好的热稳定性和酸碱稳定性,这为其在检测、治疗等领域的应用提供了传统抗体所无法比拟的优越性。因此,若提供一种能够特异性结合蛋白激酶p38γ的纳米抗体,对于以p38γ为生物标志物和治疗靶点的肿瘤疾病诊断、治疗提供了新的思路和研究方向。
技术实现要素:
4.本发明的第一目的在于提供一种特异性结合蛋白激酶p38γ的纳米抗体,此纳米抗体具有针对蛋白激酶p38γ独特的抗原互补决定区,对蛋白激酶p38 γ显示出了高度特异的结合活性,且不与p38 mapk的其他家族蛋白p38α、 p38β和p38δ发生交叉反应。同时本技术的纳米抗体具有突出的热稳定性和酸碱稳定性。
5.本发明的第二目的在于提供编码所述的特异性结合蛋白激酶p38γ的纳米抗体的
核酸。
6.本发明的第三目的在于提供含有所述的特异性结合蛋白激酶p38γ的纳米抗体的核酸的表达载体。
7.本发明的第四目的在于提供含有所述的表达载体的宿主细胞。
8.本发明的第五目的在于提供特异性结合蛋白激酶p38γ的纳米抗体在制备用于检测蛋白激酶p38γ的检测试剂盒中的应用。
9.本发明的第六目的在于提供特异性结合蛋白激酶p38γ的纳米抗体在制备治疗或预防与蛋白激酶p38γ调控作用相关的疾病药物中的应用。
10.本发明解决其技术问题是采用以下技术方案来实现的。
11.本发明提出一种特异性结合蛋白激酶p38γ的纳米抗体,所述纳米抗体具有至少一种以下所示的互补决定区:如seqidno.1所示氨基酸序列的互补决定区cdr1;如seqidno.2所示氨基酸序列的互补决定区cdr2;和如seqidno.3所示氨基酸序列的互补决定区cdr3。
12.根据一种优选实施方式,所述纳米抗体具有如seqidno.7所示的氨基酸序列。
13.本发明还提供了一种编码所述的特异性结合蛋白激酶p38γ的纳米抗体的核酸,所述核酸能够编码至少一种以下所示的氨基酸序列:如seqidno.1所示氨基酸序列;如seqidno.2所示氨基酸序列;和如seqidno.3所示氨基酸序列。
14.根据一种优选实施方式,所述核酸具有至少一种以下所示的编码序列:如seqidno.4所示的编码序列;如seqidno.5所示的编码序列;和如seqidno.6所示的编码序列。
15.根据一种优选实施方式,所述核酸具有如seqidno.8所示的编码序列。
16.本发明还提供了一种含有所述的特异性结合蛋白激酶p38γ的纳米抗体的核酸的表达载体,所述表达载体包括原核生物表达载体、真核生物表达载体或体外表达载体系统。
17.根据一种优选实施方式,所述表达载体为pet22b。
18.本发明还提供了一种含有所述的表达载体的宿主细胞,所述宿主细胞包括原核生物或真核生物。
19.本发明还提供了所述的特异性结合蛋白激酶p38γ的纳米抗体在制备用于检测蛋白激酶p38γ的检测试剂盒中的应用。
20.本发明还提供了所述的特异性结合蛋白激酶p38γ的纳米抗体在制备治疗或预防与蛋白激酶p38γ调控作用相关的疾病药物中的应用。
21.基于上述技术方案,本发明的特异性结合蛋白激酶p38γ的纳米抗体、核酸、表达载体、宿主细胞及其应用至少具有如下技术效果:
22.本发明特异性结合蛋白激酶p38γ的纳米抗体具有至少一种以下所示的互补决定区:如seqidno.1所示氨基酸序列的互补决定区cdr1;如seqidno.2所示氨基酸序列的互补决定区cdr2;和如seqidno.3所示氨基酸序列的互补决定区cdr3。使得该纳米抗体具有针对蛋白激酶p38γ独特的抗原互补决定区,对蛋白激酶p38γ显示出了高度特异的结合活性,且不与p38mapk的其他家族蛋白p38α、p38β和p38δ发生交叉反应。同时本技术的纳米抗体具有突出的热稳定性和酸碱稳定性。为检测蛋白激酶p38γ以及治疗与蛋白激酶p38γ调控作用相关的疾病提供了新方向。
附图说明
23.为了更清楚地说明本发明实施例或现有技术中的技术方案,下面将对实施例或现有技术描述中所需要使用的附图作简单地介绍,显而易见地,下面描述中的附图仅仅是本发明的一些实施例,对于本领域普通技术人员来讲,在不付出创造性劳动的前提下,还可以根据这些附图获得其他的附图。
24.图1为本发明实施例1中p38γ表达与纯化的示意图,其中图1a示出了表达载体pet28a
‑
p38γ
‑2×
strep主要元件组成;图1b示出了含有重组质粒 pet28a
‑
p38γ
‑2×
strep的表达菌株诱导表达蛋白并用magstrep“type3”xt磁珠纯化,sds
‑
page蛋白电泳分析表达及纯化产物;
25.图2为本发明实施例2中nb12
‑
1稳定结合p38γ的示意图,其中图2a示出了纳米抗体表达载体pet22b
‑
nb
‑
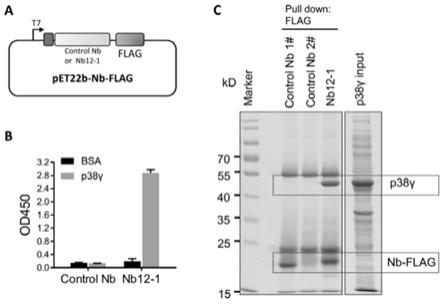
flag主要元件组成;control nb为含有相同骨架序列的对照纳米抗体;图2b示出了elisa检测含有纳米抗体表达载体的大肠杆菌细胞周至提取物与p38γ及对照抗原bsa的结合情况;图2c示出了免疫共沉淀检测含有纳米抗体表达载体的大肠杆菌细胞周至提取物与p38γ的结合情况;
26.图3为本发明实施例3中免疫共沉淀检测的nb12
‑
1与p38 mapk家族蛋白间的交叉反应情况;
27.图4为本发明实施例4中免疫共沉淀检测不同温度、不同酸碱环境处理后的nb12
‑
1的p38γ结合能力。
具体实施方式
28.为使本发明的目的、技术方案和优点更加清楚,下面将对本发明的技术方案进行详细的描述。显然,所描述的实施例仅仅是本发明一部分实施例,而不是全部的实施例。基于本发明中的实施例,本领域普通技术人员在没有做出创造性劳动的前提下所得到的所有其它实施方式,都属于本发明所保护的范围。
29.下面结合具体实施例对本发明的特异性结合蛋白激酶p38γ的纳米抗体及其应用进行具体说明。所举实例只用于解释和理解本发明,并非用于限定本发明的范围。
30.本发明提出的一种特异性结合蛋白激酶p38γ的纳米抗体,所述的纳米抗体具有至少一种以下所示的互补决定区:如seq id no.1所示氨基酸序列的互补决定区cdr1;如seq id no.2所示氨基酸序列的互补决定区cdr2;和如 seq id no.3所示氨基酸序列的互补决定区cdr3。可以理解为:本发明的纳米抗体具有三个互补决定区cdr1、cdr2和cdr3,且三个互补决定区中至少一种互补决定区满足:互补决定区cdr1具有如seq id no.1所示氨基酸序列;互补决定区cdr2具有如seq id no.2所示氨基酸序列;或者互补决定区cdr3 具有如seq id no.3所示氨基酸序列。从而使得纳米抗体形成具有针对蛋白激酶p38γ独特的抗原互补决定区,对蛋白激酶p38γ显示出了高度特异的结合活性,且不与p38 mapk的其他家族蛋白p38α、p38β和p38δ发生交叉反应。
31.进一步优选的,本发明还提供了一种编码上述特异性结合蛋白激酶p38γ的纳米抗体的核酸,所述核酸能够编码至少一种以下所示的氨基酸序列:如seqid no.1所示氨基酸序列;如seq id no.2所示氨基酸序列;和如seq id no.3 所示氨基酸序列。优选的,所述核酸具有至少一种以下所示的编码序列:如seqid no.4所示的编码序列;如seq id no.5
所示的编码序列;和如seq id no.6 所示的编码序列。以便能够编码本发明的特异性结合蛋白激酶p38γ的纳米抗体的至少一种互补决定区。
32.进一步优选的,本发明还提供了一种含有所述的特异性结合蛋白激酶p38 γ的纳米抗体的核酸的表达载体,所述表达载体包括原核生物表达载体、真核生物表达载体或体外表达载体系统。优选的,所述表达载体为pet22b。
33.进一步优选的,本发明还提供了一种含有所述的表达载体的宿主细胞,所述宿主细胞包括原核生物或真核生物。也可采用其他包含所述表达载体的体外表达系统。
34.进一步优选的,本发明还提供了所述的特异性结合蛋白激酶p38γ的纳米抗体在制备用于检测蛋白激酶p38γ的检测试剂盒中的应用。
35.进一步优选的,本发明还提供了所述的特异性结合蛋白激酶p38γ的纳米抗体在制备治疗或预防与蛋白激酶p38γ调控作用相关的疾病药物中的应用。优选的,该疾病可以是与蛋白激酶p38γ调控作用相关的肿瘤疾病。
36.以下结合实施例对本发明的特征和性能作进一步的详细描述。
37.实施例1
38.本实施例1提供了对特异性结合蛋白激酶p38γ的纳米抗体的筛选。具体步骤如下:
39.(1)依据iba公司所开发的第三代蛋白纯化系统构建p38γ表达载体,如图1a。其中,p38γ氨基酸序列如seq id no.9所示。p38γdna 编码序列如seq id no.10所示。2
×
strep标签氨基酸序列如seq id no.11 所示。2
×
strep标签dna编码序列如seq id no.12所示。将构建好的表达载体转化至大肠杆菌表达细菌bl21(de3)中,通过iptg诱导其表达,利用 magstrep“type3”xt磁珠进行蛋白纯化,利用sds
‑
page及考马斯亮蓝染色检测表达及纯化产物,最终获得高纯度p38γ蛋白,如图1b所示。
40.(2)将纯化所得p38γ蛋白包被至磁珠。将纳米抗体噬菌体文库稀释至含 2.5%bsa tbst溶液中;然后将纳米抗体文库(文库构构建见如下文献:wang, wenyi,et al."identification ofnanobodies against hepatocellular carcinoma markerglypican
‑
3."molecular immunology 131(2021):13
‑
22.)与p38γ包被磁珠室温孵育2小时,然后弃去噬菌体溶液,tbst洗涤磁珠20次,pbs洗涤磁珠10次,然后用100μl洗脱液(triethylamine,0.1m)孵育磁珠10min,最后再用100 μl 1m tris
‑
hcl溶液中和洗脱液。将洗脱液加入1ml大肠杆菌ss320,37℃孵育30min,利用辅助噬菌体m13k07扩增噬菌体,最后收集纯化噬菌体并用于下一轮筛选。
41.(3)完成第三轮筛选噬菌体侵染后,将大肠杆菌ss320涂平板,挑取40 个含噬菌体质粒的单克隆进行测序。根据测序结果,选取重复率较高的单克隆,进行纳米抗体表达及鉴定。
42.实施例2
43.本实施例提供了对纳米抗体进行鉴定的方法。
44.(1)选取实施例1中所获克隆nb12
‑
1,其dna序列如seq id no.8,该 dna序列编码氨基酸序列如seq id no.7所示。通过分子克隆将编码纳米抗体的编码序列亚克隆至表达载体pet22b中,并于其c端融合flag标签序列,见图2a。并以同样方法构建对照纳米抗体表达载体。
45.(2)将所构建纳米抗体表达载体转化至大肠杆菌表达菌株bl21(de3) 中,通过iptg诱导表达,然后利用低渗发提取细菌细胞周至蛋白。
46.(3)elisa检测表达纳米抗体细菌细胞周至蛋白与p38γ的结合:将p38 γ和bsa蛋白包被至96孔酶标板,封闭液封闭后,纳米抗体细菌细胞周至提取物37℃孵育2小时,然后抗falg鼠单克隆抗体37℃孵育1小时,然后hrp 标记的鼠二抗37℃孵育1小时,根据elisa试剂盒(索莱宝)进行显色反应及终止反应,最终检测反应溶液的450nm吸光值(od450),结果分析显示, nb12
‑
1特异性结合p38γ,见图2b。
47.(4)免疫共沉淀检测纳米抗体nb12
‑
1与p38γ的结合:纳米抗体细菌细胞周至提取物与p38γ表达细菌裂解液4℃共孵育2小时,然后加入10μl anti
‑
flag磁珠4℃再孵育1小时,tbst洗涤磁珠3次后,sds
‑
page和考马斯亮蓝染色检测免疫共沉淀结果。结果显示,nb12
‑
1共沉淀p38γ,见图2c。
48.实施例3
49.本实施例3针对nb12
‑
1与p38 mapk其它家族蛋白的交叉反应进行了检测。
50.免疫共沉淀检测nb12
‑
1与p38 mapk其它家族蛋白的交叉反应:
51.纳米抗体细菌细胞周至提取物与p38α、p38β、p38γ及p38δ表达细菌裂解液4℃共孵育2小时,然后加入10μl anti
‑
flag磁珠4℃再孵育1小时, tbst洗涤磁珠3次后,sds
‑
page和考马斯亮蓝染色检测免疫共沉淀结果。如图3所示,结果显示,nb12
‑
1特异性共沉淀p38γ,不与p38α、p38β、p38 δ交叉反应。
52.实施例4
53.本实施例对纳米抗体nb12
‑
1的热稳定性和酸碱稳定性进行了检测。
54.(1)将纳米抗体nb12
‑
1分别在4℃、18℃、37℃、42℃、65℃、90℃环境孵育1小时,然后再将其与p38γ表达细菌裂解液4℃共孵育2小时,之后加入10μl anti
‑
flag磁珠4℃再孵育1小时,tbst洗涤磁珠3次后,sds
‑
page 和考马斯亮蓝染色检测免疫共沉淀结果。如图4所示,结果显示,37℃、42℃处理后的nb12
‑
1仍然具有良好的p38γ结合能力,65℃和90℃高温处理后, nb12
‑
1的稳定性将减弱,但是保留部分p38γ结合能力。
55.(2)将纳米抗体nb12
‑
1分别在ph值为2、4、7、10、12的tbs缓冲液中孵育1小时,然后再将其与p38γ表达细菌裂解液4℃共孵育2小时,之后加入10μl anti
‑
flag磁珠4℃再孵育1小时,tbst洗涤磁珠3次后,sds
‑
page 和考马斯亮蓝染色检测免疫共沉淀结果。如图4所示,结果显示,ph值为2、 12的缓冲液处理nb12
‑
1之后,纳米抗体nb12
‑
1仍然具有良好的p38γ结合能力。
56.综上所述,本发明的特异性结合蛋白激酶p38γ的纳米抗体具有针对蛋白激酶p38γ独特的抗原互补决定区,对蛋白激酶p38γ显示出了高度特异的结合活性,且不与p38 mapk的其他家族蛋白p38α、p38β和p38δ发生交叉反应。
57.以上所述,仅为本发明的具体实施方式,但本发明的保护范围并不局限于此,任何熟悉本技术领域的技术人员在本发明揭露的技术范围内,可轻易想到变化或替换,都应涵盖在本发明的保护范围之内。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。

