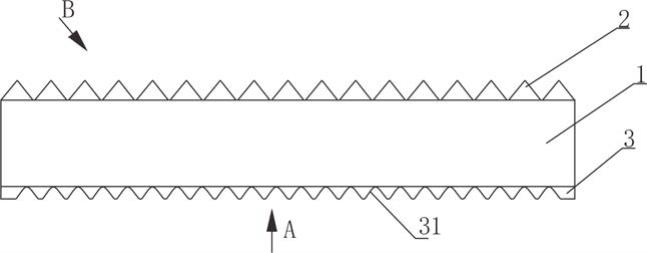
包含巨大芽孢杆菌属益生菌菌株和多不饱和脂肪酸组分的制剂
1.本发明涉及一种制剂,其包含至少一种属于巨大芽孢杆菌(bacillus megaterium)属的益生菌菌株或巨大芽孢杆菌的提取物,以及多不饱和脂肪酸组分,所述多不饱和脂肪酸组分包含选自二十碳五烯酸(epa)、二十二碳六烯酸(dha)、花生四烯酸(ara)、α亚麻酸、亚麻油酸(stearidonic acid)、二十碳四烯酸、二十二碳五烯酸、亚油酸、γ
‑
亚麻酸和/或其衍生物的至少一种ω
‑
3或ω
‑
6脂肪酸。
2.ω
‑
3脂肪酸,即α
‑
亚油酸(ala)、epa和dha的饮食摄入对人体健康特别是对例如类风湿关节炎的改善和心血管疾病危险因素的减少有益[1、2]。各种海鲜产品是饮食中epa/dha的来源,但其消耗量通常不足以满足建议的饮食限额(通常每天500mg epa和dha)[3]。这一缺口通过广泛使用含有ω
‑
3脂肪酸的膳食补充剂或强化食物来弥合[4]。膳食补充剂是营养物质或具有营养或生理作用的其他物质的集中来源,其目的是补充正常饮食(www.efsa.europa.eu/en/topics/topic/food
‑
supplements)。例如,ω
‑
3脂肪酸补充剂通常含有来自鱼油、磷虾油或藻类的epa/dha的甘油三酯或ω
‑
3乙酯。
[0003]
ω
‑
3脂肪酸通常具有抗炎作用、心脏和神经保护作用[2、5]。它们的作用方式包括直接清除活性氧,改变细胞膜流动性(其继而影响细胞信号转导事件),调节转录因子诸如pparg和nfkappab(其安排促炎和抗炎细胞因子的生物合成)的活性,和竞争性排斥通过环氧合酶和脂氧合酶转化为促炎细胞因子的基质。
[0004]
最近,已鉴定出ω
‑
3和ω
‑
6脂肪酸的几种氧合产物,并将其功能表征为其有益的健康作用的关键介质,特别是在改善慢性炎症病况方面[6]。这些产品包括maresin(mar)、e
‑
和d
‑
系列消退素(rve和rvd)、保护素、脂氧素及其前体,例如18
‑
羟基
‑
二十碳五烯酸(18
‑
hepe)、17
‑
羟基
‑
二十二碳六烯酸(17
‑
hdha)和17,18
‑
环氧二十碳四烯酸(17,18
‑
eeq),统称为特化促炎症消退(pro
‑
resolving)脂质介质(spm)。spm由脂氧合酶、环氧合酶2和细胞色素p450单加氧酶(cyp450)内源性形成,并充当活性炎症消退的有效激动剂,通过纳摩尔浓度的g蛋白偶联受体进行信号传导。在使用啮齿动物的研究中证明了spm针对多种传染性和炎性疾病的有效性[6]。例如,rve1、rvd2、保护素d1(pd1)和lxa4增强致病性牙龈假单胞菌(pseudomonas gingivalis)[7]、大肠杆菌(e.coli)[8]、单纯疱疹(herpes simples)[9]、念珠菌(candida)[10]、h5n1流感[11]的清除率。
[0005]
lxa4、lxb4、rve1、rve3、rvd1
‑
5、rvd2、pd1、mar1、mar2在牙周炎、囊性纤维化、神经炎症、缺血性中风、阿尔茨海默病[12]、动脉粥样硬化[13]、非酒精性脂肪肝疾病[14]、角膜损伤[15]、视网膜病变[16]、青光眼[17]、结肠炎[18]、哮喘[19、20]、胰岛素抗性[14]、关节炎[21]和疼痛[22]的模型中具有保护作用。此外,spm的几种前体本身已显示发挥消退作用。例如,18
‑
羟基
‑
二十碳五烯酸(18
‑
hepe)通过抑制单核细胞与血管内皮细胞的粘附[23]和通过抑制压力超负荷诱发的适应不良的心脏重塑[24]来抵消心血管疾病的发展。类似地,17,18
‑
eeq具有心脏保护、抗心律不齐、血管舒张和抗炎特性[5]。肠神经胶质细胞的ara衍生的15
‑
hete的旁分泌支持肠屏障功能,其是在例如克罗恩病中受到损害的过程[25]。
[0006]
然而,将这些有希望的临床前发现结果转化用于改善人类健康已显示具有挑战
性。如在实验研究中所做的那样通过静脉内或腹膜内注射直接递送spm对人类而言是不可行的,特别是在预防方法的情况下。含spm或spm前体的补充剂或食物的口服递送是不合理的,因为它们在生物体液中的半衰期相对较短,因此它们不太可能到达其靶组织。在这方面,wo 2017/041094公开了一种浓缩的酯化鱼油,其仅包含约0.0005%的18
‑
hepe和17
‑
hdha,并且甚至通过超临界流体萃取富集这些spm前体也不会产生超过0.05%(18
‑
hepe 17
‑
hdha)/总ω
‑
3。
[0007]
使用epa/dha的临床试验得出不确定的或无效的结果,特别是对于患有炎症性肠病、哮喘和代谢综合征特征的患者[2]。这种对人类的益处的缺乏与spm对相应动物疾病模型的有效治疗形成了鲜明对比[6]。我们认为,将ω
‑
3(和ω
‑
6)转化为spm是至关重要的步骤,这对于从旨在使用多不饱和脂肪酸(pufa)预防、治疗或治疗炎性疾病的任何干预措施递送成功的结果至关重要。我们还认为,产生spm的机构在某些条件下是功能失调的。这一想法得到了在糖尿病伤口[26]、代谢综合征[27]、哮喘[19、28]、溃疡性结肠炎[29]、克罗恩病[25]和牙周炎[30]中减少的(局部或循环)spm水平以及严重哮喘[28]、溃疡性结肠炎[29]、囊性纤维化[31]、牙周炎[30]和阿尔茨海默氏病[12]中减少的spm产生酶的表达或活性的发现结果的支持。
[0008]
因此,本发明的目的是提供一种促进生物体内spm形成的技术,从而在仅补充ω
‑
3几乎没有或没有取得成功时,为遭受上述病况并且需要新的策略来预防、改善或治愈此类和类似病况的人和动物带来益处。
[0009]
通过本发明,通过将合适的ω
‑
3源与新发现的微生物spm生产者在合适的制剂中组合来实现该目标,使得与单独的ω
‑
3源相比,该组合技术提供增强的和/或靶向的功效。合适的制剂允许组分在小肠远端的胃肠道中伴随释放,从而防止ω
‑
3源被小肠吸收,并使其更易于被微生物spm生产者代谢。
[0010]
spm的生物合成已经针对真核细胞,特别是粒细胞和单核细胞进行了详细描述。巨噬细胞可以表达spm生物合成所需的所有酶;其他仅表达选定酶的细胞类型可以与补体细胞一起表达。在肥大细胞中发现alox5,在皮肤和上皮细胞中发现alox12,在树突状细胞和肠神经胶质细胞中发现alox15[25],在上皮细胞中发现cox
‑
2和cyp450亚同种型。
[0011]
鉴于肠道菌群决定个体对食物成分的反应并随后改变健康结果,我们将其鉴定为我们的促进内源性spm生产的技术方法的靶标。靶向微生物群的策略通常包括应用益生元和益生菌,旨在改变微生物群的组成和活性。益生菌是活的微生物,当以足够的量施用时,其赋予宿主健康益处(fao
‑
who;probiotics in food.health and nutritional properties and guidelines for evaluation;fao food and nutritional paper 85,2006)。益生元支持有益微生物的生长。已经描述了ω
‑
3脂肪酸的益生元作用[32、33],但反之亦然,肠微生物对ω
‑
3的可能的代谢影响尚待确定,并已在本发明中公开。肠道驻留微生物中耗氧酶的存在受到限制;胃肠道细菌和古细菌似乎不存在环氧合酶和脂氧合酶,但致病性铜绿假单胞菌(pseudomonas aeruginosa)表达的15
‑
脂氧合酶除外[34]。cyp450单加氧酶已在芽孢杆菌属中被检测到[35]。cyp102a1(也称为cyp450bm
‑
3)是一种在巨大芽孢杆菌中发现的双功能酶,其通过连续的加氧酶和还原酶活性催化nadph依赖性的多不饱和脂肪酸的羟基化反应。该p450系统由具有两个不同的结构域的多肽链组成,一个结构域包含血红蛋白,另一个结构域包含fad还原酶。这种细菌细胞色素p450类别是可溶的,并通过
degussa gmbh的名义以上文提及的登录号于2018年11月27日(dsm 32963)和2019年10月17日保藏于dsmz。
[0022]
因此,用于根据本发明的制剂的巨大芽孢杆菌菌株选自以下组:
[0023]
a)以dsm 32963、dsm 33296和dsm 33299保藏于dsmz的巨大芽孢杆菌菌株之一;
[0024]
b)以dsm 32963保藏的巨大芽孢杆菌菌株的突变体,其具有dsm 32963菌株的所有鉴定特征,其中所述突变体优选与dsm 32963菌株具有至少95%,优选至少96、97或98%,更优选至少99或99.5%的dna序列同一性;
[0025]
c)(a)或(b)的制剂;
[0026]
d)包含如包含在(a)、(b)或(c)中的代谢物的有效混合物的制剂。
[0027]
以dsm 32963保藏于dsmz的巨大芽孢杆菌菌株表现出以下特征序列:
[0028]
a)与根据seq id no:1或seq id no:2的多核苷酸序列具有至少99.5%(尤其是100%)的序列同一性的16s rdna序列;
[0029]
b)与根据seq id no:3的多核苷酸序列具有至少99.5%(尤其是100%)的序列同一性的yqfd序列;
[0030]
c)与根据seq id no:4的多核苷酸序列具有至少99.5%(尤其是100%)的序列同一性的gyrb序列;
[0031]
d)与根据seq id no:5的多核苷酸序列具有至少99.5%(尤其是100%)的序列同一性的rpob序列;
[0032]
e)与根据seq id no:6的多核苷酸序列具有至少99.5%(尤其是100%)的序列同一性的groel序列。
[0033]
以dsm 33296保藏于dsmz的巨大芽孢杆菌菌株表现出以下特征序列:
[0034]
a)与根据seq id no:13或seq id no:14的多核苷酸序列具有至少99.5%(尤其是100%)的序列同一性的16s rdna序列;
[0035]
b)与根据seq id no:15的多核苷酸序列具有至少99.5%(尤其是100%)的序列同一性的yqfd序列;
[0036]
c)与根据seq id no:16的多核苷酸序列具有至少99.5%(尤其是100%)的序列同一性的gyrb序列;
[0037]
d)与根据seq id no:17的多核苷酸序列具有至少99.5%(尤其是100%)的序列同一性的rpob序列;
[0038]
e)与根据seq id no:18的多核苷酸序列具有至少99.5%(尤其是100%)序列同一性的groel序列。
[0039]
以dsm 33299保藏于dsmz的巨大芽孢杆菌菌株表现出以下特征序列:
[0040]
a)与根据seq id no:25或seq id no:26的多核苷酸序列具有至少99.5%(尤其是100%)的序列同一性的16s rdna序列;
[0041]
b)与根据seq id no:27的多核苷酸序列具有至少99.5%(尤其是100%)的序列同一性的yqfd序列;
[0042]
c)与根据seq id no:28的多核苷酸序列具有至少99.5%(尤其是100%)的序列同一性的gyrb序列;
[0043]
d)与根据seq id no:29的多核苷酸序列具有至少99.5%、尤其是100%的序列同
一性的rpob序列;
[0044]
e)与根据seq id no:30的多核苷酸序列具有至少99.5%(尤其是100%)的序列同一性的groel序列。
[0045]
因此,本发明的另一主题是巨大芽孢杆菌菌株,特别是如上文所述的巨大芽孢杆菌菌株,其表现出以下特征中的至少一个,优选全部:
[0046]
a)与根据seq id no:1或seq id no:2、seq id no:13或seq id no:14、seq id no:25或seq id no:26的多核苷酸序列具有至少99%、优选至少99.5%、更优选至少99.8%或99.9%、尤其是100%的序列同一性的16s rdna序列;
[0047]
b)与根据seq id no:3、seq id no:15或seq id no:27的多核苷酸序列具有至少99%、优选至少99.5%、更优选至少99.8%或99.9%、尤其是100%的序列同一性的yqfd序列;
[0048]
c)与根据seq id no:4、seq id no:16、seq id no:28的多核苷酸序列具有至少99%、优选至少99.5%、更优选至少99.8%或99.9%、尤其是100%的序列同一性的gyrb序列。
[0049]
优选地,该巨大芽孢杆菌菌株表现出以下进一步的特征中的至少一个,更优选全部:
[0050]
d)与根据seq id no:5、seq id no:17、seq id no:29的多核苷酸序列具有至少99%、优选至少99.5%、更优选至少99.8或99.9%、尤其是100%的序列同一性的rpob序列;
[0051]
e)与根据seq id no:6、seq id no:18、seq id no:30的多核苷酸序列具有至少99%、优选至少99.5%、更优选至少99.8%或99.9%、尤其是100%的序列同一性的groel序列。
[0052]
因此,本发明的一个特定主题还是巨大芽孢杆菌菌株,其表现出以下特征:
[0053]
a)根据seq id no:1或seq id no:2、seq id no:13或seq id no:14或seq id no:25或seq id no:26的16s rdna序列;
[0054]
b)根据seq id no:3、seq id no:15或seq id no:27的yqfd序列;
[0055]
c)根据seq id no:4、seq id no:16或seq id no:28的gyrb序列。
[0056]
优选地,该巨大芽孢杆菌菌株表现出以下进一步的特征:
[0057]
d)根据seq id no:5、seq id no:17或seq id no:29的rpob序列;
[0058]
e)根据seq id no:6、seq id no:18或seq id no:30的groel序列。
[0059]
在有利的配置中,epa和dha为游离脂肪酸、盐、天然甘油三酯、鱼油、磷脂酯或ω
‑
3乙酯的形式。
[0060]
epa和dha作为脂肪酸盐添加时,被益生菌菌株有效地转化为spm,其生产和应用已在之前披露。wo2016102323a1描述了包含多不饱和ω
‑
3脂肪酸盐的组合物,其可以抵抗氧化稳定存在。wo2017202935a1公开了一种制备包含ω
‑
3脂肪酸盐和胺的组合物的方法,其中包含一种或多种ω
‑
3脂肪酸、一种或多种碱性胺和20重量%或更少的水(基于糊剂的总重量)的糊剂被捏合直至获得均质的糊剂。
[0061]
因此,在本发明的优选配置中,ω
‑
3组分包含ω
‑
3脂肪酸氨基酸盐,其中所述氨基酸选自碱性氨基酸,所述碱性氨基酸选自赖氨酸、精氨酸、鸟氨酸、组氨酸、瓜氨酸、胆碱及其混合物。
[0062]
在另一个优选的配置中,氨基酸选择自选自赖氨酸、精氨酸、鸟氨酸、胆碱及其混合物的碱性氨基酸。
[0063]
最优选使用赖氨酸的氨基酸盐。
[0064]
本发明的另一优选配置是ω
‑
3分散体(推测是脂质体)的制剂,以进一步提高对益生菌菌株的生物利用度。这样的分散体制剂优选由磷脂混合物(例如脱油的向日葵卵磷脂)或确定的磷脂例如二油基磷脂酰胆碱(dopc)组成。这样的分散体制剂的最优选形式包含游离的ω
‑
3脂肪酸盐或游离的ω
‑
3脂肪酸。
[0065]
因此,在该优选的实施方案中,多不饱和脂肪酸组分包括包含至少一种磷脂和至少一种ω
‑
3脂肪酸的分散体的制剂。
[0066]
在另一个优选的实施方案中,多不饱和脂肪酸组分包括包含至少一种磷脂和阳离子与衍生自ω
‑
3或ω
‑
6脂肪酸的阴离子的至少一种脂肪酸盐的分散体的制剂。特别优选使用ω
‑
3脂肪酸。
[0067]
在本发明的替代配置中,磷脂是脱油的磷脂,其包含大于40重量%、优选70重量%、更优选大于90重量%的磷脂酰胆碱含量和小于5重量%、优选小于1重量%的磷脂酰乙醇胺含量。
[0068]
在一个替代的实施方案中,磷脂是油酸和/或亚油酸含量大于总脂肪酸的70重量%的非氢化磷脂。
[0069]
在本发明的另一优选配置中,磷脂与脂肪酸盐的质量比大于0.001,优选大于0.05,更优选大于0.01,更优选大于0.09,最优选大于0.39。
[0070]
在一个替代的实施方案中,所述制剂为粉末或液体形式,当与水在ph 6.5至7.5的ph值下混合时,其产生平均粒径小于1μm、优选小于500nm、最优选小于250nm的胶体分散体。
[0071]
在另一个实施方案中,组分彼此精细分散,使得磷脂和脂肪酸盐均以100μg或更小的量存在和可检测到。
[0072]
用于本发明制剂的肠内递送的优选制剂是提供针对胃病况的保护的制剂,或提供在小肠中制剂的靶向释放的制剂,或提供在大肠中制剂的靶向释放的制剂。因此,在优选的实施方案中,制剂包含用于延迟释放或肠或结肠释放的包衣。
[0073]
本发明的一个主题是根据本发明的制剂作为饲料或食物补充剂的用途或其在食品中的用途。根据本发明的优选食品是巧克力产品、软糖、麦片、麦片条和乳制品。
[0074]
本发明的另一个主题是本发明的制剂作为饲料或食物产品中的合益素成分的用途。
[0075]
本发明的另一个主题是一种饲料或食品组合物,其包含根据本发明的制剂和至少一种另外的饲料或食物成分,优选地选自蛋白质、碳水化合物、脂肪、其他益生菌、益生元、酶、维生素、免疫调节剂、代乳品、矿物质、氨基酸、抗球虫药、基于酸的产品、药物及其组合。
[0076]
根据本发明的饲料或食品组合物还包括丸剂、胶囊、片剂或液体形式的膳食补充剂。
[0077]
本发明的另一个主题是药物组合物,其包含根据本发明的制剂和药学上可接受的载体。
[0078]
本发明的另一主题是制剂在制备药物产品中的用途。
[0079]
当将本发明的制剂施用于动物或人类时,优选改善健康状态,特别是动物或人类
的肠道健康、心血管健康、心脏代谢健康、肺健康、关节健康、眼睛健康、精神健康、口腔健康或免疫健康。
[0080]
因此,本发明的另一个主题是作为本发明的一部分的根据本发明的组合物,其用于改善健康状态,特别是动物或人类的肠道健康、心血管健康、心脏代谢健康、肺健康、关节健康、眼睛健康、精神健康、口腔健康或免疫健康。
[0081]
根据本发明的有利配置是用于通过以下一种或多种改善动物或人的健康状态的组合物:
[0082]
‑
通经由其通过胃肠道微生物的产生增加宿主中以下脂质介质的总量:
[0083]
17
‑
羟基
‑
dha(17
‑
hdha),14
‑
羟基
‑
dha(14
‑
hdha),13
‑
羟基
‑
dha(13
‑
hdha),7
‑
羟基
‑
dha(7
‑
hdha),4
‑
羟基
‑
dha(4
‑
hdha),18
‑
羟基
‑
二十碳五烯酸(18
‑
hepe),15
‑
羟基
‑
二十碳五烯酸(15
‑
hepe),12
‑
羟基
‑
二十碳五烯酸(12
‑
hepe),11
‑
羟基
‑
二十碳五烯酸(11
‑
hepe),8
‑
羟基
‑
二十碳五烯酸(8
‑
hepe),5
‑
羟基
‑
二十碳五烯酸(5
‑
hepe),15
‑
羟基
‑
二十碳四烯酸(15
‑
hete),12
‑
羟基
‑
二十碳四烯酸(12
‑
hete),11
‑
羟基
‑
二十碳四烯酸(11
‑
hete),8
‑
羟基
‑
二十碳四烯酸(8
‑
hete),5
‑
羟基
‑
二十碳四烯酸(5
‑
hete),9
‑
羟基
‑
十八碳二烯酸(9
‑
hode),13
‑
羟基
‑
十八碳二烯酸酸(13
‑
hode),19z
‑
二十二碳六烯酸(pdx),保护素d1(pd1),阿司匹林触发的pd1(at
‑
pd1),马林素1(mar1),马林素2(mar2),白三烯b4(ltb4),t
‑
ltb4,消退素d1
‑
5(rvd1
‑
5),阿司匹林触发的rvd1(at
‑
rvd1),消退素e1(rve1),消退素e3(rve3),脂氧素a4(lxa4),脂氧素a5(lxa5),脂氧素b4(lxb4),脂氧素b5(lxb5),
[0084]
‑
增加宿主中epa的总量,
[0085]
‑
增加宿主中dha的总量,
[0086]
本发明的另一个主题是本发明的制剂使用合适的基质或载体在对皮肤、眼睛和在口腔中的局部应用中的用途。
[0087]
在优选的配置中,将制剂装载在包含纳米纤维素的预合成多相生物材料上和/或中,其中所述纳米纤维素是选自以下的细菌合成的纳米纤维素(bnc):
[0088]
‑
包含纤维素纤维或纳米晶须的网络的bnc,
[0089]
‑
包含两个或更多个不同层的纤维素原纤维的bnc,其中每个层由来自不同微生物或来自在不同条件下培养的微生物的bnc组成,
[0090]
‑
包含至少两个不同的纤维素网络的bnc,或
[0091]
‑
bnc复合材料,其进一步包含聚合物。
[0092]
纳米纤维素是指纳米结构纤维素的术语。它可以是纤维素纳米晶体(cnc或ncc)、也称为微纤化纤维素(mfc)的纤维素纳米纤维(cnf)或细菌纳米纤维素(bnc),其是指由细菌产生的纳米结构纤维素。bnc是一种由诸如komagataeibacter xylinus的菌株产生的纳米纤维聚合物,该komagataeibacter xylinus是在纤维素生产中效率最高的最佳细菌种之一。bnc是具有独特的特性的生物材料,该特征为例如:化学纯度,出色的机械强度,高柔韧性,高吸收性,由于非凡的可成型性和柔软性而具有形成任何形状和尺寸的可能性等。此外,该材料是素食的和严格素食的,并且具有高水分含量。
[0093]
细菌纤维素是三维网络,并且是固定和捕获微生物及其他物质的载体。固定的生物材料(包括微生物)用于生物活性代谢物(例如抗微生物剂、代谢生物活性物)的原位/体内生物合成,触发微生物和生物活性物的释放和/或用作用于发酵过程的固定微工厂。
[0094]
本发明的另一主题还是表现出以下特征的休眠形式的或作为营养细胞的巨大芽孢杆菌菌株用于spm的生物技术生产的用途:
[0095]
a)与根据seq id no:1或seq id no:2、seq id no:13或seq id no:14、seq id no:25或seq id no:26的多核苷酸序列具有至少99.5%、尤其是100%的序列同一性的16s rdna序列;和/或
[0096]
b)与根据seq id no:3、seq id no:15或seq id no:27的多核苷酸序列具有至少99.5%、尤其是100%的序列同一性的yqfd序列;和/或
[0097]
c)与根据seq id no:4、seq id no:16、seq id no:28的多核苷酸序列具有至少99.5%、尤其是100%的序列同一性的gyrb序列;和/或
[0098]
d)与根据seq id no:5、seq id no:17、seq id no:29的多核苷酸序列具有至少99.5%、尤其是100%的序列同一性的rpob序列;和/或
[0099]
e)与根据seq id no:6、seq id no:18、seq id no:30的多核苷酸序列具有至少99.5%、尤其是100%的序列同一性的groel序列。
[0100]
工作实施例
[0101]
实施例1:巨大芽孢杆菌菌株dsm 32963、dsm 33296和dsm 33299各自具有用于细胞色素p450单加氧酶(cyp450)的遗传序列。
[0102]
巨大芽孢杆菌菌株dsm 32963、dsm 33296和dsm 33299各自从来自威斯特伐利亚东部的原始花园的土壤样品中分离而来。它们已根据国际认可用于专利程序的微生物保存的布达佩斯条约的规定,以evonik degussa gmbh的名义以上文提及的登录号于2018年11月27日(dsm 32963)和2019年10月17日保藏于dsmz。
[0103]
巨大芽孢杆菌dsm 32963的基因组序列含有编码在氨基酸水平上与巨大芽孢杆菌atcc 14581(aaa87602.1)的p450 bm3(cyp102a1)具有97.9%的同一性的蛋白质的基因[seq id no:7]。该酶包含p450加氧酶和nadph:p
‑
450还原酶两者[46]。p450 bm3的天然底物经分析为长链脂肪酸(c12至c20),其仅在近末端位置被羟基化(ω
‑
1至ω
‑
3)[47]。
[0104]
与p450 bm3相比,对于在巨大芽孢杆菌dsm 32963的基因组序列内鉴定的序列观察到部分命中序列在氨基酸水平上21.1%至30.5%的较低序列相似性。与p450 bm3相比,这些其他潜在的细胞色素基因可能具有相似的功能[seq id no:8
‑
12](参见表1)。
[0105]
表1:针对巨大芽孢杆菌dsm 32963的蛋白质序列的p450 bm3的blastp(命中列中的seq id是指相应的核苷酸序列)
[0106]
[0107]
巨大芽孢杆菌dsm 33296的基因组序列含有编码在氨基酸水平上与巨大芽孢杆菌atcc 14581(aaa87602)的p450 bm3(cyp102a1)具有98.9%的同一性的蛋白质的基因[seq id no:19]。该酶包含p450加氧酶和nadph:p
‑
450还原酶两者[46]。p450 bm3的天然底物经分析为长链脂肪酸(c12至c20),其仅在近末端位置被羟基化(ω
‑
1至ω
‑
3)[47]。
[0108]
与p450 bm3相比,对于在巨大芽孢杆菌dsm 33296的基因组序列内鉴定的序列观察到部分命中序列在氨基酸水平上21.5%至30.7%的较低序列相似性。与p450 bm3相比,这些其他潜在的细胞色素基因可能具有相似的功能[seq id no:20
‑
24](参见表2)。
[0109]
表2:针对巨大芽孢杆菌dsm 33296的蛋白质序列的p450 bm3的blastp(命中列中的seq id是指相应的核苷酸序列)
[0110][0111]
巨大芽孢杆菌dsm 33299的基因组序列含有编码在氨基酸水平上与巨大芽孢杆菌atcc 14581(aaa87602.1)的p450 bm3(cyp102a1)具有96.1%的同一性的蛋白质的基因[seq id no:31]。该酶包含p450加氧酶和nadph:p
‑
450还原酶两者[46]。p450 bm3的天然底物经分析为长链脂肪酸(c12至c20),其仅在近末端位置被羟基化(ω
‑
1至ω
‑
3)[47]。
[0112]
与p450 bm3相比,对于在巨大芽孢杆菌dsm 33299的基因组序列内鉴定的序列观察到部分命中序列在氨基酸水平上20.9%至30.5%的较低序列相似性。与p450 bm3相比,这些其他潜在的细胞色素基因可能具有相似的功能[seq id no:32
‑
37](参见表3)。
[0113]
表3:针对巨大芽孢杆菌dsm 33299的蛋白质序列的p450 bm3的blastp(命中列中的seq id是指相应的核苷酸序列)
[0114][0115]
实施例2:在磷酸盐缓冲液中用二油基磷脂酰胆碱(dopc)制备ω
‑
3脂肪酸分散体
[0116]
为了制备ω
‑
3脂肪酸分散体的制剂,将0.8g的二油基磷脂酰胆碱(dopc,lipoid gmbh)溶解在1ml的乙醇中。添加并溶解0.2克鱼油(ω
‑
3 1400,)、ω
‑
3乙酯(500:200ee,basf)或ω
‑
3赖氨酸盐形式的游离ω
‑
3脂肪酸的赖氨酸盐(evonik)。在游离的ω
‑
3脂肪酸盐的情况下,添加20μl蒸馏水以完全溶解产品。
[0117]
形式为ω
‑
3赖氨酸盐的游离ω
‑
3脂肪酸的赖氨酸盐(evonik)含有约67%的脂肪酸和大量的ω
‑
3脂肪酸epa和dha,以及少量的ω
‑
3脂肪酸二十二碳五烯酸和ω
‑
6脂肪酸花生四烯酸、二十二碳四烯酸和二十二碳烯酸异构体。
[0118]
在45℃的温度下和在剧烈搅拌下,将1ml的相应溶液逐滴加入到20ml的ph=8的0.1m磷酸盐缓冲液中。之后,将分散体置于冰上并超声处理(branson sonifier,100%振幅,50%脉冲)15分钟,以产生纳米级分散体,推测是脂质体。最后,将分散体通过0.2μm注射器过滤器进行无菌过滤。通过动态光散射(dls)测量(zetasizer nano zs,malvern)表征所得分散体的粒度。该分散体包含40g/l的磷脂和10g/l的ω
‑
3脂肪酸或酯。
[0119]
实施例3:巨大芽孢杆菌株菌dsm 32963能够产生细胞内18
‑
羟基
‑
二十碳五烯酸(18
‑
hepe)
[0120]
对于巨大芽孢杆菌dsm 32963,可以证明产生spm的酶的相关的细胞内活性。从具有0.1%葡萄糖(lbg)的10ml luria bertami肉汤(lb,thermo fisher scientific)中,将巨大芽孢杆菌dsm 32963的培养物在100ml培养瓶中于30℃和200rpm培养24h。将完整的培养物转移至lbg中的200ml主培养物中。主培养物在2升培养瓶中于30℃和200rpm生长6小时。然后以10ml的体积份收获细胞培养物,通过离心(15min,4000rpm,室温)除去上清液,并
将细胞沉淀分别重悬于10ml lbg和2ml补充剂中(表2)。将这些培养物在100ml摇瓶中于30℃和200rpm孵育16小时。
[0121]
将不同形式的二十碳五烯酸(epa)和二十二碳六烯酸(dha)源添加到巨大芽孢杆菌dsm 32963细胞培养物中,以达到ω
‑
3赖氨酸盐(evonik的)、鱼油(的ω
‑
3 1400)和ω
‑
3乙酯(basf的500:200ee)的形式的0.4g/l的最终浓度。这些物质分别作为超声乳化液和分散体制剂(实施例2中所述的制剂)加入。
[0122]
将不含ω
‑
3脂肪酸含量的dopc制剂和pbs缓冲液用作不含epa的对照。
[0123]
表2:补充剂、储液的制备及其epa含量计算值(g/l)
[0124][0125]
通过离心(15分钟,4000rpm,室温)分离上清液,然后各自收获细胞培养物。然后,将上清液用由水/乙腈混合物组成的溶剂稀释(上清液:溶剂比例为1:2,溶剂组成:65%h2o,ph8和35%mecn)。将沉淀冷冻干燥过夜,并重悬于由水/乙腈混合物组成的溶剂中(沉淀:溶剂比例为1:2,溶剂组成:65%h2o,ph8和35%mecn)。细胞破碎是在ribolyser中的lysing matrix管(0.1mm硅胶球)中进行的。
[0126]
过滤细胞匀浆物(和稀释的上清液),然后将其用于通过lc/esi
‑
ms分析(agilent qqq 6420,gemini 3μc6
‑
phenyl)以阳性sim模式在m/z 318下检测18
‑
羟基
‑
二十碳五烯酸(18
‑
hepe),以及在m/z 302下检测前体化合物epa。
[0127]
将epa以具有dopc的ω
‑
3赖氨酸盐、ω
‑
3乙酯、ω
‑
3赖氨酸盐分散体或具有dopc的鱼油分散体的形式添加到巨大芽孢杆菌细胞中,导致18
‑
hepe的细胞相关(=细胞内 细胞外吸附的)积累(表3)。迄今为止,通过添加ω
‑
3赖氨酸盐可以实现细胞内18
‑
hepe的最高值;其是其他方法的十倍。
[0128]
表3:巨大芽孢杆菌dsm 32963细胞的细胞提取物中细胞相关18
‑
hepe的浓度(mg/ml)
[0129][0130]
实施例4:巨大芽孢杆菌dsm 32963和ω
‑
3脂肪酸盐的分散体制剂的合生元组合导致细胞外大量的18
‑
hepe
[0131]
为了研究细胞外出现的18
‑
hepe的量,按照实施例1的描述培养巨大芽孢杆菌dsm 32963细胞。将细胞重悬于10ml lbg或含9.76g/l fessif
‑
v2(biorelevant.com)(其是牛磺胆酸盐、磷脂和其他旨在模拟胆汁表面活性剂的组分的混合物)的lbg,并分别添加2ml的补充剂(表2)。另外,还将补充剂分别添加到没有细胞的摇瓶中的不同培养基中,并在相同条件下进行处理(对照)。在30℃和200rpm孵育16h后,测定培养上清液和对照的18
‑
hepe浓度(表4)。可以显示,巨大芽孢杆菌dsm 32963细胞能够从ω
‑
3赖氨酸盐分散体合成18
‑
hepe,其是可在细胞外检测的。值得注意的是,通过该方法检测的ω
‑3→
18
‑
hepe的转化率高达0.075,这超过了wo 2017/041094公开的酯化鱼油中0.0005%的18
‑
hepe的基础含量。更重要的是,我们发现巨大芽孢杆菌菌株将ω
‑
3赖氨酸盐转化为多种(最终)spm产品,其浓度甚至高于18
‑
hepe(参见实施例6),这是具有生理意义的。
[0132]
表4:培养上清液和对照的测量的18
‑
hepe浓度(mg/l)
[0133][0134]
实施例5:不同芽孢杆菌属种对epa的生物转化
[0135]
为了研究不同芽孢杆菌属种产生细胞内18
‑
hepe的能力,按照实施例1所述培养不同种的细胞。将细胞重悬于10ml含9.76g/l fessif
‑
v2(biorelevant.com)(其是牛磺胆酸盐、磷脂和其他旨在模拟胆汁表面活性剂的组分的混合物)的lbg中,并分别添加1.2ml含dopc的ω
‑
3赖氨酸盐分散体。如实施例3中所述测定在30℃和200rpm孵育16小时后细胞的内部18
‑
hepe浓度。
[0136]
仅巨大芽孢杆菌细胞能够从ω
‑
3赖氨酸盐分散体内部合成18
‑
hepe,而枯草芽孢杆菌(b.subtilis)、解淀粉芽孢杆菌(b.amyloliquefaciens)、短小芽孢杆菌(b.pumilus)和地衣芽孢杆菌(b.licheniformis)则不能。
[0137]
表5:巨大芽孢杆菌dsm 32963细胞的细胞内测量的18
‑
hepe含量(mg/ml)
[0138][0139]
实施例6:在不同的培养条件下,巨大芽孢杆菌dsm 32963从ω
‑
3脂肪酸盐产生spm
[0140]
脂质代谢组学
[0141]
细菌上清液样品经受使用rp相固相萃取的脂质提取,然后根据公开的程序[48]通过超高效液相色谱esi串联质谱分析(uplc
‑
ms/ms)进行分析。在这些条件下,大约40种不同的lm(包括5
‑
羟基
‑
二十碳五烯酸5
‑
hepe,8
‑
hepe,11
‑
hepe,12
‑
hepe,15
‑
hepe,18
‑
hepe,5
‑
羟基
‑
二十碳四烯酸(5
‑
hete),8
‑
hete,11
‑
hete,12
‑
hete,15
‑
hete,4
‑
羟基
‑
dha(4
‑
hdha),7
‑
hdha,13
‑
hdha,14
‑
hdha,17
‑
hdha,消退素a4(lxa4),lxb4,消退素e1(rve1),rve3,消退素d1
‑
5(rvd1
‑
5),at
‑
rvd1,rvd2,protectin d1(pd1),at
‑
pd1,maresin 1(mar1),mar2)和4种脂肪酸底物可以以1pg的检测下限被检测到。
[0142]
为了研究除了18
‑
hepe之外,巨大芽孢杆菌是否还能够产生其他pufa氧合产物,进行来自如实施例4中所述培养的巨大芽孢杆菌菌株32963的具有(溶解的或在分散体制剂中)的上清液(具有或不具有胆汁酸)的脂代谢组学筛选。并行处理和分析制剂的无细胞制剂,并将其用作氧合产物的非酶促的自发形成的对照。表6中给出的值显示了形成的产物的净浓度,即减去对照值后。可以看出,通过细菌已经形成了包括spm在内的许多氧合产物。几种spm的浓度远远超过了人体血浆样品中发现的spm浓度(其通常在约20
‑
100pg/ml的范围内)[27、40、41]。为了进行比较,人母乳含有约6.000pg/ml rve1和约10.000pg/ml rvd1[42]。考虑到spm在nm或甚至pm范围内在啮齿动物中体内和体内地发挥受体介导的作用的事实[6],表6中显示的发现结果强烈暗示了本发明的生理和治疗重要性。
[0143]
pufa制剂的类型对产物水平(其通常在存在pufa分散体制剂和/或添加胆汁酸作为增溶剂的情况下更高)有很大的影响。并行地,与在没有分散体制剂和胆汁酸的情况下用availom处理的样品相比,这些样品中单羟基化spm前体5
‑
hepe、11
‑
hepe、12
‑
hepe、15
‑
hepe、18
‑
hepe、5
‑
hete、8
‑
hete和9
‑
hode的丰度较低。这可以通过这些前体向二羟基化和三羟基化脂肪酸的增加的转化来解释。
[0144]
表6:巨大芽孢杆菌dsm 32963细胞的pufa氧合产物的细胞外浓度
[0145][0146]
实施例7:通过其它巨大芽孢杆菌菌株从ω
‑
3脂肪酸盐的分散体制
剂产生spm
[0147]
筛选了来自不同生境的另外47种巨大芽孢杆菌菌株的spm生产能力,以确定这是否是巨大芽孢杆菌种的普遍现象,并检测所生产的spm的类型和数量的菌株特异性差异。如实施例4中所详述地培养细胞,其中的分散体制剂用作ω
‑
3脂肪酸源。并行地处理和分析的无细胞制剂,并将其用作氧合产物的非酶促的自发形成的对照。观察到所有测试的菌株均产生可测量的(>1pg/ml)量的各种spm及其前体,这些量在菌株之间差异极大(高达2.000倍),并且rve3的浓度在大多数菌株中特别高(高达1.3μg/ml)。
[0148]
表7中给出的值显示了由两个表现最强的菌株(巨大芽孢杆菌dsm 33296和巨大芽孢杆菌dsm 33299)形成的pufa氧合产物的净浓度。
[0149]
表7:巨大芽孢杆菌dsm 33296和巨大芽孢杆菌dsm 33299细胞的pufa氧合产物的细胞外浓度。
[0150][0151]
实施例8:包含epa
‑
dha氨基酸盐和巨大芽孢杆菌菌株的胶囊作为食物补充剂或作为药物
[0152]
将以下组分填充入hpmc胶囊(00尺寸)中。
of airway inflammation in asthma.pharmacol ther 2018,186:98
‑
113.
[0180]
20.aoki h,hisada t,ishizuka t,utsugi m,kawata t,shimizu y,okajima f,dobashi k,mori m:resolvin e1 dampens airway inflammation and hyperresponsiveness in a murine model of asthma.biochem biophys res commun 2008,367(2):509
‑
515.
[0181]
21.perretti m,norling lv:actions of spm in regulating host responses in arthritis.mol aspects med 2017,58:57
‑
64.
[0182]
22.dalli j,zhu m,vlasenko na,deng b,haeggstrom jz,petasis na,serhan cn:the novel 13s,14s
‑
epoxy
‑
maresin is converted by human macrophages to maresin 1(mar1),inhibits leukotriene a4 hydrolase(lta4h),and shifts macrophage phenotype.faseb j 2013,27(7):2573
‑
2583.
[0183]
23.liu y,fang x,zhang x,huang j,he j,peng l,ye c,wang y,xue f,ai d et al:metabolic profiling of murine plasma reveals eicosapentaenoic acid metabolites protecting against endothelial activation and atherosclerosis.br j pharmacol 2018,175(8):1190
‑
1204.
[0184]
24.endo j,sano m,isobe y,fukuda k,kang jx,arai h,arita m:18
‑
hepe,an n
‑
3 fatty acid metabolite released by macrophages,prevents pressure overload
‑
induced maladaptive cardiac remodeling.j exp med 2014,211(8):1673
‑
1687.
[0185]
25.pochard c,coquenlorge s,jaulin j,cenac n,vergnolle n,meurette g,freyssinet m,neunlist m,rolli
‑
derkinderen m:defects in 15
‑
hete production and control of epithelial permeability by human enteric glial cells from patients with crohn's disease.gastroenterology 2016,150(1):168
‑
180.
[0186]
26.tang y,zhang mj,hellmann j,kosuri m,bhatnagar a,spite m:proresolution therapy for the treatment of delayed healing of diabetic wounds.diabetes 2013,62(2):618
‑
627.
[0187]
27.barden ae,mas e,croft kd,phillips m,mori ta:specialized proresolving lipid mediators in humans with the metabolic syndrome after n
‑
3 fatty acids and aspirin.am j clin nutr 2015,102(6):1357
‑
1364.
[0188]
28.miyata j,arita m:role of omega
‑
3 fatty acids and their metabolites in asthma and allergic diseases.allergol int 2015,64(1):27
‑
34.
[0189]
29.mangino mj,brounts l,harms b,heise c:lipoxin biosynthesis in inflammatory bowel disease.prostaglandins other lipid mediat 2006,79(1
‑
2):84
‑
92.
[0190]
30.wang cw,colas ra,dalli j,arnardottir hh,nguyen d,hasturk h,chiang n,van dyke te,serhan cn:maresin 1 biosynthesis and proresolving anti
‑
infective functions with human
‑
localized aggressive periodontitis leukocytes.infect immun 2015,84(3):658
‑
665.
[0191]
31.ringholz fc,buchanan pj,clarke dt,millar rg,mcdermott m,linnane b,harvey bj,mcnally p,urbach v:reduced 15
‑
lipoxygenase 2 and lipoxin a4/
resolvins and declining docosahexaenoic acid levels in human milk during the first month of lactation.lipids health dis 2013,12:89.
[0203]
43.piewngam p,zheng y,nguyen th,dickey sw,joo hs,villaruz ae,glose ka,fisher el,hunt rl,li b et al:pathogen elimination by probiotic bacillus via signalling interference.nature 2018,562(7728):532
‑
537.
[0204]
44.al
‑
thubiani asa,maher ya,fathi a,abourehab mas,alarjah m,khan msa,al
‑
ghamdi sb:identification and characterization of a novel antimicrobial peptide compound produced by bacillus megaterium strain isolated from oral microflora.saudi pharm j 2018,26(8):1089
‑
1097.
[0205]
45.miura m,ito k,hayashi m,nakajima m,tanaka t,ogura s:the effect of 5
‑
aminolevulinic acid on cytochrome p450
‑
mediated prodrug activation.plos one 2015,10(7):e0131793.
[0206]
46.ruettinger rt,wen lp,fulco aj:coding nucleotide,5'regulatory,and deduced amino acid sequences of p
‑
450bm
‑
3,a single peptide cytochrome p
‑
450:nadph
‑
p
‑
450 reductase from bacillus megaterium.j biol chem 1989,264(19):10987
‑
10995.
[0207]
47.kang jy,kim sy,kim d,kim dh,shin sm,park sh,kim kh,jung hc,pan jg,joung yh et al:characterization of diverse natural variants of cyp102a1 found within a species of bacillus megaterium.amb express 2011,1(1):1.
[0208]
48.werz o,gerstmeier j,libreros s,de la rosa x,werner m,norris pc,chiang n,serhan cn:human macrophages differentially produce specific resolvin or leukotriene signals that depend on bacterial pathogenicity.nat commun 2018,9(1):59.
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。