1.本发明涉及药物技术领域,尤其涉及一种药物与靶点之间亲和力的预测方法、装置及设备。
背景技术:
2.随着人工智能(ai)的不断发展,基于人工智能(ai)的药物设计具有巨大的潜力,可以彻底改变药物设计和药物发现。对于所有基于ai的药物设计模型,分子表示都是至关重要的。一般来说,分子表示有两种类型:第一类是特征工程,它可以计算分子的结构、物理、化学和生物学特性,并将其用作学习模型的分子描述符。本质上,分子表示为一组预定义的手工特征,包括分子式、片段、图案、拓扑特征、几何特征、构象特性、疏水性、电子特性、位阻特性等信息。大量的分子描述符已经提出并广泛用于定量构效关系(quantitative structure
‑
activity relationship,简称qsar)和学习模型。第二种是使用3d卷积神经网络和图神经网络的端到端表示学习,在这些模型中,分子表示为具有每个单元格包含某些分子特征的网格数据,或者,表示为在其顶点和边缘上嵌入了分子属性的图形。
3.最近,基于几何学的分子表征在药物设计中取得了重大进展,与以往的模型不同,分子描述符和指纹被定义为微分几何、代数拓扑和代数图理论中的几何、拓扑和组合不变量。因此,如何将数学中的分子表示方式应用于药物设计是一种值得研究的问题。
技术实现要素:
4.本发明实施例提供了一种药物与靶点之间亲和力的预测方法、装置及设备,能够准确地预测药物与靶点之间的结合亲和力。
5.第一方面,本发明实施例提供一种药物与靶点之间亲和力的预测方法,包括:
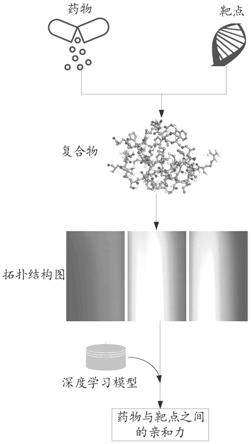
6.获取药物和用于与所述药物相互作用的靶点;
7.确定所述药物与所述靶点相互作用后的复合物;
8.计算用于标识所述复合物中原子空间特性的拓扑结构图;
9.基于所述拓扑结构图,确定所述药物与靶点之间的亲和力。
10.第二方面,本发明实施例提供一种药物与靶点之间亲和力的预测装置,包括:
11.第一获取模块,用于获取药物和用于与所述药物相互作用的靶点;
12.第一确定模块,用于确定所述药物与所述靶点相互作用后的复合物;
13.第一计算模块,用于计算用于标识所述复合物中原子空间特性的拓扑结构图;
14.第一处理模块,用于基于所述拓扑结构图,确定所述药物与靶点之间的亲和力。
15.第三方面,本发明实施例提供一种电子设备,包括:存储器、处理器;其中,所述存储器用于存储一条或多条计算机指令,其中,所述一条或多条计算机指令被所述处理器执行时实现上述第一方面中的药物与靶点之间亲和力的预测方法。
16.第四方面,本发明实施例提供了一种计算机存储介质,用于储存计算机程序,所述计算机程序使计算机执行时实现上述第一方面中的药物与靶点之间亲和力的预测方法。
17.第五方面,本发明实施例提供了一种药物与靶点之间亲和力的预测方法,包括:
18.响应于调用亲和力预测服务的请求,确定所述亲和力预测服务对应的处理资源;
19.利用所述处理资源执行如下步骤:获取药物和用于与所述药物相互作用的靶点,确定所述药物与所述靶点相互作用后的复合物,计算用于标识所述复合物中原子空间特性的拓扑结构图,基于所述拓扑结构图,确定所述药物与靶点之间的亲和力。
20.第六方面,本发明实施例提供了一种药物与靶点之间亲和力的预测装置,包括:
21.第二确定模块,用于响应于调用亲和力预测服务的请求,确定所述亲和力预测服务对应的处理资源;
22.第二处理模块,用于利用所述处理资源执行如下步骤:获取药物和用于与所述药物相互作用的靶点,确定所述药物与所述靶点相互作用后的复合物,计算用于标识所述复合物中原子空间特性的拓扑结构图,基于所述拓扑结构图,确定所述药物与靶点之间的亲和力。
23.第七方面,本发明实施例提供了一种电子设备,包括:存储器、处理器;其中,所述存储器用于存储一条或多条计算机指令,其中,所述一条或多条计算机指令被所述处理器执行时实现上述第五方面中的药物与靶点之间亲和力的预测方法。
24.第八方面,本发明实施例提供了一种计算机存储介质,用于储存计算机程序,所述计算机程序使计算机执行时实现上述第五方面中的药物与靶点之间亲和力的预测方法。
25.本实施例提供的药物与靶点之间亲和力的预测方法、装置及设备,通过获取药物和用于与所述药物相互作用的靶点,确定所述药物与所述靶点相互作用后的复合物,并计算用于标识所述复合物中原子空间特性的拓扑结构图,而后基于所述拓扑结构图来确定所述药物与靶点之间的亲和力,有效地实现了可以基于复合物所对应的拓扑结构图来确定药物与靶点之间的亲和力,从而保证了对亲和力进行确定的准确可靠性,还可以基于所预测的亲和力来确定药物和靶点作用的稳定性,从而提高了该预测方法的实用性。
附图说明
26.为了更清楚地说明本发明实施例或现有技术中的技术方案,下面将对实施例或现有技术描述中所需要使用的附图作一简单地介绍,显而易见地,下面描述中的附图是本发明的一些实施例,对于本领域普通技术人员来讲,在不付出创造性劳动的前提下,还可以根据这些附图获得其他的附图。
27.图1为本发明实施例提供的一种药物与靶点之间亲和力的预测方法的原理示意图;
28.图2为本发明实施例提供的一种药物与靶点之间亲和力的预测方法的流程示意图;
29.图3为本发明实施例提供的一种计算用于标识所述复合物中原子空间特性的拓扑结构图的流程示意图;
30.图4为本发明实施例提供的获取所述复合物中设定原子之间的相互作用距离的流程示意图;
31.图5为本发明实施例提供的基于所述第一坐标和所述第二坐标,确定所述至少一个第一原子与所述至少一个第二原子之间的相互作用距离的流程示意图;
32.图6为本发明实施例提供的基于所述拓扑结构图,确定所述药物与靶点之间的亲和力的流程示意图;
33.图7为本发明实施例提供的基于所述至少一个亲和力,确定所述药物与靶点之间的目标亲和力的流程示意图;
34.图8为本发明实施例提供的获取与所述至少一个亲和力中的每个亲和力相对应的权重系数的流程示意图;
35.图9为本发明实施例提供的一种药物与靶点之间亲和力的预测方法的流程示意图;
36.图10为本发明应用实施例提供的确定用于标识所述复合物中原子空间特性的拓扑结构图的示意图一;
37.图11为本发明应用实施例提供的确定用于标识所述复合物中原子空间特性的拓扑结构图的示意图二;
38.图12为本发明应用实施例提供的一种药物与靶点之间亲和力的预测方法的原理示意图;
39.图13为本发明实施例提供的一种药物与靶点之间亲和力的预测装置的结构示意图;
40.图14为与图13所示实施例提供的药物与靶点之间亲和力的预测装置对应的电子设备的结构示意图;
41.图15为本发明实施例提供的另一种药物与靶点之间亲和力的预测方法的流程示意图;
42.图16为本发明实施例提供的另一种药物与靶点之间亲和力的预测装置的结构示意图;
43.图17为与图16所示实施例提供的药物与靶点之间亲和力的预测装置对应的电子设备的结构示意图。
具体实施方式
44.为使本发明实施例的目的、技术方案和优点更加清楚,下面将结合本发明实施例中的附图,对本发明实施例中的技术方案进行清楚、完整地描述,显然,所描述的实施例是本发明一部分实施例,而不是全部的实施例。基于本发明中的实施例,本领域普通技术人员在没有作出创造性劳动前提下所获得的所有其他实施例,都属于本发明保护的范围。
45.在本发明实施例中使用的术语是仅仅出于描述特定实施例的目的,而非旨在限制本发明。在本发明实施例和所附权利要求书中所使用的单数形式的“一种”、“所述”和“该”也旨在包括多数形式,除非上下文清楚地表示其他含义,“多种”一般包含至少两种,但是不排除包含至少一种的情况。
46.应当理解,本文中使用的术语“和/或”仅仅是一种描述关联对象的关联关系,表示可以存在三种关系,例如,a和/或b,可以表示:单独存在a,同时存在a和b,单独存在b这三种情况。另外,本文中字符“/”,一般表示前后关联对象是一种“或”的关系。
47.取决于语境,如在此所使用的词语“如果”、“若”可以被解释成为“在
……
时”或“当
……
时”或“响应于确定”或“响应于检测”。类似地,取决于语境,短语“如果确定”或“如
果检测(陈述的条件或事件)”可以被解释成为“当确定时”或“响应于确定”或“当检测(陈述的条件或事件)时”或“响应于检测(陈述的条件或事件)”。
48.还需要说明的是,术语“包括”、“包含”或者其任何其他变体意在涵盖非排他性的包含,从而使得包括一系列要素的商品或者系统不仅包括那些要素,而且还包括没有明确列出的其他要素,或者是还包括为这种商品或者系统所固有的要素。在没有更多限制的情况下,由语句“包括一个
……”
限定的要素,并不排除在包括所述要素的商品或者系统中还存在另外的相同要素。
49.另外,下述各方法实施例中的步骤时序仅为一种举例,而非严格限定。
50.术语定义:
51.持久谱图(perspect图),用于标识拓扑特征的持久性和变化程度的图结构。
52.单纯复形,给定k=(v,s),其中,v是顶点的集合,s是2
v
的子集,如果满足:(1)由可推出τ
`
∈s;(2)或者τ
`
∩τ是τ
`
和τ的公共面,则称k=(v,s)是一个单纯复形。
53.单纯形的久性拓扑图(perspect单纯复形),为单纯形所对应的拓扑结构图,其中,给定k=(v,s),如果2
v
的任意子集都包含在s中,则称k=(v,s)是一个单纯形。
54.持久超图(perspect超图),用于标识超图的拓扑特征的持久性和变化程度的图结构。
55.最近,基于几何学的分子表征在药物设计中取得了重大进展,与以往的模型不同,分子描述符和指纹被定义为微分几何、代数拓扑和代数图理论中的几何、拓扑和组合不变量。这些模型可以在药物设计的各个步骤中显着提高学习模型的性能,包括:蛋白质
‑
配体结合亲和力预测、预测突变后蛋白质稳定性变化、毒性预测、溶剂化自由能预测、分配系数和水溶解度、结合口袋检测和药物发现。
56.由于这些先进的数学模型在药物设计中取得了巨大的成功,因此,本实施例提供了一种基于持久谱图(perspect)理论的药物与靶点之间亲和力的预测方法,该预测方法可以适用于perspect图、perspect单纯复形和perspect超图。具体的,上述预测方法的执行主体为预测装置,该预测装置可以与客户端通信连接。
57.其中,客户端可以是任何具有一定计算能力的计算设备。客户端的基本结构可以包括:至少一个处理器。处理器的数量取决于客户端的配置和类型。客户端也可以包括存储器,该存储器可以为易失性的,例如ram,也可以为非易失性的,例如只读存储器(read
‑
only memory,简称rom)、闪存等,或者也可以同时包括两种类型。存储器内通常存储有操作系统(operating system,简称os)、一个或多个应用程序,也可以存储有程序数据等。除了处理单元和存储器之外,客户端还包括一些基本配置,例如网卡芯片、io总线、显示组件以及一些外围设备等。可选地,一些外围设备可以包括,例如键盘、鼠标、输入笔、打印机等。其它外围设备在本领域中是众所周知的,在此不做赘述。可选地,客户端可以为pc(personal computer)终端、手持终端(例如:智能手机、平板电脑)等。
58.预测装置可以是指可以在网络虚拟环境中提供计算处理服务的设备,通常是指利用网络进行信息规划、对药物与靶点之间的亲和力进行预测的装置。在物理实现上,药物与靶点之间亲和力的预测装置可以是任何能够提供计算服务,响应服务请求,并进行处理的设备,例如:可以是集群服务器、常规服务器、云服务器、云主机、虚拟中心等。药物与靶点之
间亲和力的预测装置的构成主要包括处理器、硬盘、内存、系统总线等,和通用的计算机架构类似。
59.在上述本实施例中,客户端可以与药物与靶点之间亲和力的预测装置进行网络连接,该网络连接可以是无线或有线网络连接。若客户端与药物与靶点之间亲和力的预测装置是通信连接,该移动网络的网络制式可以为2g(gsm)、2.5g(gprs)、3g(wcdma、td
‑
scdma、cdma2000、utms)、4g(lte)、4g (lte )、wimax等中的任意一种。
60.在本技术实施例中,客户端用于获取药物和用于与药物相互作用的靶点,其中,药物是指需要进行亲和力预测的药物,具体的,药物和与药物相互作用的靶点可以是预先配置的,或者,药物和与药物相互作用的靶点可以是用户输入或者用户指定的,当然的,本领域技术人员也可以采用其他的方式来获取药物和与相互作用的靶点,在此不再赘述。在获取到药物和用于与药物相互作用的靶点之后,可以将药物和与药物相互作用的靶点发送至预测装置,以使预测装置可以对药物和靶点之间的亲和力进行预测处理。
61.具体的,参考附图1所示,药物与靶点之间亲和力的预测装置,用于获取药物和用于与药物相互作用的靶点,在获取到药物和靶点之后,可以将药物和靶点进行相互作用,从而可以确定药物与靶点相互作用后的复合物,而后计算用于标识复合物中原子空间特性的拓扑结构图,可以理解的是,所获得的拓扑结构图的数量为至少一组,每组拓扑结构图中包括多个拓扑结构图,并且,该拓扑结构图可以包括以下至少之一:持久谱图、单纯形的久性拓扑图、单纯形的久性拓扑图的变化特征、持久超图;其中,持久谱图用于标识拓扑特征的持久性和变化程度,持久超图用于标识超图的拓扑特征的持久性和变化程度。在获取到拓扑结构图之后,可以将拓扑结构图输入至预先训练好的深度学习模型中,深度学习模型可以对拓扑结构图进行分析处理,从而可以确定药物与靶点之间的亲和力。
62.本实施例提供的技术方案,通过获取药物和用于与药物相互作用的靶点,确定药物与靶点相互作用后的复合物,计算用于标识复合物中原子空间特性的拓扑结构图,而后基于拓扑结构图确定药物与靶点之间的亲和力,有效地实现了可以基于复合物所对应的拓扑结构图来确定药物与靶点之间的亲和力,不仅保证了对亲和力进行确定的准确可靠性,并且还可以基于所预测的亲和力来确定药物和靶点作用的稳定性,从而提高了该预测方法的实用性。
63.下面结合附图,对本发明的一些实施方式作详细说明。在各实施例之间不冲突的情况下,下述的实施例及实施例中的特征可以相互组合。
64.图2为本发明实施例提供的一种药物与靶点之间亲和力的预测方法的流程示意图;参考附图2所示,本实施例提供了一种药物与靶点之间亲和力的预测方法,该方法的执行主体为药物与靶点之间亲和力的预测装置,可以理解的是,该预测装置可以实现为软件、或者软件和硬件的组合。具体的,该药物和靶点之间亲和力的预测方法可以包括:
65.步骤s201:获取药物和用于与药物相互作用的靶点。
66.步骤s202:确定药物与靶点相互作用后的复合物。
67.步骤s203:计算用于标识复合物中原子空间特性的拓扑结构图。
68.步骤s204:基于拓扑结构图,确定药物与靶点之间的亲和力。
69.下面对上述各个步骤的具体实现过程和实现效果进行详细说明:
70.步骤s201:获取药物和用于与药物相互作用的靶点。
71.其中,药物可以是指需要进行亲和力检测的药物,靶点用于与药物进行相互作用,从而可以生成用于进行亲和力预测操作的复合物,具体的,本实施例对于药物和靶点的具体获取方式不做限定,本领域技术人员可以根据具体的应用场景和应用需求进行设置,例如:预先设置有多个药物数据和靶点数据,而后可以通过检测装置获取用户针对任意一个药物数据和任意一个靶点数据所输入的执行操作,通过所获得的执行操作确定需要进行亲和力检测的药物和与药物相互作用的靶点。或者,需要进行亲和力检测操作的药物和与药物相互作用的靶点可以存储在预设区域中,通过访问预设区域可以获取到药物和用于与药物相互作用的靶点。或者,需要进行亲和力检测操作的药物和与药物相互作用的靶点可以是第三设备发送至预测装置的,从而使得预测装置可以获取到需要进行亲和力检测操作的药物和用于与药物相互作用的靶点。
72.当然的,本领域技术人员也可以采用其他的方式来获取药物和用于与药物相互作用的靶点,只要能够保证对药物和靶点进行获取的准确可靠性即可,在此不再赘述。
73.步骤s202:确定药物与靶点相互作用后的复合物。
74.在获取到药物和靶点之后,则可以将药物和靶点进行相互作用,从而可以获得药物与靶点相互作用后的复合物。具体的,确定药物与靶点相互作用后的复合物,包括:将药物与靶点相互作用,获得药物与靶点之间的作用强度;在作用强度大于或等于预设阈值时,获得药物与靶点相互作用后的复合物。
75.具体的,在获取到药物和靶点之后,可以将药物与靶点之间进行相互作用,并可以获取到药物与靶点之间的作用强度。需要注意的是,不同的药物与不同的靶点之间进行相互作用,或者,同一药物与不同的靶点之间进行相互作用时,可以对应有不同的作用强度,例如:在药物a与靶点a之间进行相互作用时,作用强度为a
‑
a,在药物a与靶点b之间进行相互作用时,作用强度为a
‑
b,药物b与靶点a之间进行相互作用时,作用强度为b
‑
a,其中,作用强度a
‑
a、作用强度a
‑
b与作用强度b
‑
a可以相同或者不同。
76.另外,本实施例对于药物与靶点相互作用后的复合物进行确定的实现方式不做限定,本领域技术人员可以根据具体的应用场景和应用需求进行设置,例如:复合物可以是虚拟对接操作所获得的预测结构或者是通过实验检测获得的结构,一般情况下,当通过实验检测获得复合物结构时,检测获得即时稳定的复合物;而通过虚拟对接操作所获得的预测结果一般是虚拟结构,可以用于靶点发现。
77.步骤s203:计算用于标识复合物中原子空间特性的拓扑结构图。
78.在获取到复合物之后,可以对复合物进行分析识别,以计算用于标识复合物中原子空间特征的拓扑结构图,拓扑结构图的数量可以为至少一组,即拓扑结构图的数量可以为一组或多组,每组拓扑结构图可以包括多个拓扑结构图,而不同组的拓扑结构图中可以包括不同数量的拓扑结构图。另外,该拓扑结构图可以包括以下至少之一:持久谱图、单纯形的久性拓扑图、单纯形的久性拓扑图的变化特征、持久超图;其中,持久谱图用于标识拓扑特征的持久性和变化程度,持久超图用于标识超图的拓扑特征的持久性和变化程度。可以理解的是,拓扑结构图可以不仅包括上述所限定的技术特征,本领域技术人员还可以根据具体的应用场景和应用需求进行设置,例如:拓扑结构图可以包括单纯形的久性拓扑特征,上述的久性拓扑特征可以包括:久性拓扑节点特征、久性拓扑边特征等等。
79.具体的,在拓扑结构图包括持久谱图和单纯形的久性拓扑图时,拓扑结构图可以
包括多个持久谱图,而每个持久谱图可以包括一个或多个单纯形的久性拓扑图,即此时的拓扑结构图呈嵌套式结构。
80.步骤s204:基于拓扑结构图,确定药物与靶点之间的亲和力。
81.在获取到拓扑结构图之后,可以对拓扑结构图进行分析处理,以确定药物与靶点之间的亲和力。在一些实例中,所获取到的拓扑结构图的数量可以为至少一组,即拓扑结构图的数量可以为一组或多组,其中,每组拓扑结构图中可以包括多个拓扑结构图。例如,在获取到药物之后,可以计算获得与药物相对应的两组拓扑结构图,其中一组拓扑结构图中可以包括36个拓扑结构图,另外一组拓扑结构图中可以包括50个拓扑结构图。
82.此时,基于拓扑结构图,确定药物与靶点之间的亲和力可以包括:利用深度学习模型对每组拓扑结构图进行分析处理,获得与至少一组拓扑结构图相对应的至少一个亲和力,其中,深度学习模型被训练为用于基于拓扑结构图确定药物与靶点之间的亲和力;基于至少一个亲和力,确定药物与靶点之间的目标亲和力。
83.具体的,预先训练有用于基于拓扑结构图来确定药物与靶点之间的亲和力的深度学习模型,在获取到至少一组拓扑结构图之后,可以将至少一组拓扑结构图输入至深度学习模型,该深度学习模型可以对每组拓扑结构图进行分析处理,从而可以获取到与至少一组拓扑结构图相对应的至少一个亲和力。在获取到至少一个亲和力之后,可以对至少一个亲和力进行分析处理,在一些实例中,对至少一个亲和力进行分析处理可以包括对至少一个亲和力进行加权求和处理,从而可以确定靶点与药物之间的目标亲和力。
84.当然的,本领域技术人员也可以采用其他的方式来确定药物与靶点之间的亲和力,只要能够保证对药物与靶点之间的亲和力进行确定的准确可靠性,在此不再赘述。
85.本实施例提供的药物与靶点之间亲和力的预测方法,通过获取药物和用于与药物相互作用的靶点,确定药物与靶点相互作用后的复合物,并计算用于标识复合物中原子空间特性的拓扑结构图,而后基于拓扑结构图来确定药物与靶点之间的亲和力,有效地实现了可以基于复合物所对应的拓扑结构图来确定药物与靶点之间的亲和力,不仅保证了对亲和力进行确定的准确可靠性,并且还可以基于所预测的亲和力来确定药物和靶点作用的稳定性,从而提高了该预测方法的实用性。
86.图3为本发明实施例提供的一种计算用于标识复合物中原子空间特性的拓扑结构图的流程示意图;在上述实施例的基础上,参考附图3所示,本实施例提供了一种计算用于标识复合物中原子空间特性的拓扑结构图的实现方式,具体的,本实施例中的计算用于标识复合物中原子空间特性的拓扑结构图可以包括:
87.步骤s301:获取复合物中设定原子之间的相互作用距离。
88.步骤s302:基于相互作用距离,确定用于标识复合物中原子空间特性的拓扑结构图。
89.其中,在生成复合物的过程中,药物中的某些原子会与靶点中的某些原子之间进行相互作用,此时,药物中的原子与靶点原子之间会存在相互作用距离。具体的,上述的设定原子可以包括以下至少之一:位于药物中的氢原子(h)、碳原子(c)、氮原子(n)、氧原子(o)和硫原子(s),位于靶点中的氢原子(h)、碳原子(c)、氮原子(n)、氧原子(o)、硫原子(s)、磷原子(p)、氟原子(f)和氯原子(cl)、溴原子(br)和碘原子(i)。在确定复合物中的设定原子之后,可以获取复合物中设定原子之间的相互作用距离,例如:碳原子与氢原子之间的相
互作用距离,碳原子与碳原子之间的相互作用距离,碳原子与氧原子之间的相互作用距离等等。
90.在获取到相互作用距离之后,可以对相互作用距离进行分析处理,以确定用于标识复合物中原子空间特性的拓扑结构图。在一些实例中,基于相互作用距离,确定用于标识复合物中原子空间特性的拓扑结构图可以包括:基于相互作用距离,获取用于标识复合物中原子空间特性的组合拉普拉斯矩阵;基于组合拉普拉斯矩阵,确定拓扑结构图。
91.具体的,在获取到相互作用距离之后,可以对相互作用距离进行分析处理,以获取用于标识复合物中原子空间特性的组合拉普拉斯矩阵,具体的组合拉普拉斯矩阵可以表示为以下公式:
[0092][0093]
其中,表示为一个面,用于标识的k
‑
单纯形的程度,其可以是k 1单纯形的数目,表示为两个单形复数上相邻,它们有一个共同的k 1单纯形作为他们的面,与的表示内容相反;表示为两个单形复数下相邻,它们有一个共同的k
‑
1单纯形作为他们的面,与上述符号表示含义相反,用于标识两个单纯形具有相同的方向,与上述符号的表示含义相反。
[0094]
在获取到组合拉普拉斯矩阵之后,可以对组合拉普拉斯矩阵进行分析处理,以确定用于标识复合物中原子空间特性的拓扑结构图,这样有效地保证了对拓扑结构图进行获取的准确可靠性。
[0095]
图4为本发明实施例提供的获取复合物中设定原子之间的相互作用距离的流程示意图一;在上述实施例的基础上,参考附图4所示,本实施例提供了一种获取复合物中设定原子之间的相互作用距离的实现方式,具体的,本实施例中的获取复合物中设定原子之间的相互作用距离可以包括:
[0096]
步骤s401:获取与药物相对应的至少一个第一原子和与靶点相对应的至少一个第二原子。
[0097]
步骤s402:计算至少一个第一原子的第一坐标和至少一个第二原子的第二坐标。
[0098]
步骤s403:基于第一坐标和第二坐标,确定至少一个第一原子与至少一个第二原子之间的相互作用距离。
[0099]
其中,与药物相对应的至少一个第一原子可以包括以下至少之一:碳原子(c)、氮原子(n)、氧原子(o)和硫原子(s);与靶点相对应的至少一个第二原子可以包括以下至少之一:碳原子(c)、氮原子(n)、氧原子(o)、硫原子(s)、磷原子(p)、氟原子(f)和氯原子(cl)、溴原子(br)和碘原子(i)。
[0100]
在药物与靶点进行相互作用时,为了能够准确地获取到复合物中设定原子之间的相互作用距离,则可以获取与药物相对应的至少一个第一原子和与靶点相对应的至少一个第二原子,而后计算至少一个第一原子的第一坐标和至少一个第二原子的第二坐标,在获取到第一坐标和第二坐标之后,可以对第一坐标和第二坐标进行分析处理,以确定至少一个第一原子与至少一个第二原子之间的相互作用距离。
[0101]
在一些实例中,基于第一坐标和第二坐标,确定至少一个第一原子与至少一个第二原子之间的相互作用距离可以包括:基于第一坐标和第二坐标,确定至少一个第一原子与至少一个第二原子之间的欧式距离;将欧式距离,确定为至少一个第一原子与至少一个第二原子之间的相互作用距离。
[0102]
具体的,在获取到第一坐标和第二坐标之后,可以对第一坐标和第二坐标进行分析处理,以确定至少一个第一原子与至少一个第二原子之间的欧式距离,该欧式距离可以用以下公式进行表示:
[0103][0104]
其中,r
i
为第一原子的第一坐标,r
j
为第二原子的第二坐标,m(m
i
,m
j
)为欧式距离。在获取到欧式距离之后,可以将欧式距离确定为至少一个第一原子与至少一个第二原子之间的相互作用距离。
[0105]
需要注意的是,与药物相对应的至少一个第一原子的数量可以为4个,与靶点相对应的至少一个第二原子的数量可以为9个,因此,所获得的第一原子和第二原子之间的相互作用距离的数量可以为36个。
[0106]
本实施例中,通过获取与药物相对应的至少一个第一原子和与靶点相对应的至少一个第二原子,而后计算至少一个第一原子的第一坐标和至少一个第二原子的第二坐标,并基于第一坐标和第二坐标来确定至少一个第一原子与至少一个第二原子之间的相互作用距离,这样不仅提供了一种确定相互作用距离的实现方式,并且有效地保证了对相互作用距离进行确定的准确可靠性。
[0107]
图5为本发明实施例提供的基于第一坐标和第二坐标,确定至少一个第一原子与至少一个第二原子之间的相互作用距离的流程示意图;在上述实施例的基础上,参考附图5所示,本实施例提供了另一种获取复合物中设定原子之间的相互作用距离的实现方式,具体的,本实施例中的基于第一坐标和第二坐标,确定至少一个第一原子与至少一个第二原子之间的相互作用距离可以包括:
[0108]
步骤s501:获取至少一个第一原子的第一电荷信息和至少一个第二原子的第二电荷信息。
[0109]
步骤s502:基于第一坐标、第二坐标、第一电荷信息和第二电荷信息,确定至少一个第一原子与至少一个第二原子之间所存在的电荷作用距离。
[0110]
其中,在确定至少一个第一原子和至少一个第二原子之后,可以获取至少一个第一原子的第一电荷信息和与至少一个第二原子的第二电荷信息,具体的,在药物与靶点进行相互作用时,可以获取第一原子和第二原子的物理特征和化学特征,基于上述所获得物理特征和化学特征来确定第一原子的第一电荷信息和第二原子的第二电荷信息。当然的,
本领域技术人员也可以采用其他方式获取第一原子的第一电荷信息和第二原子的第二电荷信息,只要能够保证对第一原子的第一电荷信息和第二原子的第二电荷信息进行获取的准确可靠性即可。
[0111]
在获取到至少一个第一原子的第一电荷信息和至少一个第二原子的第二电荷信息之后,可以对第一坐标、第二坐标、第一电荷信息和第二电荷信息进行分析处理,以确定至少一个第一原子与至少一个第二原子之间所存在的电荷作用距离。在一些实例中,基于第一坐标、第二坐标、第一电荷信息和第二电荷信息,确定至少一个第一原子与至少一个第二原子之间所存在的电荷作用距离可以包括:基于第一坐标和第二坐标,确定至少一个第一原子与至少一个第二原子之间的欧式距离;基于欧式距离、第一电荷信息和第二电荷信息,确定至少一个第一原子与至少一个第二原子之间所存在的电荷作用距离。
[0112]
具体的,在获取到第一坐标和第二坐标之后,可以对第一坐标和第二坐标进行分析处理,以确定至少一个第一原子与至少一个第二原子之间的欧式距离,在获取到欧式距离之后,可以对欧式距离、第一电荷信息和第二电荷信息进行分析处理,以确定至少一个第一原子与至少一个第二原子之间所存在的电荷作用距离,具体的,电荷作用距离可以利用以下公式进行表示:
[0113][0114]
其中,m
e
(m
i
,m
j
)为电荷作用距离,q
i
用于标识第一原子的第一电荷信息,q
j
用于标识第二原子的第二电荷信息,r
i
用于标识第一原子的第一坐标,r
j
用于标识第二原子的第二坐标,c为设定参数。通过上述公式所获得的电荷作用距离与第一电荷信息呈正相关,电荷作用距离与第二电荷信息呈正相关,电荷作用距离与欧式距离呈负相关。
[0115]
需要注意的是,与药物相对应的至少一个第一原子的数量可以为5个,与靶点相对应的至少一个第二原子的数量可以为10个,因此,所获得的第一原子和第二原子之间的电荷作用距离的数量可以为50个。
[0116]
本实施例中,通过获取至少一个第一原子的第一电荷信息和至少一个第二原子的第二电荷信息,而后基于第一坐标、第二坐标、第一电荷信息和第二电荷信息来确定至少一个第一原子与至少一个第二原子之间所存在的电荷作用距离,这样不仅提供了又一种确定相互作用距离的实现方式,并且有效地保证了对相互作用距离进行确定的准确可靠性。
[0117]
图6为本发明实施例提供的基于拓扑结构图,确定药物与靶点之间的亲和力的流程示意图;在上述任意一个实施例的基础上,参考附图6所示,本实施例提供了一种确定药物与靶点之间的亲和力的实现方式,具体的,本实施例中的基于拓扑结构图,确定药物与靶点之间的亲和力可以包括:
[0118]
步骤s601:获取与拓扑结构图中单纯形的久性拓扑图的数量相关的设定参数。
[0119]
步骤s602:确定与设定参数相对应的神经网络模型。
[0120]
步骤s603:利用神经网络模型对拓扑结构图进行分析处理,生成与设定参数相对应的亲和力。
[0121]
其中,在拓扑结构图中包括单纯形的久性拓扑图时,单纯形的久性拓扑图的数量
与设定参数β相关,而不同的设定参数可以对应有不同的神经网络模型。因此,在获取到拓扑结构图之后,可以对拓扑结构图中所包括的单纯形的久性拓扑图的数量进行统计,而后基于单纯形的久性拓扑图的数量来获取设定参数,例如,设定参数β可以为0或者1。当然的,本领域技术人员可以根据具体的应用场景和应用需求来将设定参数β设置为其他参数,例如,设定参数β可以为2、3或者4等等。
[0122]
由于不同的设定参数可以对应有不同的神经网络模型,因此,在获取到设定参数之后,可以确定与设定参数相对应的神经网络模型,具体的,确定与设定参数相对应的神经网络模型可以包括:在设定参数为0时,确定神经网络模型为用于确定药物与靶点之间的一维亲和力的第一子网络模型;在设定参数为1时,确定神经网络模型为用于确定药物与靶点之间的二维亲和力的第二子网络模型。
[0123]
在确定神经网络模型之后,可以利用神经网络模型对拓扑结构图进行分析处理,从而可以生成与设定参数相对应的亲和力,具体的,利用神经网络模型对拓扑结构图进行分析处理,生成与设定参数相对应的亲和力可以包括:在神经网络模型为第一子网络模型时,利用第一子网络模型对拓扑结构图进行分析处理,确定与设定参数相对应的一维亲和力;在神经网络模型为第二子网络模型时,利用第二子网络模型对拓扑结构图进行分析处理,确定与设定参数相对应的二维亲和力。
[0124]
在另一些实例中,在基于不同的设定参数确定不同的神经网络模型时,神经网络模型需要进行分析处理的拓扑结构图可以存在不同的获取方式,具体的,在设定参数为0时,所获得的拓扑结构图可以为是通过计算处理所获得的用于标识复合物中原子空间特征的第一拓扑结构图;在设定参数为1时,所获得的拓扑结构图可以为是通过计算处理所获得的用于标识复合物中原子空间特征的第二拓扑结构图,第二拓扑结构图的数量为多个,且与多个不同观测参数相对应。
[0125]
在又一些实例中,计算用于标识复合物中原子空间特征的第二拓扑结构图可以包括:获取多个不同的观测参数,基于多个不同的观测参数确定多个第二拓扑结构图,例如:多个不同的观测参数可以包括η1、η2、η3和η4,四个观测参数可以对应有不同的观测角度,在获取到多个不同的观测参数之后,可以确定与上述观测参数相对应的第二拓扑结构图,可以理解的是,与不同观测参数相对应的第二拓扑结构图可以具有不同的表现形式。
[0126]
另一方面,在利用第一子网络模型对拓扑结构图进行分析处理时,由于拓扑结构图包括:由原子之间的欧式距离确定的第一拓扑结构图、由电荷作用距离确定的第二拓扑结构图;因此,在利用第一子网络模型对第一拓扑结构图进行分析处理,可以获取到一个一维亲和力;在利用第二子网络模型对第二拓扑结构图进行分析处理,可以获取到另一个一维亲和力;在利用第二子网络模型对第一拓扑结构图进行分析处理,可以获取到一个二维亲和力;在利用第二子网络模型对第二拓扑结构图进行分析处理,可以获取到另一个一维亲和力,此时,所获得的亲和力的数量为4个。
[0127]
本实施例中,通过获取与拓扑结构图中单纯形的久性拓扑图的数量相关的设定参数,而后确定与设定参数相对应的神经网络模型,并利用神经网络模型对拓扑结构图进行分析处理,从而稳定、有效地生成了与设定参数相对应的亲和力。
[0128]
图7为本发明实施例提供的基于至少一个亲和力,确定药物与靶点之间的目标亲和力的流程示意图;在上述实施例的基础上,参考附图7所示,由于所获得的亲和力的数量
可以为多个,在获取到多个亲和力之后,可以对多个亲和力进行分析处理,以确定目标亲和力,具体的,本实施例提供了一种确定药物与靶点之间的目标亲和力的实现方式,即基于至少一个亲和力,确定药物与靶点之间的目标亲和力可以包括:
[0129]
步骤s701:获取与至少一个亲和力中的每个亲和力相对应的权重系数。
[0130]
步骤s702:利用权重系数对所有的亲和力进行加权求和,获得药物与靶点之间的目标亲和力。
[0131]
其中,在获取到至少一个亲和力之后,可以确定与每个亲和力相对应的权重系数,而后基于权重系数对所有的亲和力进行加权求和,从而可以获得药物与靶点之间的目标亲和力。举例来说,至少一个亲和力包括y1、y2、y3和y4,而后可以获得与y1相对应的权重系数p1、与y2相对应的权重系数p2、与y相对应的权重系数p3、与y4相对应的权重系数p4;在获取到权重系数之后,可以利用以下公式确定目标亲和力y
c
=p1*y1 p2*y2 p3*y3 p4*y4,从而有效地保证了对目标亲和力进行确定的准确可靠性。
[0132]
图8为本发明实施例提供的获取与至少一个亲和力中的每个亲和力相对应的权重系数的流程示意图;在上述实施例的基础上,参考附图8所示,在获取与至少一个亲和力中的每个亲和力相对应的权重系数之后,本实施例中的方法还可以包括:
[0133]
步骤s801:获取与至少一个亲和力相对应的实际亲和力。
[0134]
步骤s802:利用实际亲和力和至少一个亲和力,对与至少一个亲和力中每个亲和力相对应的权重系数进行优化更新,获得优化后权重系数。
[0135]
其中,在获取到与每个亲和力相对应的权重系数之后,为了提高对目标亲和力进行预测的准确程度,可以获取到与至少一个亲和力相对应的实际亲和力,以基于实际亲和力和至少一个亲和力对权重系数进行优化处理,从而可以获得优化后权重系数。
[0136]
在一些实例中,利用实际亲和力和至少一个亲和力,对与至少一个亲和力中每个亲和力相对应的权重系数进行优化更新,获得优化后权重系数可以包括:获取至少两个亲和力与实际亲和力之间的相关系数;利用优化函数对相关系数进行最大化处理,获得与每个亲和力相对应的优化后权重系数。
[0137]
在获取到至少一个亲和力之后,可以获取至少两个亲和力与实际亲和力之间的相关系数,具体的,可以获取至少两个亲和力与实际亲和力之间的皮尔森相关系数,在获取到皮尔森相关系数之后,可以利用优化函数对相关系数进行最大化处理,从而可以获得与每个亲和力相对应的优化后权重系数。
[0138]
举例来说,至少一个亲和力可以包括y1、y2、y3和y4,实际亲和力为y
g
,而后获取与上述每个亲和力相对应的初始权重系数包括:a0、b0、c0、d0、p0、q0;可以获取与至少一个亲和力相对应的中间亲和力:y
c1
=a0y1 b0y2,y
c2
=c0y3 d0y4,y
c
=p0y
c1
q0y
c2
。在获取到中间亲和力之后,可以确定中间亲和力与实际亲和力之间的皮尔森相关系数,即cor(y
c1
,y
g
)、cor(y
c2
,y
g
)和cor(y
c
,y
g
)。
[0139]
在获取到皮尔森相关系数之后,可以利用优化方法opt=nelder
‑
mead对上述的皮尔森相关系数进行优化处理,从而可以获得优化后权重系数,具体的包括以下公式:
[0140]
a0、b0←
opt(max(cor(y
c1
,y
g
)),即通过上述公式可以对a0、b0进行优化处理,从而可以获得优化后权重系数的a1、b1;
[0141]
c0、d0←
opt(max(cor(y
c2
,y
g
)),即通过上述公式可以对c0、d0进行优化处理,从而
可以获得优化后权重系数的c1、d1;
[0142]
p0、q0←
opt(max(cor(y
c
,y
g
)),即通过上述公式可以对p0、q0进行优化处理,从而可以获得优化后权重系数的p1、q1。
[0143]
在获取到优化后的权重系数之后,可以将优化后的权重系数存储在预设区域中,通过访问预设区域即可获取到与每个亲和力相对应的优化后的权重系数,而后可以通过优化后的权重系数对至少一个亲和力进行分析处理,以确定药物与靶点之间的目标亲和力,这样有效地提高了对目标亲和力进行确定的准确可靠性。
[0144]
图9为本发明实施例提供的一种药物与靶点之间亲和力的预测方法的流程示意图;在上述实施例的基础上,参考附图9所示,在确定药物与靶点之间的目标亲和力之后,本实施例中的方法还可以包括:
[0145]
步骤s901:获取药物与靶点之间的实际亲和力。
[0146]
步骤s902:利用损失函数对实际亲和力和目标亲和力进行分析处理,确定深度学习模型的可训练参数。
[0147]
步骤s903:基于可训练参数对深度学习模型进行优化训练,获得优化后深度学习模型。
[0148]
其中,在获取到药物与靶点之间的目标亲和力之后,为了能够提高深度学习模型对药物与靶点之间的亲和力进行预测的准确率,可以获取药物与靶点之间的实际亲和力,在获取到实际亲和力和目标亲和力之后,可以利用损失函数对实际亲和力和目标亲和力进行分析处理,从而可以确定深度学习模型的可训练参数,具体的,可以通过以下公式来确定深度学习模型的可训练参数,loss=l(y
p
,y
g
),其中,y
p
为目标亲和力,y
g
为实际亲和力,l为损失函数,具体实现时,损失函数l可以为rmse函数,从而可以获得实际亲和力和目标亲和力之间的损失参数,基于上述损失参数可以确定深度学习模型的可训练参数。
[0149]
在获取到可训练参数之后,可以基于可训练参数对深度学习模型进行优化训练,从而可以获得优化后深度学习模型,该优化后深度学习模型用于对药物与靶点之间的亲和力进行预测操作,这样有效地提高了对亲和力进行预测的准确可靠性。
[0150]
在一些实例中,深度学习模型包括用于生成一维亲和力的第一模型和用于生成二维亲和力的第二模型;此时,本实施例中的基于可训练参数对深度学习模型进行优化处理,获得优化后深度学习模型可以包括:基于可训练参数对第一模型进行优化训练,获得第一优化模型;基于可训练参数对第二模型进行优化训练,获得第二优化模型;基于第一优化模型和第二优化模型,获得优化后深度学习模型。
[0151]
其中,在深度学习模型包括第一模型和第二模型时,为了保证对深度模型进行优化的质量和效果,可以对深度学习模型进行分层次优化操作,具体的,可以利用可训练参数对第一模型进行优化训练,从而可以获得第一优化模型,同时也可以利用可训练参数对第二模型进行优化训练,从而可以获得第二优化模型。
[0152]
需要注意的是,本实施例中步骤“基于可训练参数对第一模型进行优化训练,获得第一优化模型”与步骤“基于可训练参数对第二模型进行优化训练,获得第二优化模型”之间的执行顺序并不限于上述所描述的顺序,本领域技术人员可以根据具体的应用场景和应用需求进行设置,例如:步骤“基于可训练参数对第一模型进行优化训练,获得第一优化模型”与步骤“基于可训练参数对第二模型进行优化训练,获得第二优化模型”可以同时执行,
或者,步骤“基于可训练参数对第一模型进行优化训练,获得第一优化模型”可以在步骤“基于可训练参数对第二模型进行优化训练,获得第二优化模型”之后执行。
[0153]
在获取到第一优化模型和第二优化模型之后,可以对第一优化模型和第二优化模型进行分析处理,这样可以获得优化后深度学习模型,从而有效地保证了对深度学习模型进行优化的质量和效果。
[0154]
具体应用时,参考附图12所示,本应用实施例提供了一种药物与靶点之间亲和力的预测方法,该方法可以包括以下步骤:
[0155]
步骤1:获取药物和用于与药物相互作用的靶点;
[0156]
步骤2:确定药物与靶点相互作用后的复合物;
[0157]
步骤3:获取复合物中设定原子之间的相互作用距离。
[0158]
实现方式一:获取与药物相对应的至少一个第一原子和与靶点相对应的至少一个第二原子,计算至少一个第一原子的第一坐标和至少一个第二原子的第二坐标,基于第一坐标和第二坐标,确定至少一个第一原子与至少一个第二原子之间的欧式距离;将欧式距离确定为至少一个第一原子与至少一个第二原子之间的相互作用距离。
[0159]
实现方式二:基于第一坐标和第二坐标,确定至少一个第一原子与至少一个第二原子之间的欧式距离,获取至少一个第一原子的第一电荷信息和至少一个第二原子的第二电荷信息,基于欧式距离、第一电荷信息和第二电荷信息,确定至少一个第一原子与至少一个第二原子之间所存在的电荷作用距离,其中,所获得的电荷作用距离与第一电荷信息呈正相关,电荷作用距离与第二电荷信息呈正相关,电荷作用距离与欧式距离呈负相关。
[0160]
步骤4:基于相互作用距离来确定用于标识复合物中原子空间特性的两组拓扑结构图,每组拓扑结构图中包括多个拓扑结构图。
[0161]
在获取到相互作用距离之后,可以对相互作用距离进行分析处理,以确定拓扑结构图,其中,在相互作用距离为欧式距离时,可以基于欧式距离确定第一组拓扑结构图,第一组拓扑结构图中可以包括36个拓扑结构图;在相互作用距离为电荷作用距离时,可以基于电荷作用距离确定第二组拓扑结构图,第二组拓扑结构图中可以包括50个拓扑结构图。
[0162]
具体的,由于复合物中的设定原子可以包括以下至少之一:碳原子(c)、氮原子(n)、氧原子(o)、硫原子(s)、磷原子(p)、氟原子(f)和氯原子(cl)、溴原子(br)和碘原子(i),而不同的设定原子可以对应有不同的相互作用距离,因此与不同设定原子所对应的拓扑结构图也不同。下面以碳原子c为例,在获取到复合物之后,可以确定用于标识复合物中碳原子c的空间特性的拓扑结构图,在确定拓扑结构图的过程中,可以获取多个不同的观测参数,例如:多个不同的观测参数可以包括观测参数1、观测参数2、观测参数3和观测参数4,如图10所示,不同的观测参数可以对应哟不同的原子空间特性。在获取到多个不同的观测参数之后,可以确定与多个不同观测参数相对应的拓扑图,如图11所示,在不同的观测参数包括η1、η2、η3和η4时,可以确定与多个不同的观测参数相对应的拓扑结构图,如图11所示。
[0163]
步骤5:利用深度学习模型对每个拓扑结构图进行分析处理,确定每个拓扑结构图相对应的亲和力。
[0164]
其中,深度学习模型包括第一子网络模型和第二子网络模型,第一子网络模型可以对拓扑结构图进行分析处理,从而可以生成一维亲和力,具体的,由于拓扑结构图包括由欧式距离所确定的第一类拓扑结构图、由电荷作用距离所确定的第二类拓扑结构图,因此,
在第一子网络模型对拓扑结构图进行分析处理时,可以包括:第一子网络模型对第一类拓扑结构图进行分析处理,获得第一类一维亲和力y
1des
‑
idm
;第一子网络模型对第二类拓扑结构图进行分析处理,获得第二类一维亲和力y
1des
‑
iem
。
[0165]
第二子网络模型可以对拓扑结构图进行分析处理,从而可以生成二维亲和力,具体的,由于拓扑结构图包括由欧式距离所确定的第一类拓扑结构图、由电荷作用距离所确定的第二类拓扑结构图,在第二子网络模型对拓扑结构图进行分析处理时,可以包括:第二子网络模型对第一类拓扑结构图进行分析处理,获得第一类二维亲和力y
2des
‑
idm
;第二子网络模型对第二类拓扑结构图进行分析处理,获得第二类二维亲和力y
2des
‑
iem
。
[0166]
需要注意的是,在利用第二子网络模型对拓扑结构图进行分析处理时,拓扑结构图还可以包括与不同观测参数相对应的拓扑结构图,此时,第二子网络模型可以包括与多个不同观测参数相对应的网络模型,在获取到观测参数之后,则可以利用观测参数所对应的网络模型对相对应的拓扑结构图进行分析处理,从而可以有效地确定二维亲和力。
[0167]
步骤6:基于每个拓扑结构图相对应的亲和力,确定药物与靶点之间的目标亲和力。
[0168]
其中,获取与每个拓扑结构图相对应的权重系数,基于权重系数对所获得的亲和力进行加权求和处理,获得药物与靶点之间的目标亲和力,举例来说,多个亲和力包括y1、y2、y3和y4,在获取到上述多个亲和力之后,可以利用以下公式确定目标亲和力,y
c
=apy1 bpy2 cqy3 dqy4,上述的权重系数分别为ap、bp、cq和dq。
[0169]
步骤7:在获取到目标亲和力之后,获取药物和靶点之间的实际亲和力,利用损失函数对实际亲和力和目标亲和力进行分析处理,确定深度学习模型的可训练参数,基于可训练参数对深度学习模型进行优化训练,获得优化后深度学习模型。
[0170]
在获取到优化后深度学习模型之后,可以利用优化后深度学习模型对药物和靶点之间的亲和力进行预测,这样有效地保证了对亲和力进行预测的准确可靠性。具体的,在将本应用实施例所提供的预测方法应用于三个开源的数据集(包括:pdbbind
‑
v2007、pdbbind
‑
v2013和pdbbind
‑
v2016)时,相比于传统的其他预测方法,具有均方根误差更小、皮尔逊相关系数(pcc)更接近真实值的有点,具体数值可参考下述表格:
[0171][0172]
本应用实施例提供的药物与靶点之间亲和力的预测方法,通过获取药物和用于与药物相互作用的靶点,确定药物与靶点相互作用后的复合物,计算用于标识复合物中原子空间特性的拓扑结构图,而后基于拓扑结构图确定药物与靶点之间的亲和力,有效地实现
了可以基于复合物所对应的拓扑结构图来确定药物与靶点之间的亲和力,不仅保证了对亲和力进行确定的准确可靠性,并且也有利于促进药物技术领域的发展,进一步提高了该预测方法使用的准确可靠性。
[0173]
图13为本发明实施例提供的一种药物与靶点之间亲和力的预测装置的结构示意图;参考附图13所示,本实施例提供了一种药物与靶点之间亲和力的预测装置,该预测装置可以执行上述图2所示的药物与靶点之间亲和力的预测方法,具体的,该预测装置可以包括:第一获取模块11、第一确定模块12、第一计算模块13和第一处理模块14;
[0174]
第一获取模块11,用于获取药物和用于与药物相互作用的靶点;
[0175]
第一确定模块12,用于确定药物与靶点相互作用后的复合物;
[0176]
第一计算模块13,用于计算用于标识复合物中原子空间特性的拓扑结构图;
[0177]
第一处理模块14,用于基于拓扑结构图,确定药物与靶点之间的亲和力。
[0178]
在一些实例中,拓扑结构图包括以下至少之一:持久谱图、单纯形的久性拓扑图、单纯形的久性拓扑图的变化特征、持久超图;其中,持久谱图用于标识拓扑特征的持久性和变化程度,持久超图用于标识超图的拓扑特征的持久性和变化程度。
[0179]
在一些实例中,拓扑结构图呈嵌套式结构。
[0180]
在一些实例中,在第一计算模块13计算用于标识复合物中原子空间特性的拓扑结构图时,该第一计算模块13用于执行:获取复合物中设定原子之间的相互作用距离;基于相互作用距离,确定用于标识复合物中原子空间特性的拓扑结构图。
[0181]
在一些实例中,在第一计算模块13获取复合物中设定原子之间的相互作用距离时,该第一计算模块13用于执行:获取与药物相对应的至少一个第一原子和与靶点相对应的至少一个第二原子;计算至少一个第一原子的第一坐标和至少一个第二原子的第二坐标;基于第一坐标和第二坐标,确定至少一个第一原子与至少一个第二原子之间的相互作用距离。
[0182]
在一些实例中,在第一计算模块13基于第一坐标和第二坐标,确定至少一个第一原子与至少一个第二原子之间的相互作用距离时,该第一计算模块13用于执行:基于第一坐标和第二坐标,确定至少一个第一原子与至少一个第二原子之间的欧式距离;将欧式距离,确定为至少一个第一原子与至少一个第二原子之间的相互作用距离。
[0183]
在一些实例中,在第一计算模块13基于第一坐标和第二坐标,确定至少一个第一原子与至少一个第二原子之间的相互作用距离时,该第一计算模块13用于执行:获取至少一个第一原子的第一电荷信息和至少一个第二原子的第二电荷信息;基于第一坐标、第二坐标、第一电荷信息和第二电荷信息,确定至少一个第一原子与至少一个第二原子之间所存在的电荷作用距离。
[0184]
在一些实例中,在第一计算模块13基于第一坐标、第二坐标、第一电荷信息和第二电荷信息,确定至少一个第一原子与至少一个第二原子之间所存在的电荷作用距离时,该第一计算模块13用于执行:基于第一坐标和第二坐标,确定至少一个第一原子与至少一个第二原子之间的欧式距离;基于欧式距离、第一电荷信息和第二电荷信息,确定至少一个第一原子与至少一个第二原子之间所存在的电荷作用距离。
[0185]
在一些实例中,电荷作用距离与第一电荷信息呈正相关,电荷作用距离与第二电荷信息呈正相关,电荷作用距离与欧式距离呈负相关。
[0186]
在一些实例中,在第一计算模块13基于相互作用距离,确定用于标识复合物中原子空间特性的拓扑结构图时,该第一计算模块13用于执行:基于相互作用距离,获取用于标识复合物中原子空间特性的组合拉普拉斯矩阵;基于组合拉普拉斯矩阵,确定拓扑结构图。
[0187]
在一些实例中,在第一处理模块14基于拓扑结构图,确定药物与靶点之间的亲和力时,该第一处理模块14用于执行:获取与拓扑结构图中单纯形的久性拓扑图的数量相关的设定参数;确定与设定参数相对应的神经网络模型;利用神经网络模型对拓扑结构图进行分析处理,生成与设定参数相对应的亲和力。
[0188]
在一些实例中,在第一处理模块14确定与设定参数相对应的神经网络模型时,该第一处理模块14用于执行:在设定参数为0时,确定神经网络模型为用于确定药物与靶点之间的一维亲和力的第一子网络模型;在设定参数为1时,确定神经网络模型为用于确定药物与靶点之间的二维亲和力的第二子网络模型。
[0189]
在一些实例中,在第一处理模块14利用神经网络模型对拓扑结构图进行分析处理,生成与设定参数相对应的亲和力时,该第一处理模块14用于执行:在神经网络模型为第一子网络模型时,利用第一子网络模型对拓扑结构图进行分析处理,确定与设定参数相对应的一维亲和力;在神经网络模型为第二子网络模型时,利用第二子网络模型对拓扑结构图进行分析处理,确定与设定参数相对应的二维亲和力。
[0190]
在一些实例中,在第一计算模块13计算用于标识复合物中原子空间特性的拓扑结构图时,该第一计算模块13用于执行:在设定参数为0时,计算用于标识复合物中原子空间特征的第一拓扑结构图;在设定参数为1时,计算用于标识复合物中原子空间特征的第二拓扑结构图,第二拓扑结构图的数量为多个,且与多个不同观测参数相对应。
[0191]
在一些实例中,拓扑结构图的数量为至少一组;在第一处理模块14基于拓扑结构图,确定药物与靶点之间的亲和力时,该第一处理模块14用于执行:利用深度学习模型对每组拓扑结构图进行分析处理,获得与至少一组拓扑结构图相对应的至少一个亲和力,其中,深度学习模型被训练为用于基于拓扑结构图确定药物与靶点之间的亲和力;基于至少一个亲和力,确定药物与靶点之间的目标亲和力。
[0192]
在一些实例中,在第一处理模块14基于至少一个亲和力,确定药物与靶点之间的目标亲和力时,该第一处理模块14用于执行:获取与至少一个亲和力中的每个亲和力相对应的权重系数;利用权重系数对所有的亲和力进行加权求和,获得药物与靶点之间的目标亲和力。
[0193]
在一些实例中,在获取与至少一个亲和力中的每个亲和力相对应的权重系数之后,该第一处理模块14用于执行:获取与至少一个亲和力相对应的实际亲和力;利用实际亲和力和至少一个亲和力,对与至少一个亲和力中每个亲和力相对应的权重系数进行优化更新,获得优化后权重系数。
[0194]
在一些实例中,在第一处理模块14利用实际亲和力和至少一个亲和力,对与至少一个亲和力中每个亲和力相对应的权重系数进行优化更新,获得优化后权重系数时,该第一处理模块14用于执行:获取至少两个亲和力与实际亲和力之间的相关系数;利用优化函数对相关系数进行最大化处理,获得与每个亲和力相对应的优化后权重系数。
[0195]
在一些实例中,在确定药物与靶点之间的目标亲和力之后,本实施例中的第一获取模块11和第一处理模块14用于执行:
[0196]
第一获取模块11,用于获取药物与靶点之间的实际亲和力;
[0197]
第一处理模块14,用于利用损失函数对实际亲和力和目标亲和力进行分析处理,确定深度学习模型的可训练参数;基于可训练参数对深度学习模型进行优化训练,获得优化后深度学习模型。
[0198]
在一些实例中,深度学习模型包括用于生成一维亲和力的第一模型和用于生成二维亲和力的第二模型;在第一处理模块14基于可训练参数对深度学习模型进行优化处理,获得优化后深度学习模型时,该第一处理模块14用于执行:基于可训练参数对第一模型进行优化训练,获得第一优化模型;基于可训练参数对第二模型进行优化训练,获得第二优化模型;基于第一优化模型和第二优化模型,获得优化后深度学习模型。
[0199]
图13所示装置可以执行图1
‑
图11所示实施例的方法,本实施例未详细描述的部分,可参考对图1
‑
图11所示实施例的相关说明。该技术方案的执行过程和技术效果参见图1
‑
图11所示实施例中的描述,在此不再赘述。
[0200]
在一个可能的设计中,图13所示药物与靶点之间亲和力的预测装置的结构可实现为一电子设备,该电子设备可以是手机、平板电脑、服务器等各种设备。如图14所示,该电子设备可以包括:处理器21和存储器22。其中,存储器22用于存储相对应电子设备执行上述图1
‑
图11所示实施例中提供的药物与靶点之间亲和力的预测方法的程序,处理器21被配置为用于执行存储器22中存储的程序。
[0201]
程序包括一条或多条计算机指令,其中,一条或多条计算机指令被处理器21执行时能够实现如下步骤:
[0202]
获取药物和用于与药物相互作用的靶点;
[0203]
确定药物与靶点相互作用后的复合物;
[0204]
计算用于标识复合物中原子空间特性的拓扑结构图;
[0205]
基于拓扑结构图,确定药物与靶点之间的亲和力。
[0206]
进一步的,处理器21还用于执行前述图1
‑
图11所示实施例中的全部或部分步骤。
[0207]
其中,电子设备的结构中还可以包括通信接口23,用于电子设备与其他设备或通信网络通信。
[0208]
另外,本发明实施例提供了一种计算机存储介质,用于储存电子设备所用的计算机软件指令,其包含用于执行上述图1
‑
图11所示方法实施例中药物与靶点之间亲和力的预测方法所涉及的程序。
[0209]
图15为本发明实施例提供的另一种药物与靶点之间亲和力的预测方法的流程示意图;参考附图15所示,本实施例提供了另一种结构化信息的检测方法,该方法的执行主体可以为结构化信息的检测装置,可以理解的是,该结构化信息的检测装置可以实现为软件、或者软件和硬件的组合。具体的,该结构化信息的检测方法可以包括:
[0210]
步骤s1501:响应于调用亲和力预测服务的请求,确定所述亲和力预测服务对应的处理资源。
[0211]
步骤s1502:利用所述处理资源执行如下步骤:获取药物和用于与所述药物相互作用的靶点,确定所述药物与所述靶点相互作用后的复合物,计算用于标识所述复合物中原子空间特性的拓扑结构图,基于所述拓扑结构图,确定所述药物与靶点之间的亲和力。
[0212]
具体的,本发明提供的药物与靶点之间亲和力的预测方法可以在云端来执行,在
云端可以部署有若干计算节点,每个计算节点中都具有计算、存储等处理资源。在云端,可以组织由多个计算节点来提供某种服务,当然,一个计算节点也可以提供一种或多种服务。
[0213]
针对本发明提供的方案,云端可以提供有用于完成药物与靶点之间亲和力的预测方法的服务,称为药物与靶点之间亲和力的预测服务。当用户需要使用该药物与靶点之间亲和力的预测服务的时候,调用该药物与靶点之间亲和力的预测服务,以向云端触发调用该药物与靶点之间亲和力的预测服务的请求,在该请求中可以携带有对预测的药物和靶点信息。云端确定响应该请求的计算节点,利用该计算节点中的处理资源执行如下步骤:获取药物和用于与所述药物相互作用的靶点,确定所述药物与所述靶点相互作用后的复合物,计算用于标识所述复合物中原子空间特性的拓扑结构图,基于所述拓扑结构图,确定所述药物与靶点之间的亲和力。
[0214]
具体的,本实施例中的上述方法步骤的实现过程、实现原理和实现效果与上述图1
‑
图11所示实施例的方法步骤的实现过程、实现原理和实现效果相类似,本实施例未详细描述的部分,可参考对图1
‑
图11所示实施例的相关说明。
[0215]
图16为本发明实施例提供的另一种药物与靶点之间亲和力的预测装置的结构示意图;参考附图16所示,本实施例提供了另一种药物与靶点之间亲和力的预测装置,该预测装置可以执行上述图15所示的药物与靶点之间亲和力的预测方法,该检测装置可以包括:第二确定模块31和第二处理模块32;具体的,
[0216]
第二确定模块31,用于响应于调用亲和力预测服务的请求,确定所述亲和力预测服务对应的处理资源;
[0217]
第二处理模块32,用于利用所述处理资源执行如下步骤:获取药物和用于与所述药物相互作用的靶点,确定所述药物与所述靶点相互作用后的复合物,计算用于标识所述复合物中原子空间特性的拓扑结构图,基于所述拓扑结构图,确定所述药物与靶点之间的亲和力。
[0218]
图16所示装置可以执行图15所示实施例的方法,本实施例未详细描述的部分,可参考对图15所示实施例的相关说明。该技术方案的执行过程和技术效果参见图15所示实施例中的描述,在此不再赘述。
[0219]
在一个可能的设计中,图16所示药物与靶点之间亲和力的预测装置的结构可实现为一电子设备,该电子设备可以是手机、平板电脑、服务器等各种设备。如图17所示,该电子设备可以包括:第二处理器41和第二存储器42。其中,第二存储器42用于存储相对应电子设备执行上述图15所示实施例中提供的药物与靶点之间亲和力的预测方法的程序,第二处理器41被配置为用于执行第二存储器42中存储的程序。
[0220]
程序包括一条或多条计算机指令,其中,一条或多条计算机指令被第二处理器41执行时能够实现如下步骤:
[0221]
响应于调用亲和力预测服务的请求,确定所述亲和力预测服务对应的处理资源;
[0222]
利用所述处理资源执行如下步骤:获取药物和用于与所述药物相互作用的靶点,确定所述药物与所述靶点相互作用后的复合物,计算用于标识所述复合物中原子空间特性的拓扑结构图,基于所述拓扑结构图,确定所述药物与靶点之间的亲和力。
[0223]
进一步的,第二处理器41还用于执行前述图15所示实施例中的全部或部分步骤。
[0224]
其中,电子设备的结构中还可以包括第二通信接口43,用于电子设备与其他设备
或通信网络通信。
[0225]
另外,本发明实施例提供了一种计算机存储介质,用于储存电子设备所用的计算机软件指令,其包含用于执行上述图15所示方法实施例中药物与靶点之间亲和力的预测方法所涉及的程序。
[0226]
以上所描述的装置实施例仅仅是示意性的,其中所述作为分离部件说明的单元可以是或者也可以不是物理上分开的,作为单元显示的部件可以是或者也可以不是物理单元,即可以位于一个地方,或者也可以分布到多个网络单元上。可以根据实际的需要选择其中的部分或者全部模块来实现本实施例方案的目的。本领域普通技术人员在不付出创造性的劳动的情况下,即可以理解并实施。
[0227]
通过以上的实施方式的描述,本领域的技术人员可以清楚地了解到各实施方式可借助加必需的通用硬件平台的方式来实现,当然也可以通过硬件和软件结合的方式来实现。基于这样的理解,上述技术方案本质上或者说对现有技术做出贡献的部分可以以计算机产品的形式体现出来,本发明可采用在一个或多个其中包含有计算机可用程序代码的计算机可用存储介质(包括但不限于磁盘存储器、cd
‑
rom、光学存储器等)上实施的计算机程序产品的形式。
[0228]
本发明是参照根据本发明实施例的方法、设备(系统)、和计算机程序产品的流程图和/或方框图来描述的。应理解可由计算机程序指令实现流程图和/或方框图中的每一流程和/或方框、以及流程图和/或方框图中的流程和/或方框的结合。可提供这些计算机程序指令到通用计算机、专用计算机、嵌入式处理机或其他可编程设备的处理器以产生一个机器,使得通过计算机或其他可编程设备的处理器执行的指令产生用于实现在流程图一个流程或多个流程和/或方框图一个方框或多个方框中指定的功能的装置。
[0229]
这些计算机程序指令也可存储在能引导计算机或其他可编程设备以特定方式工作的计算机可读存储器中,使得存储在该计算机可读存储器中的指令产生包括指令装置的制造品,该指令装置实现在流程图一个流程或多个流程和/或方框图一个方框或多个方框中指定的功能。
[0230]
这些计算机程序指令也可装载到计算机或其他可编程设备上,使得在计算机或其他可编程设备上执行一系列操作步骤以产生计算机实现的处理,从而在计算机或其他可编程设备上执行的指令提供用于实现在流程图一个流程或多个流程和/或方框图一个方框或多个方框中指定的功能的步骤。
[0231]
在一个典型的配置中,计算设备包括一个或多个处理器(cpu)、输入/输出接口、网络接口和内存。
[0232]
内存可能包括计算机可读介质中的非永久性存储器,随机存取存储器(ram)和/或非易失性内存等形式,如只读存储器(rom)或闪存(flash ram)。内存是计算机可读介质的示例。
[0233]
计算机可读介质包括永久性和非永久性、可移动和非可移动媒体可以由任何方法或技术来实现信息存储。信息可以是计算机可读指令、数据结构、程序的模块或其他数据。计算机的存储介质的例子包括,但不限于相变内存(pram)、静态随机存取存储器(sram)、动态随机存取存储器(dram)、其他类型的随机存取存储器(ram)、只读存储器(rom)、电可擦除可编程只读存储器(eeprom)、快闪记忆体或其他内存技术、只读光盘只读存储器(cd
‑
rom)、
数字多功能光盘(dvd)或其他光学存储、磁盒式磁带,磁带磁磁盘存储或其他磁性存储设备或任何其他非传输介质,可用于存储可以被计算设备访问的信息。按照本文中的界定,计算机可读介质不包括暂存电脑可读媒体(transitory media),如调制的数据信号和载波。
[0234]
最后应说明的是:以上实施例仅用以说明本发明的技术方案,而非对其限制;尽管参照前述实施例对本发明进行了详细的说明,本领域的普通技术人员应当理解:其依然可以对前述各实施例所记载的技术方案进行修改,或者对其中部分技术特征进行等同替换;而这些修改或者替换,并不使相应技术方案的本质脱离本发明各实施例技术方案的精神和范围。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。