1.本发明属于植物基因工程技术领域,具体涉及一种黄麻黄脉病毒侵染性克隆及其构建方法。
背景技术:
2.黄麻黄脉病毒(corchorus yellow vein vietnam virus,coyvv)是单链、环状植物dna双生病毒,属于菜豆金色花叶病毒属,其基因组为双组份(即dna
‑
a和dna
‑
b)。coyvv于2006年首先在越南的黄麻上被发现,于2015在我国福建地区的黄麻上也鉴定到该病毒。虽然是旧世界发现的病毒,但coyvv具有典型的新世界双生病毒特征,即不编码av2蛋白。黄麻(corchorus capsularis),又称为绿麻、火麻等,是椴树科(tiliaceae)黄麻属(corchorus)重要的纤维作物,种植量和用途的广泛度仅次于棉花,我国长江以南广泛栽培。coyvv可侵染黄麻并造成叶片黄脉、植株矮化等症状,影响黄麻产量与品质,给我国黄麻产业带来潜在威胁。因此,研究coyvv的基因组结构、功能及其致病机制,对黄麻生产具有重要的意义。而病毒侵染性克隆的构建是研究病毒致病机制的首要选择。
技术实现要素:
3.本发明的目的在于,提供一种黄麻黄脉病毒侵染性克隆及其构建方法。本发明首次构建了黄麻黄脉病毒的侵染性克隆,为研究该病毒基因组的结构和功能及其致病机制奠定基础。
4.为实现上述目的,本发明采用如下技术方案:一种黄麻黄脉病毒侵染性克隆的构建方法,主要包括如下步骤:(1)提取黄麻叶片总dna,以此为模板,设计特异性引物coyvv
‑
dna
‑
a
‑
f1/coyvv
‑
dna
‑
a
‑
r1、coyvv
‑
dna
‑
a
‑
f2/coyvv
‑
dna
‑
a
‑
r2进行pcr扩增,获得长度分别为2.7 kb的片段a和0.5 kb的片段b。
5.(2)利用多片段无缝克隆技术,将凝胶纯化后的片段a和片段b与经bamh i和sma i对pbinplus载体进行双酶切的酶切产物pbinplus
‑
sb进行连接,连接产物热激法转化大肠杆菌感受态细胞后,提取质粒,利用bamh i和sma i双酶切验证重组质粒,筛选所得阳性克隆即为dna
‑
a侵染性克隆,标记为pbinplus
‑
coyvv
‑
1.2a。
6.(3)以黄麻叶片总dna为模板,利用φ29 dna聚合酶进行滚环扩增(rca),将扩增产物利用bamh i酶切得到2.7 kb的片段,连接于ptopo载体,即为ptopo
‑
dna
‑
b。
7.(4)利用bamh i和sma i对ptopo
‑
dna
‑
b进行双酶切,琼脂糖凝胶电泳后回收2.6 kb片段c,将片段c连接至经bamh i和sma i对pbinplus载体进行双酶切的酶切产物pbinplus
‑
sb,连接产物热激法转化大肠杆菌感受态细胞后,提取质粒,利用bamh i和sma i双酶切验证,筛选阳性克隆,标记为pbinplus
‑
dna
‑
b。
8.(5)利用bamh i对pbinplus
‑
dna
‑
b质粒进行单酶切,琼脂糖凝胶电泳回收后,进行去磷酸化处理。
9.(6)利用bamhi对ptopo
‑
dna
‑
b进行单酶切,琼脂糖凝胶电泳后回收2.7kb片段d,将片段d与步骤(5)去磷酸化的载体连接,连接产物热激法转化大肠杆菌感受态细胞后,提取质粒,利用引物b
‑
f570/b
‑
r570检测插入片段及其方向,筛选阳性克隆即为dna
‑
b侵染性克隆,标记为pbinplus
‑
coyvv
‑
2.0b。
10.(7)利用电击法将含有dna
‑
a和dna
‑
b的侵染性克隆pbinplus
‑
coyvv
‑
1.2a和pbinplus
‑
coyvv
‑
2.0b分别转入农杆菌gv3101感受态细胞;将含有病毒dna
‑
a和dna
‑
b侵染性克隆的农杆菌菌液,经由接种缓冲液处理后,接种刚长出2~3片真叶的黄麻叶片,使接种黄麻产生黄脉、花叶、斑驳、卷叶症状;并且利用pcr和southernblot检测病毒组分。
11.上述步骤(1)中所述特异性引物序列如下:coyvv
‑
dna
‑
a
‑
f1:5
’‑
caggtcgactctagaggatccaccgtgcagcagccccgc
‑3’
;coyvv
‑
dna
‑
a
‑
r1:5
’‑
ggctgctgcacggtaatattataggcgtgcagcagcg
‑3’
;coyvv
‑
dna
‑
a
‑
f2:5
’‑
aatattaccgtgcagcagccccgc
‑3’
;coyvv
‑
dna
‑
a
‑
r2:5
’‑
aattcgagctcggtacccgggtgaccttccctgtatgagca
‑3’
。
12.上述步骤(6)中所述引物序列如下:b
‑
f570:5
’‑
gacgaaccgtcacgtgcatccacg
‑3’
;b
‑
r570:5
’‑
tgtcgacagcaaagcactctgttg
‑3’
。
13.上述步骤(7)中pcr检测引物序列如下:a
‑
f534:5
’‑
aggatctatcggacctataggtcc
‑3’
;a
‑
r534:5
’‑
aggattagaggcatgagtacatgc
‑3’
;b
‑
f673:5
’‑
acgaatatcgtctgactcatgacc
‑3’
;b
‑
r673:5
’‑
tccagcatacttgtgctgagtctg
‑3’
。
14.一种上述方法构建所得的黄麻黄脉病毒侵染性克隆。
15.进一步的,方法构建所得的黄麻黄脉病毒侵染性克隆为pbinplus
‑
coyvv
‑
1.2a和pbinplus
‑
coyvv
‑
2.0b。
16.上述黄麻黄脉病毒侵染性克隆在黄麻黄脉病毒基因组的结构和功能及其致病机制研究中的应用。
17.与现有技术相比,本发明的有益效果:本发明首次构建了黄麻黄脉病毒的侵染性克隆pbinplus
‑
coyvv
‑
1.2a和pbinplus
‑
coyvv
‑
2.0b,该侵染性克隆能使接种黄麻产生黄脉、花叶、斑驳、卷叶等症状,这为研究黄麻黄脉病毒基因组的结构和功能及其致病机制奠定基础。
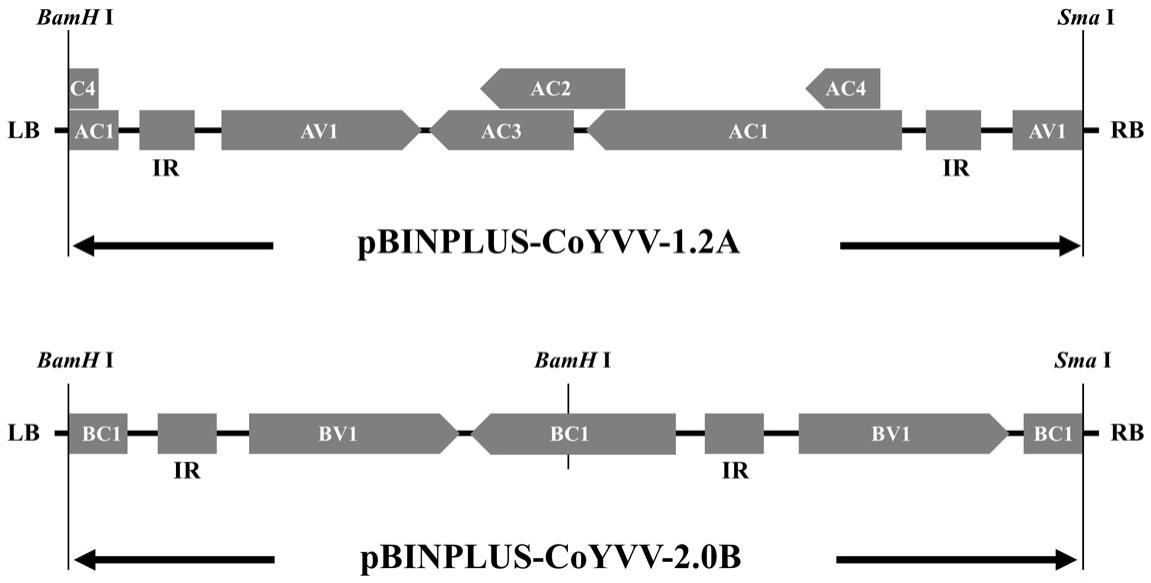
18.附图说明:图1coyvvdna
‑
a和dna
‑
b侵染性克隆构建示意图。
19.图2侵染性克隆载体酶切(dna
‑
a)及pcr(dna
‑
b)鉴定结果m代表分子量标准;泳道1代表dna
‑
a酶切检测;泳道2代表dna
‑
bpcr检测。
20.图3侵染性克隆诱导寄主植物产生症状ck代表健康黄麻;dna
‑
a dna
‑
b代表病毒侵染性克隆接种黄麻。
21.图4侵染性克隆接种黄麻的pcr检测m代表分子量标准;泳道1~3代表dna
‑
a;泳道4~6代表dna
‑
b;ck代表健康黄麻。
22.图5侵染性克隆接种黄麻后病毒dna
‑
a组分的southernblot检测。泳道1代表病
毒接种黄麻;ck代表健康黄麻。
具体实施方式
23.以下结合实施实例对本发明做进一步说明,需要指出的是,本实施实例仅用于解释本发明,而非对本发明的限制。
24.实施例1一种黄麻黄脉病毒侵染性克隆的构建方法,主要包括如下步骤:(1)植物总dna的提取(ctab法)取发病植物的新鲜叶片组织0.1 g,装入离心管中,加入钢珠,液氮中浸泡2 min,用提前预冷的离心管架固定住离心管,用力摇晃,使样品充分粉碎;加入1 ml 65℃预热的2% (w/v)ctab提取液(含2%(v/v) β
‑
巯基乙醇,1%(w/v) pvp
‑
360),65℃孵育30 min,每15 min温和颠倒数次;取出钢珠,12,000 rpm离心10 min,将上清液移至新1.5 ml离心管中,加入与上清液等体积的氯仿∶异戊醇(体积比为24∶1),涡旋震荡混匀30 s,直至水乳状为止;10,000 rpm离心10 min,转移上层水相至新离心管中;加入水相2/3体积的异丙醇,温和颠倒数次,有絮状物析出,10,000 rpm离心10 min,吸出上清,保留下面的沉淀;在沉淀中加入1 ml 75%乙醇,10,000 rpm离心5min,吸出上清,保留沉淀,室温下自然干燥10~15 min;加入30~50 μl elution buffer,涡旋振荡2 min直至充分混匀,即为植物总dna。
25.(2)dna
‑
a侵染性克隆的构建1)以植物总dna为模板,引物coyvv
‑
dna
‑
a
‑
f1(5
’‑
caggtcgactctagaggatccaccgtgcagcagccccgc
‑3’
)/coyvv
‑
dna
‑
a
‑
r1(5
’‑
ggctgctgcacggtaatattataggcgtgcagcagcg
‑3’
)、coyvv
‑
dna
‑
a
‑
f2(5
’‑
aatattaccgtgcagcagccccgc
‑3’
)/coyvv
‑
dna
‑
a
‑
r2(5
’‑
aattcgagctcggtacccgggtgaccttccctgtatgagca
‑3’
)分别对dna
‑
a进行扩增,获得长度分别为2.7 kb的片段a和0.5 kb的片段b,扩增体系为:总dna 1 μl,正向引物(10 μm) 1 μl,反向引物(10 μm)1 μl,dntp mix 0.5 μl,2
×
phanta max buffer 12.5 μl,phanta max super
‑
fidelity dna polymerase 1 μl,ddh2o 8 μl。反应程序为:95℃预变性3 min,95℃变性15 sec,52℃退火15 sec,72℃延伸1 min40 sec,35个循环,72℃终延伸10 min。琼脂糖凝胶回收。
26.2)使用fastdigest bamh i和fastdigest sma i对pbinplus载体进行双酶切,酶切反应体系为:质粒dna 1 μg,bamh i 1 μl,sma i 1 μl,10
×
fastdigest green buffer 2 μl,ddh2o 补至20 μl,37℃反应30 min。载体酶切产物标记为pbinplus
‑
sb,琼脂糖凝胶回收。
27.3)按照多片段无缝克隆试剂盒(multis one step cloning kit)的说明书,将凝胶纯化后的片段a和片段b以及酶切产物pbinplus
‑
sb,按一定比例进行混合。反应体系如下:5
×
ce multis buffer 4 μl,exnase
®ꢀ
multis 2 μl,片段a 54 ng,片段b 10 ng,酶切产物pbinplus
‑
sb 240 ng,ddh2o补水至20 μl,37℃反应30 min。连接产物热激法转化大肠杆菌dh5α感受态细胞后,提取质粒,利用fastdigest bamh i和fastdigest sma i双酶切验证得到12 kb载体片段和3.3 kb片段(图2),表明dna
‑
a侵染性克隆构建成功,标记为pbinplus
‑
coyvv
‑
1.2a。
28.(3)dna
‑
b侵染性克隆的构建
1)以植物总dna为模板,根据试剂盒说明书利用φ29 dna聚合酶(ge healthcare)进行滚环扩增(rca),将扩增产物利用fastdigest bamh i酶切得到2.7 kb的片段,连接于ptopo载体,即为ptopo
‑
dna
‑
b。
29.2)利用fastdigest bamh i和fastdigest sma i对ptopo
‑
dna
‑
b进行双酶切,酶切体系同上,琼脂糖凝胶电泳后回收较小的2.6 kb片段c,将此片段c连接至酶切产物pbinplus
‑
sb,连接体系如下:片段c 6 μl,pbinplus
‑
sb 2 μl,t4 ligase 1 μl,10
×
t4 ligase buffer 1 μl,总体积10 μl,4℃反应过夜,连接产物热激法转化大肠杆菌感受态细胞后,提取质粒,利用fastdigest bamh i和fastdigest sma i双酶切验证,筛选阳性克隆,标记为pbinplus
‑
dna
‑
b。
30.3)利用fastdigest bamh i对pbinplus
‑
dna
‑
b质粒进行单酶切,琼脂糖凝胶电泳回收后,进行去磷酸化处理,去磷酸化体系如下:单酶切载体片段17.5 μl,10
×
ciap缓冲液2 μl,ciap (takara)0.5 μl,总体积20 μl,37℃反应30 min,过柱纯化即可。
31.4)利用fastdigest bamh i对ptopo
‑
dna
‑
b进行单酶切,酶切体系如下:质粒dna 1 μg,bamh i 1 μl,10
×
fastdigest green buffer 2 μl,ddh2o补至20 μl,37℃反应30 min。琼脂糖凝胶电泳后回收较小的2.7 kb片段d。将片段d与上一步去磷酸化的pbinplus
‑
dna
‑
b载体连接,连接产物热激法转化大肠杆菌感受态细胞后,提取质粒,利用引物b
‑
f570(5
’‑
gacgaaccgtcacgtgcatccacg
‑3’
)/ b
‑
r570(5
’‑
tgtcgacagcaaagcactctgttg
‑3’
)检测插入片段及其方向,得到0.5 kb的片段(图2),表明dna
‑
b侵染性克隆构建成功,标记为pbinplus
‑
coyvv
‑
2.0b。
32.(4)侵染性克隆的转化利用电击法将以上获得的两个侵染性克隆pbinplus
‑
coyvv
‑
1.2a和pbinplus
‑
coyvv
‑
2.0b分别转入农杆菌gv3101感受态细胞。具体步骤如下:取1 μl侵染性克隆重组质粒加入50 μl冰上融化的农杆菌感受态中;电击杯于25℃烘箱中哄干10 min,冰上预冷5 min;将含质粒感受态加入电击杯,擦干杯体,电击;加600 μl无抗lb培养基至电击杯,混匀,吸出至1.5 ml离心管;28℃震荡培养1 h复苏菌体;吸取120 μl涂布含kan(50 μg/ml)和rif(50 μg/ml)的lb培养基平板;倒置于28℃培养36~48 h至菌落可见。
33.(5)农杆菌接种及检测1)将含有病毒dna
‑
a和dna
‑
b侵染性克隆的农杆菌菌液分别接种在5 ml含有kan(50 μg/ml)和rif(50 μg/ml)的lb液体培养基,220 rpm,28℃恒温振荡培养过夜至od
600
≈1.0。菌液5,000 rpm离心5 min,弃上清液,保留沉淀。加入一定体积的接种缓冲液悬浮沉淀,使其od
600
值至1.0,室温静置2~5 h。所述接种缓冲液成分为:10 mm mes、200 μm acetosyringone和10 mm mgcl2。接种时,采用医用去除针头的1 ml一次性注射器,吸取等比例混合的dna
‑
a和dna
‑
b侵染性克隆的农杆菌菌液,叶片浸润法接种刚长出2~3片真叶的黄麻叶片,接种的黄麻置于防虫温室中培养,同时设置未接种对照,定期观察其症状表现。接种30天后,接种黄麻产生黄脉、花叶、斑驳、卷叶症状(图3)。
34.2)接种60天后,采集黄麻叶片提取其总dna,利用引物a
‑
f534(5
’‑
aggatctatcggacctataggtcc
‑3’
)/a
‑
r534(5
’‑
aggattagaggcatgagtacatgc
‑3’
)和b
‑
f673(5
’‑
acgaatatcgtctgactcatgacc
‑3’
)b
‑
r673(5
’‑
tccagcatacttgtgctgagtctg
‑3’
)进行病毒两个组分的pcr检测。结果显示,接种黄麻均可检测到dna
‑
a和dna
‑
b的特异性条带,而健
康植物无任何条带(图4),说明所构建的侵染性克隆已成功侵染黄麻。
35.3)同时,接种60天后,采集黄麻叶片0.5 g,提取总基因组dna进行southern blot(roche dig high prime lab/detection kit)检测。结果显示,接种黄麻植株可成功检测到病毒dna
‑
a组分的积累,而健康黄麻植株不能检测任何特异性条带(图5),表明所构建的侵染性克隆已在黄麻体内大量复制。
36.以上所述仅为本发明的较佳实施例,凡依本发明申请专利范围所做的均等变化与修饰,皆应属本发明的涵盖范围。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。

