一种调控mil
‑
88材料催化活性的方法
技术领域
1.本发明涉及纳米酶制备领域,更具体地,涉及一种调控mil
‑
88材料催化活性的方法。
背景技术:
2.mof是由金属离子和有机配体共结晶形成的晶状多孔框架材料,近年来,金属有机框架材料作为新兴材料,因其孔隙率高、比表面积大、结构可调、合成可控等诸多优点使其成为最有前景的高孔隙度材料之一,广泛用于分析和传感诊断领域、废水处理、医疗、生物分子检测和食品安全等领域。现有的调控金属有机框架材料纳米酶活性的策略主要是粒径策略、形态学策略、表面调控策略、与其他纳米材料杂化策略、ph和温度调控策略、离子或分子调控策略、价态调控策略等。
3.随着纳米科技的快速发展,纳米酶价态调控策略一直是研究者关注的热点研究领域,但是,当前使用的价态调控策略往往有一个固有的缺陷,通过价态调控获得的mof是不稳定的,需要多次活化再循环,且无法实现价态的精确调控,限制了其进一步的应用。因此,提出一种精准调控价态从而获得高催化性能的纳米酶对于实际应用具有重要意义。但是,对于通过精准调控价态从而获得不同催化性能的纳米酶仍然是一项非常艰巨的任务。其中,外部能量的整合、结构调控、合成条件控制等方法,虽然能有效地调控价态,加速了催化反应的进程。但对于产生有用的光的特定设备的需求极大地阻碍了其实际实施,特殊调节剂和有机配体的应用成本太高而无法大规模生产和应用,且都无法实现价态的精确调节。因此,引入一种广泛应用、低成本、节能的精确控制价态的方法是十分必要的。
技术实现要素:
4.基于现有技术中存在的上述技术问题,本发明提供了一种调控mil
‑
88材料催化活性的方法,通过该方法,可精确调控mil
‑
88材料的催化活性。
5.为了实现上述目的,本发明的技术方案如下:
6.一种调控mil
‑
88材料催化活性的方法,该方法包括步骤:在制备mil
‑
88材料过程中,配体以对苯二甲酸为母体,在母体上引入不同电子性质的取代基;其中,当需要获得催化活性高的mil
‑
88材料,在所述母体引入供电子基团;当需要获得催化性能低的mil
‑
88材料,在所述母体引入吸电子基团。
7.在一些实施方式中,所述吸电子基团为
‑
no2、
‑
cn、
‑
f、
‑
cl、
‑
br、
‑
i、
‑
c≡c、
‑
och3、
‑
oh、
‑
c6h5、
‑
c=c中的一种;所述吸电子基团的吸电子效应越小,所述mil
‑
88材料的活性越低,所述吸电子基团的吸电子效应由大到小为:
‑
no2>
‑
cn>
‑
f>
‑
cl>
‑
br>
‑
i>
‑
c≡c>
‑
och3>
‑
c6h5>
‑
c=c。
8.在一些实施方式中,所述供电子基团为
‑
ch3ch2、
‑
ch3、
‑
nh2、
‑
oh中的一种;所述供电子基团的供电子效应越大,所述mil
‑
88材料的活性越高;所述供电子基团的供电子效应由大到小为:
‑
ch3ch2>
‑
ch3>
‑
nh2>
‑
oh。
9.在一些实施方式中,制备mil
‑
88材料包括以下步骤:
10.将可溶性铁盐和所述配体溶解于有机溶剂中,得到混合溶液;将所述混合溶液加热至100~120℃进行反应,得到mil
‑
88材料;其中,所述配体结构式为:
[0011][0012]
其中,r1为
‑
no2、
‑
cn、
‑
f、
‑
cl、
‑
br、
‑
i、
‑
c≡c、
‑
och3、
‑
c6h5、
‑
c=c、
‑
ch3ch2、
‑
ch3、
‑
nh2、
‑
oh中的一种。
[0013]
在一些实施方式中,制备mil
‑
88材料包括以下步骤:
[0014]
将可溶性铁盐和所述配体溶解于甲醇溶液中,得到混合溶液;将所述混合溶液加热至100℃下加热12h进行反应,反应结束后,冷却至室温,离心,洗涤,得到mil
‑
88粉末。
[0015]
在一些实施方式中,得到mil
‑
88粉末后,将所述粉末分散到甲醇中,搅拌,离心,再用甲醇进行洗涤,直至上清无色,最后在80℃的温度下干燥。
[0016]
在一些实施方式中,在所述母体上引入吸电子基团
‑
br时,所述mil
‑
88材料的价态比为0.27,催化活性为:19.87
×
103s
‑1。
[0017]
在一些实施方式中,在所述母体上引入吸电子基团
‑
no2时,所述mil
‑
88材料的价态比为0.53,催化活性为:39.54
×
103s
‑1。
[0018]
在一些实施方式中,在所述母体上引入供电子基团
‑
oh时,所述mil
‑
88材料的价态比为0.72,催化活性为70.87
×
103s
‑1。
[0019]
在一些实施方式中,在所述母体上引入供电子基团
‑
nh2时,所述mil
‑
88材料的价态比为1.12,催化活性为108.4
×
103s
‑1。
[0020]
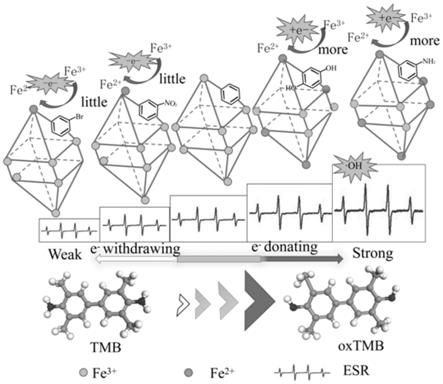
如图1所示,本发明通过在配体中引入供电子基团或吸电子基团进行mil
‑
88催化活性价态调控机制为:通过控制取代基的吸电子/供电子性质来调节铁离子的价态以促进mil
‑
88活性。供电子取代基的引入会发生电子传递促使更多的fe(ii)生成,增强了电荷转移能力并促进了羟基自由基的产生,从而增加了mil
‑
88(fe)的催化活性;吸电子取代基的引入尽管会使得fe
ii
/fe
iii
混合价的提高,但由于吸附能及空间位阻的影响降低了电荷转移能力并减少了羟基自由基的产生,从而削弱了mil
‑
88(fe)的催化活性。
[0021]
需要说明的是,本技术中,如无特别说明,所述的价态比,为fe
ii
/fe
iii
的比值。
[0022]
相较于现有技术,本发明的有益效果如下:
[0023]
(1)本发明拟选择铁元素作为金属中心元素,含有不同亲电性取代基的配体作为有机配体,制备不同形貌、不同价态mil
‑
88材料。研究亲电性取代基对金属中心元素价态的影响,元素价态对mil
‑
88材料催化活性的影响。
[0024]
(2)本发明不同于其他价态调控体系,本发明选择基于取代基的电子性质精准调控金属有机框架材料价态,开发了一种精准调控酶活方法,通过在配体中引入吸电子基团,以提高mil
‑
88材料的催化活性;通过在配体中引入供电子基团,可降低mil
‑
88材料的催化
活性。
[0025]
(3)本发明通过在配体中引入供电子基团以调控高催化活性mofs(价态比≥0.72,酶活性范围≥70.87*103s
‑1),使得基于纳米酶构建生物传感器的灵敏度提高。
[0026]
(4)本发明通过在配体中引入吸电子基团以调控催化活性相对较低的mof;另外,发明人发现催化活性相对较低的mof具有较高的稳定性,可以在广泛的ph和极性条件下使用,如强酸性食品,拓展了mil
‑
88材料在实际中应用。
附图说明
[0027]
图1为配体上的不同取代基对mof中铁离子价态的影响示意图;
[0028]
图2为不同取代基修饰的mof的fe(ii)/fe(iii)的比率及酶活的关系;
[0029]
图3为实例3构建的moflisa方法对afb1检测图;其中,a图为在标准曲线范围内afb1浓度变化的吸收光谱;b图为afb1的响应曲线;c图为moflisa方法对afb1具有特异性识别的分析结果;
[0030]
图4为实例6中所构建的moflisa方法对bpa检测中,bpa的响应曲线。
具体实施方式
[0031]
在下面的描述中阐述了很多具体细节以便于充分理解本发明。但是本发明能够以很多不同于在此描述的其它方式来实施,本领域技术人员可以在不违背本发明内涵的情况下做类似改进,因此本发明不受下面公开的具体实施的限制。
[0032]
除非另有定义,本文所使用的所有的技术和科学术语与属于本发明的技术领域的技术人员通常理解的含义相同。本文中在本发明的说明书中所使用的术语只是为了描述具体的实施例的目的,不是旨在于限制本发明。
[0033]
本发明旨在提供一种调控mil
‑
88材料催化活性的方法,该方法利用具有可预测和可设计功能的mof,选择具有过氧化物酶活性的fe
‑
mof(mil
‑
88)作为模型,通过在制备mil
‑
88材料过程中,在配体引入供电子取代基或吸电子取代基,通过调节活性位点的元素价态,引起mil
‑
88材料催化活性的变化,以实现对mil
‑
88材料催化活性的调控。具体方案如下:
[0034]
一种调控mil
‑
88材料催化活性的方法,该方法包括步骤:在制备mil
‑
88材料过程中,配体以对苯二甲酸为母体,在母体上引入不同电子性质的取代基;其中,当需要获得催化活性高的mil
‑
88材料,在所述母体引入供电子基团;当需要获得催化性能低的mil
‑
88材料,在所述母体引入吸电子基团。
[0035]
其中:所述吸电子基团为
‑
no2、
‑
cn、
‑
f、
‑
cl、
‑
br、
‑
i、
‑
c≡c、
‑
och3、
‑
c6h5、
‑
c=c中的一种;所述吸电子基团的吸电子效应越大,所述mil
‑
88材料的活性越低,所述吸电子基团的吸电子效应由大到小为:
‑
no2>
‑
cn>
‑
f>
‑
cl>
‑
br>
‑
i>
‑
c≡c>
‑
och3>
‑
c6h5>
‑
c=c。
[0036]
所述供电子基团为
‑
ch3ch2、
‑
ch3、
‑
nh2、
‑
oh中的一种;所述供电子基团的供电子效应越大,所述mil
‑
88材料的活性越高;所述供电子基团的供电子效应由大到小为:
‑
ch3ch2>
‑
ch3>
‑
nh2>
‑
oh。
[0037]
在一些实施方式中,制备mil
‑
88材料包括以下步骤:
[0038]
将可溶性铁盐和所述配体溶解于有机溶剂中,得到混合溶液;将所述混合溶液加
热至100~120℃进行反应,得到mil
‑
88材料;其中,所述配体结构式为:
[0039][0040]
其中,r1为
‑
no2、
‑
cn、
‑
f、
‑
cl、
‑
br、
‑
i、
‑
c≡c、
‑
och3、
‑
c6h5、
‑
c=c、
‑
ch3ch2、
‑
ch3、
‑
nh2、
‑
oh中的一种。
[0041]
进一步地,制备mil
‑
88材料包括以下步骤:
[0042]
将可溶性铁盐和所述配体溶解于甲醇溶液中,得到混合溶液;将所述混合溶液加热至100℃下加热12h进行反应,反应结束后,冷却至室温,离心,洗涤,得到mil
‑
88粉末;得到mil
‑
88粉末后,将所述粉末分散到甲醇中,搅拌,离心,再用甲醇进行洗涤,直至上清无色,最后在80℃的温度下干燥。
[0043]
为了充分理解本发明,下文将结合说明书附图和较佳的实施例对本发明做更全面和细致的描述,但本发明的保护范围并不限于以下具体实施例。
[0044]
除非另有定义,本发明中所使用的所有专业术语与本领域技术人员通常理解的含义相同。本发明中所使用的专业术语只是为了描述具体实施例,并不是在限制本发明的保护范围。
[0045]
除非另有特殊说明,本发明中应用到的各种原料、试剂、设备和仪器等均可在市场上购买得到或者经现有技术制备得到。
[0046]
实例1:基于nh2调控的mil
‑
88材料的制备
[0047]
mil
‑
88
‑
nh2的制备:fecl3·
6h2o(1mmol;270mg)和2
‑
氨基对苯二甲酸(1mmol;181mg)溶解于甲醇(15ml),得到混合溶液;将混合溶液转移到一个聚四氟乙烯衬里的高压灭菌器中,并在100℃的温度下加热24小时;然后冷却至室温,离心,丙酮洗净三次,再用水洗净三次,得到mil
‑
88
‑
nh2粉末。
[0048]
mil
‑
88
‑
nh2的活化:将mil
‑
88
‑
nh2粉末分散到20ml的甲醇中,搅拌16小时后,离心,用甲醇洗涤,直至上清无色;将得到的mof(mil
‑
88
‑
nh2)在80℃的空气中干燥,然后收集。采用xps测定,如图2所示,该mof的fe
ii
/fe
iii
比为1.12。
[0049]
酶反应动力学分析:检测mil
‑
88
‑
nh2的酶促动力学参数,具体方法为:
[0050]
(1)分别配制浓度为0.1mm、0.2mm,0.3mm、0.4mm、0.5mm、0.6mm、0.7mm、0.8mm、0.9mm、1.0mm的tmb和h2o2溶液;配制mil
‑
88
‑
nh2溶液的方法为:将mil
‑
88
‑
nh2粉末溶于水中,配制浓度1mm的mil
‑
88
‑
nh2溶液;
[0051]
(2)在试管中加入tmb溶液和h2o2溶液,然后加入mil
‑
88
‑
nh2溶液,在45℃恒温水浴锅中反应1min后,立即于450nm处测量吸光度值;当检测以tmb为底物的酶促动力学参数时,固定过氧化氢的浓度为0.5mm,改变tmb的浓度分别为0.1mm、0.2mm、0.3mm、0.4mm、0.5mm、0.6mm、0.7mm、0.8mm、0.9mm、1.0mm;当测量以h2o2为底物的动力学参数时,固定tmb的浓度为1mm,改变过h2o2的浓度分别为0.1mm、0.2mm、0.3mm、0.4mm、0.5mm、0.6mm、0.7mm、0.8mm、0.9mm、1.0mm;
[0052]
(3)空白对照组的处理:不加入mil
‑
88
‑
nh2溶液,其余条件相同,实验同时进行。
[0053]
利用michaelis
‑
menten方程的非线性回归拟合ν与底物浓度的关系图,根据michaelis
‑
menten方程ν=v
max
*[s]/(k
m
*[s])计算表观动力学参数,其中v
max
表示最大反应速度,[s]为底物浓度,k
m
为michaelis常数,参数k
m
和v
max
由双倒数图(或lineweavere
‑
burk图)获得,催化常数k
cat
取自k
cat
=v
max
/[e],其中[e]是基于混合价mil
‑
88
‑
nh2的摩尔浓度,该浓度是通过tem图像计算得出的,假设每个纳米酶都是半径为100纳米和宽度为1纳米的圆盘。
[0054]
测定结果为:k
cat
=108.4
×
103s
‑1。
[0055]
实例2:基于oh调控的mil
‑
88材料的制备
[0056]
mil
‑
88
‑
(oh)2的制备:fe(clo4)3·
nh2o(1mmol;354mg),2,5
‑
二羟基对苯二甲酸(1mmol;198mg)溶于5ml dmf中,得到混合溶液;将混合溶液放入衬有聚四氟乙烯的高压灭菌器中,在80℃的温度下加热12小时;反应完全后,冷却至室温;待冷却至室温后,离心,丙酮洗净三次,再用水洗净三次,得到mil
‑
88
‑
(oh)2粉末。
[0057]
mil
‑
88
‑
(oh)2的活化:将mil
‑
88
‑
(oh)2粉末分散到20ml的甲醇中,搅拌16次;离心后用甲醇洗涤,直至上清无色;将mof在80℃的空气中干燥,然后收集。采用xps测定,如图2所示,该mof的fe
ii
/fe
iii
比为0.72。
[0058]
酶反应动力学分析:采用实施例1的方法测量mil
‑
88
‑
(oh)2的酶促动力学参数。测定结果为:k
cat
=70.87
×
103s
‑1。
[0059]
实例3:mil
‑
88
‑
nh2作为类过氧化物酶构建生物传感器的应用
[0060]
功能化mof(mil
‑
88
‑
nh2)的制备:我们使用共价偶联方法将二抗(ab2)固定在mof表面,具体为:将mil
‑
88
‑
nh2溶液(1mg/ml)与1ml浓度为10.5mm的edc和浓度为8.6mm的nhs混合,以8000r/min离心10分钟以去除未反应的nhs和edc;最后,在37℃磁力搅拌下,向mil
‑
88
‑
nh2溶液中滴加1.3ml的ab2(2mg/ml),然后搅拌8h,将获得的功能mof分散在pbs缓冲溶液中,并在4℃下保存直到使用。
[0061]
mof联免疫吸附测定(moflisa)方法的构建:
[0062]
s1、配制afb1系列浓度标准溶液;
[0063]
s2、取酶标板,于每孔中加入100μl的afb1(黄曲霉毒素b1)抗原,并在4℃下孵育过夜;用洗涤缓冲液洗涤五次后,用含1%bsa(牛血清蛋白)的pbs溶液进行封闭;
[0064]
s3、在每孔中加入50μl抗体和50μl不同浓度的afb1溶液,在37℃下孵育1h;重复洗涤五次后,将功能性mof加入每个孔中,在37℃下再次孵育1h,用洗涤缓冲液再洗涤7次后,在每孔加入naac
‑
hac缓冲液、h2o2溶液和tmb溶液,孵育1h;孵育后,加入h2so4终止液,记录紫外图谱及450nm处的吸光度,制作标准曲线,如图3中a图和b图所示。
[0065]
本方法检测afb1的标准曲线如图3中b图所示,为y=
‑
0.3766x 0.52565(x=log(c))(r2=0.9917),检测范围为0.01
‑
20ng/ml,检测限为0.009ng/ml,说明该mil
‑
88
‑
nh2作为类过氧化物酶构建生物传感器具有高灵敏度。
[0066]
特异性实验分析:配制afb1类似物标准液:将afb1类似物如黄曲霉毒素b2(afb2)、黄曲霉毒素g1(afg1)、黄曲霉毒素g2(afg2)、玉米赤霉烯酮毒素(zen)、赭曲霉毒素a(ota)用甲醇稀释至其浓度为10ng/ml。我们只需在上述afb1的检测方法中将添加afb1标准溶液这一步骤替代为加入配制好的afb1类似物标准液,之后检测加入afb1和不同afb1类似物后对应
的检测体系的紫外强度。分析结果如图3中c图所示。
[0067]
实际样品测定:为了验证moflisa方法在实际样品中的可行性,使用了从当地超市购买的花生奶和豆浆进行测试。首先,在空白谷物饮料中加入不同浓度的afb1(0.5、5、10ng/ml),然后在摇床上轻轻搅拌下用甲醇
‑
水(30ml,8:2v/v)萃取5分钟,然后以5000r/min的速度离心10min去除脂肪层,离心分离的上清液用0.22μm注射器过滤器过滤以去除其他杂质,所得水相可用于进一步分析。
[0068]
表1显示moflisa方法的平均回收率为91.8%,而常规elisa为78.6%。moflisa方法的相对标准偏差(rsd,相对于平均回收率100%)(6.20%)低于常规elisa的rsd(11.65%),这表明已开发的moflisa方法具有更高的准确性和重复性。
[0069]
表1 moflisa方法和常规elisa试剂盒在雀巢花生奶样品和蚕丝豆浆样品(n=10)中用于afb1测定的应用
[0070][0071][0072]
实例4:基于no2调控的mil
‑
88材料的制备
[0073]
mil
‑
88
‑
no2的制备:fecl3·
6h2o(1mmol;270mg)和硝基对苯二甲酸(1mmol;211mg)溶于蒸馏水(5ml)得到混合溶液;将混合溶液转移到一个聚四氟乙烯衬里的高压灭菌器中,并在100℃的温度下加热12小时,反应完全后,冷却至室温;待冷却至室温后,离心,丙酮洗净,再用水洗净,得到mil
‑
88
‑
no2粉末。
[0074]
mil
‑
88
‑
no2的活化:将mil
‑
88
‑
no2粉末分散到10ml的乙醇中,搅拌16小时;离心后用乙醇洗涤,直至上清无色,最后,mof在80℃的空气中干燥,然后收集。采用xps测定,如图2所示,该mof的fe
ii
/fe
iii
比为0.53。
[0075]
酶反应动力学分析:采用实施例1的方法检测mil
‑
88
‑
no2的酶促动力学参数,测定结果为:k
cat
=39.54
×
103s
‑1。
[0076]
实例5:基于br调控的mil
‑
88材料的制备
[0077]
mil
‑
88
‑
br的制备:fecl3·
6h2o(1mmol;270mg)和2
‑
溴对苯二甲酸(1mmol;245mg)溶于dmf(5ml),得到混合溶液;将混合溶液转移到一个聚四氟乙烯衬里的高压灭菌器中,并在373k的温度下加热12小时;反应完全后,冷却至室温;待冷却至室温后,离心,丙酮洗净三次,再用水洗净三次,得到mil
‑
88
‑
br粉末。
[0078]
mil
‑
88
‑
br的活化:将mil
‑
88
‑
br粉末分散到20ml dmf中,搅拌16小时,离心后用dmf洗涤,直至上清无色;最后,mof在353k的空气中干燥,然后收集。采用xps测定,如图2所
示,该mof的fe
ii
/fe
iii
比为0.27。
[0079]
酶反应动力学分析:采用实施例1的方法检测mil
‑
88
‑
no2的酶促动力学参数,测定结果为:k
cat
=19.87
×
103s
‑1。
[0080]
实例6:mil
‑
88
‑
br作为类过氧化物酶构建生物传感器的应用
[0081]
功能化mof(mil
‑
88
‑
br)的制备:我们使用共价偶联方法将二抗(ab2)固定在mof表面,具体包括以下步骤:
[0082]
(a)配制mil
‑
88
‑
br溶液:取100mg的mil
‑
88
‑
br粉末溶于100ml水中,制成1mg/ml的mil
‑
88
‑
br溶液;
[0083]
(b)将1ml的步骤(a)的mil
‑
88
‑
br溶液与1ml浓度为10.5mm edc和1ml浓度为8.6mm的nhs混合,然后以8000r/min离心10分钟,留上清,以去除未反应的nhs和edc,得到上清液;
[0084]
(c)在37℃磁力搅拌下,向步骤(b)的上清液中滴加1.3ml的ab2(2mg/ml),然后搅拌8h,获得功能化mof;将获得的功能化mof分散在pbs缓冲溶液中,并在4℃下保存直到使用。
[0085]
moflisa方法的构建:
[0086]
s1、配制bpa系列浓度标准溶液;
[0087]
s2、取酶标板,于每孔中加入100μl的bpa(双酚a)抗原,并在4℃下孵育过夜,用洗涤缓冲液洗涤五次后,用含1%bsa的pbs溶液进行封闭;
[0088]
s3、在每孔中加入50μl抗体和50μl不同浓度的bpa标准溶液,并在37℃下孵育1h,重复洗涤步骤五次后,将功能化mof加入每个孔中,并在37℃下再次孵育1h,用洗涤缓冲液再洗涤7次后,在每孔加入naac
‑
hac缓冲液、h2o2溶液和tmb溶液;孵育1h后,加入h2so4终止液,记录紫外图谱及450nm处的吸光度,制作标准曲线。
[0089]
本方法检测bpa的标准曲线如图4所示,为y=
‑
8954x 0.0076(x=log(c))(r2=0.9921),检测范围为0.1
‑
20ng/ml,检测限为0.09ng/ml,说明该mil
‑
88
‑
br作为类过氧化物酶构建生物传感器具有较低的灵敏度和较窄的应用范围。
[0090]
特异性实验分析:配制bpa类似物标准液:将bpa类似物如4
‑
肉桂苯醛(4
‑
cp),4
‑
辛基苯酚(4
‑
op)和双酚a缩水甘油醚(bdage)用甲醇稀释至其浓度为500pg ml
‑1,bpa的浓度为100pg ml
‑1。在上述bpa的检测方法中将添加bpa标准溶液这一步骤替代为加入配制好的bpa类似物标准液,之后检测加入bpa和不同bpa类似物后对应的检测体系的紫外强度。
[0091]
实际样品测定:将bpa(5mg)溶于5ml甲醇中,制成1mg/ml bpa储备液,之后,用超纯水进一步稀释上述bpa的浓度,制成浓度为50pg/ml、100pg/ml和200pg/ml的工作溶液进行测试。为了测试橘子罐头中的bpa水平,从当地的零售商店购买了两个品牌的食品:橘子罐头(即罐头食品,来自林家铺子,http://www.leasunfood.com/)。从橙子罐头样品中收集食物样品的液体部分。每次取300μl橘子罐头,至少进行三个测试。接下来,将食物样品掺入已知水平的bpa并进行回收率测试。将50pg/ml、100pg/ml和200pg/ml的bpa加到橘子罐头中,之后检测加入不同浓度bpa标准溶液的检测体系的紫外强度。
[0092]
实际样品测定:将bpa(5mg)溶于5ml甲醇中,制成1mg/ml bpa储备液,之后,用超纯水进一步稀释上述bpa的浓度,制成浓度为50pg/ml、100pg/ml和200pg/ml的工作溶液进行测试。为了测试畅轻酸奶中的bpa水平,从当地的零售商店购买了伊利品牌的酸奶。从酸奶样品中收集食物样品的液体部分。每次取300μl酸奶,至少进行三个测试。接下来,将食物样
品掺入已知水平的bpa并进行回收率测试。将50pg/ml、100pg/ml和200pg/ml的bpa加到酸奶中,之后检测加入不同浓度bpa标准溶液的检测体系的紫外强度。
[0093]
表2显示moflisa方法检测橘子罐头的平均回收率为79.04%,而moflisa方法检测畅轻酸奶的平均回收率为92.48。这表明已开发的moflisa方法可用于强酸性食品,具有较高的准确性和重复性。
[0094]
表2 实际样品测定结果
[0095][0096]
以上所述实施例的各技术特征可以进行任意的组合,为使描述简洁,未对上述实施例中的各个技术特征所有可能的组合都进行描述,然而,只要这些技术特征的组合不存在矛盾,都应当认为是本说明书记载的范围。
[0097]
以上所述实施例仅表达了本发明的几种实施方式,其描述较为具体和详细,但并不能因此而理解为对发明专利范围的限制。应当指出的是,对于本领域的普通技术人员来说,在不脱离本发明构思的前提下,还可以做出若干变形和改进,这些都属于本发明的保护范围。因此,本发明专利的保护范围应以所附权利要求为准。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。

