1.本发明涉及用于合成n
‑
(4
‑
(4
‑
氨基
‑2‑
(2
‑
甲氧基乙基)
‑
1h
‑
咪唑并[4,5
‑
c]喹啉
‑1‑
基)丁基)
‑
n
‑
(四氢
‑
2h
‑
吡喃
‑4‑
基)乙酰胺的方法,所述化合物为可用作toll样受体激动剂,特别是作为tlr7的激动剂的咪唑并喹啉衍生物,其促进特定细胞因子的诱导。此外,本发明还提供了可用于合成n
‑
(4
‑
(4
‑
氨基
‑2‑
(2
‑
甲氧基乙基)
‑
1h
‑
咪唑并[4,5
‑
c]喹啉
‑1‑
基)丁基)
‑
n
‑
(四氢
‑
2h
‑
吡喃
‑4‑
基)乙酰胺的中间体。
背景技术:
[0002]
本公开内容一般性地涉及用于制备toll样受体7激动剂及其合成中间体的有机合成方法学领域。toll样受体(toll
‑
like receptor,tlr)目前包含13种具有不同特异性的受体的基因家族,其中11种在人中发现,其是细胞病原体模式识别系统的一部分,该系统已进化为防御多种感染(细菌、病毒、真菌)。tlr的激活导致细胞因子响应,例如释放干扰素以及激活特定的免疫细胞。组织中选定的tlr的功能表达差异很大。部分受体位于细胞表面,例如在例如上皮细胞上的tlr4(受大肠杆菌脂多糖lps刺激),或者位于特定免疫细胞的内体膜上的tlr3、tlr7、tlr8和tlr9。后者都被核酸激活,但是识别不同类型的核酸。例如,tlr9被包含cpg子序列的单链dna激活,tlr7和tlr8被单链rna激活,而tlr3被双链rna激活。
[0003]
已经鉴定出一些小分子(some small
‑
molecule,smol)tlr7或tlr8激动剂。这些激动剂可分为嘌呤样分子,例如7
‑
硫代
‑8‑
氧鸟嘌呤(7
‑
thia
‑8‑
oxoguanosine,tog,艾沙托立宾(isatoribine))或基于咪唑并喹啉的化合物(如咪喹莫特(imiquimod))。咪喹莫特是迄今为止唯一批准的确定tlr7激动剂,以5%乳膏销售其产生约80%的浅表基底细胞癌(全球最常见的癌症)的5年清除率。咪喹莫特激活tlr7。tlr7的功能性表达似乎仅限于特定的免疫细胞,即在人中,已知类浆细胞样树突状细胞、b细胞以及可能的嗜酸性粒细胞被tlr7激动剂激活。
[0004]
几年来,全世界一直在努力开发利用tlr7、tlr8或tlr9激动剂诱导的强大免疫激活来治疗癌症。然而,癌症免疫治疗经历了很长的失败历史。但是,近年来,有关癌症免疫监视和免疫细胞亚群功能的知识得到了极大的改善。tlr7、tlr8或tlr9激动剂正处于临床开发,以用于癌症的单一治疗或组合治疗或作为疫苗佐剂。
[0005]
用于癌症免疫治疗的tlr激动剂方法不同于使用例如细胞因子、干扰素或单价疫苗接种的早期工作。tlr激动剂介导的免疫激活是通过特定的免疫细胞(主要是树突状细胞和b细胞,其次是其他细胞)的多效性的,其产生先天性和适应性免疫应答。而且,不是诱导仅一种干扰素,而是许多不同的同工型一起,并且不仅是i型(α、β),而且还(间接地)诱导ii型(γ)干扰素。至少对于局部施用,提供了出色的概念证明。这表明抗原是由肿瘤释放的,并且免疫治疗原则上可用于癌症适应证,甚至在单一治疗方法中也是如此。但是,对于全身施用途径,tlr7激动剂的临床概念证明尚待定。对于晚期癌症和全身施用(特别是皮下或静脉内施用途径),显然这样的tlr激动剂与其他治疗性干预措施组合可提供更强
的,即协同的效力。
[0006]
在癌症的早期阶段,情况可能会有所不同。肿瘤转移是患者中肿瘤发展的严重方面,主要是因为在已经发生转移时已太晚检测到肿瘤。已建立的肿瘤治疗主要包括具有较窄治疗窗口的细胞毒性药物。因此,对于仍可能抑制转移扩散的早期肿瘤阶段的治疗,对具有良好耐受性和安全性的新治疗的需求很高。
[0007]
免疫系统的激活,并且特别是toll样受体(tlr)信号转导的激活提供了新的有前途的方法。在鼠renca肺转移模型中测试了tlr9激动剂cpg
‑
odn(如h2006或h1826)和tlr7激动剂(如鸟苷衍生物艾沙托立宾或咪喹莫德衍生物)。所有经测试的分子以良好的耐受性几乎完全抑制了肺转移的出现。这为用于抑制癌症转移的这样的分子的临床开发提供了令人信服的理由,并指出了这样的药物的全身施用的可能性。然而,如果与核酸类型tlr9激动剂相比,smol类型tlr7激动剂具有建立的和成本有效的合成的优势,并且非常适合局部施用以及全身施用。
[0008]
us
‑
b
‑
6,573,273描述了含有脲、硫脲、酰脲、磺酰脲或氨基甲酸酯官能团的咪唑并喹啉和四氢咪唑并喹啉化合物。据说所述化合物可用作免疫调节剂。
[0009]
us
‑
b
‑
6,677,349描述了在1
‑
位含有磺酰胺官能团的咪唑并喹啉和四氢咪唑并喹啉化合物。据说所述化合物可用作免疫调节剂。
[0010]
us
‑
a
‑
2003/0144283和wo
‑
a
‑
00/76505描述了在1
‑
位含有酰胺官能团的咪唑并喹啉和四氢咪唑并喹啉化合物。据说所述化合物可用作免疫调节剂。
[0011]
wo
‑
a
‑
2005/051324描述了在1
‑
位被肟或特殊的n
‑
氧化物官能团取代的咪唑并喹啉、吡啶和萘啶环体系。据说所述化合物可用作免疫调节剂。
[0012]
wo
‑
a
‑
2009/118296描述了咪唑并喹啉化合物。所述化合物被描述为toll样受体激动剂/tlr7激活剂。
[0013]
n
‑
(4
‑
(4
‑
氨基
‑2‑
(2
‑
甲氧基乙基)
‑
1h
‑
咪唑并[4,5
‑
c]喹啉
‑1‑
基)丁基)
‑
n
‑
(四氢
‑
2h
‑
吡喃
‑4‑
基)乙酰胺及其制备方法公开于pct/ep2018/073470中,其通过引用并入于此。
[0014]
本公开内容提供了用于制备n
‑
(4
‑
(4
‑
氨基
‑2‑
(2
‑
甲氧基乙基)
‑
1h
‑
咪唑并[4,5
‑
c]喹啉
‑1‑
基)丁基)
‑
n
‑
(四氢
‑
2h
‑
吡喃
‑4‑
基)乙酰胺或其溶剂合物或盐的新方法,其使用新中间体。
技术实现要素:
[0015]
本发明的第一方面提供了用于合成n
‑
(4
‑
(4
‑
氨基
‑2‑
(2
‑
甲氧基乙基)
‑
1h
‑
咪唑并[4,5
‑
c]喹啉
‑1‑
基)丁基)
‑
n
‑
(四氢
‑
2h
‑
吡喃
‑4‑
基)乙酰胺或其溶剂合物或盐的方法,如下文进一步描述的。所述化合物是tlr7的激动剂或激活剂,并且可作为细胞因子诱导物质。所述化合物具有以下化学式(i):
[0016][0017]
第一方面的方法包括以下步骤:
[0018]
a)提供式(3)化合物或其溶剂合物或盐,其中r1和r2各自独立地选自
‑
h和胺基保护基团,并且r1和r2中的至少一个是胺基保护基团:
[0019][0020]
b)使式(3)化合物或其溶剂合物或盐与一种或更多种试剂反应以除去r1和r2位的胺基保护基团,以得到式(4)化合物或其溶剂合物或盐:
[0021][0022]
c)使式(4)化合物或其溶剂合物或盐与用于引入(i)四氢吡喃基和(ii)乙酰基的一种或更多种试剂反应,以得到式(5)化合物或其溶剂合物或盐:
[0023]
以及
[0024]
d)使式(5)化合物或其溶剂合物或盐进行氧化胺化反应以得到式(i)化合物或其溶剂合物或盐。第一方面的方法的优选实施方案在下文、在权利要求书中以及在图1a至1h、2a至2d、3a至3g、4a至4h、5a至5e和6a至6d中的任一个中详细说明。
[0025]
在第二方面中,本发明提供了化合物及其溶剂合物或盐,所述化合物选自以下:
[0026][0027]
这些化合物是可用于第一方面的方法的中间体。
[0028]
在第三方面中,本发明提供了第二方面的化合物用于合成式(i)化合物的用途。
附图说明
[0029]
图1a至1h示出了本发明的方法的一些优选实施方案。在图1a至1h中提及的取代基(例如,r1、r2、r
10
)和缩写(例如,thp、ptsa)具有与说明书中指定的相同的含义。
[0030]
图2a至2d示出了本发明的方法的步骤a)的一些优选实施方案。
[0031]
图3a至3g示出了本发明的方法的步骤b)的一些优选实施方案。
[0032]
图4a至4h示出了本发明的方法的步骤c)的一些优选实施方案。
[0033]
图5a至5e示出了本发明的方法的步骤d)的一些优选实施方案。
[0034]
图6a至6d示出了可在本发明的方法的步骤d)之后进行的步骤(沉淀和/或结晶)的一些优选实施方案。
[0035]
图7示出了通过本发明的方法获得的富马酸加成盐形式的式(4)化合物的谱(1h nmr,d2o,400mhz)。
[0036]
图8示出了通过本发明的方法获得的富马酸加成盐形式的式(4)化合物(命名为sc 103439)的色谱(hplc)。
[0037]
图9示出了通过本发明的方法获得的式(5)化合物的谱(1h nmr,cdcl3,500mhz)。
[0038]
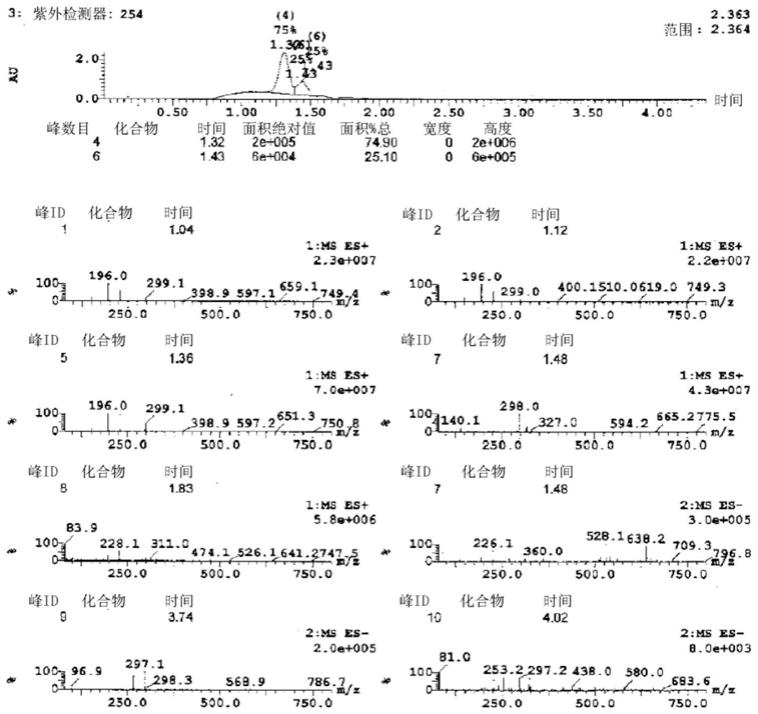
图10示出了通过本发明的方法获得的式(5)化合物(命名为sc 102714)的色谱(hplc)。
[0039]
图11示出了在本发明的方法的步骤d)之后立即获得的粗制品形式的式(i)化合物(即,在步骤d)之后式(i)化合物未经过沉淀和/或结晶步骤)的谱(1h nmr,cdcl3,500mhz)。
[0040]
图12示出了在本发明的方法的步骤d)之后立即获得的粗制品形式的式(i)化合物(即,在步骤d)之后式(i)化合物未经过沉淀和/或结晶步骤)的色谱(hplc)。在图12中式(i)化合物被命名为sc100745。
[0041]
图13示出了在本发明的方法的最终结晶步骤之后获得的式(i)化合物的谱(1h nmr,吡啶
‑
d5 500mhz)。
[0042]
图14示出了在本发明的方法的最终结晶步骤之后获得的式(i)化合物的质谱(esi)。
[0043]
图15示出了在本发明的方法的最终结晶步骤之后获得的式(i)化合物的谱(hplc)。在图15中式(i)化合物被命名为sc100745。
[0044]
图16是使用色谱纯化步骤用于合成n
‑
(4
‑
(4
‑
氨基
‑2‑
(2
‑
甲氧基乙基)
‑
1h
‑
咪唑并[4,5
‑
c]喹啉
‑1‑
基)丁基)
‑
n
‑
(四氢
‑
2h
‑
吡喃
‑4‑
基)乙酰胺的比较方法b的概述。
[0045]
图17示出了通过使用比较方法b获得的式(4)化合物的色谱(hplc)。
[0046]
图18示出了通过使用比较方法b获得的式(4)化合物的thp加合物的色谱(hplc)。
[0047]
图19示出了通过使用比较方法b获得的式(5)化合物的色谱(hplc)。
[0048]
图20示出了通过使用比较方法b获得的式(i)化合物的色谱(hplc)。在图20中式(i)化合物被命名为sc100745。
具体实施方式
[0049]
尽管下文更详细地描述了本发明,但是应理解,本发明不限于本文中所描述的具体方法、方案和试剂,因为这些可变化。还应理解,本文中使用的术语仅用于描述具体实施方案的目的,并不旨在限制本发明的范围,本发明的范围将仅由所附权利要求书限定。除非另有限定,否则本文中使用的所有技术术语和科学术语具有与本领域普通技术人员通常理解的相同的含义。
[0050]
在下文中,将更详细地描述本发明的要素。这些要素以具体实施方案列出,然而,应理解,这些要素可以以任何方式和任何数量组合以形成另外的实施方案。多方面描述的实例和优选实施方案不应被解释为将本发明仅限于明确描述的实施方案。该描述应被理解为支持和涵盖将明确描述的实施方案与任何数量的所公开和/或优选的要素组合的实施方案。此外,除非上下文另外指明,否则本技术中的所有描述的要素的任何排列和组合应被视为通过本技术的说明书公开。例如,如果在本发明的方法的一个优选实施方案中在步骤d)之后进行溶剂交换,并且在本发明的方法的另一个优选实施方案中在步骤d)之后进行结晶步骤,那么在本发明的方法的另一个优选实施方案中,在步骤d)之后进行溶剂交换并且在步骤d)之后进行结晶步骤。
[0051]
优选地,本文中使用的术语如"a multilingual glossary of biotechnological terms:(iupac recommendations)",h.g.w.leuenberger,b.nagel,and h.eds.,helvetica chimica acta,ch
‑
4010basel,switzerland,(1995)中所述进行限定。
[0052]
除非另外指明,否则本发明的实践将使用常规化学方法,这些方法在本领域的文献(参见,例如,organikum,deutscher verlag der wissenschaften,berlin 1990;streitwieser/heathcook,"organische chemie",vch,1990;beyer/walter,"lehrbuch der organischen chemie",s.hirzel verlag stuttgart,1988;carey/sundberg,"organische chemie",vch,1995;march,"advanced organic chemistry",john wiley&sons,1985;chemie lexikon,falbe/regitz(hrsg.),georg thieme verlag stuttgart,new york,1989)中进行了解释。
[0053]
在整个本说明书和随附的权利要求书中,除非上下文另有要求,否则词语“包含/包括”以及变化形式将被理解为暗含包括所述的成员、整数或步骤或者成员、整数或步骤的组,但不排除任何其他成员、整数或步骤或者成员、整数或步骤的组。术语“基本上由......组成”意指排除任何实质意义的其他成员、整数或步骤。术语“包含/包括”包括术语“基本上由......组成”,“基本上由......组成”又包括术语“由......组成”。因此,在本技术中每
次出现时,术语“包含/包括”可用术语“基本上由......组成”或“由......组成”代替。同样,在本技术中每次出现时,术语“基本上由......组成”可用术语“由......组成”代替。
[0054]
除非在本文中另外指明或与上下文明显矛盾,否则在描述本发明的上下文中(尤其是在权利要求的上下文中)使用的没有数量词修饰的名词及类似的引用表示一个/种或更多个/种。本文中值的范围的记载仅旨在用作单独引用落入该范围的每个单独的值的速记方法。除非本文中另外指明,否则将每个单独的值并入本说明书中,如同其在本文中被单独记载一样。除非本文中另外指明或者与上下文明显矛盾,否则本文中描述的所有方法均可以以任何合适的顺序进行。除非另外要求,否则本文中提供的任何和所有实例或示例性语言(例如,“例如”)的使用仅旨在更好地举例说明本发明,并且不对本发明的范围构成限制。说明书中的任何语言均不应被解释为表示对本发明的实践必要的任何未要求保护的要素。
[0055]
本文中使用的“和/或”被认为是两个指定特征或组分具有或不具有二者中的另一者中的每一种的特定公开内容。例如“x和/或y”被认为是(i)x、(ii)y以及(iii)x和y中每一种的特定公开内容,就如同各自单独地在本文中列出一样。
[0056]
在本发明的上下文中,术语“约”和“大约”可互换使用,并且表示普通技术人员所理解的精确度区间以仍确保所讨论的特征的技术效果。该术语通常指示与指示数值的偏差为
±
5%、
±
4%、
±
3%、
±
2%、
±
1%、
±
0.9%、
±
0.8%、
±
0.7%、
±
0.6%、
±
0.5%、
±
0.4%、
±
0.3%、
±
0.2%、
±
0.1%、
±
0.05%,以及例如
±
0.01%。如普通技术人员将理解的,对于给定技术效果的数值的特定的这样的偏差将取决于技术效果的性质。例如,天然的或生物的技术效果的这样的偏差通常可比人造的或改造的技术效果的偏差更大。
[0057]
本文中对值的范围的记载仅旨在用作单独引用落入该范围的每个单独的值的速记方法。除非本文中另外指明,否则将每个单独的值并入本说明书中,如同其在本文中被单独记载一样。
[0058]
除非另外要求,否则本文中提供的任何和所有实例或示例性语言(例如,“例如”)的使用仅旨在更好地举例说明本发明,并且不对本发明的范围构成限制。说明书中的任何语言均不应被解释为表示对本发明的实践必要的任何未要求保护的要素。
[0059]
术语“烷基”是指饱和直链或支链烃的单价基团。优选地,烷基包含1至12个(例如1至10个)碳原子,即1、2、3、4、5、6、7、8、9、10、11或12个碳原子(例如1、2、3、4、5、6、7、8、9或10个碳原子),更优选1至8个碳原子,例如1至6或1至4个碳原子。示例性烷基包括甲基、乙基、丙基、异丙基(也称为2
‑
丙基或1
‑
甲基乙基)、丁基、异丁基、叔丁基、正戊基、异戊基、仲戊基、新戊基、1,2
‑
二甲基
‑
丙基、异戊基、正己基、异己基、仲己基、正庚基、异庚基、正辛基、2
‑
乙基
‑
己基、正壬基、正癸基、正十一烷基、正十二烷基等。“经取代的烷基”意指烷基的一个或更多个(例如1至与烷基结合的氢原子的最大数目,例如1、2、3、4、5、6、7、8、9或多至10个,例如1至5、1至4、或1至3、或者1或2个)氢原子被除氢之外的取代基替代(当替代多于一个氢原子时,取代基可以是相同或不同的)。优选地,除氢之外的取代基是如本文中所指定的第1级取代基、第2级取代基或第3级取代基,例如卤素、
‑
oh、
‑
nh2、
‑
nhch3、
‑
n(ch3)2、
‑
cn、
‑
och3、
‑
ocf3或任选取代的芳基。经取代的烷基的一些实例包括三氟甲基、2
‑
羟乙基、2
‑
氨基乙基、2
‑
(二甲氨基)乙基、芳基烷基(也称为“芳烷基”,例如苄基)或杂芳基烷基(也称为“杂芳烷基”)。
[0060]
术语“烯基”是指具有至少一个碳
‑
碳双键的不饱和直链或支链烃的单价基团。一般而言,烯基中碳
‑
碳双键的最大数目可等于通过将烯基中碳原子的数目除以2而计算得到的整数,并且如果烯基中碳原子的数目是奇数,则将除法结果舍入到下一整数。例如,对于具有9个碳原子的烯基,碳
‑
碳双键的最大数目为4。优选地,烯基具有1至6个(例如1至4个),即1、2、3、4、5或6个碳
‑
碳双键。优选地,烯基包含2至12个(例如2至10个)碳原子,即2、3、4、5、6、7、8、9、10、11或12个碳原子(例如2、3、4、5、6、7、8、9或10个碳原子),更优选2至8个碳原子,例如2至6个碳原子或2至4个碳原子。因此,在一个优选实施方案中,烯基包含2至12个(例如2至10个)碳原子和1、2、3、4、5或6个(例如,1、2、3、4或5个)碳
‑
碳双键,更优选地,其包含2至8个碳原子和1、2、3或4个碳
‑
碳双键,例如2至6个碳原子和1、2或3个碳
‑
碳双键或者2至4个碳原子和1或2个碳
‑
碳双键。碳
‑
碳双键可呈顺式(z)或反式(e)构型。一些示例性烯基包括乙烯基、1
‑
丙烯基、2
‑
丙烯基(即烯丙基)、1
‑
丁烯基、2
‑
丁烯基、3
‑
丁烯基、1
‑
戊烯基、2
‑
戊烯基、3
‑
戊烯基、4
‑
戊烯基、1
‑
己烯基、2
‑
己烯基、3
‑
己烯基、4
‑
己烯基、5
‑
己烯基、1
‑
庚烯基、2
‑
庚烯基、3
‑
庚烯基、4
‑
庚烯基、5
‑
庚烯基、6
‑
庚烯基、1
‑
辛烯基、2
‑
辛烯基、3
‑
辛烯基、4
‑
辛烯基、5
‑
辛烯基、6
‑
辛烯基、7
‑
辛烯基、1
‑
壬烯基、2
‑
壬烯基、3
‑
壬烯基、4
‑
壬烯基、5
‑
壬烯基、6
‑
壬烯基、7
‑
壬烯基、8
‑
壬烯基、1
‑
癸烯基、2
‑
癸烯基、3
‑
癸烯基、4
‑
癸烯基、5
‑
癸烯基、6
‑
癸烯基、7
‑
癸烯基、8
‑
癸烯基、9
‑
癸烯基、1
‑
十一碳烯基、2
‑
十一碳烯基、3
‑
十一碳烯基、4
‑
十一碳烯基、5
‑
十一碳烯基、6
‑
十一碳烯基、7
‑
十一碳烯基、8
‑
十一碳烯基、9
‑
十一碳烯基、10
‑
十一碳烯基、1
‑
十二碳烯基、2
‑
十二碳烯基、3
‑
十二碳烯基、4
‑
十二碳烯基、5
‑
十二碳烯基、6
‑
十二碳烯基、7
‑
十二碳烯基、8
‑
十二碳烯基、9
‑
十二碳烯基、10
‑
十二碳烯基、11
‑
十二碳烯基等。如果烯基与氮原子连接,则双键不能在氮原子的α位。“经取代的烯基”意指烯基的一个或更多个(例如1至与烯基结合的氢原子的最大数目,例如1、2、3、4、5、6、7、8、9或多至10个,例如1至5、1至4、或1至3、或1或2个)氢原子被除氢之外的取代基替代(当替代多于一个氢原子时,取代基可以是相同或不同的)。优选地,除氢之外的取代基是如本文中所指定的第1级取代基、第2级取代基或第3级取代基,例如卤素或任选取代的芳基。经取代的烯基的一个实例是苯乙烯基(即2
‑
苯基乙烯基)。
[0061]
术语“炔基”是指具有至少一个碳
‑
碳三键的不饱和直链或支链烃的单价基团。一般而言,炔基中碳
‑
碳三键的最大数目可等于通过将炔基中碳原子的数目除以2而计算得到的整数,并且如果炔基中碳原子的数目是奇数,则将除法结果舍入到下一整数。例如,对于具有9个碳原子的炔基,碳
‑
碳三键的最大数目为4。优选地,炔基具有1至6个(例如1至4个),即1、2、3、4、5或6个,更优选1或2个碳
‑
碳三键。优选地,炔基包含2至12个(例如2至10个)碳原子(例如1、2、3、4、5、6、7、8、9或10个碳原子),即,2、3、4、5、6、7、8、9、10、11或12个碳原子,更优选2至8个碳原子,例如2至6个碳原子或2至4个碳原子。因此,在一个优选实施方案中,炔基包含2至12个(例如2至10个)碳原子和1、2、3、4、5或6个(例如1、2、3、4或5个(优选1、2或3个))碳
‑
碳三键,更优选地,其包含2至8个碳原子和1、2、3或4个(优选1或2个)碳
‑
碳三键,例如2至6个碳原子和1、2或3个碳
‑
碳三键或者2至4个碳原子和1或2个碳
‑
碳三键。一些示例性炔基包括乙炔基、1
‑
丙炔基、2
‑
丙炔基、1
‑
丁炔基、2
‑
丁炔基、3
‑
丁炔基、1
‑
戊炔基、2
‑
戊炔基、3
‑
戊炔基、4
‑
戊炔基、1
‑
己炔基、2
‑
己炔基、3
‑
己炔基、4
‑
己炔基、5
‑
己炔基、1
‑
庚炔基、2
‑
庚炔基、3
‑
庚炔基、4
‑
庚炔基、5
‑
庚炔基、6
‑
庚炔基、1
‑
辛炔基、2
‑
辛炔基、3
‑
辛炔基、4
‑
辛炔基、5
‑
辛炔基、6
‑
辛炔基、7
‑
辛炔基、1
‑
壬炔基、2
‑
壬炔基、3
‑
壬炔基、4
‑
壬炔基、5
‑
壬炔基、6
‑
壬炔基、7
‑
壬炔基、8
‑
壬炔基、1
‑
癸炔基、2
‑
癸炔基、3
‑
癸炔基、4
‑
癸炔基、5
‑
癸炔基、6
‑
癸炔基、7
‑
癸炔基、8
‑
癸炔基、9
‑
癸炔基等。如果炔基与氮原子连接,则三键不能在氮原子的α位。“经取代的炔基”意指炔基的一个或更多个(例如1至与炔基结合的氢原子的最大数目,例如1、2、3、4、5、6、7、8、9或多至10个,例如1至5、1至4、或1至3、或者1或2个)氢原子被除氢之外的取代基替代(当替代多于一个氢原子时,取代基可以是相同或不同的)。优选地,除氢之外的取代基是如本文中所指定的第1级取代基、第2级取代基或第3级取代基,例如卤素或任选取代的芳基。
[0062]
术语“芳基”或“芳香环”是指芳香环状烃的单价基团。优选地,芳基包含可布置在一个环(例如苯基)或者两个或更多个稠环(例如萘基)中的3至14个(例如,5、6、7、8、9或10个,例如5、6或10个)碳原子。示例性芳基包括环丙烯基(cyclopropanylium)、环戊二烯基、苯基、茚基、萘基、基、芴基、蒽基和菲基。优选地,“芳基”是指包含6个碳原子的单环或包含10个碳原子的芳香族双环体系。一些优选的实例是苯基和萘基。芳基不包括富勒烯。“经取代的芳基”意指芳基的一个或更多个(例如1至与芳基结合的氢原子的最大数目,例如1、2、3、4、5、6、7、8、9或多至10个,例如1至5、1至4、或1至3、或者1或2个)氢原子被除氢之外的取代基替代(当替代多于一个氢原子时,取代基可以是相同或不同的)。优选地,除氢之外的取代基是如本文中所指定的第1级取代基、第2级取代基或第3级取代基,例如卤素、
‑
oh、
‑
nh2、
‑
nhch3、
‑
n(ch3)2、
‑
cn、
‑
och3、
‑
ocf3、硝基、烷基(例如c1‑6烷基)、烯基(例如c2‑6烯基)和炔基(例如,c2‑6炔基)。经取代的芳基的一些实例包括联苯基、2
‑
氟苯基、2
‑
氯
‑6‑
甲基苯基、苯胺基、3
‑
硝基苯基、4
‑
羟基苯基、甲氧基苯基(即2
‑
、3
‑
或4
‑
甲氧基苯基)和4
‑
乙氧基苯基。
[0063]
术语“杂芳基”或“杂芳香环”意指其中芳基中的一个或更多个碳原子被杂原子(例如o、s或n)替代的如上所限定的芳基。优选地,杂芳基是指其中1、2或3个碳原子被相同或不同的o、n或s杂原子替代的五或六元芳香族单环。或者,其意指其中1、2、3、4或5个碳原子被相同或不同的o、n或s杂原子替代的芳香族双环或三环体系。优选地,在杂芳基的每个环中,o原子的最大数目为1,s原子的最大数目为1,并且o和s原子的最大总数目为2。例如,3至14元杂芳基包括单环杂芳基(例如,5或6元)、双环杂芳基(例如,9或10元),和三环杂芳基(例如,13或14元)。示例性杂芳基包括呋喃基、噻吩基、唑基、异唑基、二唑基、吡咯基、咪唑基、吡唑基、三唑基、四唑基、噻唑基、异噻唑基、噻二唑基、吡啶基(pyridyl,也被称为吡啶基(pyridinyl))、嘧啶基、吡嗪基、三嗪基、苯并呋喃基、吲哚基、异吲哚基、苯并噻吩基、1h
‑
吲唑基、苯并咪唑基、苯并唑基、吲哚并嗪基(indoxazinyl)、苯并异唑基、苯并噻唑基、苯并异噻唑基、苯并三唑基、喹啉基、异喹啉基、苯并二嗪基、喹喔啉基、喹唑啉基、苯并三嗪基、哒嗪基、吩嗪基、噻唑并吡啶基、吡咯并噻唑基、吩噻嗪基、异苯并呋喃基、色烯基、吨基、吩噻基、吡咯嗪基(pyrrolizinyl)、吲嗪基、吲唑基、嘌呤基、喹嗪基(quinolizinyl)、酞嗪基、萘啶基、噌啉基、蝶啶基、咔唑基、菲啶基、吖啶基、啶基(perimidinyl)、菲咯啉基(phenanthrolinyl)、吩嗪基、唑并吡啶基、异唑并吡啶基、吡咯并唑基和吡咯并吡咯基。示例性5或6元杂芳基包括呋喃基、噻吩基、唑基、异唑基、二唑基、吡咯基、咪唑基、吡唑基、三唑基、噻唑基、异噻唑基、噻二唑基、吡啶基、嘧
啶基、吡嗪基、三嗪基和哒嗪基。“经取代的杂芳基”意指杂芳基的一个或更多个(例如1至与杂芳基结合的氢原子的最大数目,例如1、2、3、4、5、6、7、8、9或多至10个,例如1至5、1至4、或1至3、或者1或2个)氢原子被除氢之外的取代基替代(当替代多于一个氢原子时,取代基可以是相同或不同的)。优选地,除氢之外的取代基是如本文中所指定的第1级取代基、第2级取代基或第3级取代基,例如卤素、
‑
oh、
‑
nh2、
‑
nhch3、
‑
n(ch3)2、
‑
cn、
‑
och3、
‑
ocf3、烷基(例如c1‑6烷基)、烯基(例如c2‑6烯基)和炔基(例如c2‑6炔基)。经取代的杂芳基的一些实例包括2,4
‑
二甲基吡啶
‑3‑
基、2
‑
甲基
‑4‑
溴吡啶
‑3‑
基、3
‑
甲基
‑2‑
吡啶
‑2‑
基、3
‑
氯
‑5‑
甲基吡啶
‑4‑
基、4
‑
氯
‑2‑
甲基吡啶
‑3‑
基、3,5
‑
二甲基吡啶
‑4‑
基、2
‑
甲基吡啶
‑3‑
基、2
‑
氯
‑4‑
甲基
‑
噻吩
‑3‑
基、1,3,5
‑
三甲基吡唑
‑4‑
基、3,5
‑
二甲基
‑
1,2
‑
二唑
‑4‑
基、1,2,4
‑
三甲基吡咯
‑3‑
基、3
‑
苯基吡咯基、2,3'
‑
二呋喃基、4
‑
甲基吡啶基、2
‑
或3
‑
乙基吲哚基。
[0064]
术语“环烷基”或“环脂肪族”表示具有优选3至14个碳原子,例如3至12或3至10个碳原子,即3、4、5、6、7、8、9、10、11、12、13或14个碳原子(例如3、4、5、6、7、8、9或10个碳原子),更优选3至7个碳原子的“烷基”和“烯基”的环状非芳香族形式。示例性环烷基包括环丙基、环丙烯基、环丁基、环丁烯基、环戊基、环戊烯基、环己基、环己烯基、环庚基、环庚烯基、环辛基、环辛烯基、环壬基、环壬烯基、环癸基、环癸烯基和金刚烷基。术语“环烷基”还旨在包括其双环和三环形式。如果形成双环,则优选各个环在两个邻近的碳原子上彼此连接,然而,或者,两个环通过同一碳原子连接,即,它们形成螺环体系或它们形成“桥连”环体系。环烷基的一些优选实例包括c3‑8‑
环烷基,特别是环丙基、环丁基、环戊基、环己基、环庚基、环辛基、螺[3,3]庚基、螺[3,4]辛基、螺[4,3]辛基、双环[4.1.0]庚基、双环[3.2.0]庚基、双环[2.2.1]庚基、双环[2.2.2]辛基、双环[5.1.0]辛基和双环[4.2.0]辛基。环烷基不包括富勒烯。“经取代的环烷基”意指环烷基的一个或更多个(例如1至与环烷基结合的氢原子的最大数目,例如1、2、3、4、5、6、7、8、9或多至10个,例如1至5、1至4、或1至3、或者1或2个)氢原子被除氢之外的取代基替代(当替代多于一个氢原子时,取代基可以是相同或不同的)。优选地,除氢之外的取代基是如本文中所指定的第1级取代基、第2级取代基或第3级取代基,例如卤素、
‑
oh、
‑
nh2、
‑
nhch3、
‑
n(ch3)2、
‑
cn、
‑
och3、
‑
ocf3、=o、=s、=nh、烷基(例如c1‑6烷基)、烯基(例如c2‑6烯基)和炔基(例如c2‑6炔基)。经取代的环烷基的一些实例包括氧代环己基、氧代环戊基、氟代环己基和氧代环己烯基。
[0065]
术语“杂环烷基”或“杂环”意指其中环烷基中的1、2、3或4个环碳原子被杂原子(例如选自o、s、s(o)、s(o)2、n、b、si和p,优选选自o、s、s(o)2和n,更优选选自o、s和n的那些)替代的如上限定的环烷基。如果杂环烷基的环仅包含一种类型的杂原子,则在所述杂环烷基的环中的所述杂原子的最大数目可为如下:2个o原子(优选1个o原子)、2个s原子(优选1个s原子)、4个n原子(例如1、2或3个n原子)、2个b原子(优选1个b原子)、1个si原子和/或1个p原子。如果杂环烷基的环包含两种或更多种类型的杂原子,则在所述杂环烷基的环中的所述杂原子的最大数目可为如下:1个o原子、1个s原子、2个n原子(优选1个n原子)、1个b原子、1个si原子和/或1个p原子,其中在所述杂环烷基的环中的杂原子的最大总数目为4并且在所述杂环烷基的环中的每个杂原子的最大总数目如下:1个o原子、1个s原子、1或2个n原子、1个b原子(优选0个b原子)、1个si原子(优选0个si原子)和/或1个p原子(优选0个p原子)。在一个实施方案中,杂环烷基的杂原子选自o、s和n。在该实施方案中,优选地,在杂环烷基的每个环中,o原子的最大数目为1,s原子的最大数目为1,并且o和s原子的最大总数目为2。例
如,3至14元杂环烷基包括单环杂环烷基(例如,3、4、5、6或7元,优选4至7元)、双环杂环烷基(例如,8、9或10元)和三环杂环烷基(例如,12、13或14元)。如果杂环烷基包含两个或更多个环,则这些环是稠合的(例如在喹啉基或嘌呤基中),是螺环部分,是桥接结构,通过双键连接,或者是其组合。换言之,未经取代的杂环烷基不包含通过单键连接的两个杂环烷基。术语“杂环烷基”也旨在包含上述杂芳基的部分或完全氢化形式(例如二氢、四氢、六氢、八氢、十氢、十二氢等,或全氢形式)。示例性杂环烷基包括氮杂环丁烷基、吗啉基、异苯并二氢吡喃基、苯并二氢吡喃基、吡咯烷基、咪唑烷基、吡唑烷基、哌啶基、哌嗪基、二氢吲哚基、异二氢吲哚基、triazininanyl;吡咯基、咪唑基和吡唑基的二氢形式;呋喃基、噻吩基、唑基、异唑基、二唑基、三唑基、噻唑基、噻唑基、噻二唑基、吡啶基、吡嗪基和三嗪基的二氢和四氢形式;嘧啶基、哒嗪基、吡咯并噻唑基和吡咯嗪基的二氢、四氢和六氢形式。“经取代的杂环烷基”意指杂环烷基的一个或更多个(例如1至与杂环烷基结合的氢原子的最大数目,例如1、2、3、4、5、6、7、8、9或多至10个,例如1至5、1至4、或1至3、或者1或2个)氢原子被除氢之外的取代基替代(当替代多于一个氢原子时,取代基可以是相同或不同的)。优选地,除氢之外的取代基是如本文中所指定的第1级取代基、第2级取代基或第3级取代基,例如卤素、
‑
oh、
‑
nh2、
‑
nhch3、
‑
n(ch3)2、
‑
cn、
‑
och3、
‑
ocf3、=o、=s、=nh、烷基(例如c1‑6烷基)、烯基(例如c2‑6烯基)和炔基(例如c2‑6炔基)。
[0066]
本文中使用的不饱和化合物或基团的表述“部分氢化形式”意指通过形式上向最初的不饱和化合物或基团添加氢而除去不饱和的一部分同时不除去全部不饱和部分。本文中使用的不饱和化合物或基团的短语“完全氢化形式”与术语“全氢”可互换使用,并且意指通过形式上向最初的不饱和化合物或基团添加氢而除去全部的不饱和。例如,5元杂芳基的部分氢化形式(在环中包含2个双键,例如呋喃)包括所述5元杂芳基的二氢形式(例如2,3
‑
二氢呋喃或2,5
‑
二氢呋喃),而所述5元杂芳基的四氢形式(例如四氢呋喃,即thf)是所述5元杂芳基的完全氢化(或全氢)形式。同样,对于在环中具有3个双键的6元杂芳基(例如吡啶基),部分氢化形式包括二氢和四氢形式(例如二氢吡啶基和四氢吡啶基),而六氢形式(在杂芳基吡啶基的情况下,例如哌啶基)是所述6元杂芳基的完全氢化(或全氢)衍生物。因此,如果芳基或杂芳基包含由环原子之间的双键和三键组成的至少4个不饱和部分,则芳基或杂芳基的六氢形式可仅被认为是根据本发明的部分氢化形式。
[0067]
在烃的上下文中使用的术语“芳香族”意指整个分子必须是芳香族的。例如,如果单环芳基被氢化(部分或完全),则出于本发明的目的,将所得氢化环状结构分类为环烷基。同样地,如果将双环或多环芳基(例如萘基)氢化,则出于本发明的目的,将所得氢化双环或多环结构(例如1,2
‑
二氢萘基)分类为环烷基(即使一个环(例如在1,2
‑
二氢萘基中)仍为芳香族的)。在本技术中,在杂芳基与杂环烷基之间有相似的区别。例如,出于本发明的目的,将二氢吲哚基,即吲哚基的二氢变体分类为杂环烷基,这是由于双环结构的仅一个环是芳香族的并且环原子之一是杂原子。
[0068]
本文中使用的术语“多环”意指该结构具有两个或更多个(例如2、3、4、5、6、7、8、9或10个),优选2、3、4或5个,更优选2、3或4个环。因此,根据本发明,术语“多环”不包括单环结构,其中该结构仅包含一个环。多环基团的实例是稠合结构(例如萘基或蒽基)、螺环化合物、通过单键或双键连接的环(例如联苯)和桥接结构(例如冰片基)。示例性多环结构是具
有至少两个环的上述指定的那些芳基、杂芳基、环烷基和杂环烷基。
[0069]
术语“卤素(halogen)”或“卤素(halo)”意指氟、氯、溴或碘。
[0070]
术语“叠氮基”意指
‑
n3。
[0071]
术语“n
‑
氧化物”意指氧化胺或n
‑
氧化胺,其是包含官能团(r
n
)3n
‑
o
‑
或(r
n
)3n
‑
oh,即n
‑
o配位共价键的化学化合物,其中r
n
独立地选自氢、烷基、烯基、炔基、芳基、杂芳基、环烷基和杂环烷基,其中烷基、烯基、炔基、芳基、杂芳基、环烷基和杂环烷基中的每一个任选地被一个或更多个(例如1个至与烷基、烯基、炔基、芳基、杂芳基、环烷基或杂环烷基结合的氢原子的最大数目,例如1、2、3、4、5、6、7、8、9或多至10个,例如1至5、1至4、或1至3、或者1或2个)独立选择的r
20
取代,r
20
优选为如本文中所指定的第1级取代基、第2级取代基或第3级取代基。
[0072]
术语“任选地取代”指示一个或更多个(例如1至与基团结合的氢原子的最大数目,例如1、2、3、4、5、6、7、8、9或多至10个,例如1至5、1至4、或1至3、或者1或2个)氢原子可被不同于氢的基团(即第1级取代基)替代,所述基团例如烷基(优选c1‑6烷基)、烯基(优选c2‑6烯基)、炔基(优选c2‑6炔基)、芳基(优选6至14元芳基)、杂芳基(优选3至14元杂芳基)、环烷基(优选3至14元环烷基)、杂环烷基(优选3至14元杂环烷基)、卤素、
‑
cn、叠氮基、
‑
no2、
‑
or
71
、
‑
n(r
72
)(r
73
)、
‑
s(o)0‑2r
71
、
‑
s(o)1‑2or
71
、
‑
os(o)1‑2r
71
、
‑
os(o)1‑2or
71
、
‑
s(o)1‑2n(r
72
)(r
73
)、
‑
os(o)1‑2n(r
72
)(r
73
)、
‑
n(r
71
)s(o)1‑2r
71
、
‑
nr
71
s(o)1‑2or
71
、
‑
nr
71
s(o)1‑2n(r
72
)(r
73
)、
‑
op(o)(or
71
)2、
‑
c(=x1)r
71
、
‑
c(=x1)x1r
71
、
‑
x1c(=x1)r
71
和
‑
x1c(=x1)x1r
71
,和/或者与环烷基或杂环烷基的同一碳原子结合的任何两个第1级取代基可连接在一起形成=x1,其中第1级取代基的烷基、烯基、炔基、芳基、杂芳基、环烷基和杂环烷基中的每一个本身可被选自以下的一个或更多个(例如,一个、两个或三个)取代基(即第2级取代基)取代:c1‑6烷基、c2‑6烯基、c2‑6炔基、6至14元芳基、3至14元杂芳基、3至14元环烷基、3至14元杂环烷基、卤素、
‑
cf3、
‑
cn、叠氮基、
‑
no2、
‑
or
81
、
‑
n(r
82
)(r
83
)、
‑
s(o)0‑2r
81
、
‑
s(o)1‑2or
81
、
‑
os(o)1‑2r
81
、
‑
os(o)1‑2or
81
、
‑
s(o)1‑2n(r
82
)(r
83
)、
‑
os(o)1‑2n(r
82
)(r
83
)、
‑
n(r
81
)s(o)1‑2r
81
、
‑
nr
81
s(o)1‑2or
81
、
‑
nr
81
s(o)1‑2n(r
82
)(r
83
)、
‑
op(o)(or
81
)2、
‑
c(=x2)r
81
、
‑
c(=x2)x2r
81
、
‑
x2c(=x2)r
81
和
‑
x2c(=x2)x2r
81
,和/或与作为第1级取代基的环烷基或杂环烷基的同一碳原子结合的任何两个第2级取代基可连接在一起形成=x2,其中第2级取代基的c1‑6烷基、c2‑6烯基、c2‑6炔基、6至14元芳基、3至14元杂芳基、3至14元环烷基、3至14元杂环烷基中的每一个任选地被独立地选自以下的一个或更多个(例如,一个、两个或三个)取代基(即第3级取代基)取代:c1‑3烷基、卤素、
‑
cf3、
‑
cn、叠氮基、
‑
no2、
‑
oh、
‑
o(c1‑3烷基)、
‑
ocf3、
‑
s(c1‑3烷基)、
‑
nh2、
‑
nh(c1‑3烷基)、
‑
n(c1‑3烷基)2、
‑
nhs(o)2(c1‑3烷基)、
‑
s(o)2nh2‑
z
(c1‑3烷基)
z
、
‑
c(=o)oh、
‑
c(=o)o(c1‑3烷基)、
‑
c(=o)nh2‑
z
(c1‑3烷基)
z
、
‑
nhc(=o)(c1‑3烷基)、
‑
nhc(=nh)nh
z
‑2(c1‑3烷基)
z
和
‑
n(c1‑3烷基)c(=nh)nh2‑
z
(c1‑3烷基)
z
,其中每个z独立地为0、1或2并且每个c1‑3烷基独立地为甲基、乙基、丙基或异丙基,和或与作为第2级取代基的3至14元环烷基或杂环烷基的同一碳原子结合的任何两个第3级取代基可连接在一起形成=o、=s、=nh或=n(c1‑3烷基);
[0073]
其中:
[0074]
r
71
、r
72
和r
73
各自独立地选自h、c1‑6烷基、c2‑6烯基、c2‑6炔基、3至7元环烷基、5或6元芳基、5或6元杂芳基和3至7元杂环烷基,其中c1‑6烷基、c2‑6烯基、c2‑6炔基、3至7元环烷基、5或6元芳基、5或6元杂芳基和3至7元杂环烷基中的每一个任选地被独立地选自以下的一个、
两个或三个取代基取代:c1‑3烷基、卤素、
‑
cf3、
‑
cn、叠氮基、
‑
no2、
‑
oh、
‑
o(c1‑3烷基)、
‑
ocf3、=o、
‑
s(c1‑3烷基)、
‑
nh2、
‑
nh(c1‑3烷基)、
‑
n(c1‑3烷基)2、
‑
nhs(o)2(c1‑3烷基)、
‑
s(o)2nh2‑
z
(c1‑3烷基)
z
、
‑
c(=o)(c1‑3烷基)、
‑
c(=o)oh、
‑
c(=o)o(c1‑3烷基)、
‑
c(=o)nh2‑
z
(c1‑3烷基)
z
、
‑
nhc(=o)(c1‑3烷基)、
‑
nhc(=nh)nh
z
‑2(c1‑3烷基)
z
和
‑
n(c1‑3烷基)c(=nh)nh2‑
z
(c1‑3烷基)
z
,其中每个z独立地为0、1或2并且每个c1‑3烷基独立地为甲基、乙基、丙基或异丙基;
[0075]
r
81
、r
82
和r
83
各自独立地选自h、c1‑4烷基、c2‑4烯基、c2‑4炔基、3至6元环烷基、5或6元芳基、5或6元杂芳基和3至6元杂环烷基,其中c1‑4烷基、c2‑4烯基、c2‑4炔基、3至6元环烷基、5或6元芳基、5或6元杂芳基和3至6元杂环烷基中的每一个任选地被独立地选自以下的一个、两个或三个取代基取代:c1‑3烷基、卤素、
‑
cf3、
‑
cn、叠氮基、
‑
no2、
‑
oh、
‑
o(c1‑3烷基)、
‑
ocf3、=o、
‑
s(c1‑3烷基)、
‑
nh2、
‑
nh(c1‑3烷基)、
‑
n(c1‑3烷基)2、
‑
nhs(o)2(c1‑3烷基)、
‑
s(o)2nh2‑
z
(c1‑3烷基)
z
、
‑
c(=o)(c1‑3烷基)、
‑
c(=o)oh、
‑
c(=o)o(c1‑3烷基)、
‑
c(=o)nh2‑
z
(c1‑3烷基)
z
、
‑
nhc(=o)(c1‑3烷基)、
‑
nhc(=nh)nh
z
‑2(c1‑3烷基)
z
和
‑
n(c1‑3烷基)c(=nh)nh2‑
z
(c1‑3烷基)
z
,其中每个z独立地为0、1或2并且每个c1‑3烷基独立地为甲基、乙基、丙基或异丙基;以及
[0076]
x1和x2各自独立地选自o、s和n(r
84
),其中r
84
是h或c1‑3烷基。
[0077]
典型的第1级取代基优选地选自以下:c1‑6烷基、c2‑6烯基、c2‑6炔基、6至14元(例如6至10元)芳基、3至14元(例如5或6元)杂芳基、3至14元(例如3至7元)环烷基、3至14元(例如3至7元)杂环烷基、卤素、
‑
cn、叠氮基、
‑
no2、
‑
or
71
、
‑
n(r
72
)(r
73
)、
‑
s(o)0‑2r
71
、
‑
s(o)1‑2or
71
、
‑
os(o)1‑2r
71
、
‑
os(o)1‑2or
71
、
‑
s(o)1‑2n(r
72
)(r
73
)、
‑
os(o)1‑2n(r
72
)(r
73
)、
‑
n(r
71
)s(o)1‑2r
71
、
‑
nr
71
s(o)1‑2or
71
、
‑
c(=x1)r
71
、
‑
c(=x1)x1r
71
、
‑
x1c(=x1)r
71
和
‑
x1c(=x1)x1r
71
,例如c1‑4烷基、c2‑4烯基、c2‑4炔基、6元芳基、5或6元杂芳基、3至7元环烷基、3至7元(例如5或6元)杂环烷基、卤素、
‑
cf3、
‑
cn、叠氮基、
‑
no2、
‑
oh、
‑
o(c1‑3烷基)、
‑
s(c1‑3烷基)、
‑
nh2、
‑
nh(c1‑3烷基)、
‑
n(c1‑3烷基)2、
‑
nhs(o)2(c1‑3烷基)、
‑
s(o)2nh2‑
z
(c1‑3烷基)
z
、
‑
c(=o)oh、
‑
c(=o)o(c1‑3烷基)、
‑
c(=o)nh2‑
z
(c1‑3烷基)
z
、
‑
nhc(=o)(c1‑3烷基)、
‑
nhc(=nh)nh
z
‑2(c1‑3烷基)
z
和
‑
n(c1‑3烷基)c(=nh)nh2‑
z
(c1‑3烷基)
z
,其中每个z独立地为0、1或2并且每个c1‑3烷基独立地为甲基、乙基、丙基或异丙基;其中x1独立地选自o、s、nh和n(ch3);并且r
71
、r
72
和r
73
中的每一个如上所限定,或者优选地,独立地选自h、c1‑4烷基、c2‑4烯基、c2‑4炔基、5或6元环烷基、5或6元芳基、5或6元杂芳基和5或6元杂环烷基,其中烷基、烯基、炔基、环烷基、芳基、杂芳基和杂环烷基中的每一个任选地被独立地选自以下的一个、两个或三个取代基取代:c1‑3烷基、卤素、
‑
cf3、
‑
cn、叠氮基、
‑
no2、
‑
oh、
‑
o(c1‑3烷基)、
‑
s(c1‑3烷基)、
‑
nh2、
‑
nh(c1‑3烷基)、
‑
n(c1‑3烷基)2、
‑
nhs(o)2(c1‑3烷基)、
‑
s(o)2nh2‑
z
(c1‑3烷基)
z
、
‑
c(=o)oh、
‑
c(=o)o(c1‑3烷基)、
‑
c(=o)nh2‑
z
(c1‑3烷基)
z
、
‑
nhc(=o)(c1‑3烷基)、
‑
nhc(=nh)nh
z
‑2(c1‑3烷基)
z
和
‑
n(c1‑3烷基)c(=nh)nh2‑
z
(c1‑3烷基)
z
,其中每个z独立地为0、1或2并且每个c1‑3烷基独立地为甲基、乙基、丙基或异丙基。第1级取代基的一些具体实例独立地选自以下:c1‑3烷基、苯基、咪唑基、噻唑基、环戊基、环己基、二氢噻唑基、噻唑烷基、卤素、
‑
cf3、
‑
cn、
‑
oh、
‑
o(c1‑3烷基)、
‑
s(c1‑3烷基)、
‑
nh2、
‑
nh(c1‑3烷基)、
‑
n(c1‑3烷基)2、
‑
nhs(o)2(c1‑3烷基)、
‑
c(=o)oh、
‑
c(=o)o(c1‑3烷基)、
‑
c(=o)nh2‑
z
(c1‑3烷基)
z
、
‑
nhc(=o)(c1‑3烷基)、
‑
nhc(=nh)nh
z
‑2(c1‑3烷基)
z
和
‑
n(c1‑3烷基)c(=nh)nh2‑
z
(c1‑3烷基)
z
,其中每个z独立地为0、1或2并且每个c1‑3烷基独立地为甲基、乙基、丙基或异丙基。特别优选的第1级取代基独立地选自c1‑3烷基、苯基、噻唑烷基、卤素(例如f、cl或br)、
‑
nh2、
‑
nhs(o)2(c1‑3烷基)、
‑
nhc(=o)(c1‑3烷基)和
‑
nhc(=nh)nh
z
‑2(c1‑3烷基)
z
,其中z
为0、1或2且每个c1‑3烷基独立地为甲基、乙基、丙基或异丙基。
[0078]
典型的第2级取代基优选地选自c1‑4烷基、c2‑4烯基、c2‑4炔基、6或10元芳基、5或6元杂芳基、5或6元环烷基、5或6元杂环烷基、卤素、=o、=s、
‑
cf3、
‑
cn、叠氮基、
‑
no2、
‑
oh、
‑
o(c1‑3烷基)、
‑
s(c1‑3烷基)、
‑
nh2、
‑
nh(c1‑3烷基)、
‑
n(c1‑3烷基)2、
‑
nhs(o)2(c1‑3烷基)、
‑
s(o)2nh2‑
z
(c1‑3烷基)
z
、
‑
c(=o)oh、
‑
c(=o)o(c1‑3烷基)、
‑
c(=o)nh2‑
z
(c1‑3烷基)
z
、
‑
nhc(=o)(c1‑3烷基)、
‑
nhc(=nh)nh
z
‑2(c1‑3烷基)
z
和
‑
n(c1‑3烷基)c(=nh)nh2‑
z
(c1‑3烷基)
z
,其中每个z独立地是0、1或2并且每个c1‑3烷基独立地是甲基、乙基、丙基或异丙基。第2级取代基的一些具体实例独立地选自以下:c1‑3烷基、苯基、5或6元杂芳基、5或6元环烷基、5或6元杂环烷基、卤素、=o、=s、
‑
cf3、
‑
cn、
‑
oh、
‑
o(c1‑3烷基)、
‑
s(c1‑3烷基)、
‑
nh2、
‑
nh(c1‑3烷基)、
‑
n(c1‑3烷基)2、
‑
nhs(o)2(c1‑3烷基)、
‑
c(=o)oh、
‑
c(=o)o(c1‑3烷基)、
‑
c(=o)nh2‑
z
(c1‑3烷基)
z
、
‑
nhc(=o)(c1‑3烷基)、
‑
nhc(=nh)nh
z
‑2(c1‑3烷基)
z
和
‑
n(c1‑3烷基)c(=nh)nh2‑
z
(c1‑3烷基)
z
,其中每个z独立地为0、1或2并且每个c1‑3烷基独立地为甲基、乙基、丙基或异丙基。特别优选的第2级取代基独立地选自甲基、乙基、丙基、异丙基、苯基、=o和=s。
[0079]
典型的第3级取代基优选地选自c1‑3烷基、苯基、卤素、
‑
cf3、
‑
oh、
‑
och3、
‑
sch3、
‑
nh2‑
z
(ch3)
z
、
‑
c(=o)oh和
‑
c(=o)och3,其中z为0、1或2并且c1‑3烷基为甲基、乙基、丙基或异丙基。特别优选的第3级取代基选自甲基、乙基、丙基、异丙基、卤素(例如f、cl或br)和
‑
cf3,例如卤素(例如f、cl或br),和
‑
cf3。
[0080]
本文中使用的术语“任选的”或“任选地”意指随后描述的事件、状况或情况可发生或可不发生,并且所述描述包括其中所述事件、状况或情况发生的实例以及其中所述事件、状况或情况不发生的实例。
[0081]“异构体”是具有相同分子式但结构不同(“结构异构体”)或者官能团和/或原子的几何(空间)位置不同(“立体异构体”)的化合物。“对映体”是为彼此不可重叠镜像的立体异构体对。“外消旋混合物”或“外消旋体”包含等量的对映体对,并用前缀(
±
)表示。“非对映体”是不可重叠且彼此不是镜像的立体异构体。“互变异构体”是同一化学物质的结构异构体,其由于单个原子或原子团的迁移而自发和可逆地相互转化,即使当是纯的时;即互变异构体处于彼此的动态化学平衡中。互变异构体的一些实例是酮
‑
烯醇
‑
互变异构的异构体。“构象异构体”是仅通过围绕形式上的单键旋转即可相互转化的立体异构体,并且特别是包含那些导致(杂)环的不同3维形式,例如环己烷的椅型、半椅型、船型和扭船型的立体异构体。
[0082]
本文中所指的“多晶型”意指固体材料(例如化合物)能够以多于一种的形式或晶体结构存在,即“多晶型变体”或“多晶型”。术语“多晶型变体”、“多晶型”和“多晶型物”在本发明中可互换使用。根据本发明,这些“多晶型变体”包括结晶形式、无定形形式、溶剂合物和水合物。主要地,存在不同多晶型的原因是由于结晶过程中使用的条件不同,例如以下:
[0083]
·
溶剂效应(在极性和非极性溶剂中晶体的堆积可不同);
[0084]
·
某些杂质抑制生长模式并且有利于亚稳态多晶型物的生长;
[0085]
·
材料所结晶的过饱和水平(其中一般而言高于溶解度的浓度越高,形成亚稳态的可能性越大);
[0086]
·
进行结晶的温度;
[0087]
·
共价键的几何形状(导致构象多晶型的差异);
[0088]
·
搅拌条件的改变。
[0089]
多晶型可具有不同的化学、物理和/或药理学特性,包括但不限于熔点、x射线晶体和衍射图、化学反应性、溶解性、溶出速率、蒸汽压、密度、吸湿性、流动性、稳定性、压实性和生物利用度。多晶型可在特定温度下自发地从亚稳态形式(不稳定形式)转变为稳定形式。根据奥斯特瓦尔德法则(ostwald’s rule),一般而言先结晶的不是最稳定的多晶型物,而是最不稳定的多晶型物。因此,化学化合物,例如本发明的化合物的质量、效力、安全性、加工性和/或制造可被多晶型影响。通常,选择化合物(例如本发明的化合物)的最稳定的多晶型物是因为其转化为另一种多晶型物的可能性最小。然而,由于稳定性以外的原因,例如,溶解性、溶出速率和/或生物利用度,可选择不是最稳定的多晶型的多晶型。
[0090]
本文中使用的术语材料的“结晶形式”意指所述材料的最小组分(即,原子、分子或离子)形成晶体结构。本文中所指的“晶体结构”意指在结晶液体或固体中原子或分子的独特三维排列,其特征在于图案、以特定方式排列的原子组以及表现出长程有序和对称的晶格。晶格是在三维上周期性重复的点阵列,并且图案位于晶格的点上。晶格的亚单位是晶胞。晶格参数是晶胞边缘的长度和晶胞之间的角度。晶体的对称性体现在其空间群中。为了描述晶体结构,需要以下参数:化学式、晶格参数、空间群、原子的坐标和点位置的占有数。
[0091]
本文中使用的术语材料的“无定形形式”意指所述材料的最小组分(即,原子、分子或离子)不是排列在晶格中而是随机排列。因此,与存在短程有序(与下一个邻近原子的距离恒定)和长程有序(基本晶格的周期性重复)的晶体不同,在无定形形式中仅存在短程有序。
[0092]
本文中使用的术语“溶剂合物”是指溶出的材料在溶剂(例如有机溶剂(例如,脂肪醇(例如甲醇、乙醇、正丙醇、异丙醇)、丙酮、乙腈、乙醚等)、水或这些液体中的两种或更多种的混合物))中的加成络合物,其中加成络合物以晶体或混合晶体的形式存在。加成络合物中所包含溶剂的量可以是化学计量的或非化学计量的。“水合物”是其中溶剂是水的溶剂合物。
[0093]
在经同位素标记的化合物中,一个或更多个原子被具有相同质子数但中子数不同的相应原子替代。例如,氢原子可以被氘原子替代。可用于本发明化合物的示例性同位素包括氘、
11
c、
13
c、
14
c、
15
n、
18
f、
32
p、
32
s、
35
s、
36
cl和
125
i。
[0094]
在本发明的方法中使用和/或合成的并且包含碱性官能团的化合物可与多种无机酸或有机酸形成盐,特别是可药用盐。在本发明的方法中使用和/或合成的并且包含酸性官能团的化合物可与多种无机碱或有机碱形成盐,特别是可药用盐。下文给出了示例性无机酸/碱和有机酸/碱以及这些化合物的示例性酸/碱加成盐。在本发明的方法中使用和/或合成的并且包含碱性和酸性官能团二者的化合物可转化为碱或酸加成盐。在本发明的方法中使用和/或合成的化合物的中性形式可通过使盐与碱或酸接触并以常规方式分离母体化合物而再生。盐优选为可药用盐。
[0095]
术语“可药用”是指不与药物组合物的活性组分的(例如治疗)作用相互作用的材料的无毒性。
[0096]“可药用盐”包括例如酸加成盐,其可例如通过将化合物的溶液与可药用酸例如盐酸、硫酸、富马酸、马来酸、琥珀酸、乙酸、苯甲酸、柠檬酸、酒石酸、碳酸或磷酸的溶液混合而形成。此外,当化合物带有酸性部分时,其合适的可药用盐可包括碱金属盐(例如钠盐或钾
盐)、碱土金属盐(例如钙盐或镁盐)、以及与合适的有机配体(例如使用抗衡阴离子如卤化物、氢氧根、羧酸根、硫酸根、磷酸根、硝酸根、烷基磺酸根和芳基磺酸根形成的铵、季铵和胺阳离子)形成的盐。可药用盐的一些说明性实例包括但不限于乙酸盐、己二酸盐、藻酸盐、精氨酸盐、抗坏血酸盐、天冬氨酸盐、苯磺酸盐、苯甲酸盐、碳酸氢盐、硫酸氢盐、酒石酸氢盐、硼酸盐、溴化物、丁酸盐、乙二胺四乙酸钙、樟脑酸盐、樟脑磺酸盐、右旋樟脑磺酸盐、碳酸盐、氯化物、柠檬酸盐、克拉维酸盐、环戊烷丙酸盐、二葡萄糖酸盐、二盐酸盐、十二烷基硫酸盐、依地酸盐、乙二磺酸盐、依托酸盐(estolate)、乙磺酸盐(esylate)、乙磺酸盐(ethanesulfonate)、甲酸盐、富马酸盐、半乳酸盐(galactate)、半乳糖醛酸盐、葡萄糖酸盐、葡庚糖酸盐、葡糖酸盐、谷氨酸盐、甘油磷酸盐、乙醇酰阿散酸盐(glycolylarsanilate)、半硫酸盐、庚酸盐、己酸盐、己基间苯二酚盐、海巴明(hydrabamine)、氢溴酸盐、盐酸盐、氢碘酸盐、2
‑
羟基
‑
乙磺酸盐、羟基萘酸盐、碘化物、异丁酸盐、异硫氰酸盐、乳酸盐、乳糖醛酸盐、月桂酸盐、月桂基硫酸盐、苹果酸盐、马来酸盐、丙二酸盐、扁桃酸盐、甲磺酸盐、甲烷磺酸盐、甲基硫酸盐、粘酸盐、2
‑
萘磺酸盐、萘磺酸盐、烟酸盐、硝酸盐、n
‑
甲基葡萄糖铵盐、油酸盐、草酸盐、扑酸盐(双羟萘酸盐)、棕榈酸盐、泛酸盐、果胶酸盐、过硫酸盐、3
‑
苯基丙酸盐、磷酸盐/二磷酸盐、邻苯二甲酸盐、苦味酸盐、新戊酸盐、聚半乳糖醛酸盐、丙酸盐、水杨酸盐、硬脂酸盐、硫酸盐、辛二酸盐、琥珀酸盐、鞣酸盐、酒石酸盐、茶氯酸盐、甲苯磺酸盐、甲苯磺酸盐、三乙基碘盐(triethiodide)、十一烷酸盐、戊酸盐等(参见,例如,berge et al.,"pharmaceutical salts",j.pharm.sci.,66,pp.1
‑
19(1977))。
[0097]
本文中与反应混合物一起使用的表述“回流温度”是指反应混合物中包含的液体的沸点,其具有反应混合物中包含的所有液体的最低沸点。
[0098]
在本说明书的正文通篇引用了数个文件。无论是上文还是下文,本文引用的每篇文献(包括所有专利、专利申请、科学出版物、制造商的说明书、指南等),其均在此以其整体通过引用并入。本文中的任何内容都不应当被解释为承认本发明无权由于在先发明而先于这样的公开内容。
[0099]
在一个优选实施方案中,通过本发明的方法获得的产物(特别是式(i)化合物)基本上不含污染物。
[0100]
本文中与通过本发明的方法获得的产物一起使用的术语“基本上不含污染物”意指通过本发明的方法获得的产物中污染物的量为基于所述产物的总重量的至多5重量%(优选至多4重量%、至多3重量%、至多2重量%、至多1重量%、至多0.5重量%、至多0.1重量%、至多0.05重量%、至多0.01重量%、至多0.005重量%、至多0.001重量%)。
[0101]
本文在合成目的化合物(例如式(i)化合物或其溶剂合物或盐,或者式(3)、(4)和(5)中的任一个的中间体))的上下文中使用的术语“无色谱的方式”意指在所述合成的至少一个步骤中(优选在所述合成的所有步骤中)通过色谱以外的方法,优选通过沉淀目的化合物,任选地用合适的溶剂(特别是目的化合物在其中难溶的溶剂)洗涤经沉淀的目的化合物,并任选地干燥经沉淀的目的化合物,来实现目的化合物与其他化合物(例如污染物)的分离。然而,本文在合成目的化合物的上下文中使用的术语“无色谱的方式”并不意味着对在合成期间获得的样品的分析是使用色谱进行的(即,以无色谱的方式进行的合成目的化合物的方法仅排除制备步骤使用色谱,但不排除分析步骤使用色谱)。
[0102]
本文中使用的术语“当量”意指包含1摩尔氢(即1.008g氢)或1摩尔不同元素(例如,12.011g碳或15.999g氧)的化合物的量。例如,浓度为40g/l的naoh溶液与(i)浓度为56.5g/l的koh溶液,(ii)浓度为36.5g的hcl溶液;或(iv)浓度为49g/l的h2so4溶液当量。此外,在例如第一化合物与第二化合物的缩合反应的上下文中,其中第一和第二化合物以1:1的摩尔比反应,术语“1当量”意指使用x摩尔(例如,x=2)的第一化合物和x摩尔的第二化合物,即第一化合物的摩尔量与第二化合物的摩尔量相同。
[0103]
本文中使用的术语“难溶性”化合物和“不溶性”化合物在溶剂的上下文中可互换,并且意指在标准条件下小于0.5重量份(优选地,小于0.4重量份,例如小于0.3重量份、小于0.2重量份、小于0.1重量份、小于0.09重量份、小于0.08重量份、小于0.07重量份、小于0.06重量份、小于0.05重量份、小于0.04重量份、小于0.03重量份、小于0.02重量份、小于0.01重量份、小于0.009重量份、小于0.005重量份或小于0.004重量份)的化合物溶于100重量份溶剂中。
[0104]
本文中使用的术语“标准条件”是指25℃的温度和101.325kpa的绝对压力。
[0105]
在第一方面中,本发明涉及用于合成n
‑
(4
‑
(4
‑
氨基
‑2‑
(2
‑
甲氧基乙基)
‑
1h
‑
咪唑并[4,5
‑
c]喹啉
‑1‑
基)丁基)
‑
n
‑
(四氢
‑
2h
‑
吡喃
‑4‑
基)乙酰胺(即式(i)化合物)、其溶剂合物或盐。在本发明的上下文中,新中间体是作为新合成方法的一部分产生的。总之,本发明提供了用于合成n
‑
(4
‑
(4
‑
氨基
‑2‑
(2
‑
甲氧基乙基)
‑
1h
‑
咪唑并[4,5
‑
c]喹啉
‑1‑
基)丁基)
‑
n
‑
(四氢
‑
2h
‑
吡喃
‑4‑
基)乙酰胺、其溶剂合物或盐的经改进的有效的方法。
[0106]
更具体地,本发明涉及用于合成n
‑
(4
‑
(4
‑
氨基
‑2‑
(2
‑
甲氧基乙基)
‑
1h
‑
咪唑并[4,5
‑
c]喹啉
‑1‑
基)丁基)
‑
n
‑
(四氢
‑
2h
‑
吡喃
‑4‑
基)乙酰胺、其溶剂合物或盐的方法,该方法包括以下步骤:
[0107]
a)提供式(3)化合物或其溶剂合物或盐,其中r1和r2各自独立地选自
‑
h和胺基保护基团,并且r1和r2中的至少一个是胺基保护基团:
[0108][0109]
b)使式(3)化合物或其溶剂合物或盐与一种或更多种试剂反应以除去r1和r2位的胺基保护基团,以得到式(4)化合物或其溶剂合物或盐:
[0110]
[0111]
c)使式(4)化合物或其溶剂合物或盐与用于引入(i)四氢吡喃基和(ii)乙酰基的一种或更多种试剂反应,以得到式(5)化合物或其溶剂合物或盐:
[0112][0113]
以及
[0114]
d)使式(5)化合物或其溶剂合物或盐进行氧化胺化反应以得到式(i)化合物或其溶剂合物或盐。
[0115]
在第一方面的方法(特别是如图1a、1b、1c、1d和1e中任一个所指定的本发明方法,或者包括(1)如图2a所指定的步骤a)和/或(2)如图3a、3b、3c、3d和3e中任一个所指定的步骤b)的本发明的方法)的一个实施方案中,r1和r2各自独立地选自
‑
h、叔丁氧基羰基(boc)、9
‑
芴基甲氧基羰基(fmoc)、苄氧基羰基(cbz)、甲苯磺酸酯(ts)、苄基(bn)、烯丙氧基羰基(alloc)、三苯甲基(trt)、二甲氧基三苯甲基(dmt)和单甲氧基三苯甲基(mmt)。优选地,r1和r2中的一个是h并且另一个是胺基保护基团,例如选自叔丁氧基羰基(boc)、9
‑
芴基甲氧基羰基(fmoc)、苄氧基羰基(cbz)、甲苯磺酸酯(ts)、苄基(bn)、烯丙氧基羰基(alloc)、三苯甲基(trt)、二甲氧基三苯甲基(dmt)和单甲氧基三苯甲基(mmt),更优选地,选自叔丁氧基羰基(boc)、9
‑
芴基甲氧基羰基(fmoc)和烯丙氧基羰基(alloc)。在第一方面的方法(特别是如图1a、1b、1c、1d和1e中任一个所指定的本发明方法,或者包括(1)如图2a所指定的步骤a)和/或(2)如图3a、3b、3c、3d和3e中任一个所指定的步骤b)的本发明的方法)的一个特别优选的实施方案中,r1和r2中的一个是h并且另一个是叔丁氧基羰基(boc)。
[0116]
在第一方面的方法的任何上述实施方案中,步骤a)可包括使式(1)化合物或其溶剂合物或盐与hooc(ch2)2och3(式(2))或其衍生物反应以得到式(3)化合物或其溶剂合物或盐:
[0117][0118]
在该实施方案中(例如在如图1a和1b中任一个所指定的方法中),可使用式2的任何衍生物,只要所述衍生物与式(1)化合物或其溶剂合物或盐缩合而得到式(3)化合物即可。示例性式(2)化合物的衍生物包括但不限于羧酸卤化物、原酸酯和1,1
‑
二烷氧基烷基链烷酸酯。在第一方面的方法的一个优选实施方案中,式(2)的衍生物是原酸酯,优选具有式(r
10
o)3c(ch2)2och3的原酸酯(参见,例如图1c、1d、1e、1f、2a、2b和2c中的任一个),其中每个r
10
独立地选自烷基、烯基、炔基、芳基、杂芳基、环烷基和杂环烷基,其中任一个任选地被一
个或更多个(例如1至与烷基、烯基、炔基、芳基、杂芳基、环烷基或杂环烷基结合的氢原子的最大数目,例如1、2、3、4、5、6、7、8、9或多至10个,例如1至5、1至4、或1至3、或者1或2个)独立选择的r
20
取代,r
20
优选为如本文中所指定的第1级取代基、第2级取代基或第3级取代基。在一个实施方案中,每个r
10
独立地选自c1‑
12
烷基,例如c1‑8烷基,例如甲基、乙基或丙基。在一个实施方案中,相对于1当量的式(1)化合物,用于与式(1)化合物反应的式(2)化合物或其衍生物的量可为1至1.5当量(例如1.0至1.4当量、1.1至1.3当量、1.2至1.3当量)。
[0119]
在第一方面的方法(特别是如图1a、1b、1c、1d、1e、1f、1g和1h中任一个所指定的本发明方法,或者包括如图2a、2b、2c和2d中任一个所指定的步骤a)的本发明的方法)的任何上述实施方案中,式(1)化合物与式(2)化合物的反应可(i)在溶剂中进行;(ii)在存在酸的情况下进行;(iii)在合适的温度下进行;和/或(iv)持续足够的时间量。
[0120]
在第一方面的方法(特别是如图1a、1b、1c、1d和1e中任一个所指定的本发明方法,或者包括如图2a所指定的步骤a)的本发明的方法)的任何上述实施方案中,式(1)化合物与式(2)化合物的反应可在溶剂中进行,例如芳香族溶剂,优选甲苯中进行。相对于1重量份的式(1)化合物,用于该反应的溶剂的量可以是2至20体积份(例如3至18体积份、4至16体积份、6至14体积份、8至12体积份、9至10体积份)。
[0121]
在第一方面的方法(特别是如图1a、1b、1c、1d和1e中任一个所指定的本发明方法,或者包括如图2a所指定的步骤a)的本发明的方法)的任何上述实施方案中,式(1)化合物与式(2)化合物的反应可在存在酸,例如无机酸或有机酸(例如对甲苯磺酸)的情况下进行。相对于1当量的式(1)化合物,用于该反应的酸的量可以是0.01至0.1当量(例如0.02至0.09当量、0.02至0.08当量、0.03至0.07当量、0.03至0.06当量、0.04至0.05当量)。
[0122]
在第一方面的方法(特别是如图1a、1b、1c、1d、1e、1f、1g和1h中任一个所指定的本发明方法,或者包括如图2a、2b、2c和2d中任一个所指定的步骤a)的本发明的方法)的任何上述实施方案中,式(1)化合物与式(2)化合物的反应可在任何合适的温度下进行,例如在标准条件(例如,在25℃)下、在降低的温度(例如
‑
10℃至10℃)下或在升高的温度下(例如,在50℃或更高,例如在包含式(1)化合物、式(2)化合物和/或式(3)化合物的反应混合物的回流温度下)进行。示例性的温度范围为0℃至120℃,例如25℃至溶剂的回流温度(如果存在的话)。
[0123]
在第一方面的方法的任何上述实施方案中,式(1)化合物与式(2)化合物的反应可持续足够的时间量(特别是如图1a、1b、1c、1d、1e、1f、1g和1h中任一个所指定的本发明方法,或者包括如图2a、2b、2c和2d中任一个所指定的步骤a)的本发明的方法),例如在0.5至10小时,优选1至9小时,更优选1.5至8小时,更优选2至7小时,更优选2.5至6小时,更优选3至5小时的范围内进行。替代地,式(1)化合物与式(2)化合物的反应可进行至反应基本上完成,即直至基本上消耗式(1)化合物的全部初始量(例如,≥初始量的99.0%)。
[0124]
在第一方面的方法(特别是如图1a、1b、1c、1d、1e、1f、1g和1h中任一个所指定的本发明方法,或者包括如图2a、2b、2c和2d中任一个所指定的步骤a)的本发明的方法)的任何上述实施方案中,在式(1)化合物与式(2)化合物的反应进行持续了足够的时间量(例如,直至反应基本上完成,即直至基本上消耗式(1)化合物的全部初始量)之后,可将反应混合物冷却至低于用于式(1)化合物与式(2)化合物的反应的最高温度的任何温度,优选达到进行下一步的温度或温度范围。
[0125]
在第一方面的方法的步骤b)中,使式(3)化合物或其溶剂合物或盐与一种或更多种试剂反应以除去r1和r2位的胺基保护基团以得到式(4)化合物或其溶剂合物或盐:
[0126][0127]
因此,换言之,在步骤b)中,将式(3)化合物的受保护的伯胺基脱保护以得到具有游离主要氨基的式(4)化合物。
[0128]
在第一方面的方法(特别是如图1a、1b、1c、1d、1e、1f、1g和1h中任一个所指定的本发明方法,或者包括如图3a、3b、3c、3d、3e、3f和3g中任一个所指定的步骤b)的本发明的方法)的任何上述实施方案中,步骤b)可(i)在溶剂中进行;(ii)在合适的温度下进行;和/或(iii)持续足够的时间量。用于步骤b)中的脱保护反应的反应条件和一种或更多种试剂是变化的并且主要取决于在r1和/或r2位使用的特定胺基保护基团。然而,技术人员熟悉保护技术,并且因此知晓用于将受保护的伯胺基脱保护的合适方法(包括条件(例如,温度、反应时间、溶剂等)和试剂);参见,例如"greene's protective groups in organic synthesis",peter g.m.wuts(ed.),2014,john wiley&sons,inc。用于除去常见胺基保护基团boc、trt、fmoc、cbz和alloc的示例性条件和/或试剂如下:
[0129]
(1)boc:添加强酸(例如,选自三氟乙酸(tfa;例如,在dcm中为25至50%)、hcl(例如,在有机溶剂中为4至6m)、ch3so3h(例如,在二氧六环中为2m)和(h3c)3sicl(tmscl;例如,在dcm中为1mtmscl
‑
苯酚));
[0130]
(2)trt:添加强酸(例如,tfa(例如,在dcm中为1%或在dcm中的0.2%、1%h2o)、hobt(例如,在2,2,2
‑
三氟乙醇中为0.1m)或三氯乙酸(tca;例如,在dcm中为3%));
[0131]
(3)fmoc:添加碱,特别是仲胺(例如nh3(例如,作为液体;约10小时)、吗啉或哌啶(在几分钟内)、二乙胺(dea;例如,10%)、二甲基乙酰胺(dma;例如,2小时)、或有机溶剂中的聚合(硅胶或聚苯乙烯)仲胺(即哌嗪或哌啶);
[0132]
(4)cbz:催化氢解或添加强酸(例如,hbr(例如,在乙酸中)、tfa(例如,在高温下;tfa
‑
苯硫醚)、hf(例如,液体)或bbr3);
[0133]
(5)alloc:经pd催化将烯丙基转移至亲核试剂或清除剂(例如,pd(pph)3;清除剂:在有机溶剂中的h3n
·
bh3、me2nh
·
bh3或phsih3)
[0134]
在第一方面的方法(特别是如图1a、1b、1c、1d和1e中任一个所指定的本发明方法,或者包括如图3a、3b、3c、3d和3e中任一个所指定的步骤b)的本发明的方法)的任何上述实施方案中,在步骤b)中r1和r2各自可独立地选自
‑
h和叔丁氧基羰基(boc),并且在步骤b)中用于除去胺基保护基团的一种或更多种试剂可选自三氟乙酸(tfa)、hcl、ch3so3h和(h3c)3sicl(tmscl)。
[0135]
在第一方面的方法(特别是如图1a、1b、1c、1d、1e、1f、1g和1h中任一个所指定的本发明方法,或者包括如图3a、3b、3c、3d、3e、3f和3g中任一个所指定的步骤b)的本发明的方
法)的任何上述实施方案中,步骤b)可在溶剂中进行,例如芳香族溶剂,例如,用于步骤a)的溶剂,优选甲苯中进行。
[0136]
在第一方面的方法(特别是如图1a、1b、1c、1d、1e、1f、1g和1h中任一个所指定的本发明方法,或者包括如图3a、3b、3c、3d、3e、3f和3g中任一个所指定的步骤b)的本发明的方法)的任何上述实施方案中,步骤b)可在任何合适的温度下进行,例如在标准条件下(例如,在25℃)、在降低的温度(例如
‑
10℃至10℃)下或在升高的温度(例如,在50℃或更高,例如在包含式(4)化合物、用于除去r1和r2位的胺基保护基团的一种或更多种试剂、和/或式(4)化合物的反应混合物的回流温度)下进行,这取决于在步骤b)中使用的特定脱保护反应,例如0℃至40℃。如果,例如,r1和r2各自独立地选自
‑
h和叔丁氧基羰基(boc)(参见,例如,如图1f、1g和1h中任一个所指定的本发明方法,或者包括如图3f和3g中任一个所指定的步骤b)的本发明方法),用于步骤b)中脱保护反应的示例性温度范围为0℃至30℃,例如10℃至25℃。在第一方面的方法(特别是如图1a、1b、1c、1d、1e、1f、1g和1h中任一个所指定的本发明方法,或者包括如图3a、3b、3c、3d、3e、3f和3g中任一个所指定的步骤b)的本发明的方法)的一个实施方案中,相对于1当量的式(3)化合物,步骤b)中用于去除r1和r2位的胺基保护基团的一种或更多种试剂的量可以是1.5至10当量(例如2.0至9当量、2.5至8当量、3至7当量、3.5至7当量、4至6当量)。
[0137]
在第一方面的方法(特别是如图1a、1b、1c、1d、1e、1f、1g和1h中任一个所指定的本发明方法,或者包括如图3a、3b、3c、3d、3e、3f和3g中任一个所指定的步骤b)的本发明的方法)的任何上述实施方案中,步骤b)优选地持续足够的时间量,例如在0.5至5小时,优选1至4.5小时,更优选1.5至4小时,更优选2至3.5小时,更优选2.5至3小时的范围内进行。替代地,进行步骤b)直至反应基本上完成,即直至基本上消耗式(3)化合物的全部初始量(例如,≥初始量的99.0%)。
[0138]
在第一方面的方法的任何上述实施方案中,其中在步骤b)中添加酸(特别是在如图1f、1g和1h中任一个所指定的本发明方法的一些实施方案中,或者在包括如图3f和3g中任一个所指定的步骤b)的第一方面的方法的一些实施方案中),优选地,在式(3)化合物与用于除去r1和r2位的胺基保护基团的一种或更多种试剂的反应已进行了足够的时间量(例如,直至反应基本上完成,即直至基本上消耗式(3)化合物的全部初始量)之后,添加碱,优选地是为了中和酸。例如,添加这样的量的碱以产生具有去质子化伯胺基(即,在存在酸的情况下,基团
‑
nh2代替质子化基团
‑
nh
3
)的式(4)化合物。碱可以是适合使质子化伯胺基去质子化的任何碱,并且举例说明性的碱包括但不限于naoh、koh、碳酸盐(例如k2co3或cs2co3)、有机胺(例如环胺(例如,1,8
‑
二氮杂双环十一碳
‑7‑
烯(dbu)))、醇盐(这样的叔丁醇钠或叔丁醇钾)、胺盐(例如二异丙基氨基锂(lda)或四甲基哌啶锂(litmp))、或基于硅的酰胺(例如双(三甲基甲硅烷基)酰胺钠(nahmds)或双(三甲基甲硅烷基)酰胺钾(khmds))。优选地,与碱的反应在合适的温度下(例如,在标准条件(例如,在25℃)下、在降低的温度(例如
‑
10℃至10℃)下或在升高的温度(例如,在50℃或更高)下进行,例如在0℃至40℃(例如,在0℃至35℃或10℃至30℃))进行;和/或持续足够的时间量(例如,在0.5至5小时,优选1至4.5小时,更优选1.5至4小时,更优选2至3.5小时,更优选2.5至3小时的范围内)。替代地,碱的添加持续到式(4)化合物的质子化伯胺基
‑
nh
3
的去质子化基本上完成,例如直到包含式(4)化合物的反应混合物的ph≥12。
[0139]
在第一方面的方法(特别是如图1a、1b、1c、1d、1e、1f、1g和1h中任一个所指定的本发明方法,或者包括如图3a、3b、3c、3d、3e、3f和3g中任一个所指定的步骤b)的本发明的方法)的任何上述实施方案中,在步骤b)之后并且在添加碱之前,本发明的方法可还包括进行溶剂交换的步骤。对于本发明的方法的该实施方案特别优选地在添加碱之前进行溶剂交换,其中具有去质子化伯胺基的式(4)化合物在溶剂交换之后的溶剂中比在步骤b)使用的溶剂(即在溶剂交换之前的溶剂)中溶解更好。在一个优选实施方案中,在溶剂交换之后的溶剂包含卤化有机溶剂(例如dcm)任选地与水的混合物(例如,5体积份的卤化有机溶剂(例如dcm)和2体积份的水)。在一个实施方案中,在溶剂交换之后,反应混合物基本上不含步骤b)中使用的(即在溶剂交换之前的)溶剂,例如,在溶剂交换之后,反应混合物包含≤1.0重量%的步骤b)中使用的(即在溶剂交换之前的)溶剂。
[0140]
在第一方面的方法(特别是如图1a所指定的本发明方法,或者包括如图3a所指定的步骤b)的本发明的方法)的任何上述实施方案中,在步骤b)之后并且在步骤c)之前,第一方面的方法可还包括使式(4)化合物或其溶剂合物或盐沉淀的步骤。在该实施方案(特别是如图1b、1c、1d、1e、1f、1g和1h中任一个所指定的本发明方法,或者包括如图3b、3c、3d、3e、3f和3g中任一个所指定的步骤b)的本发明的方法)中,使式(4)化合物或其溶剂合物或盐沉淀的步骤可通过向式(4)化合物或其溶剂合物或盐中添加酸,以使式(4)化合物的酸加成盐沉淀来实现。任选地,在添加酸之前或之后进行溶剂交换以增强式(4)化合物的酸加成盐的沉淀。优选地,在溶剂交换之后的溶剂是具有去质子化伯胺基的式(4)化合物可溶于其中的溶剂。还优选地,在溶剂交换之后,反应混合物基本上不含在发生溶剂交换之前存在的溶剂,例如,在溶剂交换之后,反应混合物包含≤1.0重量%的在发生溶剂交换之前存在的溶剂。在一个实施方案中,向式(4)化合物或其溶剂合物或盐中添加的以使式(4)化合物的酸加成盐沉淀的酸是有机酸,例如有机二酸,例如草酸、丙二酸、琥珀酸、戊二酸、己二酸、马来酸、富马酸或戊烯二酸,优选富马酸。在一个实施方案(特别是如图1d、1e、1f、1g和1h中任一个所指定的本发明方法,或者包括如图3c、3d、3e、3f和3g中任一个所指定的步骤b)的本发明的方法的实施方案)中,在溶剂交换之后的溶剂是醇溶剂,例如甲醇、乙醇、1
‑
丙醇或2
‑
丙醇,优选乙醇。优选地(特别是在如图1d、1e、1f、1g和1h中任一个所指定的本发明方法,或者包括如图3c、3d、3e、3f和3g中任一个所指定的步骤b)的本发明的方法的该实施方案中),式(4)化合物的酸加成盐的沉淀在合适的温度(例如0℃至40℃,例如10℃至30℃或15℃至25℃)下进行和/或持续足够的时间量(例如,2至20小时,优选4至18小时,更优选6至16小时,更优选8至14小时,更优选10至13小时的范围内)。在一个实施方案中(特别是在如图1d、1e、1f、1g和1h中任一个所指定的本发明方法,或者包括如图3c、3d、3e、3f和3g中任一个所指定的步骤b)的本发明的方法的该实施方案中),收集(例如通过过滤)经沉淀的式(4)化合物的酸加成盐,任选地洗涤(例如,用式(4)化合物的酸加成盐在其中难溶或不溶的溶剂(例如,醚溶剂,例如叔丁基甲基醚))并且任选地干燥(例如,在合适的温度下(例如30℃至50℃,优选40℃至45℃)和/或持续足够的时间量(例如4至20小时,例如6至18小时、8至16小时、8至15小时或10至13小时的范围内)),其中任选的洗涤和/或干燥可在惰性气氛(例如氮气)下进行。
[0141]
在第一方面的方法的步骤c)中,使式(4)化合物或其溶剂合物或盐与用于引入(i)四氢吡喃基和(ii)乙酰基的一种或更多种试剂反应以产生式(5)化合物或其溶剂合物或
盐:
[0142][0143]
因此,换言之,在步骤c)中,伯胺基转化为带有四氢吡喃基和乙酰基的叔胺基。
[0144]
在第一方面的方法(特别是如图1d、1e、1f、1g和1h中任一个所指定的本发明方法,或者包括如图4c、4d、4e、4f、4g和4h中任一个所指定的步骤c)的本发明的方法)的任何上述实施方案中,其中在步骤c)中式(4)化合物为酸加成盐的形式,优选地,式(4)化合物的酸加成盐转化为具有去质子化伯胺基的式(4)化合物,然后与用于引入四氢吡喃基和乙酰基的一种或更多种试剂反应。为此,可将酸加成盐形式的式(4)化合物溶解于酸加成盐可溶于其中的溶剂(例如卤化有机溶剂,例如dcm)中,添加水性碱(例如,水性碱),并收集包含具有去质子化伯胺基的式(4)化合物的有机相。碱可以是适合使质子化伯胺基去质子化的任何碱,并且举例说明性的碱包括但不限于naoh、koh、碳酸盐(例如k2co3或cs2co3)、有机胺(例如环胺(例如,1,8
‑
二氮杂双环十一碳
‑7‑
烯(dbu)))、醇盐(这样的叔丁醇钠或叔丁醇钾)、胺盐(例如二异丙基氨基锂(lda)或四甲基哌啶锂(litmp))、或基于硅的酰胺(例如双(三甲基甲硅烷基)酰胺钠(nahmds)或双(三甲基甲硅烷基)酰胺钾(khmds))。优选地,与碱的反应在合适的温度下(例如,在标准条件(例如,在25℃)下、在降低的温度(例如
‑
10℃至10℃)下或在升高的温度(例如,在50℃或更高)下进行,例如在0℃至40℃(例如,在0℃至35℃或10℃至30℃))进行;和/或持续足够的时间量(例如,在0.5至5小时,优选1至4.5小时,更优选1.5至4小时,更优选2至3.5小时,更优选2.5至3小时的范围内)。替代地,碱的添加持续到式(4)化合物的质子化伯胺基
‑
nh
3
的去质子化基本上完成,例如直到包含式(4)化合物的反应混合物的ph≥12。
[0145]
在第一方面的方法(特别是如图1a、1b、1c、1d和1e中任一个所指定的本发明方法,或者包括如图4a、4b、4c、4d、4e和4f中任一个所指定的步骤c)的本发明的方法)的任何上述实施方案中,在步骤c)中用于引入四氢吡喃基的一种或更多种试剂可以是四氢吡喃酮和还原剂。还原剂可以是适合于进行还原胺化反应的任何还原剂,例如硼氢化物,例如三乙酰氧基硼氢化钠(stab)。在第一方面的方法(特别是如图1a、1b、1c、1d、1e、1f、1g和1h中任一个所指定的本发明方法,或者包括如图4a、4b、4c、4d、4e、4f、4g和4h中任一个所指定的步骤c)的本发明的方法)的一个实施方案中,相对于1当量的式(4)化合物,四氢吡喃酮的量为0.90至1.5当量(例如0.95至1.4当量、1.00至1.3当量、1.05至1.25当量、1.1至1.20当量)。优选地,相对于1当量的式(4)化合物,还原剂的量在1.0至2.5当量(例如1.1至2.4当量、1.2至2.3当量、1.3至2.2当量、1.4至2.1当量、1.5至2.0当量、1.6至1.9当量、1.7至1.8当量)的范围内。
[0146]
在第一方面的方法(特别是如图1a、1b、1c、1d、1e、1f、1g和1h中任一个所指定的本发明方法,或者包括如图4a、4b、4c、4d、4e、4f、4g和4h中任一个所指定的步骤c)的本发明的
方法)的任何上述实施方案中,在步骤c)中,式(4)化合物或其溶剂合物或盐与用于引入四氢吡喃基的一种或更多种试剂的反应可(i)在溶剂中;(ii)在存在酸的情况下;(iii)在合适的温度下;和/或(iv)持续足够的时间量。
[0147]
在第一方面的方法(特别是如图1a、1b、1c、1d、1e、1f、1g和1h中任一个所指定的本发明方法,或者包括如图4a、4b、4c、4d、4e、4f、4g和4h中任一个所指定的步骤c)的本发明的方法)的任何上述实施方案中,在步骤c)中,式(4)化合物或其溶剂合物或盐与用于引入四氢吡喃基的一种或更多种试剂的反应可在溶剂中进行,特别是在式(4)化合物或其溶剂合物或盐可溶于其中的溶剂(例如卤化有机溶剂,例如dcm)中进行。相对于1重量份的式(4)化合物,用于该反应的溶剂的量可以是2至20体积份(例如3至18体积份、4至16体积份、6至14体积份、8至12体积份、9至10体积份)。
[0148]
在第一方面的方法(特别是如图1a、1b、1c、1d、1e、1f、1g和1h中任一个所指定的本发明方法,或者包括如图4a、4b、4c、4d、4e、4f、4g和4h中任一个所指定的步骤c)的本发明的方法)的任何上述实施方案中,在步骤c)中,式(4)化合物或其溶剂合物或盐与用于引入四氢吡喃基的一种或更多种试剂的反应可在存在酸,例如无机酸或有机酸,例如乙酸的情况下进行。相对于1当量的式(4)化合物,用于该反应的酸的量可以是0.85至1.4当量(例如0.90至1.3当量、0.95至1.2当量、1.00至1.1当量)。
[0149]
在第一方面的方法(特别是如图1a、1b、1c、1d、1e、1f、1g和1h中任一个所指定的本发明方法,或者包括如图4a、4b、4c、4d、4e、4f、4g和4h中任一个所指定的步骤c)的本发明的方法)的任何上述实施方案中,在步骤c)中,式(4)化合物或其溶剂合物或盐与用于引入四氢吡喃基的一种或更多种试剂的反应可在合适的温度下进行,例如在标准条件(例如,在25℃)下、在降低的温度(例如
‑
10℃至10℃)下或在升高的温度(例如,在50℃或更高)下进行。示例性温度范围为
‑
20℃至40℃(例如,
‑
15℃至30℃或
‑
10℃至25℃)。
[0150]
在第一方面的方法(特别是如图1a、1b、1c、1d、1e、1f、1g和1h中任一个所指定的本发明方法,或者包括如图4a、4b、4c、4d、4e、4f、4g和4h中任一个所指定的步骤c)的本发明的方法)的任何上述实施方案中,在步骤c)中,式(4)化合物或其溶剂合物或盐与用于引入四氢吡喃基的一种或更多种试剂的反应可持续足够的时间量,例如在5小时至24小时,例如7小时至23小时、9小时至21小时、11小时至20小时、13小时至19小时或15小时至18小时的范围内。替代地,式(4)化合物或其溶剂合物或盐与用于引入四氢吡喃基的一种或更多种试剂的反应可进行直至反应基本上完成,即直至基本上消耗式(4)化合物的全部初始量(例如,≥初始量的99.5%)。
[0151]
在第一方面的方法(特别是如图1a、1b、1c、1d、1e、1f、1g和1h中任一个所指定的本发明方法,或者包括如图4a、4b、4c、4d、4e、4f、4g和4h中任一个所指定的步骤c)的本发明的方法)的任何上述实施方案中,优选地,在式(4)化合物或其溶剂合物或盐与用于引入四氢吡喃基的一种或更多种试剂已反应之后(例如,在所述反应基本上完成之后),添加碱(例如水性碱(例如naoh水溶液)以淬灭该反应。此后,有机相可与水相分离,任选地洗涤,使用固体干燥剂(例如固体mgso4)干燥,和/或浓缩(例如,在减压下)。
[0152]
在第一方面的方法(特别是如图1a、1b、1c、1d和1e中任一个所指定的本发明方法,或者包括如图4a、4b、4c、4d、4e、4f和4g中任一个所指定的步骤c)的本发明的方法)的任何上述实施方案中,在步骤c)中,用于引入乙酰基的一种或更多种试剂可选自乙酸酐和乙酸
卤化物。在一个实施方案中,相对于1当量的式(4)化合物,用于引入乙酰基的一种或更多种试剂的量为0.80至1.5当量(例如0.85至1.4当量、0.90至1.3当量、0.95至1.2当量、1.00至1.1当量)。
[0153]
在第一方面的方法(特别是如图1a、1b、1c、1d、1e、1f、1g和1h中任一个所指定的本发明方法,或者包括如图4a、4b、4c、4d、4e、4f、4g和4h中任一个所指定的步骤c)的本发明的方法)的任何上述实施方案中,在步骤c)中,式(4)化合物或其溶剂合物或盐与用于引入乙酰基的一种或更多种试剂的反应可(i)在溶剂中进行;(ii)在合适的温度下进行;和/或(iii)持续足够的时间量。
[0154]
在第一方面的方法(特别是如图1a、1b、1c、1d、1e、1f、1g和1h中任一个所指定的本发明方法,或者包括如图4a、4b、4c、4d、4e、4f、4g和4h中任一个所指定的步骤c)的本发明的方法)的任何上述实施方案中,在步骤c)中,式(4)化合物或其溶剂合物或盐与用于引入乙酰基的一种或更多种试剂的反应可在溶剂中进行,特别是在式(4)化合物或其溶剂合物或盐可溶于其中的溶剂(例如,在用于引入四氢吡喃基的反应中使用的溶剂,例如卤化有机溶剂,例如dcm)中进行。相对于1重量份的式(4)化合物,用于该反应的溶剂的量可以是2至20体积份(例如3至18体积份、4至16体积份、6至14体积份、8至12体积份、9至10体积份)。
[0155]
在第一方面的方法(特别是如图1a、1b、1c、1d、1e、1f、1g和1h中任一个所指定的本发明方法,或者包括如图4a、4b、4c、4d、4e、4f、4g和4h中任一个所指定的步骤c)的本发明的方法)的任何上述实施方案中,在步骤c)中,式(4)化合物或其溶剂合物或盐与用于引入乙酰基的一种或更多种试剂的反应可在合适的温度下进行,例如在标准条件(例如,在25℃)下、在降低的温度(例如
‑
10℃至10℃)下或在升高的温度(例如,在50℃或更高)下进行。示例性温度范围为0℃至50℃(例如,10℃至40℃或20℃至30℃)。
[0156]
在第一方面的方法(特别是如图1a、1b、1c、1d、1e、1f、1g和1h中任一个所指定的本发明方法,或者包括如图4a、4b、4c、4d、4e、4f、4g和4h中任一个所指定的步骤c)的本发明的方法)的任何上述实施方案中,在步骤c)中,式(4)化合物或其溶剂合物或盐与用于引入乙酰基的一种或更多种试剂的反应可持续足够的时间量,例如在6小时至48小时,例如8小时至46小时、10小时至44小时、12小时至42小时、14小时至40小时、16小时至38小时、18小时至36小时、20小时至34小时、22小时至32小时或24小时至30小时的范围内。替代地,式(4)化合物或其溶剂合物或盐与用于引入乙酰基的一种或更多种试剂的反应可进行直至反应基本上完成,即直至基本上消耗式(4)化合物的全部初始量(例如,≥初始量的99.5%)。
[0157]
应当理解,在第一方面的方法(特别是如图1a、1b、1c、1d、1e、1f、1g和1h中任一个所指定的本发明方法,或者包括如图4a、4b、4c、4d、4e、4f、4g和4h中任一个所指定的步骤c)的本发明的方法)的任何上述实施方案中,式(4)化合物或其溶剂合物或盐可首先与用于引入四氢吡喃基的一种或更多种试剂反应,随后与用于引入乙酰基的一种或更多种试剂反应。替代地,在第一方面的方法(特别是如图1a、1b、1c、1d、1e、1f、1g和1h中任一个所指定的本发明方法,或者包括如图4a、4b、4c、4d、4e、4f、4g和4h中任一个所指定的步骤c)的本发明的方法)的任何上述实施方案中,式(4)化合物或其溶剂合物或盐可首先与用于引入乙酰基的一种或更多种试剂反应,随后与用于引入四氢吡喃基的一种或更多种试剂反应。因此,在第一方面的方法(特别是如图1a、1b、1c、1d、1e、1f、1g和1h中任一个所指定的本发明方法,或者包括如图4a、4b、4c、4d、4e、4f、4g和4h中任一个所指定的步骤c)的本发明的方法)的任
何上述实施方案的一个模式中,式(4)化合物或其溶剂合物或盐首先与用于引入乙酰基的一种或更多种试剂反应并与用于引入四氢吡喃基的一种或更多种试剂反应。然而,在第一方面的方法(特别是如图1a、1b、1c、1d、1e、1f、1g和1h中任一个所指定的本发明方法,或者包括如图4a、4b、4c、4d、4e、4f、4g和4h中任一个所指定的步骤c)的本发明的方法)的任何上述实施方案的一个替代和优选模式中,式(4)化合物或其溶剂合物或盐首先与用于引入四氢吡喃基的一种或更多种试剂反应,随后与用于引入乙酰基的一种或更多种试剂反应。
[0158]
在第一方面的方法(特别是如图1a、1b、1c、1d、1e、1f、1g和1h中任一个所指定的本发明方法,或者包括如图4a、4b、4c、4d、4e、4f、4g和4h中任一个所指定的步骤c)的本发明的方法)的任何上述实施方案中,优选地,在步骤c)之后,添加碱(优选地,水性碱,这样的碳酸盐(例如na2co3、k2co3、nahco3或khco3)的水溶液),有机相可与水相分离,任选地洗涤,使用固体干燥剂(例如固体mgso4)干燥,和/或浓缩(例如,在减压下和在≤30℃的温度下)。
[0159]
在第一方面的方法(特别是如图1a所指定的本发明方法,或者包括如图4a所指定的步骤c)的本发明的方法)的任何上述实施方案中,在步骤c)之后并且在步骤d)之前,第一方面的方法可还包括使式(5)化合物或其溶剂合物或盐沉淀的步骤。在该实施方案中(特别是如图1b、1c、1d、1e、1f、1g和1h中任一个所指定的本发明方法,或者包括如图4b、4c、4d、4e、4f、4g和4h中任一个所指定的步骤c)的本发明的方法)中,使式(5)化合物或其溶剂合物或盐沉淀的步骤可通过进行溶剂交换来实现。优选地,在溶剂交换之后的溶剂为式(5)化合物或溶剂合物或盐在其中难溶或不溶的溶剂。还优选地,在溶剂交换之后,反应混合物基本上不含在发生溶剂交换之前存在的溶剂,例如,在溶剂交换之后,反应混合物包含≤10重量%(优选≤1.0重量%)的在发生溶剂交换之前存在的溶剂。在一个实施方案(特别是如图1b、1c、1d、1e、1f、1g和1h中任一个所指定的本发明方法,或者包括如图4b、4c、4d、4e、4f、4g和4h中任一个所指定的步骤c)的本发明的方法的一个实施方案)中,在溶剂交换之后的溶剂为醚溶剂,如叔丁基甲基醚。优选地(特别是在如图1b、1c、1d、1e、1f、1g和1h中任一个所指定的本发明方法的一些实施方案中,或者在包括如图4b、4c、4d、4e、4f、4g和4h中任一个所指定的步骤c)的本发明的方法的一些实施方案中),式(5)化合物或溶剂合物或盐的沉淀在合适的温度(例如0℃至40℃,例如10℃至30℃或15℃至25℃)下进行和/或持续足够的时间量(例如,在0.5小时至5小时,优选1至4小时,更优选2至3小时的范围内)。在一个实施方案(特别是如图1b、1c、1d、1e、1f、1g和1h中任一个所指定的本发明方法,或者包括如图4b、4c、4d、4e、4f、4g和4h中任一个所指定的步骤c)的本发明的方法的一个实施方案)中,收集(例如通过过滤)经沉淀的式(5)化合物或溶剂合物或盐,任选地洗涤(例如,用式(5)化合物或溶剂合物或盐的酸加成盐在其中难溶或不溶的溶剂(例如,醚溶剂,例如叔丁基甲基醚))并且任选地干燥(例如,在合适的温度下(例如30℃至50℃之间,优选40℃至45℃)和/或持续足够的时间量(例如4至20小时,例如6至18小时、8至16小时、8至15小时或10至13小时的范围内)),其中任选的洗涤和/或干燥可在惰性气氛(例如氮气)下进行。
[0160]
在第一方面的方法的步骤d)中,使式(5)化合物或其溶剂合物或盐进行氧化胺化反应以得到式(i)化合物或其溶剂合物或盐。在第一方面的方法(特别是如图1a、1b、1c、1d、1e、1f、1g和1h中任一个所指定的本发明方法,或者包括如图5a、5b、5c、5d和5e中任一个所指定的步骤d)的本发明的方法)的任何上述实施方案中,步骤d)可包括使式(5)化合物或其溶剂合物或盐首先与氧化剂反应(为了制备n
‑
氧化物中间体),任选地添加碱(优选地为了
使n
‑
氧化物中间体去质子化),随后使n
‑
氧化物中间体与酰化剂和胺化剂反应。在一个实施方案中,氧化剂选自能够形成n
‑
氧化物的氧化剂(例如过氧化物)。一种合适的氧化剂是3
‑
氯过氧苯甲酸(也称为mcpba)。在一个实施方案(特别是如图1a、1b、1c、1d、1e、1f、1g和1h中任一个所指定的本发明方法,或者包括如图5a、5b、5c、5d和5e中任一个所指定的步骤d)的本发明的方法的一个实施方案)中,相对于1当量的式(5)化合物,氧化剂的量为1.0至2.0当量(例如1.1至1.9当量、1.2至1.8当量、1.3至1.7当量、1.4至1.6当量)的范围内。
[0161]
在第一方面的方法(特别是如图1a、1b、1c、1d、1e、1f、1g和1h中任一个所指定的本发明方法,或者包括如图5a、5b、5c、5d和5e中任一个所指定的步骤d)的本发明的方法)的任何上述实施方案中,式(5)化合物或其溶剂合物或盐与氧化剂的氧化反应可(i)在溶剂中进行;(ii)在合适的温度下进行;和/或(iii)持续足够的时间量。
[0162]
在第一方面的方法(特别是如图1a、1b、1c、1d、1e、1f、1g和1h中任一个所指定的本发明方法,或者包括如图5a、5b、5c、5d和5e中任一个所指定的步骤d)的本发明的方法)的任何上述实施方案中,在步骤d)中,式(5)化合物或其溶剂合物或盐与氧化剂的氧化反应可在溶剂中进行,特别是在式(5)化合物或其溶剂合物或盐可溶于其中的溶剂(例如卤化有机溶剂,例如dcm)中进行。相对于1重量份的式(5)化合物,用于该反应的溶剂的量可以是2至20体积份(例如3至18体积份、4至16体积份、6至14体积份、8至12体积份、9至10体积份)。
[0163]
在第一方面的方法(特别是如图1a、1b、1c、1d、1e、1f、1g和1h中任一个所指定的本发明方法,或者包括如图5a、5b、5c、5d和5e中任一个所指定的步骤d)的本发明的方法)的任何上述实施方案中,在步骤d)中,式(5)化合物或其溶剂合物或盐与氧化剂的氧化反应可在合适的温度下进行,例如在标准条件(例如,在25℃)下、在降低的温度(例如
‑
20℃至10℃)下或在升高的温度(例如,在50℃或更高)下进行。示例性温度范围为
‑
10℃至40℃(例如,0℃至30℃或10℃至25℃)。
[0164]
在第一方面的方法(特别是如图1a、1b、1c、1d、1e、1f、1g和1h中任一个所指定的本发明方法,或者包括如图5a、5b、5c、5d和5e中任一个所指定的步骤d)的本发明的方法)的任何上述实施方案中,在步骤d)中,式(5)化合物或其溶剂合物或盐与氧化剂的氧化反应可持续足够的时间量,例如持续在0.5小时至12小时,例如1小时至11小时、2小时至10小时、3小时至9小时,4小时至8小时,或5小时至7小时的范围内的时间量。替代地,式(5)化合物或其溶剂合物或盐与氧化剂的氧化反应可进行直至反应基本上完成,即直至基本上消耗式(5)化合物的全部初始量(例如,≥初始量的96%)。
[0165]
在第一方面的方法(特别是如图1a、1b、1c、1d和1e中任一个所指定的本发明方法,或者包括如图5a、5b和5c中任一个所指定的步骤d)的本发明的方法)的任何上述实施方案中,在步骤d)中,酰化剂可选自烷基磺酰卤化物和芳基磺酰卤化物。在这方面可使用的示例性酰化剂包括甲磺酰氯、苯磺酰氯和对甲苯磺酰氯。在一个实施方案(特别是如图1a、1b、1c、1d、1e、1f、1g和1h中任一个所指定的本发明方法,或者包括如图5a、5b、5c、5d和5e中任一个所指定的步骤d)的本发明的方法的一个实施方案)中,相对于1当量的式(5)化合物的n
‑
氧化物中间体,使用的酰化剂的量在1.0至2.0当量(例如1.1至1.9当量、1.2至1.8当量、1.3至1.7当量、1.4至1.6当量)的范围内。
[0166]
在第一方面的方法(特别是如图1a、1b、1c、1d和1e中任一个所指定的本发明方法,或者包括如图5a、5b和5c中任一个所指定的步骤d)的本发明的方法)的任何上述实施方案
中,在步骤d)中,胺化剂可选自氨及其盐,例如氨水、氢氧化铵、碳酸铵、碳酸氢铵或磷酸铵。在一个实施方案(特别是如图1a、1b、1c、1d、1e、1f、1g和1h中任一个所指定的本发明方法,或者包括如图5a、5b、5c、5d和5e中任一个所指定的步骤d)的本发明的方法)中,相对于1当量的式(5)化合物的n
‑
氧化物中间体,使用的胺化剂的量在1.0至4.0当量(例如1.5至3.5当量、2.0至3.0当量)的范围内。
[0167]
在第一方面的方法(特别是如图1a、1b、1c、1d、1e、1f、1g和1h中任一个所指定的本发明方法,或者包括如图5a、5b、5c、5d和5e中任一个所指定的步骤d)的本发明的方法)的任何上述实施方案中,在步骤d)中,式(5)化合物的n
‑
氧化物中间体与酰化剂和胺化剂的反应可(i)在溶剂中;(ii)在合适的温度下;和/或(iii)持续足够的时间量。
[0168]
在第一方面的方法(特别是如图1a、1b、1c、1d、1e、1f、1g和1h中任一个所指定的本发明方法,或者包括如图5a、5b、5c、5d和5e中任一个所指定的步骤d)的本发明的方法)的任何上述实施方案中,在步骤d)中,式(5)化合物的n
‑
氧化物中间体与酰化剂和胺化剂的反应可在溶剂中进行,特别是在式(5)化合物的n
‑
氧化物中间体可溶于其中的溶剂(例如卤化有机溶剂,例如dcm)中进行。相对于1重量份的式(5)化合物或式(5)化合物的n
‑
氧化物中间体,用于该反应的溶剂的量可以是2至20体积份(例如3至18体积份、4至16体积份、6至14体积份、8至12体积份、9至10体积份)。
[0169]
在第一方面的方法(特别是如图1a、1b、1c、1d、1e、1f、1g和1h中任一个所指定的本发明方法,或者包括如图5a、5b、5c、5d和5e中任一个所指定的步骤d)的本发明的方法)的任何上述实施方案中,在步骤d)中,式(5)化合物的n
‑
氧化物中间体与酰化剂和胺化剂的反应可在合适的温度下进行,例如在标准条件(例如,在25℃)下、在降低的温度(例如
‑
20℃至10℃)下或在升高的温度(例如,在50℃或更高)下进行。示例性温度范围为
‑
10℃至40℃(例如,0℃至30℃或10℃至25℃)。
[0170]
在第一方面的方法(特别是如图1a、1b、1c、1d、1e、1f、1g和1h中任一个所指定的本发明方法,或者包括如图5a、5b、5c、5d和5e中任一个所指定的步骤d)的本发明的方法)的任何上述实施方案中,在步骤d)中,式(5)化合物的n
‑
氧化物中间体与酰化剂和胺化剂的反应可持续足够的时间量,例如持续在0.5小时至12小时,例如1小时至11小时、2小时至10小时、3小时至9小时,4小时至8小时,或5小时至7小时的范围内的时间量。替代地,式(5)化合物的n
‑
氧化物中间体与酰化剂和胺化剂的反应可进行直至反应基本上完成,即直至基本上消耗式(5)化合物或式(5)化合物的n
‑
氧化物中间体的全部初始量(例如,≥初始量的99.5%)。
[0171]
在第一方面的方法(特别是如图1a、1b、1c、1d、1e、1f、1g和1h中任一个所指定的本发明方法,或者包括如图5a、5b、5c、5d和5e中任一个所指定的步骤d)的本发明的方法)的任何上述实施方案中,在步骤d)之后,即在式(5)化合物的n
‑
氧化物中间体与酰化剂和胺化剂的反应发生之后,可将包含式(i)化合物的有机相与水相分离,任选地洗涤,使用固体干燥剂(例如固体mgso4)干燥,和/或浓缩(例如,在减压下)。
[0172]
在第一方面的方法(特别是如图1a所指定的本发明方法,或者包括如图6a所指定的步骤的本发明的方法)的任何上述实施方案中,在步骤d)之后,第一方面的方法可还包括使式(i)化合物或其溶剂合物或盐沉淀的步骤。在该实施方案中(特别是如图1b、1c和1d中任一个所指定的本发明方法,或者包括如图6b和6c中任一个所指定的步骤的本发明的方法)中,使式(5)化合物或其溶剂合物或盐沉淀的步骤可通过进行溶剂交换来实现。优选地
(特别是在如图1e、1f、1g和1h中任一个所指定的本发明方法的一些实施方案中,或者在包括如图6d所指定的步骤的本发明的方法的一些实施方案中),在溶剂交换之后的溶剂为式(i)化合物或溶剂合物或盐在其中难溶或不溶的溶剂。还优选地(特别是在如图1e、1f、1g和1h中任一个所指定的本发明方法的一些实施方案中,或者在包括如图6d所指定的步骤的本发明的方法的一些实施方案中),在溶剂交换之后,反应混合物基本上不含在发生溶剂交换之前存在的溶剂,例如,在溶剂交换之后,反应混合物包含≤1.0重量%的在发生溶剂交换之前存在的溶剂。在一个实施方案(特别是如图1e、1f、1g和1h中任一个所指定的本发明方法,或者包括如图6d所指定的步骤的本发明的方法的一个实施方案)中,在溶剂交换之后的溶剂是醇溶剂,例如2
‑
丙醇。优选地(特别是在如图1b、1c、1d、1e、1f、1g和1h中任一个所指定的本发明方法的一些实施方案中,或者在包括如图6b、6c和6d中任一个所指定的步骤的本发明的方法的一些实施方案中),式(i)化合物或溶剂合物或盐的沉淀在合适的温度(例如0℃至40℃,例如10℃至30℃或15℃至25℃)下和/或持续足够的时间量(例如,在0.5小时至5小时,优选1至4小时,更优选2至3小时的范围内)而进行。在一个实施方案(特别是如图1b、1c、1d、1e、1f、1g和1h中任一个所指定的本发明方法,或者在包括如图6b、6c和6d中任一个所指定的步骤的本发明的方法的一个实施方案)中,收集(例如通过过滤)经沉淀的式(i)化合物或溶剂合物或盐,任选地洗涤(例如,用经沉淀的式(i)化合物或溶剂合物或盐在其中难溶或不溶的溶剂(例如,醚溶剂,例如叔丁基甲基醚))并且任选地干燥(例如,在合适的温度下(例如30℃至50℃之间,优选40℃至45℃)和/或持续足够的时间量(例如4至20小时,例如6至18小时、8至16小时、8至15小时或10至13小时的范围内)),其中任选的洗涤和/或干燥可在惰性气氛(例如氮气)下进行。
[0173]
在第一方面的方法(特别是如图1a所指定的本发明方法,或者在包括如图6a所指定的步骤的本发明的方法的一些实施方案中)的任何上述实施方案中,在步骤d)之后或在式(i)化合物或其溶剂合物或盐沉淀之后,第一方面的方法可还包括使式(i)化合物或其溶剂合物或盐结晶,例如从醇溶剂,优选水性醇溶剂中结晶的步骤。优选地,在该结晶步骤中使用的醇溶剂,优选水性醇溶剂是式(i)化合物或其溶剂合物或盐至少在升高的温度(例如,60℃至80℃,例如65℃至70℃)下可溶于其中的溶剂。为此,示例性醇溶剂,优选水性醇溶剂选自甲醇、乙醇、1
‑
丙醇、2
‑
丙醇,以及其与水的混合物,例如在乙醇中5%的水。
[0174]
在一个模式中(特别是在如图1b、1c、1d、1e、1f、1g和1h中任一个所指定的本发明方法的一些实施方案中,或者在包括如图6b、6c和6d中任一个所指定的步骤的本发明的方法的一些实施方案中),式(i)化合物或其溶剂合物或盐的结晶包括将从步骤d)获得的式(i)化合物或其溶剂合物或盐在合适的温度(例如,60℃至80℃,例如65℃至70℃)下溶解于醇溶剂,优选水性醇溶剂中;在合适的时间段(例如,2小时至5小时,例如2.5小时至3.5小时)内降低温度(例如降低约20℃,优选地降低至40℃至60℃,例如45℃至50℃);任选地添加式(i)化合物或其溶剂合物或盐的晶种;任选地进一步降低温度(例如,降低至
‑
5℃至10℃,例如0℃至5℃);收集固体(即,式(i)化合物或其溶剂合物或盐);任选地用合适的溶剂(例如,式(i)化合物或其溶剂合物或盐在其中难溶或不溶的溶剂,例如醚溶剂,例如叔丁基甲基醚)洗涤固体,其中任选的洗涤优选在不使用氮气层的情况下进行;任选地干燥(例如,在合适的温度(例如30℃至50℃,优选35℃至40℃)下和/或持续足够的时间量(例如在4至70小时,例如6至60小时、8小时至50小时、10小时至40小时或12小时至30小时的范围内));
并且任选地重复使式(i)化合物或其溶剂合物或盐结晶。
[0175]
在第一方面的方法(特别是如图1a、1b、1c、1d、1e、1f、1g和1h中任一个所指定的本发明方法,或者包括(1)如图2a、2b、2c和2d中任一个所指定的步骤a)、(2)如图3a、3b、3c、3d、3f和3g中任一个所指定的步骤b)、(3)如图4a、4b、4c、4d、4e、4f、4g和4h中任一个所指定的步骤c)、(4)如图5a、5b、5c、5d和5e中任一个所指定的步骤d)、和/或(5)如图6a、6b、6c和6d中任一个所指定的步骤的本发明的方法),优选地,步骤a)至d)中的一个或更多个(例如,步骤a)、步骤b)、步骤c)、或步骤d);或者步骤a)和b)、步骤a)和c)、步骤a)和d)、步骤b)和c)、步骤b)和d)、或步骤c)和d);或者步骤a)、b)和c),步骤a)、b)和d),或步骤b)、c)和d);或者步骤a)、b)、c)和d))或所有步骤(即第一方面的全部方法)以无色谱的方式进行。换言之,优选地,在第一方面的方法(特别是如图1a、1b、1c、1d、1e、1f、1g和1h中任一个所指定的本发明方法,或者包括(1)如图2a、2b、2c和2d中任一个所指定的步骤a)、(2)如图3a、3b、3c、3d、3f和3g中任一个所指定的步骤b)、(3)如图4a、4b、4c、4d、4e、4f、4g和4h中任一个所指定的步骤c)、(4)如图5a、5b、5c、5d和5e中任一个所指定的步骤d)、和/或(5)如图6a、6b、6c和6d中任一个所指定的步骤的本发明的方法)的步骤a)至d)中的一个或更多个中,目的化合物(即,式(i)化合物或其溶剂合物或盐或者式(3)、(4)和(5)中任一种的中间体)相对于其他化合物(例如污染物)的分离是通过色谱以外的方式,优选通过使目的化合物沉淀,任选地用合适的溶剂(特别是目的化合物在其中难溶的溶剂)洗涤经沉淀的目的化合物,并任选地干燥经沉淀的目的化合物的方式完成的。因此,优选地,第一方面的方法的涉及制备目的化合物的那些步骤(即制备步骤)在不使用色谱的情况下进行,而第一方面的方法的涉及对目的化合物和/或其污染物的分析的任选步骤(即分析步骤)可使用色谱进行。
[0176]
特别地,本发明人发现可在第一方面的方法的制备步骤中避免色谱并且通过使用替代方式,特别是沉淀目的化合物(即,式(i)化合物或其溶剂合物或盐或者式(3)、(4)和(5)中任一种的中间体)的方式,可获得更大规模、更高收率和类似于通过使用数个色谱纯化步骤的用于合成n
‑
(4
‑
(4
‑
氨基
‑2‑
(2
‑
甲氧基乙基)
‑
1h
‑
咪唑并[4,5
‑
c]喹啉
‑1‑
基)丁基)
‑
n
‑
(四氢
‑
2h
‑
吡喃
‑4‑
基)乙酰胺的比较方法获得的纯度的式(i)化合物或其溶剂合物或盐。
[0177]
在第二方面中,本发明提供了化合物及其溶剂合物或盐,所述化合物选自以下:
[0178][0179]
这些化合物是可用于第一方面的方法的中间体。
[0180]
在第三方面中,本发明提供了第二方面的化合物用于合成式(i)化合物的用途。在这个方面中,应注意,上文针对第一方面指定的实施方案同样适用于第三方面。因此,例如,
在第三方面的一个实施方案中,使式(5)化合物或其溶剂合物或盐进行氧化胺化反应以得到式(i)化合物或其溶剂合物或盐,并且,任选地,使式(i)化合物或溶剂合物或盐结晶,优选从醇溶剂中结晶。
[0181]
实施例
[0182]
缩写
[0183]
在整个说明书中使用以下缩写:sm:用于相应合成步骤的起始材料;ipc:过程控制;dcm:二氯甲烷;tbme:叔丁基甲基醚;meoh: 甲醇;etoh:乙醇;hcl:盐酸;naoh:氢氧化钠;ac2o:乙酸酐;hplc:高效液相色谱;lod:干燥失重;ipa:2
‑
丙醇;ptscl或tscl:对甲苯磺酰氯;ptsa:对甲苯磺酸;stab:三乙酰氧基硼氢化钠;eq.:当量;vol.:体积;nmr:核磁共振;ppm:百万分之;thp:四氢吡喃基;ac2o:乙酸酐;mcpba:3
‑
氯过氧苯甲酸。
[0184]
实施例1
‑
使用本发明的方法合成n
‑
(4
‑
(4
‑
氨基
‑2‑
(2
‑
甲氧基乙基)
‑
1h
‑
咪唑并[4,5
‑
c]喹啉
‑1‑
基)丁基)
‑
n
‑
(四氢
‑
2h
‑
吡喃
‑4‑
基)乙酰胺
[0185]
步骤a):提供式(3)化合物
[0186]
将化合物1(1当量)、对甲苯磺酸一水合物(0.05当量)和甲苯(10体积)装入反应器。在添加1,1,1,3
‑
四甲氧基丙烷(1.2当量)之后,将反应器的内容物调节至在约95℃回流并且使用hplc监测化合物1的含量。
[0187]
步骤b):制备式(4)化合物
[0188]
当化合物1的含量下降至初始面积的≤1.0%面积(通过hplc确定)时,将反应器的内容物调节至10℃至15℃,向反应器中添加6n hcl(5体积)超过约1小时,从而维持温度≤25℃。将反应器的内容物在20℃至25℃下搅拌至少2小时,并通过hplc监测反应完成。收集包含所期望产物的下部水层,排出上部有机层,将收集的包含所期望产物的水层转移至反应器中,添加dcm(5体积),将反应混合物搅拌15分钟并允许静置15分钟。排出下部有机层,将水(2体积)添加至反应器,并将反应器的内容物调节至0℃至5℃。将naoh(11当量)分批添加至反应器,同时维持温度≤30℃。在将反应混合物的ph调节至≥12之后,将反应混合物的温度提高至20℃至25℃,添加dcm(5体积),并将反应混合物搅拌15分钟并允许静置15分钟。收集包含所期望产物的下部有机层,添加dcm(5体积),并将反应混合物搅拌15分钟并允许静置15分钟。收集包含产物的下部有机层,排出上部水层,并在反应器中组合2次收集的有机层。将溶剂进行交换为乙醇,直到反应混合物中dcm的量≤1%。确定化合物4的量,添加富马酸(1当量,其基于确定的化合物4的量),并将反应混合物在20℃至25℃下搅拌至少12小时以沉淀富马酸加成盐形式的式(4)化合物。在至少30分钟内添加tbme(10体积)并将反应混合物在20℃至25℃下搅拌1至2小时。在氮气下使用过滤收集沉淀物,用tbme(2
×
3体积)洗涤反应器,并使用该洗涤溶液在氮气下洗涤沉淀物。将收集的沉淀物在40℃至45℃下干燥至少12小时。
[0189]
表1
[0190]
输入输出产率通过hplc的纯度7.30kg8.50kg92%95.428%面积
[0191]
步骤c):制备式(5)化合物
[0192]
将从步骤b)获得的富马酸加成盐形式的化合物4(1当量)、dcm(5体积)和2m naoh(10体积)添加至反应器,并将反应混合物搅拌15分钟并允许静置15分钟。收集包含游离碱
形式的化合物4的下部有机层,用dcm(5体积)萃取水相,并收集下部有机层。在排出上部水层之后,将2次的有机层装入反应器中,将mgso4(0.2重量%)添加至反应器,搅拌反应混合物5分钟并过滤反应器中内容物以除去mgso4。将滤液装入新的干净的反应器中,添加四氢吡喃酮(1.1当量)和乙酸(1当量),将反应混合物的温度调节至
‑
10℃至0℃。分批添加stab(1.8当量),同时维持温度≤0℃。在添加完成之后,将温度提高至20℃至25℃,将反应混合物搅拌至少18小时,并通过hplc监测反应完成。一旦化合物4靶标的含量≤初始面积的0.50%,则将反应混合物冷却至10℃至15℃并通过添加2m naoh(10体积)缓慢地进行淬灭,同时维持温度≤25℃。在naoh添加完成之后,将反应混合物搅拌15分钟并允许静置15分钟。收集包含所期望产物的下部有机层,用dcm(10体积)萃取上部水层,收集包含所期望产物的下部有机层,并排出上部水层。将mgso4(0.2重量%)添加至反应器并将2次的有机层装入反应器中并且将反应混合物搅拌至少15分钟。通过过滤除去mgso4并用dcm(1体积)洗涤mgso4饼(mgso4cake)。滤液在干净的反应器中组合并且在减压下在35℃至40℃下降低至约10至12体积。将反应混合物的温度调节至20℃至25℃,缓慢添加乙酸酐(1当量)同时维持温度为20℃至30℃。在添加完成之后,将反应混合物的温度调节至20℃至25℃,将反应混合物搅拌至少24小时,并且使用hplc监测四氢吡喃基加合物和stab的含量。一旦四氢吡喃基加合物和stab各自的含量≤初始面积的0.50%,则反应通过添加5%nahco3溶液(10体积)缓慢地进行淬灭,并且将反应搅拌15分钟并允许静止15分钟。收集包含所期望产物的下部有机层并装入干净的反应器中。添加mgso4(0.2重量%),将反应混合物搅拌至少15分钟,随后过滤以除去mgso4。用dcm(1体积)洗涤反应器并且该洗涤溶液用于漂洗mgso4饼。将滤液重新装入干净的反应器中并在减压下在≤30℃下降低至6至7体积。将溶剂进行交换为tbme,直到反应混合物中dcm的含量≤10%。随后,添加tbme(3体积),将反应混合物的温度调节至20℃至25℃,并将反应混合物搅拌至少1小时。在氮气下过滤悬浮液,并用tbme(2
×
2体积)洗涤反应器和滤饼。将收集的沉淀物在35℃至40℃下干燥至少12小时。
[0193]
表2
[0194]
输入输出产率通过hplc的纯度8.40kg6.41kg74%94.88%面积
[0195]
步骤d):制备式(i)化合物
[0196]
将从步骤c)获得的化合物5(1当量)装入反应器中,添加dcm(10体积),并将反应混合物的温度调节至
‑
10℃至0℃。将70%mcpba(1.5当量)分批添加至反应器,同时维持温度≤0℃。在添加完成之后,将反应混合物的温度调节至20℃至25℃,将反应混合物搅拌至少2小时,并使用hplc监测反应混合物中化合物5的含量。一旦反应混合物中化合物5的含量≤初始量的4%,则将反应混合物的温度调节至0℃至5℃,并且添加氢氧化铵(10体积)同时维持温度≤20℃。在添加完成之后,将反应混合物的温度调节至0℃至5℃。将溶解在dcm(3体积)中的ptscl(1.5当量)缓慢添加至反应器,同时维持温度≤10℃。在添加完成之后,将反应混合物的温度调节至20℃至25℃,将反应混合物搅拌至少2小时,并使用hplc监测反应混合物中n
‑
氧化物中间体的含量。一旦反应混合物中n
‑
氧化物中间体的含量≤初始量的0.5%,则将反应混合物的温度调节至30℃至35℃并将反应混合物搅拌至少2小时。将反应混合物的温度调节至20℃至25℃,收集包含所期望产物的下部有机层,装入干净的反应器中,添加mgso4(0.2重量%),并将反应混合物搅拌至少15分钟。过滤反应混合物以除去
mgso4,用dcm(1体积)洗涤反应器并且该洗涤溶液用于漂洗mgso4饼。滤液在干净的反应器中组合并在减压下在35℃至40℃下降低至约10体积,并且确定所得溶液中式(i)化合物的含量。
[0197]
表3
[0198]
输入输出产率6.35kg7.7kg*113%
[0199]
步骤e):沉淀式(i)化合物
[0200]
将从步骤d)获得的式(i)化合物(1当量)的粗制溶液装入反应器中。将溶剂进行交换为ipa,直到反应混合物中dcm的含量≤1%。随后,将反应混合物的温度调节至5℃至10℃并将反应混合物搅拌至少1小时。过滤悬浮液,用ipa(2体积)洗涤反应器,将洗涤溶液冷却至5℃至10℃随后用于漂洗滤饼。用tbme(2
×
5体积)洗涤反应器并将每种洗涤溶液用于漂洗滤饼。收集的沉淀物在35℃至40℃下干燥至少12小时
[0201]
表4
[0202]
输入输出产率通过hplc的纯度3.00kg1.62kg54%*96.18%面积3.00kg1.70kg57%*未进行第4步
[0203]
*典型产率。当输入是粗制产品时,预期产率=45至60%理论值。
[0204]
步骤f):式(i)化合物的结晶
[0205]
将在乙醇中5%的水(10体积)装入反应器中并且添加从步骤e)获得的式(i)化合物(1当量)。将反应混合物的温度调节至65℃至70℃并保持30分钟至1小时。一旦所有的式(i)化合物溶解,则过滤溶液并将滤液装入预热至65℃至70℃的干净的反应器中。在3小时
±
30分钟内将溶液的温度调节至45℃至50℃。添加式(i)化合物的晶种,在至少7小时内将反应混合物的温度调节至0℃至5℃,并将反应混合物在0℃至5℃下搅拌至少2小时。过滤悬浮液,用在乙醇中5%的水(2体积)洗涤反应器,将洗涤溶液的温度调节至0℃至5℃并用于漂洗滤饼。用tbme(2体积)洗涤反应器,并将洗涤溶液用于漂洗滤饼。任选地,重复结晶步骤。
[0206]
表5
[0207]
输入输出产率通过hplc的纯度1.60kg1.19kg71%99.0%面积
[0208]
本发明的方法的总产率、通过所述方法产生的式(i)化合物的量以及合成所需的时间在下表6中给出。
[0209]
实施例2
‑
使用色谱纯化步骤(比较方法b)比较合成n
‑
(4
‑
(4
‑
氨基
‑2‑
(2
‑
甲氧基乙基)
‑
1h
‑
咪唑并[4,5
‑
c]喹啉
‑1‑
基)丁基)
‑
n
‑
(四氢
‑
2h
‑
吡喃
‑4‑
基)乙酰胺
[0210]
n
‑
(4
‑
(4
‑
氨基
‑2‑
(2
‑
甲氧基乙基)
‑
1h
‑
咪唑并[4,5
‑
c]喹啉
‑1‑
基)丁基)
‑
n
‑
(四氢
‑
2h
‑
吡喃
‑4‑
基)乙酰胺根据图11中所示的方法制备,该方法类似于本发明的方法,但其使用3个色谱纯化步骤(一个在除去boc保护基团之后;一个在与四氢吡喃酮反应之后;以及一个在氧化胺化之后)。比较方法b的总产率、通过所述方法产生的式(i)化合物的量以及合成所需的时间在下表6中给出。
[0211]
表6
[0212] 本发明的方法比较方法b总产率31%11%色谱纯化03产生的量1.19kg10.42g纯度99.0%99.5%时间7.5周5周
[0213]
从表6中存在的结果可看出,本发明的方法提供了比比较方法b更高的产率,并且能够以比比较方法b高得多的量(约1.2kg vs.约10g,即多于102倍),并且以与通过使用比较方法b获得的纯度相当的纯度来提供式(i)化合物。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。

