针对降钙素基因相关肽(cgrp)的肽免疫原及其用于预防和治疗偏头痛的制剂
本技术是pct国际申请,其要求2018年12月31日提交的美国临时申请序列号62/787,102的优先权(其全部内容通过引用并入本文)。
【技术领域】
1.本公开是关于靶向降钙素基因相关肽(cgrp)的肽免疫原构建体及其制剂,以用于预防和治疗偏头痛。
背景技术:
2.偏头痛是一种常见的身体病况,在美国影响多达3700万人。偏头痛被认为是一种全身性疾病,而不仅是头痛。最近的研究表明,早在偏头痛症状出现前24小时,大脑中的变化就可能开始发生。偏头痛的症状因患病个体而异,但可能包括严重的搏动性头痛(通常仅在头部的一侧)、恶心、呕吐、光敏感(畏光)、声音敏感(畏声)或这些症状的组合。即使在头痛消失后,这些症状仍然持续。
3.偏头痛有多种亚型,其症状包括虚弱、麻木、视力改变或丧失、眩晕和说话困难(一些患者可能看起来像是中风)。由这种慢性疾病引起的无能是非常严重的,可导致工作日的中断和丧失参加家庭活动的能力。
4.有时人们可能会使用“顿挫性(abortive)”药物治疗,这种药物在早期服用时可以阻止偏头痛的发作。对于许多患者而言,预防性药物可以减少偏头痛的发生频率和严重程度。但是,许多用于预防或治疗偏头痛的药物主要是针对其他疾病(例如癫痫发作、抑郁、高血压和肌肉痉挛)而开发的。
5.研究人员数十年来一直致力于开发专门针对偏头痛的“靶向”预防疗法。降钙素基因相关肽(cgrp)是在周围和中枢神经元中合成的分子。它涉及包括偏头痛在内的不同疼痛过程,并且作用如同血管扩张剂。用于偏头痛的顿挫性药物治疗着重在于在偏头痛开始时阻止cgrp活化。已显示小分子cgrp拮抗剂药物可基于某些措施减轻偏头痛,但这些拮抗剂可能具有包括肝毒性在内的严重的副作用。
6.靶向cgrp分子的单株抗体对疼痛过程具有抑制效果,且可用作顿挫性药物治疗。针对cgrp的单株抗体可具有长半衰期,这意味着其与每日给药的常规的偏头痛药物(除了肉毒杆菌毒素以外,肉毒杆菌毒素为每90天注射一次) 相比可以较低的频率给药。用于偏头痛的单株抗体可以每月一次的频率进行皮下注射,且到目前为止已证实其在偏头痛的天数方面有统计学上显著的减少。多家不同的制药公司正在开发这些新的抗体以供fda批准。
7.虽然可以证明此种单株抗cgrp或抗cgrp受体抗体在偏头痛的免疫治疗是有效的,但是它们昂贵且必须每月给药以维持对血清和体液cgrp水平的充分抑制以及由此产生的临床效益。通过安全且耐受性良好的疫苗接种方法之靶向cgrp分子的具有成本效益的免疫治疗对于偏头痛治疗而言仍是令人兴奋的新干预手段和发展。
8.典型的肽/半抗原
‑
载体蛋白免疫原制备方法存在许多缺点和不足。例如,制备方
法涉及复杂的化学耦合步骤,它们使用昂贵的药物级klh或类毒素蛋白作为t辅助细胞载体,利用此蛋白免疫原所引发的大多数抗体都是针对载体蛋白而不是针对目标b细胞表位等。
9.鉴于使用单株抗体治疗和典型的肽/半抗原
‑
载体蛋白制剂在经济和实践上的缺点和局限性,显然仍有需求(此需求在于要开发能够针对cgrp上之功能位点引发高特异性免疫反应的有效免疫治疗组合物,此组合物须可易于患者使用,能够按照严格的优良制备作业规范(gmp)生产,并且需具有成本效益以在全球应用治疗偏头痛患者)未被满足。
10.针对位于以上背景技术部分中的陈述可以找到引用其他支持文献的两篇文献回顾,在此以引用的方式将其整体并入本文。第一篇文献包含有关cgrp和cgrp受体的最新评论(网站:en.wikipedia.org/wiki/calcitonin_gene
‑
related_peptide),而第二篇文献探讨cgrp讯息传递的生物学特性、cgrp在偏头痛中的作用的重要临床证据(包括靶向cgrp治疗的疗效)、cgrp在三叉血管系统中的作用,以及对于三叉神经节在偏头痛病理生理学中之重要作用的新见解(edvinsson,etal.,2018)。
11.参考文献
12.1.chang,j.c.c.,etal.,
″
adjuvantactivityofincompletefreund
′
sadjuvant,
″
advanceddrugdeliveryreviews,32(3):173
‑
186(1998)
13.2.
″
calcitoningene
‑
relatedpeptide,
″
wikipedia,thefreeencyclopedia,websiteaddress:en.wikipedia.org/wiki/calcitonin_gene
‑
related_peptide(accesseddecember30,2018).
14.3.edvinsson,l.,etal.,“cgrpasthetargetofnewmigrainetherapies
‑
successfultranslationfrombenchtoclinic”,nat.rev.neurol.,14(6):338
‑
350(2018)
15.4.fields,g.b.,etal.,chapter3insyntheticpeptides:auser’sguide,ed.grant,w.h.freeman&co.,newyork,ny,p.77(1992).
16.5.russell,f.a.,etal.,“calcitoningene
‑
relatedpeptide:physiologyandpathophysiology”,physiol.rev.,94(4):1099
‑
1142(2014)
17.6.tajti,j.,etal.,“messengermoleculesandreceptormrnainthehumantrigeminalganglion”,j.auton.nerv.syst.28;76(2
‑
3):176
‑
83(1999)
18.7.traggiai,e.,etal.,“anefficientmethodtomakehumanmonoclonalantibodiesfrommemorybcells:potentneutralizationofsarscoronavirus”,naturemedicine,10:871
‑
875(2004).
19.8.watkins,h.a.,etal.,“structure
‑
activityrelationshipsfora
‑
calcitoningene
‑
relatedpeptide”,br.j.pharmacol.,170(7):1308
‑
22(2013).
技术实现要素:
20.本公开是关于作为b细胞表位之降钙素基因相关肽(cgrp)的部分。本公开还关于含有来自cgrp之b细胞表位的肽免疫原构建体、含有此肽免疫原构建体的组合物、制备和使用此肽免疫原构建体的方法,以及利用此肽免疫原构建体制备的抗体。
21.本公开的一个方面是关于在用于预防及/或治疗偏头痛之肽免疫原构建体及其制
剂中作为b细胞表位之来自不同生物体的cgrp的部分。公开的 cgrp肽免疫原构建体(seq id nos:116
‑
127和130
‑
180)具有30个或更多个的总氨基酸,且含有功能性b细胞表位肽(功能性b细胞表位肽具有衍生自来自人类、狨猿(marmoset)或大鼠/小鼠的cgrp(即分别为seq id nos:1
‑
3)约7至约 30个的氨基酸(表1的seq id nos:4
‑
13、15
‑
19和20
‑
24)。功能性b细胞表位肽可通过任选的异源性间隔区连接至衍生自病原体蛋白的异源性t辅助细胞 (th)表位肽(例如seq id nos:74
‑
115),以形成公开的肽免疫原构建体。
22.公开的cgrp肽免疫原构建体可含有具有约7至约30个氨基酸的cgrp b 细胞表位肽。b细胞表位肽可衍生自位于cgrp分子羧基端和中间区域的 cgrp受体结合区域(例如,表1所示的seq id nos:5
‑
9和15
‑
22)。b细胞表位肽也可衍生自位于cgrp分子氨基端和中间区域之环状的c2
‑
c7环状结构附近的cgrp受体活化位点(例如表1所示的seq id nos:4、10
‑
13和23
‑
24)。设计的cgrp b细胞表位肽可在cgrp肽的氨基端或羧基端与衍生自病原体蛋白的异源性th表位(例如表2的seq id nos:74
‑
115)连接。b细胞和th表位共同作用,以刺激与各种物种的全长cgrp(seq id no:1
‑
3)交叉反应的高特异性抗体的产生。
23.在某些实施方案中,用于增强cgrp b细胞表位肽之异源性th表位是衍生自天然病原体ebv bplf1(seq id no:112)、ebv cp(seq id no:109)、破伤风梭菌(seq id nos:74、77、104、106
‑
108)、霍乱毒素(seq id no:81)和曼氏血吸虫(seq id no:80),以及那些衍生自麻疹病毒融合蛋白(mvf 1至5) 和b型肝炎表面抗原(hbsag 1至3)的理想化人工th表位,其以单一序列或组合序列(例如seq id nos:75、82
‑
99)形式存在。
24.公开的cgrp肽免疫原构建体含有设计的b细胞和th表位肽,二者共同作用以刺激针对cgrp功能性位点(包括位于cgrp分子羧基端的cgrp受体结合区域或涉及受体活化之环状的c2
‑
c7环状结构)的高特异性抗体的产生,以对易患或患有偏头痛的患者提供治疗性免疫反应。
25.本公开的另一个方面是关于含有cgrp肽免疫原构建体的肽组合物。在一些实施方案中,组合物包含一种肽免疫原构建体。在其他实施方案中,肽组合物包含cgrp肽免疫原构建体的混合物。在某些实施方案中,cgrp肽免疫原构建体的混合物具有衍生自不同病原体的异源性th表位,其可用于允许覆盖患者中广泛的遗传背景,导致免疫后更高百分比的反应率,用于预防及/或治疗偏头痛。
26.在本公开肽组合物中可以观察到于cgrp免疫原构建体的协同性增强。衍生自这种含有cgrp肽免疫原构建体之组合物给药的抗体反应大多数(>90%) 是集中在针对cgrp功能性位点或受体结合区域肽(seq id nos:4
‑
13和15
‑
24) 之欲求交叉反应上,没有很多,如果有的话,则是针对用于免疫原性增强的异源性th表位。这与使用常规载体蛋白(例如用于此种肽抗原性增强的klh、类毒素或其他生物载体)的标准方法形成鲜明对比。
27.本公开还关于用于预防及/或治疗偏头痛的药物组合物和制剂。在一些实施方案中,药物组合物包含稳定化的免疫刺激复合物,其通过将cpg寡聚合物与含有cgrp肽免疫原构建体之混合物的肽组合物混合通过静电结合而形成,以进一步增强cgrp肽免疫原性,此cgrp肽免疫原对全长cgrp(例如seq id nos:1
‑
3)具有欲求交叉反应性。
28.在其他实施方案中,药物组合物包含与矿物盐(包括铝胶 (alhydrogel)或磷酸铝(adju
‑
phos))接触以形成悬浮液剂型或与作为佐剂之montanide
tm isa 51或720接触以形成油包水乳液之cgrp肽免疫原构建体混合物的肽组合物,用于预防及/或治疗偏头痛。
29.此外,本公开还提供用于cgrp肽免疫原构建体及其制剂之低成本制备和质量控管的方法,此cgrp肽免疫原构建体及其制剂可用于在动物中预防及/ 或治疗偏头痛。
30.本公开还关于针对揭露之cgrp肽免疫原构建体的抗体。特别地,本公开的cgrp肽免疫原构建体能够刺激与全长cgrp分子交叉反应的高度特异性功能性抗体的产生。本公开的抗体利用高特异性结合至cgrp,没有很多,如果有的话,则是针对用于免疫原性增强的异源性th表位,此与利用用于此种肽抗原性增强的常规蛋白或其他生物载体所制备的抗体形成鲜明对比。因此,相较于其他肽或蛋白质免疫原,公开的cgrp肽免疫原构建体能够破坏针对自身cgrp的免疫耐受性,具有高反应率。
31.在一些实施方案中,当将肽免疫原构建体施用个体时,公开的抗体针对并特异性地结合至位于cgrp分子羧基端部分的cgrp受体结合位点(例如 seq id nos:5
‑
9和15
‑
22)。利用这些cgrp肽免疫原构建体引发的高度特异性抗体可以抑制cgrp和cgrp受体的结合,以及下游活化事件(由cgrp之环状的c2
‑
c7环状结构附近的区域所引起的细胞camp升高),导致偏头痛的有效预防及/或治疗。
32.在其他实施方案中,当将本发明肽免疫原构建体(例如seq id nos:4、 10
‑
13和23
‑
24)施用个体时,公开的抗体是针对负责下游细胞活化事件之位于环状的c2
‑
c7环状结构附近的cgrp氨基端或中间区域,或是针对cgrp受体结合位点的羧基端和中间区域。利用cgrp肽免疫原构建体引发的高度特异性抗体可以抑制(1)cgrp和cgrp受体的结合,以及(2)由cgrp之环状的c2
‑
c7 环状结构附近的区域所引起的下游活化事件,导致对细胞camp升高的抑制,因此导致对偏头痛患者的有效治疗。
33.基于它们独特的特征和性质,由cgrp肽免疫原构建体引发的公开的抗体能够提供预防性免疫治疗方法来治疗患有偏头痛的患者。
34.在另一个方面,本发明提供针对cgrp的人类单株抗体,其由接受含有本公开cgrp肽免疫原构建体之组合物的患者所诱导产生。traggiai,e.,et al, 2004描述一种由来自人类患者血液中分离的b细胞制备人类单株抗体的有效方法,此文献以引用方式并入本文。
35.本公开还关于制备公开的cgrp肽免疫原构建体、组合物和抗体的方法。公开的方法可提供用于cgrp肽免疫原构建体与含有此构建体之组合物的低成本制备和质量控管,此构建体及组合物可用于用以治疗患有偏头痛之患者的方法中。
36.本公开还包括使用公开的cgrp肽免疫原构建体及/或针对cgrp肽免疫原构建体的抗体于易患或患有偏头痛的个体中进行预防及/或治疗的方法。用以于个体中预防及/或治疗偏头痛的方法包括对个体施用含有公开的cgrp肽免疫原构建体之组合物。在某些实施方案中,方法中使用的组合物含有公开的cgrp肽免疫原构建体,cgrp肽免疫原构建体通过静电结合与带有负电荷的寡核苷酸(例如cpg寡聚合物)形成稳定的免疫刺激复合物,其可进一步与佐剂添加,供患有偏头痛的患者施用。
37.公开的方法还包括用于施用cgrp肽免疫原构建体的给药方案、剂型和给药途径,以于个体中预防及/或治疗偏头痛。
38.【图式简单说明】
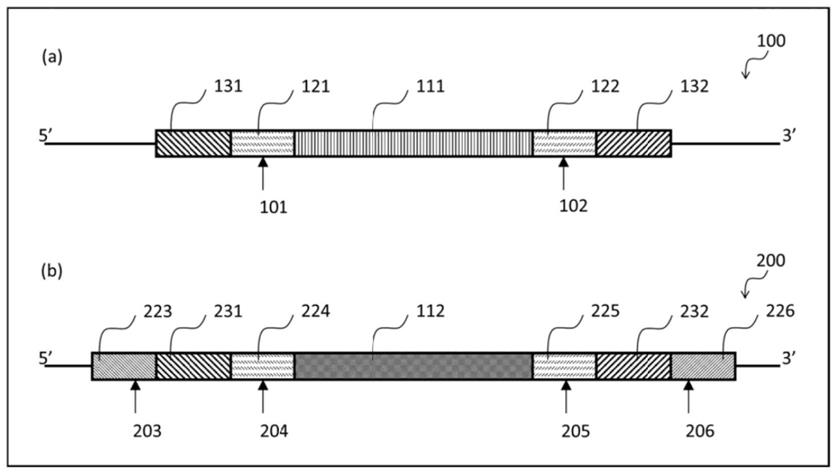
39.第1图显示来自多种物种的cgrp序列比对,多种物种包括人类(seq idno:1)、小鼠(seq id no:3)、大鼠(seq id no:3)、狨猿(seq id no:2)和许多其他物种(包括马、鸡、猪、绵羊、牛、狗、负鼠、壁虎、青蛙、河豚、比目鱼、金鱼、鲑鱼、青鳉、斑马鱼)。此图式改编自
watkins,et al.,2013。
40.第2图描述用于偏头痛治疗之高精密度cgrp专门设计肽免疫原构建体及其制剂从发现到商业化的途径。
41.第3图描述在天竺鼠中之cgrp肽免疫原构建体(seq id nos:116
‑
118、 124
‑
127、128、129、131、133、135、137、119
‑
122、139、123、130)(此些 cgrp肽免疫原构建体具有衍生自cgrp分子氨基端、中间、羧基端区域之 cgrp b细胞表位肽)的免疫原性研究结果。
42.第4图描述在来自代表性cgrp肽免疫原构建体(seq id nos:116
‑
118、 124
‑
127、128、129、131、133、135、137、119
‑
123、130、139和150)之天竺鼠免疫血清(收集自6wpi采血)的纯化抗体存在下在cgrp活化的细胞培养物中的中和活性,中和活性表示为细胞内camp产生的ic
50
。
43.第5图显示配制于adjuphos和isa51制剂中之代表性cgrp肽免疫原构建体(seq id nos:123、131、141、151)于balb/c小鼠中的免疫原性研究结果,来自于7wpi、10wpi和13wpi采血之天竺鼠免疫血清纯化而来相对应的抗体具有反应性且与全长人类cgrp分子具有交叉反应性。
44.第6图显示当与单独佐剂或生理盐水之对照品相比较时在利用配制于如所示的adjuphos或isa乳液制剂中之cgrp肽免疫原构建体(seq id nos: 123、131、141)在0、3和6wpi进行免疫接种之balb/c小鼠中所测量到对辣椒素诱导的皮肤血流的抑制作用。
45.【实施方式】
46.本公开是关于作为b细胞表位之降钙素基因相关肽(cgrp)的部分。本公开还关于含有来自cgrp之b细胞表位的肽免疫原构建体、含有此肽免疫原构建体的组合物、制备和使用此肽免疫原构建体的方法,以及利用此肽免疫原构建体制备的抗体。
47.本公开的一个方面是关于在用于预防及/或治疗偏头痛之肽免疫原构建体及其制剂中作为b细胞表位之来自不同生物体的cgrp的部分。公开的 cgrp肽免疫原构建体(seq id nos:116
‑
127和130
‑
180)具有30个或更多个的总氨基酸,且含有功能性b细胞表位肽(功能性b细胞表位肽具有衍生自来自人类、狨猿或大鼠/小鼠的cgrp(即分别为seq id nos:1
‑
3)约7至约30个的氨基酸(表1的seq id nos:4
‑
13、15
‑
19和20
‑
24)。功能性b细胞表位肽可通过任选的异源性间隔区连接至衍生自病原体蛋白的异源性t辅助细胞(th)表位肽(例如seq id nos:74
‑
115),以形成公开的肽免疫原构建体。
48.公开的cgrp肽免疫原构建体可含有具有约7至约30个氨基酸的cgrp b 细胞表位肽。b细胞表位肽可衍生自位于cgrp分子羧基端和中间区域的 cgrp受体结合区域(例如,表1所示的seq id nos:5
‑
9和15
‑
22)。b细胞表位肽也可衍生自位于cgrp分子氨基端和中间区域之环状的c2
‑
c7环状结构附近的cgrp受体活化位点(例如表1所示的seq id nos:4、10
‑
13、20
‑
22)。设计的cgrp b细胞表位肽可在cgrp肽的氨基端或羧基端与衍生自病原体蛋白的异源性th表位(例如表2的seq id nos:74
‑
115)连接。b细胞和th表位共同作用,以刺激与各种物种的全长cgrp(seq id no:1
‑
3)交叉反应的高特异性抗体的产生。
49.在某些实施方案中,用于增强cgrp b细胞表位肽之异源性th表位是衍生自天然病原体ebv bplf1(seq id no:112)、ebv cp(seq id no:109)、破伤风梭菌(seq id nos:74、77、104、106
‑
108)、霍乱毒素(seq id no:81)和曼氏血吸虫(seq id no:80),以及那些衍生自麻疹病毒融合蛋白(mvf 1至5) 和b型肝炎表面抗原(hbsag1至3)的理想化人工th表位,
其以单一序列或组合序列(例如seq id nos:75、82
‑
99)形式存在。
50.公开的cgrp肽免疫原构建体含有设计的b细胞和th表位肽,二者共同作用以刺激针对cgrp功能性位点(包括位于cgrp分子羧基端的cgrp受体结合区域或涉及受体活化之环状的c2
‑
c7环状结构)的高特异性抗体的产生,以对易患或患有偏头痛的患者提供治疗性免疫反应。
51.本公开的另一个方面是关于含有cgrp肽免疫原构建体的肽组合物。在一些实施方案中,组合物包含一种肽免疫原构建体。在其他实施方案中,肽组合物包含cgrp肽免疫原构建体的混合物。在某些实施方案中,cgrp肽免疫原构建体的混合物具有衍生自不同病原体的异源性th表位,其可用于允许覆盖患者中广泛的遗传背景,导致免疫后更高百分比的反应率,用于预防及/或治疗偏头痛。
52.在本公开肽组合物中可以观察到于cgrp免疫原构建体的协同性增强。衍生自这种含有cgrp肽免疫原构建体之组合物给药的抗体反应大多数(>90%) 是集中在针对cgrp功能性位点或受体结合区域肽(seq id nos:4
‑
13、15
‑
19 和20
‑
24)之欲求交叉反应上,没有很多,如果有的话,则是针对用于免疫原性增强的异源性th表位。这与使用常规载体蛋白(例如用于此种肽抗原性增强的 klh、类毒素或其他生物载体)的标准方法形成鲜明对比。
53.本公开还关于用于预防及/或治疗偏头痛的药物组合物和制剂。在一些实施方案中,药物组合物包含稳定化的免疫刺激复合物,其通过将cpg寡聚合物与含有cgrp肽免疫原构建体之混合物的肽组合物混合通过静电结合而形成,以进一步增强cgrp肽免疫原性,此cgrp肽免疫原对全长cgrp(例如 seq id nos:1
‑
3)具有欲求交叉反应性。
54.在其他实施方案中,药物组合物包含与矿物盐(包括铝胶 (alhydrogel)或磷酸铝(adju
‑
phos))接触以形成悬浮液剂型或与作为佐剂之montanide
tm isa 51或720接触以形成油包水乳液之cgrp肽免疫原构建体混合物的肽组合物,用于预防及/或治疗偏头痛。
55.此外,本公开还提供用于cgrp肽免疫原构建体及其制剂之低成本制备和质量控管的方法,此cgrp肽免疫原构建体及其制剂可用于在动物中预防及/ 或治疗偏头痛。
56.本公开还关于针对揭露之cgrp肽免疫原构建体的抗体。特别地,本公开的cgrp肽免疫原构建体能够刺激与全长cgrp分子交叉反应的高度特异性功能性抗体的产生。本公开的抗体利用高特异性结合至cgrp,没有很多,如果有的话,则是针对用于免疫原性增强的异源性th表位,此与利用用于此种肽抗原性增强的常规蛋白或其他生物载体所制备的抗体形成鲜明对比。因此,相较于其他肽或蛋白质免疫原,公开的cgrp肽免疫原构建体能够破坏针对自身cgrp的免疫耐受性,具有高反应率。
57.在一些实施方案中,当将肽免疫原构建体施用个体时,公开的抗体针对并特异性地结合至位于cgrp分子羧基端部分的cgrp受体结合位点(例如 seq id nos:5
‑
9和15
‑
22)。利用这些cgrp肽免疫原构建体引发的高度特异性抗体可以抑制cgrp和cgrp受体的结合,以及下游活化事件(由cgrp之环状的c2
‑
c7环状结构附近的区域所引起的细胞camp升高),导致偏头痛的有效预防及/或治疗。
58.在其他实施方案中,当将本发明肽免疫原构建体(例如seq id nos:4、 10
‑
13和23
‑
24)施用个体时,公开的抗体是针对负责下游细胞活化事件之位于环状的c2
‑
c7环状结构附近的cgrp氨基端或中间区域,或是针对cgrp受体结合位点的羧基端和中间区域。利用cgrp肽免疫原构建体引发的高度特异性抗体可以抑制(1)cgrp和cgrp受体的结合,以及(2)
由cgrp之环状的c2
‑
c7 环状结构附近的区域所引起的下游活化事件,导致对细胞camp升高的抑制,因此导致对偏头痛患者的有效治疗。
59.基于它们独特的特征和性质,由cgrp肽免疫原构建体引发的公开的抗体能够提供预防性免疫治疗方法来治疗患有偏头痛的患者。
60.在另一个方面,本发明提供针对cgrp的人类单株抗体,其由接受含有本公开cgrp肽免疫原构建体之组合物的患者所诱导产生。traggiai,e.,et al, 2004描述一种由来自人类患者血液中分离的b细胞制备人类单株抗体的有效方法,此文献以引用方式并入本文。
61.本公开还关于制备公开的cgrp肽免疫原构建体、组合物和抗体的方法。公开的方法可提供用于cgrp肽免疫原构建体与含有此构建体之组合物的低成本制备和质量控管,此构建体及组合物可用于用以治疗患有偏头痛之患者的方法中。
62.本公开还包括使用公开的cgrp肽免疫原构建体及/或针对cgrp肽免疫原构建体的抗体于易患或患有偏头痛的个体中进行预防及/或治疗的方法。用以于个体中预防及/或治疗偏头痛的方法包括对个体施用含有公开的cgrp肽免疫原构建体之组合物。在某些实施方案中,方法中使用的组合物含有公开的cgrp肽免疫原构建体,cgrp肽免疫原构建体通过静电结合与带有负电荷的寡核苷酸(例如cpg寡聚合物)形成稳定的免疫刺激复合物,其可进一步与佐剂添加,供患有偏头痛的患者施用。
63.公开的方法还包括用于施用cgrp肽免疫原构建体的给药方案、剂型和给药途径,以于个体中预防及/或治疗偏头痛。
64.通则
65.本文使用的章节标题仅用于组织的目的,不应被理解为限制所述主题。本技术中引用的所有参考文献或参考文献的部分出于任何目的通过引用明确地将整体并入本文。
66.除非特别说明,在此使用的所有技术和科学用语如本发明所属技术领域中具有通常知识者的通常理解具有相同意义。除非上下文清楚地指出,否则单词“一(a)”、“一(an)”和“该(the)”包含复数形式。类似地,单词“或(or)”是意指包括“和(and)”,除非上下文另有明确说明。因此,“包含a或b”是指包括a,或b,或a和b。更应被理解的是,用于给定多肽之所有的氨基酸大小和所有分子量或分子质量值是近似的,并且被提供作为描述之用。然而类似或等同于在此描述者的方法和材料可被用于以下所述的公开的方法、合适的方法和材料的实践或测试中。在此提及的所有出版物、专利申请、专利和其它参考文献通过引用整体并入本文。在冲突的情况下,以本说明书(包括术语的解释)为准。此外,本文公开的材料、方法和实施例仅是说明性的而非意指加以限制。
67.cgrp肽免疫原构建体
68.本公开提供含有b细胞表位肽的肽免疫原构建体,此b细胞表位肽具有来自cgrp(seq id nos:1
‑
3)或其片段之氨基酸序列。cgrp肽免疫原构建体可含有具有约7至约30个氨基酸的cgrp b细胞表位肽。b细胞表位肽可来自(1) 位于cgrp分子羧基端/中间区域的cgrp受体结合区域(例如,表1所示的seqid nos:5
‑
9和15
‑
22);或(2)来自位于cgrp分子氨基端/中间区域之环状的c2
‑
c7环状结构附近的cgrp受体活化位点(例如表1所示的seq id nos:4、 10
‑
13和23
‑
24)。b细胞表位直接地或是通过任选的异源性间隔区共价地连接至衍生自病原体蛋白质的异源性t辅助细胞(th)表位(例如表2的seq id nos: 74
‑
115)。这些结构(含有设计的b细胞和th细胞表位共同作用)刺激与各种物种的全长cgrp(seq id no:1
‑
3)交叉反应的高特异性抗体的产生。
69.本文使用术语“cgrp肽免疫原构建体”或“肽免疫原构建体”是指具有约30个以上氨基酸的肽,其含有(a)具有来自全长cgrp(seq id nos:1
‑
3)之约 7个以上连续氨基酸残基的b细胞表位;(b)异源性th表位;以及(c)任选的异源性间隔区。
70.在某些实施方案中,cgrp肽免疫原构建体可利用以下分子式作为代表:
71.(th)
m
‑
(a)
n
‑
(cgrp功能性b细胞表位肽)
‑
x
72.或
73.(cgrp功能性b细胞表位肽)
‑
(a)
n
‑
(th)
m
‑‑
x
74.或
75.(th)
m
‑
(a)
n
‑
(cgrp功能性b细胞表位肽)
‑
(a)
n
‑
(th)
m
‑
x
76.其中
77.th为异源性t辅助细胞表位;
78.a为异源性间隔区;
79.(cgrp功能性b细胞表位肽)为具有涉及受体结合或受体活化的来自 cgrp的7至30个氨基酸残基的b细胞表位肽;
80.x为氨基酸的α
‑
cooh或α
‑
conh2;
81.m为1至约4;以及
82.n为0至约10。
83.基于许多理论基础设计和选择本公开的cgrp肽免疫原构建体,包括:
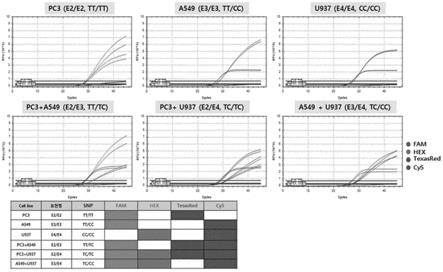
84.i.cgrp b细胞表位肽本身是非免疫原性的,以避免自体t细胞活化;
85.ii.通过使用蛋白质载体或有效的t辅助细胞表位,可以使cgrp b细胞表位肽具有免疫原性;
86.iii.当cgrp b细胞表位肽成为免疫原性的并施用宿主时,肽免疫原构建体:
87.a.引发优先针对cgrp b细胞表位(而非蛋白质载体或t辅助细胞表位)的高效价抗体;
88.b.在接受免疫的宿主中破坏免疫耐受性并产生与cgrp(seq id nos: 1
‑
3)交叉反应的高度特异性抗体;
89.c.产生可以抑制cgrp和cgrp受体结合以及相关下游事件(例如细胞内 camp产量增加)的高度特异性抗体;以及
90.d.产生能够在体内造成辣椒素诱导的皮肤血流减少的高度特异性抗体。
91.公开的cgrp肽免疫原构建体及其制剂可有效地发挥药物组合物的作用,以预防及/或治疗易患或患有偏头痛的个体。
92.公开的cgrp肽免疫原构建体的各种组分在下文进一步详细描述。
93.a.来自cgrp的b细胞表位肽
94.本公开关于用于产生高效价抗体的新颖肽组合物,所述高效价抗体对多种物种之降钙素基因相关肽(cgrp)蛋白(例如seq id nos:1
‑
3)具有特异性。肽免疫原构建体的位点特异性使针对位于cgrp上其他区域的不相关位点或位于载体蛋白上的不相关位点的抗体产生最小化,从而提供高安全系数。
95.本文使用术语“cgrp”是指属于降钙素(ct)肽家族之37个氨基酸的神经肽α
‑
cgrp。
人类cgrp衍生自uniprotkb:p06881
‑
1且具有seq id no:1的氨基酸序列。狨猿(callithrix jacchus)cgrp衍生自genbank accession no.: aal35592.1且具有seq id no:2的氨基酸序列。大鼠(rattus norvegicus)cgrp 衍生自uniprotkb:p01256,而小鼠(mus musculus)cgrp衍生自uniprotkb: q99ja0,且大鼠和小鼠cgrp都具有seq id no:3的氨基酸序列。在本公开中所使用cgrp的氨基酸序列如表1所示。
96.在人类中,cgrp衍生自编码降钙素的基因,是由位于11号染色体上的降钙素/cgrp基因的选择性剪接所形成。在人类中,cgrp具有两种同型异构物:α
‑
cgrp和β
‑
cgrp。α
‑
同型异构物与β
‑
同型异构物的差别在于位于第3、22和 25个位置的氨基酸。在平滑肌细胞内的分子层次上,cgrp可通过其羧基端区域与其受体结合,然后通过使用其环状结构区域活化受体。具有双硫键之环状的c2
‑
c7环状结构在受体活化中具有核心作用,并且与细胞内camp的升高密切相关。在哺乳类动物的血浆中,cgrp的半衰期约为10分钟。在人类三叉神经节中,cgrp反应性神经元占所有神经元的50%(tajti,et al.,1999)。
97.cgrp在中枢和周围神经系统中广泛表现。它主要与紧邻血管的小的无髓鞘感觉神经元有关。cgrp是有效的血管扩张剂,且局部施用cgrp会导致血液流量短暂增加。cgrp还与疼痛传播、疼痛调节和神经性炎症有关。利用辣椒素通过瞬态受体电位阳离子通道v1的活化可使cgrp从感觉神经元释放。雷射都卜勒成像仪(ldi)已用于检测由cgrp所引起之皮肤血流的结果变化。
98.如同在多种疼痛模型中于cgrp敲除小鼠的减弱反应所证明cgrp也与炎症性疼痛相关。这种在疼痛感知中的作用与在感觉神经元中cgrp的表现是一致的。
99.本公开的一个方面是利用靶向cgrp之主动免疫疗法以发挥长期cgrp阻断作用和临床功效,用以预防及/或治疗cgrp
‑
偏头痛。因此,本公开关于靶向全长cgrp蛋白(seq id no:1
‑
3)之部分的肽免疫原构建体及其制剂,以用于预防和治疗偏头痛。
100.cgrp肽免疫原构建体的b细胞表位部分可包含来自全长cgrp蛋白(以 seq id nos:1
‑
3代表)的任何部分的约7至约30个氨基酸。在某些实施方案中,基于设计理论基础筛选和选择的b细胞表位肽包含如表1所示的seq id nos: 4
‑
13和15
‑
24的氨基酸序列。
101.在一些实施方案中,b细胞表位肽来自位于cgrp分子羧基端/中间区域 r11
‑
f37(seq id no:9)的cgrp受体结合区域,或其片段(例如seq id nos: 5
‑
8和15
‑
22)。在其他实施方案中,b细胞表位肽来自位于环状的c2
‑
c7环状结构附近的cgrp受体活化区域(例如a1
‑
n25(seq id no:13))或其片段(例如 seq id nos:4、10
‑
12和23
‑
24)。
102.本公开的cgrp b细胞表位肽还包括cgrp的免疫功能类似物或同源物。 cgrp b细胞表位肽的免疫功能类似物或同源物包括保留与原始肽免疫原性实质相同的的变异物。免疫功能类似物可具有于氨基酸位置的保留性取代、总电荷改变、与其他官能基共价连接或氨基酸的添加、插入或删除及/或其任意组合(例如seq id nos:9 vs 25的cgrp肽)。
103.由包含来自cgrp的这些b细胞表位的肽免疫原构建体产生的抗体是高度特异性的,并且与各种物种的全长cgrp(例如,seq id nos:1
‑
3)有交叉反应。基于它们独特的特征和性质,由cgrp肽免疫原构建体引发的公开的抗体能够提供预防性免疫治疗方法以预防及/或治疗偏头痛。
104.b.异源性t辅助细胞表位(th表位)
105.本公开提供肽免疫原构建体,其包含来自cgrp的b细胞表位,b细胞表位直接地或
是通过任选的异源性间隔区共价连接至异源性t辅助细胞(th)表位。
106.于cgrp肽免疫原构建体中的异源性th表位可增强cgrp片段的免疫原性,其促进针对基于设计理论筛选和选择的优化目标cgrp b细胞表位肽之特异性高效价抗体的产生。
107.本文使用术语“异源性”是指衍生自并非cgrp野生型序列之部分或与其同源之氨基酸序列的氨基酸序列。因此,异源性th表位为衍生自非天然存在于cgrp之氨基酸序列的th表位(即th表位对cgrp而言不是自体衍生的)。因为th表位对cgrp而言是异源性的,当异源性th表位共价连接至cgrp b细胞表位肽时,cgrp的天然氨基酸序列不会向氨基端或羧基端方向延伸。
108.本公开的异源性th表位可为不具有天然存在于cgrp之氨基酸序列的任何th表位。th表位还可具有针对多种物种第2类mhc分子的混杂结合基序。在某些实施方案中,th表位包含多个混杂的第2类mhc结合基序,以允许t辅助细胞的最大活化,从而导致免疫反应的启动和调节。较佳的th表位本身为非免疫原性的(即如果有的话,很少利用cgrp肽免疫原构建体所产生抗体是针对th表位),因此允许针对cgrp分子之目标b细胞表位肽的非常集中的免疫反应。
109.本公开的th表位包括,但不限于,衍生自外来病原菌之氨基酸序列,如表2(seq id nos:74
‑
115)所例示。此外,th表位包括理想化人工th表位和组合的理想化人工th表位(例如seq id nos:75和82
‑
99)。异源性th表位肽以组合序列(例如seq id nos:85、91、94和97)呈现,包含基于特定肽之同源物的可变残基在肽骨架内于特定位置处作为代表的氨基酸残基的混合物。可以利用在合成过程期间在特定位置添加选定受保护之氨基酸的混合物,而非一个特定的氨基酸,于单一过程中合成组合肽的集合。此种组合异源性th表位肽集合可允许对具有不同遗传背景之动物广泛的th表位覆盖。异源性th表位肽之代表性组合序列包含如表2所示的seq id nos:85、91、94和97。本发明的 th表位肽对来自基因多样性群体的动物和患者提供广泛的反应性和免疫原性。
110.c.异源性间隔区
111.公开的cgrp肽免疫原构建体任选地包含异源性间隔区,其将cgrp b细胞表位肽共价连接至异源性t辅助细胞(th)表位。
112.如上所述,术语“异源性”是指衍生自并非cgrp天然型序列之部分或与其同源之氨基酸序列的氨基酸序列。因此,当异源性间隔区共价连接至cgrp b细胞表位肽时,cgrp的天然氨基酸序列不会向氨基端或羧基端方向延伸,因为间隔区对cgrp序列而言是异源性的。
113.间隔区为能够将两个氨基酸及/或肽连接在一起的任何分子或化学结构。依据应用的不同,间隔区的长度或极性可能会有所不同。间隔区连接可通过酰胺或羧基连结,但是其他官能基也是可能的。间隔区可包括化学化合物、天然存在的氨基酸或非天然存在的氨基酸。
114.间隔区可为cgrp肽免疫原构建体提供结构特征。结构上,间隔区提供th 表位与cgrp片段的b细胞表位的物理分离。通过间隔区的物理分离可破坏通过将th表位连接至b细胞表位所产生的任何人工二级结构。另外,通过间隔区之表位的物理分离可消除th细胞及/或b细胞反应之间的干扰。此外,可设计间隔区以产生或修饰肽免疫原构建体的二级结构。例如,可设计间隔区以作为柔性铰链,用以增强th表位和b细胞表位的分离。柔性铰链间隔区也可允许所呈现之肽免疫原与适当的th细胞和b细胞之间更有效率的交互作用,以增强
对th表位和b细胞表位的免疫反应。编码柔性铰链之序列的例示见于通常富含脯胺酸的免疫球蛋白重链铰链区。利用序列pro
‑
pro
‑
xaa
‑
pro
‑
xaa
‑
pro (seq id no:71)提供了一种作为间隔区使用之特别有用的柔性铰链,其中xaa 是任意氨基酸,以天门冬胺酸为较佳。
115.间隔区也可为cgrp肽免疫原构建体提供功能特征。例如,可设计间隔区以改变cgrp肽免疫原构建体的总电荷,其可影响肽免疫原构建体的溶解度。此外,改变cgrp肽免疫原构建体的总电荷可影响肽免疫原构建体与其他化合物和试剂结合的能力。如下文进一步详细讨论的,cgrp肽免疫原构建体可通过静电结合与高度带电的寡核苷酸(例如cpg寡聚合物)形成稳定的免疫刺激复合物。cgrp肽免疫原构建体的总电荷对于形成这些稳定的免疫刺激复合物是重要的。
116.可作为间隔区的化学化合物包括,但不限于,(2
‑
胺乙氧基)乙酸(aea)、 5
‑
胺基戊酸(ava)、6
‑
胺基己酸(ahx)、8
‑
胺基
‑
3,6
‑
二氧杂辛酸(aeea, mini
‑
peg1)、12
‑
胺基
‑
4,7,10
‑
三氧杂十二酸(mini
‑
peg2)、15
‑
胺基
‑
4,7,10,13
‑
四氧杂十五烷酸(mini
‑
peg3)、trioxatridecan
‑
succinamic acid(ttds)、12
‑
胺基十二烷酸、fmoc
‑5‑
胺基
‑3‑
氧戊酸(o1pen)等。
117.天然存在的氨基酸包括丙胺酸、精胺酸、天门冬酰胺酸、天门冬胺酸、半胱胺酸、麸胺酸、麸酰胺酸、甘胺酸、组胺酸、异白胺酸、白胺酸、离胺酸、甲硫胺酸、苯丙胺酸、脯胺酸、丝胺酸、苏胺酸、色胺酸、酪胺酸和缬胺酸。
118.非天然存在的氨基酸包括,但不限于,ε
‑
n离胺酸、β
‑
丙胺酸、鸟胺酸、正白胺酸、正缬胺酸、羟脯胺酸、甲状腺素、γ
‑
胺基丁酸、高丝胺酸、瓜胺酸、胺基苯甲酸、6
‑
胺基己酸(aca;6
‑
胺基己酸)、3
‑
硫醇丙酸(mpa)、3
‑
硝基酪胺酸、焦麸胺酸等。
119.cgrp肽免疫原构建体中的间隔区可共价连接在th表位和cgrp b细胞表位肽的氨基端或羧基端。在一些实施方案中,间隔区共价连接至th表位的羧基端和cgrp b细胞表位肽的氨基端。在其他实施方案中,间隔区共价连接至 cgrp b细胞表位肽的羧基端和th表位的氨基端。在某些实施方案中,可使用一个以上的间隔区,例如,当在cgrp肽免疫原构建体中存在一个以上的th 表位时。当使用一个以上的间隔区时,每个间隔区可以彼此相同或不同。此外,当cgrp肽免疫原构建体中存在一个以上的th表位时,可利用间隔区分隔开th表位,间隔区可为相同或不同,利用间隔区将th表位与cgrp b细胞表位肽分开。间隔区相对于th表位或cgrp b细胞表位肽的排列没有限制。
120.在某些实施方案中,异源性间隔区是天然存在的氨基酸或非天然存在的氨基酸。在其他实施方案中,间隔区包含一个以上的天然存在或非天然存在的氨基酸。在具体实施方案中,间隔区为lys
‑
、gly
‑
、lys
‑
lys
‑
lys
‑
、(α,ε
‑
n)lys、ε
‑
n
‑
lys
‑
lys
‑
lys
‑
lys(seq id no:72)或lys
‑
lys
‑
lys
‑
ε
‑
n
‑
lys(seq id no: 73)。
121.d.cgrp肽免疫原构建体的具体实施方案
122.在某些实施方案中,cgrp肽免疫原构建体可利用以下分子式表示:
123.(th)
m
‑
(a)
n
‑
(cgrp功能性b细胞表位肽)
‑
x
124.或
125.(cgrp功能性b细胞表位肽)
‑
(a)
n
‑
(th)
m
‑
x
126.或
127.(th)
m
‑
(a)
n
‑
(cgrp功能性b细胞表位肽)
‑
(a)
n
‑
(th)
m
‑
x
128.其中
129.th为异源性t辅助细胞表位;
130.a为异源性间隔区;
131.(cgrp功能性b细胞表位肽)为具有涉及受体结合或受体活化的来自cgrp的7至30个氨基酸残基的b细胞表位肽;
132.x为氨基酸的α
‑
cooh或α
‑
conh2;
133.m为1至约4;以及
134.n为0至约10。
135.b细胞表位肽可包含来自全长cgrp蛋白(以seq id nos:1
‑
3代表)的任何部分的约7至约30个氨基酸。在某些实施方案中,b细胞表位具有选自如表1 所示seq id nos:4
‑
13和15
‑
22中任一的氨基酸序列。在某些实施方案中,b 细胞表位肽来自位于cgrp分子羧基端/中间区域r11
‑
f37(seq id no:9)的 cgrp受体结合区域,或其片段(例如seq id nos:5
‑
8和15
‑
22)。在其他实施方案中,b细胞表位肽来自位于环状的c2
‑
c7环状结构附近的cgrp受体活化区域(例如a1
‑
n25(seq id no:13))或其片段(例如seq id nos:4、10
‑
12和 23
‑
24)。
136.cgrp肽免疫原构建体中的异源性th表位具有选自seq id nos:74
‑
115 及其组合中任一的氨基酸序列,如表2所示。在一些实施方案中,cgrp肽免疫原构建体含有一个以上的th表位。
137.任选的异源性间隔区是选自lys
‑
、gly
‑
、lys
‑
lys
‑
lys
‑
、(α,ε
‑
n)lys、 pro
‑
pro
‑
xaa
‑
pro
‑
xaa
‑
pro(seq id no:71)、ε
‑
n
‑
lys
‑
lys
‑
lys
‑
lys(seq id no: 72)、lys
‑
lys
‑
lys
‑
ε
‑
n
‑
lys(seq id no:73)及其任意组合中的任一个,其中xaa 是任何氨基酸,但以天门冬胺酸为较佳。在具体实施方案中,异源性间隔区为g
‑
n
‑
lys
‑
lys
‑
lys
‑
lys(seq id no:72)或lys
‑
lys
‑
lys
‑
ε
‑
n
‑
lys(seq id no: 73)。
138.在某些实施方案中,cgrp肽免疫原构建体具有选自如表3所示seq idnos:116
‑
127和130
‑
180中任一个的氨基酸序列。
139.包含th表位之cgrp肽免疫原构建体是于与cgrp片段串联的单一固相肽合成中同时产生。th表位也可包括th表位的免疫类似物。免疫th类似物包括免疫增强类似物、交叉反应类似物和任何这些th表位的片段,其足以增强或刺激对cgrp b细胞表位肽的免疫反应。
140.在cgrp肽免疫原构建体中的th表位可共价连接于cgrp b细胞表位肽的氨基端或羧基端。在一些实施方案中,th表位是共价连接至cgrp b细胞表位肽的氨基端。在其他实施方案中,th表位是共价连接至cgrp b细胞表位肽的羧基端。在某些实施方案中,一个以上的th表位共价连接至cgrp b细胞表位肽。当一个以上的th表位连接至cgrp b细胞表位肽时,每一个th表位可具有相同氨基酸序列或不同氨基酸序列。另外,当一个以上的th表位连接至cgrpb细胞表位肽时,th表位可以任何顺序排列。例如,th表位可连续地连接至 cgrp b细胞表位肽的氨基端,或连续地连接至cgrp b细胞表位肽的羧基端,或当不同的th表位共价连接至cgrp b细胞表位肽的羧基端时,th表位可共价连接至cgrp b细胞表位肽的氨基端。th表位相对于cgrp b细胞表位肽的排列并无限制。
141.在一些实施方案中,th表位直接地共价连接至cgrp b细胞表位肽。在其他实施方案中,th表位通过异源性间隔区共价连接至cgrp片段。
142.e.变异物、同源物和功能类似物
143.也可使用上述免疫原肽构建体的变异物和类似物,其可诱导抗体及/或与抗体交叉反应,而此抗体是针对较佳的cgrp b细胞表位肽。类似物(包括等位基因、物种以及诱导变异物),通常于一个、两个或几个位置上有别于天然存在的肽,通常是由于保留性取代。类似物通常展现与天然肽至少80或90%的序列一致性。一些类似物还包括非天然氨基酸或在一个、两个或几个位置上之氨基端或羧基端氨基酸的修饰。
144.作为功能类似物的变异物可具有于氨基酸位置上的保留性取代、总电荷改变、与其他官能基共价连接或氨基酸的添加、插入或删除及/或其任意组合。
145.保留性取代是指一个氨基酸残基被另一个具有相似化学性质的氨基酸残基所取代。例如,非极性(疏水性)氨基酸包括丙胺酸、白胺酸、异白胺酸、缬胺酸、脯胺酸、苯丙胺酸、色胺酸和甲硫胺酸;极性中性氨基酸包括甘胺酸、丝胺酸、苏胺酸、半胱胺酸、酪胺酸、天门冬酰胺酸和麸酰胺酸;带正电的(碱性)氨基酸包括精胺酸、离胺酸和组胺酸;而带负电的(酸性)氨基酸包括天门冬胺酸和麸胺酸。
146.在一个特定实施方案中,功能类似物与原始氨基酸序列具有至少50%的一致性。在另一实施方案中,功能类似物与原始氨基酸序列具有至少80%的一致性。在又一实施方案中,功能类似物与原始氨基酸序列具有至少85%的一致性。在又一实施方案中,功能类似物与原始氨基酸序列具有至少90%的一致性。
147.th表位肽的功能免疫类似物也是有效的,且被包括作为本发明的一部分。功能免疫th类似物可包含于th表位中从1至约5个氨基酸残基的保留性取代、添加、删除和插入,其实质上未改变th表位的th刺激功能。如上文针对cgrpb细胞表位肽所描述的,可以利用天然或非天然氨基酸完成保留性取代、添加和插入。表2辨识了th表位肽之功能类似物的另一种变异物。具体而言,mvf1 和mvf2 th的seq id nos:75和82是mvf4和mvf5 th的seq id nos:94和98 的功能类似物,因为利用在氨基端和羧基端将各两个氨基酸删除(seq idnos:75和82)或插入(seq id nos:94和98)而使其氨基酸骨架有所区别。在类似序列的这两个系列之间的差异并不会影响包含于此些序列中之th表位的功能。因此,功能免疫th类似物包括衍生自麻疹病毒融合蛋白mvf1
‑
4 ths(seqid nos:75、82、85和94)和衍生自肝炎表面蛋白质hbsag 1
‑
3 ths(seq idnos:91、97和99)之th表位的多种版本。
148.组合物
149.本公开还提供包含公开的cgrp免疫原肽构建体的组合物。
150.a.肽细合物
151.包含公开的cgrp肽免疫原构建体的组合物可为液体或固体/冻干形式。液体组合物可包括不改变cgrp肽免疫原构建体之结构或功能特性的水、缓冲液、溶剂、盐及/或任何其他可接受的试剂。肽组合物可含有一种或多种公开的cgrp肽免疫原构建体。
152.b.药物组合物
153.本公开还关于包含公开的cgrp肽免疫原构建体的药物组合物。
154.药物组合物可含有药学上可接受的递送系统中的载体及/或其他添加剂。因此,药物组合物可含有cgrp肽免疫原构建体的药学上有效剂量以及药学上可接受的载体、佐剂及/或其它赋形剂(例如稀释剂、添加剂、稳定剂、防腐剂、助溶剂、缓冲剂等)。
155.药物组合物可含有一种或多种佐剂,其作用是加速、延长或增强针对 cgrp肽免疫原构建体的免疫反应,而本身不具有任何特异性抗原作用。药物组合物中使用的佐剂可包
id nos:85、91、94和97)的cgrp肽免疫原构建体(seq id nos: 161
‑
163)以等莫耳比率混合,用于制剂中,以允许对具有不同遗传背景之宿主群体最大覆盖。
164.此外,藉由cgrp肽免疫原构建体(例如具有seq id no:108的) 所引发的抗体反应大部分(>90%)是集中在针对cgrp之b细胞表位肽的所欲求的交叉反应性,没有太多,如果有的话,则是针对用于免疫原性增强的异源性th表位(实施方案6,表10)。此与利用用于此种cgrp肽抗原性增强的常规蛋白(例如klh)或其他生物蛋白载体所制备的抗体形成鲜明对比。
165.在其他实施方案中,包含肽组合物的药物组合物,例如cgrp肽免疫原构建体混合物与作为佐剂之矿物盐(包括明矾凝胶(alhydrogel)或磷酸铝 (adjuphos))接触形成悬浮液剂型,用以施用宿主。
166.含有cgrp肽免疫原构建体的药物组合物可用以于施用后在宿主中引发免疫反应并产生抗体。
167.c.免疫刺激复合物
168.本公开也关于含有与cpg寡核苷酸形成免疫刺激复合物的cgrp肽免疫原构建体的药物组合物。此种免疫刺激复合物特别适合作为佐剂和肽免疫原稳定剂。免疫刺激复合物呈微粒形式,其可有效地将cgrp肽免疫原呈现给免疫系统的细胞以产生免疫反应。免疫刺激复合物可配制成用于肠胃外施用的悬浮液。免疫刺激复合物还可配制成油包水(w/o)乳液形式,作为与矿物盐或原位凝胶聚合物结合的悬浮液,用于在肠胃外施用后将cgrp肽免疫原构建体有效递送至宿主免疫系统的细胞。
169.稳定化的免疫刺激复合物可藉由通过静电结合将cgrp肽免疫原构建体与阴离子型分子、寡核苷酸、多核苷酸或其组合复合而形成。稳定化的免疫刺激复合物可作为免疫原递送系统并入药物组合物中。
170.在某些实施方案中,将cgrp肽免疫原构建体设计成包含阳离子部份,其于范围为5.0至8.0的ph下带有正电荷。cgrp肽免疫原构建体或构建体的混合物的阳离子部份的净电荷计算是依据,每个离胺酸(k)、精胺酸(r)或组胺酸(h) 带有 1电荷,每个天门冬胺酸(d)或麸胺酸(e)带有
‑
1电荷,以及序列中其他氨基酸所带的电荷为0。将在cgrp肽免疫原构建体之阳离子部份中的电荷相加,并表示为净平均电荷。适合的肽免疫原具有净平均正电荷为 1的阳离子部份。较佳地,肽免疫原具有范围大于 2之净正电荷。在一些实施方案中,cgrp 肽免疫原构建体的阳离子部份为异源性间隔区。在某些实施方案中,当间隔区序列为(α,ε
‑
n)lys、(α,ε
‑
n)
‑
lys
‑
lys
‑
lys
‑
lys(seq id no:72)或 lys
‑
lys
‑
lys
‑
ε
‑
n
‑
lys(seq id no:73)时,cgrp肽免疫原构建体的阳离子部份具有 4的电荷。
171.如本文所述的“阴离子型分子”是指在范围为5.0至8.0的ph下带有负电荷的任何分子。在某些实施方案中,阴离子型分子是寡聚合物或聚合物。寡聚合物或聚合物上的净负电荷计算是依据,在寡聚合物中的每个磷酸二酯或硫代磷酸酯基团带有
‑
1电荷。适合的阴离子型寡核苷酸是具有8至64个核苷酸碱基的单链dna分子,cpg基序的重复数在1至10的范围内。较佳地,cpg免疫刺激性单链dna分子含有18至48个核苷酸碱基,cpg基序的重复数在3至8的范围内。
172.更佳地,阴离子型寡核苷酸可以分子式5
′
x1cgx23
′
表示,其中c和g是未甲基化的;且x1是选自由a(腺嘌呤)、g(鸟嘌呤)和t(胸腺嘧啶)组成的群组;且x2是c(胞嘧啶)或t(胸腺
id nos:74
‑
115)或任选的异源性间隔区。
182.方法
183.本公开也关于用以制备和使用cgrp肽免疫原构建体、组合物和药物组合物的方法。
184.a.cgrp肽免疫原构建体的制备方法
185.本公开的cgrp肽免疫原构建体可利用普通技术人员所熟知的化学合成方法加以制备(参见例如fields,et al.,1992)。cgrp肽免疫原构建体可利用自动化美利弗德(merrifield)固相合成法来合成,利用侧链受保护之氨基酸,以t
‑
boc 或f
‑
moc化学保护α
‑
nh2,在例如应用生物系统肽合成仪430a或431型(appliedbiosystems peptide synthesizer model 430a或431)上进行。包含th表位之组合数据库肽的cgrp肽免疫原构建体的制备可通过提供用于在给定可变位置进行偶联的替代性氨基酸的混合物而达成。
186.在欲求之cgrp肽免疫原构建体组装完成后,依照标准程序处理树脂,将肽从树脂上切下,并将氨基酸侧链上的官能基切除。可利用hplc纯化游离的肽,并利用例如氨基酸分析或定序以描述生化特性。肽的纯化和表征方法是本发明所属技术领域中具有通常知识者所熟知的。
187.可以控制和确定通过此化学过程所产生之肽的质量,且结果是cgrp肽免疫原构建体的再现性、免疫原性和产量可以获得保证。通过固相肽合成之 cgrp肽免疫原构建体的制备的详细描述显示于实施方案1中。
188.已经发现允许保留欲求免疫活性之结构变异范围比起允许保留小分子药物特定药物活性或与生物来源药品共同产生的大分子中存在欲求活性及非欲求毒性的结构变异范围更具包容性。
189.因此,与欲求肽具有相似的色层分析和免疫学特性的肽类似物,不论是刻意设计或因合成过程错误而无法避免地作为删除序列副产物的混合物产生的,其通常如经纯化之欲求的肽制剂具有相同的效果。只要建立严格的qc程序,以监控制备过程与产品评估过程,确保使用这些肽之终产物的再现性与功效,则经设计的类似物与非预期的类似物的混合物也是有效的。
190.也可利用包括核酸分子、载体及/或宿主细胞的重组dna技术来制备 cgrp肽免疫原构建体。因此,编码cgrp肽免疫原构建体及其免疫功能类似物的核酸分子也包括在本公开中作为本发明的一部分。类似地,包含核酸分子的载体(包括表现载体)以及含有载体的宿主细胞也包括在本公开中作为本发明的一部分。
191.各种例示性实施方案也包括制备cgrp肽免疫原构建体及其免疫功能类似物的方法。例如,方法可包括在表现肽及/或类似物的条件下培养宿主细胞之步骤,宿主细胞包含含有编码cgrp肽免疫原构建体及/或其免疫功能类似物之核酸分子的表现载体。较长的合成肽免疫原可利用公知的重组dna技术来合成。这些技术可于具有详细实验计划之众所周知的标准手册中加以提供。为了构建编码本发明肽的基因,将氨基酸序列反向转译以获得编码氨基酸序列的核酸序列,较佳地利用对于其中具有待表现基因的生物体来说最适合的密码子。接下来,通常通过合成编码肽和任何调节因子(如有必要的话)的寡核苷酸以制备合成基因。将合成基因插入适合的选殖载体内并转染到宿主细胞中。然后在适合所选表现系统和宿主的合适条件下表现肽。利用标准方法纯化肽并描述其特性。
192.b.免疫刺激复合物的制备方法
193.各种例示性实施方案还包括制备包含cgrp肽免疫原构建体和cpg寡脱氧核苷酸(odn)分子的免疫刺激复合物的方法。稳定化的免疫刺激复合物 (isc)衍生自cgrp肽免疫原构建体的阳离子部份和聚阴离子cpg odn分子。自行组合系统是由电荷的静电中和所驱动。cgrp肽免疫原构建体之阳离子部分对阴离子寡聚合物的莫耳电价比例的化学计量决定缔合的程度。cgrp肽免疫原构建体和cpg odn的非共价静电结合是完全可再现的过程。此肽/cpg odn免疫刺激复合物聚集体有助于呈现至免疫系统中“专业的(professional)”抗原呈现细胞(apc),因此可进一步增强复合物的免疫原性。在制备过程中,可轻易地描绘此些复合物的特征以控制质量。肽/cpg isc在体内具有良好的耐受性。设计这种包含cpg odn和cgrp肽免疫原构建体的新颖微粒系统,以利用与cpg odn使用相关的广义b细胞促有丝分裂(mitogenicity),但促进平衡的th
‑
1/th
‑
2型反应。
194.在公开的药物组合物中的cpg odn在由相反电荷静电中和所介导的过程中100%结合至免疫原,导致微米大小之微粒的形成。微粒形式允许来自cpg佐剂常规使用之cpg剂量的显著减少,不利的先天性免疫反应的可能性更低,且促进包括抗原呈现细胞(apc)在内的替代性免疫原处理途径。因此,此种剂型在概念上是新颖的,且通过替代的机制藉由促进免疫反应的刺激而提供潜在的优点。
195.c.药物组合物的制备方法
196.各种例示性实施方案还包括含有cgrp肽免疫原构建体的药物组合物。在某些实施方案中,药物组合物是利用油包水乳液和具有矿物盐的悬浮液的剂型。
197.为了使药物组合物可被广大群体所使用,安全性成为另一个需要考虑的重要因素。尽管在许多临床试验中都使用了油包水乳液,但基于其安全性,明矾仍然是制剂中使用的主要佐剂。因此,明矾或其矿物盐磷酸铝 (adjuphos)经常作为制剂中的佐剂供临床应用。
198.其他佐剂和免疫刺激剂包括3de
‑
o
‑
acylated monophosphoryl lipid a (mpl)或3
‑
dmp、聚合或单体氨基酸,例如聚麸胺酸或聚离胺酸。此种佐剂可以与或不与其他特定的免疫刺激剂一起使用,免疫刺激剂例如胞壁酰肽 (muramyl peptides)(例如n
‑
acetylmuramyl
‑
l
‑
threonyl
‑
d
‑
isoglutamine (thr
‑
mdp)、n
‑
acetyl
‑
normuramyl
‑
l
‑
alanyl
‑
d
‑
isoglutamine(nor
‑
mdp)、 n
‑
acetylmuramyl
‑
l
‑
alanyl
‑
d
‑
isoglutaminyl
‑
l
‑
alanine
‑2‑
(1
′‑2′ꢀ
dipalmitoyl
‑
sn
‑
glycero
‑3‑
hydroxyphosphoryloxy)
‑
ethylamine(mtp
‑
pe)、 n
‑
acetylglucsaminyl
‑
n
‑
acetylmuramyl
‑
l
‑
al
‑
d
‑
isoglu
‑
l
‑
ala
‑
dipalmitoxypropylamide(dtp
‑
dpp)theramide
tm
,或其他细菌细胞壁成份。水包油乳液包含mf59(参见van nest等人的专利申请案wo 90/14837,其通过引用整体并入本文),包含5%角鲨烯、0.5%tween 80,以及0.5%span 85(任选含有不同量的mtp
‑
pe),利用微射流机配制成次微米颗粒;saf,包含10%角鲨烯、0.4% tween 80、5%pluronic
‑
嵌段共聚合物l121,以及thr
‑
mdp,利用微射流化形成次微米乳液或利用漩涡震荡以产生大颗粒乳液;以及ribit
m
佐剂系统(ras) (ribi immunochem,hamilton,mont.),其包含2%角鲨烯、0.2%tween 80,以及一种或多种的细菌细胞壁成份,细菌细胞壁成份选自由monophosphoryllipida(mpl)、海藻糖二霉菌酸酯(tdm)以及细胞壁骨架(cws)组成的群组,较佳为mpl cws(detox
tm
)。其他佐剂包含弗氏完全佐剂(cfa)、弗氏不完全佐剂(ifa),以及细胞因子(例如介白素(il
‑
1、
il
‑
2和il
‑
12)、巨噬细胞群落刺激因子(m
‑
csf),以及肿瘤坏死因子(tnf
‑
α))。
199.佐剂的选择取决于含有佐剂之免疫原制剂的稳定性、给药途径、给药计划、佐剂对接受免疫之物种的功效,且在人类,药学上可接受的佐剂是指已经被相关监管机构批准或可批准用于人类给药的佐剂。例如单独明矾、mpl 或弗氏不完全佐剂((chang,et al.,1998),其通过引用整体并入本文)或其任选地所有组合适于人类施用。
200.组合物可包括药学上可接受的无毒载体或稀释剂,其被定义为通常用于配制供动物或人类给药的药物组合物的载体。选择稀释剂以免影响组合物的生物活性。此种稀释剂的范例是蒸馏水、生理磷酸缓冲盐水、林格氏液、葡萄糖溶液和汉克溶液。此外,药物组合物或剂型还可包含其他载体、佐剂或无毒的,非治疗性的,非免疫原性的稳定剂等。
201.药物组合物还可包括大的缓慢代谢的大分子(例如蛋白质、多醣类(例如甲壳素)、聚乳酸、聚乙醇酸和共聚合物(例如胶乳功能化琼脂糖(1atexfunctionalized sepharose)、琼脂糖(agarose)、纤维素等)、聚合氨基酸、氨基酸共聚物,以及脂质聚集体(例如油滴或脂质体)。另外,这些载体可作为免疫刺激剂(即佐剂)。
202.本发明的药物组合物可进一步包含合适的递送载体。合适的递送载体包括,但不限于,病毒、细菌、可生物降解的微球体、微粒、奈米粒子、脂质体、胶原蛋白微球和螺旋体(cochleates)。
203.d.药物组合物的使用方法
204.本公开也包括使用包含cgrp肽免疫原构建体之药物组合物的方法。
205.在某些实施方案中,包含cgrp肽免疫原构建体之药物组合物可用于治疗偏头痛。
206.在一些实施方案中,方法包含施用包含cgrp肽免疫原构建体之药学上有效剂量的药物组合物给有其需要的宿主。在某些实施方案中,方法包含施用包含cgrp肽免疫原构建体之药学上有效剂量的药物组合物给温血动物(例如人类、食蟹猕猴、小鼠),以引发可与人类cgrp蛋白(seq id no:1)或来自其他物种之cgrp蛋白(例如seq id nos:2和3)交叉反应的高特异性抗体。
207.在某些实施方案中,含有cgrp肽免疫原构建体的药物组合物可用于治疗偏头痛,如在体内辣椒素诱导的背侧血流模型所示。
208.e.体外功能分析和体内概念验证研究
209.由cgrp肽免疫原构建体在接受免疫的宿主中所引发的抗体可用于体外功能分析。这些功能分析包括但不限于:
210.(1)与cgrp蛋白(seq id nos:1
‑
3)的体外结合;
211.(2)体外抑制cgrp与其受体的结合;
212.(3)体外抑制细胞内camp升高;
213.(4)在小鼠体内抑制辣椒素诱导的背侧血流模型。
具体实施方案
214.(1)一种cgrp肽免疫原构建体,其具有约30个或更多个的氨基酸,以以下分子式表示:
215.(th)
m
‑
(a)
n
‑
(cgrp功能性b细胞表位肽)
‑
x
216.或
217.(cgrp功能性b细胞表位肽)
‑
(a)
n
‑
(th)
m
‑
x
218.或
219.(th)
m
‑
(a)
n
‑
(cgrp功能性b细胞表位肽)
‑
(a)
n
‑
(th)
m
‑
x
220.其中
221.th为异源性t辅助细胞表位;
222.a为异源性间隔区;
223.(cgrp功能性b细胞表位肽)为具有衍生自cgrp受体结合或活化区域的7至约30个氨基酸残基的b细胞表位肽,具有如表1所示cgrp(seqidnos:1
‑
3)之seqidnos:4
‑
13和15
‑
24;
224.x为氨基酸的α
‑
cooh或α
‑
conh2;
225.m为1至约4;以及
226.n为0至约10。
227.(2)如(1)所述的cgrp肽免疫原构建体,其中cgrp受体结合或活化区域是选自由seqidnos:4
‑
13和15
‑
24组成之群组。
228.(3)如(1)或(2)任一所述的cgrp肽免疫原构建体,其中异源性t辅助细胞表位是选自由seqidnos:74
‑
115组成之群组。
229.(4)如(1)所述的cgrp肽免疫原构建体,其中肽免疫原构建体是选自由seqidnos:120
‑
127和130
‑
180组成之群组。
230.(5)一种cgrp肽免疫原构建体,包含:
231.a.b细胞表位,其包含来自cgrp序列seqidnos:1至3的约7至约30个的氨基酸残基;
232.b.t辅助细胞表位,其包含选自由seqidnos:74
‑
115及其任意组合组成之群组的氨基酸序列;以及
233.c.任选的异源性间隔区,其是选自由氨基酸、lys
‑
、gly
‑
、lys
‑
lys
‑
lys
‑
、(α,ε
‑
n)lys、ε
‑
n
‑
lys
‑
lys
‑
lys
‑
lys(seqidno:72)、lys
‑
lys
‑
lys
‑
g
‑
n
‑
lys(seqidno:73)和pro
‑
pro
‑
xaa
‑
pro
‑
xaa
‑
pro(seqidno:71)及其任意组合组成之群组,
234.其中b细胞表位是直接或通过任选的异源性间隔区共价连接至t辅助细胞表位。
235.(6)如(5)所述的cgrp肽免疫原构建体,其中b细胞表位是选自由seqidnos:4
‑
13和15
‑
24组成之群组。
236.(7)如(5)所述的cgrp肽免疫原构建体,其中t辅助细胞表位是选自由seqidnos:78、77、80
‑
82、85、91、94、97、98
‑
99、106
‑
109、112及其任意组合组成之群组。
237.(8)如(5)所述的cgrp肽免疫原构建体,其中任选的异源性间隔区为(α,ε
‑
n)lys、g
‑
n
‑
lys
‑
lys
‑
lys
‑
lys(seqidno:72)、lys
‑
lys
‑
lys
‑
ε
‑
n
‑
lys(seqidno:73)或pro
‑
pro
‑
xaa
‑
pro
‑
xaa
‑
pro(seqidno:71),其中xaa为任意氨基酸。
238.(9)如(5)所述的cgrp肽免疫原构建体,其中t辅助细胞表位是共价连接至b细胞表位的氨基端。
239.(10)如(5)所述的cgrp肽免疫原构建体,其中t辅助细胞表位是通过任选的异源性间隔区共价连接至b细胞表位的氨基端。
240.(11)一种组合物,其包含如(1)所述的cgrp肽免疫原构建体。
241.(12)一种药物组合物,其包含:
242.a.如(1)所述的肽免疫原构建体;以及
243.b.药学上可接受的递送载体及/或佐剂。
244.(13)如(12)所述的药物组合物,其中
245.a.cgrp功能性b细胞表位肽是选自由seq id nos:4
‑
13和15
‑
24组成之群组;
246.b.异源性t辅助细胞表位是选自由seq id nos:74
‑
115组成之群组,以及
247.c.异源性间隔区是选自由氨基酸、lys
‑
、gly
‑
、lys
‑
lys
‑
lys
‑
、(α,ε
‑
n)lys、ε
‑
n
‑
lys
‑
lys
‑
lys
‑
lys(seq id no:72)、lys
‑
lys
‑
lys
‑
ε
‑
n
‑
lys(seq id no:73) 和pro
‑
pro
‑
xaa
‑
pro
‑
xaa
‑
pro(seq id no:71)及其任意组合组成之群组;以及
248.其中cgrp肽免疫原构建体与cpg寡脱氧核苷酸(odn)混合以形成稳定化的免疫刺激复合物。
249.(14)如(12)所述的药物组合物,其中
250.a.cgrp肽免疫原构建体是选自由seq id nos:120
‑
127和130
‑
180组成之群组;以及
251.其中cgrp肽免疫原构建体与cpg寡脱氧核苷酸(odn)混合以形成稳定化的免疫刺激复合物。
252.(15)一种用以在动物中产生针对cgrp之抗体的方法,其包含对动物施用如(12)所述的药物组合物。
253.(16)一种分离的抗体或其表位结合片段,其特异性地结合至seq id nos: 4
‑
13和15
‑
24的cgrp受体结合或活化区域。
254.(17)如(16)所述的分离的抗体或其表位结合片段,其结合至cgrp肽免疫原构建体。
255.(18)一种组合物,其包含如(16)所述的分离的抗体或其表位结合片段。
256.(19)一种用以在动物中预防及/或治疗偏头痛的方法,其包含对动物施用如(12)所述的药物组合物。
257.实施例1.cgrp相关肽的合成及其制剂的制备
258.a.cgrp相关肽的合成
259.描述了包含在cgrp肽免疫原构建体开发工作中用以合成cgrp相关肽的方法。以小规模量合成的肽用于血清学分析、实验室试验和田间试验,大规模(千克)量合成的肽则用于药物组合物的工业/商业生产。为了表位鉴定,以及为了筛选和选择用于有效靶向cgrp之治疗性疫苗中的最佳肽免疫原构建体,设计了具有长度为约10至70个氨基酸之序列的大量cgrp相关抗原性肽。
260.人类、小鼠、大鼠和猕猴物种之代表性全长cgrp(seq id nos:1
‑
3)、 cgrp肽片段,以及在各种血清学分析中供表位鉴定使用的10
‑
mer肽,列于表 1(seq id nos:1
‑
70)中。
261.将选择的cgrp b细胞表位肽通过合成方法连接至衍生自病原体蛋白(包括麻疹病毒融合蛋白(mvf)、b型肝炎表面抗原蛋白(hbsag)、流行性感冒病毒、破伤风梭菌,以及epstein
‑
barr病毒(ebv))之经周密设计的t辅助细胞(th) 表位肽(如表2所示(seq id nos:74
‑
115)),以制成cgrp肽免疫原构建体。th 表位肽是以单一序列(seq id nos:74
‑
84、86
‑
90、92
‑
93、95
‑
96、98
‑
115)或组合数据库(seq id nos:85、91、94和97)形式使用,以增强
其各自cgrp肽免疫原构建体的免疫原性。
262.表3(seq id nos:116
‑
180)中鉴定了选自数百种肽构建体的代表性cgrp 肽免疫原构建体。用于供抗cgrp抗体侦测及/或测量之免疫原性研究或相关血清学测试的所有肽是在应用生物系统肽合成仪430a、431及/或433型上利用 f
‑
moc化学小规模合成。每一个肽是通过在固相载体上的独立合成所制备,在三官能基氨基酸的氨基端与侧链保护基团具有f
‑
moc保护。将完整的肽从固相载体上切下,并用90%三氟乙酸(tfa)移除侧链保护基团。利用基质辅助雷射脱附游离飞行时间(maldi
‑
tof)质谱仪评估合成的肽产物以确定正确的氨基酸组成。也利用反相hplc(rp
‑
hplc)评估各个合成肽以确认产物的合成样态与浓度。尽管严格控制合成过程(包括逐步地监测偶合效率),由于在延长循环中某些意外事件,包括氨基酸的插入、删除、取代及提前终止,仍可能产生肽类似物。因此,合成产物一般包括多种肽类似物与目标肽。
263.尽管包括这些非预期的肽类似物,但最后的合成肽产物仍可用作免疫应用,包括免疫诊断(作为抗体捕捉抗原)与药物组合物(作为肽免疫原)。一般来说,只要开发一严格的qc程序来监测制备过程及产品质量评估程序,以确保使用这些肽之最终产物的再现性与功效,此肽类似物,包括刻意设计或合成程序中产生的副产物混合物,通常可如欲求肽的纯化产物同样有效。可利用客制的自动肽合成仪ubi2003或类似机型以15mmole至150mmole的规模合成数百至数千克的大量肽。
264.对于供临床试验之最终药物组合物使用的活性成分,可利用预备的 rp
‑
hplc于浅洗提梯度下纯化cgrp相关肽免疫原构建体,并利用 maldi
‑
tof质谱、氨基酸分析和rp
‑
hplc描绘纯度与一致性的特性。
265.b.含有cgrp肽免疫原构建体之组合物的制备
266.制备采用油包水乳液和具有矿物盐之悬浮液的剂型。为了设计药物组合物供广大族群使用,安全性成为另一个需要考虑的重要因素。尽管在人类许多药物组合物的临床试验中使用油包水乳液,但基于其安全性,明矾仍然是用于药物组合物中的主要佐剂。因此,明矾或其矿物盐adjuphos(磷酸铝) 经常作为佐剂供临床应用制剂的使用。
267.简而言之,在以下描述的每个实验组中所指定的剂型通常包含所有类型专门设计的cgrp肽免疫原构建体。利用代表免疫原b细胞表位肽之相对应 cgrp肽,针对其相对免疫原性,于天竺鼠中仔细评估超过200种专门设计的 cgrp肽免疫原构建体。利用涂覆选自seq id nos:1
‑
70之肽的孔盘以elisa 试验在各种同源性肽中分析表位鉴定和血清学交叉反应。
268.如指定,利用经核准供人类使用的油剂seppic montanide
tm isa 51以油包水乳液形式,或与矿物盐adjuphos(磷酸铝)或alhydrogel(明矾) 混合,以配制不同量的cgrp肽免疫原构建体。通常利用将cgrp肽免疫原构建体以约20至2000μg/ml浓度溶解于水中,并与montanide
tm isa 51配制成油包水乳液(1∶1体积),或者与矿物盐adjuphos或alhydrogel(明矾) (1∶1体积)配制,以制成组合物。将组合物置于室温下约30分钟,并在免疫接种前利用漩涡震荡混合约10至15秒。利用2至3个剂量的特定组合物免疫接种动物,其在时间0(初次免疫)和初次免疫后(wpi)3周(加强免疫)施用,任选5或 6wpi进行第二次加强免疫,通过肌内途径投药。然后利用选定的b细胞表位肽测试来自接受免疫接种之动物的血清,以评估存在于剂型中的各种cgrp 肽免疫原构建体的免疫原性,以及相对应血清与cgrp蛋白的交
叉反应性。针对其相对应血清的功能特性,将最初在天竺鼠筛选中发现的那些具有强免疫原性的cgrp肽免疫原构建体在体外实验中做进一步测试。然后,以油包水乳液、矿物盐和基于明矾的配方制备所选的候选cgrp肽免疫原构建体按照免疫方案在指定的特定期间内进行给药方案。
269.在试验用新药申请之后于患有偏头痛之患者中进行临床试验的提交准备中,只有最有希望的cgrp肽免疫原构建体会在被纳入供于glp指导的临床前研究中针对免疫原性、持续时间、毒性和功效研究之最终剂型之前会进行进一步广泛的评估。
270.以下实施例是用于说明本发明,且不用以限制本发明的范围。
271.实施例2.血清学试验和试剂
272.以下详细描述用以评估cgrp肽免疫原构建体及其制剂之功能性免疫原性的血清学试验和试剂。
273.a.供免疫原性和抗体特异性分析之基于cgrp或cgrp b细胞表位肽的 elisa试验
274.开发并于下文描述于以下实施例中所述用以评估免疫血清样品的elisa 试验。利用配制于ph 9.5之10mm碳酸氢钠缓冲液(除非另有说明)中浓度为2 μg/ml(除非另有说明)的cgrp或cgrp b细胞表位肽等(seq id nos:1至70),将其以100μl体积于37℃下作用1小时,以分别地涂覆96孔盘的孔洞。
275.将以cgrp或cgrp b细胞表位肽涂覆的孔洞与250μl配制于pbs中浓度为3重量百分比的明胶于37℃下反应1小时,以阻断非特异性蛋白质结合位点,接着利用含有0.05体积百分比20的pbs洗涤孔洞三次并干燥。利用含有20体积百分比正常山羊血清、1重量百分比明胶和0.05体积百分比20的pbs以1∶20比例(除非另有说明)稀释待测血清。将100μl稀释样品(例如血清、血浆)加入每个孔洞并于37℃下反应60分钟。然后利用配制于 pbs中浓度为0.05体积百分比的20洗涤孔洞6次,以移除未结合的抗体。使用辣根过氧化物酶(hrp)共轭物种(例如天竺鼠或大鼠)特异性山羊多株抗igg抗体或蛋白质a/g作为标记的示踪剂,以在阳性孔洞中与形成的抗体/ 肽抗原复合物结合。将100微升hrp标记的侦测试剂以预滴定的最佳稀释倍数配制于内含1体积百分比正常山羊血清与0.05体积百分比20的pbs 中,将其加到每个孔洞中,并在37℃下再反应30分钟。利用内含0.05体积百分比20的pbs洗涤孔洞6次以移除未结合的抗体,并与100μl包含 0.04重量百分比3’,3’,5’,5
’‑
四甲基联苯胺(tmb)和0.12体积百分比过氧化氢于柠檬酸钠缓冲液中的受质混合物再反应15分钟。藉由形成有色产物利用受质混合物以侦测过氧化物酶标记。藉由加入100μl的1.0m硫酸终止反应并测定450nm处的吸光值(a
450
)。为了测定接受各种肽疫苗制剂之疫苗接种动物的抗体效价,将从1∶100至1∶10,000之10倍连续稀释的血清或从1∶100至1∶4.19x 108之4倍连续稀释的血清进行测试,且利用a
450
临界值设为0.5之a
450
的线性回归分析计算测试血清的效价,以log
10
表示。
276.b.利用基于th肽的elisa试验评估针对th肽的抗体反应性
277.以类似的elisa方法并如上所述进行,利用配制于ph 9.5之10mm碳酸氢钠缓冲液(除非另有说明)中浓度为2μg/ml(除非另有说明)的100μl th肽于 37℃下作用1小时,以分别地涂覆96孔elisa盘的孔洞。为了测定接受各种 cgrp肽疫苗制剂之疫苗接种动物的抗体效价,将从1∶100至1∶10,000之10倍连续稀释的血清进行测试,且利用a
450
临界值设为0.5之
a
450
的线性回归分析计算测试血清的效价,以log
10
表示。
278.c.通过基于b细胞表位簇10
‑
mer肽之elisa试验利用表位鉴定对目标cgrpb细胞表位肽进行精细特异性分析
279.利用基于b细胞表位簇10
‑
mer肽之elisa试验利用表位鉴定对来自利用cgrp肽免疫原构建体免疫接种之宿主的抗cgrp抗体进行精细特异性分析。简而言之,依照上述抗体elisa方法的步骤,以二重复方式,利用每孔洞每0.1ml含有0.5μg之个别cgrp或相关10
‑
mer肽(seqidnos:26
‑
70涂覆96孔盘的孔洞,然后将100μl血清样品(配制于pbs中,稀释倍数为1∶100)于10
‑
mer盘中进行反应。为了特异性确认,利用相对应cgrp肽或非相关的对照肽对来自接受免疫之宿主的抗cgrp抗体进行与目标b细胞表位相关精细特异性分析。
280.d.免疫原性评估
281.依照实验疫苗接种程序收集来自动物或人类个体的免疫前和免疫血清样品,并在56℃下加热30分钟以使血清补体因子失活。在施用疫苗制剂后,根据程序获得血液样品,并利用基于相对应cgrpb细胞表位肽的elisa试验评估其针对特定靶点的免疫原性。测试了连续稀释的血清,并将稀释倍数之倒数取对数(log
10
)以表示阳性效价。对于其能力(引发针对目标抗原内欲求表位特异性之高效价抗体反应和与cgrp蛋白高交叉反应性,且同时将针对用以提供欲求b细胞反应增强之“t辅助细胞表位”之抗体反应性维持在低至可忽略),而评估特定疫苗制剂的免疫原性。
282.实施例3.在针对细胞内camp产生之体外试验中评估利用cgrp肽免疫原构建体及其制剂所引发之抗体的功能特性
283.进一步测试免疫疫苗中之免疫血清或纯化的抗cgrp抗体抑制cgrp诱导的细胞内camp产生的能力。
284.a.抗体纯化
285.根据抗体纯化试剂盒(thermofisher,catno.89953)的使用手册,遵循所有抗体纯化程序。针对每个组别各自的igg纯化浓度仔细校正以用于体外测定。
286.b.细胞制备和维持
287.l6(crl
‑
1458
tm
)细胞株购自atcc。此细胞株的基础培养基是atcc配制的达尔伯克氏改良伊格尔氏培养基(dulbecco
′
smodifiedeagle
′
smedium),货号为30
‑
2002。加入胎牛血清至终浓度为10%以制成完整的生长培养基。并将其置于温度为37℃含有95%空气、5%co2的环境培养。
288.c.在有/无iggs状况下进行cgrp处理
289.使用基于细胞的camp活化测定针对体外中和活性进一步筛选抗cgrpiggs。所有步骤均在384孔圆底低体积微量盘(mediomics,llc货号163301)中进行。在抗cgrpigg(终浓度为1
‑
20μg/ml)存在下,将五微升的大鼠α
‑
cgrp(终浓度为10nm)在室温下反应30分钟。然后将配置于1xkrb
‑
ibms缓冲液中的大鼠l6肌肉细胞(体积为5微升,细胞数目为5000个)加入。将微量盘在室温下反应30分钟。
290.d.基于细胞的cgrp中和测试(camp水平检测)
291.在反应后,按照制备商的说明使用mediomicsbridge
‑
itcamp全合一(allinone)荧光测定(mediomics,货号122938/122939)进行camp活化。将10μl的camp全合一检测溶液添加到每个孔洞中,并通过上下吸液混合以裂解细胞与开始camp检测。覆盖微量盘以
避免蒸发和暴露于光线。将微量盘在室温下反应30分钟,通过荧光读取器(spectramax i3x multi
‑
modemicroplate reader)侦测荧光强度(以波长485nm激发,侦测540nm波长处的发散)。以百分比记录数据。0%代表仅有l6细胞,而100%代表cgrp处理的l6细胞。
292.实施例4.用于安全性、免疫原性、毒性和功效研究的动物
293.a.天竺鼠:
294.在成熟,未与抗原接触或未受抗原刺激的成年雄性和雌性 duncan
‑
hartley天竺鼠(300
‑
350g/bw)中进行免疫原性研究。实验中每一组使用至少3只天竺鼠。在联合生物医学公司(ubi)作为试验委托者之签订合约的动物设施依照经核准的iacuc申请进行涉及duncan
‑
hartley天竺鼠(8
‑
12周龄;covance research laboratories,denver,pa,usa)的试验计划。
295.b.食蟹猕猴:
296.在ubi作为试验委托者之签订合约的动物设施依照经核准的iacuc申请于成年雄性和雌性猴子(食蟹猕猴,约3
‑
4岁;昭衍新药研究中心,中国苏州) 进行免疫原性和重复剂量毒性研究。
297.c.小鼠
298.在辣椒素诱发(challenge)前于0、3、6、9、12wpi对雌性balb/c小鼠(n=6 只/组)注射5次,其是在一注射部位(后肢股四头肌)利用待测疫苗(40μg/0.1ml/ 剂)或对照品(0.1ml/剂)进行肌肉注射(im)。将动物饲养在联亚生技(ubi asia) 实验室的动物设施中,并在固定温度(22℃)、湿度(72%)、12小时光照/12小时黑暗周期之条件下适应环境1周。小鼠可随意进食鼠粮和水。所有试验计划均遵循实验动物护理原则。如试验计划所述进行采血。利用elisa分析针对抗 cgrp(小鼠)检测抗体效价。
299.实施例5.提供于天竺鼠中进行cgrp肽构建体免疫原性评估的疫苗制剂
300.在各个实验中使用的药物组合物和疫苗制剂如以下内容所示更加详细地描述。
301.简而言之,在每个实验组中所指定的剂型通常含有所有类型专门设计的 cgrp肽免疫原构建体,其具有cgrp b细胞表位肽片段,cgrp b细胞表位肽片段通过不同类型间隔区(例如εlys(εk)或lysine
‑
lysine
‑
lysine(kkk)以增强肽构建体的溶解度)连接至混杂t辅助细胞表位,混杂t辅助细胞表位包含衍生自麻疹病毒融合蛋白和b型肝炎表面抗原的两组人工t辅助细胞表位。cgrp b 细胞表位肽连接至专门设计的肽构建体的氨基端或羧基端。最初针对其与相对应cgrp b细胞表位肽的相对免疫原性在天竺鼠中对数百种专门设计的 cgrp肽免疫原构建体进行评估。如指定,将不同量的cgrp肽免疫原构建体配制于使用经核准供人类疫苗使用的油剂seppic montanide isa 51的油包水乳液中或使用矿物盐(adjuphos)或alhydrogel(明矾)的悬浮液中。通常利用将cgrp肽构建体以约20至800μg/ml浓度溶解于水中,并与 montanide isa 51配制成油包水乳液(1∶1体积),或者与矿物盐(adjuphos) 或alhydrogel(明矾)(1∶1体积)配制,以制成疫苗制剂。将疫苗制剂置于室温下约30分钟,并在免疫接种前利用漩涡震荡混合约10至15秒。
302.利用2至5个剂量的特定疫苗制剂免疫接种一些动物,其在时间0(初次免疫)和初次免疫后(wpi)3周(加强免疫)施用,任选5或6wpi进行第二次加强免疫,通过肌内途径投药。然后,针对在个别疫苗制剂中使用之相对应cgrp 肽免疫原构建体的免疫原性,以及针对其与相对应cgrp b细胞表位肽或全长 cgrp的交叉反应性,以评估这些接受免疫的动物。
针对在如免疫方案指定之特定期间内的给药方案,将在天竺鼠初次筛选中具有强免疫原性的那些cgrp 肽免疫原构建体在猕猴中以油包水乳液、矿物质盐类和以明矾为基底的制剂中进行进一步测试。
303.利用相对应小鼠cgrp肽免疫原构建体,针对其于小鼠中突破免疫耐受性的能力,只将最有希望的cgrp肽免疫原构建体候选物进行进一步广泛评估。在小鼠中具有最佳免疫原性的cgrp肽免疫原构建体,其可引发针对内源性 cgrp的抗cgrp抗体效价;特别是具有在小鼠模型中抑制辣椒素诱导的皮肤血流的能力。将优化的cgrp肽免疫原构建体纳入最终疫苗剂型中,提供在提交研究性新药申请准备之glp指导的免疫原性、持续时间、毒性和功效证明的研究中和在偏头痛患者进行的临床试验中使用。
304.实施例6.用于治疗偏头痛之包含cgrp肽免疫原构建体的多组分疫苗制剂的设计合理性、筛选、鉴定、功能特性评估和优化
305.基于第1至2图提供的科学信息,选择cgrp作为设计的目标分子和本发明的内容。第1图显示来自人类(seq id no:1)、猕猴(seq id no:2)、小鼠/大鼠(seq id no:3)和许多其他物种的cgrp序列的比对;第2图描述基于高精密度专门设计合成肽的疫苗发现到商业化的途径。第2图描述这些步骤的简要综述,并附有流程图,此流程图标识cgrp疫苗制剂从发现到商业化(工业化)的开发过程。对每个步骤的详细评估和分析,带来令人愉悦和令人不愉快的惊喜,在过往导致无数的实验,最终将导致安全且有效的cgrp疫苗制剂的商业化。
306.a.设计历史
307.每种肽免疫原构建体或免疫治疗产品都需要自己的设计重点和方法,设计重点和方法是基于其特定的疾病机制和干预所需的目标蛋白。对于偏头痛的治疗,根据如第1图概述的可用科学信息,选择cgrp作为目标分子。如第2 图所示,从发现到商业化的过程通常需要一至数十年才能完成。与用于干预之功能位点相关的cgrp b细胞表位肽的鉴定是免疫原构建体设计的关键。在各种制剂中包含各种t辅助细胞支持物(t helper support)(载体蛋白或合适的t 辅助细胞肽)在天竺鼠中进行连续的先导免疫原性研究,且之后在特定体外功能分析或于选定的动物模型所进行的体内概念验证研究中评估所引发纯化抗体或使用特定cgrp肽免疫原构建体之疫苗制剂的功能特性。经过广泛的血清学验证,然后在非人类灵长类动物中进一步测试候选cgrp b细胞表位肽免疫原构建体,以进一步验证cgrp肽免疫原设计的免疫原性和方向。然后以不同的混合物配制选择的cgrp肽免疫原构建体,以评估当组合使用时在肽构建体间与各自交互作用有关之功能特性的细微差异。经过额外的评估,确定最终的肽构建体、肽组合物及其制剂,以及制剂的各个物理参数,从而导致最终产品的开发过程。
308.基于多种设计理论选择cgrp肽免疫原构建体的氨基酸序列。这些理论中的几个包括使用cgrp b细胞表位肽序列,内容如下:
309.(i)cgrp内缺乏自体t辅助细胞表位以避免自体t细胞活化(如先前在治疗阿兹海默症使用靶向aβ1‑
42
之an1792疫苗的临床试验中所报导,自体t细胞活化可能导致大脑发炎,进而造成脑膜炎球菌性脑炎)。
310.(ii)本身是非免疫原性的,因为其为自身的分子;
311.(iii)当施用宿主时,通过使用蛋白质载体或有效的t辅助细胞表位,可以使其获得免疫原性;
312.(iv)引发针对cgrp肽序列(b细胞表位)且非针对蛋白质载体或有效的t 辅助细胞表位的高效价抗体;
313.(v)引发高效价的抗体,其可抑制由于cgrp和cgrp受体交互作用以及细胞活化所引起的细胞内camp升高;以及
314.(vi)此疫苗制剂在施用动物模型(例如balb/c小鼠)时可抑制辣椒素诱导的背侧血流,可作为治疗偏头痛的概念验证证据。
315.b.用于药物组合物之cgrp肽免疫原构建体的设计和验证,此药物组合物具有治疗偏头痛患者的潜力
316.为了产生最有效的肽构建体以包含进入药物组合物中,人类cgrp b细胞表位肽的组库(例如seq id nos:4
‑
24)和衍生自各种病原体或人工t辅助细胞表位的混杂t辅助细胞表位(例如seq id nos:74
‑
115)被进一步设计并制成例如代表性cgrp肽免疫原构建体(例如seq id nos:116
‑
180),提供最初用于天竺鼠的免疫原性研究。
317.i)从受体结合或受体活化区域中选择cgrp b细胞表位肽序列进行设计
318.选择位于cgrp中间/羧基端区域的cgrp受体结合区域和来自cgrp氨基端c2
‑
c7环状结构/中间区域的受体活化区域进行cgrp b细胞表位设计,然后进一步制成肽免疫原构建体以在天竺鼠引发免疫血清,免疫血清起初提供通过在cgrp b细胞表位肽涂覆的微量盘上利用elisa进行免疫原性测定,然后提供进行体外功能分析评估。
319.cgrp与cgrp受体结合后,cgrp受体会在细胞内传递活化讯号,从而在其他细胞事件中导致细胞内camp水平升高。当与缺乏抗体的对照组相比时,如第4图和在第3图内显示之表格所示,来自天竺鼠免疫血清针对特定 cgrp肽免疫原构建体之纯化的抗体具有能力去中和cgrp功能特性,能力评估为抑制50%的camp升高的ic
50
。
320.起初利用isa 51和cpg配制这些cgrp肽免疫原构建体,以400μg/1ml的剂量在天竺鼠中进行初次免疫,并以100μg/0.25ml的剂量进行加强免疫(3、6 和9wpi),供免疫原性研究。为了测试在天竺鼠中的免疫原性,使用elisa试验,将来自各次(wpi)采血的天竺鼠免疫血清以10倍连续稀释的方式从1∶100 稀释至1∶10000。以每孔洞0.5μg肽的量利用相对应小鼠/大鼠cgrp b细胞表位肽和全长cgrp肽涂覆elisa微量盘。利用a
450
临界值设为0.5之a
450
的线性回归分析计算测试血清的效价,以log
10
表示,如第3图所示,在表4、5和6则显示代表性b细胞表位衍生的cgrp肽免疫原构建体的详细效价。尽管设计的短cgrp肽由于其缺乏内源性th表位而通常是非免疫原性的,但是外源性th表位的添加可增强特定cgrp肽免疫原构建体的免疫原性。来自表4、5和6以及第3图之各种结构的反应性/特异性模式的详细分析可评估cgrp分子内某些残基所赋予的免疫原性,此有助于进一步设计最佳的肽免疫原构建体。
321.ii)在所选cgrp b细胞表位内缺乏自体t辅助细胞表位以避免自体t细胞活化
322.如表7所示,代表性的cgrp b细胞表位,例如具有seq id nos:5、6和15 的那些,当提供给对应物肽免疫原构建体使用于有效疫苗制剂中给药时,它们本身未引发针对cgrp的任何抗体,因此是在所选cgrp b细胞表位内缺乏非欲求内源性ths表位。
323.iii)利用cgrp肽免疫原构建体所引起的集中抗体反应仅靶向cgrp b 细胞表位
324.众所周知,用以加强针对标靶b细胞表位肽之免疫反应的所有载体蛋白 (例如钥孔血蓝蛋白(klh)、白喉类毒素(dt)和破伤风类毒素(tt)蛋白)),通过将这种b细胞表位肽
与各自载体蛋白化学共轭可引发超过90%的抗体是针对增强载体蛋白,而少于10%的抗体是针对免疫宿主中的标靶b细胞表位。
325.因此评估本发明cgrp肽免疫原构建体的特异性是重要的。两个代表的cgrp肽免疫原构建体(来自表9的seqidnos:142和143)具有来自cgrp20
‑
37和22
‑
37之不同长度的b细胞表位,b细胞表位通过间隔区序列连接至异源性t辅助细胞表位(seqidno:98),被制备用于抗原性评估。将(用于b细胞表位免疫增强作用之t辅助细胞表位肽)涂覆在微量盘上,并将天竺鼠的免疫血清用于测试与用于免疫增强作用之肽的交叉反应性。如表8所示,与这些结构对相对应目标cgrpb细胞表位肽的高免疫原性(即使仅注射一剂,针对cgrpb细胞表位所产生之抗体的高效价(>5log
10
)说明了这一点)形成鲜明对比,发现大多数(如果不是全部)免疫血清与肽无反应性。
326.总之,简单的免疫原设计(包含连接至精心选择的t辅助细胞表位的目标cgrpb细胞表位肽)可产生仅针对相对应cgrpb细胞表位肽的集中的免疫反应。对于药物组合物设计而言,其产生的免疫反应越具有特异性,则其为组合物提供的安全性越高。因此,本发明cgrp肽免疫原构建体为高特异性的,但对其b细胞目标是高度有效的。
327.iv)利用针对所选cgrp肽免疫原构建体的免疫血清进行精细的表位鉴定(epitopemapping)
328.如表9所示,在精细表位鉴定研究中,将抗体结合位点定位至在目标b细胞表位区域内的特定残基上,合成45个重迭的10
‑
mer肽(seqidnos:26
‑
70),其涵盖第
‑
9个氨基酸至第45个氨基酸的序列,涵盖cgrp分子加工前后cgrp的全长区域和前驱物序列。将这些10
‑
mer肽作为固相免疫吸附物分别涂覆至96孔微量盘上。将以1∶100稀释比例配制于样品稀释缓冲液中的汇集的天竺鼠抗血清加到利用2.0μg/ml的10
‑
mer肽涂覆的微量盘孔洞中,随后在37℃下培养1小时。在利用洗涤缓冲液洗涤微量盘孔洞后,加入辣根过氧化物酶(hrp)共轭重组蛋白a/g并培养30分钟。利用pbs再次洗涤后,将受质加入孔洞中,利用elisa微量盘式分析仪测量450nm处的吸光值,以二重复方式分析样品。cgrp肽免疫原所引发免疫血清与相对应cgrpb细胞表位肽涂覆孔洞的结合代表最大的抗体结合信号。
329.表9所示的精细表位鉴定结果显示,来自cgrp肽免疫原构建体seqidnos:122、123、127、129、130、132、137和139(包含来自源自氨基酸11至37之受体结合区域以及来自氨基酸1
‑
25、11
‑
25、8
‑
18、11
‑
35、11
‑
37、15
‑
37和18
‑
37之位于c2
‑
c7环状结构附近的抗体活化区域的cgrpb细胞表位肽)的汇集的天竺鼠血清诱导主要针对来自氨基酸1
‑
37(seqidno:1)之10
‑
mer肽簇的高效价抗体,与肽具有高度交叉反应,主要是与以下氨基酸有不同形式的交叉反应:1
‑
13是与b表位1
‑
25;15
‑
26是与b表位11
‑
25;非主要是与b表位8
‑
18;22
‑
33和26
‑
36是与b表位11
‑
35;23
‑
33和28
‑
37是与b表位11
‑
37;23
‑
33和28
‑
37是与b表位18
‑
37;22
‑
33和26
‑
36是与b表位11
‑
35;17
‑
26、20
‑
30和28
‑
37是与b表位15
‑
37。令人感兴趣的是发现,尽管采用了相同的b细胞表位来设计肽免疫原构建体seqidnos:123和130,但是与seqidno:130相比,seqidno:123只有间隔区差异(具有额外的kkk间隔区)。在结构seqidno:130(其具有较短的间隔区无kkk残基)中发现具有针对aas20
‑
30和aas26
‑
36的额外反应性。
330.总而言之,设计的合成cgrp肽免疫原构建体在天竺鼠中诱导了强大的免疫反应,
产生了针对cgrp中不同的10
‑
mer肽簇的多株抗体,这些10
‑
mer肽簇与各自羧基端附近的cgrp受体结合区域和位于c2
‑
c7环状结构附近的受体活化区域都非常接近,可提供重要的医学干预。表位鉴定和功能分析评估将允许鉴定用于疫苗制剂的最佳肽免疫原构建体。
331.实施例7.在体外模式下对利用cgrp肽免疫原构建体及其制剂所引发的抗体进行功能特性评估
332.如表4、5、6、7、8和9所示,在证明从利用精心挑选的候选cgrp免疫原构建体免疫之天竺鼠的免疫血清纯化而来的抗体具有高免疫原性和交叉反应性之后,设计了以下研究以评估来自每只动物在6wpi收集之这些免疫血清的代表性纯化的iggs能否能够抑制在cgrp与其受体结合后由于cgrp中c2
‑
c7 环状结构的活化而导致camp的细胞内升高。
333.在平滑肌细胞内的分子层次上,cgrp可通过其羧基端区域与其受体结合,然后通过使用其环状结构区域活化受体(参考文献)。具有双硫键之环状的 c2
‑
c7环状结构在受体活化中具有核心作用,受体活化与细胞内camp的升高密切相关。在中和测定中,使用多种抗cgrp iggs来表征其潜在的抗cgrp影响。具体地,使用细胞内camp水平的改变通过功能药理学评估效果。此体外功能评估对于评估那些针对本发明cgrp肽免疫原构建体之天竺鼠免疫血清的抗cgrp作用特别重要,在实施例4中详述测定方法。
334.利用抗cgrp抗体在cgrp活化的磷酸化中抑制细胞内camp升高
335.如实施例4所述收集来自每只动物之6wpi采血的免疫血清并纯化抗体。如实施例6所示,针对其个别免疫原性在天竺鼠中测试21种cgrp肽免疫原构建体。基于其在肽免疫原构建体中所使用的个别目标b细胞表位肽而将纯化的抗体分为三类。它们分别地针对来自氨基端区域、中间区域和羧基端区域的b 细胞表位肽。以在cgrp处理的l6细胞中检测到之camp的百分比记录数据。 0%代表仅l6细胞,而100%代表cgrp处理的l6细胞。如第4图以及随附的表格所示,对于camp水平而言,包含来自氨基端、中间或羧基端区域之cgrp b 细胞表位肽的结构展现从0.60至>20的ic
50
(μg/ml)。出于实际目的,我们使用小于10μg/ml的ic
50
作为显著的抗体介导的camp产生抑制。表现出有效功能免疫原性之代表性结构的排名(具有从低到高的ic
50
μg/ml)为seq id nos: 130>127>150>125>137>123>121>119>124>131>126>133>120> 129>135>116~117~118~128~139,且利用在cgrp 37
‑
mer结构中高达几个残基的精密度,我们可以描绘出cgrp肽免疫原构建体的最佳设计。
336.总之,如上所示之cgrp肽免疫原构建体在其个别功能特性的相对排名对于在后续cgrp疫苗制剂中的使用具有价值以证明功能性功效。
337.实施例8.作为cgrp疫苗概念验证研究在balb/c小鼠辣椒素诱导的皮肤血流模型以预防性模式对代表性小鼠cgrp肽免疫原构建体进行评估
338.a.试验理论基础
339.降钙素基因相关肽(cgrp)是37个氨基酸的肽,在中枢和周围神经系统中广泛表现。它主要与紧邻血管的小的无髓鞘感觉神经元有关。cgrp是有效的血管扩张剂,且局部施用cgrp会导致血液流量短暂增加。cgrp还与疼痛传播、疼痛调节和神经性炎症有关。利用辣椒素通过瞬态受体电位阳离子通道的活化可使cgrp从感觉神经元释放。
340.雷射都卜勒成像仪(ldi)已用于检测皮肤血流的结果变化,此变化已证明主要是由cgrp所引起。如同在多种疼痛模型中于cgrp敲除小鼠的减弱反应所证明cgrp也与炎症性疼痛相关。这种在疼痛感知中的作用与在感觉神经元中cgrp的表现是一致的。
341.在哺乳类动物的血浆中,cgrp的半衰期约为10分钟。在人类三叉神经节中,cgrp免疫反应性神经元占所有神经元的50%(tajti,et al.,1999)。通过使用抗cgrp疫苗接种方法靶向cgrp以治疗偏头痛可满足未被满足的医疗需求,其具有长期cgrp阻断的潜力在长的持续时间中具有经济效益地以预防模式治疗偏头痛。
342.设计此研究以在balb/c小鼠模型中测试人类cgrp肽免疫原构建体对应物之代表性对应物的鼠cgrp肽免疫原构建体,其在实施例7中鉴定为具有减少辣椒素诱导的皮肤血流的能力,此模型作为概念验证研究以说明抗cgrp 疫苗治疗偏头痛的功效。
343.b.试验没计
344.代表性试验项目:
345.以下列出本试验中使用的cgrp肽免疫原构建体疫苗制剂:
346.第1组:(seq id no:123)p4799kb:
347.以isa51和cpg3配制的
‑
aa11
‑
37(人类αcgrp)
348.第2组:(seq id no:141)p5154kb:
349.以isa51和cpg3配制的
‑
aa11
‑
37(人类αcgrp)
350.第3组:(seq id no:151)p5155kb:
351.以isa51和cpg3配制的
‑
aa11
‑
37(大鼠/小鼠αcgrp)
352.第4组:(seq id no:123)p4799kb:
353.以adjuphos和cpg3配制的
‑
aa11
‑
37(人类αcgrp)
354.第5组:(seq id no:131)p5144kb:
355.以isa51和cpg3配制的
‑
aa11
‑
25(人类αcgrp)
356.在表2中列出这些项目以及组别信息。
357.对照物质:
358.第6组:isa51和cpg3
359.第7组:adjuphos和cpg3
360.第8组:生理盐水
361.组别和剂量:
362.分组执行如下:
363.个体识别:
364.利用苦味酸(picric acid)记号识别受试动物。
365.组识别:
366.正确标记鼠笼以进行识别,标记包括试验名称、iacuc编号、给药途径、观察期间、笼号、每笼动物数量、种类、品系、性别、入室日期、入室周龄,动物编号、饲育人和代理人。
367.给药途径和注射部位:
368.在辣椒素诱发(challenge)前于0、3、6、9、12wpi对雌性balb/c小鼠(n=6 只/组)注射5次,其是在一注射部位(后肢股四头肌)利用待测疫苗(40μg/0.1ml/ 剂)或对照品(0.1ml/剂)进行肌肉注射(im)。
369.处理程序:
370.在处理过程中于0、3、6、9和12wpi总共注射5次对照品或试验项目。
371.生物样品的收集和制备:
372.在室温下静置至少30分钟至最多60分钟的时间将血液凝结在试管中,以分离血清与血凝块。通过使用冷冻离心机以1,000x g离心10分钟以移除血凝块。立即将血清转移到无菌的1.5ml微量离心管(聚丙烯管)中。在处理期间,将所有样品保持在湿冰上。未使用的血清样品在
‑
80℃下冷冻保存。
373.雷射都卜勒成像仪(ldi):
374.在实验当天,将小鼠的后背剃毛,并将小鼠置于位于ldi仪器下方的加热垫上。利用25mg/kg的舒泰(zoletil)诱导麻醉,并在扫描前将动物在麻醉下稳定约20分钟。以两次基线扫描作为开始之后是扫描系列。
375.将2μl辣椒素溶液(将50mg辣椒素配制于溶液中,此溶液含有83.4μletoh、55.6μl tween 20和27.8μl纯水,其以3∶2∶1比例配制)涂在置于动物后背之两个o形圈中的每一个上。每2.5分钟扫描一次,继续扫描10分钟。使用 moorvms
‑
ldf软件分析感兴趣区域的数据。利用excel工作表计算在每个时间点来自感兴趣区域的讯号的平均值。数据报告为始于基线之变化的百分比。
376.抗体效价的免疫学分析:
377.收集血清或csf样品,并使用全长人类cgrp进行抗原涂覆通过如实施例 2所示制备的elisa试剂盒测量抗cgrp抗体效价。将血清样品从起始稀释浓度1∶1000进行3倍连续稀释。利用自动微量盘读取仪侦测吸光值a
450
以测定抗体elisa效价,以log
10
表示。
378.c.试验结果
379.注射部位反应:
380.免疫程序有时会导致注射部位出现轻微且暂时性的肿胀。
381.来自接受免疫接种之小鼠免疫血清的抗体效价:
382.代表性的elisa结果显示,来自小鼠对应物的两个肽免疫原构建体(例如 seq id no:151)和cgrp肽免疫原构建体(seq id nos:132和141)不仅诱导针对其个别b细胞表位肽(seq id nos:15和9)的高免疫原性效价,也发现来自这两种免疫血清的抗体针对其同源全长人类cgrp具有中等交叉反应性,如第 5图所示。此研究表明,两种代表性cgrp肽免疫原能够诱导对人类cgrp b 细胞表位肽与其小鼠对应物肽具有交叉反应性的特定抗体。在此poc动物试验中,小鼠/大鼠cgrp b细胞表位肽免疫原构建体对应物使用(比更有效的组合th肽库)作为t辅助细胞肽以进一步增强所选结构在小鼠中的免疫原性(例如seq id no:132、134、136、138、140、141和151)以及连接符(例如seq id no:72)。
383.ldi结果:
384.用于皮肤血流测量的辣椒素模型在动物和人类中都是体内药效动力学模型。它是非侵入性的,技术上并不复杂,并且给出了快速且客观的结果变量。此模型可被重复测试,且测量结果具有足够的再现性。因此,此模型为cgrp 阻断疗法的临床评估提供理想的评估方法。就像所有其他生物标志物模型一样,此模型也有其局限性。辣椒素模型仍然是所欲研究项目之自然发生的病理生理过程的模拟。药物或疫苗诱导的抗体对辣椒素诱导的皮肤血流的影响可能会提供抗cgrp活性的趋势,这表明它们抑制外周皮肤血流的功效。
385.如第6图所示,当与生理盐水或各种单独佐剂制剂的对照品相比时,配制于含有cpg之adjuphos和isa51制剂中具有seq id nos:123、131、141和 151的cgrp肽免疫原构建体均形成肽/cpg复合物,其在接受三次免疫接种后在接受疫苗接种的小鼠中引起显著且具特异性的抗cgrp抗体效价(log
10
从4 到6)。动物在8wpi、12wpi和14wpi进行测量,分别显示出对辣椒素诱导的皮肤微血管血流的抑制(第6图)。在所测量的时间内,这种抑制作用的持续时间持续14周。尽管在于免疫原性研究中之所选抗体制剂的效价或其针对个别抗体之camp抑制功效在体外分析测量中的相对应ic
50
s值中发现差异,但三种代表性cgrp肽免疫原构建体(例如seq id nos:123、131和141)及其制剂在于这些接受免疫接种的小鼠中具有相似的能力去减少辣椒素诱导的皮肤血流,此表明使用这些cgrp肽免疫原构建体治疗偏头痛的功效。
386.表1
387.用于血清学测定中的α
‑
cgrp及其片段的氨基酸序列
388.[0389][0390]
表2
[0391]
应用于设计α
‑
cgrp肽免疫原构建体的包括理想化人工th表位的病原体蛋白来源th表位的氨基酸序列
[0392][0393]
表3
[0394]
α
‑
cgrp肽免疫原构建体的氨基酸序列
[0395]
[0396][0397]
*
.肽通过与半胱氨酸二硫键与标出的半胱氨酸环化
[0398]
表4
[0399]
天竺鼠中α
‑
cgrp肽免疫原构建体的免疫原性评估
[0400]
[0401][0402]
表6
[0403]
天竺鼠中α
‑
cgrp肽免疫原构建体的免疫原性评估
[0404][0405]
表7
[0406]
免疫血清与全长cgrp的交叉反应
[0407][0408]
表8
[0409]
所选cgrp b表位序列内内源th表位的缺乏
[0410][0411]
表9
[0412]
天竺鼠中针对所选cgrp肽免疫原构建体的th表位部分的免疫原性评估
[0413]
[0414]
[0415]
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。