一种pd@nico2o4双功能纳米仿酶及其制备方法与应用
技术领域
1.本发明涉及重金属汞检测技术领域,尤其涉及一种pd@nico2o4双功能纳米仿酶及其制备方法与应用。
背景技术:
2.本发明背景技术中公开的信息仅仅旨在增加对本发明的总体背景的理解,而不必然被视为承认或以任何形式暗示该信息构成已经成为本领域一般技术人员所公知的现有技术。
3.纳米模拟酶/仿酶作为一种高效的仿生催化剂,具有较高的底物特异性、选择性和催化效率,稳定性高、能够在温和的条件下催化某些比色底物发生特殊的显色反应,从而使比色信号放大,已广泛应用仿生催化、生物传感和环境分析检测等领域。
4.汞是毒性和污染性最大的重金属污染物之一,在自然环境下无法降解或生物转变,容易在生物体内聚集,且具有很强的亲硫性能(如
‑
sh基团),从而使生物蛋白或生物酶变性、失活,严重威胁着人类的健康。为此,世界卫生组织限定饮用水中重金属汞的含量不能超过3.0
×
10
‑8mol/l。
5.然而,本发明人发现,目前常见的金属基纳米模拟酶存在组分相对简单、形貌单一、单功能催化性能等问题,因此,本发明人认为开拓一种组分与形貌协同效应强的多组分、多功能纳米模拟酶,探讨其在高效、便捷、灵敏的重金属汞离子检测应用,对有效消除其污染具有重要的意义。
技术实现要素:
6.针对上述的问题,本发明提出一种pd@nico2o4双功能纳米仿酶及其制备方法与应用,本发明在聚乙烯吡咯烷酮(pvp)的模板导向下合成了一种二维氧化钴镍稳定钯纳米四面体复合材料:pd@nico2o4,能够高效地对环境水、生物、医药等样品中的痕量重金属汞进行可视性比色检测。
7.具体地,为实现上述目的,本发明的技术方案如下所示:
8.在本发明的第一方面,公开一种pd@nico2o4纳米仿酶,包括:nico2o4基底、pd纳米颗粒,其中:所述pd纳米颗粒为四面体/三棱锥结构,其负载在所述nico2o4基底上。
9.进一步地,所述pd纳米颗粒与nico2o4基底之间通过pd与ni和/或co原子间的金属键作用连接。
10.进一步地,所述pd四面体纳米颗粒的粒径在10~15nm之间,通过pd、ni或co间的金属键共用自由电子作用,均匀分散在所述nico2o4基底的表面上,从而使pd@nico2o4具有纳米pd的氧化模拟酶和nico2o4的过氧化模拟酶性能,同时二者具有很好的协同增强效应;另外,pd四面体纳米颗粒具有不同的面、线、点催化活性位点,不同的表面能从而赋予了四面体的钯纳米粒子具有特殊的催化活性。
11.进一步地,所述nico2o4基底为二维片状结构,从而为pd纳米颗粒的负载提供超大
的比表面积。
12.在本发明的第二方面,公开一种pd@nico2o4纳米仿酶的制备方法,包括如下步骤:
13.(1)提供含有co
2
离子、ni
2
离子、pd
2
离子、聚乙烯吡咯烷酮的碱性混合液,加入乙二醇后混匀,得前驱体混合液。
14.(2)微波处理所述前驱体混合液,反应完成后分离出固体产物,去除聚乙烯吡咯烷酮形成的模板,即得。
15.进一步地,步骤(1)中,将co
2
离子源、ni
2
离子源、pd
2
离子源分散在中性聚乙烯吡咯烷酮溶液中,搅拌均匀后加入氨水和乙二醇继续搅拌,得所述前驱体混合液。
16.进一步地,所述co
2
离子源包括:co(no3)2、coso4、cocl2、co(ch3coo)2等中的至少一种。
17.进一步地,所述ni
2
离子源包括:ni(no3)2、niso4、nicl2、ni(ch3coo)2等中的至少一种。
18.进一步地,所述pd
2
离子源包括:na2pdcl4、k2pdcl4、pd(ch3coo)2、pdcl2等中的至少一种。
19.进一步地,步骤(1)中,所述co
2
离子、ni
2
离子、pd
2
离子、聚乙烯吡咯烷酮的比例为0.2~0.5mmol:0.1~0.4mmol:0.05~0.1mmol:160~300mg。
20.进一步地,步骤(1)中,所述碱性混合液通过加入氨水形成,可选地,所述氨水与乙二醇的体积比为100~500μl:10~50ml,所述氨水浓度为25~28%。在本发明中,所述氨水可以提供弱碱性环境,使ni/co离子形成氢氧化物,同时可以与pd
2
配位,形成四面体配合物。
21.进一步地,采用超声分散的方式将co
2
离子源、ni
2
离子源、pd
2
离子源分散在中性聚乙烯吡咯烷酮溶液中,促进各金属离子在聚乙烯吡咯烷酮溶液中的分散。
22.进一步地,步骤(2)中,所述微波处理的功率为450~700w,处理时间为10~25min。微波是一种特殊的自内而外的加热方式,通过微波处理,不仅加热快、反应均质、选择性高、还可以促进反应并改善所合成纳米晶体的结晶度等优点。
23.进一步地,步骤(2)中,离心分离出固体产物,然后用乙醇、水离心洗涤,完成后对固体产物真空干燥,即得目标产物pd@nico2o4纳米仿酶。
24.在本发明的第三方面,公开所述pd@nico2o4纳米仿酶在环境水、生物、医药等领域中的应用。
25.进一步地,所述应用为利用所述pd@nico2o4纳米仿酶进行重金属hg
2
的测试方法,包括如下步骤:
26.s1、在pd@nico2o4标准溶液中加入比色底物3,3’,5,5
’‑
四甲基联苯胺(tmb)、磷酸氢二钠
‑
柠檬酸缓冲溶液、h2o2、待测样品液,得待测液。
27.s2、观察所述待测液的颜色变化。
28.进一步地,步骤s1中,所述标准溶液为浓度0.1mg/ml的pd@nico2o4溶液。
29.进一步地,步骤s2中,所述颜色变化为浅蓝色到深蓝色的可视性颜色变化,即表示待测样品液中含有含hg
2
。
30.本发明pd@nico2o4‑
tmb体系仿酶检测重金属hg
2
的原理为:双功能纳米酶pd@nico2o4在空气中催化氧化3,3’,5,5
’‑
四甲基联苯胺(tmb)生成蓝色的氧化物oxtmb,其氧化
能力在h2o2存在下进一步加强,并在652nm处产生特征的紫外
‑
可见吸收峰。当有痕量重金属hg
2
存在下,由于其氧化电势大于pd氧化电势,pd@nico2o4中的pd0可以把hg
2
还原成单质汞,进一步在钯纳米表面形成pd
‑
hg合金,增强其纳米酶催化活性,pd@nico2o4‑
tmb体系的颜色进一步加深,652nm处紫外
‑
可见吸收峰加强。
31.与现有技术相比,本发明具有以下有益效果:
32.(1)采用在以中性聚乙烯吡咯烷酮(pvp)模板导向下,通过微波辅助优化合成了一种二维氧化钴镍复合四面体纳米钯仿酶(pd@nico2o4),其中:所述nico2o4基底通过ni和/或co原子上的空d轨道与pvp富电子的配位键作用负载在pvp模板上,由于pvp模板可溶,在合成后水离心洗涤的过程中可以方便地去除,而pvp模板可使nico2o4形成二维结构,避免形成无规则的纳米颗粒。四面体pd颗粒通过pd,ni或co间的金属键共用自由电子作用,均匀分散在所述nico2o4基底的表面上,从而使pd@nico2o4具有纳米pd的氧化模拟酶和nico2o4的过氧化模拟酶性能,同时二者具有很好的协同增强效应;另外,pd四面体纳米颗粒具有不同的面、线、点催化活性位点,不同的表面能从而赋予了四面体的钯纳米粒子具有特殊的催化活性。
33.(2)本发明合成的pd@nico2o4这种纳米仿酶具有良好的纳米模拟氧化酶活性或者模拟过氧化酶活性,即双功能纳米酶;尤其是在超痕量汞离子存在下,能够在室温和空气条件下即可快速催化氧化3,3’,5,5
’‑
四甲基联苯胺(tmb)生成蓝色的氧化物oxtmb,具有很强的视觉增敏效应,而且pd@nico2o4纳米仿酶的活性在h2o2存在下进一步加强,并在652nm处产生特征的紫外
‑
可见吸收峰,便于高效地对环境水、商用果汁饮料等中超痕量hg
2
的可视化检测,方便快捷,灵敏度高,检测结果准确。
34.(3)本发明这种pd@nico2o4纳米仿酶催化tmb和h2o2的米氏常数(km)分别为0.047mm和0.25mm,最大起始速率(vmax)分别为2.13
×
10
‑8m
·
s
‑1和3.08
×
10
‑8m
·
s
‑1。可用于环境水、生物、医药等样中痕量重金属汞的可视性比色检测,检出限可达9.5
×
10
‑
10
m,样品中hg
2
回收率97.4~102.6%之间,相对误差(rsd)小于3.7%,有效保证了模拟酶的催化活性以及重金属汞离子比色检测的灵敏度。
35.(4)经过测试,检测样品中常见的共存离子(如ag
、ba
2
、bi
3
、ca
2
、co
2
、cr
3
、cu
2
、fe
2
、fe
3
、k
、mn
2
、ni
2
、pb
2
、zn
2
等)对比色检测hg
2
无明显干扰,说明本发明合成的pd@nico2o4纳米仿酶具有良好的抗干扰性,表现出了对hg
2
优异的专一性和选择性。
附图说明
36.构成本发明的一部分的说明书附图用来提供对本发明的进一步理解,本发明的示意性实施例及其说明用于解释本发明,并不构成对本发明的不当限定。以下,结合附图来详细说明本发明的实施方案,其中:
37.图1为本发明第一实施例制备的pd@nico2o4纳米仿酶的tem。
38.图2为本发明第一实施例制备的pd@nico2o4纳米仿酶的元素分析eds;其中:插图为hr
‑
tem。
39.图3为本发明第一实施例制备的pd@nico2o4纳米仿酶的xps图谱(图a)、xrd图谱(图b)。
40.图4为本发明第一实施例制备的pd@nico2o4纳米仿酶在n2、o2、h2o2或o2/h2o2同时存
在下模拟酶活性对比和颜色变化图(插图)。
41.图5为体系ph、材料组份的摩尔比、反应温度、tmb浓度、h2o2浓度、反应时间对本发明第一实施例制备的pd@nico2o4纳米仿酶活性的影响曲线图。
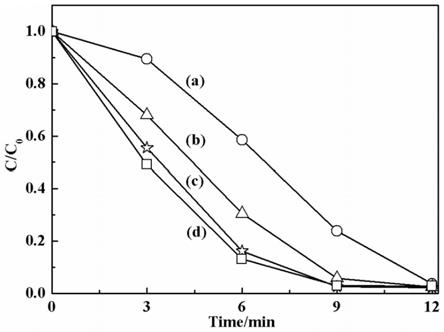
42.图6为本发明第一实施例制备的pd@nico2o4纳米仿酶的动力学曲线。
43.图7为本发明第一实施例制备的pd@nico2o4纳米仿酶随h2o2、tmb浓度变化的双倒数曲线图;其中:c图为tmb浓度变化的双倒数曲线图,d图为h2o2浓度变化的双倒数曲线图。
44.图8为不同的干扰离子(ag
、ba
2
、bi
3
、ca
2
、co
2
、cr
3
、cu
2
、fe
2
、fe
3
、k
、mn
2
、ni
2
、pb
2
、zn
2
)对第一实施例制备的pd@nico2o4纳米仿酶的光谱性能的影响(a图)和比色性能图(b图)。
45.图9为干扰离子与hg
2
共存时,对本发明第一实施例制备的pd@nico2o4纳米仿酶光谱性能的影响图。
46.图10为比色传感重金属hg
2
的光谱滴定曲线,其中:从上到下曲线代表的依次为hg
2
浓度依次为:0、0.4、0.8、1.6、2.4、4.0、6.0、10.0、15.0、20.0、38.0、64.0、80.0、100.0、120.0
×
10
‑8m,插图为颜色变化图片。
47.图11为本发明第一实施例制备的pd@nico2o4纳米仿酶的吸光强度(a
653
)和汞离子的浓度(c
hg2
)间的线性关系。
具体实施方式
48.在接下来的描述中进一步阐述了本发明的具体细节用于充分理解本发明。本发明中的说明书所使用的术语只是为了用于说明本发明的优点和特点,不是旨在于限制本发明。
49.除非另行定义,本发明中所使用的所有专业与科学术语属于本发明的技术领域的技术人员所理解的含义相同。如无特殊说明,本发明所使用的药品或试剂均按照产品说明书使用或采用所属领域的常规使用方法。现根据说明书附图和具体实施方式对本发明的技术方案作进一步说明。
50.第一实施例
51.一种pd@nico2o4双功能纳米仿酶的制备方法,包括如下步骤:
52.(1)准确称取116.4mg(0.4mmol)co(no3)2·
9h2o、58.2mg(0.2mmol)ni(no3)2·
6h2o和9.8mg(0.067mmol)na2pdcl4超声分散于5ml 40mg/ml的中性聚乙烯吡咯烷酮(pvp,m
w
30000)溶液中。连续搅拌10min后,加入质量浓度为25%的氨水300μl和乙二醇30ml继续搅拌1h,得到前驱体混合液。
53.(2)将步骤(1)得到的前驱体混合液转移至微波合成仪中,微波(600w、140℃)反应20min,冷却至室温后,用乙醇和水各离心(转速为6000rpm)洗涤3次,除去模板pvp,然后在60℃对离心得到的固体产物进行真空干燥,即得pd@nico2o4纳米仿酶。
54.第二实施例
55.一种pd@nico2o4双功能纳米仿酶的制备方法,包括如下步骤:
56.(1)准确称取0.5mmol coso4·
7h2o、0.4mmol niso4·
7h2o和0.1mmol pd(ch3coo)2超声分散于7.5ml 40mg/ml的中性聚乙烯吡咯烷酮(pvp,m
w
30000)溶液中。连续搅拌15min后,加入质量浓度为25%的氨水500μl和乙二醇50ml继续搅拌1h,得到前驱体混合液。
57.(2)将步骤(1)得到的前驱体混合液转移至微波合成仪中,微波(700w、140℃)反应10min,冷却至室温后,用乙醇和水各离心(转速为6000rpm)洗涤3次,除去模板pvp,然后在60℃对离心得到的固体产物进行真空干燥,即得pd@nico2o4纳米仿酶。
58.第三实施例
59.一种pd@nico2o4双功能纳米仿酶的制备方法,包括如下步骤:
60.(1)准确称取0.2mmol cocl2·
6h2o、0.1mmol nicl2·
6h2o和0.05mmol pdcl2·
2h2o超声分散于4ml 40mg/ml的中性聚乙烯吡咯烷酮(pvp,m
w
30000)溶液中。连续搅拌10min后,加入质量浓度为28%的氨水100μl和乙二醇10ml继续搅拌1h,得到前驱体混合液。
61.(2)将步骤(1)得到的前驱体混合液转移至微波合成仪中,微波(450w、140℃)反应25min,冷却至室温后,用乙醇和水各离心(转速为6000rpm)洗涤3次,除去模板pvp,然后在60℃对离心得到的固体产物进行真空干燥,即得pd@nico2o4纳米仿酶。
62.性能表征、测试:
63.1、采用透射电镜对第一实施例制备的pd@nico2o4纳米仿酶进行微观观察和成分检测,结果如图1至图3所示。从图1可以看出制备的pd纳米颗粒为四面体结构,分散地均匀分散在二维nico2o4基底上,粒径10~15nm,其中,所述二维nico2o4基底能够为pd纳米颗粒的负载提供超大的比表面积,从而提供大量催化反应活性位点,而四面体的钯纳米粒子具有特殊的催化活性。进一步地,从图2可以看出明显的0.225nm、0.240nm和0.250nm三种晶格间距,分别归属于pd的(111)晶面和nico2o4的(311)与(220
×
311)晶面。从图3a中可以看出xps图谱中包含了pd、co、ni、o所有元素;图3b可以看出二维nico2o4基底的特征晶体衍射信号(2θ=31.6,36.5,44.3,54.8,59.0,64.7和71.6)和纳米pd的特征晶体衍射信号(2θ=41.9,47.6and 67.9)。
64.2、第一实施例的pd@nico2o4纳米仿酶对重金属离子的检测能力测试,包括如下步骤:
65.(1)0.1mg/ml pd@nico2o4标准溶液的配制:称取0.01g所述pd@nico2o4样品,超声条件下将其分散到100ml纯净水中,配制成浓度为0.1mg/ml的pd@nico2o4标准溶液,在室温下避光保存,备用。
66.(2)hg
2
标准溶液的配制:向100ml容量瓶中加入0.0027g hgcl2,待完全溶解后,用水定容到100ml,配制出浓度为1.0
×
10
‑4mol/l,在室温下保存、备用。
67.(3)待测样品的制备:随机量取50.0ml尿样、环境水、商用果汁饮料和药剂样品各1份,经4μm的微孔过滤膜过滤三次,得到待测样品,将待测样品置于冰箱中(4℃)保存,备用。
68.(4)pd@nico2o4模拟氧化酶催化活性的测试:量取400μl(0.1mg/ml)pd@nico2o4ns标准溶液和100μl(1.5mm)tmb,置于3ml容量瓶中,充分混合,用磷酸氢二钠
‑
柠檬酸缓冲溶液(ph=4.0)定容至3.0ml,室温下陈化40min,测量紫外
‑
可见吸收光谱,测量250~800nm范围内的吸收光谱,记录652nm处的吸收强度(a
652
),并观察溶液颜色的变化。
69.(5)pd@nico2o4模拟过氧化酶催化活性的测试:量取400μl所述pd@nico2o4标准溶液,100μl(1.5mm)tmb和100μl(1.5mm)h2o2,置于3ml容量瓶中,充分混合,用磷酸氢二钠
‑
柠檬酸缓冲溶液(ph=4.0)定容至3.0ml,室温下陈化40min,测量紫外
‑
可见吸收光谱,测量250~800nm范围内的吸收光谱,记录652nm处的吸收强度(a
652
),并观察溶液颜色变化。
70.结果如图4所示,可以看出:在n2氛围中pd@nico2o4‑
tmb体系为无色,在652nm处吸
收强度很弱;在空气或h2o2存在的条件下,pd@nico2o4纳米仿酶能够在常温下催化氧化tmb成浅蓝的oxtem,在652nm处产生明显的紫外
‑
可见特征吸收峰;进一步在氧气存在下加入适量的h2o2,体系在652nm处的吸收强度及颜色明显增强。表明pd@nico2o4具有双功能纳米模拟氧化酶活性或者模拟过氧化酶活性,当氧气和h2o2同时存在下,具有很强的协同增强效应。
71.(6)酶活性实验条件的优化:为获得最佳的pd@nico2o4纳米仿酶催化活性,本试验探讨了体系ph、材料组份的摩尔比、反应温度、tmb浓度、h2o2浓度及反应时间等因素的影响,即按照上述(4)和(5)的方法,研究了ph(2.5~7.0)、pd:co摩尔比(1:10~1:4)、反应温度(20~50℃)、tmb含量(0.01~0.10mm)或h2o2(0.05~0.45mm)对pd@nico2o4纳米仿酶催化活性的影响。
72.结果如图5至图7所示,从图5中可以看出:优化条件下(ph=4.0,0.06mm的tmb,30℃下陈化40min或ph=4.0,0.09mm的tmb,0.30mm的h2o2,30℃下陈化40min),所述pd@nico2o4纳米仿酶具有良好的纳米模拟氧化酶活性或者模拟过氧化酶活性;从图6和图7中可以看出:所述pd@nico2o4纳米仿酶催化tmb和h2o2的米氏常数(k
m
)分别为0.047mm和0.25mm,最大起始速率(v
max
)分别为2.13
×
10
‑8m
·
s
‑1和3.08
×
10
‑8m
·
s
‑1,这意味着pd@nico2o4纳米仿酶具有良好的仿酶催化活性和催化速率,能够快速的催化tmb、h2o2等底物反应至完全,实现目标待测物的检测。
73.(7)图8和图9研究了常见环境金属离子对pd@nico2o4纳米仿酶的活性选择性,从图8和图9中可以看出,在微量重金属汞离子存在下,可协同催化氧化比色底物3,3’,5,5
’‑
四甲基联苯胺(tmb)生成蓝色的氧化物oxtmb,具有很强的视觉增敏效应;pd@nico2o4纳米仿酶的活性在痕量hg
2
存在下进一步加强,便于高效地对环境水、商用果汁饮料等中超痕量hg
2
的可视化检测。
74.同时,检测样品中常见的共存离子:ag
、ba
2
、bi
3
、ca
2
、co
2
、cr
3
、cu
2
、fe
2
、fe
3
、k
、mn
2
、ni
2
、pb
2
、zn
2
等对比色检测hg
2
无明显干扰,pd@nico2o4‑
tmb体系对hg
2
具有专一的选择性比色响应,并伴有从无色变为蓝色的颜色变化,从而使pd@nico2o4纳米仿酶能够在不需借助其他观察仪器的情况下,即可进行检测样品中精细微量元素的快速高效裸眼检测。
75.(8)酶催化比色检测汞离子含量的方法:取400μl所述pd@nico2o4标准溶液于3ml容量瓶中,加入180μl(1.5mm)tmb和200μl ph=4.0的磷酸氢二钠
‑
柠檬酸缓冲溶液、180μl(1.0m)h2o2和100μl 100μl不同浓度的hg
2
标准溶液或待测样品,混合均匀,并用磷酸氢二钠
‑
柠檬酸缓冲溶液(ph=4.0)定容至3.0ml,室温下陈放40min,测量300~800nm范围内的uv
‑
vis吸收光谱及颜色变化并相互对比。根据653nm波长处的吸光度(a
653
)与hg
2
浓度(c
hg2
)间的线性关系,计算待测样品中hg
2
的浓度。
76.结果如图10和图11所示,研究了pd@nico2o4‑
tmb体系在652nm处的吸收强度(a
652
)与c
hg2
之间的关系,结果表明:pd@nico2o4‑
tmb体系在652nm处的吸收强度(a
652
)对c
hg2
存在特殊的分区间线性比率关系,即:在0.0~50.0
×
10
‑9m c
hg2
范围内,线性回归方程为a
652
=0.0061c
hg2
0.3691(r2=0.9883);在50.0~400.0
×
10
‑9m c
hg2
范围内,线性回归方程为a
652
=0.0012c
hg2
0.6348(r2=0.9964),最低检测限低达9.5
×
10
‑
10
m。根据653nm波长处的吸光度(a
653
)与hg
2
浓度(c
hg2
)间的线性关系,计算待测样品中hg
2
的浓度。
77.(9)按照上述(8)酶催化比色检测汞离子含量的方法,对尿样、环境水、商用果汁饮
料和药剂样品中痕量重金属hg
2
进比色检测,结果见表1。
78.表1样品中痕量重金属hg
2
检测结果(n=5)
a
[0079][0080]
a
pb,ph 4.0,
[0081]
从表1的测试结果可以看出,样品中hg
2
回收率97.4~102.6%之间,相对误差(rsd)小于3.7%,这说明上所述pd@nico2o4纳米仿酶应用于尿样、环境水、商用果汁饮料和药剂样品中痕量重金属hg
2
时,具有方便快捷,灵敏度高,检测结果准确等特点,能够有效对样品中超痕量hg
2
进行检测。
[0082]
以上所述仅说明了本发明的几个实施方式,并不能因此而理解是对本发明专利范围的限制。应当指出,对于本领域的其他人员来说,在不脱离本发明的构思和范围的情况下,还可进行修改替换改进等,这些都属于本发明的保护范围。因此,本发明的专利保护范围应以所描述的根据权利要求为准。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。