一种三元复合光催化材料及其制备方法、及降解水中ppcps的方法
技术领域
1.本发明涉及光催化剂技术领域,特别涉及一种三元复合光催化材料及其制备方法、及降解水中ppcps的方法。
背景技术:
2.药品和个人护理用品(ppcps)是近年来出现的一类新型污染物,该类污染物浓度较低,但是结构复杂,具有较强的生物活性,其潜在危害不容忽视,因此日益受到人们关注。其中卡马西平(cbz)作为一种典型的抗癫痫药物,是ppcps中最有代表性的一种物质。由于卡马西平的广泛使用,导致其大量排放到环境中。此外,人类服用卡马西平后由于体内代谢作用以及卡马西平母体在环境中的降解会产生多种衍生物(即小分子中间物),这些衍生物的毒性可能比母体化合物强,并且更难以降解,因此研究卡马西平及其衍生物的环境行为及其去除十分重要。
3.利用半导体光催化剂的光催化高级氧化技术在降解ppcps日益受到重视,越来越多的新型催化剂被相继开发。半导体光催化剂在水体处理应用中的原理,是由于光对光催化剂的激发使得电子跃迁,从而产生光生载流子的电子和空穴,进而产生一些活性物质攻击ppcps从而达到降解ppcps的效果。
4.近年来,石墨化氮化碳(g
‑
c3n4)的光催化活性引起了人们的广泛关注,主要是由于g
‑
c3n4具有良好的化学稳定性及可直接利用可见光等优点,因而在光催化氧化环境污染物等方面具有广阔的前景。但是由于电子
‑
空穴易复合,使其光催化活性较低。
技术实现要素:
5.本发明的主要目的是提出一种三元复合光催化材料及其制备方法、及降解水中ppcps的方法,旨在解决现有光催化剂的电子
‑
空穴易复合的问题。
6.为实现上述目的,本发明提出一种三元复合光催化材料,所述三元复合光催化材料包括二氧化钛、石墨化氮化碳和铁纳米管,其中,以所述石墨化氮化碳为载体,所述铁纳米管和部分所述二氧化钛负载于所述石墨化氮化碳上,所述二氧化钛余下部分附着在所述铁纳米管上。
7.进一步地,本发明还提出一种如上所述的三元复合光催化材料的制备方法,该制备方法包括以下步骤:
8.s10、将fe(no3)2·
6h2o与三聚氰胺混匀,并粉碎,得到混合粉体,将所述混合粉体在氮气或惰性气体的保护下加热,升温至600~800℃后煅烧1~2h,然后冷却,得到粗产品,将所述粗产品纯化处理,得到铁纳米管;
9.s20、将石墨化氮化碳、二氧化钛、所述铁纳米管分散于无水乙醇中,得到悬浮液,将所述悬浮液进行干燥,得到固态的中间产物;
10.s30、将所述中间产物进行粉碎,然后在惰性气体或氮气气氛下,先升温至t1煅烧
30~60min,再继续升温至t2煅烧1~2h,得到三元复合光催化材料;
11.其中,所述t1为200~300℃,所述t2为300~500℃,且t1<t2。
12.可选地,在步骤s20之前,还包括以下步骤:
13.将三聚氰胺在500~600℃下煅烧3~8h,然后粉碎成粉末,得到石墨化氮化碳。
14.可选地,步骤s10中:
15.所述纯化处理包括:将所述粗产品在浓盐酸中浸泡20~28h后,再将所述粗产品水洗多次,得到铁纳米管。
16.可选地,步骤s10中:
17.所述fe(no3)2·
6h2o与三聚氰胺的质量比为0.5~2:0.5~6;和/或,
18.升温至600~800℃的过程中,升温速率为2~20℃/min。
19.可选地,步骤s20中:
20.所述石墨化氮化碳、二氧化钛、铁纳米管和无水乙醇的质量体积比为1.5~3.2g:2.4~6.3g:0.03g~0.15g:90~110ml。
21.可选地,步骤s20包括:
22.将石墨化氮化碳、二氧化钛、所述铁纳米管和无水乙醇混匀,然后超声分散20~40min,得到悬浮液;
23.将所述悬浮液边搅拌边在50~70℃下进行恒温干燥,得到固态的中间产物。
24.可选地,步骤s30中:
25.升温至t1的过程中,升温速率为3~5℃/min;和/或,
26.升温至t2的过程中,升温速率为3~5℃/min。
27.此外,本发明还提出一种降解水中ppcps的方法,即使用如上所述的三元复合光催化材料处理含ppcps的水溶液。
28.可选地,所述ppcps包括卡马西平。
29.本发明提供的技术方案中,所述三元复合光催化材料包括二氧化钛、石墨化氮化碳和铁纳米管,且所述铁纳米管和部分所述二氧化钛负载于所述石墨化氮化碳上,所述二氧化钛余下部分附着在所述铁纳米管上,通过铁纳米管对二氧化钛的掺杂,改变了二氧化钛的晶型结构、表面官能团、表面羟基等表面特性,不仅促进了三元复合光催化材料对可见光的吸收性能,同时还提高了其对ppcps初步降解后得到的小分子中间物的催化活性,从而大幅度提高了处理后的水溶液的矿化度;同时,由于石墨化氮化碳具备更窄的带隙能和更负的导带位置,如此,tio2与之耦合可发生异质电荷转移,利于光生电子
‑
空穴的分离,从而大幅度提高了其在可见光区的催化性能,使制得的三元复合光催化材料具有很好的循环稳定性和光催化活性。
附图说明
30.为了更清楚地说明本发明实施例或现有技术中的技术方案,下面将对实施例或现有技术描述中所需要使用的附图作简单地介绍,显而易见地,下面描述中的附图仅仅为本发明的一些实施例,对于本领域普通技术人员来讲,在不付出创造性劳动的前提下,还可以根据这些附图获得其他相关的附图。
31.图1为本发明提供的三元复合光催化材料的一实施例的sem图;
32.图2为本发明实施例1制得的三元复合光催化材料的tem图;
33.图3为本发明实施例1制得的三元复合光催化材料的傅里叶红外图像;
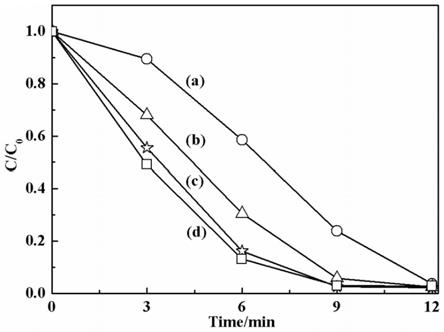
34.图4为本发明实施例和对比例制得的光催化材料在可见光下对卡马西平的降解效果图;
35.图5为本发明实施例1制得的光催化材料降解卡马西平的稳定性测试图;
36.图6为本发明对比例2制得的光催化材料降解卡马西平的稳定性测试图。
37.附图标号说明:
38.标号名称标号名称1铁纳米管2二氧化钛
39.本发明目的的实现、功能特点及优点将结合实施例,参照附图做进一步说明。
具体实施方式
40.为使本发明实施例的目的、技术方案和优点更加清楚,下面将对本发明实施例中的技术方案进行清楚、完整地描述。实施例中未注明具体条件者,按照常规条件或制造商建议的条件进行。所用试剂或仪器未注明生产厂商者,均为可以通过市售购买获得的常规产品。
41.另外,全文中出现的“和/或”的含义,包括三个并列的方案,以“a和/或b”为例,包括a方案、或b方案、或a和b同时满足的方案。此外,各个实施例之间的技术方案可以相互结合,但是必须是以本领域普通技术人员能够实现为基础,当技术方案的结合出现相互矛盾或无法实现时应当认为这种技术方案的结合不存在,也不在本发明要求的保护范围之内。基于本发明中的实施例,本领域普通技术人员在没有作出创造性劳动前提下所获得的所有其他实施例,都属于本发明保护的范围。
42.近年来,石墨化氮化碳(g
‑
c3n4)的光催化活性引起了人们的广泛关注,主要是由于g
‑
c3n4具有良好的化学稳定性及可直接利用可见光等优点,因而在光催化氧化环境污染物等方面具有广阔的前景。但是由于其光的利用率低及电子
‑
空穴易复合,使其应用受到限制。
43.鉴于此,本发明提出一种三元复合光催化材料,所述三元复合光催化材料包括二氧化钛(tio2)、石墨化氮化碳(g
‑
c3n4)和铁纳米管(cnfe),其中,以所述石墨化氮化碳为载体,所述铁纳米管和部分所述二氧化钛负载于所述石墨化氮化碳上,所述二氧化钛余下部分附着在所述铁纳米管上。
44.请参阅图1,在一实施例中,在三元复合光催化材料中,由于二氧化钛2是纳米颗粒,所以在铁纳米管1和石墨化氮化碳(图中未示出)上都附着有二氧化钛2,而石墨化氮化碳在这三者中是最大的,且为片状,因此,二氧化钛2和铁纳米管1又会附着在石墨化氮化碳片层上面。需要说明的是,在图1中,由于片状的石墨化氮化碳位于聚集的二氧化钛的下方,所以图中未示出。
45.其中,二氧化钛作为典型的半导体材料,原料易得、成本低、化学性好、稳定性高。石墨化氮化碳具有良好的化学稳定性及可直接利用可见光等优点,且具备比二氧化钛更窄的带隙能和更负的导带位置,二氧化钛与之耦合可发生异质电荷转移,
46.本发明提供的技术方案中,所述三元复合光催化材料包括二氧化钛、石墨化氮化
碳和铁纳米管,且所述铁纳米管和部分所述二氧化钛负载于所述石墨化氮化碳上,所述二氧化钛余下部分附着在所述铁纳米管上,其中,二氧化钛作为典型的半导体材料,原料易得、成本低、化学性好、稳定性高。石墨化氮化碳具有良好的化学稳定性及可直接利用可见光等优点,通过铁纳米管对二氧化钛的掺杂,改变了二氧化钛的晶型结构、表面官能团、表面羟基等表面特性,不仅促进了三元复合光催化材料对可见光的吸收性能,同时还提高了其对ppcps初步降解后得到的小分子中间物的催化活性,从而大幅度提高了处理后的水溶液的矿化度;此外,由于石墨化氮化碳具备比二氧化钛更窄的带隙能和更负的导带位置,如此,tio2与之耦合可发生异质电荷转移,利于光生电子
‑
空穴的分离,从而大幅度提高了其在可见光区的催化性能,使制得的三元复合光催化材料具有很好的稳定性和光催化活性。
47.基于上述目的,本发明还提出一种三元复合光催化材料的制备方法,在一实施例中,所述制备方法包括以下步骤:
48.步骤s10、将fe(no3)2·
6h2o与三聚氰胺混匀,并粉碎,得到混合粉体,将所述混合粉体在氮气或惰性气体的保护下加热,升温至600~800℃后煅烧1~2h,然后冷却,得到粗产品,将所述粗产品纯化处理,得到铁纳米管;
49.其中,fe(no3)2·
6h2o与三聚氰胺的质量比为0.5~2:0.5~6,使制得的铁纳米管(cnfe)的效果较好。具体地,在本实施例中,升温至600~800℃的过程中,升温速率为2~20℃/min。
50.具体地,所述纯化处理包括:将冷却后的所述粗产品在浓盐酸中浸泡20~28h后,再将所述粗产品水洗多次,得到铁纳米管。如此,可通过纯化处理以去除粗产品中的一些金属离子杂质。为了使去除杂质的效果较好,浓盐酸的摩尔浓度为2mol/l~5mol/l。
51.步骤s20、将石墨化氮化碳、二氧化钛、所述铁纳米管分散于无水乙醇中,得到悬浮液,将所述悬浮液进行干燥,得到固态的中间产物;
52.本发明不限制所述石墨化氮化碳的来源,可以按常规方法制得,在本实施例中,所述石墨化氮化碳按如下方式制得(也即,在步骤s20之前还包括以下步骤):将三聚氰胺在500~600℃下煅烧3~8h,然后粉碎成粉末,得到石墨化氮化碳。
53.具体地,将三聚氰胺放入带盖的氧化铝坩埚中,再放入马弗炉中在500~600℃下煅烧3~8h,再用玛瑙研钵研磨并收集粉末,得到石墨化氮化碳(g
‑
c3n4)。通过高温煅烧法,制得了纯的石墨化氮化碳,且通过将三聚氰胺放入带盖的氧化铝坩埚中,减少了在高温下的挥发损失。进一步地,在本实施例中,以2~10℃/min的升温速率升温至500~600℃,如此,制得的石墨化氮化碳的成型效果好,也即,制备得到的为长条状的石墨化氮化碳,而不是为一小节一小节断断续续的条状,从而使最终制得的三元复合光催化材料的催化活性较好。
54.本发明也不限制所述二氧化钛的来源,可以为购买得到的普通二氧化钛,也可以为纳米二氧化钛,可以理解的是,采用纳米二氧化钛制得三元复合光催化材料的催化活性更好。
55.其中,所述石墨化氮化碳、二氧化钛、铁纳米管和无水乙醇的质量体积比为1.5~3.2g:2.4~6.3g:0.03g~0.15g:90~110ml。
56.具体实施时,步骤s20包括:
57.步骤s21、将石墨化氮化碳、二氧化钛、所述铁纳米管和无水乙醇混匀,然后超声分
散20~40min,得到悬浮液;
58.通过超声分散方式,使石墨化氮化碳、二氧化钛和铁纳米管在无水乙醇中的分散效果较好。
59.步骤s22、将所述悬浮液边搅拌边在50~70℃下进行恒温干燥,得到固态的中间产物。
60.可以理解的是,所述惰性气体包括氩气,通过将混合粉体在氮气或惰性气体的保护下加热,避免了混合粉体碳化而导致无法得到铁纳米管。
61.步骤s30、将所述中间产物进行粉碎,然后在氮气或氩气气氛下,先升温至t1煅烧30~60min,再继续升温至t2煅烧1~2h,得到三元复合光催化材料。
62.其中,所述t1为200~300℃,所述t2为300~500℃,且t1<t2,通过梯度升温、并在不同温度下煅烧一段时间的方式,使中间产物可在t1温度下煅烧30~60min时成型,然后进一步对其进行煅烧,以使三元复合光催化材料中的铁纳米管、石墨化氮化碳和二氧化钛达到较优状态,从而使三元复合光催化材料(tcncnfe
‑
500
)的催化活性优良。
63.如果升温速率过快,会导致中间产物的煅烧不均匀,影响其最终得到的光催化材料的催化性能,如果升温速率过慢,升温所需时间较长,且制得的光催化材料的铁纳米管等组分的性能不好,从而影响其催化活性。在本实施例中,升温至t1的过程中,升温速率为3~5℃/min;和/或,升温至t2的过程中,升温速率为3~5℃/min,在此升温速率下,对中间产物的煅烧均匀,且所需时间适宜,制得的三元复合光催化材料的催化活性好。
64.此外,本发明还提出一种降解水中ppcps的方法,即使用如上所述的三元复合光催化材料处理含ppcps的水溶液。可以理解的是,所述三元复合光催化材料对ppcps均有一定的降解作用。
65.具体实施时,在反应器中加入含卡马西平的水溶液,其ph由0.1m hcl或naoh来调控,然后投入三元复合物光催化材料和过一硫酸盐(pms),在光照之前,在黑暗中进行吸附实验30min以实现cbz与光催化剂之间的充分接触建立吸附平衡,然后用可见光源照射,以降解水溶液中的卡马西平。
66.在本实施例中,ppcps包括卡马西平,本发明主要验证了三元复合光催化材料对卡马西平的降解效果,验证结果显示,其对卡马西平的降解效果好,且降解后的水溶液中的矿化度高。具体地,在所述三元复合光催化材料中,通过铁纳米管对二氧化钛的掺杂,改变了tio2晶型结构、表面官能团、表面羟基等表面特性,在促进过一硫酸盐(pms)在水中生成硫酸根自由基和羟基自由基的基础上,同时提高了对卡马西平初步降解得到的小分子中间产物的催化活性,从而大幅度提高了处理后的水溶液的矿化度。
67.以下结合具体实施例和附图对本发明的技术方案作进一步详细说明,应当理解,以下实施例仅仅用以解释本发明,并不用于限定本发明。
68.实施例1
69.(1)将20g三聚氰胺放入带盖的氧化铝坩埚中,再放入马弗炉中以5℃/min的升温速率升温至500℃并在此温度下煅烧5h,然后用玛瑙研钵研磨并收集粉末,得到g
‑
c3n4。
70.(2)称取2g fe(no3)2·
6h2o、2g三聚氰胺混匀,并研磨,得到混合粉体,将上述混合粉体在氮气保护下加热、以5℃/min的升温速率升温至700℃后煅烧1.5h,自然冷却至室温,得到粗产品,将得到的粗产品浸泡在200ml摩尔浓度为3mol/l的浓盐酸中24h,然后缓慢倒
掉浓盐酸,并将粗产品进行水洗数次,得到cnfe。
71.(3)将1.5g g
‑
c3n4、2.4g tio2、0.05mg cnfe和100ml无水乙醇混匀,然后超声分散30min,得到悬浮液,通过恒温加热搅拌器在60℃下将上述悬浮液边搅拌边进行恒温干燥,形成固态的中间产物。
72.(4)将上述制备的中间产物研磨成粉末,在氮气的保护下,以3℃/min的升温速率升温至300℃,煅烧50min,然后继续以3℃/min的升温速率升温至500℃,煅烧时间为2h,得到纳米颗粒,即三元复合光催化材料。
73.实施例2
74.(1)将20g三聚氰胺放入带盖的氧化铝坩埚中,再放入马弗炉中以2℃/min的升温速率升温至550℃并在此温度下煅烧5h,然后用玛瑙研钵研磨并收集粉末,得到g
‑
c3n4。
75.(2)称取0.5g fe(no3)2·
6h2o、3g三聚氰胺混匀,并研磨,得到混合粉体,将上述混合粉体在氩气保护下加热、以2℃/min的升温速率升温至600℃后煅烧2h,自然冷却至室温,得到粗产品,将得到的粗产品浸泡在200ml摩尔浓度为2mol/l的浓盐酸中28h,然后缓慢倒掉浓盐酸,并将粗产品进行水洗数次,得到cnfe。
76.(3)将3.2g g
‑
c3n4、6.3g tio2、0.03mg cnfe和110ml无水乙醇混匀,然后超声分散30min,得到悬浮液,通过恒温加热搅拌器在60℃下将上述悬浮液边搅拌边进行恒温干燥,形成固态的中间产物。
77.(4)将上述制备的中间产物研磨成粉末,在氮气的保护下,以3℃/min的升温速率升温至200℃,煅烧60min,然后继续以4℃/min的升温速率升温至600℃,煅烧时间为1h,得到纳米颗粒,即三元复合光催化材料。
78.实施例3
79.(1)将20g三聚氰胺放入带盖的氧化铝坩埚中,再放入马弗炉中以10℃/min的升温速率升温至600℃并在此温度下煅烧5h,然后用玛瑙研钵研磨并收集粉末,得到g
‑
c3n4。
80.(2)称取1g fe(no3)2·
6h2o、0.5g三聚氰胺混匀,并研磨,得到混合粉体,将上述混合粉体在氮气保护下加热、以20℃/min的升温速率升温至800℃后煅烧1h,自然冷却至室温,得到粗产品,将得到的粗产品浸泡在200ml摩尔浓度为5mol/l的浓盐酸中20h,然后缓慢倒掉浓盐酸,并将粗产品进行水洗数次,得到cnfe。
81.(3)将2.3g g
‑
c3n4、3.5g tio2、0.15mg cnfe和90ml无水乙醇混匀,然后超声分散30min,得到悬浮液,通过恒温加热搅拌器在70℃下将上述悬浮液边搅拌边进行恒温干燥,形成固态的中间产物。
82.(4)将上述制备的中间产物研磨成粉末,在氮气的保护下,以5℃/min的升温速率升温至250℃,煅烧30min,然后继续以5℃/min的升温速率升温至400℃,煅烧时间为1.5h,得到纳米颗粒,即三元复合光催化材料。
83.实施例4
84.(1)将20g三聚氰胺放入带盖的氧化铝坩埚中,再放入马弗炉中以7℃/min的升温速率升温至500℃并在此温度下煅烧5h,然后用玛瑙研钵研磨并收集粉末,得到g
‑
c3n4。
85.(2)称取2g fe(no3)2·
6h2o、6g三聚氰胺混匀,并研磨,得到混合粉体,将上述混合粉体在氩气保护下加热、以10℃/min的升温速率升温至700℃后煅烧1.5h,自然冷却至室温,得到粗产品,将得到的粗产品浸泡在200ml摩尔浓度为4mol/l的浓盐酸中25h,然后缓慢
倒掉浓盐酸,并将粗产品进行水洗数次,得到cnfe。
86.(3)将2.7g g
‑
c3n4、4.5g tio2、0.10mg cnfe和100ml无水乙醇混匀,然后超声分散30min,得到悬浮液,通过恒温加热搅拌器在50℃下将上述悬浮液边搅拌边进行恒温干燥,形成固态的中间产物。
87.(4)将上述制备的中间产物研磨成粉末,在氮气的保护下,以4℃/min的升温速率升温至300℃,煅烧40min,然后继续以4℃/min的升温速率升温至500℃,煅烧时间为1h,得到纳米颗粒,即三元复合光催化材料(tcncnfe
‑
500
)。
88.对比例1
89.将20g三聚氰胺放入带盖的氧化铝坩埚中,再放入马弗炉中以5℃/min的升温速率升温至500℃并在此温度下煅烧5h,然后用玛瑙研钵研磨并收集粉末,得到石墨化氮化碳(g
‑
c3n4)。
90.对比例2
91.称取2g fe(no3)2·
6h2o、2g三聚氰胺混匀,并研磨,得到混合粉体,将上述混合粉体在氮气保护下加热、以5℃/min的升温速率升温至700℃后煅烧1.5h,自然冷却至室温,得到粗产品,将得到的粗产品浸泡在200ml摩尔浓度为3mol/l的浓盐酸中24h,然后缓慢倒掉浓盐酸,并将粗产品进行水洗数次,得到铁纳米管(cnfe)。
92.对比例3
93.(1)将5g g
‑
c3n4、7.5g tio2和90ml无水乙醇混匀,然后超声分散30min,得到悬浮液,通过恒温加热搅拌器在70℃下将上述悬浮液边搅拌边进行恒温干燥,形成固态的中间产物。
94.(2)将上述制备的中间产物研磨成粉末,在氮气的保护下,以4℃/min的升温速率升温至300℃,煅烧40min,然后继续以4℃/min的升温速率升温至500℃,煅烧时间为1h,得到纳米颗粒,即得到g
‑
c3n4/tio2二元复合光催化材料。
95.应用实施例1
96.(1)在反应器中加入100ml含有卡马西平的水溶液,其ph由0.1m hcl或naoh来调控,初始卡马西平的浓度为5mg/l,ph值为7;
97.(2)向配制好的含有卡马西平的水溶液中投入过一硫酸盐(pms)和实施例1制得的三元复合光催化材料,其中,三元复合光催化材料(tcncnfe
‑
500
)的投加量为0.50g/l,pms的投加量为2mm,在光照之前,在黑暗中进行吸附实验30min以实现卡马西平与光催化剂之间的充分接触建立吸附平衡;
98.(3)将带有滤光片(400nm)的300w氙灯水平放置在反应器外作为可见光源,用光子密度计测得在反应器中反应溶液表面的平均光强为200mw/cm2即2个标准太阳光强(am3g)。为了保持恒定的反应温度,在反应器周围施加冷却水循环系统,并采用缓慢磁力搅拌进行实验。
99.通过高效液相色谱仪监测和分析溶液中卡马西平的浓度变化,检测结果如图4所示,图4表明,tcncnfe
‑
500
处理含有卡马西平的水溶液5min后,卡马西平的残余率(残余率=卡马西平的残余量/初始量)为0,也即实施例1制得的三元复合光催化材料在5min后对卡马西平的去除率高达100%。
100.应用对比例1
101.步骤与应用实施例1相同,不同之处在于,将步骤(2)中的实施例1制得的三元复合光催化材料替换为对比例1制得的石墨化氮化碳(投入量与三元复合光催化材料一样)。
102.通过高效液相色谱仪监测和分析溶液中卡马西平的浓度变化,检测结果如图4所示,图4表明,在5min后,卡马西平的残余率为98%,也即,对比例1制得的石墨化氮化碳对卡马西平的去除率仅为3%。
103.应用对比例2
104.步骤与应用实施例1相同,不同之处在于,将步骤(2)中的实施例1制得的三元复合光催化材料替换为对比例2制得的铁纳米管(投入量与三元复合光催化材料一样)。
105.通过高效液相色谱仪监测和分析溶液中卡马西平的浓度变化,实验结果如图4所示,图4表明,在5min后,卡马西平的残余率为0,也即,对比例2制得的铁纳米管对卡马西平的去除率仅为100%。
106.应用对比例3
107.步骤与应用实施例1相同,不同之处在于,将步骤(2)中的实施例1制得的三元复合光催化材料替换为对比例3制得的g
‑
c3n4/tio2(投入量与三元复合光催化材料一样)。
108.通过高效液相色谱仪监测和分析溶液中卡马西平的浓度变化,检测结果如图4所示,图4表明,在5min后,卡马西平的残余率为80%,也即对比例3制得的g
‑
c3n4/tio2对卡马西平的去除率仅为20%。
109.应用对比例4
110.步骤与应用实施例1相同,不同之处在于,将步骤(2)中的实施例1制得的三元复合光催化材料替换为市面上购买得到的普通二氧化钛纳米颗粒(投入量与三元复合光催化材料一样)。
111.通过高效液相色谱仪监测和分析溶液中卡马西平的浓度变化,检测结果如图4所示,图4表明,在5min后,卡马西平的残余率为98%,普通二氧化钛纳米颗粒在5min后对卡马西平的去除率仅为2%左右。
112.同时通过总有机碳(toc)分析仪测试卡马西平水溶液中矿化度,结果如表1所示。
113.表1不同应用例对卡马西平的矿化能力
[0114][0115]
由表1可以看出,应用对比例对卡马西平的矿化度均较低,而本发明实施例1制得的三元复合光催化材料对卡马西平的矿化度较好。
[0116]
将实施例1制得的三元复合光催化材料用扫描电子显微镜(sem)观察,结果如图1所示;同时将其用透射电子显微镜(tem)观察,结果如图2所示;将实施例1制得的三元复合光催化材料用傅里叶红外光谱仪进行检测,结果如图3所示。
[0117]
由图1可以看出,经过铁纳米管掺杂的修饰,tio2/g
‑
c3n4依旧保持了原来的片状和颗粒形貌。
[0118]
由图2可以看出,二氧化钛能够在片状的石墨化氮化碳上均匀分布,明显抑制了二氧化钛的团聚。
[0119]
由图3可以看出,二氧化钛和石墨化氮化碳的特征官能团均在三元复合光催化材料(tcncnfe
‑
500
)中体现。
[0120]
进一步地,将实施例1制得的三元复合光催化材料按应用实施例1的方法进行循环稳定性实验,结果如图5所示,将对比例2制得的铁纳米管按应用实施例1的方法进行循环稳定性实验(每个循环的处理时间为5分钟),结果如图6所示:
[0121]
由图5可以看出,本发明实施例1制得的三元复合光催化材料,在连续5个循环后,处理含有卡马西平的水溶液5min后,卡马西平仅有10%以下的残余率,也即三元复合光催化材料依旧对卡马西平具有90%以上的去除率。由图6可以看出,本发明对比例2制得的铁纳米管,在第2个循环时,处理含有卡马西平的水溶液5min后,对卡马西平有33%的去除率,在第3个循环处理时,对卡马西平仅有10%的去除率,第4个循环时,仅有8%的去除率,第5个循环时,仅有1%的去除率。
[0122]
由上述内容可以看出,本发明实施例1制得三元复合光催化材料,光催化活性比对比例的石墨化氮化碳、普通二氧化钛纳米颗粒和g
‑
c3n4/tio2对卡马西平的去除率均更好,其矿化度也比对比例1
‑
4更好,而对比例2提供的铁纳米管虽然对卡马西平的去除率也较优,但其循环稳定性差,也即,实用性差,成本较高。
[0123]
需要说明的是,由于实施例2
‑
4的三元复合光催化材料的原理与实施例1一样,因此,其形貌结构以及催化性能也与实施例1差不多,在此不做赘述。
[0124]
综上所述,本发明通过对原料以及制备步骤、制备条件的设计,使制得的三元复合光催化材料对卡马西平的催化速率、矿化度均较好,且同时具有很好的循环稳定性和光催化活性,实用性强。
[0125]
以上仅为本发明的优选实施例,并非因此限制本发明的专利范围,对于本领域的技术人员来说,本发明可以有各种更改和变化。凡在本发明的精神和原则之内,所作的任何修改、等同替换、改进等,均应包括在本发明的专利保护范围内。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。