1.本发明涉及医药技术领域,具体涉及从传统中药樟科山胡椒属植物鼎湖钓樟(lindera chunii merr.)的干燥块根中分离得到的一种乌药烷型倍半萜并香叶基苯聚合物的制备方法及应用。
背景技术:
2.鼎湖钓樟(lindera chunii merr.)为樟科山胡椒属植物的干燥块根,在我国具有悠久的使用历史。本品苦、温,归肝、胃经,具有祛风杀虫、敛疮止血、行气宽中、散瘀止痛。主治疥癣痒疮,外伤出血,手足皲裂,跌打肿痛等病症。
3.宫颈癌指的是原发于宫颈上皮细胞的恶性肿瘤,是一种严重危害女性健康的恶性疾病,目前宫颈癌的发病率越来越高,20
‑
60岁的女性均有可能患上宫颈癌。
技术实现要素:
4.本发明的目的在于提供一种乌药烷型倍半萜并香叶基苯聚合物,及其制备方法与在抗肿瘤药物筛选方面的应用。该化合物分离自樟科山胡椒属植物鼎湖钓樟(lindera chunii merr.)的干燥块根,命名为lindechunisin a。该化合物的制备方法采用了天然产物化学领域较为成熟分离纯化手段,在实际操作中容易实现。经体外生物活性研究表明lindechunisin a对人宫颈癌细胞hela细胞具有一定的抑制作用。
5.一种乌药烷型倍半萜并香叶基苯聚合物,命名为lindechunisin a,其化学结构式如下所示:。
6.本发明还提供了上述乌药烷型倍半萜并香叶基苯聚合物的制备方法,包括如下步骤:(1) 将鼎湖钓樟干燥块根粉碎,获得粗粉,乙醇加热回流提取,滤过,合并提取液,浓缩,得到总浸膏;(2) 将步骤(1)的总浸膏分散于水中,然后用石油醚萃取,得到石油醚相提取物;(3) 将将步骤(2)的提取物先经过硅胶柱层析,石油醚
‑
丙酮梯度洗脱,薄层色谱检视后,得到a
–
g七个组分,组分e经过反相c
‑
18柱层析甲醇
‑
水梯度洗脱后,再分别经过反相c
‑
8乙腈
‑
水等度洗脱和反相c
‑
18甲醇
‑
水等度洗脱,得到乌药烷型倍半萜并香叶基苯聚合物lindechunisin a。
7.优选地,所述步骤(3)的石油醚
‑
丙酮梯度洗脱过程中,石油醚和丙酮的体积比为
100:0至0:100;所述甲醇
‑
水梯度洗脱中,甲醇和水的体积比为20:80至100:0。
8.优选地,所述步骤(3)的乙腈
‑
水等度洗脱的乙腈和水的体积比为50:50;甲醇
‑
水等度洗脱的甲醇和水的体积比为60:40。
9.最后本发明还提供了上述乌药烷型倍半萜并香叶基苯聚合物在制备抗肿瘤药物上的应用。
10.优选地,应用在制备治疗宫颈癌的药物上的应用。
11.本发明的有益效果:1. 新化合物本发明从樟科山胡椒属植物鼎湖钓樟的干燥块根中分离得到了1个结构新颖的乌药烷型倍半萜并香叶基苯聚合物,该类化合物在天然界中较为少见,本发明丰富了该类化合物的化学多样性,为化合物领域增加了1种新的化合物,也为鼎湖钓樟的化学分类学研究提供了新的证据。
12.2. 提取方法简单该化合物的制备方法都采用了天然产物化学领域较为成熟的技术手段,在实际操作容易实现。
13.3. 体外细胞毒活性体外生物活性实验表明,该化合物对hela细胞具有一定的抑制活性,即可用于制备治疗宫颈癌的药物。
附图说明
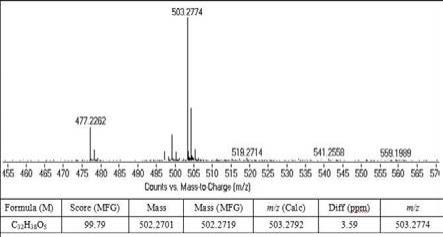
14.图1 化合物lindechunisin a的高分辨质谱;图2 化合物lindechunisin a的氢谱;图3化合物lindechunisin a的碳谱;图4 化合物lindechunisin a的1h
‑1h cosy 谱;图5 化合物lindechunisin a的hsqc谱;图6 化合物lindechunisin a的hmbc谱;图7 化合物lindechunisin a的noesy谱;图8 化合物lindechunisin a的紫外吸收图谱;图9 化合物lindechunisin a的圆二色谱;图10 化合物lindechunisin a的红外图谱。
具体实施方式
15.实施例1 lindechunisin a的制备提取:将樟科山胡椒属植物鼎湖钓樟(产于浙江丽水,8.0 kg)的干燥块根粉碎。过10目筛子,以80%乙醇回流提取3次,每次1至2小时,过滤合并提取液,提取液减压浓缩,提取浓缩液加水稀释后用等体积的石油醚萃取4次,减压回收溶剂分别得到石油醚相提取物。
16.分离:将上一步得到的石油醚相提取物(115.0 g)经硅胶柱层析,以体积比石油醚
‑
丙酮(100:0至0:100)梯度洗脱,进一步经过反相c18硅胶柱层析甲醇
‑
水(20:80至100:0)梯度洗脱,再经过半制备高效液相色谱c8柱分离乙腈
‑
水(50:50)洗脱,最后经过半制备
高效液相色谱c18柱分离甲醇
‑
水(60:40)得到lindechunisin a (3.0 mg)。
17.lindechunisin a[α]22.5 d
ꢀ–
25.7 (c 0.2, meoh);紫外光谱 (甲醇): λ
max (log ε): 195 (5.20), 320 (4.11);圆二色谱 (甲醇): 200 (δε 1.58) nm, 260 (δε
ꢀ–
1.27) nm, 315 (δε
ꢀ–
0.88) nm,红外光谱, ν
max
3743, 3438, 2362, 1646, 1517, 1427, 1342, 999 cm
‑1;lindechunisin a的氢谱和碳谱数据见表1;高分辨质谱 m/z 503.2774 [m h]
(计算值为 c
32
h
39
o5, 503.2792)。
[0018]
表1 lindechunisin a的氢谱和碳谱数据实施例2 体外细胞毒活性的测定采用四甲基偶氮唑蓝(mtt)法对化合物lindechunisin a进行细胞毒活性研究,用
含10%胎牛血清的培养液(dmem)配成5
×
105/ml的hela细胞悬液,每孔体积100 μl接种到96孔培养,培养24 h后加入待测化合物lindechunisin a,设置3个复孔。另设置阴性对照组(细胞培养液),每组均设置3个复孔。加入lindechunisin a后将培养板置于5% co2、37℃饱和湿度培养箱中培养48 h,每孔加入mtt溶液20 μl,继续孵育4 h后终止培养,弃上清液,每孔加入100 μl dmso溶液,使其充分溶解,将培养板放置在酶标仪上,选取波长为490 nm记录吸光度值,计算其相应的抑制率,在初筛中对肿瘤细胞生长抑制率设定4个浓度(12.5, 25, 50, 100 μmol/l),计算结果用spss 18.0软件得出半数抑制浓度(ic
50
)。体外细胞毒活性测定结果表明,该化合物对hela细胞具有一定的抑制作用,其ic
50 = 52.6 μmol/l。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。

