1.本发明属于医学检验技术领域,具体涉及一种消除羟苯磺酸钙干扰的游离脂肪酸测定试剂盒。
背景技术:
2.游离脂肪酸(non esterified fatty acid,nefa)是指血清中未与甘油、胆固醇等酯化的脂肪酸,又称非酯化脂肪酸或未酯化脂肪酸,在血浆中半衰期2
‑
3分钟,正常情况下,血浆中含量极少。血清中的nefa代谢活性极高,极易受脂肪代谢、糖代谢及内分泌代谢的影响。随着研究的深入和技术的不断进步,血清nefa与疾病的关系逐渐明晰,nefa已被证实与心脑血管、呼吸、消化、内分泌、免疫等系统疾病的发生发展,以及肿瘤和创伤性应激等的能量代谢关系密切。
3.乙酰辅酶a合成酶(acs)
‑
乙酰辅酶a氧化酶(acod)偶联的酶法测定法是目前临床测试nefa的主要方法,检测原理是人血清中游离脂肪酸和辅酶a在乙酰辅酶a合成酶的作用下反应生成脂酰辅酶a,脂酰辅酶a在乙酰辅酶a氧化酶的作用下生成h2o2,随后通过trinder’s反应在过氧化物酶的作用下生成有色物质。临床应用发现,该法极容易受羟苯磺酸钙干扰而使结果存在较大偏差甚至得出错误结果
1.,其可能的原因是羟苯磺酸钙还原了反应过程中生成的h2o2而对测定造成负干扰。羟苯磺酸钙是临床用于治疗多种原因引起的毛细血管疾病,如糖尿病视网膜病变、静脉曲张、静脉炎、腿痉挛、痰痒性皮炎等症的常见药物,服用该药物后,患者的血清样本中不可避免的存在较高浓度的该药物。
4.因此,提供一种能够排除羟苯磺酸钙影响的游离脂肪酸的测定方法及试剂盒对临床检测具有十分重要的意义。
5.[1]侯立安,国秀芝,邱玲,等.羟苯磺酸钙对酶法游离脂肪酸检测的负干扰[j].检验医学.2016,(11).936
‑
940.
技术实现要素:
[0006]
为了解决上述问题,本发明提供了一种可消除羟苯磺酸钙干扰的游离脂肪酸测定试剂盒。
[0007]
一方面,本发明提供了一种消除羟苯磺酸钙干扰的游离脂肪酸测定试剂盒。
[0008]
所述的游离脂肪酸测定试剂盒中包括试剂1;所述的试剂1中包括含有过氧化氢、tritonx
‑
100的ph6.50的柠檬酸缓冲液。
[0009]
优选地,所述的试剂1中,过氧化氢浓度为1.0
‑
3.0mmol/l、tritonx
‑
100浓度为1
‑
3ml/l、ph6.50的柠檬酸缓冲液浓度为30
‑
80mmol/l。
[0010]
进一步优选地,所述的试剂1中,过氧化氢浓度为1.5
‑
2.5mmol/l、tritonx
‑
100浓度为1.5
‑
2.5ml/l、ph6.50的柠檬酸缓冲液浓度为50
‑
60mmol/l。
[0011]
更进一步地,所述的试剂1中,过氧化氢浓度为2.0mmol/l、tritonx
‑
100浓度为2ml/l、ph6.50的柠檬酸缓冲液浓度为55mmol/l。
[0012]
所述的游离脂肪酸测定试剂盒中还包括试剂2;所述的试剂2中包括含有乙酰辅酶a合成酶、过氧化氢酶、辅酶a、三磷酸腺苷、todb、tritonx
‑
100、proclin300、海藻糖的ph7.2的tris缓冲液。
[0013]
优选地,所述的试剂2中,乙酰辅酶a合成酶浓度为1
‑
5ku/l、过氧化氢酶浓度为600
‑
1800ku/l、辅酶a浓度为0.2
‑
0.8g/l、三磷酸腺苷浓度为2
‑
8mmol/l、todb浓度为1
‑
3mmol/l、tritonx
‑
100浓度为1
‑
3ml/l、proclin300浓度为0.02
‑
2ml/l、海藻糖浓度为20
‑
100g/l、ph7.2的tris缓冲液浓度为50
‑
100mmol/l。
[0014]
进一步优选地,所述的试剂2中,乙酰辅酶a合成酶浓度为2
‑
4ku/l、过氧化氢酶浓度为1000
‑
1400ku/l、辅酶a浓度为0.4
‑
0.6g/l、三磷酸腺苷浓度为4
‑
6mmol/l、todb浓度为1.5
‑
2.5mmol/l、tritonx
‑
100浓度为1.5
‑
2.5ml/l、proclin300浓度为0.1
‑
1ml/l、海藻糖浓度为40
‑
80g/l、ph7.2的tris缓冲液浓度为60
‑
90mmol/l。
[0015]
更进一步地,所述的试剂2中,乙酰辅酶a合成酶浓度为3ku/l、过氧化氢酶浓度为1200ku/l、辅酶a浓度为0.5g/l、三磷酸腺苷浓度为5mmol/l、todb浓度为2mmol/l、tritonx
‑
100浓度为2ml/l、proclin300浓度为0.2ml/l、海藻糖浓度为60g/l、ph7.2的tris缓冲液浓度为75mmol/l。
[0016]
所述的游离脂肪酸测定试剂盒中还包括试剂3;所述的试剂3中包括含有乙酰辅酶a氧化酶、过氧化物酶、4
‑
aap、tritonx
‑
100、n
‑
乙基顺丁烯二酰亚胺、5,5
‑
二巯基
‑
2,2
‑
二硝基苯甲酸、2
‑
甲基
‑4‑
异噻唑啉
‑3‑
酮、叠氮钠、海藻糖的ph7.2的tris缓冲液。
[0017]
优选地,所述的试剂3中,乙酰辅酶a氧化酶的浓度为20
‑
120ku/l、过氧化物酶浓度为20
‑
200ku/l、4
‑
aap浓度为1
‑
5mmol/l、tritonx
‑
100浓度为1
‑
3ml/l、n
‑
乙基顺丁烯二酰亚胺浓度为2
‑
8mmol/l、5,5
‑
二巯基
‑
2,2
‑
二硝基苯甲酸浓度为1
‑
3mmol/l、2
‑
甲基
‑4‑
异噻唑啉
‑3‑
酮浓度为1
‑
3mmol/l、叠氮钠浓度为3
‑
5g/l、海藻糖浓度为20
‑
100g/l、ph7.2的tris缓冲液浓度为50
‑
100mmol/l。
[0018]
进一步优选地,所述的试剂3中,乙酰辅酶a氧化酶的浓度为40
‑
100ku/l、过氧化物酶浓度为60
‑
160ku/l、4
‑
aap浓度为2
‑
4mmol/l、tritonx
‑
100浓度为1.5
‑
2.5ml/l、n
‑
乙基顺丁烯二酰亚胺浓度为4
‑
6mmol/l、5,5
‑
二巯基
‑
2,2
‑
二硝基苯甲酸浓度为1.5
‑
2.5mmol/l、2
‑
甲基
‑4‑
异噻唑啉
‑3‑
酮浓度为1.5
‑
2.5mmol/l、叠氮钠浓度为3.5
‑
4.5g/l、海藻糖浓度为40
‑
80g/l、ph7.2的tris缓冲液的浓度为60
‑
90mmol/l。
[0019]
更进一步地,所述的试剂3中,乙酰辅酶a氧化酶的浓度为70ku/l、过氧化物酶浓度为110ku/l、4
‑
aap浓度为3mmol/l、tritonx
‑
100浓度为2ml/l、n
‑
乙基顺丁烯二酰亚胺浓度为5mmol/l、5,5
‑
二巯基
‑
2,2
‑
二硝基苯甲酸浓度为2mmol/l、2
‑
甲基
‑4‑
异噻唑啉
‑3‑
酮浓度为2mmol/l、叠氮钠浓度为4g/l、海藻糖浓度为60g/l、ph7.2的tris缓冲液的浓度为75mmol/l。
[0020]
在一些实施例中,所述的游离脂肪酸测定试剂盒中由以下成分组成:
[0021]
试剂1:过氧化氢浓度为2.0mmol/l、tritonx
‑
100浓度为2ml/l、ph6.50柠檬酸缓冲液浓度为55mmol/l;试剂2:乙酰辅酶a合成酶浓度为3ku/l、过氧化氢酶浓度为1200ku/l、辅酶a浓度为0.5g/l、三磷酸腺苷浓度为5mmol/l、todb浓度为2mmol/l、tritonx
‑
100浓度为2ml/l、proclin300浓度为0.2ml/l、海藻糖浓度为60g/l、ph7.2的tris缓冲液75mmol/l;试剂3:乙酰辅酶a氧化酶的浓度为70ku/l、过氧化物酶浓度为110ku/l、4
‑
aap浓度为3mmol/l、
tritonx
‑
100浓度为2ml/l、n
‑
乙基顺丁烯二酰亚胺浓度为5mmol/l、5,5
‑
二巯基
‑
2,2
‑
二硝基苯甲酸浓度为2mmol/l、2
‑
甲基
‑4‑
异噻唑啉
‑3‑
酮浓度为2mmol/l、叠氮钠浓度为4g/l、海藻糖浓度为60g/l、ph7.2的tris缓冲液浓度为75mmol/l。
[0022]
本发明试剂盒的测定原理为:
[0023]
第一步,配制含有过氧化氢、tritonx
‑
100的ph6.50柠檬酸缓冲液为试剂1,按一定比例加入血清样本。样本中可能含有的羟苯磺酸钙等还原性物质被过氧化氢氧化而失去还原能力。
[0024]
第二步,配制含有乙酰辅酶a合成酶、过氧化氢酶、辅酶a、三磷酸腺苷、todb、tritonx
‑
100、proclin300、海藻糖的ph7.2 tris缓冲液为试剂2,将试剂2按一定比例加入到第一步试剂1和待测血清样品的混合溶液中。试剂1中剩余的过氧化氢被试剂2中过氧化氢酶所分解;血清中游离脂肪酸在乙酰辅酶a合成酶作用下与辅酶a反应生成脂酰辅酶a,检测560nm的吸光度值a1。
[0025]
第三步,配制含乙酰辅酶a氧化酶、过氧化物酶、4
‑
aap、tritonx
‑
100、n
‑
乙基顺丁烯二酰亚胺、5,5
‑
二巯基
‑
2,2
‑
二硝基苯甲酸、2
‑
甲基
‑4‑
异噻唑啉
‑3‑
酮、叠氮钠、海藻糖的ph7.2 tris缓冲液为试剂3,将试剂3按一定比例加入到第二步反应所得的混合溶液中。试剂3中的叠氮钠将混合溶液中过氧化氢酶活性完全抑制;混合溶液中的脂酰辅酶a在乙酰辅酶a氧化酶的作用下生成过氧化氢,过氧化氢再在过氧化物酶的作用下与4
‑
氨基安替比林和todb反应生成紫红色化合物,引起560nm处的吸光度值上升,检测560nm的吸光度值a2,与标准对照后计算出游离脂肪酸浓度c。
[0026]
另一方面,本发明还提供了前述游离脂肪酸测定试剂盒的使用方法。
[0027]
具体地,包括以下步骤:
[0028]
(1)配制含有过氧化氢、tritonx
‑
100的ph6.50的柠檬酸缓冲液为试剂1,按一定比例加入血清样本;
[0029]
(2)配制含有乙酰辅酶a合成酶、过氧化氢酶、辅酶a、三磷酸腺苷、todb、tritonx
‑
100、proclin300、海藻糖的ph7.2 tris缓冲液为试剂2,将试剂2按一定比例加入到第一步试剂1和待测血清样品的混合溶液中,检测560nm的吸光度值au,1;
[0030]
(3)配制含乙酰辅酶a氧化酶、过氧化物酶、4
‑
aap、tritonx
‑
100、n
‑
乙基顺丁烯二酰亚胺、5,5
‑
二巯基
‑
2,2
‑
二硝基苯甲酸、2
‑
甲基
‑4‑
异噻唑啉
‑3‑
酮、叠氮钠、海藻糖的ph7.2 tris缓冲液为试剂3,将试剂3按一定比例加入到第二步反应所得的混合溶液中,检测560nm的吸光度值au,2;与标准对照后计算出游离脂肪酸浓度c。
[0031]
具体地,所述的步骤(1)中的反应条件为在37℃环境中反应180
‑
300秒。
[0032]
具体地,所述的步骤(1)中的血清样本与试剂1的体积比为v血清:v试剂i=4:140。
[0033]
具体地,所述的步骤(2)中的反应条件为在37℃环境中反应180
‑
300秒。
[0034]
具体地,所述的步骤(2)中的血清样本与试剂1、试剂2的体积比为v血清:v试剂1:v试剂2=4:140:60。
[0035]
具体地,所述的步骤(3)中的反应条件为在37℃环境中反应180
‑
300秒。
[0036]
具体地,所述的步骤(3)中的血清样本与试剂1、试剂2的体积比为v血清:v试剂1:v试剂2:v试剂3=4:140:60:45。
[0037]
具体地,所述的步骤(3)中所述的游离脂肪酸浓度的计算公式为:
tritonx
‑
100、浓度为0.02ml/l的proclin300、浓度为20g/l的海藻糖、浓度为50mmol/l的ph 7.20的tris
‑
hcl缓冲液。
[0050]
试剂3包括浓度为20ku/l的乙酰辅酶a氧化酶、浓度为20ku/l的过氧化物酶、浓度为1mmol/l的4
‑
aap、浓度为1ml/l的tritonx
‑
100、浓度为2mmol/l的n
‑
乙基顺丁烯二酰亚胺、浓度为1mmol/l的5,5
‑
二巯基
‑
2,2
‑
二硝基苯甲酸、浓度为1mmol/l的2
‑
甲基
‑4‑
异噻唑啉
‑3‑
酮、浓度为3g/l的叠氮钠、浓度为20g/l的海藻糖、浓度为50mmol/l的ph 7.20的tris
‑
hcl缓冲液。
[0051]
测定样品液时,采用的仪器为beckman lx20全自动生化分析仪,反应温度为37℃,样本体积为4μl,试剂1体积为140μl,试剂2体积为60μl,试剂3体积为45μl,测定主/副波长为560/800nm。试剂1和样本混合后在测定温度反应180秒;加入试剂2混匀后反应180秒,分别读取空白管、标准管、血清管的吸光度值ab,1、as,1、au,1;继续加入试剂3后反应180秒,分别读取空白管、标准管、血清管的吸光度值ab,2、as,2、au,2,由仪器自动计算出样本中的游离脂肪酸浓度。定标曲线的拟合方式为线性拟合。
[0052]
用本法分别测定了不添加和添加不同浓度羟苯磺酸钙对不同浓度游离脂肪酸样本测定的影响,计算干扰率,检测结果如下表1。
[0053]
表1为本实施例所述试剂盒测定的不同羟苯磺酸钙浓度下游离脂肪酸浓度与空白血清的百分偏差(%)。
[0054]
表1
[0055][0056]
从表1中可以看出,所有的百分偏差(%)均小于10%。
[0057]
实施例2一种可消除羟苯磺酸钙干扰的游离脂肪酸测定试剂盒
[0058]
包括试剂1、试剂2和试剂3。
[0059]
试剂1包括浓度为3.0mmol/l的过氧化氢、浓度为3ml/l的tritonx
‑
100、浓度为80mmol/l的ph6.50柠檬酸缓冲液。
[0060]
试剂2包括浓度为5ku/l的乙酰辅酶a合成酶、浓度为1800ku/l的过氧化氢酶、浓度为0.8g/l的辅酶a、浓度为8mmol/l的三磷酸腺苷、浓度为3mmol/l的todb、浓度为3ml/l tritonx
‑
100、浓度为2ml/l的proclin300、浓度为100g/l的海藻糖、浓度为100mmol/l的ph 7.20的tris
‑
hcl缓冲液。
[0061]
试剂3包括浓度为120ku/l的乙酰辅酶a氧化酶、浓度为200ku/l的过氧化物酶、浓度为5mmol/l的4
‑
aap、浓度为3ml/l的tritonx
‑
100、浓度为8mmol/l的n
‑
乙基顺丁烯二酰亚胺、浓度为3mmol/l的5,5
‑
二巯基
‑
2,2
‑
二硝基苯甲酸、浓度为3mmol/l的2
‑
甲基
‑4‑
异噻唑啉
‑3‑
酮、浓度为5g/l的叠氮钠、浓度为100g/l的海藻糖、浓度为100mmol/l的ph 7.20的tris
‑
hcl缓冲液。
[0062]
测定样品液时,采用的仪器为beckman cx4全自动生化分析仪,反应温度为37℃,
样本体积为4μl,试剂1体积为140μl,试剂2体积为60μl,试剂3体积为45μl,测定主/副波长为560/800nm。试剂1和样本混合后在测定温度反应240秒;加入试剂2混匀后反应240秒,分别读取空白管、标准管、血清管的吸光度值ab,1、as,1、au,1;继续加入试剂3后反应240秒,分别读取空白管、标准管、血清管的吸光度值ab,2、as,2、au,2,由仪器自动计算出样本中的游离脂肪酸浓度。定标曲线的拟合方式为线性拟合。
[0063]
用本法分别测定了不添加和添加不同浓度羟苯磺酸钙对不同浓度游离脂肪酸样本测定的影响,计算干扰率。表2为本实施例所述方法测定的不同羟苯磺酸钙浓度下游离脂肪酸浓度与空白血清的百分偏差(%)。
[0064]
表2
[0065][0066]
从表2中可以看出,所有的百分偏差(%)均小于10%。
[0067]
实施例3一种可消除羟苯磺酸钙干扰的游离脂肪酸测定试剂盒
[0068]
包括试剂1、试剂2和试剂3。
[0069]
试剂1包括浓度为2.0mmol/l的过氧化氢、浓度为2ml/l的tritonx
‑
100、浓度为55mmol/l的ph6.50柠檬酸缓冲液。
[0070]
试剂2包括浓度为3ku/l的乙酰辅酶a合成酶、浓度为1200ku/l的过氧化氢酶、浓度为0.5g/l的辅酶a、浓度为5mmol/l的三磷酸腺苷、浓度为2mmol/l的todb、浓度为2ml/l tritonx
‑
100、浓度为0.2ml/l的proclin300、浓度为60g/l的海藻糖、浓度为75mmol/l的ph7.20的tris
‑
hcl缓冲液。
[0071]
试剂3包括浓度为70ku/l的乙酰辅酶a氧化酶、浓度为110ku/l的过氧化物酶、浓度为3mmol/l的4
‑
aap、浓度为2ml/l的tritonx
‑
100、浓度为5mmol/l的n
‑
乙基顺丁烯二酰亚胺、浓度为2mmol/l的5,5
‑
二巯基
‑
2,2
‑
二硝基苯甲酸、浓度为2mmol/l的2
‑
甲基
‑4‑
异噻唑啉
‑3‑
酮、浓度为4g/l的叠氮钠、浓度为60g/l的海藻糖、浓度为75mmol/l的ph7.20的tris
‑
hcl缓冲液。
[0072]
测定样品液时,采用的仪器为日本岛津uv2201紫外可见分光光度计,反应温度为37℃,样本体积为4μl,试剂1体积为140μl,试剂2体积为60μl,试剂3体积为45μl,测定主/副波长为560/800nm。试剂1和样本混合后在测定温度反应300秒;加入试剂2混匀后反应300秒,分别读取空白管、标准管、血清管的吸光度值ab,1、as,1、au,1;继续加入试剂3后反应300秒,分别读取空白管、标准管、血清管的吸光度值ab,2、as,2、au,2,计算出样本中的游离脂肪酸浓度。定标曲线的拟合方式为线性拟合。
[0073]
用本法分别测定了不添加和添加不同浓度羟苯磺酸钙对不同浓度游离脂肪酸样本测定的影响,计算干扰率。表3为本实施例所述方法测定的不同羟苯磺酸钙浓度下游离脂肪酸浓度与空白血清的百分偏差(%)。
[0074]
表3
[0075][0076]
从表3中可以看出,所有的百分偏差(%)均小于10%。
[0077]
实施例4试剂盒的精密度考察
[0078]
取低浓度(0.5mmol/l)、中浓度(1.0mmol/l)、高浓度(1.5mmol/l)的游离脂肪酸样本,同一天内采用本发明实施例1
‑
3试剂盒重复测定20次,计算批内cv,然后采用相同样本连续测定20天,计算批间cv,结果见表4
‑
6。
[0079]
表4
[0080][0081][0082]
表5
[0083] 平均值(批内)批内cv(%)平均值(批间)批间cv(%)实施例11.002.21.022.8实施例20.992.31.012.9实施例31.002.41.042.9
[0084]
表6
[0085] 平均值(批内)批内cv(%)平均值(批间)批间cv(%)实施例11.521.90.522.3实施例21.511.80.522.2实施例31.542.00.512.4
[0086]
实施例5试剂盒的稳定性考察
[0087]
将本发明实施例1
‑
3制备的试剂盒在4℃冰箱环境下放置12个月,然后按照实施例4的方法测定nefa均值和cv值,样本为中浓度(1.0mmol/l)游离脂肪酸样本,结果见表7。
[0088]
表7
[0089] 平均值(批内)批内cv(%)平均值(批间)批间cv(%)实施例11.043.11.023.7实施例21.033.31.013.8实施例31.053.51.043.9
[0090]
对比例
[0091]
以实施例1
‑
3的技术方案为基础,区别仅在于试剂1中不添加过氧化氢,仪器参数、检测步骤同对应的实施例1
‑
3,从而得到对应的对比例1
‑
3(对比例1对应实施例1,对比例2
对应实施例2,对比例3对应实施例3),各对比例测定的不同羟苯磺酸钙浓度下游离脂肪酸浓度与空白血清的百分偏差(%)分别见表8
‑
10:
[0092]
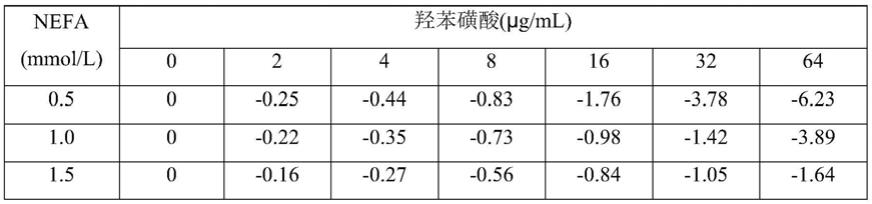
表8.对比例1测定结果
[0093][0094][0095]
表9.对比例2测定结果
[0096][0097]
表10.对比例3测定结果
[0098][0099]
可以看出,各对比例的百分偏差(%)均远远大于实施例的百分偏差(%)。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。