对相关申请的引用
本申请要求于2018年11月19日提交的美国临时申请62/769,511、于2019年7月24提交的美国临时申请62/878,250、以及于2019年8月5日提交的美国临时申请62/882,945的优先权,这些临时申请的内容通过整体引用结合到本申请中,如同逐字陈述一样。
本公开的方案涉及一种用于向患者均匀地施用溶液的装置、系统和方法。更具体地说,该装置、系统和方法针对用于治疗患者的表面(包括皮肤伤口)的溶液。
背景技术:
传染病往往在本应安全的地点染上,例如救护车、医院、诊所、以及辅助生活设施等其他区域。向患者或受试者喷洒消毒剂的传统方式已不再有效。多年来,医疗行业在治疗有消毒剂问题(例如皮肤伤口)的患者方面取得了很大进展,包括在应用于伤口的干细胞的使用以及遗传特异性治疗方面的进展。虽然不同的治疗方案在不断发展,但是身体对各种治疗形式有不同的反应。此外,一直缺乏对于如何以最经济的方式提供这些治疗的关注。
关于干细胞,可以理解的是,通常在加湿培养箱中在37℃/5%co2条件下对其进行培养,使用营养丰富的培养基来维持感兴趣的给定干细胞的存活。可向生长培养基中补充不同的营养因子,以保持干细胞健康并增殖。干细胞会无分化地增殖,而细胞在较低的温度(例如<30℃)下生长会表现出缓慢增殖,抑制蛋白质的产生,并且在某些情况下某些干细胞会在体外分化。已知的是,细胞在48℃以上温度(例如>52℃)下体外生长会增加蛋白质和dna降解的风险。干细胞在30℃下体外生长会提高某些受体/离子通道的细胞表面表达,并且在某些情况下表现出分化。细胞功能在98.6℉(37℃)的正常生理温度下最佳,但在较高的温度下,细胞膜的流动性提高,允许潜在的有害蛋白质和其他分子进出细胞;在高于58℃时,细胞会经历凋亡途径,这导致细胞死亡。
此外,皮肤移植可能需要数周甚至数月才能愈合。在恢复期内,患者易受感染。虽然研究人员已经在实验室再生皮肤数十年了,但这个过程较长,可能需要2-3周。此外,生成的皮肤通常是脆弱的,并且在培养时的产生和维护成本很高。在某些情况下,表皮培养物不能固定下来,并且在此过程中会损失大量的精力和试剂。虽然皮肤已经被移植和/或置于患者的伤口/烧伤或感兴趣区域上,但由于分泌物的原因,在下面会形成水泡,并且会向上推压皮层,导致进一步损伤。目前正在开始利用通过专门的施加装置施加的干细胞来解决这些问题。
对于伤口愈合来说,这个过程是一个复杂的动态过程,具有多个阶段,包括趋化因子、细胞因子、生长因子和各种细胞之间的协调信号传递。这一过程在任何阶段中断都可能导致伤口慢性化和/或导致异常的表皮形成。慢性伤口指伤口不能在可预测的时间内愈合并停留在伤口愈合的一个或多个阶段(止血、炎症、增殖或重建),其中最常见的是炎症阶段。这些伤口会给患者带来严重的身心压力,并给患者和整个医疗系统带来沉重的经济负担。基于干细胞的治疗途径因其自我更新和分化为多种细胞的能力而已成为再生医学领域一种大有前途的新干预手段。
此外,细胞膜的完整性可能受到某些力的损害,包括化学力、机械力和电力。在通过注射器输送悬浮人脐静脉内皮细胞(huvec)的研究中,已经检查了力/剪应力的大小。例如,一项研究发现,在以1000微升/分钟的流速输送时,细胞的急性存活率降低(58.7%)。参见aguado等人于2012年发表的文章。将人脐静脉内皮细胞(huvec)悬浮在75k交联藻酸盐溶液(水凝胶)中能提高急性存活率(88.9%)。在大鼠间充质干细胞和人脂肪干细胞(hasc)的情况中也观察了到类似的结果。
本公开的方案解决了本领域的这些问题和其他问题。
技术实现要素:
本公开的主题是一种用于向患者的治疗部位施用治疗溶液的施用装置。
在一些实例中,公开了一种用于向患者的治疗部位施用治疗溶液的施用装置,所述治疗溶液被该施用装置电纺,以向治疗部位施用。所述施用装置可包括施用装置壳体;可移除地设置在壳体内的药筒,当布置在壳体内时,该药筒能够储存具有至少一种电纺介质的治疗溶液;具有与药筒流体连通的远侧喷嘴的可旋转针头,该远侧喷嘴配置为将治疗溶液的电纺液滴从施用装置沿径向输送到治疗部位。
在一些实施例中,所述施用装置可包括在药筒设置在壳体中时与药筒电连通的辅助电极和可旋转地连接至可旋转针头的近端的电机,其中所述电机配置为以一种或多种转速旋转所述可旋转针头。旋转针头的电机对药筒中的治疗溶液加压,并将治疗溶液从远侧喷嘴排出,以产生治疗溶液的细雾。
在一些示例中,所述施用装置可包括通过供应管与药筒流体连通的压力泵;以及配置为通过远侧喷嘴从药筒蒸发治疗溶液的电纺风扇。
在一些示例中,所述远侧喷嘴包括文丘里管。
在一些示例中,所述风扇配置为迫使流体通过文丘里管,从而加速流体流动以迅速蒸发治疗溶液的溶剂,然后向治疗部位输送细丝基质。
在一些示例中,所述可旋转针头包括用于对药筒内的流体加压的近侧密封件和邻近远侧喷嘴的远侧密封件。
在一些示例中,所述可旋转针头可包括具有内腔的细长主体;沿着该细长主体的长度布置的多个径向分开的进料管孔;以及从远侧喷嘴向外突出的多个径向分开的分配元件,这些分配元件配置为共同输送带静电的治疗溶液的喷雾或液流。
在一些示例中,所述分配元件共同形成沿径向取向或处于任何朝前角度的针头阵列,这有助于以预定的喷射模式施用治疗溶液。
在一些示例中,所述分配元件处于垂直于可旋转针头的纵向轴线的取向。
在一些示例中,所述治疗溶液包括聚合物和溶剂,并且所述可旋转针头配置为旋转,溶解聚合物,并从远侧喷嘴径向喷射溶解的聚合物,然后使治疗溶液受到较高速度的气流的作用,从而干燥溶剂并使所得到的纤维垫重定向到治疗部位。
在一些示例中,所述可旋转针头沿轴向置于药筒的针腔内,该针腔包括穿过药筒的两端之间的中央部分的大致细长形的内腔。
在一些示例中,所述治疗溶液包括混合物,该混合物包括用于治疗部位的消毒剂和/或干细胞之中的至少一种。
在一些示例中,所述电纺液滴在治疗部位上形成包括电纺纤维垫的液体绷带。
在一些示例中,所述纤维垫包括至少两层由不同的电纺介质制成的层。
在一些示例中,所述纤维垫包括至少一种药剂。
在一些示例中,所述治疗溶液包括消毒药筒,该消毒药筒包括混合试剂及一定百分比的抗菌溶液。
在一些示例中,所述治疗溶液包括具有止痛特性的试剂。
在一些示例中,所述混合物还包括用于鉴定治疗溶液的内容物的跟踪物质。
在一些示例中,所述跟踪物质是能够通过光学读取器观测以鉴定混合物的内容物的硅胶。
在一些示例中,所述施用装置壳体包括握柄和激活机构,该激活机构配置为激活施用装置的治疗溶液,使治疗溶液流过施用装置和药筒并从远侧喷嘴泵出。
在一些示例中,所述药筒是一次性的。
在一些示例中,所述施用装置包括配置为在远端喷嘴和辅助电极上产生电势差的电源。该电势差的范围在5千伏至50千伏、20千伏至30千伏和/或类似范围内。但是,也可根据需要或要求考虑其他范围。
在一些示例中,所述治疗部位是创面或开放性伤口。
在一些示例中,所述治疗部位是患者皮肤上的感染部位。
在一些示例中,公开了一种产生包含电纺纤维垫的液体绷带的方法,该方法包括向用于在治疗部位产生和输送液体绷带的施用装置中的药筒内的治疗溶液施加电势。所述施用装置可包括施用装置壳体;可移除地设置在壳体内的药筒,当布置在壳体内时,该药筒能够储存具有至少一种电纺介质的治疗溶液;具有与药筒流体连通的远侧喷嘴的可旋转针头,该远侧喷嘴配置为将治疗溶液的电纺液滴从施用装置沿径向输送到治疗部位;以及通过可旋转针头对治疗溶液进行电纺。
在一些示例中,所述方法可包括通过可旋转地连接至可旋转针头的近端的电机来旋转可旋转针头的近端,从而对药筒中的治疗溶液加压;并且通过旋转可旋转针头的电机将治疗溶液从远侧喷嘴驱出,并在治疗部位上产生治疗溶液的细雾。
在一些示例中,所述方法可包括通过施用装置的电纺风扇从药筒通过远侧喷嘴蒸发治疗溶液。
在一些示例中,所述方法可包括通过施用装置的电纺风扇迫使流体通过远侧喷嘴的文丘里管,从而加速流体的流动以迅速蒸发治疗溶液的溶剂,然后;通过远侧喷嘴在治疗部位输送细纤维垫。
在一些示例中,所述可旋转针头包括具有内腔的细长主体;沿着该细长主体的长度布置的多个径向分开的进料管孔;以及从远侧喷嘴向外突出的多个径向分开的分配元件,这些分配元件配置为共同输送带静电的治疗溶液的喷雾或液流。
在一些示例中,所述方法可包括旋转所述可旋转针头,从而溶解治疗溶液的聚合物,并且从远侧喷嘴径向喷射溶解的聚合物;使治疗溶液受到较高速度的气流的作用,从而干燥溶剂;然后将所得的纤维垫沉积到治疗部位。
在一些示例中,所述方法可包括将所述可旋转针头沿轴向置于药筒的针腔内,该针腔包括穿过药筒的两端之间的中央部分的大致细长形的内腔。
在一些示例中,所述方法可包括用治疗溶液的电纺液滴形成液体绷带。
在一些示例中,所述方法可包括通过施用装置的握柄和激活机构使施用装置的电源致动,该电源配置为在药筒被置于壳体内时在远端喷嘴和与药筒电连通的辅助电极上产生电势差。
在一些示例中,所述施用装置可包括施用装置壳体。药筒可以是可移除的,并布置在壳体内。在布置在壳体内时,该药筒可与治疗溶液储存器流体连通。该药筒可包括用于对施用装置和/或药筒的治疗溶液进行静电充电的静电模块。所述治疗溶液配置为流过静电模块并流向喷嘴,由此静电模块在治疗溶液流过时与治疗溶液物理接触,并向治疗溶液施加电荷。
在一些示例中,所述治疗溶液储存在施用装置的治疗溶液储存器中。
在一些示例中,所述治疗溶液最初是通过药筒的孔口输送到药筒内的。
在一些示例中,所述治疗溶液是由针头通过所述孔口输送的;并且其中所述药筒是一次性的。
在一些示例中,所述孔口包括一个或多个护帽或阀门机构,用于控制治疗溶液通过其流入药筒。
在一些示例中,所述药筒包括药筒壳体和设置在药筒壳体的下表面上的一个或多个喷嘴导引件,所述一个或多个导引件配置为导引药筒壳体并使其可滑动地接合为与施用装置的喷嘴的相应导引表面锁定接合的状态。
在一些示例中,所述药筒包括药筒壳体以及最终用户可从外部触及的释放按钮,该按钮配置为穿过药筒的表面,并使药筒壳体在与施用装置安全锁定的状态和解锁状态之间移动。
在一些示例中,所述药筒包括药筒壳体和设置在该壳体内的第一托盘。该第一托盘可包括具有开口的分隔构件阵列,在向治疗溶液施加电荷时,治疗溶液通过该开口。所述药筒还可包括用于向第一托盘输送电荷的压电元件。所述药筒还可包括在壳体内设置在第一托盘下方的第二托盘,该第二托盘包括具有开口的分隔构件阵列,治疗溶液在流过第一托盘之后通过该开口。在治疗溶液流过第一托盘之后,当治疗溶液流过分隔构件时,第二托盘可向治疗溶液施加热量。
在一些示例中,在第一和/或第二托盘的分隔构件之间设有聚合材料,用于在治疗溶液通过第一和/或第二托盘的开口时分隔治疗溶液的细胞。
在一些示例中,第一和/或第二托盘的上表面上的开口大于第一和/或第二托盘的下表面上的开口。
在一些示例中,第一和/或第二托盘的开口配置为在被静电充电之前分隔治疗溶液的细胞。
在一些示例中,第一和/或第二托盘的开口是锥形或渐缩的。
在一些示例中,所述治疗溶液基本上由干细胞组成。
在一些示例中,所述治疗溶液包括混合物,该混合物包括用于治疗部位的消毒剂。
在一些示例中,所述治疗溶液包括混合物,该混合物包括用于治疗部位的消毒剂和干细胞之中的至少一种。所述混合物可包括用于鉴定治疗溶液的内容物的跟踪物质。所述跟踪物质可以是能够通过光学读取器观测以鉴定混合物的内容物的硅胶。
在一些示例中,所述治疗部位是创面或开放性伤口。
在一些示例中,所述治疗部位是患者皮肤上的感染部位。
在一些示例中,所述药筒的喷嘴是9伏压电喷嘴。
在一些示例中,所述药筒的喷嘴配置为将施用装置的溶液沿水平方向均匀地施用8至12英寸。
在一些示例中,所述药筒的喷嘴配置为将施用装置的溶液沿竖直方向均匀地施用8至12英寸。
在一些示例中,所述施用装置以0.05至20微米范围内的离散颗粒形式施用所述溶液。
在一些示例中,所述施用装置包括设置在施用装置壳体内的泵,该泵将流体从治疗溶液贮存器泵送过药筒,并使其到达喷嘴。
在一些示例中,所述施用装置壳体包括握柄和激活机构,该激活机构配置为激活施用装置的治疗溶液,使治疗溶液流过施用装置和药筒并从喷嘴泵出。
在一些示例中,一个罩盖铰接到施用装置壳体上,并可在关闭形态和打开形态之间铰接地移动。在关闭形态中,可在罩盖和施用装置壳体之间形成用于接收药筒的腔室。在打开形态中,该罩盖可围绕施用装置壳体的共享轴线铰接地向上移动,使得施用装置可接收药筒。
在一些示例中,公开了一种用于向患者的治疗部位施用治疗溶液的系统。该系统包括如本公开所述的任何施用装置以及能够接收该施用装置并对该施用装置的内部电源充电的基站。
在一些示例中,所述系统包括光学读取器,该光学读取器能够在治疗溶液处于施用装置内时读取和鉴定治疗溶液的跟踪物质。在一些示例中,所述光学读取器包括在一个移动装置中,该移动装置配置为读取编码信息以验证、识别或鉴定与治疗溶液相关的信息。在一些示例中,所述基站配置为以感应方式对施用装置的内部电源充电。
在一些示例中,提供了一种用于向患者的治疗部位施用治疗溶液的系统。该系统可包括如本文所述的任何施用装置以及能够接收该施用装置并对该施用装置的内部电源充电的基站。
在一些示例中,所述系统包括光学读取器,该光学读取器能够在治疗溶液处于施用装置内时读取和鉴定治疗溶液的跟踪物质。
在一些示例中,所述基站配置为以感应方式对施用装置的内部电源充电。
在一些示例中,公开了一种方法,该方法包括通过与施用装置组装在一起的药筒对用于治疗患者的治疗部位的治疗溶液进行静电充电;并且通过施用装置的喷嘴在患者的治疗部位上均匀地施用治疗溶液。
在一些示例中,所述方法在静电充电步骤之前包括将药筒与施用装置可移除地组装在一起;丢弃药筒;可移除地组装包含治疗溶液的第二药筒;并且通过施用装置的喷嘴在患者的治疗部位上均匀地施用第二药筒的治疗溶液。
在一些示例中,所述方法包括在伤口形成后90分钟内施用治疗溶液。
在一些示例中,所述方法在静电充电步骤之前包括将干细胞混合到治疗溶液中。
在一些示例中,所述均匀施用步骤还包括向治疗部位输送粒度在0.05至20微米范围内的治疗溶液的离散颗粒。
在一些示例中,所述方法包括通过将用于治疗部位的消毒剂和/或干细胞之中的至少一种混合在一起以形成治疗溶液。
在一些示例中,所述方法包括用与治疗部位的消毒剂和/或干细胞中的至少一种混合的跟踪物质形成治疗溶液;并且使用布置在施用装置外部的光学读取器鉴定治疗溶液的内容物;若治疗溶液是真品,则执行通过施用装置在患者的治疗部位上均匀施用治疗溶液的步骤。
在一些示例中,所述光学读取器包括在一个移动装置中,该移动装置配置为读取编码信息以验证、识别或鉴定与治疗溶液相关的信息。
在一些示例中,所述跟踪物质是硅胶。
在一些示例中,所述方法包括将施用装置无线连接至移动装置;处理关于施用装置和药筒的当前工作状况的数据,所述当前工作状况包括电池的电量、喷嘴设置、患者信息、最终用户信息、以及一个或多个预定治疗部位的剂量设定,并且其中所述数据包括当前的总记录编号、电池功率的设置、治疗溶液的流速、治疗溶液的液位和治疗溶液的性质。
在一些示例中,所述方法包括通过移动装置控制施用装置的操作设置和时间计划。在一些示例中,所述治疗溶液性质包括治疗溶液类型、浓度、药物和消毒剂。
在一些示例中,所述方法包括在移动装置的用户界面中呈现经过处理的数据。
在一些示例中,所述治疗部位是患者皮肤上的创面、开放性伤口或感染部位。
在一些示例中,所述方法包括在治疗溶液通过药筒的第一托盘的开口时通过向治疗溶液施加电荷来对治疗溶液进行静电充电;将药筒的第二托盘置于第一托盘下方;并且在治疗溶液通过第二托盘的开口时通过第二托盘加热带电的治疗溶液。
在一些示例中,所述向第一托盘施加电荷的步骤是从药筒的压电元件进行的。
在一些示例中,第一和/或第二托盘的开口是锥形或渐缩的。
在一些示例中,公开了一种使用施用装置产生并向治疗部位施用治疗溶液的应用。该应用包括通过与施用装置组装在一起的药筒对用于患者的治疗部位的治疗溶液进行静电充电;并且通过施用装置的喷嘴在患者的治疗部位上均匀地施用治疗溶液。
在一些示例中,所述应用在静电充电步骤之前包括将药筒与施用装置可移除地组装在一起;丢弃药筒;可移除地组装包含治疗溶液的第二药筒;并且通过施用装置的喷嘴在患者的治疗部位上均匀地施用第二药筒的治疗溶液。
在一些示例中,所述应用包括在伤口形成后90分钟内施用治疗溶液。
在一些示例中,所述应用在静电充电步骤之前包括将干细胞混合到治疗溶液中。
在一些示例中,所述均匀施用步骤还包括向治疗部位输送粒度在0.05至20微米范围内的治疗溶液的离散颗粒。
在一些示例中,所述应用的治疗溶液基本上由干细胞组成。
在一些示例中,所述应用包括通过将用于治疗部位的消毒剂和/或干细胞之中的至少一种混合在一起以形成治疗溶液。
在一些示例中,所述应用包括用与治疗部位的消毒剂和/或干细胞中的至少一种混合的跟踪物质形成治疗溶液;使用布置在施用装置外部的光学读取器鉴定治疗溶液的内容物;若治疗溶液是真品,则执行通过施用装置在患者的治疗部位上均匀施用治疗溶液的步骤。
在一些示例中,所述光学读取器包括在一个移动装置中,该移动装置配置为读取编码信息以验证、识别或鉴定与治疗溶液相关的信息。
在一些示例中,所述跟踪物质是硅胶。
在一些示例中,所述应用包括将施用装置无线连接至移动装置;处理关于施用装置和药筒的当前工作状况的数据,所述当前工作状况包括电池的电量、喷嘴设置、患者信息、最终用户信息、以及一个或多个预定治疗部位的剂量设定,并且其中所述数据包括当前的总记录编号、电池功率的设置、治疗溶液的流速、治疗溶液的液位和治疗溶液的性质。
在一些示例中,所述应用包括通过移动装置控制施用装置的操作设置和时间计划。
在一些示例中,所述治疗溶液性质包括治疗溶液类型、浓度、药物和消毒剂。
在一些示例中,所述应用包括在移动装置的用户界面中呈现经过处理的数据。
在一些示例中,所述治疗部位是创面或开放性伤口。
在一些示例中,所述治疗部位是患者皮肤上的感染部位。
在一些示例中,所述应用的施用装置包括施用装置壳体;可移除地设置在该壳体中的药筒,在布置在该壳体内时,所述药筒配置为与治疗溶液流体连通,所述药筒包括布置在壳体内用于对治疗溶液进行静电充电的静电模块;以及用于施用治疗溶液的喷嘴;其中所述治疗溶液配置为流过静电模块并流向喷嘴,由此静电模块在治疗溶液流过时与治疗溶液物理接触,并对治疗溶液进行静电充电。
在一些示例中,所述应用包括在治疗溶液通过药筒的第一托盘的开口时通过向治疗溶液施加电荷来对治疗溶液进行静电充电;将药筒的第二托盘置于第一托盘下方;并且在治疗溶液通过第二托盘的开口时通过第二托盘加热带电的治疗溶液。
在一些示例中,所述向第一托盘施加电荷的步骤是从药筒的压电元件进行的。
在一些示例中,第一和/或第二托盘的开口是锥形或渐缩的。
在一些示例中,公开了一种使用施用装置产生并向治疗部位施用包括电纺纤维垫的液体绷带的应用,所述应用包括:向施用装置内的药筒的治疗溶液施加电势,以在治疗部位上产生液体绷带,该施用装置包括施用装置壳体;可移除地设置在壳体内的药筒,当布置在壳体内时,该药筒能够储存具有至少一种电纺介质的治疗溶液;具有与药筒流体连通的远侧喷嘴的可旋转针头,该远侧喷嘴配置为将治疗溶液的电纺液滴从施用装置沿径向输送到治疗部位;以及通过可旋转针头对治疗溶液进行电纺。
在一些示例中,所述应用包括通过可旋转地连接至可旋转针头的近端的电机来旋转可旋转针头的近端,从而对药筒中的治疗溶液加压;并且通过旋转可旋转针头的电机将治疗溶液从远侧喷嘴驱出,并在治疗部位上产生治疗溶液的细雾。
在一些示例中,所述应用包括通过施用装置的电纺风扇从药筒通过远侧喷嘴蒸发治疗溶液。
在一些示例中,所述应用包括通过施用装置的电纺风扇迫使流体通过远侧喷嘴的文丘里管,从而加速流体的流动以迅速蒸发治疗溶液的溶剂,然后;通过远侧喷嘴在治疗部位输送细纤维垫。
在一些示例中,所述应用包括可旋转针头,该可旋转针头包括具有内腔的细长主体;沿着该细长主体的长度布置的多个径向分开的进料管孔;以及从远侧喷嘴向外突出的多个径向分开的分配元件,这些分配元件配置为共同输送带静电的治疗溶液的喷雾或液流。
在一些示例中,所述应用包括旋转所述可旋转针头,从而溶解治疗溶液的聚合物,并且从远侧喷嘴径向喷射溶解的聚合物;使治疗溶液受到较高速度的气流的作用,从而干燥溶剂;然后将所得的纤维垫沉积到治疗部位。
在一些示例中,所述应用包括将所述可旋转针头沿轴向置于药筒的针腔内,该针腔包括穿过药筒的两端之间的中央部分的大致细长形的内腔。
在一些示例中,所述应用包括用治疗溶液的电纺液滴形成液体绷带。
在一些示例中,所述应用包括通过施用装置的握柄和激活机构使施用装置的电源致动,该电源配置为在远端喷嘴和与药筒电连通的辅助电极上产生电势差。
在一些示例中,所述电势差在5千伏到50千伏范围内。
在一些示例中,所述应用包括在20千伏到30千伏范围内的电势差。
在一些示例中,公开了一种应用,该应用包括对用于患者的治疗部位的治疗溶液进行静电充电;并且通过本公开的任何施用装置在患者的治疗部位上均匀地施用治疗溶液。
为了实现前述目的和相关目的,在本文中将结合以下说明和附图说明某些示例性方面。但是,这些方面仅示出了可采用所要求的主题的原理的多种方式中的几种,并且所要求的主题意图包括所有这些方面及其等同内容。通过结合附图考虑以下详细说明,其他优点和新颖特征可变得明显。
附图说明
现在将结合附图在以下说明中进一步论述本发明的上述方面和其他方面,在附图中,相似的附图标记表示不同附图中的相似结构元件和特征。附图不一定是按比例绘制的,其重点是示出本发明的原理。附图仅通过示例性方式而非限制性方式示出了本发明的装置的一个或多个实施例。
图1示出了设有示例性的底座和药筒组件的示例性施用装置的透视图;
图2a示出了示例性施用装置的透视图;
图2b示出了示例性施用装置的透视图;
图3示出了图1-2b的示例性施用装置处于分解状态时的透视图;
图4示出了示例性施用装置在其罩盖处于打开状态时的透视图,其中示出了处于组装好的状态的药筒;
图5a示出了示例性施用装置在其罩盖处于关闭状态时的透视图;
图5b示出了示例性施用装置在其罩盖处于打开状态时的透视图,其中示出了药筒在组装到施用装置的药筒接收室中之前的形态;
图6示出了所述示例性施用装置在其罩盖处于打开状态并且内部电源处于分解状态时的透视图;
图7a示出了示例性药筒的透视图;
图7b示出了示例性药筒的透视图;
图8示出了沿着示例性药筒的水平中心线截取的横截面的透视图;
图9示出了沿着示例性药筒的另一个水平中心线截取的横截面的透视图;
图10示出了沿着示例性药筒的另一个水平中心线截取的横截面的透视图;
图11示出了本公开的示例性药筒的示例性托盘的横截面的近视侧视图;
图12示出了另一种示例性施用装置的透视图;
图13示出了图12的示例性施用装置的另一透视图,该施用装置与示例性底座、药筒和光学读取器组装在一起;
图14a示出了示例性药筒的透视图;
图14b示出了示例性药筒的透视图;
图15a示出了另一种示例性施用装置的透视图;
图15b示出了带有示例性接地电极的图15a的示例性施用装置的透视图;
图16示出了沿着图15的示例性施用装置的中心线的横截面的透视图;
图17示出了图15的施用装置的示例性远侧尖端的近视透视截面图;
图18示出了图15-16的示例性施用装置的近视后透视图;
图19a示出了示例性药筒的透视图;
图19b示出了图19a的示例性药筒的透视图;
图19c示出了图19a的示例性药筒的透视图;
图20a示出了与图15-16的示例性施用装置一起使用的示例性针头的透视图;
图20b示出了图20a的针头的示例性远侧尖端的近视透视图;
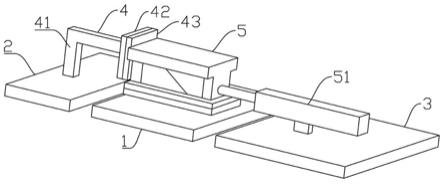
图21示出了设有示例性底座和药筒组件的图15-16的示例性施用装置的透视图;
图22示出了设有示例性底座和药筒组件的另一种示例性施用装置的透视图;
图23示出了图22所示的施用装置的分解透视图;
图24a-24c示出了图22中的示例性药筒的透视图;
图25示出了患者的示例性伤口部位处的示例性电场;
图26示出了本公开的示例性实施例的系统架构的示意图;
图27是示出能够按照在本文中说明的一个或多个实施例实现本公开的各个方面的通用计算系统的计算机架构图;
图28是示出能够按照在本文中说明的一个或多个实施例实现本公开的各个方面的通用计算系统的计算机架构图;
图29示出了移动装置上的应用程序的示例性事件查看器;
图30示出了本公开的示例性方法的示意性概图;
图31示出了本公开的示例性方法的示意性概图;
图32示出了本公开的示例性方法的示意性概图。
具体实施方式
虽然在本文中详细说明了所公开的技术的一些示例性实施例,但是应理解,也可设想其他实施例。因此,所公开的技术的范围并不局限于在以下说明中阐述的或在附图中示出的部件的构造和布置的细节。所公开的技术可有其他实施例,并且能够以各种方式实践或实施。
还应说明的是,除非在上下文中另有明示,否则在说明书和所附权利要求中所使用的单数形式“一”、“一个”和“所述”包括复数指代物。“包括”或“包含”或“含有”指在组合物、制品或方法中至少存在所提及的化合物、元素、颗粒或方法步骤,但不排除其他化合物、材料、颗粒、方法步骤的存在,即使此类其他化合物、材料、颗粒、方法步骤具有与所提及的化合物、材料、颗粒、方法步骤相同的功能。
在说明示例性实施例时,为了清楚起见,将借助于术语进行说明。每个术语均应理解为具有其被本领域技术人员所理解的最广泛的含义,并且包括以类似方式操作以实现类似目的的所有技术等同内容。还应理解,提及方法的一个或多个步骤并不排除存在另外的方法步骤或所标明的步骤之间的中间方法步骤。在不脱离所公开的技术的范围的情况下,方法的步骤可按与本文所述的顺序不同的顺序执行。类似地,还应理解,提及装置或系统中的一个或多个部件并不排除在所标明的部件之间存在另外的部件或中间部件。
在本文中所述的“受试者”或“患者”的脉管系统可以是人或任何动物的伤口部位或治疗部位。应理解,动物可以是任何适用种类的动物,包括但不限于哺乳动物、兽类动物、家畜动物或宠物型动物等。例如,动物可以是特别选择的具有类似于人类的某些特征的实验动物(例如鼠、狗、猪、猴等)。应理解,例如,受试者可以是任何适用的人类患者。
在本文中所述的“操作者”可包括医生、外科医师或者与受试者的治疗部位的治疗溶液的施用相关联的任何其他个人或输送仪器。
在本文中所述的“治疗溶液”可以是包含干细胞和/或哺乳动物原代细胞、消毒剂或可被输送到治疗部位以治疗患者的任何其他药物的液体溶液。治疗溶液可包含任何浓度的成分或成分混合物,包括基本上仅包含干细胞和/或哺乳动物原代细胞、消毒剂或任何其他所需或要求的药物的情况。术语“治疗溶液”还可包含与治疗溶液混合的一种或多种跟踪物质。
术语“远侧”或“近侧”在以下说明中是相对于治疗医师或医疗介入者的位置或方向使用的。“远侧”指远离医生或介入者的位置或远离医生或介入者的方向。“近侧”指靠近医生或医疗介入者的位置或朝向医生或医疗介入者的方向。
虽然现有的干细胞施用装置在满足消毒剂和患者治疗需求方面比移植更有效,但是干细胞和其他溶液的施用可通过使用在下文中更具体地论述的静电技术显著增强。本公开的施用装置和相关系统及方法能增强干细胞向患者的治疗部位的施用,包括皮肤伤口部位,例如创面。
可以理解的是,离子表面活性剂是在其配方中含有阳离子或阴离子的表面活性剂。在此方面,表面活性剂分子的头部带有净电荷。该电荷可以是正电荷,也可以是负电荷。若电荷是正电荷,则在此称为阳离子表面活性剂。相反,若电荷是负电荷,则在此称为阴离子表面活性剂。有时,这些化合物包含带有两个带相反电荷的离子基团的头部,在此称为两性离子表面活性剂。阴离子表面活性剂在分子的头部中包含带负电荷的功能基团。这些功能基团可包括磺酸盐、磷酸盐、硫酸盐和羧酸盐等。阳离子表面活性剂在分子的头部中包含带正电荷的功能基团。这些表面活性剂大多可用作抗微生物剂、抗真菌剂等,因为它们能破坏细菌和病毒的细胞膜。这些分子中最常见的功能基团是铵离子。
非离子表面活性剂是在其配方中没有净电荷的表面活性剂,这意味着分子在水中溶解时不会经历任何电离。此外,非离子表面活性剂具有共价键合的含氧亲水基团,这些基团与疏水母体结构结合。这些氧原子可导致表面活性剂分子的氢键结合。由于氢键结合受温度影响,因此温度升高会降低这些表面活性剂的溶出度。正电荷已显现出能改善从施用装置施用的治疗溶液的覆盖均匀性和对治疗部位的总覆盖率。此外,已经证实较低水平的“ ”电荷不会改变化学防腐剂和局部麻醉剂在本公开的治疗溶液中的预期作用。
一些治疗溶液已被证明带有可改变化学物质的负电荷或正电荷。如在下文中更具体地论述的,身体细胞的自然休眠状态是负电的(即,负电荷状态)。例如请参考本公开的图14。这种不平衡是由细胞内外的钾和钠离子造成的,这些离子在患者体内形成了电容。离子表面活性剂是在其配方中含有阳离子或阴离子的表面活性剂。其中,表面活性剂分子的头部携带净电荷。该电荷可以是正电荷,也可以是负电荷。可以理解的是,有些化学物质需要负电荷或中性电荷。在一些示例中,本公开的施用装置和相关系统可配置为在手指触摸时切换极性(例如通过致动器、开关、数字指示器等)。
在一些示例中,本公开利用了前述技术,使其治疗溶液带正电,然后将治疗溶液的带正电的分子从其施用装置输送到治疗部位,以达到电子平衡。在达到这种平衡时,治疗溶液会均匀地施加到治疗部位,因为治疗溶液的带正电荷的分子会通过均匀地施加到带负电荷的治疗部位来寻求平衡。在一些实施例中,可通过使静电荷通过施用装置的治疗溶液并通过其药筒的相应锥形阵列来使治疗溶液带正电,该药筒利用静电荷模块向干细胞和防腐剂施加正电荷或负电荷。尤其是,本公开的施用装置和相关系统可配置为向治疗溶液施加(“ ”)(“-”)或(中性)电荷,并向治疗部位(例如预定目标)施加“-”电荷。在一些示例中,施用装置也可通过关闭而进入中性状态。但是,也可设想对此进行逆转,并且可根据需要或要求用施用装置施加正静电荷,因为治疗溶液中的某些化学物质可能需要负电荷而不是正电荷。
本公开的使治疗溶液带正电荷的施用装置的一个示例可以是一种使治疗溶液带正电荷然后将带电荷的治疗溶液(例如包含干细胞的溶液)施用到治疗部位上的施用装置。在一个示例中,该施用装置包括静电输送系统,从而治疗溶液通过与施用装置布置在一起的药筒的电极。然后可从施用装置的喷嘴将施用装置的带电粒子施加到患者的治疗部位(例如带负电的治疗部位),治疗溶液的带电粒子被感应到治疗部位上,以在被施加的溶液的液雾中形成电场电荷。
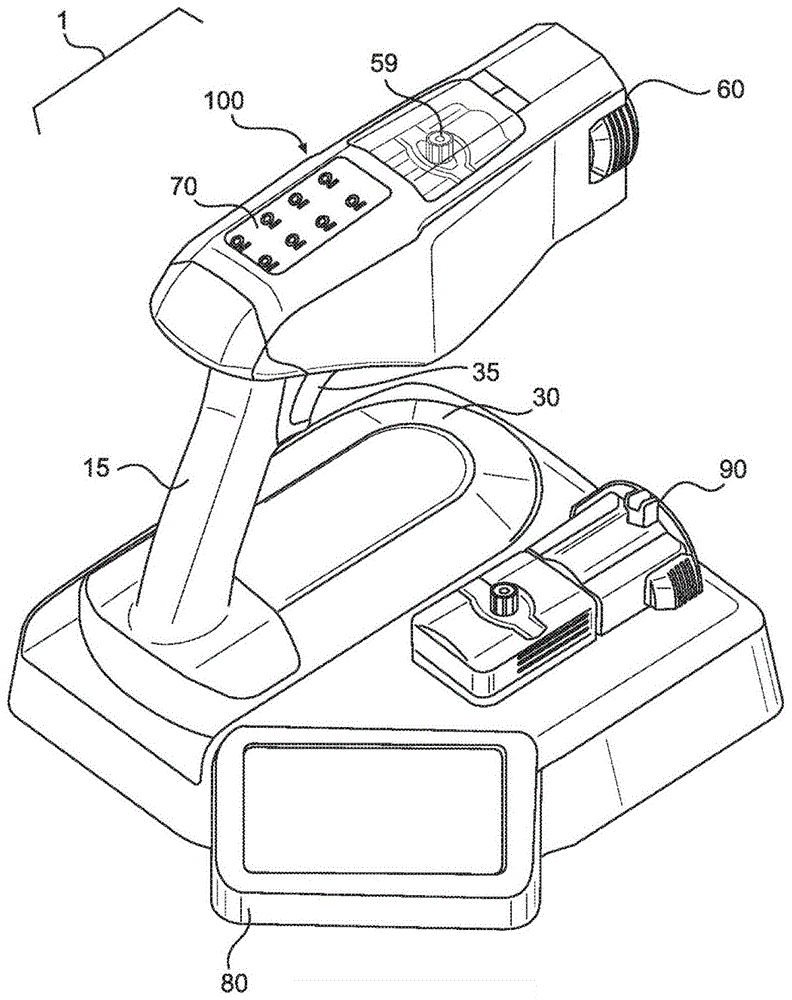
现在请看附图,图1-2b分别示出了静电治疗溶液施用装置100的前视和后视透视图,该静电治疗溶液施用装置100配置为对治疗溶液进行充电、雾化,并向患者的治疗部位施加治疗溶液。施用装置100可包括施用装置壳体10,该壳体10包括配置为由用户握持的握柄15。施用装置壳体10的握柄15可包括可由用户握持的人体工程学形状,当然,施用装置壳体10的确切尺寸和形状以及任何组成特征可以有所不同。一个罩盖20可枢转地连接至施用装置壳体10的上表面,以形成药筒接收室25。当罩盖20围绕施用装置壳体10的共享轴线移动到打开形态时,可将药筒50可移除地插入到药筒接收室25中。在一些实施例中,罩盖20可以是部分或完全透明的,或者包括具有一定透明度的某些部分,以使光学读取器能扫描和识别包含在药筒50内的治疗溶液,这在下文中会更具体地论述。相反,在关闭形态中,罩盖20可沿着其周边密封或与施用装置壳体10的相应表面严密接触,以封闭药筒接收室25。一个或多个底座部分30从握柄15延伸,以在重复使用之间处于平坦表面上。部分30可配置为处于底座80上或底座80内,如图1所示。此外,图1示出了用于鉴定药筒50的治疗溶液的内容物的一种示例性光学读取器90,这将在下文中更具体地论述。
施用装置100可具有用于激活或停用施用装置100的致动器35,包括接通系统电源、激活内置的泵p、向治疗溶液施加静电荷、以及将治疗溶液从药筒50通过喷嘴60输送到治疗部位上。壳体10还可包括位于施用装置10的外表面上的显示器70,该显示器70能够向最终用户提供输出指示,包括与内置电源、泵的设置、治疗溶液的设置等相关的数据。施用装置100可包括靠近或邻近朝向施用装置壳体10的前端的喷嘴60的治疗溶液输送区域,该区域具有开口,喷嘴60和相应的雾化治疗溶液可通过该开口排出。施用装置壳体10还可在其内部包括用于容纳治疗溶液的内置罐。在一些实施例中,所述罐也可根据需要或要求可移除地附接。
如图1-2b所示的施用装置还可包括带有喷嘴60的药筒50,该喷嘴60能够加热、施加静电荷并将治疗溶液输送到治疗部位,这在下文中将更具体地论述。腔室25接收药筒50,并能够与喷嘴60流体连通,用于供应可被喷嘴60充电和雾化的治疗溶液。
图3示出了处于分解状态的施用装置100。施用装置100的壳体10可由单个整体件形成,或者由多个分立构件形成,这些分立构件连接在一起,形成用于容纳施用装置100的构造的内腔。施用装置100可包括泵p以及内部电源,该内部电源包括一个或多个电池b,例如锂离子电池。施用装置100的电路板可配置为将直流电转换为交流电,以向泵p以及施用装置100的其他构造供电。施用装置100还可包括保护电路模块(pcm)。
请转到图4,其中提供了处于打开状态的施用装置100的透视图,示出了在施用装置100的腔室25内处于组装好的状态的药筒50。当罩盖20处于打开形态时,可将药筒50装载到施用装置100的腔室25中。在此打开形态中,药筒50也可包含治疗溶液(或者可稍后将治疗溶液添加到药筒50中)。在治疗溶液处于药筒50中时,可通过光学读取器(例如具有光学读取器的移动装置)鉴定治疗溶液,以验证预定的治疗溶液实际上是被输送给正确的患者的溶液,并防止假治疗溶液)。在一些示例中,所述光学读取器可观测治疗溶液内的跟踪物质(例如硅胶跟踪颗粒)。
施用装置100和相关系统1也可使用针对治疗溶液的跟踪系统,以节约治疗溶液的资源并保证患者安全。尤其是,近年来出现了关于伪造治疗药品和确保患者接受其病情所需的治疗的问题,因为现有技术不能充分提供有效地验证特定治疗药品是否确实是为患者开出的治疗药品的途径。
为了解决这些问题和其他问题,可在本公开的施用装置的某些实施例中包括治疗验证系统。在一些示例中,治疗验证系统可包括硅胶条形码,从而硅胶的粒度范围可以是5.0-20微米。硅胶条形码可与治疗溶液混合,并针对特定治疗或患者进行编码,这样可用于在施用前进行鉴定。这又使从制造商到医疗用户的链条更安全,并确保尽可能最佳的患者安全性。
在一些示例中,在采用硅胶治疗验证系统时,未发现硅胶纳米颗粒与干细胞在同一培养基中时会导致细胞毒性增加。
此外,在一些示例中,包括药筒壳体52的药筒50可具有条形码信息,以进一步跟踪和鉴定与施用装置100、治疗溶液和/或患者相关的信息。在一些示例中,当药筒50在使用前插入到光学读取器中或与光学读取器可操作地耦合时,可使用压印在硅胶上的识别数据识别经过认证的干细胞或治疗溶液的其他信息。光学读取器可以是移动装置,它可读取编码信息以验证、识别或鉴定与治疗溶液相关的信息。在一些示例中,光学读取器可与系统的一个或多个led对准并由其读取。
请转到图5a,该图提供了处于打开状态的施用装置100的透视图,示出了处于关闭状态的施用装置100的罩盖20。相比之下,图5b示出了罩盖20已经与施用装置100一起围绕共享轴线20枢转,使得罩盖现在处于打开形态。在打开时,可将药筒50输送至腔室25并与其组装在一起,包括相对于施用装置100的前喷嘴区域的喷嘴60。
当罩盖20处于打开形态时,可将药筒50装载到施用装置100的腔室25中。在此打开形态中,药筒50也可包含治疗溶液(或者可稍后将治疗溶液添加到药筒50中)。在治疗溶液处于药筒50中时,可通过光学读取器(例如具有光学读取器的移动装置)鉴定治疗溶液,以验证预定的治疗溶液实际上是被输送给正确的患者的溶液,并防止假治疗溶液)。还可想到也可检测药筒50的其他信息,包括治疗溶液的剩余量、自上次检测或检查以来施用的量以及该溶液的施用时间、患者、以及患者的相应预定治疗部位等。在一些示例中,所述光学读取器可观测治疗溶液内的跟踪物质(例如硅胶跟踪颗粒)。
请转到图6,能看到握柄15已经被移除以露出电池仓,该电池仓包含施用装置的内部电源、一个或多个电池b。另外,在图6中能类似地看到罩盖20处于打开形态,其中腔室25能够在其中接收药筒50。
请转到图7a和7b,其中示出了示例性药筒50的近视透视图。在一个示例中,药筒50可具有矩形壳体52(当然,可根据需要或要求考虑其他形状)。壳体52可由聚碳酸酯、医用级塑料制成,并且可以是一次性的。在一些示例中,药筒50可以是一次性的,而在其他示例中,药筒50的某些构造(例如压电系统)不是一次性的,但其他示例性构造(例如壳体52)分别是一次性的。图8、9和10示出了沿着药筒50的不同水平中心线截取的类似的药筒透视截面图,还示出了药筒50的构造是如何定向和组装在一起的。药筒50可配置为对治疗溶液施加正电荷,以便从施用装置100施用。而带正电的治疗溶液又寻求与由患者的带负电的治疗部位提供的负电位平衡。这对于实现治疗溶液对治疗部位的更好的覆盖是特别有利的,因为在喷嘴60施加带正电的颗粒时药筒50的颗粒不会堆积,因为每个颗粒都带正电,因而不会落在自身上。
在壳体的上表面上可设有孔口59,以接收治疗溶液(例如针头可通过该孔口输送溶液)。在一些示例中,孔口59可包括一个或多个护帽或阀门机构,用于控制治疗溶液通过其的流动。在一些示例中,治疗溶液可包含可追踪的自体和/或异体干细胞,以在使用前鉴定治疗溶液。在一些示例中,通过在治疗溶液中包含在细胞被收获并冷冻保存时处于细胞上的硅胶纳米颗粒,可追溯治疗溶液的来源。
在一些示例中,冷冻保存是通过将治疗溶液冷却到非常低的温度来保存细胞、细胞器、组织和任何其他生物构造的一种过程。干细胞和其他活组织不能通过简单的冷却或冷冻长期储存,因为在冷冻和解冻期间发生的冰晶形成、渗透冲击和膜损伤会导致细胞死亡。在过去的十年里,随着冷冻保护剂(cpa)和温度控制设备的使用,冷冻保存的成功率有所提高。
所设想的一种与本公开的治疗溶液一起使用的示例性方法包括玻璃化冷冻方法,该玻璃化冷冻方法涉及一种在细胞材料的快速冷却中使用的冷冻保护剂。这种与本公开的施用装置和治疗溶液一起使用的玻璃化冷冻方法快速、廉价,并且已经用于体外受精用精子、人类胚胎和卵母细胞的冷冻储存。
另一种示例性方法是缓慢冷却方法,这种方法允许在少于1m(摩尔)的冷冻保护剂(cpa)的存在下以大约1℃/分钟的速率冷却。考虑使用的冷冻制剂可包含50%胎牛血清(fbs)、40%培养基、10%二甲基亚砜(dmso),或者90%fbs、10%dmso。
在一些示例中,在准备好应用冷冻保存的细胞时,治疗溶液的细胞材料的解冻可包括以下步骤:(1)将溶液在水浴中升温至37℃推荐温度;(2)用70%乙醇或异丙醇擦拭低温试管;(3)可将该试管置于生物安全罩内,以便打开试管以释放压力,然后重新拧紧试管;(4)在37℃水浴中快速解冻一小瓶冷冻细胞,时间不超过2分钟;(5)用70%乙醇擦拭试管,并移回生物安全罩中;(6)将试管中的内容物无菌地转移到装有预热介质/溶液的锥形试管中;(7)在室温下在台式离心机中以300xg速度对细胞悬液离心大约10分钟(当然,也可考虑其他参数,例如在室温下以1000转/分的速度离心5分钟);(8)在生物安全罩中吸取溶液,注意不要扰动球团;(9)用预热的培养基/溶液轻轻冲击试管,使球团重新悬浮;和/或(10)添加适量的所需培养基/溶液,可再次进行细胞计数以添加所需的量,从而获得所需的细胞浓度。执行一个或多个前述解冻步骤会导致较轻微的细胞损失,包括在冲洗步骤期间,但是这是必要的,目的是去除可能对干细胞有害的cpa。无论如何,细胞现在已经准备好装载到施用装置上进行输送。
在验证后(例如在从可操作地装载的药筒读取信息时通过光学读取器或与之配套的系统底座等进行),可通过孔口59将治疗溶液(包括其自体和/或同种异体干细胞悬液)无菌地装载到药筒壳体52中。在引入到药筒壳体中之后,治疗溶液(包括自体/同种异体干细胞悬液)可通过位于药筒壳体的加热表面上的第一托盘54的细胞孔到达位于其单元孔处的第二托盘56的流体静压腔,在该处输送正电荷。然后可使用压电喷嘴将治疗溶液从药筒50通过喷嘴60输送到期望的治疗部位,该压电喷嘴将治疗溶液均匀和/或一致地分布到治疗部位(例如创面)。
应理解,可使用药筒50中的第二托盘56(例如热板)将干细胞悬浮液保持在生理温度。药筒50又可通过将温度保持在生理水平来优化和增加用于输送的治疗溶液的干细胞和任何其他生物物质的存活率。药筒50可通过托盘56的高压离子放电单元喷射高压离子。托盘56的单元将在本文中更详细地说明,但是能看到这些单元被有选择性地置于托盘56上,以从类似地流过托盘54的单元的治疗溶液接收先前加热的治疗溶液。在被加热和充电后,治疗溶液的液滴可从喷嘴60施用到治疗部位。在一些示例中,在药筒与施用装置100的腔室25组装在一起时,泵p可与药筒50流体连通。药筒50可包括静电模块,该静电模块电连接至托盘56和/或托盘54,并配置为通过其单元对托盘56和/或托盘54进行静电充电。但是,本公开的解决方案不限于此,相应的托盘可包括一个或多个电极、环和/或管,用于在向治疗部位施用治疗溶液之前对治疗溶液进行静电充电,而不是通过相应托盘的开放单元向治疗溶液施加电荷。
在托盘56下方的托盘58上也可设置压电元件57,由此压电元件57配置为对治疗溶液充正电。众所周知,压电效应是某些材料响应于施加的机械应力而产生电荷的一种能力。在一些示例中,在治疗溶液被施用装置100施用时,带电溶液通过压电喷嘴喷出,并在空气中破碎成微小的带电液滴。由于所有液滴都携带相同的电荷,因此它们会相互排斥,在空气中形成均匀的细雾。借助于细雾与目标物体之间的电吸引力,它们像“磁铁”一样被拉向目标物体,该目标物体的表面上通过地面感应出相反的电荷。由于我们的喷雾器能产生非常细小的轻质带电液滴,这些细小的液滴会以很高的流动性扩散,因此能到达目标物体的边缘甚至背面,在某些情况下能实现所期望的360度覆盖,这有时称为静电“环绕效果”。当在由药筒50引起的静电场内施加治疗溶液时,治疗溶液可在相反的场电荷周围环绕360度,在此情况下,所述相反的场电荷是带负电的治疗部位。元件57可以是由电池供电的压电雾化元件,它位于泵p的下游,并且相对于托盘54、56位于治疗溶液的流动路径中。元件57可被驱动从而以超声波频率振动,其振动方式使得治疗溶液被雾化。
在此说明的方案的压电效应的独特特征之一是该压电效应是可逆的。换句话说,虽然考虑了治疗溶液带正电从而可将其施加到带负电的治疗部位的情况,但是也考虑了相反的情况,因为表现出直接压电效应(在施加应力时产生电力)的材料也表现出相反的压电效应(当施加电场时产生应力)。
药筒50的喷嘴60可以是配置为向治疗部位施用雾化的治疗溶液的喷嘴组件。在一个示例中,泵p用于向喷嘴60的喷嘴提供气压。泵p可以是活塞泵、与螺线管结合工作的气动微型泵、在施用装置中抽真空以使流体从储存器流向喷嘴60的泵等。喷嘴60可包括带有内腔的细长管状构件,该内腔具有终止于圆锥形、锥形、截锥形或任何其他弯曲或平直的反向或成形表面的尖端。该表面的形状使得来自喷嘴60的流体被以粒径在5微米至40微米范围内的治疗溶液的雾化液滴的形式施用。喷嘴60可机械耦合至药筒50。
喷嘴60(尤其是本公开的某些示例性喷嘴)的有利之处在于,喷嘴60以最小的力(包括治疗溶液的细胞膜上的剪切力和压力)向治疗部位施用治疗溶液,而不是像通过某些其他方式(例如可注射的注射器)输送治疗溶液那样。众所周知,干细胞的注射输送存在着施用后的细胞存活率问题,而本公开的喷嘴60解决了这些问题和其他问题,因为喷嘴60在治疗溶液中施用干细胞避免了现有注射方式中的剪切力和压力。喷嘴60的有利之处还在于,治疗溶液的操作施用可在不需要任何气压的情况下进行(例如氧气瓶),或者可使用气动泵驱动喷嘴。在一些示例中,喷嘴60可输送粒径大约在1-7微米范围内的颗粒。在一些示例中,可通过增加内置在电源电路板(pcb)和压电元件57内的一系列参数来调节喷嘴60的频率和振荡频率,以增加较大分子。
在图11中能更清楚地看到,在一些示例中,药筒50可在每个分隔构件65之间包括由聚合材料制成的微泡63,这样的有利之处在于,这能防止治疗溶液的细胞仅位于药筒壳体52内的托盘54、56的顶部。这样,在治疗溶液的每个干细胞进入相应的分隔构件65时能保护干细胞壁,不会因损伤干细胞壁而导致干细胞浪费。
在一些示例中,施用装置100和相应的构造可包括内部电源,例如先前说明的可更换和/或可充电的电池b。所述一个或多个电池b可包括锂离子电池,该锂离子电池包括碳阳极、由锂钴氧化物制成的阴极、以及由包含锂盐的有机溶剂构成的电解质:在某些示例中,可使用3400mah的锂离子电池,该锂离子电池在用于施用装置100时可维持40小时运行时间而无需充电。在此示例中,9v压电元件可从9v电源得电,从而保持压电元件57稳定。也可考虑其他示例性电池。在其他示例中,施用装置100和相应的构造可与外部电源(例如壁装电源插座)电连通。
虽然施用装置100可由电池b供电,但是为了实现一种电平衡系统,它仍可通过施用装置100内的静电模块向水性治疗溶液施加电荷,在此必须提供相反的电荷以补偿耗散到液体治疗溶液中的电荷。这是通过握柄上的接地板有效地实现的;相反的电荷可通过接地板从用户流向静电模块,以平衡流失到液体治疗溶液中的电荷。
在图11中还示出了药筒50的托盘54、56的横截面的近视侧视图。在使用期间,可施加静电荷,使其穿过治疗溶液并通过托盘56(和/或托盘54)的单元65。从图中能够看出,单元65可基本上为圆锥形或锥形,具有接收治疗溶液的较大开口65a以及直径小于开口65a的开口65b。每个单元65可以是成形的三维几何形状,从托盘上表面的平坦底部到较小开口65b处的点(称为顶点)平滑地逐渐变小。可有选择性地布置和分隔单元65,从而在治疗溶液的细胞进入每个单元65时,通过最大限度地减少穿过其中的治疗溶液的细胞的数量来避免堆积。这又有助于降低治疗溶液中的干细胞壁的压力,而在用高压操控时,干细胞壁可能破裂。通过在锥形电池65的每一个上施加最高0.5至5kv的电压,这种电荷允许治疗溶液的细胞在通过开口65a、65b滴落时被充电,从而产生轻微的电荷。
在某些示例中,当治疗溶液的干细胞通过托盘54、56的分隔构件(例如单元65)时,可通入低电压,从而对治疗溶液的细胞充电。然后,在一些示例中,治疗溶液的干细胞在按照由分隔构件65的取向限定的模式到达第二托盘56上时可被均匀加热。但是,该设计不限于此,相反,第一托盘54可加热治疗溶液,而第二托盘56可通过相应的构件65施加静电荷。
在包含干细胞的治疗溶液从托盘54的一个成型分隔构件65流向托盘56的另一个构件65时,治疗溶液可被加热到精确的预定温度,这又使得治疗溶液的细胞基团获得更均匀的加热温度。此外,治疗溶液的细胞可被继续充电,直到细胞或防腐剂遇到压电喷嘴60。虽然在图11中仅示出了圆锥形单元65,但是也可设想用于向治疗溶液(包含干细胞和防腐剂)施加正电荷或负电荷的其他形状和设计。
众所周知,干细胞的存活和存活率取决于输送方式,已发现细胞存活率在10%-30%之间,但是新出现的新方法正在提高存活率。本文所述的干细胞的施用方式已被证明具有优势,这至少是因为在细胞通过锥形板时低电压通过顶部托盘54和中央托盘56对细胞充电,从而确保了存活和存活率。对以一定的模式滴入一系列狭窄通道的液滴进行加热,从而以更小的批量进行加热,我们的锥形设计使各个单元能均匀地加热。在一些实施例中,具有独特轮廓的单元65配置为通过在每个65单元之间布置一种或多种多泡聚合材料63来避免仅使治疗溶液的细胞或防腐剂处于托盘54、56的顶部。相反,通过在治疗溶液进入单元65时减少对治疗溶液的干细胞壁的影响,可提高效率并减少治疗溶液的浪费。
图12-13示出了施用装置200的另一个实施例,该施用装置200与前面说明的施用装置100类似。像前面的实施例中一样,施用装置200具有壳体210,该壳体210形成可由最终用户抓握的握柄215。施用装置200可具有致动器235,该致动器235配置为激活或停用施用装置200(包括其内部泵(未示出)),并从施用装置200向治疗部位输送治疗溶液。致动器235还可配置为激活和停用药筒250(未示出,但是与药筒50类似)的静电充电件,以对治疗溶液充电并将带静电的治疗溶液输送到患者的治疗部位。施用装置200也可具有与腔室25类似的药筒接收室225,从而药筒250可插入由腔室225形成的腔体中,如图12所示。
图13特别示出了与系统1类似的系统201,该系统201包括与底座280和光学读取器290组装在一起的施用装置200,该施用装置200在此处于分解状态。光学读取器290可容纳在光学接收室295中。在施用装置200和/或光学读取器290与底座280一起储存时,可对每个的相应电源充电(例如感应充电)。图13还示出了施用装置200在插入腔室225之后与药筒250和静电喷嘴260组装在一起。
请转到图14a和14b,其中示出了示例性药筒250的近视透视图。在一个示例中,药筒250可具有矩形壳体252(当然,可根据需要或要求考虑其他形状)。与前面说明的药筒50和壳体52类似,壳体252可由聚碳酸酯、医用级塑料制成,并且可以是一次性的。药筒250可配置为对治疗溶液施加电荷,以便从施用装置200施用。而带电的治疗溶液又寻求与由患者的带电治疗部位提供的负或正地电位平衡。与药筒50类似的是,药筒250也可在壳体252的上表面上具有孔口259,以接收治疗溶液(例如可输送溶液的针头)。在一些示例中,孔口259可包括一个或多个护帽或阀门机构,用于控制治疗溶液通过其的流动。在一些实施例中,药筒250可包括位于壳体252的后表面(即,与喷嘴260相对的表面)上的一个或多个连接器272,以便于与腔室225操作连接。在一些实施例中,当在连接器270与腔室225的施用装置之间实现操作连接时,很容易检测与药筒250相关的信息,以鉴定治疗溶液。例如,底座280的显示屏、施用装置200或一些外部装置(例如可操作地连接至底座280和/或施用装置200的计算装置)可指示患者的姓名、治疗溶液的剩余量、预定的治疗部位、以及与治疗溶液相关的其他识别信息。在一些示例中,药筒250可包括一个或多个磁性连接器272,以在药筒250插入到腔室225中时便于腔室225与药筒250之间的对准。
本公开的光学读取器290可包括外壳、致动器、内部电源和/或包含在其中的一个或多个光学读取器机构。在实际应用中,光学读取器290可包括一个或多个读取器机构,所述读取器机构配置为读取药筒250(包括其中的治疗溶液容器)的信息或印刷在壳体252上的识别信息。所述一个或多个光学读取器机构可包括光源、对应的光电二极管、激光扫描机构、具有针对材料(例如带条形码的硅胶)的图像处理能力的基于摄像头的读取器、led扫描器、全向扫描器等。光学读取器290还能够在药筒250设置在腔室225内的同时扫描药筒250及其内部的任何内容物,例如通过透过观察窗或罩盖220的透明部分观察药筒250来进行。
应理解,可将本公开的包含干细胞的任何治疗溶液的每毫升(cc)细胞数调节到特定的治疗浓度,或者使其符合特定的治疗浓度。例如,干细胞的治疗相关浓度的范围可从100个细胞/微升到40,000个细胞/微升。因此,根据伤口/损伤的大小和严重程度,本公开的任何药筒的容积和浓度该可供临床医生使用。
图15a-16示出了施用装置300的另一个实施例,该施用装置300与前面说明的施用装置100和施用装置200类似。施用装置300配置为实施直接充电方法,以在使用中对水性治疗溶液进行充电,以便从液化聚合物产生涂层。具体而言,施用装置300可以是用于为创伤、烧伤、割伤等伤口提供液化绷带并产生人造皮肤的电纺装置。
在电纺中,应理解,当所施加的电势的增加量超过一定量时,来自存储单元的聚合物溶液可通过聚集在液滴尖端的电荷的排斥力而从开口施加或喷射。在带电溶液到达某个收集点时,溶液会干燥并形成无纺纤维垫,在这种情况下,该收集点可以是患者的伤口部位。在本公开中,直接充电应理解为低压电极和水性治疗溶液彼此物理接触。像前面的实施例中一样,施用装置300具有壳体310,该壳体310形成可由最终用户抓握的握柄315。施用装置300可具有致动器335,该致动器335配置为激活或停用施用装置300(包括其内部泵(未示出)),并从施用装置300向治疗部位输送治疗溶液。致动器335还可配置为激活和停用药筒350(未示出,但是与药筒50、250类似)的静电充电件,以对治疗溶液充电并将带静电的治疗溶液输送到患者的治疗部位。
药筒350可包含具有溶解在一种或多种溶剂中的聚合物试剂的治疗溶液。在加压时,混合物可在旋转的同时通过带有径向喷嘴的分配针头370。在该试剂被迫通过针头370的径向旋转喷嘴时,空气流可蒸发溶剂,并产生将被输送到伤口部位的基质。施用装置300也可具有与腔室25类似的药筒接收室325,从而药筒350可插入由腔室325形成的腔体中。图15b示出了施用装置300的示例性接地电极440的透视图,该接地电极440将附接至患者以便接地。
在使用施用装置300的一些示例中,在从喷嘴360施用治疗溶液时,可产生电纺多孔纳米纤维,这些纤维模拟细胞外基质成分(ecm)的重要特征,包括提供有利于组织再生和伤口愈合的支架。在一些示例中,这种电纺纳米纤维可通过跨膜受体或细胞内信号通路调节皮肤细胞行为。这个示例的纳米纤维可结合有可维持接种在支架上的原代细胞的增殖和迁移的生物活性材料(例如dna、酶和生长因子)。
所设想的与施用装置300结合使用的生物聚合物可包括在过去通常用作伤口敷料的动物脂肪、植物纤维和蜂蜜膏等材料。伤口处理的一个重要方面是对受伤部位进行适当的充氧以促进伤口愈合。氧气对细胞代谢、能量产生和伤口愈合的所有阶段都至关重要。白细胞产生的用于氧化杀死病原体的超氧化物依赖于氧气水平。暂时缺氧已被证明能刺激伤口愈合,但慢性缺氧会延迟这一过程。缺氧诱导巨噬细胞、成纤维细胞和角质形成细胞产生细胞因子和生长因子,这些因子对细胞增殖、迁移和趋化性以及伤口愈合中的血管生成至关重要。在正常氧化期间,活性氧(ros)能诱导伤口愈合。
施用装置300的示例性液体皮肤绷带可包括生物相容性聚合物,不限于用于适当的伤口覆盖的合成聚合物。示例性液体皮肤绷带的溶液还可包括由不止一种天然聚合物组成的混合溶液,该混合溶液通过本发明的施用装置输送到治疗部位。所得的皮肤绷带因具有渗透性而允许氧气通过,从而实现一种有氧环境。示例性液体皮肤绷带的溶液可以是柔性的,并且包括抗微生物特性。
所设想的在本公开的伤口敷料中使用和/或与本公开的伤口敷料结合使用的市售聚合物的一个非详尽列表包括:聚合物泡沫(例如flexan、biopatch、crafoams、biatain、cutinova)、聚合水凝胶(例如cultinova凝胶、biolex、tegagel、felxderm第二皮肤、干式敷料)、聚合藻酸盐(例如alginsan、algisite、sorbsan、kaltostat、omiderm)、以及聚合水胶体(例如idosorb、debrisan、sorbex、douderm)。慢性缺氧还会提高细胞因子和蛋白酶的水平,从而对周围组织造成损害。利用在本文中公开的人工皮肤绷带的静电输送方法,在通过本文所公开的一种或多种途径进行干细胞施用后,可通过本公开的药筒进行喷射,这对解决这些问题特别有利。在一些示例中,人造皮肤绷带的输送是为了保护伤口免受侵入性病原体的侵害,并可透过氧气以促进正确愈合。
天然聚合物因其生物可降解性、生物相容性和与细胞外基质(ecm)的相似性而在现代医学中普遍用于烧伤和创伤伤口敷料。多糖可用于创伤和烧伤处理,虽然它们的化学性质差异很大。用于此目的的多糖可以是酸性的、碱性的、或硫酸化的。一些例子有同多糖(例如纤维素、葡聚糖和淀粉)和/或在整个链的长度上重复的单体。海藻酸盐是从加工的海藻中获得的多糖,它也可用于伤口敷料,并且是吸收性的,并形成亲水凝胶。考虑使用的其他物质包括琼脂、果胶和牛血清。考虑与液体绷带溶液结合使用的其他天然材料包括胶原、壳聚糖、透明质酸和羧甲基壳聚糖。生物可降解聚合物能有效地与此示例一起用于多种生物医学应用,如药物输送、牙科、整形外科和组织工程。此实施例的药筒还可包括具有抗微生物特性、可渗透编织的生物相容且稳定的聚合物敷料、以及用于干细胞组织再生的保护性支撑材料。
请再参考图15a-15b,药筒350可以是一次性的,并且配置为与具有电纺输送系统的施用装置300结合使用,以将聚合物纤维基质施用到伤口上,实现快速愈合。在一些示例中,药筒350可包含治疗溶液,包括含有溶解在适当溶剂中的聚合物的治疗溶液。在加压时,该溶液可在旋转的同时通过带有径向喷嘴360的分配针头370。在此示例的治疗溶液被迫通过径向旋转喷嘴360时,空气流可蒸发溶剂,并产生将被输送到患者的伤口部位的基质。
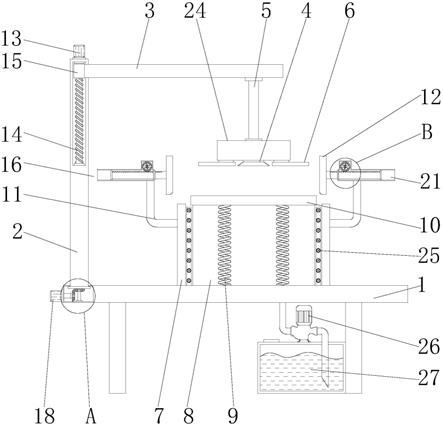
图16特别沿着中心线的横截面示出了系统301,以揭示其某些内部部件和特征。施用装置300可与光学读取器(未示出)结合使用,并且配置为与药筒350和径向喷嘴360结合使用。电机m被示为与针头370连通,该针头370与径向齿轮376连接,该径向齿轮376配置为驱动并旋转针头370。压力泵390被示为设置在药筒360下方,并紧邻电纺风扇f。管395可配置为高压供应管,并且连接至泵390,并与药筒350的存储罐流体连通。风扇f配置为蒸发从药筒350喷射的治疗溶液,包括聚合物溶液。
图17示出了施用装置300的示例性远侧尖端的近视透视截面图。针头370可包括远侧尖端372,该远侧尖端372具有用于高速气流的文丘里管,由此可向尖端372供应室温或高温空气,以促进蒸发和纤维基质的产生。可向尖端372的文丘里管供应室温或高温空气,以便于最佳蒸发和纤维基质生成。
能看到针头370沿轴向处于药筒350的针头室353内。药筒350可包括在药筒350内布置在腔室353与药筒350的外壳之间的治疗溶液储存器354。储存器354可填充有单种治疗溶液制剂或多种治疗溶液制剂,包括包含溶剂、聚合物和/或其他活性成分或药物的制剂。储存器354可由耐溶剂材料构成。药筒还可包括布置在壳体352的上表面上的孔口359,该孔口用于接收治疗溶液(例如针头可通过该孔口输送溶液)。在一些示例中,孔口359可包括一个或多个护帽或阀门机构,用于控制治疗溶液通过其的流动。
图18示出了与施用装置300组装在一起的药筒350的近视后透视图。从图中能够看出,如前文所述,泵390可对储存器354加压,并使治疗溶液被迫通过针头370的尖端,因此可选择泵390以根据输送的聚合物溶液提供不同的压力。
请转到图19a和19c,其中示出了示例性药筒350的透视图。药筒350可具有矩形壳体352(当然,可根据需要或要求考虑其他形状),可由聚碳酸酯、医用级塑料制成,并且可以是一次性的。药筒350可配置为通过电纺对治疗溶液施加电荷,以便从施用装置300施用。药筒350可填充有治疗溶液,包括包含专用聚合物试剂的溶液。储存器354可由泵390加压(例如参见图16)。在储存器354被泵390加压时,针头370的进料管377对流体加压并将流体供应至针孔。
当电机m在接头376处连接至针头370时,电机m旋转针头370,并且所产生的高压将流体、治疗溶液从喷嘴360排出,以在治疗部位产生治疗溶液的细雾。然后风扇f迫使流体(例如空气)通过尖端372的文丘里管,从而加速流体流动以快速蒸发治疗溶液的溶剂,然后输送细丝基质,该细丝基质沉积在伤口表面上。储存器壳体354中的管374两端的o型圈377实现密封,并允许对储存器354加压。
在本示例的电纺过程开始时,电荷通过针头370进入聚合物治疗溶液,从而因在聚合物液滴上感应电荷而导致治疗溶液内的不稳定性。与此同时,电荷的相互排斥产生与表面张力相反的力,最终治疗溶液沿电场方向流动。电场的进一步增加导致液滴(例如球形)变形并呈现圆锥形。在此阶段,可从锥形聚合物液滴中出现超细纳米纤维。
此示例的电场强度可克服液滴的表面张力并产生带电液体射流。然后,该射流被拉长,并被静电排斥力持续搅动,直到它沉积在接地的收集器上。溶剂在途中蒸发,并且射流固化从而形成无纺纤维膜。这种技术的处理灵活性使得能够从诸如合成聚合物、天然聚合物、半导体、陶瓷或它们的组合等多种前体材料制造纤维。
只有在聚合物溶液具有足够的内聚力时,才能形成稳定的电荷射流。在此过程中,内部和外部电荷力会导致液体射流的抖动,这使得溶液中的聚合物链拉伸并相互滑过,由此产生直径小到足以称其为纳米纤维的纤维。应理解,有多个因素影响电纺过程。这些因素分类为电纺参数、溶液和环境参数。电纺参数可包括施加的电场、针头与收集器之间的距离、流速和针头直径。溶液参数包括溶剂、聚合物浓度、粘度和溶液电导率。环境参数包括相对湿度和温度。这些参数之中的一个或多个直接影响在治疗溶液的施用装置中从施用装置300产生光滑且无珠的电纺纤维的过程。
图20a示出了针头370的透视图。图20b示出了在截面a-a处截取的图20a的针头的远侧尖端372的近视透视图。尤其是,针头370可包括很细长的管374,沿着管374的长度设有多个径向分开的进料管孔378。尖端372还可包括从管374向外突出的多个径向分开的分配元件371,以产生带静电的治疗溶液的液雾或液流。元件371可共同形成处于径向方向或朝前的任何角度的针头阵列,这有助于优选或所需的喷射施用模式。在经由接头376连接至电机m时,针头组件370可旋转,进而能够使带电聚合物相对于针头纵轴b径向流动。在一些示例中,元件371可相对于轴线b处于垂直或某个角度(例如0到90度之间的角度,例如45度)的取向。元件371的任何数量或尺寸(包括高度、喷嘴尺寸、从管374开始的每个元件的长度)可以变化,以使纤维材料在伤口部位作为液体绷带施用时形成覆盖层的任何组合。优选如图所示的针头370配置为旋转并径向喷射溶解的聚合物,然后使该治疗溶液受到速度非常高的气流的作用,该气流干燥溶剂并将纤维束重定向到目标位置。在一些示例中,作为图20a-20b所示的配置的结果,还可提供更宽的散布模式。
图21示出了与系统1/201类似的系统301,该系统301包括与底座380组装在一起的施用装置300。在施用装置300与底座380一起储存时,可对施用装置的各个电源充电(例如感应充电)。图21还示出了施用装置300在插入施用装置300的腔室325之后与药筒350和静电喷嘴360组装在一起。系统301还可包括备用药筒350以及用作控制中心的显示器d,该显示器d显示系统状态信息、患者信息、药筒信息等。应理解,底座380可配置为监控并向用户通知所有系统功能。施用装置300和/或底座380还可根据需要或要求利用加热器来加热治疗溶液、排出的气流和/或针头的溶液输送机构。
在一些示例中,本公开的药筒可包括消毒药筒,该消毒药筒包括具有一定百分比的抗菌溶液的混合试剂。该混合试剂可包括双胍类试剂(例如氯己定,又称为葡萄糖酸氯己定,它是防腐产品中广泛使用的生物杀灭剂;尤其是用于洗手和口腔产品,但也作为消毒剂和防腐剂)。这些消毒剂具有广谱效力、对于皮肤的直接性和低刺激性。该混合试剂还可包括碘载体(例如倍他定,例如聚维酮碘和泊洛沙姆碘,它们比碘水溶液稳定得多,具有较少刺激性,并能发挥更好的杀微生物作用)。通过施加正电荷而静电输送的溶液可使得试剂在损伤部位均匀分布,并结合至已知带负电荷的细菌膜上,从而破坏细胞的完整性。
大多数表面消毒剂或除污剂要么对具有挑战性的病原体(或难降解污染物)的效能很低,要么由对用户有毒且对环境有害的刺激性化学物质组成,因此受到限制。尤其是,有毒化学品的使用需要规定的使用浓度和规定的接触时间,以达到预期的抗菌效果。但是,这些化学品的处理和使用除了给环境带来危害之外,还经常给用户带来危险,并且会对被消毒(或净化)的材料造成损害。在本文中公开的内容说明了一种通过激活待处理表面处或附近的氧化混合物对表面和空气间层进行消毒或净化的方法。本公开中的某些示例的治疗溶液解决了本领域中的这些问题和其他问题。
例如,本公开的消毒剂治疗溶液的组成和化学性质可包括用于高级医院消毒、酒店和设施清洁、卫生和除臭、表面消毒和去污以及农业植物(温室和农作物)和土壤处理的氧化混合物。在一些示例中,可“活化”混合物的组分以提高抗菌和去污性能。
在一些示例中,产生治疗溶液的氧化混合物的组分和方法设计为形成在活化时促进和维持活性氧类(ros)的形成的混合物。在待清洁、消毒或净化的表面上或附近形成ros能提高无毒组合物的抗菌效能(或净化效能)。此外,所述组合物可以是基于过氧化物的(例如至少一种过酸、过碳酸盐、过硫酸盐、过硼酸盐和/或过氧化物的混合物),并且可按支持活化以形成ros且排除抑制ros的组分和条件的方式配制和/或制备。所述混合物可选地包含其他组分,包括洗涤剂、表面活性剂、助洗剂、酸碱度调节剂、香料和/或颜色添加剂等。
在一些示例中,可激活所述氧化混合物,以将有效浓度的ros输送到表面上。例如,氧化混合物可包括在待消毒或净化的表面处或附近的氧化混合物的化学活化和/或光解活化。本公开还可包括一种将化学活化剂、活化剂混合物或催化光子引入待消毒表面处或附近的喷雾或薄雾中的方法。本公开还可包括一种使用活化的(例如增强的)氧化混合物对施用装置的喷嘴与表面之间的空气间层进行消毒和/或净化的方法。
在一些示例中,可在待净化或消毒的表面处或附近活化所述氧化混合物。ros的寿命极短,需要在表面或表面附近活化。所述氧化混合物可通过非均相化学物质(催化剂)、均相化学物质(催化剂)或激活光子活化。活化方法可包括引入活化剂(催化剂)组分并将其与来自施用装置的氧化混合物的薄雾或喷雾混合。一部分氧化混合物可立即与催化剂反应,在来自施用装置的治疗溶液流中形成ros。另一部分氧化混合物可夹带活化化学物质(催化剂)组分(例如在非均相催化剂和均相催化剂的情况下),并且可将一部分活化化学物质(催化剂)与氧化混合物一起输送到表面上。在覆盖在表面上时,该活化化学物质(催化剂)可继续反应,并在待净化或消毒的表面上产生ros。
应理解,此实施例的均相化学活化剂例如可包括水溶性过渡金属络合物和可溶性过渡金属盐。也可使用可溶性光催化剂。应理解,多相化学活化剂可包括臭氧气体(o3)、不溶于水的过渡金属(小颗粒)或其他不溶性的活化材料,例如活性炭。也可使用不溶性光催化剂。应理解,可将光子从氧化混合物的施用装置引入到治疗溶液流中。同样,可在表面被氧化混合物覆盖后向该表面引入光子。光子可以是特定波长的,或者在直接激活氧化剂以形成ros的波长范围内。在另一个实施例中,光子可具有活化同质和/或异质光催化剂的波长。将活化化学物质(催化剂)、或者活化剂(催化剂)的混合物或它们的组合、至少一种化学活化剂(催化剂)和活化光子从氧化混合物的施用装置引入治疗溶液流中,以在被喷射的表面处和附近形成ros。
在一些示例中,可使用臭氧气体作为化学活化剂。可将规定浓度的一定量的臭氧气体按规定的体积比混合到水性活化剂流中。臭氧气体可在喷嘴前或喷嘴后混合,并且可存在于三(3)个区域中:1)一些立即溶解(o3溶解)并开始反应,2)一部分臭氧被夹带在喷雾中(o3夹带),并以未溶解和未反应的状态输送到表面上,以及3)剩余部分存在于喷射器与所述表面之间的空气间层中(o3气态)。
活化剂引入的另一个示例性模式包括使用双罐,其中在一个罐中可容纳有较高浓度的活化剂(均匀混合液或异质悬浮液),而在另一个罐中容纳有水性氧化混合物。此实施例允许混合两股液流,其中活化剂存在于允许较高浓度的溶剂中。这可通过在施用装置本身中布置双罐或者采用向施用装置喷嘴供液的分体罐来实现。罐的一侧可包括含水氧化剂,而罐的另一侧可包括溶解在提高臭氧溶解度的溶剂(例如酒精)中的臭氧。这两种独立的混合物可在喷嘴前或喷嘴后泵入并混合在一起。
在一些示例中,为了减轻与伤口部位的慢性/急性创伤和/或烧伤相关的不适和疼痛,试剂可具有附加的止痛性质。试剂可包含一定百分比的以下物质:在按照建议局部应用时通常耐受性良好且无毒的经过批准的药物试剂,例如利多卡因、丁卡因、苯佐卡因。试剂还可包含能减轻与表皮损伤相关的不适的任何经过批准的止痛药液。其他物质的例子包括但不限于盐酸普拉克辛、樟脑、薄荷醇、苯酚和苯海拉明,这些物质可缓解自由神经末梢刺激引起的疼痛。
就疼痛处理而言,疼痛可理解为是由自由神经末梢的刺激引起的。在神经末梢受到刺激时,钠进入神经元,导致神经去极化并产生动作电位。该动作电位继续传播到中枢神经系统(cns),并发出疼痛信号。镇痛药的药理作用是抑制神经元膜上的电压依赖性门控钠通道(vdsc)和抑制动作电位的传播。还可能存在只有消毒剂是在此示例性实施例的药筒中待施用的独立试剂的情况。这也适用于配有专用的输送药筒的止痛溶液。因此,可将一次性试剂药筒装载到本发明的施用装置上,然后临床医生可将试剂输送到伤口部位,并执行输送治疗生物制剂(例如同种异体或自体干细胞溶液)的下一步骤。本公开的溶液又通过消除感染的易感性和减轻与表皮创伤相关的不适加速伤口愈合过程。
在一些示例中,在神经末梢受到刺激时,钠进入神经元,导致神经去极化并产生动作电位。该动作电位继续传播到中枢神经系统(cns),并发出疼痛信号。镇痛药的药理作用是抑制神经元膜上的电压依赖性门控钠通道(vdsc)和抑制动作电位的传播。还可能存在只有消毒剂是在药筒中待施用的独立试剂的情况。这也适用于配有专用的输送药筒的止痛溶液。
可将本实施例的药筒及其一次性试剂装载到本公开的施用装置上,临床医生可将试剂输送到损伤部位,并执行输送治疗生物制剂的下一步骤(例如施用同种异体/自体干细胞)。此过程又可通过消除感染的易感性和减轻与表皮创伤相关的不适加速伤口愈合。
图22示出了具有施用装置400的系统401。图23示出了系统401的分解图。从图中能够看出,施用装置400具有壳体410,该壳体410形成可由最终用户抓握的握柄415。施用装置400可具有致动器435,该致动器435配置为激活或停用施用装置400(包括其内部泵(未示出)),并从施用装置400向治疗部位输送治疗溶液。致动器435还可配置为激活和停用药筒350(未示出,但是与药筒50、250、350类似)的静电充电件,以对治疗溶液充电并将带静电的治疗溶液输送到患者的治疗部位。与上述药筒一样,药筒450可包含具有溶解在一种或多种溶剂中的聚合物试剂的治疗溶液。药筒450可具有矩形壳体452(当然,可根据需要或要求考虑其他形状),可由一个或多个聚碳酸酯或医用级塑料模制件制成,并且可以是一次性的。药筒450可配置为对治疗溶液施加电荷,以便从施用装置400施用。在加压时,混合物可被迫通过喷嘴460,从而将产生基质的溶液输送到伤口部位。药筒450也可以是一次性的,并配置为与施用装置400结合使用。
施用装置400也可具有与腔室25、225、325类似的药筒接收室425,从而药筒450可插入由腔室425形成的腔体中。在使用施用装置400的一些示例中,在从喷嘴460施用治疗溶液时,可产生静电和/或电纺多孔纳米纤维,这些纤维模拟细胞外基质成分(ecm)的重要特征,包括提供有利于组织再生和伤口愈合的支架。在一些示例中,这种电纺纳米纤维可通过跨膜受体或细胞内信号通路调节皮肤细胞行为。这个示例的纳米纤维可结合有可维持接种在支架上的原代细胞的增殖和迁移的生物活性材料(例如dna、酶和生长因子)。喷嘴460可耦合至药筒450和电机m的电纺输送系统,以将聚合物纤维基质施加到伤口上实现快速愈合,这分别类似于施用装置300和药筒350。如图23所示,电机m可设置为与喷嘴460和药筒450以及电池b和电路板c连通。在药筒450中可设有一根管作为高压供应管,并且该管连接至药筒450的储罐并与其流体连通。在一些示例中,与施用装置300类似的是,施用装置400可设有泵,所述泵可对储存器454加压并使治疗溶液被迫通过喷嘴460。
图24a至24c示出了药筒450的不同透视图。药筒450可包括前电机接收面473,该接收面配置为在与施用装置400组装时机械地耦合至电机m。药筒450还可包括与所述面473相反的后喷嘴接收面475,一个或多个喷嘴面安装件462可有选择性地置于后喷嘴接收面475上,以导引、对准和可滑动地接收喷嘴460。例如,如图23所示,喷嘴460包括从喷嘴460的喷嘴主体向外延伸的对准导引件,从而每个导引件配置为使喷嘴与面473对准、配合,并正确排列成组装形态,直到喷嘴460与设置在药筒450和电机m内的治疗溶液储存器454的治疗溶液流体连通,或者相反(例如将药筒450导引到与施用装置400组装的位置)。在药筒450的下表面上可设置喷嘴通道476,该喷嘴通道类似地配置为将喷嘴可滑动地导引到适当位置,或者相反(例如导引药筒450进入与施用装置400组装的位置)。
从图中能看出,药筒450还可包括释放按钮482,该释放按钮482至少部分地位于壳体452的上表面上。在一些示例中,按钮482可通过可操作地连接至表面或紧邻表面的偏压构件(例如弹簧)连接至药筒450。此外,壳体452可在其上表面上包括孔,按钮482可通过该孔在锁定状态与解锁状态之间移动。在使用时,移动按钮482(例如上下移动)可使按钮482将施用装置400与药筒450牢固锁定,如图22所示,或者可根据需要或要求将药筒450从该状态释放为解锁状态。
储存器454可填充有单种治疗溶液制剂或多种治疗溶液制剂,包括包含溶剂、聚合物和/或其他活性成分或药物的制剂。储存器454可由耐溶剂材料构成。药筒还可包括布置在壳体452的上表面上的孔口459,该孔口用于接收治疗溶液(例如针头可通过该孔口输送溶液)。在一些示例中,孔口459可包括一个或多个护帽或阀门机构,用于控制治疗溶液通过其的流动。
图25示出了患者的伤口部位处的示例性电场的示意性概图,由此示出了与细胞迁移相关的电矢量。在一些示例中,本公开的施用装置可使用高压泵p(例如160-180psi)对流体加压,并且其药筒(50/250)的静电模块可对相应治疗溶液的分子进行充电和电离。治疗溶液可通过相应的喷嘴以精细带电、均匀分布的液雾的形式施加,并借助于静电吸引力从各个方向粘附到治疗部位。在一些示例中,施用装置可包括流量计和相关电路。操作中的治疗溶液量可作为离散记录行记录在施用装置的计算系统的内部存储器中。还可无线地访问和/或保存和下载这些记录(例如通过移动装置以
施用装置可包括由标称电压为14.8伏、最大电压为16.8伏的电池组供电的内部电源。还可包括一个或多个led以提供指示,包括与治疗溶液或施用装置的功率相关的信息。例如,蓝色led可用作用户的
在成功连接至移动装置后(例如参见图26和图28),相应的施用装置可自动传输关于施用装置的当前工作状况的数据,包括记录号、电池电力、治疗溶液的流速和/或类似数据。移动装置还可无线地访问、查看和/或保存先前的记录,由此每个记录行可包括记录号、日期和时间(如果有)、初始功率水平、最终功率水平、总治疗溶液流量、与治疗溶液相关联的验证码(例如与治疗溶液的硅胶相关联的条形码)和/或类似数据。
在一些示例中,若从系统的流量计接收到一个或多个脉冲信号,则电路可开始记录流量和其他相关数据。但是,若未接收到这样的脉冲信号,则不能启动记录操作。此外,若没有与移动装置建立连接,则“00”会被写入日期/时间字段,否则会为该记录保存实际开始日期和时间(从便携装置导出)。
施用装置可包括由标称电压为14.8伏(最大电压为16.8伏)的可更换电池组供电的一个或多个电池b。在一些示例中,电池b可包括四个串联的18650电池(每个3.7伏)。通过将电池数量增加一倍,容量可增加一倍,待机电流可小于10μa。在一些示例中,电池功率指示可由一个或多个led反映。例如,四个绿色led可表示>16伏;三个绿色led可表示>14.6伏;两个绿色led可表示>13.2伏;一个绿色led可表示>12伏;一个红色led可表示<11.8伏。在这样的示例中,施用装置可能不会被其致动器35/235激活。此外,在一些示例中,若在预定的持续时间内(例如在泵p启动后30秒内)没有记录到治疗溶液的流动,则施用装置可配置为自动停用,并快速闪烁以指示问题。
在一些示例中,移动装置和/或施用装置的无线模块必须经历握手过程,以避免与移动装置的其他不相关的应用连接。在这些方面,在成功连接至移动装置之后,施用装置可自动传输关于当前工作状况的数据,包括当前的记录总数、电池功率设置、治疗溶液流速、治疗溶液液位和性质(例如,治疗溶液类型包括干细胞、药物、消毒剂的浓度等)。在一些示例中,用户还可在驻留在移动装置中的应用中读取先前记录的每组数据。在一些示例中,存储器可存储多达4000组数据,并且在存储器存满时,新数据可覆盖旧数据。
图26示出了本公开的示例性实施例的系统架构的示意图。根据某些实施例,系统2600可包括面向用户的前端装置,该前端装置包括软件、固件和/或硬件,用于在使用之前、期间和之后监视和/或控制本公开的任何施用装置。在一些实施例中,该用户界面可包括如图28所示的移动计算装置2810(例如智能电话)上的移动应用程序(“app”)或其他可执行软件。应理解,装置2810可以是本公开的类似地配置为与服务器2620、2640通信的光学读取器(例如光学读取器90/290)。在另一个实施例中,所述界面可包括可通过浏览器或其他软件访问的基于网络的应用程序、或者桌面应用程序。在一些示例中,所述移动应用程序可包括用于管理使用本公开的任何施用装置(或多个施用装置)的一个或多个位置的客户端。该应用程序可配置为提供或支持用于管理本公开的任何施用装置的功能。此外,该应用程序可提供常规操作设置和调度,并可在手动和自动控制期间手动接管本公开的任何施用装置、角色管理、警报;和/或评论和共享功能及与施用装置的治疗溶液相关的支持。根据某些示例,该应用程序可在仪表板视图中呈现关于相关联的治疗溶液、患者、最终用户、治疗部位、剂量等的信息。在一个示例中,可显示施用装置的操作状态和/或电池电量和/或其他可显示的信息,包括患者目的地、相应喷嘴的位置或设置、与治疗溶液相关联的数据等。选择用户界面项目可调出具有可编辑的细节和控制的视图,以管理施用装置的状态。
根据某些示例,用户可接收指示相应施用装置的一个或多个当前操作的状态的通知(例如警报消息)。例如,在新操作开始时,用户可通过应用程序接收通知。通知的形式包括应用程序内部的应用程序通知、电子邮件和消息传递(例如sms、mms等)。在一些示例中,可根据一个或多个治疗参数自动选择适当的施用装置进行操作。
系统2600可包括本公开的任何施用装置、网络服务器2620、数据库服务器2640,每个装置都是直接或无线地连接的(例如通过3g/4g、射频、本地无线网络等)。数据库服务器2640可通过一个或多个网络可操作地连接至一个或多个网络服务器2620,每个服务器可操作以永久存储和/或连续更新存储主数据的数据库(例如相应施用装置、患者、治疗溶液等的数据)。
网路服务器2620可包括后端架构,该后端架构可包括一个或多个数据库服务器2640,或者与一个或多个数据库服务器2640通信,由此系统300的功能可在多个服务器之间划分,这可由一个或多个独立提供商提供。在一个示例实施例中,数据库服务器2640可存储主数据以及日志和跟踪信息。数据库服务器的软件可基于对象关系数据库系统postgressql,该数据库服务器不受此限制,可根据需要或要求使用其他途径。此数据库服务器2640不限于仅组织和存储数据,还可用于消除对应用服务器(例如第二层)的需求。在一些实施例中,几乎每个功能需求都可通过使用数据库的编程语言pl/pgsql来实现。该数据库还可基于json规范向网络服务器2620提供用于数据交换的应用编程接口(api)。在一些实施例中,数据库服务器2640也可直接与相应施用装置和/或移动装置2810的所述功能交互。
图27是示出能够按照在本文中说明的一个或多个实施例实现本公开的各个方面的通用计算系统的计算机架构图。计算机2700可配置为执行与本公开的实施例相关联的一个或多个功能。例如,计算机2700可配置为执行操作,以管理和有效地使用相应的施用装置,并向相应的患者输送治疗溶液。应理解,计算机2700可在单个计算装置或由多个连接的计算装置形成的计算系统中实现。计算机2700可配置为执行各种分布式计算任务,其中处理和/或存储资源可分布在多个装置中。图27所示的系统的数据采集和显示计算机2750和/或操作员控制台2710可包括计算机2700的一个或多个系统和组件。
如图所示,计算机2700包括处理单元2702(“cpu”)、系统存储器2704和将存储器2704耦合至cpu2702的系统总线2706。计算机2700还包括用于存储程序模块2714的大容量存储装置2712。程序模块2714可用于分析和/或修改施用装置的当前设置,以及对患者进行个性化治疗,包括向患者输送治疗溶液的方式和量。例如,使计算机2700针对患者的治疗部位使用施用装置,如本公开的任何附图所述。程序模块2714可包括成像应用程序2718,该成像应用程序用于执行如本文所述的数据采集和/或处理功能,例如采集和/或处理与感兴趣区域的磁共振成像对应的图像数据。计算机2700可包括用于存储数据的数据存储2720,所述数据可包括与成像相关的数据2722,例如从根据本公开的各种实施例的磁共振成像的具体实现获取的数据。
大容量存储装置2712通过连接至总线2706的大容量存储控制器(未示出)连接至cpu2702。大容量存储装置2712及其相关联的计算机存储介质为计算机2700提供非易失性存储能力。虽然在本文中包含的计算机存储介质的说明指诸如硬盘或光盘驱动器等大容量存储装置,但是本领域技术人员应理解,计算机存储介质可以是能够被计算机2700访问的任何可用的计算机存储介质。
作为一个非限制性示例,计算机存储介质(在此也称为“计算机可读存储介质”)可包括以用于存储信息(例如计算机存储指令、数据结构、程序模块或其他数据)的任何方法或技术实现的易失性和非易失性、可移动和不可移动介质。例如,计算机存储介质包括但不限于随机存取存储器(ram)、只读存储器(rom)、可编程只读存储器(eprom)、电可擦可编程只读存储器(eeprom)、闪存或其他固态存储技术、cd-rom、数字多功能盘(“dvd”)、hd-dvd、blu-ray或其他光学存储装置、磁带盒、磁带、磁盘存储器或其他磁性存储装置,或者可用于存储所需信息并可由计算机2700访问的任何其他介质。在本文中说明的“计算机存储介质”或“计算机可读存储介质”不包括瞬态信号。
根据多个实施例,计算机2700可使用经由连接至总线2706的网络接口单元2710通过网络2716与其他本地或远程计算机的连接在网络化环境中操作。网络接口单元2710可便于计算装置的输入和输出连接至一个或多个适当的网络和/或连接,例如局域网(lan)、广域网(wan)、互联网、蜂窝网络、射频(rf)网络、支持蓝牙的网络、支持wi-fi的网络、基于卫星的网络、或者用于与外部设备和/或系统通信的其他有线和/或无线网络。
计算机2700还可包括接收和处理来自任何数量的输入装置的输入的输入/输出控制器2708。输入装置可包括键盘、鼠标、触控笔、触摸屏、麦克风、音频采集装置和图像/视频采集装置中的一种或多种。最终用户可利用输入装置与用户界面(例如图形用户界面)交互,以管理由计算机2700执行的各种功能。总线2706可使处理单元2702能够向/从大容量存储装置2712或其他计算机存储介质读取代码和/或数据。
计算机存储介质可代表使用任何适当的技术实现的存储元件形式的装置,包括但不限于半导体、磁性材料、光学器件等。计算机存储介质可代表存储器组件,无论其采用的是ram、rom、闪存还是其他类型的技术。计算机存储介质还可代表辅助存储装置,无论其是以硬盘驱动器还是以其他方式实现的。硬盘驱动器实现形式可以是固态形式,或者可包括存储磁编码信息的旋转介质。包括成像应用程序2718的程序模块2714可包括在被加载到处理单元2702中并被执行时使得计算机2700提供与本公开的附图中示出的一个或多个实施例相关联的功能的指令。程序模块2714还可提供各种工具或技术,通过这些工具或技术,计算机2700可使用在本说明书论述的组件、流程和数据结构参与整个系统或操作环境。
一般而言,程序模块2714可在被加载到处理单元2702中并被执行时将处理单元2702和整个计算机2700从通用计算系统转变为专用计算系统。处理单元2702可由任何数量的晶体管或其他分立电路元件构成,它们可单独或共同处于任何数量的状态。更具体地说,响应于包含在程序模块2714内的可执行指令,处理单元2702可作为有限状态机操作。这些计算机可执行指令可通过指定处理单元2702如何在状态之间转换来转换处理单元2702,从而转换构成处理单元2702的晶体管或其他分立硬件元件。
对程序模块2714进行编码也可转换计算机存储介质的物理结构。在本说明书的不同实现方案中,物理结构的具体转换可能取决于各种因素。这些因素的例子可包括但不限于用于实现计算机存储介质的技术,不论该计算机存储介质是主存储装置、辅助存储装置、还是其他存储装置。例如,若计算机存储介质被实现为基于半导体的存储器,则当软件被编码在其中时,程序模块2714可转换半导体存储器的物理状态。例如,程序模块2714可转换构成半导体存储器的晶体管、电容或其他分立电路元件的状态。
作为另一个例子,计算机存储介质可使用磁或光技术来实现。在这样的实现方式中,当软件被编码在磁性或光学介质中时,程序模块2714可转换该磁性或光学介质的物理状态。这些转换可包括改变给定磁介质内的特定位置的磁特性。这些转换还可包括改变给定光学介质内的特定位置的物理特征或特性,以改变这些位置的光学特性。在不脱离本说明书的范围的情况下,物理介质的其他转换也是可能的,提供前述例子只是为了便于论述。
图28示出了与施用装置和任何相应的治疗溶液一起使用的移动装置2810的一个示例性实施例的示意性概图。移动装置2810可以是配置为采集图像的任何电子装置,例如移动电话、媒体播放器、便携式游戏装置、平板电脑等。应说明的是,本公开不限于任何单一类型的移动装置。根据本公开的任何先前公开的实施例,装置2810可与外部计算装置(例如服务器2620、2640)和/或系统(例如计算系统2700)无线连接并由其控制,例如与本文公开的任何计算系统无线连接并由其控制,由此这种外部系统可操作以执行与治疗方案及施用装置相关的指令。或者,装置2810可在本地传输针对患者及其治疗部位的相应施用装置和任何相应治疗溶液、治疗方案等的数据。
装置2810可通过驻留在装置2810上的应用程序与外部计算装置可操作地通信。装置2810可包括配置为采集治疗部位(例如伤口部位)的图像或视频以便分析和/或分类治疗部位(例如确定所需治疗的类型)的光学系统,例如内置摄像头。
装置2810的示例性架构可包括中央处理单元,在其中处理计算机指令;作为通信接口并提供用于在显示器上呈现视频、图形、图像和文本的功能的显示接口、以及向键盘提供通信接口的键盘接口;以及向装置2810和/或耦合至装置2810的任何外部计算装置提供通信接口的定点装置接口。所述架构的示例性实施例可包括向天线提供通信接口的天线接口。示例性实施例可包括可向外部装置或网络提供通信接口的网络连接接口。
在某些实施例中,可提供摄像头接口,该摄像头接口作为通信接口,并提供用于从内至摄像头采集数字图像的功能以及可视化治疗部位或相应治疗方案的某些方面的能力,包括与其相关联的任何跟踪物质(例如具有跟踪特征的硅胶,用于鉴定患者的治疗溶液)。根据一些示例实施例,可提供随机存取存储器(ram),可在其易失性存储装置中存储计算机指令和数据,以便由cpu处理。所述架构可包括只读存储器(rom),可在其非易失性存储装置中存储用于基本输入和输出(i/o)、启动或从键盘接收击键等基本系统功能的不变低级系统代码或数据。根据一个示例实施例,所述架构可包括存储介质或其他适当类型的存储器(例如随机存取存储器(ram)、只读存储器(rom)、可编程只读存储器(prom)、可擦除可编程只读存储器(eprom)、电可擦除可编程只读存储器(eeprom)、磁盘、光盘、软盘、硬盘、可移动磁带盒、闪存驱动器),其中存储的文件包括操作系统、应用程序(包括网络浏览器应用程序、小部件或小工具引擎和/或其他应用程序等,可根据需要而定)和数据文件。根据一个示例性实施例,所述架构可包括向功率组件提供适当的交流(ac)或直流(dc)电流的电源。根据一个示例实施例,所述架构可包括允许所述装置通过电话网络发送和接收声音的电话子系统。组成装置和cpu可通过总线相互通信。
请转到图29,其中示出了移动装置2810的应用程序的示例性活跃事件或先前事件查看器。如前文所述,装置2810的一种示例性应用程序可包括用于相应施用装置和相应最终用户和/或患者的任何数量的不同控件和指示器。例如,在图29中示出了查看器,该查看器显示与具有同步时间标记的事件相关的信息、与相应施用装置的连接状态,其中,还可定义一个或多个警报,包括功率水平、治疗溶液数据、记录的事件数量、运行时间等。
在图30中,公开了方法3000,该方法包括对患者治疗部位的治疗溶液进行静电充电的步骤3010;以及通过施用装置将治疗溶液均匀地施用在患者的治疗部位上的步骤3020。
在图31中,公开了方法3100,该方法包括对患者治疗部位的治疗溶液进行静电充电的步骤3110;通过施用装置将治疗溶液均匀地施用在患者的治疗部位上的步骤3120;用与治疗部位的消毒剂和/或干细胞中的至少一种混合的跟踪材料形成治疗溶液的步骤3130;使用布置在施用装置外部的光学读取器鉴定治疗溶液的内容物的步骤3140;以及若治疗溶液是真品则通过施用装置在患者的治疗部位上均匀施用治疗溶液的步骤3150。
在图32中,公开了产生包含电纺纤维垫的液体绷带的方法3200。方法3200可包括向用于在治疗部位产生和输送液体绷带的施用装置中的药筒的治疗溶液施加电势的步骤3210。该施用装置可以是本公开的任何一种,包括施用装置300。方法3200还可包括通过可旋转针头电纺治疗溶液的步骤3220。
在某些示例中,还与在本文中论述的其他实施例一起公开了一种能够实现均匀的施用(例如用于有针对性地施用的治疗溶液的液雾、喷雾或成组液滴)的新充电方法。本公开的示例性系统还提供了一种能够跟踪患者的治疗溶液以确保将正确的溶液施用给正确的患者的仪器。
在一些示例中,本公开的施用装置和相关系统配置为使用如本文所述的压电系统输送包含痤疮药物和/或治疗剂的治疗溶液。在此示例中,药筒可以是一次性的,并且包含由医生在门诊环境中向感兴趣部位输送的治疗溶液。可设想,施用装置和相关系统可配置为治疗各种类型的寻常痤疮,包括非炎性痤疮和炎性痤疮,因而治疗溶液可包含处方药和/或非处方药。这一点尤其重要,因为预计痤疮治疗的全球市场非常大。(例如,2016年的全球市场价值为49亿美元,预计到2025年将超过70亿美元)。如上所述,治疗溶液可包括用于抗炎、抗菌和抗感染的处方药物。在一些实施例中,治疗溶液可包括可通过本公开的静电系统输送的药物,例如过氧化苯甲酰和局部维a醇治疗药物。
在一些示例中,人类干细胞的输送可包括以下操作参数:使用250伏;200μf电容;1000欧姆电阻和指数衰减波形。应理解,以较低的刺激水平(例如5v/cm,8ms,5hz)使用电刺激(es)也能表现出β转化生长因子(tgf-β)和骨形态发生蛋白(bmp)增加。但是,也可根据需要或要求考虑更低的es(1v/cm,8ms,5hz)。
治疗溶液的静电输送的另一个方面可以是向试剂药筒添加附加组分,这会通过结合支架蛋白(例如层粘连蛋白、纤维蛋白、胶原蛋白、或细胞外基质(ecm)的某些组分)实现细胞物质的粘附。这些生物分子能够在任何类型的伤口愈合过程中为输送的干细胞提供附加支撑。还可包含专有的ecm因子,这些因子可提高向感兴趣区域输送的细胞的存活率。
临床医生期望实现加速愈合、防止伤口挛缩和疤痕形成、尽早伤口闭合和理想的皮肤再生。它们的治疗潜力在很大程度上是由于其分泌促再生细胞因子的能力,这使它们成为治疗慢性创伤和烧伤的一种有吸引力的选择。将干细胞药筒无菌地装载到静电输送装置上,并喷洒在伤口部位。含有干细胞的溶液是与生理相关的缓冲液,该缓冲液还可含有某些生长因子或营养因子,这些生长因子或营养因子会支持并加速治疗性干细胞的愈合作用。这些因子可包括成纤维细胞生长因子(fgf)、表皮生长因子(egf)、血小板衍生的生长因子(pdgf)、肝细胞生长因子(hgf)、血管内皮生长因子(vegf)和β转化生长因子(tgf-β)。
干细胞药筒的试剂还可具有携带基因治疗物质的能力,以靶向和修正与由dna、rna、生长因子、底物和/或细胞缺陷引起的表皮突变相关的任何遗传缺陷。干细胞溶液还可包括可为与任何类型的伤口愈合过程相关的任何不同阶段提供有益特性的药物试剂,例如小分子、生物活性肽和/或抗体。
在一些示例中,由体内的成纤维细胞分泌胶原蛋白,胶原蛋白是一种结构蛋白,它刺激细胞迁移。胶原蛋白可吸引成纤维细胞,从而在伤口愈合过程中促进新组织的沉积。i型胶原蛋白可以是一种生物相容的丰富蛋白质,存在于身体的结缔组织中。胶原蛋白可在止血中发挥主要作用,以促进伤口愈合,并直接支持成纤维细胞的生长、附着、分化和角质细胞的迁移。
在一些示例中,壳聚糖是所考虑的与治疗溶液结合使用的另一种聚合物。在用于烧伤伤口愈合时,壳聚糖的特殊柔韧性和弹性可显著减少疤痕的形成。壳聚糖因其静电功能能刺激胶原蛋白的合成和fgf,这能提高伤口愈合率。
在一些示例中,还设想了使用压电致动器输送作为皮肤敷料的生物材料的生物打印可与本公开的施用装置、系统和药筒结合使用。典型情况下,生物墨水可在物理上作为负载细胞的水凝胶或在印刷后立即移除的牺牲支撑材料,或者作为向组织提供特定机械特性的机械支撑材料。生物墨水可以是纯天然材料,例如胶原蛋白、纤维蛋白、透明质酸和藻酸盐,它们可以水凝胶的形式用于细胞或合成材料。这种材料可包括聚己内酯(pcl)、聚乳酸(pla)、聚乙交酯(pga)、乳酸/羟基乙酸共聚物(plga)和聚乙二醇(peg)聚合物、或者包含天然和合成材料组合的混合生物材料,它们可提供机械支撑,例如与气动排出方法相比提高细胞存活率。
pga是一种具有优良的降解行为的材料。此外,可考虑使用合成聚合物(例如聚偏二氟乙烯(pvdf)和聚丙烯(pp))作为伤口敷料材料。聚己内酯(pcl)、聚乙二醇(peg)、聚氧化乙烯(peo)、聚氨酯(pu)、聚乙烯醇(pva)、聚乳酸(pla)和乳酸/羟基乙酸共聚物(plga)是所考虑使用的合成材料,由于其良好的生物相容性、生物降解性和无毒特性,它们已被美国食品及药品监督管理局(fda)批准用于生物医学应用。
在一些示例中,所述施用装置和相关系统具有作为带压电喷嘴的手持便携式静电装置的独特特征,该压电喷嘴具有配置为提供伤口护理和治疗的大部分(如果不是全部)特性。在一些示例中,可设想同时或以其他方式使用多个药筒,由此所述系统能够为任何类型的创伤和/或烧伤提供消毒和止痛特性。所述施用装置和相关系统最好包括在感兴趣部位上输送(例如喷雾)治疗性生物制剂(例如干细胞)以加速伤口愈合的能力,并具有追踪所产生的细胞的来源的潜在能力。
在一些示例中,所述施用装置和相关系统可配置为用于向患者的喉咙输送治疗溶液。例如,考虑到患者可能遇到的疼痛程度和口腔感染程度,喉痛药物的输送可能很困难。目前的护理和干预标准是口漱和/或喷麻醉剂(例如可待因),这对于患者来说是痛苦和麻烦的。因此,本公开的施用装置的静电输送系统配置为解决这些问题。具体而言,本发明的施用装置和相关系统配置为向治疗部位(例如感染的咽喉)输送治疗溶液,所输送的治疗溶液可比目前使用的治疗溶液少得多,并且带静电的药物可到达漱口水目前无法覆盖的更大区域。在一些实施例中,施用装置可使用在患者的食道/气道中建立的跨上皮电位(tep),并且若受到溃疡或开放性伤口的干扰,该气道可作为带电治疗溶液的途径或目标,以覆盖治疗部位的感兴趣区域。
在一些示例中,所述施用装置和相关系统可配置为用于向鼻内输送治疗溶液。例如,向鼻内输送治疗溶液(包括干细胞)在治疗始于早期新生儿缺氧缺血性脑损伤、胶质母细胞瘤、中风以及其他神经退行性疾病的潜在中枢神经系统(cns)疾病方面具有新兴的治疗潜力。神经退行性疾病的一些例子包括帕金森氏症、亨廷顿氏症和阿尔茨海默氏症。在此方面,本公开的施用装置可配置为对感兴趣的干细胞进行静电充电,并通过鼻腔施用。干细胞的迁移可经由可支配鼻腔远侧区域的嗅觉区域的嗅觉神经和/或三叉神经进行。此实施例的治疗价值及其在间充质干细胞(msc)或其他干细胞(胚胎、神经元干细胞)的压电鼻内输送方面的用途可具有巨大的益处,以解决许多患者的未满足的医疗需求。
在一些示例中,所述施用装置和相关系统还可配置为用于治疗心血管系统。例如,心脏病发作的主要因素是斑块在动脉内皮壁上的积聚,这导致血流阻塞和最终的心力衰竭。预防心脏病发作的一种常用疗法包括放置支架。但是,使用支架可能导致再狭窄或进一步损伤动脉壁的其他状况。本公开的施用装置和相关系统可通过利用受干扰的跨上皮电位和可通过电场途径迁移到受伤部位的带静电的干细胞来解决这一问题,并在恢复上皮功能和动脉完整性方面提供治疗潜力。
具体的配置、材料的选择以及各种元件的尺寸和形状可根据要求使用根据所公开的技术的原理构造的系统或方法的特定设计规范或约束条件而变化。所公开的技术的范围意图涵盖这种变化。因此,当前公开的实施例在所有方面都被认为是示例性的而非限制性的。因此,从前述内容显而易见的是,虽然示出并说明了本公开的一些特定形式,但是在不脱离本公开的精神和范围的情况下,可做出各种修改,并且本公开意图涵盖落入其等同内容的含义和范围内的所有变化。
本文用于企业家、创业者技术爱好者查询,结果仅供参考。