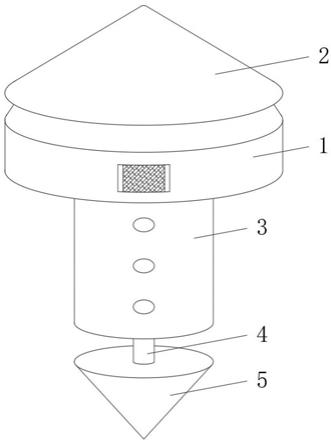
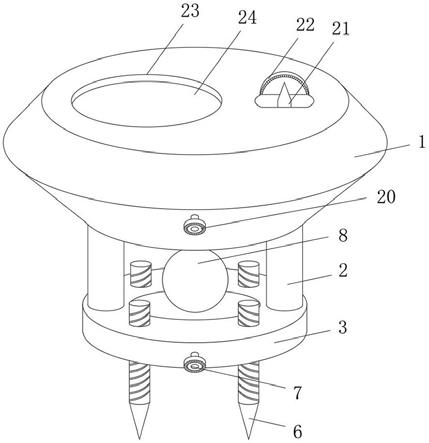
用于分子电子学的导电合成肽
1.受让人:roswell biotechnologies,inc.
2.发明人:barry merriman,tim geiser,venkatesh alagarswamy govindaraj
3.相关申请的交叉引证
4.本技术要求2019年1月10日提交的名称为“用于分子电子学的导电合成肽”的美国临时专利申请序列号no.62/790,828的优先权和权益,出于所有目的,其公开内容整体并入本文。
技术领域
5.本公开一般地涉及合成肽,并且特别地涉及具有α螺旋排列的传导性合成肽,其可以在分子电子学中用作分子导线。
背景技术:
6.分子电子学的广阔领域是由aviram和ratner在1970年代引入的。他们的理念是通过使用单分子作为电路组件来实现电路缩小的终极目标。图1说明了分子连接在纳米级电极之间的一般理念,以及将分子与电极(小阴影方块)结合的一些共轭基团或机制。在一些实施方式中,随时间变化的电流i可以通过该分子,如电流与时间的插图所示。在各个实施方式中,分子元件可以调节该电流,例如在逻辑处理电路或感测电路中。
7.诸如此类的分子电路元件可以提供多种功能,例如电线、电阻器、开关、整流器、致动器或传感器,具体取决于分子和操作条件。这里有趣的是此类结构作为传感器的应用,其中,分子与电路中分子的相互作用为单分子传感提供了基础。作为电路元件令人感兴趣的是各种形式的分子导线,它们可用于在分子电路中的两点之间提供导电连接,如图1所示。
8.对于本领域技术人员而言,术语分子导线宽松地指具有规则或重复结构的分子,其具有相对长、细的结构,并且是导电或半导电的。已被充分研究的此类分子导线的例子包括碳纳米管、石墨烯带、α螺旋蛋白、双链dna螺旋以及由芳族环形成的各种合成有机聚合物,诸如众所周知的例子聚噻吩(由噻吩环结构单元形成的聚合物)和pedot(聚(3,4
‑
亚乙基二氧噻吩))分子。
9.尽管之前对分子导线进行了研究,但仍需要新分子用于电子分子电路,并且特别是可以通过已建立的合成化学方法生产的具有精确分子结构的分子。
技术实现要素:
10.在本公开的各种实施方式中,描述了可在分子电子电路中用作分子导线的导电性合成肽。本文的合成肽可以通过自下而上的合成化学生产,以便合成肽可以(a)包含精确的分子结构,例如减少分子电子电路性能的可变性,(b)根据需要包含位于分子上精确位置的特定附接基团,和(c)可以以高纯度和低成本高效地大批量生产。
11.在各个实施方式中,一种合成肽,包含式:[x1x2]
m
x3[x4]
n
x3[x2x1]
m
,其中,每个x1独立地包含含有约5至约15个氨基酸的材料结合肽、蛋白酶切割序列或肽捕获标签;每个x2独
立地包含富含甘氨酸/丝氨酸{g,s}的接头或c1
‑
c20碳链分子接头;每个x3独立地包含共价键、单个氨基酸、过渡性螺旋
‑
促进基序、金属结合基团或含有约5至约15个氨基酸的材料结合肽;每个x4独立地包含含有约4至约40个氨基酸的α螺旋基序;每个m独立为0至4;且每个n为1至40。
[0012]
在各个实施方式中,x4的至少一个实例包含缀合位点。在各个方面,缀合位点可以包含半胱氨酸、赖氨酸、酪氨酸、生物素、叠氮化物或点击化学基团,以便该合成肽可以与生物分子(例如结合探针)缀合。在各个实施方式中,结合探针可以包含聚合酶或抗体。
[0013]
在各个实施方式中,x1的至少一个实例可以包含与seq id no:6、7、8、9、10、11、16、18或29中任一个具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的氨基酸序列。
[0014]
在各个实施方式中,x2的至少一个实例可以包含甘氨酸、丝氨酸、gs、gsg、seq id no:24、与seq id no:25具有至少80%序列同一性的氨基酸序列、或c1
‑
c20碳链分子接头。
[0015]
在各个实施方式中,对于任何一组[x1x2]
m
x3,如果m≠0,则x3包含共价键、单个氨基酸或过渡性螺旋
‑
促进基序。另外,在任何一组[x1x2]
m
x3中,如果m=0,则x3包含金属结合基团或含有约5至约15个氨基酸的材料结合肽。在各个方面,由子结构[x1x2]
m
x3表示的合成肽的末端被定制用于特定用途,诸如结合金属或缀合至生物分子。在各个实施方式中,m的两个实例都不能为零,在这种情况下,合成肽的一个末端保留了[x1x2]
m
子结构。
[0016]
在各个实施方式中,一种金属结合基团,可以包含c、cc、ccc、seq id no:32、seq id no:33、seq id no:5、seq id no:35或序列ccxxcc的flash结合基序,其中,x为任何氨基酸。
[0017]
在各个实施方式中,x4的至少一个实例可以包含与seq id no:1、2、3、4、13、17、20、22、23、26、27、28或31中任一个具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的氨基酸序列。
[0018]
在各个实施方式中,根据本公开的合成肽具有与seq id no:14有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的氨基酸。
[0019]
在各个实施方式中,根据本公开的合成肽具有与seq id no:15有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的氨基酸序列。
[0020]
在各个实施方式中,根据本公开的合成肽具有与seq id no:19有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的氨基酸序列。
[0021]
在各个实施方式中,根据本公开的合成肽具有与seq id no:21有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的氨基酸序列。
[0022]
在各个实施方式中,公开了一种分子电子电路。分子电子电路包括:第一电极;第二电极,通过纳米间隙与第一电极间隔开;包括根据通式[x1x2]
m
x3[x4]
n
x3[x2x1]
m
的合成肽的桥接分子导线,电连接至第一电极和第二电极以桥接纳米间隙;以及缀合至缀合位点的聚合酶,其中,电路包括通过合成肽的导电通路。
[0023]
在各个实施方式中,公开了一种分子传感器。该传感器包括一种分子电子电路,该分子电子电路包括:第一电极;第二电极,通过纳米间隙与第一电极间隔开;包含根据式[x1x2]
m
x3[x4]
n
x3[x2x1]
m
的合成肽的桥接分子导线,电连接至第一电极和第二电极以桥接纳米间隙;以及缀合至缀合位点的聚合酶,其中,电路包括通过合成肽的导电通路;以及电连
接至第一电极和第二电极中至少一者的跨阻放大器,该跨阻放大器提供包含可测量电参数的输出。
[0024]
在各个实施方式中,一种cmos芯片装置包括这些传感器的阵列。
[0025]
在各个实施方式中,公开了一种对dna分子进行测序的方法。该方法包括:提供包含分子电子电路的传感器,该分子电子电路包括第一电极;通过纳米间隙与第一电极间隔开的第二电极;包含根据式[x1x2]
m
x3[x4]
n
x3[x2x1]
m
的合成肽的桥接分子导线,电连接至第一和第二电极以桥接纳米间隙;和缀合至缀合位点的聚合酶;其中,电路包括通过合成肽的导电通路;和电连接至第一电极和第二电极中至少一者的跨阻放大器,该跨阻放大器提供包含可测量电参数的输出;启动通过电路的电压或电流中的至少一者;使电路暴露于含有引物引发的(primed)单链dna和/或dntp的溶液中;以及测量当聚合酶接合并延伸模板时通过电路的电信号,其中,处理电信号以识别提供有关由聚合酶处理的dna分子的潜在序列信息的特征。
[0026]
在各个实施方式中,一种分子电子电路,包括:通过纳米间隙间隔开的第一电极和第二电极;根据式[x1x2]
m
x3[x4]
n
x3[x2x1]
m
的第一合成肽,电连接在第一电极和聚合酶的第一位点之间;根据式[x1x2]
m
x3[x4]
n
x3[x2x1]
m
的第二合成肽,电连接在第二电极和聚合酶的第二位点之间,其中,电路包括通过聚合酶的一部分的导电通路。
[0027]
在各个实施方式中,一种分子传感器,包括:分子电子电路,该分子电子电路包括:通过纳米间隙间隔开的第一电极和第二电极;根据式[x1x2]
m
x3[x4]
n
x3[x2x1]
m
的第一合成肽,连接在第一电极与聚合酶的第一位点之间;根据式[x1x2]
m
x3[x4]
n
x3[x2x1]
m
的第二合成肽,电连接在第二电极与聚合酶的第二位点之间,其中,电路包括通过聚合酶的一部分的导电通路;以及电连接至第一电极和第二电极中至少一者的跨阻放大器,该跨阻放大器提供包含可测量电参数的输出。
[0028]
在各个实施方式中,一种cmos芯片装置,包括这些传感器的阵列。
[0029]
在各个实施方式中,一种对dna分子进行测序的方法,包括:提供包含分子电子电路的传感器,该分子电子电路包括:通过纳米间隙间隔开的第一电极和第二电极;根据式[x1x2]mx3[x4]nx3[x2x1]m的第一合成肽,电连接在第一电极与聚合酶的第一位点之间;根据式[x1x2]
m
x3[x4]
n
x3[x2x1]
m
的第二合成肽,电连接在第二电极和聚合酶的第二位点之间,其中,电路包括通过聚合酶的一部分的导电通路;以及电连接至第一电极和第二电极中至少一者的跨阻放大器,该跨阻放大器提供包含可测量电参数的输出;启动通过电路的电压或电流中的至少一者;使电路暴露于含有引物引发的单链dna和/或dntp的溶液;以及测量当聚合酶接合并延伸模板时通过电路的电信号,其中,处理电信号以识别提供有关由聚合酶处理的dna分子的潜在序列信息的特征。
附图说明
[0030]
本公开的主题在说明书的结论部分被特别指出和明确要求保护。然而,当结合附图考虑时,通过参考详细描述和权利要求可以最佳地获得对本公开的更完整的理解:
[0031]
图1示出了分子电子电路的一般概念,导电分子完成纳米电极之间的电路;
[0032]
图2示出了根据各个实施方式,将结合探针分子接合到电子电路中分子导线上以充当能够检测结合探针与其靶之间的结合事件的传感器的一般概念;
[0033]
图3示出了根据各个实施方式的结合探针,其包含使用两个分子导线元件或臂分子直接连线至电流路径的分子导线;
[0034]
图4示出了根据各个实施方式,使用经由连接至探针内的内部蛋白质α
‑
螺旋结构的分子导线制成的连接,直接连线至电流路径的结合探针;
[0035]
图5示出了根据各个实施方式,使用经由连接至探针内的内部蛋白质β
‑
片层结构的分子导线制成的连接,直接连线至电流路径的结合探针;
[0036]
图6示出了根据各个实施方式直接连线至电流路径的结合探针,其使用制成的额外分子导线连接来稳定或定向探针,或增加与探针的连接的导电性;
[0037]
图7示出了根据各个实施方式直接连线至电路中的结合探针的示意图,其使用两个分子导线连接器,还与分子导线具有一点缀合,并且利用了一对电极以测量组合传导;
[0038]
图8示出了根据各个实施方式直接连线至电路中的结合探针的示意图,其使用两个分子导线连接器,还与分子导线具有一点缀合,并且利用两对电极独立地测量这两种传导模式;
[0039]
图9示出了根据各个实施方式直接连线至电路的电流路径的示意图,其中,结合探针是igg抗体,显示具有一个fab结构域与其抗原结合靶标结合,其中,将特异性内部β
‑
片层用于接触,并且分子导线臂提供与电极的导电连接;
[0040]
图10示出了根据各个实施方式的核酸杂交结合探针分子的示意图,核酸杂交结合探针分子单链rna或dna或其他xna核酸类似物寡聚体组成,使用两个分子导线直接连线至电路的电流路径,其中,位于单链末端处或附近的位点缀合至分子导电连接器,以提供与电极的导电连接;
[0041]
图11示出了大肠杆菌pol i klenow片段聚合酶的蛋白质结构视图,图示了存在的α
‑
螺旋、β
‑
片层和连接环结构;
[0042]
图12示出了根据各个实施方式,缀合至电子电路中的分子导线充当能够检测酶活性的传感器的聚合酶分子的示意图;
[0043]
图13示出了根据各个实施方式,直接连线到电路的电流路径中充当能够检测酶活性的传感器的聚合酶的示意图,其中,将特异性内部α
‑
螺旋用于接触点,并且分子导线臂提供了从这些接触点到电极的导电连接;
[0044]
图14示出了使用两个分子导线连接器直接连线至电路的电流路径的聚合酶的示意图,并且其中,连线了额外的分子导线臂以提供稳定和固定的空间取向以及与电极或基板的额外导电连接;
[0045]
图15a
‑
e示出了seq id no:4的各种表示:图15a带状图,图15b序列骨架的球棒模型,图15c空间填充模型,图15d完整分子的球棒模型,和图15e空间填充模型。
[0046]
图16a
‑
c示出了seq id no:4的分子效果图,虚线代表螺旋中的氢键和氨基酸侧链之间的盐桥;
[0047]
图17a
‑
c示出了基于重复eeeerrrr(seq id no:2)(e4r4)α
‑
螺旋基序的肽α螺旋的分子效果图,虚线代表螺旋中的氢键和氨基酸侧链之间的盐桥;
[0048]
图18示出了基于重复eayar(seq id no:3)α螺旋基序的肽α
‑
螺旋的分子效果图,虚线代表螺旋中的氢键和氨基酸侧链之间的盐桥;
[0049]
图19示出了来自该细菌的特定主要菌毛蛋白链(iva型)的晶体结构(蛋白质数据
库条目pdb id 2m7g_a)。用带状图和显示所有侧链的叠加球棒模型可视化的x射线晶体结构显示,菌毛蛋白具有α螺旋结构,13圈长,并且可见3个芳香环侧链;
[0050]
图20示出了分别基于eaaar(seq id no:1)和eeeerrrr(seq id no:2)重复α螺旋基序的15nm长的合成肽seq id no:15和seq id no:19观察到的电流分布,显示合成肽seq id no:15具有更高的电导率;和
[0051]
图21示出了实验的电流与时间轨迹,其中,使具有seq id no:21且基于eaaar(seq id no:1)重复α螺旋基序的25nm合成肽在中央半胱氨酸处与dna寡核苷酸缀合,并且用于感测与引物引发的模板结合的聚合酶以及结合到聚合酶袋中的核甘酸。
具体实施方式
[0052]
在本公开的各个实施方式中,描述了一种合成肽。在各个实施方式中,本文的合成肽表现出导电性并且可用于分子电子学,诸如单分子电子分子传感器,以及用于集成到cmos半导体芯片装置中的电路中。
[0053]
在各个实施方式中,合成肽包含整体α螺旋构象,或包含至少一个内部α螺旋段。在各个实施方式中,合成肽具有设计用于向肽提供整体α螺旋构象的氨基酸序列,或具有设计用于提供至少一个内部α螺旋段的氨基酸序列。在各个实施方式中,本文的合成肽包含重复螺旋段或“螺旋基序”。
[0054]
在各个实施方式中,本文的合成肽包含线性一级结构并由此包含序列的两个相反端部,可以称为末端,第一末端位于或靠近肽的n
‑
末端且第二末端位于或靠近肽的c
‑
末端。任一个或两个末端可用于位点特异性缀合,诸如附接至金属电极或附接至外部化学基团。
[0055]
在各个实施方式中,本文的合成肽还包含在末端之间并且沿肽氨基酸序列的内部位点,其可以用于将另一分子以位点特异性选择方式缀合至合成肽。内部位点可以包含单个半胱氨酸(缩写为c或cys)、或赖氨酸(k或lys)、或酪氨酸(y或tyr)、或具有用于缀合的化学修饰的氨基酸,诸如添加硫醇、生物素、叠氮化物、或点击化学基团。
[0056]
定义
[0057]
如本文所用,术语“肽”是指任何连续单链的氨基酸,其中,氨基酸是以肽键接合的标准的、非标准的或修饰的或氨基酸类似物。在各个实施方式中,本文的肽可以为10至300个氨基酸长度,或20至200个氨基酸长度。
[0058]
如本文所用,术语“基序”是根据本公开的合成肽内的特征。在各个例子中,基序可以是α螺旋基序,意指具有α螺旋二级结构的肽内的氨基酸片段。在其他例子中,基序可以是具有另一种功能目的的肽内的一个或多个氨基酸,诸如包含可用于将合成肽锚定至金属的材料结合肽的基序。在其他方面,基序可以包含化学成分,诸如有机化学的官能团(例如胺、硫醇等),或者基序可以包含化学接头(例如一或两个氨基酸,一串三个氨基酸,(聚)乙氧基化物系链,1,4
‑
亚苯基连接等)。
[0059]
如本文所用,术语“α螺旋”是指肽的螺旋二次结构,如在x射线晶体学领域中描述蛋白质结构元素的背景中所用的。在本文中,合在肽的区段可以具有α螺旋次级结构,并且该区段可以替代地称为“螺旋段”或“螺旋基序”。本文中的合成肽可以包含一个或多个螺旋基序,诸如重复α螺旋基序。在一些情况下,当忽略肽两端的结合肽时,可以使用术语“α螺旋”来代替基本上为α螺旋二次构象的肽的术语“合成肽”。在各个例子中,“α螺旋”可以是指
可在分子电子电路中用作导电桥联分子的合成肽。
[0060]
如本文所用,术语“分子”是指原子的共价键合组装,或类似明确定义且稳定结合的原子装配。
[0061]
如本文所用,术语“分子电子学”是指掺入单个分子或涉及少数分子的小分子复合物作为电路中的元件的电路。此类小复合物可以仅涉及两个或三个分子,并且在各个实施方式中,少于10或少于30。分子电子学传感器是分子电子学的一个例子。
[0062]
如本文所用,术语“分子导线”是指相对长且薄的分子或少数分子的装配,当结合到电路中时,其可以导电,例如通过跨越一对电极或接触点以进行电荷转移。此种装配可以是导体或半导体,并且可具有线性或非线性电流
‑
电压特性。它们还可以展示带隙,该带隙抑制低于阈值电压的传导。分子导线的长度可以为约数纳米至约数微米。能够具有导电性的本文的合成肽可以在分子电子电路中作为分子导线独自发挥功能。或者根据本公开的合成肽可以组装成包含更大结构的分子导线,诸如例如包含如在纱线中的长丝一样布置的肽束。在合成肽可以直接用于分子电子电路中的情况下,术语“合成肽”和“分子导线”可以互换使用。
[0063]
如本文所用,术语“合成肽”是指制造而不是自然发生的肽,即已经过人工方式设计、改造和/或生产的肽。因此,“合成的”不应狭义地解释为指完全通过基于有机化学方法的线性或收敛化学合成组装的肽。本文的合成肽也可以通过蛋白质表达和基因工程制成。也就是说,可以在蛋白质表达系统中制备合成肽,表达插入到此类系统中的合成dna基因。另外,可以通过有机合成将通过蛋白质表达基因工程生产的合成肽进一步功能化,诸如添加官能团、去除保护基等。尽管是制造的,本文的合成肽可能受到天然存在的肽的启发,并且可以包含天然存在的氨基酸序列。
[0064]
如本文所用,术语“末端”或复数“末端”是指根据本公开的合成肽的氨基酸序列的端部,并且允许区分合成肽的α螺旋和导电芯以及提供其他功能的末端区域(诸如用于结合电极或用于标签的缀合)。序列的“端部”不应被解释为序列的实际物理端(一个原子或一个氨基酸),而应更广泛地解释为合成肽的末端区域,其在空间上可以比仅一个氨基酸更长。换言之,合成肽的末端,无论是n
‑
还是c
‑
端,可以包含单个氨基酸、氨基酸序列、接头和官能团的各种组合、接头和氨基酸短序列的各种组合等。在各个实施方式中,合成肽的末端可以包含序列末尾的半胱氨酸,以使硫醇(
‑
sh)官能团可与金属缀合。在其他例子中,合成肽的末端可以包含已经功能化以包括未天然附属物(如叠氮基团)的单个氨基酸。在其他例子中,序列的末端可以包含材料结合肽,或对特定金属(例如金或钯)具有特异性的材料结合肽的双、三或四重复。在其他例子中,合成肽的末端可以包含金属结合基团,诸如与包含一个、两个或三个氨基酸的中间接头串在一起的硫化物
‑
s
‑
原子。
[0065]
如本文所用,在两个或更多个肽序列的背景下的术语“序列同一性”和“序列同一性百分比”是指当将两个或更多个序列或子序列比较和对比以获得最大对应性时,如使用用于此类氨基酸序列对较的序列比较算法之一(例如blastp或本领域普通技术人员可用的其他算法)或通过目视检查进行测量的,两个或多个序列或子序列具有的相同氨基酸残基的特定百分比。取决于应用,序列同一性百分比可以存在于被比较序列的区域上,例如存在于α螺旋区段,或者存在于要比较的两个序列的全长上。对于序列比较,通常一个序列作为参考序列,测试序列与其进行比较。当使用序列比较算法时,将测试序列和参考序列输入计
算机,必要时指定子序列坐标,并指定序列算法程序参数。然后,序列比较算法基于指定的程序参数计算测试序列相对于参考序列的序列同一性百分比。
[0066]
如本文所用,术语“聚合物”是指作为化学构件单元的链的分子,化学构件单元取自确定有限的构件单元分子集并通过共价键彼此连接。
[0067]
如本文所用,术语“芳香环”具有有机化学中sp2杂化碳原子环的常见含义,具有或不具有中间杂原子,中间杂原子具有一对电子,其中,环中每个原子的轨道中的电子是离域的。术语芳香族分子或芳香族氨基酸是指分子结构中包含芳香环的实体。
[0068]
本文使用的惯例是所有氨基酸或蛋白质序列从n
‑
末端到c
‑
末端书写。
[0069]
如本文所用,术语“结合探针”是指优先结合特定靶分子或靶分子家族的分子或分子复合物。抗体或抗体片段是结合探针的一个例子。酶,例如聚合酶,也是结合探针的一个例子。在本文的各个实施方式中,结合探针可以附接至合成肽,用作分子电子电路中电极之间的桥接分子导线。
[0070]
如本文所用,术语“酶”是指催化化学反应的分子或分子复合物,通常包含一个或多个蛋白质。术语聚合酶是指将dna或rna互补物合成到dna或rna单链模板的酶。在各个实施方式中,酶用作分子电子电路中的结合探针。
[0071]
如本文所用,术语“盐桥”是指肽中存在的带正电和带负电的氨基酸残基之间形成的弱键合现象,氨基酸残基在空间邻近,使得可以形成这样的键。
[0072]
如本文所用,术语“桥”或“桥分子”或桥接是指可用于在电极之间形成导电桥的分子,其适用于本文讨论的所有在末端具有合适连接基团的合成肽。相关术语“臂”或“臂分子”是指与跨越电极之间形成对比,以跨越电极和生物分子或探针分子的方式使用合成肽,并且也适用于本文讨论的所有在末端具有合适连接基团的合成肽。
[0073]
如本文所用,术语“电极”是指电路中的电接触点之一,其用于通过完整的电路传导电子。这种电极通常由金属或掺杂半导体制成,具有相对高的导电性,并且还可以对其表面进行衍生化以促进适当的电气和机械连接,例如使用分子导线。
[0074]
具有用于促进在分子电子电路中用作导电分子导线的结构基序的合成肽
[0075]
在各个实施方式中,本文的合成肽包含特定的结构基序,用于通过肽结构增强导电性并提供各种缀合位点,例如在肽的一个或两个末端以及末端之间。
[0076]
在各个实施方式中,根据本公开的合成肽可以通过以下一般结构表示:[x1x2]
m
x3[x4]
n
x3[x2x1]
m
,其中,[x4]
n
表示重复n次的重复α螺旋基序x4,并且其中,在序列两端的组合[x1x2]
m
x3表示合成肽的末端。一般结构具有两个重要方面。第一,一般结构中的基序x1、x2、x3和x4并不单个氨基酸,而是可以是氨基酸序列。作为一个例子,x4可以为eaaar(seq id no:1),这不是单个氨基酸。第二,重要的是需要理解,重复子结构中的基序的每个实例,诸如在一般结构中括号内出现的x1、x2和x4是独立选择的。例如,在子结构[x4]
n
中,当n=3时,即[x4]3,可以表示为x4’
x
4”x4”’
,x4’
、x
4”和x4”’
可以是不同的基序,例如不同的氨基酸序列。在各个实施方式中,x4的至少一个实例包含缀合位点。另外,肽任一端的两个x3基序各自不必相同,合成肽的每个末端[x1x2]
m
x3也不必相同。换言之,以上一般结构可能意味着通过符合式的合成肽的中点存在某种对称性,但是由该一般结构涵盖的任何物种不同具有此种对称性。例如,由[x1x2]
m
x3表示的n末端可以被设计成与金结合,而其他末端,如由[x1x2]
m
x3表示的c末端,可以被设计成与钯结合,使得合成肽物种可以桥接在不同金属的电极之间。在各
个实施方式中,m的一个实例可以为0,而m的其他实例可以为1、2或3。即在各个实施方式中,对于合成肽的两个末端部,m均不为0。在各个例子中,一个末端[x1x2]
m
x3可以包括标签序列。在各个实施方式中,m的一个实例为0,而m的其他实例不为0,使得合成肽端部的一个末端为x3,例如,其可以被设计用于点击化学缀合至生物分子,而在其他末端为子结构[x1x2]
m
,其中,m=1、2或3,可以设计为结合金属。
[0077]
最后,作为一般规则,上面的一般结构不应暗示结构中基序的相对长度,即合成肽的区段。换言之,如所写出的一般结构可能表明[x4]
n
表示的内螺旋核部分的长度比[x1x2]
m
x3表示的两个末端的组合短,但情况并非一定如此。例如,n可以为21并且x4可以为5个氨基酸的肽,由此[x4]
n
的长度为105个氨基酸,而[x1x2]
m
x3的整体可以只是半胱氨酸(c),即当m为0且x3为半胱氨酸时。
[0078]
基序x1、x2、x3和x4的性质和其拉风以及重复单位m和n的范围的定义如下。
[0079]
在各个实施方式中,并入特定的结构基序,特别是螺旋基序,将α螺旋结构提升到合成肽的至少一部分。取决于这些α螺旋段内的氨基酸序列,通过合成肽促进了导电性。这些基序例如可以包含:
[0080]
(1)在肽链的i和i 5位或在肽链的i和i 4位具有相反电荷侧链的氨基酸,其可以的α螺旋构象中的残基之间形成盐桥;
[0081]
(2)具有芳香环残基的氨基酸;
[0082]
(3)在i和i 4或i和i 5位具有芳香环残基的氨基酸,使得这些环在α螺旋构象中可以在空间上相邻;
[0083]
(4)烃链订书钉,以稳定α
‑
螺旋结构,其中,此类订书钉可以在链中的i与i 4或i 5残基之间,以将相邻的位点钉在α
‑
螺旋构象中;或
[0084]
(5)模仿或受生物导电蛋白启发的氨基酸序列基序,其本质上具有电荷转移的生物学功能。
[0085]
为了一般性说明α螺旋肽概念,图15显示了α
‑
螺旋肽的五种不同图形表示。本示例中的肽由40个氨基酸组成,一级氨基酸序列(使用标准aug氨基酸代码单字母名称书写)由8个重复的基序eaaar(seq id no:1)组成(e=谷氨酸,a=丙氨酸,r=精氨酸),或用紧凑的符号表示为8x(eaaar)(seq id no:4),或以从n末端到c末端的标准方向明确地写为eaaareaaareaaareaaareaaareaaareaaareaaar(seq id no:4)。
[0086]
图15a
‑
e示出了seq id no:4的各种表示。图15a是肽的α螺旋结构的蛋白质带状图,图15b是蛋白质肽键骨架的球棒模型,图15c是蛋白质肽键骨架的空间填充模型,图15d是包括氨基酸侧链的完整分子结构的球棒模型,和图15e是包括氨基酸侧链的完整分子结构的空间填充模型。
[0087]
α螺旋的一般结构由每螺旋转3.6个氨基酸组成,每个螺旋转的长度为0.54nm,且螺旋核直径为1.2nm。因此,图15a
‑
e示出的seq id no:4的示例肽的长度为40个氨基酸或11.1个螺旋转,或6.0nm。
[0088]
在各个实施方式中,根据本公开的合成肽包含与seq id no:4具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的序列。在各个实施方式中,合成肽包含seq id no:4。在各个实施方式中,此类合成肽用作分子电子电路的导电分子导线。在各个实施方式中,这种α螺旋结构可以是较大合成肽的中央芯。
[0089]
在本公开的各个实施方式中,α螺旋肽可以被设计成具有在3nm至100nm范围内的精确长度,或在一些实施方式中,5nm至50nm,或在其他实施方式中,7nm至30nm、10nm至25nm或10nm至15nm。
[0090]
合成肽可以通过既定的肽合成方法制得,例如合成有机化学和生物化学领域的技术人员已知的那些。这些方法可包括但不限于肽键合氨基酸的固相合成或溶液相合成,并可进一步包括使用此类合成片段的化学连接以有效地产生更长的肽。所使用的氨基酸构建块可以包含生物学中出现的标准22种蛋白质氨基酸,以及使用非蛋白氨基酸,包括所谓的非标准氨基酸(nsaa)或非天然氨基酸(uaa),诸如众所周知的苯丙氨酸(f)化学修饰形式的例子,命名为pacf(对乙酰基
‑
f)、pazf(对叠氮基
‑
f)和pbpf(对苯甲酰基
‑
dl
‑
f)。
[0091]
根据本公开的合成肽也可以通过代表肽序列的合成基因的表达来制得。此种蛋白质表达方法是公知的,并且通常涉及将合成dna片段(“基因”)克隆到细菌或其他表达载体中,表达并纯化出产生的目的蛋白。对于此类表达系统,在各个实施方式中,可以在目的靶肽的一个末端(c或n末端)添加捕获标签肽(诸如his标签或flag标签或本领域已知的其他标签),并且这种标签在捕获后可以被去除或不被除去。如果这样的小标签或相关肽残留物留在原地,它通常不会影响本文的合成肽的效用。
[0092]
在表达的情况下,如果使用为此目的而制造的表达系统,也可以将nsaa添加到肽中,例如在所谓的“扩展遗传密码”的情况中。此类表达系统依赖于使用具有经修饰的遗传密码的细菌载体、带有所需nsaa的定制转移rna的共表达,对于扩展遗传密码领域的技术人员来说这是众所周知的,例如,生物学家peter g.schultz和george m.church开创了用于表达具有nsaa的蛋白质的此类系统。迄今为止,已经使用基于大肠杆菌的此类系统来表达包括超过70种不同nsaa的蛋白质。
[0093]
位于或靠近肽末端的结合基团,可以位于或靠近α
‑
螺旋区段的末端,可用于将肽缀合到分子电路中,可以包含氨基酸半胱氨酸(c),该半胱氨酸(c)可用于基于硫醇的缀合,诸如与金属电极表面的硫醇
‑
金属结合,或者也可用于与作为缀合化学的马来酰亚胺的半胱氨酸
‑
马来酰亚胺选择性结合,或用于半胱氨酸
‑
半胱氨酸或半胱氨酸
‑
硫硫化物桥
‑
基缀合。结合基团还可以包含富含半胱氨酸的基序,cc、ccc、cccc(seq id no:32)、ccccc(seq id no:33)或“flash”四
‑
c基序ccxxcc(x=任何氨基酸),诸如cccgcc(seq id no:5)或ccpgcc(seq id no:35)。位于或靠近螺旋区段末端的缀合基团还可以包括具有能够与同源
‑
衍生表面结合的基团(诸如叠氮基团或胺基团)或能够参与点击化学结合的基团的氨基酸。位于或靠近螺旋区段末端的缀合基团还可包含材料结合肽。材料结合肽是长度通常在5到15个氨基酸范围内的肽,具有能够与特定材料结合的氨基酸序列。许多这样的材料结合肽是生物缀合领域的技术人员已知的。一个例子,已知选择性地结合金的布朗金结合肽具有氨基酸序列mhgktqatsgtiqs(seq id no:6)。参见例如s.brown,“metal
‑
recognition by repeating polypeptides,”nature biotechnology,15,269
‑
272,1997。其他已知的金属结合肽包括但不限于wagakrlvlrre(seq id no:7)、vsgsspds(seq id no:8)、tgtsvliatpyv(seq id no:9)、lkahlppsrlps(seq id no:10)和qqswpis(seq id no:16)。最后一个例子是钯结合肽。
[0094]
此外,结合基团可以包含排列为由短间隔肽隔开的一系列串联重复的这种结合肽。例如,可以存在由肽接头
‑
gsg
‑
隔开的三个拷贝的金结合肽,诸如氨基酸序列
mhgktqatsgtiqs
‑
gsg
‑
mhgktqatsgtiqs
‑
gsg
‑
mhgktqatsgtiqs(seq id no:11)。此基团可以包括在肽分子导线的任一末端,并且可以包括附加的短肽接头,诸如
‑
gsg
‑
或由g和s组成的其他短肽,或其他常见的柔性水溶性肽接头序列,以将其与一级α
‑
螺旋区段偏移,以免破坏螺旋构象。在各个实施方式中,在结合基团中可以有2至5此类重复。
[0095]
在各个实施方式中,根据本公开的合成肽包含与seq id no:11具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的序列。在各个实施方式中,合成肽包含seq id no:11。在各个实施方式中,此类合成肽用作分子电子电路的导电分子导线。在各个实施方式中,这一序列可以是较大合成肽的一个或两个末端的一部分。
[0096]
在各个实施方式中,肽中的内部结合位点,诸如靠近沿氨基酸序列的中心位置,可以在特定位点包含半胱氨酸氨基酸以提供基于半胱氨酸的缀合,诸如半胱氨酸
‑
马来酰亚胺缀合。内部结合位点也可以在肽中的特定位置包含具有诸如叠氮基或胺基等残基的标准、非标准或经修饰的氨基酸,其可以经进特定的缀合反应。例如,包含叠氮官能团的氨基酸可以用于点击化学缀合反应。在各个实施方式中,内部结合位点可以被包括在α螺旋基序中,诸如在包含α螺旋核区段的合成肽中还包含重复的α螺旋基序,其中,一个或多个α螺旋重复包括半胱氨酸。
[0097]
能够在肽中发挥内部结合位点作用的一个或多个分离的氨基酸通常不会破坏肽的α螺旋结构,即使它们偏离了定义螺旋结构的精确重复基序,或者即使放置在两个此类串联基序重复之间,也是如此。在一些实施方式中,内部结合位点在肽链中的位置以及肽的端基将被隔开,以使在螺旋构象中,肽可以结合在电路中的适当位置并与辅助分子缀合,而不会扭曲螺旋几何,同时允许辅助分子相对于电路的电极和基板按需要定向。例如,当以最小能量构型结合至电极并且螺旋区段处于其标准最小能量构象时,肽端基团可以导致内部结合基团远离电路下层基板定向,在溶液中最大地可用于其他辅助分子结合。
[0098]
图16、17和18中的示例说明了使用盐桥来稳定螺旋结构并提供传导路径。盐桥是在沿3
‑
dα螺旋结构空间上相邻的氨基酸之间形成的。这些通常在氨基酸序列中的i和i 4或i 5位。这些示例说明了原理,但不限制本公开的范围,本公开的范围包括可以实现类似效果的其他氨基酸序列。一般来说,盐桥可以发生在带正电和带负电的氨基酸残基之间,例如标准氨基酸r、h、k(带正电)和e、d(带负电)。在各个实施方式中,也可以使用带电的nsaa。
[0099]
图16a
‑
c示出了seq id no:4的分子效果图,其基于重复的eaaar(seq id no:1)螺旋肽基序,效果图中的虚线1610代表螺旋中的氢键,且虚线1620代表e和r氨基酸侧链之间的盐桥(为清楚起见,未显示其他侧链)。当将分子导线连接在分子电路中时,分子内氢键和盐桥为穿越包含基序eaaar(seq id no:1)重复的分子导线的电子提供了有利的传导路径。盐桥显示为i和i 4氨基酸e和r的相互作用侧链,进一步有助于稳定螺旋结构。
[0100]
图17a
‑
c示出了包含eeeerrrr(seq id no:2)(e4r4)螺旋肽基序的重复的合成肽的分子效果图,效果图中的虚线1710表示螺旋中的氢键且效果图中的虚线1720表示e和r氨基酸侧链之间的盐桥(为清楚起见,未示出其他侧链)。
[0101]
在各个实施方式中,通过在合成肽中并入包含芳香环的氨基酸来实现提高的导电性。芳香环富含电子,为通过蛋白质的电子传导提供支持。通过将此类芳香环侧链并入到合成肽的α螺旋区段中,可以进一步增强通过肽的传导。
[0102]
图18示出了一种合成肽,其基于基序eayar(seq id no:3)的重复,虚线1810表示
氢键,并且其中,示出了侧链e、r和芳香族y(1830)。e和r侧链提供盐桥1820,并且y基团(酪氨酸)1830提供芳香环以增强导电性。天然存在的带有芳香环的氨基酸是f、w、y、p(苯丙氨酸、色氨酸、酪氨酸、脯氨酸),并且这些以及非非磺化芳香胺(nsaa)可以用于此效果。在各个实施方式中,芳香族氨基酸在肽链中以i和i 4和/或i和i 5间隔开,使得芳香环在螺旋结构中在空间上彼此靠近,为从环到环的电子跳跃提供连续的传导路径。
[0103]
在各个实施方式中,通过包含与生物导电螺旋蛋白的肽区段高度相似的合成肽区段来实现增强的导电性,生物导电螺旋蛋白诸如已知在各种生物过程中进行电子转移或电荷转移的蛋白质、或作为执行此类传导功能的复合物的一部分的蛋白质。
[0104]
这种生物蛋白质家族的一个例子是细菌pilin(菌毛蛋白),诸如例如硫还原地杆菌(一种革兰氏阴性金属还原菌)pili蛋白。该属于1987年被发现,并因其金属还原和电子传导特性而被充分研究。参见例如k.xiao,et al,“low energy atomic models suggesting a pilus structure that could account for electrical conductivity of geobacter sulfurreducens pili,”scientific reports,march 22,2016,(doi:10.1038/srep23385)。
[0105]
在生物系统中,单个pilin蛋白链被扭曲成由21条链组成的螺旋超结构“细丝”,它在细菌中的电子传递中起关键作用。
[0106]
xiao,et al.(如上)阐明了生物pilin蛋白和pilin细丝的导电特性的基础。xiao,et al.(如上)的图3示出了硫还原地杆菌菌毛的预测模型结构的结果:(a)包含21个单链螺旋蛋白亚基的完整细丝超结构模型,每个亚基具有不同的阴影;(b)示出了超结构的几何参数;和(c)示出了超结构的端视图。
[0107]
xiao,et al.(如上)的图4显示了芳香环如何通过细丝超结构进行组织,空间相邻的芳香环链通过超结构(a、b、c和d)形成连续的传导路径,并将这一芳香环结构与来自假单胞菌的地杆菌同源模型进行比较(e,f):(a)显示了菌毛模型中的芳香环;(b)显示了相邻芳香环的细节,这些环在细丝的长度上重复。环之间的最近的原子间隔环的中心间隔“p”表示参考原体。“p 3”和“p 4”分别表示沿螺旋组装更远的第3个和第4个原体;(c)含有21个单体的模型的端视图(模型长度);(d)模型细丝的横截面(厚),其中,以不同阴影示出了来自不同单体的残基。phel、phe24和tyr27的芳香环在横截面中不透明且偏离中心;(e)基于假单胞菌的地杆菌同源模型的横截面;(f)模型中没有中央通道(左)相对于同源模型中的中央通道(右)。
[0108]
本文中的图19示出了来自该细菌的特定主要pilin链(iva型)的晶体结构(蛋白质数据库条目pdb id 2m7g_a)。用带状图和显示所有侧链的叠加球棒模型可视化的x射线晶体结构显示,pilin蛋白具有α螺旋结构,13圈长,并且可见3个芳香环侧链。
[0109]
图19所示的这种pilin蛋白的具体氨基酸组成为从pdb条目中提取的61个氨基酸序列:
[0110]
pdb:来自硫还原地杆菌的导电细菌纳米导线的iva型主要pilin的2m7g_a结构:
[0111]
ftliellivv aiigilaaia ipqfsayrvk aynsaassdl mlktalesa faddqtyppe s(seq id no:12)。
[0112]
xiao,et al.(如上)表明芳香环提供了传导机制,而且这些环在3
‑
d结构中排列得很近,以创建芳香环的半连续传导路径。在导电生物蛋白质领域中还知道,芳香环(通常是
酪氨酸)可在赋予蛋白质导电性方面发挥一些作用。导电性至少假设是由于芳香环的存在带来的,芳香环富含电子并在环周围提供高导电性。
[0113]
对于本公开的肽,并且基于对生物导电蛋白的观察,可以向合成肽序列中添加芳香族氨基酸以增强合成肽α螺旋的导电性。在各个实施方式中,可以添加酪氨酸(y)。在某些方面,可以在3
‑
dα螺旋结构中彼此靠近的位置添加芳香族氨基酸以形成其中芳香环更紧密且连接间隔开的传导路径。图18中示出了一个这种示例,其中,α螺旋基于重复的基序eayar(seq id no:3),由此在位置i和i 5包酷氨酸,如图18所示,导致围绕螺旋盘旋的环图案,为穿过结构的电子提供螺旋传导增强路径。
[0114]
在各个实施方式中,并且基于对生物导电蛋白的观察,来自α螺旋生物导电蛋白的整个区段作为串联重复被并入到合成的α螺旋肽中,以增强导电性。这些区段可以与生物序列相同,或者与生物序列高度相似,诸如与生物氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性。在各个实施方式中,诸如在将分子导线用于水性介质中的情况下(诸如在生物传感器中),取自或受生物蛋白质启发的序列的一部分应该是可溶性或亲水性区段,或者不包含任何跨膜区段的区段,以促进螺旋的溶解度并使分子导线保持在分子电路中的溶液中,而不是移位或沉淀到基板上,并且防止在水性介质中的处理过程中发生沉淀或聚集,诸如在分子导线自组装为电路或组装至其他生物分子组分(诸如附接酶)期间。
[0115]
在各个实施方式中,基于上述pilin序列pdb:2m7g_a的合成螺旋肽分子导线,是在从生物氨基酸序列提取26个氨基酸区段(上面带下划线的)(即qfsayrvkaynsaassdlrnlktale(seq id no:13))并且使用该序列作为合成肽核中的重复基序的基础上形成的。这是一种水溶性结构域,并且具有包含这种结构域、1例序列qfsayrvkaynsaassdlrnlktcle(seq id no:31)和金结合肽序列seq id no:6的3个重复的分子导线结构的完整合成肽包含以下氨基酸序列:
[0116]
mhgktqatsgtiqs
‑
gsg
‑
mhgktqatsgtiqs
‑
gsg
‑
mhgktqatsgtiqs
‑
gsg
‑
qfsayrvkaynsaassdlrnlktale
‑
qfsayrvkaynsaassdlrnlktcle
‑
qfsayrvkaynsaassdlrnlktale
‑
qfsayrvkaynsaassdlrnlktale
‑
gsg
‑
mhgktqatsgtiqs
‑
gsg
‑
mhgktqatsgtiqs
‑
gsg
‑
mhgktqatsgtiqs(seq id no:14)。
[0117]
在各个实施方式中,根据本公开的合成肽包含与seq id no:14具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的序列。在各个实施方式中,合成肽包含seq id no:14。在各个实施方式中,此类合成肽用作分子电子电路的导电分子导线。
[0118]
包含seq id no:14的这种构建体含有基于26个氨基酸生物区段的4个串联重复的螺旋区段,但其中,第二重复包括在基序的位置24代替a的半胱氨酸(c)。这一位于内部的胱氨酸充当用于半胱氨酸
‑
马来酰亚胺缀合反应的特定缀合位点,诸如用于将结合探针附接至合成肽。此外,根据本公开,这种104个氨基酸的螺旋区段通过金结合肽mhgktqatsgtiqs(seq id no:6)的三重串联重复侧翼于n末端和c末端,使用柔性、可溶性接头
‑
gsg
‑
将每个重复和一级螺旋分开。总的来说,具有seq id no:14的合成肽的长度为206个氨基酸,分子量为21.37kda,pi(蛋白质等电点,或中性电荷的ph值)为10.08,并且内部螺旋区段长为15.5nm,具有约28.9个螺旋转。
[0119]
在各个实施方式中,根据本公开的合成肽包含以下187个氨基酸的序列:
[0120]
qqswpis
‑
gsg
‑
qqswpis
‑
gsg
‑
enlyfqg
‑
gsg
‑
qqswpis
‑
gsg
‑
a
‑
eaaar
‑
eaaar
‑
eaaar
‑
eaaar
‑
eaaar
‑
eaaar
‑
eaaar
‑
eaaar
‑
eaaar
‑
eaaar
‑
eacar
‑
eaaar
‑
eaaar
‑
eaaar
‑
eaaar
‑
eaaar
‑
eaaar
‑
eaaar
‑
eaaar
‑
eaaar
‑
eaaar
‑
a
‑
gsg
‑
qqswpis
‑
gsg
‑
enlyfqg
‑
gsg
‑
qqswpis
‑
gsg
‑
qqswpis(seq id no:15)。
[0121]
这一合成肽基于螺旋基序eaaar(seq id no:1)。基于氨基酸长度和已知每转0.54nm的α
‑
螺旋间距和每转3.6个氨基酸,其具有15.6nm长的α
‑
螺旋区段。序列进一步的特征是在每个端部具有由gsg接头间隔开的三重重复的钯结合肽qqswpis(seq id no:16)。序列eacar(seq id no:17)是定位在合成肽中心的螺旋基序。这种螺旋基序是eaaar(seq id no:1),其经用位于中心的单个半胱氨酸代替丙氨酸(a)进行修饰以在合成肽中提供缀合位点,诸如例如以用于基于马来酰亚胺或apn的缀合反应。尽管在seq id no:15中,经修饰的螺旋基序eacar(seq id no:17)精确定位在序列的中点,这一示例不应被视为是限制性的,因为位点特异性缀合位点(在本例中为c)可以向序列中的任一方向移动。在位置41和147,在一级α螺旋的各端存在单一的丙氨酸(a)残基,以避免一级α螺旋直接附接至接头gsg以及螺旋末端二级结构的可能破坏。相反,中间丙氨酸a提供了过渡性螺旋
‑
促进氨基酸,并且在某些方面用作螺旋结构中的牺牲位点。seq id no:15还包括tev蛋白酶切割序列enlyfqg(seq id no:18),其添加用于提供切割多个钯结合肽序列的选项。其他tev蛋白酶切割序列包括使用s、a、m或c中的任一个替换p1’位置的g。
[0122]
在各个实施方式中,根据本公开的合成肽包含与seq id no:15具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的序列。在各个实施方式中,合成肽包含seq id no:15。在各个实施方式中,此种合成肽用作分子电子电路的导电分子导线。
[0123]
在各个实施方式中,根据本公开的合成肽包含以下164个氨基酸的序列:
[0124]
qqswpis
‑
gsg
‑
qqswpis
‑
gsg
‑
qqswpis
‑
gsg
‑
eeeerrrr
‑
eeeerrrr
‑
eeeerrrr
‑
eeeerrrr
‑
eeeerrrr
‑
eeeerrrr
‑
eeeecrrr
‑
eeeerrrr
‑
eeeerrrr
‑
eeeerrrr
‑
eeeerrrr
‑
eeeerrrr
‑
eeeerrrr
‑
gsg
‑
qqswpis
‑
gsg
‑
qqswpis
‑
gsg
‑
qqswpis(seq id no:19)。
[0125]
这合成肽基于螺旋基序eeeerrrr(seq id no:2)。基于氨基酸长度和已知每转0.54nm的α
‑
螺旋间距以及每转3.6个氨基酸,其具有15.75nm长的α
‑
螺旋区段。该序列的进一步特征是在每一端由gsg接头间隔开的三重重复的钯结合肽qqswpis(seq id no:16)。序列eeeecrrr(seq id no:20)是定位在合成肽中心的螺旋基序。这一螺旋基序是eeeerrrr(seq id no:2),其经用大致位于中心的单个半胱氨酸代替精氨酸(r)进行修饰以在合成肽中提供缀合位点,诸如例如以用于基于马来酰亚胺或apn的缀合反应。
[0126]
在各个实施方式中,根据本公开的合成肽包含与seq id no:19具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的序列。在各个实施方式中,合成肽包含seq id no:19。在各个实施方式中,此种合成肽用作分子电子电路的导电分子导线。
[0127]
在各个实施方式中,根据本公开的合成肽包含以下227个氨基酸的序列:
[0128]
qqswpis
‑
gsg
‑
qqswpis
‑
gsg
‑
qqswpis
‑
gsg
‑
a
‑
eaaar
‑
eaaar
‑
eaaar
‑
eaaar
‑
eaaar
‑
eaaar
‑
eaaar
‑
eaaar
‑
eaaar
‑
eaaar
‑
eaaar
‑
eaaar
‑
eaaar
‑
eaaar
‑
eaaar
‑
eaaar
‑
eacak
‑
eaaar
‑
eaaar
‑
eaaar
‑
eaaar
‑
eaaar
‑
eaaar
‑
eaaar
‑
eaaar
‑
eaaar
‑
eaaar
‑
eaaar
‑
eaaar
‑
eaaar
‑
eaaar
‑
eaaar
‑
eaaar
‑
a
‑
gsg
‑
qqswpis
‑
gsg
‑
qqswpis
‑
gsg
‑
qqswpis(seq id no:21)。
[0129]
这一合成肽基于螺旋基序eaaar(seq id no:1)。基于氨基酸长度和已知的每转
0.54nm的α
‑
螺旋间距以及每转3.6个氨基酸,其具有25.4nm长的α
‑
螺旋区段。该序列的进一步特征是在每一端由gsg接头间隔开的三重重复的钯结合肽qqswpis(seq id no:16)。序列eacar(seq id no:17)是定位在合成肽中心的螺旋基序。这一螺旋基序是eaaar(seq id no:1),其经用位于中心的单个半胱氨酸代替丙氨酸(a)进行修饰以在合成肽中提供缀合位点,诸如例如以用于基于马来酰亚胺或apn的缀合反应。尽管在seq id no:21中,经修饰的螺旋基序eacar(seq id no:17)精确地定位在序列的中点,但这一示例不应被视为限制性的,因为位点特异性缀合位点(在本例中为c)可以向该序列的任一方向移动。在位置31和197,在一级α螺旋的每一端存在单个丙氨酸(a)残基以避免该一级α螺旋直接附接至接头gsg以及螺旋末端二级结构的可能破坏。相反,中间丙氨酸a提供过渡性螺旋
‑
促进氨基酸,并在某些方面作为螺旋结构中的牺牲位点。
[0130]
在各个实施方式中,根据本公开的合成肽包含与seq id no:21具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的序列。在各个实施方式中,合成肽包含seq id no:21。在各个实施方式中,此合成肽用作分子电子电路的导电分子导线。
[0131]
应当理解的是,使用本文相同的原则可以在结构上想到能够用作分子导线的其他合成肽,并且以上示例仅用于说明这些原则,并不限制范围。应当理解的是,除了pilin之外,还有其他生物天然存在的导电蛋白螺旋可作为此类合成螺旋肽的基础,诸如胶原细丝、动力蛋白、驱动蛋白、分子马达的成分、细胞色素的元件或免疫球蛋白链。
[0132]
可在分子电子电路用作分子桥的合成导电肽的结构变化
[0133]
螺旋桥长度:在各个实施方式中,通过缩短或延长一个或多个螺旋区段和/或通过扩展或减少螺旋基序的重复,本文的合成肽可以被设计成特定长度。呈现的所有螺旋基序都可以被认为是定义任意长的螺旋,例如基序eaaar(seq id no:1)可以在合成肽中无限重复,eaaar
…
eaaar,并且从中提取的任何序列区段都可以提供任何所需长度的桥螺旋。对于用于跨越间隔电极之间的肽桥,如图1或图12所示,优选长度为5nm至100nm,且更优选10nm至50nm,且最优选15nm至40nm。对于用作探针分子和电极之间的连接臂的合成肽,诸如图13所示,优选长度为2nm至50nm,且更优选5nm至30nm,且最优选7nm至20nm。对于自然发生的螺旋序列,即在生物起源的蛋白质内存在的α螺旋序列,从这些中取出的子区段可以用作较短的桥,并且相对于天然存在的α螺旋,通过重复螺旋序列的全部或一个子区段或多个子区段允许更长的桥接。
[0134]
氨基酸序列相似性:对于上文提供的螺旋氨基酸序列,可以具有类似特性和效用的其他优选序列包括与所提供的那些序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的序列。类似地,对于任何天然存在的α螺旋序列,由此提取的与天然形式具有至少80%、至少85%、至少90%、至少95%或至少98%序列相似性的至少5个氨基酸的区段可以提供优选的桥螺旋,或者重复以创建桥螺旋的区段。
[0135]
功能相似的氨基酸取代:对于本文所描述的任何螺旋序列,预期可以进行某些单个氨基酸取代保留螺旋结构和其他功能。例如,用促进螺旋结构的氨基酸替换螺旋中的一个或多个氨基酸有望提供类似结构和效用的螺旋。特别已知的是,氨基酸a、m、l、e和k促进螺旋形成,并且特别是这些可以替代螺旋中的氨基酸并可能保留螺旋结构。更一般地说,已经为每个氨基酸开发了评分,对它们形成螺旋的倾向性、或者与螺旋结构相容、或者更频繁地出现在天然存在的螺旋中进行排序。预期相似或更佳评分的氨基酸的取代将保留甚至增
强螺旋结构。一种此类评分是螺旋倾向(参考:pace,c.n.,&scholtz,j.m.(1998).a helix propensity scale based on experimental studies of peptides and proteins.biophysical journal,75(1),422
‑
427,其从数字上将氨基酸从最螺旋相容(低分)到最不相容(高分)排列为:ala=0,leu=0.21,arg=0.21,met=0.24,lys=0.26,gin=0.39,glu=0.40,ile=0.41,trp=0.49,ser=0.50,tyr=0.53,phe=0.54,val=0.61,his=0.61,asn=0.65,thr=0.66,cys=0.68,asp=0.69和gly=1)。
[0136]
此外,在位于螺旋中空间相邻的i与i 4或i 5位带相反电荷的氨基酸之间形成的盐桥,诸如eaaar(seq id no:1)和eeeerrrr(seq id no:2)基序所示,可以通过放置任何盐桥氨基酸对形成,其通常包括与带负电荷的氨基酸{e,d}盐
‑
桥接的带正电荷的氨基酸{r,k,h}。因此,从本文所描述的任何序列开始,并且取代序列中位置i处的{r,k,h}之一以及位置i 4或i 5处的{e,d}之一,预计会形成盐桥,要么保持已经存在的一个,要么添加一个以提高稳定性或导电性。例如,所描述的基序eaaar(seq id no:1)和eeeerrrr(seq id no:2)暗示了功能上取代的基序,诸如daaak(seq id no:22)和eeddrkhk(seq id no:23)。在螺旋中出现芳香环氨基酸的情况下,或引入此类以潜在地增加导电性,可以考虑任何芳香环氨基酸,诸如f、w、v或p。
[0137]
更一般地,将氨基酸分类为相似的组,诸如带电的(正、负)、极性的、疏水性的或亲水性的、或芳香族的,也指导了通过相似类型的氨基酸替换给定氨基酸的大量取代,这预计将具有类似的功能。所有此类取代均在可应用于本文所描述示例性序列的修饰范围内。
[0138]
非标准氨基酸取代。非标准氨基酸(naa),也称为非天然氨基酸(uaa),是除生物蛋白质中出现的22种氨基酸以外的氨基酸。特别地,有许多这样的naa是标准氨基酸的化学修饰形式,可以用作标准氨基酸的替代品。这些可以使用肽化学合成,或在实施了非标准遗传密码的表达系统中表达,或通过对蛋白质内的标准氨基酸进行化学修饰而掺入蛋白质中。此类naa仍然可以体现螺旋倾向、盐桥、芳香环、间隔子/接头、或与电极结合的重要设计原则—特别是当它们是体现这些特性的同源标准氨基酸的修饰形式时。因此,对属于类似形式的naa的标准氨基酸的取代提供了一大类可以对本文所描述的序列进行的改变,这有望提供类似的结构和效用。可以使用肽化学合成,或通过在已经实施了非标准遗传密码的表达系统中表达,或通过对蛋白质内的标准氨基酸进行化学修饰,将这些naa掺入到蛋白质中。
[0139]
接头变化:在所提供的示例中,将氨基酸序列gsg用作在桥的末端、一级螺旋之间以及末端的一个或多个结合基团之间的接头/间隔子。蛋白质工程领域的技术人员已知种类繁多的此类接头,其中,它们被用于隔开或减少蛋白质中目的功能结构域之间的空间干扰,并且这些中的许多可以在本文所描述的序列中用作替代接头/间隔子。例如,其他常见的接头是g/s序列,诸如g、gs、sg、gsgs(seq id no:24)、gsssgsssg(seq id no:25)等。更一般地,富含{g,s}的序列提供了方便且常用的接头。更一般地,文献中使用了种类繁多的接头/间隔子,并且这些中的任何一个都可以在本文所描述的序列中适用于替代接头。一般来说,这些接头往往是形成柔性和亲水链的序列,其可以通过高{s,g}含量的短序列方便地完成。优选地,此类接头较短,优选1至10个氨基酸,但更长的接头也可行。在http://parts.igem.org/protein_domains/linker上可以找到各种应用中使用的各种接头/间隔子的汇编。除了诸如gsg等肽接头/间隔子之外,在通过化学合成制得的肽的情况下,可以使
用其他柔性分子接头,这允许将非氨基酸元件添加到肽链中。一种常见的此类家族可以是短碳链接头,诸如c3、c6或c12(3、6、或12烃链)。在此种情况下,可以使用这些或其他短分子接头代替肽接头,诸如gsg。
[0140]
钉住的(stapled)螺旋:一种用于稳定α螺旋的已知技术是在螺旋转之间使用烃订书钉,以将它们化学连接在一起。任何本文所描述的螺旋还可以被修饰以包含一个或多个订书钉以进一步稳定螺旋。此类方法描述于例如:hydrocarbon
‑
stapled peptides:principles,practice,and progress,loren d.walensky and gregory h.bird,journal of medicinal chemistry,57(15),6275
‑
6288(2014)。
[0141]
功能类似的基序变化:本文描述的螺旋基序具有许多体现相同设计原则的直接延伸。例如,基序eaaar(seq id no:1),可以暗示功能相似的基序eaaarraaae(seq id no:26)或eaaaraaraaar(seq id no:27)等,它们使用螺旋形成氨基酸a并且具有可以在i和i 4位之间形成的e
‑
r盐桥。或者例如,基序eeeerrrr(seq id no:2)可以暗示更长形式的功能类似基序eeeerrrrrrrreeee(seq id no:28),其仍然将每个e/r与i 4r/e配对。提出的基序eaaar(seq id no:1)和eeeerrrr(seq id no:2)只是这些家族中最简单和/或最短的,而许多更长和/或更复杂的基序模式可以体现相同的原则。
[0142]
一般桥接架构:超出本文提供的具体示例序列(诸如seq id no:14、15、19和21)的合成肽结构的范围包括包含以下通式的合成肽:
[0143]
[x1x2]
m
x3[x4]
n
x3[x2x1]
m
,
[0144]
其中,
[0145]
每个x1独立地为包含约5至约15个氨基酸的材料结合肽、蛋白酶切割序列、或肽捕获标签;
[0146]
每个x2独立地为富含甘氨酸/丝氨酸{g,s}的接头或c1
‑
c20碳链分子接头;
[0147]
每个x3独立地为共价键、单个氨基酸、过渡性螺旋
‑
促进基序、金属结合基团、或包含约5至约15个氨基酸的材料结合肽;
[0148]
每个x4独立地为包含约4至约40个氨基酸的α螺旋基序;
[0149]
每个m独立地为0至4;且
[0150]
n为1至40。
[0151]
涵盖在种类[x1x2]
m
x3[x4]
n
x3[x2x1]
m
内的合成肽的物种的每一个,其中,每个基序以及n和m的范围如本文定义,可以用作桥接跨越间隔开的电极的导电分子导线,如图2所示,或用作在电极与结合探针上特定位点之间缀合的合成肽臂分子,如图13所示。导电合成肽的效应的差异至少部分地取决于是否沿合成肽的序列提供了缀合位点,诸如用于将探针分子附接至合成肽的缀合位点,以及[x1x2]
m
和x3基序的构型,诸如这些基序是否被设计用于结合至金属电极或生物分子(诸如结合探针)和合成肽的末端是否相同或不同。如上所讨论的,合成桥肽的特征可以在于在肽序列中具有半胱氨酸(c)或其他缀合位点,诸如靠近沿合成肽长度的中点。也就是说,x4α螺旋基序中的至少一个可以包含缀合位点,诸如半胱氨酸残基。在各个实施方式中,x1基序包含材料结合肽,其可以使用中间富含甘氨酸/丝氨酸的接头x2(诸如
‑
gsg
‑
)以三重排列。在这些情形下,当m不为0时,x3可以在三重排列的材料结合序列与由重复的α螺旋基序组成的核α螺旋区段之间用作间隔子。在某些示例中,当m不为0时,x3可以是过渡性螺旋
‑
促进氨基酸,如丙氨酸(a)。当不需要过渡性螺旋
‑
促进氨基酸
时,x3可以只是共价键。
[0152]
在如上讨论的其他示例中,一个或两个[x1x2]
m
末端基序的全部可以完全不存在,即当m=0时。在m=0的各个实施方式中,意味着[x1x2]
m
区段不存在,x3可以接替合成肽任一端或两端末端区域中结合基序的角色。例如,当m=0时,x3可以包含半胱氨酸(从而在肽末端提供单个
‑
sh基团),或者可以包含用于特异性缀合的更复杂的排列,诸如一串两个或更多个半胱氨酸氨基酸,或材料结合肽。在其他情况下,当m=0时,x3可以包含具有用于特异性结合的叠氮基团或其他官能团的非天然氨基酸。
[0153]
尽管以上的一般性讨论提供了关于如何选择基序以赋予合成肽以各种物理属性的一些观点,但以下基序选项进一步定义了合成肽的通式的范围,[x1x2]
m
x3[x4]
n
x3[x2x1]
m
:
[0154]
在各个实施方式中,每个x1可以包含含有约5至约15个氨基酸的材料结合肽、蛋白酶切割序列或肽捕获标签中的任何一个。在某些示例中,x1包含与seq id no:6、7、8、9、10、11、16、18或29中任一个具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的氨基酸序列。在某些示例中,x1包含seq id no:6、7、8、9、10、11、16、18或29中的任何一个。在各个实施方式中,x1包含配置为与特定金属结合的序列。重要的是要记住,可以独立地选择x1的每个实例,以便在必要时,合成肽的n末端和c末端可以不同。当配置为结合结构域,x1可以由材料结合肽或一系列由中间接头x2间隔开的此种材料结合肽序列组成,或者可以包含与某些材料或官能团结合/缀合的氨基酸,诸如可以结合各种金属或缀合基团马来酰亚胺的半胱氨酸。结合结构域还可以包含其他已知的缀合基团,诸如硫醇、生物素、马来酰亚胺、apn、赖氨酸、叠氮化物、或胺、或缀合化学领域技术人员已知的许多其他基团。肽靶标标签可以含有抗体的肽靶标,诸如flag表位标签、his标签(聚组氨酸)、myc标签、ha、gst或其他表位标签,或为缀合靶标的肽基团,诸如avi标签或醛标签。在其他示例中,出于合成原因,x1可以在肽的一个末端包含捕获标签,或者一个或两个末端可以包括蛋白酶切割序列,以便在偶联至其他元件之前或之后,可以诸如从先前连接的电极或其他电路元件、或可能缀合的其他生物分子上消化掉合成肽。
[0155]
在各个实施方式中,x2可以包含富含甘氨酸/丝氨酸的接头或烃类接头。对于前者,在其他富含甘氨酸/丝氨酸的序列中,g、s、
‑
gs
‑
和
‑
gsg
‑
被设想为非限制性选项,甚至多达至少10个或更多个氨基酸。接头x2也可以包含“系链”,称为“c1至c20碳链分子接头”。对c1到c20碳链分子接头的性质的唯一限制是它是二价的,以便接头可以将合成肽的一部分连接到另一部分。在各个实施方式中,此种接头包括但不限于亚甲基
‑
ch2‑
及其同系物
‑
(cf2)
p
‑
(其中,p=1至约20),从1eo至多达约10eo的乙氧基化物,1,4
‑
亚苯基,
‑
co2‑
,
‑
c(o)
‑
nh
‑
等。c1
‑
c20接头还可以包括碳原子和杂原子的任何组合,并且可以是无环的、环状的、脂肪族的、或芳香族的、或其组合。在各个实施方式中,x2可以包含氨基酸序列与c1
‑
c20非氨基酸物种的组合。可以为某些器件定制x2的长度,诸如取决于金属电极上的接触面积,或使结合至合成肽上的探针分子与金属电极之间达到所需的分离距离。例如,x2可以特意地较长,以使材料结合肽x1远离附接至约合成肽中点(即靠近[x4]
n
区段的中心)的结合探针。
[0156]
在各个实施方式中,基序x3可以包含共价键、单个氨基酸、过渡性螺旋
‑
促进基序、金属结合基团、或包含约5至约15个氨基酸的材料结合肽。如所讨论的,x3的选择至少部分取决于x1的选择,特别是如果m=0并且合成肽的末端完全由x3的性质限定。当x3包含“共价键”时,则合成肽不存在x3并且由[x4]
n
定义的内部α螺旋区段的末端直接与x2键合。换言之,
声明x3可以是共价键相当于声明x3的存在是可选的。在各个实施方式中,x3可以包含单个氨基酸,诸如丙氨酸(a),其用作不会损害由[x4]
n
限定的α螺旋区段的间隔子。在各个实施方式中,x3可以包含比仅一个氨基酸更长的间隔子,并且可以包含过渡性螺旋
‑
促进基序,一种促进α螺旋二级构象的间隔子。此种过渡性螺旋
‑
促进基序可以包含至多约5个氨基酸,并且可以如聚丙氨酸序列一样简单。
[0157]
在各个实施方式中,诸如当m=0时,x3可以包含金属结合基团。本文中已经详细地讨论了此类金属结合基团的选择,并且包括诸如硫醇基团、碳烯、胺基团、重氮基团、或能够至少在一定程度上结合金属(如au、pt或pd)的任何其他官能团等物种。在各个实施方式中,金属结合基团可以包含提供硫醇基的氨基酸(即半胱氨酸)或经衍生以包括不是产生自氨基酸且能够结合金属的官能团的氨基酸。换句话说,x3可以包含单个氨基酸,但不是选择以充当促进α螺旋构象的间隔子的单个氨基酸,单个氨基酸可以经选择,因为它提供能够结合金属的官能团。在各个实施方式中,x3可以包含两个或更多个半胱氨酸残基,诸如一串六个或更多个半胱氨酸。在各个实施方式中,x3可以包含四
‑
半胱氨酸flash结合基序ccxxcc,(x=任何氨基酸),诸如cccgcc(seq id no:5),如上所描述。在各个实施方式中,x3可以包含flash结合基序ccxxcc,其中,xx是脯氨酸
‑
丝氨酸,即ccpscc(seq id no:34)。
[0158]
在各个实施方式中,合成肽的螺旋核部分,即[x4]
n
,可以包含与该部分连接的促进α螺旋二级结构的任何氨基酸序列重复,诸如qfsayrvkaynsaassdlrnlktale(seq id no:13)或包含seq id no:1或2的重复基序。从示例中可以明显看出,重复整数n以及重复的α螺旋基序x4的序列长度可以对合成肽的整体长度具有深远影响,并且这两个变量以及末端部分的选择都可以被操纵以定义非常精确长度的合成肽。如前所描述,如果要将合成肽用作桥接间隔开的电极或将生物分子连接到分子电子电路中的电极的分子导线,则可预测且精确的长度对于合成肽来说很重要。
[0159]
螺旋内(例如经重复以定义合成肽的α螺旋核的x4α螺旋基序的至少一个内)的缀合位点可以是氨基酸,诸如半胱氨酸或赖氨酸,或者其可以是经修饰的氨基酸,诸如附接有游离叠氮基团的赖氨酸、或附接有生物素的赖氨酸、或通过化学修饰或合成放置在肽内的经修饰的氨基酸或非氨基酸位点。此外,并且此类一级缀合位点可以被化学官能化或转化为用于缀合的其他基团,诸如通过使用与半胱氨酸反应的叠氮化物
‑
马来酰亚胺双官能接头将半胱氨酸转化为叠氮化物。从一级缀合位点转化为所需的缀合基团的许多其他此类转化是可能的,并且是缀合化学领域技术人员众所周知的。
[0160]
在各个实施方式中,式[x1x2]
m
x3[x4]
n
x3[x2x1]
m
的合成肽包含与seq id no:14具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的氨基酸序列。在具体的示例中,合成肽包含seq id no.14。
[0161]
在各个实施方式中,式[x1x2]
m
x3[x4]
n
x3[x2x1]
m
的合成肽包含与seq id no:15具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的氨基酸序列。在具体的示例中,合成肽包含seq id no.15。
[0162]
在各个实施方式中,式[x1x2]
m
x3[x4]
n
x3[x2x1]
m
的合成肽包含与seq id no:19具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的氨基酸序列。在具体的示例中,合成肽包含seq id no.19。
[0163]
在各个实施方式中,式[x1x2]
m
x3[x4]
n
x3[x2x1]
m
的合成肽包含与seq id no:21具有
至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的氨基酸序列。在具体的示例中,合成肽包含seq id no.21。
[0164]
桥分子的制造:化学肽合成和蛋白质表达的已知方法可用于产生本文所描述的桥分子。在化学肽合成的情况下,在化学偶联步骤中连续添加氨基酸以合成目的链时,也可以添加经修饰的/非天然氨基酸,以及添加内部或末端非氨基酸基团,例如化学接头或缀合基团。在蛋白质表达的情况下,靶桥必须完全由氨基酸构成,并产生相应的基因,放入诸如大肠杆菌细菌等生物表达系统中,并且表达基因以产生所得蛋白质,后从培养的细胞中提取和纯化蛋白质。此类蛋白质可以被进一步化学修饰以产生某些所需的基团,诸如使半胱氨酸与马来酰亚胺反应以在位点缀合其他基团,或者使赖氨酸与nhs反应,或与末端氨基或羧基反应。通常可以从将这些过程作为服务执行的商业供应商处订购由这两种方法中任何一种制成的桥。已被遗传修饰以使用非标准氨基酸的表达系统也可用于将此类naa插入蛋白质产品中。
[0165]
本文的原则还扩展到被组织为上述单链螺旋肽束的分子导线。例如,如上所描述的由三螺旋链形成的三重螺旋是这一概念的进一步扩展。对于一个此类实施方式,这样的示例可能基于合成形式的胶原蛋白,其自然形成三重螺旋。类似地,pilin自然地组织成多链超结构,因此可以由由pilin驱动的合成分子导线形成类似的多链结构。
[0166]
合成肽作为分子导线在分子电子学中的用途
[0167]
根据本公开的传导性合成肽具有至少两个值得注意的应用。它们可以用作分子导线以在其他关键分子电路元件之间形成导电连接,诸如图3、4、5和6所示。在这些示出的器件中,肽的主要功能是提供一个导电路径,其不会过度阻碍电子或其他电荷载流子通过电路的传输。在另一值得注意的应用中,合成肽的导电性由于与其直接环境的相互作用而发生变化,在此种情况下,它可以作为传感器结构的一部分。
[0168]
在一些实施方式中,导线直接与环境中的分子(诸如气体环境中的气体分子,或液体环境中溶液中的分子)相互作用,并且由于这些相互作用而改变电导率或电阻(见图1)。在其他实施方式中,诸如图2所示,将次级分子缀合至跨越电极的主要分子导线,并且这种次级分子与其结合靶的相互作用可以产生局部环境变化,从而调节导线的导电性,从而通过监测在施加电压下流经该复合体的电流,为这些相互作用提供传感器,如图2所示。在此类传感器系统中,由靶底物与酶接合产生的局部电荷扰动扰乱了通过主要导线的电荷传输,并由此记录为导电率或电流相对于时间的变化,如i与t电流图插图的步升步化所示。提供信息的电流变化可能是增加、或减少、脉冲或其他时间变化。
[0169]
出于说明的目的且不限制本公开的范围,图2
‑
10和12
‑
14示出了各种此类分子传感器构建体,其包含在分子电子电路中充当分子导线的一个或多个本文公开的合成肽,其中,合成肽在各附图中示意性地显示为球棒表示(图1
‑
8)或为长细条(在图9
‑
10和12
‑
14)。用于将合成肽连接到电极和/或其他分子的缀合系统在附图中用小阴影方块示意性地表示在合成肽/生物分子和合成肽/电极/基底的交叉处。此缀合点可以代表任何已知用于在两个分子/原子(金属)组分之间建立特定连接的分子缀合,诸如点击化学偶联、硫醇
‑
金属结合、生物素
‑
亲和素结合、材料结合肽、重氮
‑
金属结合、碳烯
‑
金属结合、半胱氨酸
‑
马来酰亚胺偶联、胺反应性交联或者化学缀合、生物缀合或材料表面缀合领域技术人员已知的许多其他分子缀合。这种缀合所需的同源元件通常整合在如本文设计和制造的合成肽的结构和
附接位点中。简而言之,包含充当分子导线的合成肽的电子结构如以下附图所示:
[0170]
图2示出了缀合至跨越两个电极的合成肽的结合探针分子。这一电路用作传感器,其中,在施加的电压下,当探针分子与其同源靶分子结合时,通过调节导线的电导率产生电流步升信号(电导率增加)。在各个实施方式中,结合探针分子包含酶,诸如聚合酶,并且该传感器可用于测序dna。
[0171]
在各个实施方式中,图2的传感器包括进行性酶分子电子学传感器。在各个示例中,该传感器包括:第一电极;通过电极间隙与第一电极间隔开的第二电极;包含进行性酶的传感器复合物,该进行性酶缀合至电连接至第一电极和第二电极并且桥接它们之间的间隙的根据本公开的合成肽。进行性酶可以包含天然或基因工程聚合酶、逆转录酶、解旋酶、外切、或用于包装病毒dna的分子马达。对于工作传感器,将跨阻放大器电连接至第一电极和第二电极中的至少一者,跨阻放大器提供包含可测量电参数的输出;其中,可测量电参数包含对应于进行性酶的酶促活性的可区分信号。
[0172]
图3示出了其中结合探针分子通过充当臂分子的两个合成肽直接电连接至一对间隔开的电极的构造,臂分子在此处主要作为探针分子的导电连接器,探针分子本身当结合其同源靶时会改变其导电率。本文用作臂分子的合成肽仅需要在末端官能化,因为不需要沿着肽序列的中心点进行缀合。并入了根据本公开的合成肽的图2或图3的构造均可以用作dna测序的传感器。
[0173]
在各个实施方式中,一种分子电子电路包括由基底上的纳米间隙间隔开的第一和第二电极,以及电连接至第一和第二电极并由此桥接纳米间隙的合成肽。例如,图2示出了这一实施方式。在各个实施方式中,下层基底包含sio2。在各个实施方式中,电极包含金属,诸如au、pt或pd。在各个实施方式中,第一电极和第二电极是电路中的正电极和负电极。在各个实施方式中,将桥接合成肽缀合至结合探针,诸如聚合酶。缀合位点可以基本上位于合成肽序列的中央,以防止附接的聚合酶与电极对中的任何一个电极接触。在各个实施方式中,可以将栅电极放置在电极之间和桥接肽的下方,诸如基底中的掩埋栅极。在各个实施方式中,将跨阻放大器电连接至第一电极和第二电极的至少一个,跨阻放大器提供包含可测量电参数的输出;其中,可测量电参数包含对应于涉及与桥接肽缀合的结合探针的结合事件的可区分信号。
[0174]
在各个实施方式中,一种分子电子电路包括通过基底上的纳米间隙间隔开的第一和第二电极,以及充当臂分子的两个合成肽,合成肽将结合探针(诸如聚合酶)电连接至第一电极和第二电极,由此桥接纳米间隙并且迫使导电电路通过结合探针的一部分。例如,图3示出了这一实施方式。在各个实施方式中,下层基底包含sio2。在各个实施方式中,电极包含金属,诸如au、pt或pd。在各个实施方式中,第一电极和第二电极是电路中的正电极和负电极。两个合成肽臂分子的长度决定了结合探针如何位于电极的中央,并且这些长度可以精确设计,以防止附接的聚合酶与电极对中的任何一个电极接触。在各个实施方式中,可以将栅电极放置在电极之间并且在桥接肽下方,诸如基底中的掩埋栅电极。在各个实施方式中,将跨阻放大器电连接至第一电极和第二电极的至少一个,跨阻放大器提供包含可测量电参数的输出;其中,可测量电参数包含对应于涉及通过肽臂分子电连线到电路中的结合探针的结合事件的可区分信号。
[0175]
诸如在图2和图3的背景下所描述的且包含根据本公开的一个或多个合成肽的传
感器电路可以在芯片上排列为阵列,以便多个这样的传感器可以作为dna测序系统运行。在系统的各个方面,系统还包括cmos传感器阵列芯片,其包括传感器阵列和执行可测量电参数测量的支持像素电路。
[0176]
在系统的各个方面,系统包括至少两个cmos传感器阵列芯片;电子硬件系统,用于控制和管理芯片的电气输入和数据输出;流体系统,用于将缓冲溶液中的合成dna分子引入芯片;以及信号处理和数据记录系统,用于捕获可区分信号并将可区分信号转换回信息。
[0177]
图4
‑
10和12
‑
14示出了分子电子电路的其他构造,其包括一个或多个根据本公开各个实施方式的合成肽。这些电路可以是如上图2和图3所描述的生物传感器的一部分,并且如所讨论的,这些传感器可以在芯片上排列为阵列。
[0178]
图4示出了分子电子电路的一个特例,其中,探针分子是具有内部α螺旋作为其结构一部分的蛋白质,并且两个合成肽将蛋白质的内部α螺旋的端部连接至正电极和负电极,以提供通过探针分子的一部分的导电通路。
[0179]
图5示出了进一步的变型,替代地,将合成肽臂分子连接至蛋白质探针分子内的内部β片层,再次创建了优选的导电路径。
[0180]
图6示出了一传感器构造,其中,使用三个合成肽臂分子将探针连线至电极,以与电极具有多重量连接。
[0181]
图7示出了以图2的调制方式使用一个合成肽,用两个其他合成肽将探针分子直接连接至第一和第二电极。
[0182]
图8示出了稍微更复杂的构造,其中,合成肽臂分子将探针连接至多个电极系统,从而允许多个同时测量。
[0183]
图9示出了图3的一个具体例,其中,探针分子为igg抗体蛋白,并且同源结合靶是相应的抗原,并且其中,此类系统可以用于检测抗体
‑
抗原结合。
[0184]
图10示出了图3的一个具体例,其中,探针分子是单链dna寡核苷酸,并且其结合靶是互补寡核苷酸,并且其中,此类系统可用于检测杂交探针结合。
[0185]
图11示出了klenow聚合酶的详细蛋白质结构,当聚合酶复制模板时,它可以在感测dna序列的背景下用作结合探针。
[0186]
图12、13和14示出了根据本公开的合成肽分别在作为图2、4和6的具体实例的各个构造中用于连接聚合酶的用途,并且所得电路可以用作通过聚合酶的模板过程序列的传感器。
[0187]
根据本公开的用作分子导线的导电合成肽可以是分子电子学传感器中使用的分子传感器复合物的一部分。在任一图2
‑
14所公开的实施方式中,在这些电路中使用的桥接合成肽和/或合成肽臂分子可以包含本文公开的合成肽的任何一个。可以利用本文中的合成肽的分子传感器还公开于美国专利no.9,829,456;10,036,064;10,125,420;10,151,722和10,508,296;以及美国专利申请公开no.20180340220中,其各自通过引用整体并入本文。如通过引用并入本文,此类传感器可布置在由cmos工艺生产的芯片上的传感器阵列中。所公开的传感器可用于dna测序。
[0188]
在各个实施方式中,公开了一种对dna分子进行测序的方法。该方法包括:提供电路,该电路还包括正电极;与正电极间隔开的负电极;导电合成肽,该导电合成肽电连接至正电极和负电极;和聚合酶,该聚合酶在沿合成肽序列定位的缀合位点处缀合至合成肽;启
动通过电路的电压或电流中的至少一者;使电路暴露于含有引物引发的单链dna和/或dntp的溶液中;以及测量当聚合酶接合并延伸模板时通过电路的电信号,其中,处理电信号以识别提供关于由聚合酶处理的dna分子潜在序列的信息的特征。在各个实施方式中,连接在正电极与负电极之间的合成肽包含式:[x1x2]mx3[x4]nx3[x2x1]
m
,其中:
[0189]
每个x1独立地为包含约5至约15个氨基酸的材料结合肽、蛋白酶切割序列、或肽捕获标签;
[0190]
每个x2独立地为富含甘氨酸/丝氨酸{g,s}的接头或c1
‑
c20碳链分子接头;
[0191]
每个x3独立地为共价键、单个氨基酸、过渡性螺旋
‑
促进基序、金属结合基团、或包含约5至约15个氨基酸的材料结合肽;
[0192]
每个x4独立地为包含约4至约40个氨基酸的α螺旋基序;
[0193]
每个m独立地为0至4;且
[0194]
n为1至40,
[0195]
其中,x4的至少一个实例包含缀合位点。
[0196]
在各个实施方式中,缀合位点包含硫醇、生物素、叠氮化物、胺、点击化学基团、半胱氨酸、赖氨酸或酪氨酸、或能够将合成肽缀合至诸如聚合酶等生物分子的任何官能团。
[0197]
在各个实施方式中,公开了对dna分子进行测序的另一种方法。该方法包括:提供电路,该电路还包括正电极;与正电极间隔开的负电极;电连接至正电极和聚合酶上第一位点的第一导电合成肽臂分子,和电连接至负电极和聚合酶上第二位点的第二导电合成肽臂分子,由此提供通过聚合酶的导电通路;启动通过电路的电压或电流中的至少一者;将电路暴露于含有引物引发的单链dna和/或dntp的溶液中;以及测量当聚合酶接合并延伸模板时通过电路的电信号,其中,处理电信号以识别提供关于由聚合酶处理的dna分子潜在序列的信息的特征。在各个实施方式中,第一和第二合成肽臂分子的每一个均包含式:
[0198]
[x1x2]
m
x3[x4]
n
x3[x2x1]
m
,其中:
[0199]
每个x1独立地为包含约5至约15个氨基酸的材料结合肽、蛋白酶切割序列、或肽捕获标签;
[0200]
每个x2独立地为富含甘氨酸/丝氨酸{g,s}的接头或c1
‑
c20碳链分子接头;
[0201]
每个x3独立地为共价键、单个氨基酸、过渡性螺旋
‑
促进基序、金属结合基团、或包含约5至约15个氨基酸的材料结合肽;
[0202]
每个x4独立地为包含约4至约40个氨基酸的α螺旋基序;
[0203]
每个m独立地为0至4;且
[0204]
n为1至40。
[0205]
在各个实施方式中,合成肽的[x1x2]
m
或x3基序中的至少一个被配置为将合成肽的末端结合至正电极、负电极、聚合酶上第一位点或聚合酶上第二位点中的任何一个。
[0206]
实施例
[0207]
桥效用的实验验证:
[0208]
制造了包含重复α螺旋基序eaaar(seq id no:1)和α螺旋基序eeeerrrr(seq id no:2)的各种合成肽,其在末端具有钯结合肽以及可用于缀合的中央半胱氨酸残基,并且具有约15.6nm、15.75nm和25.4nm的长度(对于桥的α螺旋部分,不包括接头和结合肽)和接近整数个螺旋转,使得结合基团可以接触电极表面而不会在螺旋上产生过大的扭转应力。用
id no:19的合成肽)和20pa(具有seq id no:15的合成肽),并且这些被解释为在单桥中观察到的导电性,并因此seq id no:15展现出比seq id no:19更高的导电性。更有更高阶电流(接近30pa和45pa)的少数群体被解释为来自跨越电极间隙的多个桥。
[0218]
桥传感器实验:
[0219]
在这些实验中,配置了具有seq id no:21的25.4nm长的合成肽,以创建检测结合和酶活性事件的传感器。使用标准半胱氨酸缀合化学,将合成肽中的中央半胱氨酸c缀合至线性单链dna寡核苷酸的5’末端。所附接的寡核苷酸作为探针分子与引物dna寡核苷酸结合。由此产生的合成肽和dna寡核苷酸探针分子的组装桥接横跨钯电极,这些电极被制造和部署用于实验,如上述桥导电性实验。一旦在溶液中建立,首先允许该桥/探针组装与互补引物寡核苷酸结合,提供第一类型的结合事件以进行检测,并且其建立了3’末端引物位点,即为从模板寡核苷酸5’末端与桥接肽的半胱氨酸相接处的缀合交汇位点除去5个碱基。然后,向溶液中引入聚合酶,使该聚合酶与引物们点结合,并且提供第二类型的结合事件以进行检测。将聚合酶保持在非催化缓冲液中(将锶用作二价阳离子),以便其不会掺入核苷酸中,并它们因此可逆地结合和退出袋,又提供了第三类型的结合事件供传感器检测。
[0220]
图21显示了整个实验的电流
‑
时间曲线,其在5000秒的过程中显示,当加入聚合酶时,传感器检测到强电流尖峰,并在加入核苷酸后检测到一系列强尖峰。这些尖峰被解释为信号聚合酶与桥上的引物复合物结合,然后是核苷酸非生产性地且瞬时地结合到聚合酶袋中。该实验说明了这种桥肽在传感器背景下的用途。
[0221]
提供了可以在各种排列的分子电子电路中用作导电桥联分子或臂分子的合成肽。在本文的详细描述中,提及“各个实施方式”、“一个实施方式”、“一个实施方式”、“一个示例实施方式”等表示所描述的实施方式可以包括特定的特征、结构或特性,但可不一定每个实施方式都包括所描述的特定的特征、结构或特性。此外,此类短语不一定是指同一实施方式。另外,当关联一个实施方式描述特定特征、结构或特性时,应认为在本领域技术人员的知识范围内,无论是否明确描述,其均影响关联其他实施方式的此类特征、结构或特性。在阅读说明书后,相关领域的技术人员将清楚如何在替代实施方式中实施本公开。
[0222]
已经关于具体实施方式在本文中描述了益处、其他优点和问题的解决方案。然而,所描述的益处、优点、问题的解决方案以及可导致任何益处、优点或解决方案发生或变得更显著的任何要素都不能被解释为本公开的关键、必须或必要特征或要素。因此,本公开的范围仅受所附权利要求书的限制,其中,对单数形式的要素的引用并非旨在表示“一个且仅一个”(除非明确如此说明),而是表示“一个或多个”。此外,当在权利要求或说明书中使用类似于
‘
a、b和c中的至少一个’或
‘
a、b或c中的至少一个’的短语的情况下,意旨该短语应解释为表示a可单独存在于一个实施方式中,b可单独存在于一个实施方式中,c可单独存在于一个实施方式中,或者要素a、b和c的任意组合可存在于单个实施方式中;例如,a和b,a和c,b和c,或a和b和c。
[0223]
本领域普通技术人员已知的与上述各个实施方式的要素等效的所有结构、化学和功能等效物均通过引用明确并入本文并且旨在被本权利要求所涵盖。此外,化学实体、分子电子结构或方法不必解决本公开寻求解决的每一个问题,以使其包含在本权利要求中。另外,本公开中的任何要素、组件或方法步骤均不旨在奉献给公众,无论权利要求中是否明确列举该要素、组件或方法步骤。没有任何声明要素旨在援引35u.s.c.112(f),除了使用短语
“
用于
……
的手段(means for)”来明确叙述该要素。如本文所用,术语“包含(comprises)”、“包括(comprising)”或其任何其他变型旨在涵盖非排他性的包括,以便包含一系列要素的化学品、化学组合物、工艺、方法、制品或装置不仅包括这些要素,而且还可包括未明确列出的或此类化学品、化学组合物、工艺、方法、制品或装置所固有的其他要素。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。