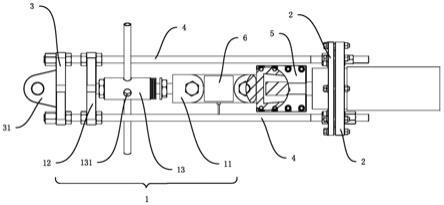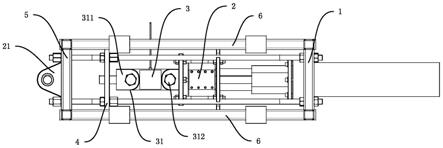
1.本发明属于中药质量分析技术领域,具体涉及一种消痞和胃胶囊的高效液相色谱(hplc)指纹图谱测定方法。
背景技术:
2.消痞和胃胶囊源于苗族,由隔山消、刺梨叶、柳枝和三七四味中药组成,具有理气和胃、消痞止痛、通脉活络的功效,可用于治疗脾胃气滞所致的胃脘灼热胀痛、泛吐酸水、痞满嘈杂等症。临床上还可用于治疗胃癌前病变、功能性消化不良等胃肠道疾病。隔山消,又称白首乌,归脾、胃、肾经,具有消食化积、养阴补虚、抗衰老、补血提气等药理活性。隔山消中主要的活性成分包括c21甾体皂苷类和苯乙酮类化合物,4
‑
羟基苯乙酮为代表性化合物。刺梨叶,归脾、肾、胃经,其主要含有氨基酸、酚酸类、黄酮类化合物,可用于治疗积食饱胀,疥痛金疮。柳枝,为杨柳科植物垂柳的枝条,归胃、肝经,常被用于治疗发烧、皮肤病、感染等慢性炎症,其镇痛、解热、抗炎的特性与其中的活性成分水杨苷及其衍生物密切相关;三七,为五加科植物三七的干燥根,专入胃、肝经,有止血散血定痛的功效,三七总皂苷(包括三七皂苷r1、人参皂苷rg1、人参皂苷rb1和人参皂苷re等组分)是三七的主要活性成分,其含量高达12%。
3.消痞和胃胶囊现收载于国家药品监督管理局国家药品标准中,其质控方法主要采用单一物质的含量测定,但针对单味药成分的测定分析方法并不能反映中药复方整体的质量水平,其质量稳定性也难以保证。
技术实现要素:
4.为了改善上述技术问题,本发明提供消痞和胃胶囊的指纹图谱的构建方法或检测方法,包括取消痞和胃胶囊的供试品溶液,进行hplc检测,hplc检测条件包括:采用c18色谱柱,以水相为流动相a,乙腈为流动相b,进行梯度洗脱。
5.根据本发明,梯度洗脱程序为:
[0006][0007]
优选地,梯度洗脱程序为:
[0008][0009]
根据本发明,c18色谱柱可以为symmetryshieldtmrp18或c18色谱柱,在本发明的一个实施方式中,为c18色谱柱,示例性为c
18
柱[(1.5
‑
4.6)mm i.d.
×
(150
‑
250)mm,1.5
‑
5μm)]。
[0010]
根据本发明,所述检测波长为200~206nm,在本发明的一个实施方式中,为203nm。
[0011]
根据本发明,所述检测的进样量为2.0~8.0μl,在本发明的一个实施方式中,进样量为5.0μl。
[0012]
根据本发明,所述检测的流速为0.8
‑
1.3ml/min,在本发明的一个实施方式中,流速为1.0ml
·
min
‑1。
[0013]
根据本发明,所述检测的柱温为20~40℃,在本发明的一个实施方式中为30℃。
[0014]
根据本发明,所述供试品溶液的制备方法包括取消痞和胃胶囊内容物,加入溶剂提取。所述溶剂可以是本领域中常用于天然化合物提取的溶剂,包括但不限于醇或者醇的
水溶液。在本发明的一些实施方式中,醇选自甲醇、乙醇。在本发明的一些实施方式中,提取溶剂例如选自60
‑
85%的甲醇水溶液,示例性的为75%的甲醇水溶液。
[0015]
所述提取方法可以是本领域常用的天然化合物提取方法,包括但不限于超声提取或回流提取。在本发明的一些实施方式中,采用回流提取。例如,所述回流提取的时间为0.5
‑
2h,示例性为0.5h、1h、2h。
[0016]
根据本发明,所述供试品溶液制备时胶囊内容物重量和加入提取溶剂的体积比为10~30mg胶囊内容物/ml,示例性为10mg胶囊内容物/ml、20mg胶囊内容物/ml、30mg胶囊内容物/ml。
[0017]
根据本发明,所述供试品溶液的制备方法还包括对提取液进行固液分离得到供试品溶液的操作。所述固液分离可以是本领域常用的分离手段,包括但不限于过滤和离心。在本发明的一个实施方式中,采用过滤,例如,采用0.45μm微孔滤膜过滤。
[0018]
在本发明的消痞和胃胶囊指纹图谱构建方法中,还进一步包括对标准品溶液进行相同hplc条件的检测。
[0019]
根据本发明,所述标准品包括水杨苷、表儿茶素、4
‑
羟基苯乙酮、三七皂苷r1、人参皂苷rg1和人参皂苷rb1。
[0020]
根据本发明,所述标准品溶液是单一每个标准品的溶液,和/或,6种标准品混合物的溶液。
[0021]
根据本发明,所述构建方法还包括配置标准品溶液,所述标准品溶液的制备方法包括制备每个标准品的溶液,分别取水杨苷、表儿茶素、4
‑
羟基苯乙酮、三七皂苷r1、人参皂苷rg1和人参皂苷rb1,用溶剂溶解,得到每个标准品的溶液。
[0022]
根据本发明,所述标准品溶液的制备方法还可以包括制备标准品混合物的溶液,取水杨苷、表儿茶素、4
‑
羟基苯乙酮、三七皂苷r1、人参皂苷rg1和人参皂苷rb1,混合,用溶剂溶解,得到标准品混合物的溶液。
[0023]
根据本发明,制备标准品溶液的所述溶剂选自甲醇和/或乙醇,在本发明的一个实施方式中为甲醇。
[0024]
根据本发明,所述每个标准品溶液或者标准品混合物溶液的水杨苷、表儿茶素、4
‑
羟基苯乙酮、三七皂苷r1、人参皂苷rg1和人参皂苷rb1的浓度分别为20~25μg/ml、5~10μg/ml、2~10μg/ml、110~120μg/ml、400~410μg/ml、360~380μg/ml;在本发明的一个实施方式中,所述标准品溶液中水杨苷、表儿茶素、4
‑
羟基苯乙酮、三七皂苷r1、人参皂苷rg1和人参皂苷rb1的浓度分别为21.8μg/ml、8.04μg/ml、6.66μg/ml、114.4μg/ml、408μg/ml、368μg/ml。
[0025]
根据本发明,所述构建方法中使用不同批次消痞和胃胶囊样品进行指纹图谱构建,所述不同批次至少为5个批次;更优选为至少10个批次。
[0026]
利用本发明提供的液相色谱指纹图谱构建方法得到消痞和胃胶囊的指纹图谱有17个共有特征峰,其中:3号峰为水杨苷、6号峰为表儿茶素、7号峰为4
‑
羟基苯乙酮、9号峰为三七皂苷r1、10号峰为人参皂苷rg1和12号峰为人参皂苷rb1。
[0027]
所述指纹图谱当以12号峰人参皂苷rb1的色谱峰为参照(s)时,17个共有特征峰的相对保留时间为:
[0028][0029][0030]
所述指纹图谱当以12号峰人参皂苷rb1的色谱峰为参照(s)时,各共有特征峰的相对峰面积为:
[0031][0032][0033]
根据本发明,所述消痞和胃胶囊的指纹图谱的构建方法或检测方法,包括以下步骤:
[0034]
(1)取水杨苷、表儿茶素、4
‑
羟基苯乙酮、三七皂苷r1、人参皂苷rg1和人参皂苷rb1为对照品,分别制成各对照品溶液,任选进一步制备6种标准品混合物的溶液;
[0035]
(2)取消痞和胃胶囊内容物,加入75%甲醇,水浴回流,经0.45μm微孔滤膜过滤,取续滤液作为供试品溶液;
[0036]
(3)分别吸取上述对照品溶液和供试品溶液各5μl,注入液相色谱仪进行测定,色谱条件如下:采用c18色谱柱(4.6mm
×
150mm,5μm);流动相a相(水相),b相为(乙腈);梯度洗脱流速为1.0ml
·
min
‑1;柱温30℃;检测波长为203nm,理论板数按人参皂苷rb1计算应不低于5000,得到不同批次消痞和胃胶囊色谱图、各对照品的色谱图,任选6种标准品混合物的色谱图;
[0037]
(4)生成指纹图谱:通过各对照品的色谱图与任选6种标准品混合物标准品色谱图指认色谱峰,以不同批次的消痞和胃胶囊的色谱图制作消痞和胃胶囊指纹图谱。
[0038]
在上述技术方案的基础上,根据本发明的消痞和胃胶囊指纹图谱的检测方法,依据前述hplc检测条件以及供试品溶液制备方法,将待测消痞和胃胶囊制成供试品溶液,进行hplc检测,将检测待测消痞和胃胶囊的指纹图谱与本发明构建的消痞和胃胶囊指纹图谱
进行比较,相对保留时间应在规定值的
±
5%之内为合格产品,与所述指纹图谱进行相似性评价,相似度大于0.8,优选大于0.90为合格产品。
[0039]
本发明还提供由本发明的指纹图谱构建方得到的消痞和胃胶囊的指纹图谱。所述指纹图谱基本如图2中b所示。
[0040]
本发明还提供所述消痞和胃胶囊指纹图谱构建方法和/或检测方法在消痞和胃胶囊质量控制中的应用。
[0041]
在本发明中,“任选”、“任选地”或“任选存在”是指随后描述的事件或情形可以但不一定出现,并且该描述包括其中所述事件或情形出现的情况和不出现的情况。
[0042]
在本发明中,“包含”和“包括”均为开放式表达,即包括本发明所指明的内容,但并不排除其他方面的内容。应当理解,“包含”和“包括”可以涵盖封闭式的含义,即“由
……
组成”。
[0043]
本发明的有益效果:
[0044]
中药指纹图谱主要用于评价中药材及其制剂质量的稳定性和重现性。本发明通过采用化学指纹图谱质控方法快速、直观地辨识消痞和胃胶囊的药效物质基础,共确定了17个共有峰,指认其中6个组分(水杨苷、表儿茶素、4
‑
羟基苯乙酮、三七皂苷r1、人参皂苷rg1和人参皂苷rb1),从而为消痞和胃胶囊全面质量标准的建立奠定基础。
[0045]
本发明通过比较不同提取溶剂甲醇、75%甲醇、50%甲醇和水;不同提取时间30min、1h和2h;不同提取方法超声提取和水浴回流提取,最终确定75%甲醇、水浴回流2h为优选的供试品溶液制备方法。
[0046]
本发明先后采用了symmetryshieldtmrp18(4.6mm
×
150mm,5μm)、diamon c18(2)(4.6mm
×
150mm,5μm)和c18色谱柱(4.6mm
×
150mm,5μm),结果发现在c18色谱柱(4.6mm
×
150mm,5μm)下分离得到的色谱图各组分的峰形较好,且具有较好的分离度。因而可作为后续研究优选的色谱柱。
[0047]
本发明通过分析10批消痞和胃胶囊,从而建立了消痞和胃胶囊的hplc指纹图谱测定方法,并对其质量进行了综合评价。通过精密度、重复性、稳定性实验,验证了本发明方法具有较高的稳定性和可信度,因而可作为消痞和胃胶囊指纹图谱的测定方法。
附图说明
[0048]
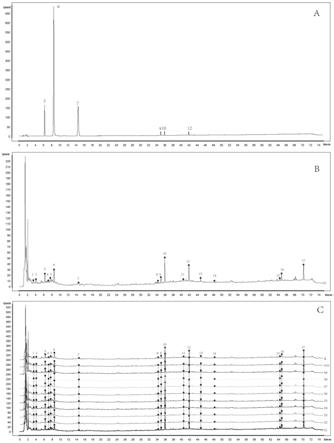
图1为不同色谱柱条件下获得的消痞和胃胶囊指纹图谱,图中a为symmetryshieldtmrp18色谱柱条件下消痞和胃胶囊指纹图谱;b为diamon c18(2)色谱柱条件下消痞和胃胶囊指纹图谱;c为c18色谱柱条件下消痞和胃胶囊指纹图谱。
[0049]
图2中a为混合对照品色谱图;图2中b为消痞和胃胶囊的指纹图谱;图2中c为10批次消痞和胃胶囊hplc指纹图谱叠加图。
具体实施方式
[0050]
下文将结合具体实施例对本发明的技术方案做更进一步的详细说明。应当理解,下列实施例仅为示例性地说明和解释本发明,而不应被解释为对本发明保护范围的限制。凡基于本发明上述内容所实现的技术均涵盖在本发明旨在保护的范围内。
[0051]
除非另有说明,以下实施例中使用的原料和试剂均为市售商品,或者可以通过已知方法制备。
[0052]
实施例1消痞和胃胶囊标准指纹图谱的建立
[0053]
1.仪器与材料
[0054]
1.1仪器
[0055]
高效液相色谱仪(型号:u3000,赛默飞世尔科技有限公司),电热恒温水浴锅(型号:hh
‑
s4a,北京科伟永兴仪器有限公司);xs105型电子天平(赛多利斯科学仪器(北京)有限公司);milli
‑
q超纯水纯化系统(北京五洲东方科技有限公司)。
[0056]
1.2材料
[0057]
水杨苷(纯度≥98%,批号y12s6s1,上海源叶生物科技有限公司),表儿茶素(纯度≥98%,批号110878
‑
201703,中国食品药品检定研究院),4
‑
羟基苯乙酮(纯度≥98%,批号t21j6c1,上海源叶生物科技有限公司),三七皂苷r1(纯度≥98%,批号110745
‑
201921,中国食品药品检定研究院),人参皂苷rg1(纯度≥98%,批号110703
‑
202034,中国食品药品检定研究院),人参皂苷rb1(纯度≥98%,批号110704
‑
202129,中国食品药品检定研究院);消痞和胃胶囊10批(批号s1
‑
s10),批号分别为20200702,20200701,20190102,20200104,20200105,20200201,20200601,20200603,20200604,20200602,来源贵州永乐药业有限公司;色谱纯乙腈;色谱纯甲醇;超纯水。
[0058]
2.方法与结果
[0059]
2.1色谱条件
[0060]
hplc指纹图谱分析条件采用c18色谱柱(4.6mm
×
150mm,5μm);流动相a相(水相),b相为(乙腈);梯度洗脱;流速为1.0ml
·
min
‑1;柱温30℃;进样量5μl,检测波长为203nm。
[0061]
表1梯度洗脱方法
[0062][0063][0064]
2.2对照品溶液制备
[0065]
分别取水杨苷、表儿茶素、4
‑
羟基苯乙酮、三七皂苷r1、人参皂苷rg1和人参皂苷rb1对照品,精密称定,加甲醇制成含有水杨苷21.8μg/ml,表儿茶素8.04μg/ml,4
‑
羟基苯乙酮6.66μg/ml,三七皂苷r1 114.4μg/ml,人参皂苷rg1408μg/ml和人参皂苷rb1 368μg/ml的混合对照品溶液。
[0066]
同时,分别取水杨苷、表儿茶素、4
‑
羟基苯乙酮、三七皂苷r1、人参皂苷rg1和人参皂苷rb1对照品,精密称定,分别加甲醇制成水杨苷21.8μg/ml,表儿茶素8.04μg/ml,4
‑
羟基苯乙酮6.66μg/ml,三七皂苷r1 114.4μg/ml,人参皂苷rg1 408μg/ml和人参皂苷rb1 368μg/ml的各对照品的单一溶液。
[0067]
2.3供试品溶液制备
[0068]
取消痞和胃胶囊内容物,混匀,精密称取细粉0.5g,置于具塞锥形瓶中,精密加入75%甲醇25ml,称定重量,水浴回流2h,放冷,称重,用75%甲醇补足重量,摇匀,经0.45μm微孔滤膜过滤,取续滤液即得。
[0069]
2.4消痞和胃胶囊hplc指纹图谱分析
[0070]
2.4.1精密度试验
[0071]
取同一批次(批号:20200702)的消痞和胃胶囊供试品,连续进样6次,记录各共有色谱峰的保留时间和峰面积,以12号峰人参皂苷rb1的保留时间与峰面积为参照,换算出各共有峰的相对保留时间和相对峰面积,以考察色谱峰的相对保留时间和相对峰面积比值的一致性。结果表明:各共有峰的相对保留时间rsd均小于1%,相对峰面积的rsd均小于2.7%,由此表明本发明的测定方法稳定、系统紧密度良好、方法稳定可靠。
[0072]
2.4.2稳定性试验
[0073]
取同一批次(批号:20200702)的消痞和胃胶囊供试品,在不同的时间点(0h、2h、4h、6h、8h、12h、24h)进样分析,记录各共有色谱峰的保留时间和峰面积,以12号峰人参皂苷rb1的保留时间与峰面积为参照,换算出各共有峰的相对保留时间和相对峰面积,以考察色谱峰的相对保留时间和相对峰面积比值的一致性。结果表明:各共有峰的相对保留时间rsd均小于1%,相对峰面积的rsd均小于2.74%。由此表明本发明的消痞和胃胶囊样品在实验条件下稳定性良好,在24h内能保证分析结果的可靠性。
[0074]
2.4.3重复性试验
[0075]
取同一批次(批号:20200702)的消痞和胃胶囊供试品,按照“2.3”项下方法平行制备6份供试品溶液,分别进样分析,并记录各共有色谱峰的保留时间和峰面积,以12号峰人参皂苷rb1的保留时间与峰面积为参照,换算出各共有峰的相对保留时间和相对峰面积,以考察色谱峰的相对保留时间和相对峰面积比值的一致性。由此表明:各共有峰的相对保留时间rsd均小于1%,相对峰面积的rsd均小于3.29%,由此表明本发明的方法稳定可靠,利于推广。
[0076]
2.4.4消痞和胃胶囊hplc指纹图谱的建立和相似度评价
[0077]
取10个批次的消痞和胃胶囊(批号:20200702,20200701,20190102,20200104,20200105,20200201,20200601,20200603,20200604,20200602),按照“2.3”项下的方法分别制备供试品溶液,并进样分析,分别记录色谱图。选择具有代表性的图谱(批号20200702的消痞和胃胶囊)为对照指纹图谱,采用药典委推荐的《中药色谱指纹图谱相似度评价系统》进行分析,以色谱图相似度(similarity)作为指纹图谱评价指标,采用多点校正全谱匹
配生成指纹图谱共有模式。各批次样品与对照指纹图谱的相似度分别为(0.999、0.999、0.999、0.996、0.999、0.994、0.998、0.998、0.999、0.993)。
[0078]
2.4.5指纹图谱中共有峰的指认,相对峰面积和相对保留时间的计算
[0079]
利用相似度评价系统软件处理,10批指纹图谱中共检测到17个峰。与混合对照品比对,标定出6个色谱峰,其中:3号峰为水杨苷、6号峰为表儿茶素、7号峰为4
‑
羟基苯乙酮、9号峰为三七皂苷r1、10号峰为人参皂苷rg1和12号峰为人参皂苷rb1。其保留时间分别为6.26min、8.52min、14.555min、34.968min、35.906min和41.963min。其中12号峰峰形较好,前后无杂质峰干扰,分离完全,因此被选作参考峰,用于计算其他共有峰的相对峰面积和相对保留时间,结果见下表2和表3。
[0080]
表2 10批样品(s1~s10)中17个共有峰的相对峰面积
[0081][0082]
表3 10批样品(s1~s10)中17个共有峰的相对保留时间
[0083]
[0084][0085]
以上,对本发明的实施方式进行了说明。但是,本发明不限定于上述实施方式。凡在本发明的精神和原则之内,所做的任何修改、等同替换、改进等,均应包含在本发明的保护范围之内。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。