1.本发明属于电池领域,具体涉及一种锰离子电池。
背景技术:
2.在已报道的电池中,锂离子电池是通过单电子反应提供能量,其理论比容量较低。以嵌入/脱出反应为主的锌离子、钠离子、钾离子、镁离子等电池,放电时,电解液中的金属阳离子(如li
、zn
2
、na
等)嵌入正极材料;在充电时,嵌入正极的金属阳离子进入电解液,嵌入/脱出反应占据主导地位,从而提供电池容量。因金属离子尺寸较大,正极结构不稳定,嵌入/脱出反应困难,导致循环稳定性较差,能量密度较低。
3.因此,现有的电池有待改进。
技术实现要素:
4.本发明旨在至少在一定程度上解决相关技术中的技术问题之一。为此,本发明的一个目的在于提出一种锰离子电池,该锰离子电池循环寿命长、比能量高且安全性高。
5.本发明提出了一种锰离子电池,根据本发明的实施例,所述锰离子电池的正极包括锰基化合物和导电基底材料中的至少之一,负极包括锌、锡、镍、锰、锂、钠、铝、钛和碳材料中的至少之一,电解液包括mn
2
和/或所述负极对应金属的阳离子,其中,在充电过程,所述电解液中的mn
2
失去电子被氧化为二氧化锰沉积在所述正极上;在放电过程,所述正极上的锰得到电子被还原成mn
2
溶解在所述电解液中。
6.根据本发明实施例的锰离子电池,该锰离子电池的正极包括锰基化合物和导电基底材料中的至少之一,负极包括锌、锡、镍、锰、锂、钠、铝、钛和碳材料中的至少之一,电解液包括mn
2
和/或所述负极对应金属的阳离子。该锰离子电池放电时,一方面,正极侧发生的反应为:(1)当正极为锰基化合物时,正极一定发生的反应为锰基化合物中的部分高价态锰被还原成mn
2
,发生溶解反应进入电解液,或者通过电解液进入负极,同时可能伴随发生的反应为电解液中的负极提供的阳离子以嵌入反应、表面反应或其他反应的形式与正极锰基化合物结合(几个反应可能同时发生,或只发生其一),此外还可能伴随有质子反应,即电解液解离的氢质子(h
)嵌入正极;(2)当正极为导电基底材料时,由于充电时电解液中的mn
2
在阳极(即放电时的正极)被氧化为锰基化合物,锰基化合物覆盖在导电基底材料表面,此时导电基底材料正极相当于锰基化合物正极,后续发生的发生与正极为锰基化合物的反应一致。另一方面,负极材料的标准电极电位较低,锌、锡、镍、锰、锂、钠、铝、钛和碳材料中的至少之一在该锰离子电池的负极侧被氧化成阳离子态溶进电解液,同时,可能伴随发生的反应为电解液中的mn
2
以沉积、嵌入、螯合或者表面反应的方式进入负极;该锰离子电池充电时,发生的反应过程与上述充电过程相反,锰基化合物中锰的溶解反应占据主导地位。由此,该锰离子电池在充放电循环过程中,每次充电过程都会有新的沉积正极活性物质即锰基化合物和负极活性物质即锌、锡、镍、锰、锂、钠、铝、钛和碳材料中的至少之一生成,再在随后的放电过程重新溶解到电解液中,该反应过程稳定高效,因此该锰离子电池具有很长
的循环寿命,而且由于正负极的溶解沉积反应均发生在电极表面,不受离子在电极晶体结构内部扩散的控制,因此具有很高的功率密度和安全性。总之,该锰离子电池循环寿命长、比能量高且安全性高。
7.另外,根据本发明上述实施例的锰离子电池还可以具有如下附加的技术特征:
8.在本发明的一些实施例中,所述锰基化合物包括锰基氧化物、锰盐和锰羟基氧化物中的至少之一。由此,可以提高该锰离子电池循环寿命、比能量和安全性。
9.在本发明的一些实施例中,所述锰基氧化物包括α
‑
mno2、β
‑
mno2、δ
‑
mno2、ε
‑
mno2和γ
‑
mno2中的至少之一。由此,可以提高该锰离子电池循环寿命、比能量和安全性。
10.在本发明的一些实施例中,所述正极为导电基底材料,所述电解液至少包括mn
2
。由此,可以提高该锰离子电池循环寿命、比能量和安全性。
11.在本发明的一些实施例中,所述导电基底材料的厚度为0.1~20mm。由此,可以提高该锰离子电池循环寿命、比能量和安全性。
12.在本发明的一些实施例中,所述导电基底材料包括碳毡、碳纸、碳布、石墨毡、石墨板和石墨网中的至少之一。
13.在本发明的一些实施例中,所述负极的锌、锡、镍、锰、锂、钠、铝和钛以金属单质、合金、氧化物和螯合物中的至少一种形式提供。
14.在本发明的一些实施例中,所述负极为包括碳材料和选自锌、锡、镍、锰、锂、钠、铝和钛中的至少之一组成的合金。在本发明的一些实施例中,所述负极的碳材料包括石墨烯、介孔碳、碳纳米管、乙炔黑、石墨和炭黑中的至少之一。
15.在本发明的一些实施例中,其中,所述mn
2
的浓度为0~20mol/l,所述负极对应金属阳离子的浓度为0.01~20mol/l。由此,可以提高该锰离子电池循环寿命、比能量和安全性。
16.本发明的附加方面和优点将在下面的描述中部分给出,部分将从下面的描述中变得明显,或通过本发明的实践了解到。
附图说明
17.本发明的上述和/或附加的方面和优点从结合下面附图对实施例的描述中将变得明显和容易理解,其中:
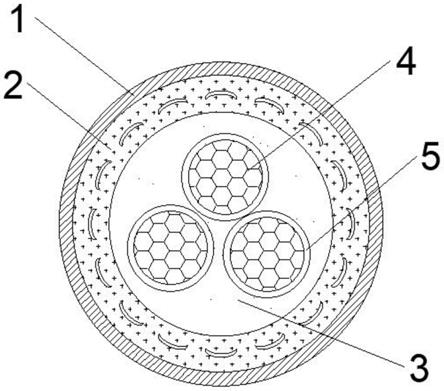
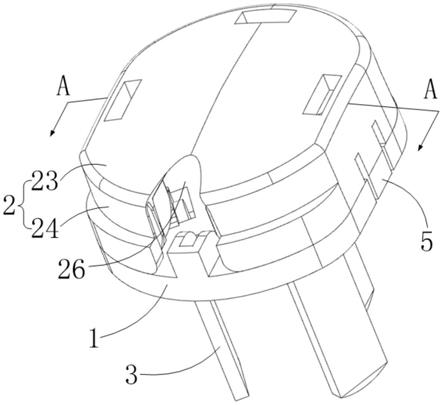
18.图1是根据本发明的一个实施例的锰离子电池放电时的工作原理图(以正极为锰基氧化物、负极为金属m为例);
19.图2是实施例1的正极片表面沉积层的sem图。
具体实施方式
20.下面详细描述本发明的实施例,旨在用于解释本发明,而不能理解为对本发明的限制。
21.本发明提出了一种锰离子电池,该锰离子电池的正极包括锰基化合物和导电基底材料中的至少之一,负极包括锌、锡、镍、锰、锂、钠、铝、钛和碳材料中的至少之一,电解液包括mn
2
和/或负极对应金属的阳离子,其中,在充电过程,电解液中的mn
2
失去电子被氧化为二氧化锰沉积在正极上;在放电过程,正极上的锰得到电子被还原成mn
2
溶解在电解液中。
22.发明人发现,该锰离子电池的正极包括锰基化合物和导电基底材料中的至少之一,负极包括锌、锡、镍、锰、锂、钠、铝、钛和碳材料中的至少之一,电解液包括mn
2
和/或所述负极对应金属的阳离子。参考图1,该锰离子电池放电时,一方面,正极侧发生的反应为:(1)当正极为锰基化合物时,正极一定发生的反应为锰基化合物中的部分高价态锰被还原成mn
2
,发生溶解反应进入电解液,或者通过电解液进入负极,同时可能伴随发生的反应为电解液中的负极提供的阳离子以嵌入反应、表面反应或其他反应的形式与正极锰基化合物结合(几个反应可能同时发生,或只发生其一),此外还可能伴随有质子反应,即电解液解离的氢质子(h
)嵌入正极;(2)当正极为导电基底材料时,由于充电时电解液中的mn
2
在阳极(即放电时的正极)被氧化为锰基化合物,锰基化合物覆盖在导电基底材料表面,此时导电基底材料正极相当于锰基化合物正极,后续发生的发生与正极为锰基化合物的反应一致。另一方面,负极材料的标准电极电位较低,锌、锡、镍、锰、锂、钠、铝、钛和碳材料中的至少之一在该锰离子电池的负极侧被氧化成阳离子态溶进电解液,同时,可能伴随发生的反应为电解液中的mn
2
以沉积、嵌入、螯合或者表面反应的方式进入负极;该锰离子电池充电时,发生的反应过程与上述充电过程相反,锰基化合物中锰的溶解反应占据主导地位。由此,该锰离子电池在充放电循环过程中,每次充电过程都会有新的沉积正极活性物质即锰基化合物和负极活性物质即锌、锡、镍、锰、锂、钠、铝、钛和碳材料中的至少之一生成,再在随后的放电过程重新溶解到电解液中,该反应过程稳定高效,因此该锰离子电池具有很长的循环寿命,而且由于正负极的溶解沉积反应均发生在电极表面,不受离子在电极晶体结构内部扩散的控制,因此具有很高的功率密度和安全性。总之,该锰离子电池循环寿命长、比能量高、安全性高。
23.需要说明的是,上述锰基化合物的类型并不受特别限制,锰基化合物可以选择锰基氧化物、锰盐和锰羟基氧化物中的至少之一,优选为锰基氧化物,例如,mno2、mnco3、mn2o3、mn3o4、mnooh,更优选为各种晶型的mno2,包括α
‑
mno2、β
‑
mno2、δ
‑
mno2、ε
‑
mno2、和γ
‑
mno2中的至少之一。发明人发现,当正极材料为锰基化合物时,在放电过程中,正极一定发生的反应为锰基化合物中的部分高价态锰被还原成mn
2
,发生溶解反应进入电解液,或者通过电解液进入负极,同时可能伴随发生的反应为电解液中的负极提供的阳离子以嵌入反应、表面反应或其他反应的形式与正极锰基化合物结合(几个反应可能同时发生,或只发生其一),此外还可能伴随有质子反应,即电解液解离的氢质子(h
)嵌入正极。
24.需要说明的是,上述导电基底材料的类型也不受特别限制,导电基底材料可以选择碳毡、碳纸、碳布、石墨毡、石墨板和石墨网中的至少之一。发明人发现,当正极为导电基底材料时,在放电过程中,由于充电时电解液中的mn
2
在阳极(即放电时的正极)被氧化为锰基化合物,锰基化合物覆盖在导电基底材料表面,此时导电基底材料正极相当于锰基化合物正极,后续发生的发生与当正极为锰基化合物的反应一致。具体地,导电基底材料的厚度为0.1~20mm。发明人发现,当导电基底的厚度过大,mn
2
趋于在表面沉积,导致沉积物在导电基底上分布不均匀,影响电池倍率性能,并且,导电基底厚度过大,会影响电池的能量密度;当导电基底的厚度过小,mn
2
没有足够多的活性位点进行沉积,导致电池容量受损。
25.进一步地,当正极为导电基底材料时,电解液至少包括mn
2
,mn
2
的浓度为0.01~20mol/l。发明人发现,当mn
2
的浓度过高时,会导致表面沉积层过于致密,在放电时会影响正极片内部的mn
2
溶出,从而影响电池的容量;当mn
2
的浓度过低时,电解液的离子导电率
变低,且正极极片中过多的mn
2
被溶解,从而影响电池的倍率性能及循环性能。
26.进一步地,负极的锌、锡、镍、锰、锂、钠、铝和钛以金属单质、合金、氧化物和螯合物中的至少一种形式提供。负极的碳材料包括石墨烯、介孔碳、碳纳米管、乙炔黑、石墨和炭黑中的至少之一。根据本发明的一些实施例,负极可以为包括碳材料和选自锌、锡、镍、锰、锂、钠、铝和钛中的至少之一组成的合金。具体的,在放电过程中,负极材料的标准电极电位较低,锌、锡、镍、锰、锂、钠、铝、钛和碳材料中的至少之一在该锰离子电池的负极侧被氧化成阳离子态溶进电解液,同时,可能伴随发生的反应为电解液中的mn
2
以沉积、嵌入、螯合或者表面反应的方式进入负极。
27.进一步地,电解液包括mn
2
和负极对应金属的阳离子,其中,mn
2
的浓度为0~20mol/l,优选0.01~20mol/l,负极对应金属阳离子的浓度为0.01~20mol/l。发明人发现,当mn
2
的浓度过高时,会导致表面沉积层过于致密,在放电时会影响正极片内部的mn
2
溶出,从而影响电池的容量;当mn
2
的浓度过低时,电解液的离子导电率变低,且正极极片中过多的mn
2
被溶解,从而影响电池的倍率性能及循环性能。此外,当负极对应金属阳离子的浓度过高时,会导致过多的金属阳离子以嵌入、表面反应或者其他反应的形式,与正极锰基化合物结合,容易造成正极锰基化合物结构坍塌,影响电池的循环性能;当负极对应金属阳离子的浓度过低时,电解液的离子导电率变低,且易造成负极极片发生穿孔、腐蚀等不利于电池寿命的现象。
28.下面参考具体实施例,对本发明进行描述,需要说明的是,这些实施例仅仅是描述性的,而不以任何方式限制本发明。
29.实施例1
30.电池组装:mno2作正极,金属锌作负极,隔膜为agm隔膜。电解液:zn
2
浓度为1.0mol/l,mn
2
浓度为0.2mol/l;
31.电池测试:25℃环境,电池在50ma/g电流密度下,该体系电池循环100圈,克容量为204.6mah/g,容量保持率为93.5%。
32.验证mn
2
沉积/溶解反应占据主导的方法:
33.经过前4次充放电活化后,对电池的第5次充电和放电过程以电压为截点,进行拆解,通过icp对电解液中zn
2
和mn
2
的浓度进行检测,通过mn
2
的浓度差,可以计算出mn
2
沉积或者溶解的质量,再根据mn
2
/mn的电化学当量,计算出mn反应所提供的容量,通过测试设备读取总的容量,即可得出mn反应的容量占比。另外,对循环100圈后的正极片的表面进行扫描电镜拍摄,如图2所示,表面沉积层为mno2。
34.图1
[0035][0036][0037]
结果显示:在充电过程中,电解液中mn
2
浓度逐渐降低,表明电解液中的mn
2
正在正极发生沉积反应,沉积反应所提供的容量占总充电容量的74.0%;在放电过程中,电解液中的mn
2
浓度逐渐升高,表明正极中mn发生溶解反应,溶解反应所提供的容量占总充电容量的79.1%。
[0038]
实施例2
[0039]
电池组装:以厚度为0.4mm的石墨毡为正极基底,金属锌作负极,隔膜为agm隔膜。电解液:zn
2
浓度为1.0mol/l,mn
2
浓度为0.4mol/l;
[0040]
电池测试:25℃环境,电池在2ma/cm2电流密度下,该体系电池循环100圈,面容量为6.51mah/cm2,容量保持率为91.2%。
[0041]
mn沉积/溶解反应的容量占比:在第5圈时,沉积反应所提供的容量占总充电容量的84%,溶解反应所提供的容量占总充电容量的81.5%。
[0042]
实施例3
[0043]
将负极更换为sno2/c,电解液:sn
2
浓度为1.0mol/l,mn
2
浓度为0.2mol/l;其他同实施例1。
[0044]
该体系电池循环100圈,克容量为199.2mah/g,容量保持率为92.7%。
[0045]
mn沉积/溶解反应的容量占比:在第5圈时,沉积反应所提供的容量占总充电容量
的83.6%,溶解反应所提供的容量占总充电容量的81.9%。
[0046]
实施例4
[0047]
将负极更换为ni,电解液:ni
2
浓度为1.0mol/l,mn
2
浓度为0.2mol/l;其他同实施例1。
[0048]
该体系电池循环100圈,克容量为180.8mah/g,容量保持率为87.0%。
[0049]
mn沉积/溶解反应的容量占比:在第5圈时,沉积反应所提供的容量占总充电容量的72.2%,溶解反应所提供的容量占总充电容量的74.2%。
[0050]
实施例5
[0051]
将负极更换为li,电解液:li
浓度为1.0mol/l,mn
2
浓度为0.2mol/l;其他同实施例1。
[0052]
该体系电池循环100圈,克容量为246.2mah/g,容量保持率为89.2%。
[0053]
mn沉积/溶解反应的容量占比:在第5圈时,沉积反应所提供的容量占总充电容量的75.9%,溶解反应所提供的容量占总充电容量的80.7%。
[0054]
实施例6
[0055]
将负极更换为mn,电解液:mn
2
浓度为1.2mol/l;其他同实施例1。
[0056]
该体系电池循环100圈,克容量为200.3mah/g,容量保持率为96.2%。
[0057]
mn沉积/溶解反应的容量占比:在第5圈时,沉积反应所提供的容量占总充电容量的100%,溶解反应所提供的容量占总充电容量的100%。
[0058]
实施例7
[0059]
将负极更换为锡锌合金,电解液:sn
2
浓度为0.5mol/l,zn
2
浓度为0.5mol/l,mn
2
浓度为0.2mol/l;其他同实施例1。
[0060]
该体系电池循环100圈,克容量为188.9mah/g,容量保持率为91.1%。
[0061]
mn沉积/溶解反应的容量占比:在第5圈时,沉积反应所提供的容量占总充电容量的69.3%,溶解反应所提供的容量占总充电容量的75.3%。
[0062]
实施例8
[0063]
将负极更换为石墨烯,电解液:mn
2
浓度为1.2mol/l;其他同实施例1。
[0064]
该体系电池循环100圈,克容量为155.3mah/g,容量保持率为91.2%。
[0065]
mn沉积/溶解反应的容量占比:在第5圈时,沉积反应所提供的容量占总充电容量的100%,溶解反应所提供的容量占总充电容量的100%。
[0066]
实施例9
[0067]
将负极更换为能螯合mn
2
的高分子螯合物及导电碳材料复合物:螯合物为二乙烯三胺
‑
mn,电解液为:1.2mol/l的mn
2
。其他同实施例1。
[0068]
该体系电池循环100圈,克容量为198.6mah/g,容量保持率为94.2%。
[0069]
mn沉积/溶解反应的容量占比:在第5圈时,沉积反应所提供的容量占总充电容量的100%,溶解反应所提供的容量占总充电容量的100%。
[0070]
实施例10
[0071]
将负极更换为na,电解液为:1.0mol/l的na
,0.2mol/l的mn
2
。其他同实施例1。
[0072]
该体系电池循环100圈,克容量为195.6mah/g,容量保持率为94.1%。
[0073]
mn沉积/溶解反应的容量占比:在第5圈时,沉积反应所提供的容量占总充电容量
的72.3%,溶解反应所提供的容量占总充电容量的76.8%。
[0074]
实施例11
[0075]
将负极更换为al,电解液为:1.0mol/l的al
3
,0.2mol/l的mn
2
。其他同实施例1。
[0076]
该体系电池循环100圈,克容量为198.0mah/g,容量保持率为90.7%。
[0077]
mn沉积/溶解反应的容量占比:在第5圈时,沉积反应所提供的容量占总充电容量的78.4%,溶解反应所提供的容量占总充电容量的80.1%。
[0078]
实施例12
[0079]
将负极更换为ti,电解液为:1.0mol/l的ti
4
,0.2mol/l的mn
2
。其他同实施例1。
[0080]
该体系电池循环100圈,克容量为201.9mah/g,容量保持率为94.0%。
[0081]
mn沉积/溶解反应的容量占比:在第5圈时,沉积反应所提供的容量占总充电容量的80.7%,溶解反应所提供的容量占总充电容量的82.5%。
[0082]
对比例1
[0083]
将负极更换为金属cu,电解液:cu
2
浓度为1.0mol/l,mn
2
浓度为0.2mol/l;其他同实施例1。
[0084]
该体系电池循环100圈,克容量为193.0mah/g,容量保持率为88.2%。
[0085]
mn沉积/溶解反应的容量占比:在第5圈时,沉积反应所提供的容量占总充电容量的82.3%,溶解反应所提供的容量占总充电容量的80.1%。
[0086]
对比例2
[0087]
将负极更换为金属pb,电解液:pb
2
浓度为1.0mol/l,mn
2
浓度为0.2mol/l;其他同实施例1。
[0088]
该体系电池循环100圈,克容量为189.6mah/g,容量保持率为84.9%。
[0089]
mn沉积/溶解反应的容量占比:在第5圈时,沉积反应所提供的容量占总充电容量的71.2%,溶解反应所提供的容量占总充电容量的76.6%。
[0090]
图2
[0091]
[0092][0093]
在本说明书的描述中,参考术语“一个实施例”、“一些实施例”、“示例”、“具体示例”、或“一些示例”等的描述意指结合该实施例或示例描述的具体特征、结构、材料或者特点包含于本发明的至少一个实施例或示例中。在本说明书中,对上述术语的示意性表述不必须针对的是相同的实施例或示例。而且,描述的具体特征、结构、材料或者特点可以在任一个或多个实施例或示例中以合适的方式结合。此外,在不相互矛盾的情况下,本领域的技术人员可以将本说明书中描述的不同实施例或示例以及不同实施例或示例的特征进行结合和组合。
[0094]
尽管上面已经示出和描述了本发明的实施例,可以理解的是,上述实施例是示例性的,不能理解为对本发明的限制,本领域的普通技术人员在本发明的范围内可以对上述实施例进行变化、修改、替换和变型。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。