含有非天然氨基酸连接的海兔毒素衍生物的组合物、涉及该海兔毒素衍生物的方法及其用途
1.交叉引用
2.本技术是申请号为201811251863.0的中国发明专利申请(其申请日为2012年5月24日,发明名称为“含有非天然氨基酸连接的海兔毒素衍生物”)的分案申请,该中国专利申请是申请号为201280036296.1的中国发明专利申请(其申请日为2012年5月24日,发明名称为“含有非天然氨基酸连接的海兔毒素衍生物的组合物、涉及该海兔毒素衍生物的方法及其用途”)的分案申请,原申请为国际申请号为pct/us2012/039472的中国国家阶段申请,该申请主张2011年5月27日提交的名称是“含有非天然氨基酸连接的海兔毒素衍生物的组合物、涉及其的方法以及其用途(compositions containing,methods involving,and uses of non
‑
natural amino acid linked dolastatin derivatives)”的美国临时申请案第61/491,146号的优先权,所述专利的内容以全文引用的方式并入本文中。
技术领域
3.本发明涉及含有非天然氨基酸连接的海兔毒素衍生物的组合物、其的方法以及其用途。
背景技术:
4.将非基因编码的氨基酸(即,“非天然氨基酸”)并入蛋白质中的能力允许引入可提供天然存在的官能团(如赖氨酸的ε
‑
nh2、半胱氨酸的巯基
‑
sh、组氨酸的亚氨基等)的有价值替代物的化学官能团。已知某些化学官能团对20种常见的基因编码的氨基酸中所见的官能团呈惰性,但完全并且有效地与可并入于非天然氨基酸上的官能团反应形成稳定键。
5.方法现可用于选择性引入未见于蛋白质中、对20种常见的基因编码的氨基酸中所见的所有官能团呈化学惰性并且可用于与包含某些官能团的试剂有效并且选择性地反应形成稳定共价键的化学官能团。
技术实现要素:
6.本文披露具有一个或一个以上连接基团的毒性部分,连接于非天然氨基酸的毒性基团,以及制造所述非天然氨基酸和多肽的方法。
7.本发明的一些实施例描述一种化合物或其盐,包含式(i):
[0008][0009]
其中:
[0010]
z具有以下结构:
[0011][0012]
r5是h、cor8、c1‑
c6烷基或噻唑;
[0013]
r8是oh或
‑
nh
‑
(亚烷基
‑
o)
n
‑
nh2;
[0014]
r6是oh或h;
[0015]
ar是苯基或吡啶;
[0016]
r7是c1‑
c6烷基或氢;
[0017]
y是选自由以下组成的群组:羟胺、甲基、醛、经保护的醛、酮、经保护的酮、硫酯、酯、二羰基、肼、脒、亚胺、二胺、叠氮化物、酮
‑
胺、酮
‑
炔烃、炔烃、环炔烃以及烯
‑
二酮;
[0018]
l是选自由以下组成的群组的连接基团:
‑
亚烷基
‑
、
‑
亚烷基
‑
c(o)
‑
、
‑
(亚烷基
‑
o)
n
‑
亚烷基
‑
、
‑
(亚烷基
‑
o)
n
‑
亚烷基
‑
c(o)
‑
、
‑
(亚烷基
‑
o)
n
‑
(ch2)
n'
‑
nhc(o)
‑
(ch2)
n”‑
c(me)2‑
s
‑
s
‑
(ch2)
n”'
‑
nhc(o)
‑
(亚烷基
‑
o)
n
””
‑
亚烷基
‑
、
‑
(亚烷基
‑
o)
n
‑
亚烷基
‑
w
‑
、
‑
亚烷基
‑
c(o)
‑
w
‑
、
‑
(亚烷基
‑
o)
n
‑
亚烷基
‑
u
‑
亚烷基
‑
c(o)
‑
以及
‑
(亚烷基
‑
o)
n
‑
亚烷基
‑
u
‑
亚烷基
‑
;
[0019]
w具有以下结构:
[0020][0021]
u具有以下结构:
[0022][0023]
或l不存在,y是甲基,r5是cor8,并且r8是
‑
nh
‑
(亚烷基
‑
o)
n
‑
nh2;并且
[0024]
n、n'、n"、n'"以及n""各自独立地是大于或等于1的整数。
[0025]
在一些实施例中,r5是噻唑。在其它实施例中,r6是h。在某些实施例中,ar是苯基。在另外的或附加的实施例中,r7是甲基。在一些实施例中,n是0到20、0到10或0到5的整数。
[0026]
在一些实施例中,描述一种化合物,包含式(ii):
[0027][0028]
在某些实施例中,l是
‑
(亚烷基
‑
o)
n
‑
亚烷基
‑
。在特定实施例中,每个亚烷基是
‑
ch2ch2‑
,n等于3,并且r7是甲基。在其它实施例中,l是
‑
亚烷基
‑
。在特定实施例中,每个亚烷基是
‑
ch2ch2‑
并且r7是甲基或氢。在某些实施例中,l是
‑
(亚烷基
‑
o)
n
‑
亚烷基
‑
c(o)
‑
。在某些特定实施例中,每个亚烷基是
‑
ch2ch2‑
,n等于4,并且r7是甲基。在另外的或替代实施例中,l是
‑
(亚烷基
‑
o)
n
‑
(ch2)
n'
‑
nhc(o)
‑
(ch2)
n”‑
c(me)2‑
s
‑
s
‑
(ch2)
n”'
‑
nhc(o)
‑
(亚烷基
‑
o)
n
””
‑
亚烷基
‑
。在特定实施例中,每个亚烷基是
‑
ch2ch2‑
,n等于1,n'等于2,n"等于1,n'"等于2,n""等于4,并且r7是甲基。
[0029]
在一些实施例中,y是叠氮化物。在其它实施例中,y是环辛炔。在特定实施例中,所述环辛炔具有以下结构:
[0030][0031]
每个r
19
独立地选自由以下组成的群组:c1‑
c6烷基、c1‑
c6烷氧基、酯、醚、硫醚、氨基烷基、卤素、烷基酯、芳基酯、酰胺、芳基酰胺、烷基卤化物、烷基胺、烷基磺酸、烷基硝基、硫酯、磺酰基酯、卤磺酰基、腈、烷基腈以及硝基;并且
[0032]
q是0、1、2、3、4、5、6、7、8、9、10或11。
[0033]
本发明的一些实施例描述一种化合物或其盐,包含式(iii)、(iv)、(v)或(vi):
[0034]
[0035][0036]
其中:
[0037]
z具有以下结构:
[0038][0039]
r5是h、cor8、c1‑
c6烷基或噻唑;
[0040]
r8是oh;
[0041]
r6是oh或h;
[0042]
ar是苯基或吡啶;
[0043]
r7是c1‑
c6烷基或氢;
[0044]
y和v各自选自由以下组成的群组:羟胺、甲基、醛、经保护的醛、酮、经保护的酮、硫酯、酯、二羰基、肼、脒、亚胺、二胺、叠氮化物、酮
‑
胺、酮
‑
炔烃、炔烃、环炔烃以及烯
‑
二酮;
[0045]
l1、l2、l3以及l4各自是独立地选自由以下组成的群组的连接基团:一键、
‑
亚烷基
‑
、
‑
(亚烷基
‑
o)
n
‑
亚烷基
‑
j
‑
、
‑
亚烷基'
‑
j
‑
(亚烷基
‑
o)
n
‑
亚烷基
‑
、
‑
j
‑
(亚烷基
‑
o)
n
‑
亚烷基
‑
、
‑
(亚烷基
‑
o)
n
‑
亚烷基
‑
j
‑
(亚烷基
‑
o)
n
'
‑
亚烷基
‑
j'
‑
、
‑
(亚烷基
‑
o)
n
‑
亚烷基
‑
j
‑
亚烷基'
‑
、
‑
w
‑
、
‑
亚烷基
‑
w
‑
、亚烷基'
‑
j
‑
(亚烷基
‑
nme)
n
‑
亚烷基
‑
w
‑
、
‑
j
‑
(亚烷基
‑
nme)
n
‑
亚烷基
‑
w
‑
、
‑
j
‑
亚烷基
‑
nme
‑
亚烷基'
‑
nme
‑
亚烷基"
‑
w
‑
以及
‑
亚烷基
‑
j
‑
亚烷基'
‑
nme
‑
亚烷基"
‑
nme
‑
亚烷基'"
‑
w
‑
;
[0046]
w具有以下结构:
[0047][0048]
j和j'各自独立地具有以下结构:
[0049]
并且
[0050]
n和n'各自独立地是大于或等于1的整数。
[0051]
在某些实施例中,描述一种化合物,包含式(vii):
[0052][0053]
在某些实施例中,l1是
‑
(亚烷基
‑
o)
n
‑
亚烷基
‑
j
‑
,l2是
‑
亚烷基'
‑
j'
‑
(亚烷基
‑
o)
n
'
‑
亚烷基
‑
,l3是
‑
j"
‑
(亚烷基
‑
o)
n
"
‑
亚烷基
‑
,亚烷基是
‑
ch2ch2‑
,亚烷基'是
‑
(ch2)4‑
,n是1,n'和n"是3,j具有结构j'和j"具有结构并且r7是甲基。在其它实施例中,l1是
‑
j
‑
(亚烷基
‑
o)
n
‑
亚烷基
‑
,l2是
‑
(亚烷基
‑
o)
n'
‑
亚烷基
‑
j'
‑
亚烷基'
‑
,l3是
‑
(亚烷基
‑
o)
n”‑
亚烷基
‑
j"
‑
,亚烷基是
‑
ch2ch2‑
,亚烷基'是
‑
(ch2)4‑
,n是1,n'和n"是4,并且j、j'以及j"具有结构
[0054]
在一些实施例中,y是叠氮化物。在其它实施例中,y是环辛炔。在特定实施例中,所述环辛炔具有以下结构:
[0055][0056]
每个r
19
独立地选自由以下组成的群组:c1‑
c6烷基、c1‑
c6烷氧基、酯、醚、硫醚、氨基烷基、卤素、烷基酯、芳基酯、酰胺、芳基酰胺、烷基卤化物、烷基胺、烷基磺酸、烷基硝基、硫酯、磺酰基酯、卤磺酰基、腈、烷基腈以及硝基;并且
[0057]
q是0、1、2、3、4、5、6、7、8、9、10或11。
[0058]
本发明的某些实施例描述一种化合物,包含式(viii)或(ix):
[0059][0060]
其中:
[0061]
a是任选的,并且当存在时是低碳亚烷基、经取代的低碳亚烷基、低碳亚环烷基、经取代的低碳亚环烷基、低碳亚烯基、经取代的低碳亚烯基、亚炔基、低碳亚杂烷基、经取代的亚杂烷基、低碳亚杂环烷基、经取代的低碳亚杂环烷基、亚芳基、经取代的亚芳基、亚杂芳基、经取代的亚杂芳基、亚烷芳基、经取代的亚烷芳基、亚芳烷基或经取代的亚芳烷基;
[0062]
b是任选的,并且当存在时是选自由以下组成的群组的连接基团:低碳亚烷基、经取代的低碳亚烷基、低碳亚烯基、经取代的低碳亚烯基、低碳亚杂烷基、经取代的低碳亚杂烷基、
‑
o
‑
、
‑
o
‑
(亚烷基或经取代的亚烷基)
‑
、
‑
s
‑
、
‑
s
‑
(亚烷基或经取代的亚烷基)
‑
、
‑
s(o)
k
‑
(其中k是1、2或3)、
‑
s(o)
k
(亚烷基或经取代的亚烷基)
‑
、
‑
c(o)
‑
、
‑
c(o)
‑
(亚烷基或经取代的亚烷基)
‑
、
‑
c(s)
‑
、
‑
c(s)
‑
(亚烷基或经取代的亚烷基)
‑
、
‑
n(r')
‑
、
‑
nr'
‑
(亚烷基或经取代的亚烷基)
‑
、
‑
c(o)n(r')
‑
、
‑
con(r')
‑
(亚烷基或经取代的亚烷基)
‑
、
‑
csn(r')
‑
、
‑
csn(r')
‑
(亚烷基或经取代的亚烷基)
‑
、
‑
n(r')co
‑
(亚烷基或经取代的亚烷基)
‑
、
‑
n(r')c(o)o
‑
、
‑
s(o)
k
n(r')
‑
、
‑
n(r')c(o)n(r')
‑
、
‑
n(r')c(s)n(r')
‑
、
‑
n(r')s(o)
k
n(r')
‑
、
‑
n(r')
‑
n=、
‑
c(r')=n
‑
、
‑
c(r')=n
‑
n(r')
‑
、
‑
c(r')=n
‑
n=、
‑
c(r')2‑
n=n
‑
以及
‑
c(r')2‑
n(r')
‑
n
(r')
‑
,其中每个r'独立地是h、烷基或经取代的烷基;
[0063]
r是h、烷基、经取代的烷基、环烷基或经取代的环烷基;
[0064]
r1是h、氨基保护基、树脂、至少一个氨基酸、多肽或多核苷酸;
[0065]
r2是oh、酯保护基、树脂、至少一个氨基酸、多肽或多核苷酸;
[0066]
r3和r4各自独立地是h、卤素、低碳烷基或经取代的低碳烷基,或r3和r4或两个r3基团任选地形成环烷基或杂环烷基;
[0067]
z具有以下结构:
[0068][0069]
r5是h、co2h、c1‑
c6烷基或噻唑;
[0070]
r6是oh或h;
[0071]
ar是苯基或吡啶;
[0072]
r7是c1‑
c6烷基或氢;
[0073]
l是选自由以下组成的群组的连接基团:
‑
亚烷基
‑
、
‑
亚烷基
‑
c(o)
‑
、
‑
(亚烷基
‑
o)
n
‑
亚烷基
‑
、
‑
(亚烷基
‑
o)
n
‑
亚烷基
‑
c(o)
‑
、
‑
(亚烷基
‑
o)
n
‑
(ch2)
n'
‑
nhc(o)
‑
(ch2)
n”‑
c(me)2‑
s
‑
s
‑
(ch2)
n”'
‑
nhc(o)
‑
(亚烷基
‑
o)
n
””
‑
亚烷基
‑
、
‑
(亚烷基
‑
o)
n
‑
亚烷基
‑
w
‑
、
‑
亚烷基
‑
c(o)
‑
w
‑
、
‑
(亚烷基
‑
o)
n
‑
亚烷基
‑
u
‑
亚烷基
‑
c(o)
‑
以及
‑
(亚烷基
‑
o)
n
‑
亚烷基
‑
u
‑
亚烷基
‑
;
[0074]
w具有以下结构:
[0075][0076]
u具有以下结构:
[0077]
并且
[0078]
n、n'、n"、n'"以及n""各自独立地是大于或等于1的整数;
[0079]
或其活性代谢物或医药学上可接受的前药或溶剂化物。
[0080]
在一些实施例中,r1是多肽。在特定实施例中,所述多肽是抗体。在某些特定实施例中,所述抗体是赫赛汀。在其它实施例中,r2是多肽。在特定实施例中,所述多肽是抗体。在某些特定实施例中,所述抗体是赫赛汀。
[0081]
本发明的一些实施例描述一种化合物或其盐,包含式(x)、(xi)、(xii)或(xiii):
[0082][0083]
[0084]
其中:
[0085]
a是任选的,并且当存在时是低碳亚烷基、经取代的低碳亚烷基、低碳亚环烷基、经取代的低碳亚环烷基、低碳亚烯基、经取代的低碳亚烯基、亚炔基、低碳亚杂烷基、经取代的亚杂烷基、低碳亚杂环烷基、经取代的低碳亚杂环烷基、亚芳基、经取代的亚芳基、亚杂芳基、经取代的亚杂芳基、亚烷芳基、经取代的亚烷芳基、亚芳烷基或经取代的亚芳烷基;
[0086]
b是任选的,并且当存在时是选自由以下组成的群组的连接基团:低碳亚烷基、经取代的低碳亚烷基、低碳亚烯基、经取代的低碳亚烯基、低碳亚杂烷基、经取代的低碳亚杂烷基、
‑
o
‑
、
‑
o
‑
(亚烷基或经取代的亚烷基)
‑
、
‑
s
‑
、
‑
s
‑
(亚烷基或经取代的亚烷基)
‑
、
‑
s(o)
k
‑
(其中k是1、2或3)、
‑
s(o)
k
(亚烷基或经取代的亚烷基)
‑
、
‑
c(o)
‑
、
‑
c(o)
‑
(亚烷基或经取代的亚烷基)
‑
、
‑
c(s)
‑
、
‑
c(s)
‑
(亚烷基或经取代的亚烷基)
‑
、
‑
n(r')
‑
、
‑
nr'
‑
(亚烷基或经取代的亚烷基)
‑
、
‑
c(o)n(r')
‑
、
‑
con(r')
‑
(亚烷基或经取代的亚烷基)
‑
、
‑
csn(r')
‑
、
‑
csn(r')
‑
(亚烷基或经取代的亚烷基)
‑
、
‑
n(r')co
‑
(亚烷基或经取代的亚烷基)
‑
、
‑
n(r')c(o)o
‑
、
‑
s(o)
k
n(r')
‑
、
‑
n(r')c(o)n(r')
‑
、
‑
n(r')c(s)n(r')
‑
、
‑
n(r')s(o)
k
n(r')
‑
、
‑
n(r')
‑
n=、
‑
c(r')=n
‑
、
‑
c(r')=n
‑
n(r')
‑
、
‑
c(r')=n
‑
n=、
‑
c(r')2‑
n=n
‑
以及
‑
c(r')2‑
n(r')
‑
n(r')
‑
,其中每个r'独立地是h、烷基或经取代的烷基;
[0087]
r是h、烷基、经取代的烷基、环烷基或经取代的环烷基;
[0088]
r1是h、氨基保护基、树脂、至少一个氨基酸、多肽或多核苷酸;
[0089]
r2是oh、酯保护基、树脂、至少一个氨基酸、多肽或多核苷酸;
[0090]
r3和r4各自独立地是h、卤素、低碳烷基或经取代的低碳烷基,或r3和r4或两个r3基团任选地形成环烷基或杂环烷基;
[0091]
z具有以下结构:
[0092][0093]
r5是h、co2h、c1‑
c6烷基或噻唑;
[0094]
r6是oh或h;
[0095]
ar是苯基或吡啶;
[0096]
r7是c1‑
c6烷基或氢;
[0097]
l1、l2、l3以及l4各自是独立地选自由以下组成的群组的连接基团:一键、
‑
亚烷基
‑
、
‑
(亚烷基
‑
o)
n
‑
亚烷基
‑
j
‑
、
‑
亚烷基'
‑
j
‑
(亚烷基
‑
o)
n
‑
亚烷基
‑
、
‑
j
‑
(亚烷基
‑
o)
n
‑
亚烷基
‑
、
‑
(亚烷基
‑
o)
n
‑
亚烷基
‑
j
‑
(亚烷基
‑
o)
n
'
‑
亚烷基
‑
j'
‑
、
‑
(亚烷基
‑
o)
n
‑
亚烷基
‑
j
‑
亚烷基'
‑
、
‑
w
‑
、
‑
亚烷基
‑
w
‑
、亚烷基'
‑
j
‑
(亚烷基
‑
nme)
n
‑
亚烷基
‑
w
‑
、
‑
j
‑
(亚烷基
‑
nme)
n
‑
亚烷基
‑
w
‑
、
‑
j
‑
亚烷基
‑
nme
‑
亚烷基'
‑
nme
‑
亚烷基"
‑
w
‑
以及
‑
亚烷基
‑
j
‑
亚烷基'
‑
nme
‑
亚烷基"
‑
nme
‑
亚烷基'"
‑
w
‑
;
[0098]
w具有以下结构:
[0099][0100]
j和j'各自独立地具有以下结构:
[0101]
并且
[0102]
n和n'各自独立地是大于或等于1的整数。
[0103]
在一些实施例中,r1是多肽。在特定实施例中,所述多肽是抗体。在某些特定实施例中,所述抗体是赫赛汀。在其它实施例中,r2是多肽。在特定实施例中,所述多肽是抗体。在某些特定实施例中,所述抗体是赫赛汀。
[0104]
在一些实施例中,本文提供一种用于衍生包含式(i)、(iii)、(iv)、(v)或(vi)的海兔毒素类似物的方法,所述方法包含使所述海兔毒素类似物与式(xxxvii)试剂接触,其中式(i)、(iii)、(iv)、(v)或(vi)对应于:
[0105]
[0106]
[0107][0108]
其中:
[0109]
z具有以下结构:
[0110][0111]
r5是h、cor8、c1‑
c6烷基或噻唑;
[0112]
r8是oh或
‑
nh
‑
(亚烷基
‑
o)
n
‑
nh2;
[0113]
r6是oh或h;
[0114]
ar是苯基或吡啶;
[0115]
r7是c1‑
c6烷基或氢;
[0116]
y是nh2‑
o
‑
或甲基;
[0117]
l、l1、l2、l3以及l4各自是选自由以下组成的群组的连接基团:一键、
‑
亚烷基
‑
、
‑
亚烷基
‑
c(o)
‑
、
‑
(亚烷基
‑
o)
n
‑
亚烷基
‑
、
‑
(亚烷基
‑
o)
n
‑
亚烷基
‑
c(o)
‑
、
‑
(亚烷基
‑
o)
n
‑
(ch2)
n'
‑
nhc(o)
‑
(ch2)
n”‑
c(me)2‑
s
‑
s
‑
(ch2)
n”'
‑
nhc(o)
‑
(亚烷基
‑
o)
n
””
‑
亚烷基
‑
、
‑
(亚烷基
‑
o)
n
‑
亚烷基
‑
w
‑
、
‑
亚烷基
‑
c(o)
‑
w
‑
、
‑
(亚烷基
‑
o)
n
‑
亚烷基
‑
j
‑
、
‑
亚烷基'
‑
j
‑
(亚烷基
‑
o)
n
‑
亚烷基
‑
、
‑
(亚烷基
‑
o)
n
‑
亚烷基
‑
j
‑
亚烷基'、
‑
j
‑
(亚烷基
‑
o)
n
‑
亚烷基
‑
、
‑
(亚烷基
‑
o)
n
‑
亚烷基
‑
j
‑
(亚烷基
‑
o)
n
'
‑
亚烷基
‑
j'
‑
、
‑
w
‑
、
‑
亚烷基
‑
w
‑
、亚烷基'
‑
j
‑
(亚烷基
‑
nme)
n
‑
亚烷基
‑
w
‑
以及j
‑
(亚烷基
‑
nme)
n
‑
亚烷基
‑
w
‑
、
‑
(亚烷基
‑
o)
n
‑
亚烷基
‑
u
‑
亚烷基
‑
c(o)
‑
、
‑
(亚烷基
‑
o)
n
‑
亚烷基
‑
u
‑
亚烷基
‑
、
‑
j
‑
亚烷基
‑
nme
‑
亚烷基'
‑
nme
‑
亚烷基"
‑
w
‑
以及
‑
亚烷基
‑
j
‑
亚烷基'
‑
nme
‑
亚烷基"
‑
nme
‑
亚烷基'"
‑
w
‑
;
[0118]
w具有以下结构:
[0119][0120]
u具有以下结构:
[0121][0122]
j和j'各自独立地具有以下结构:
[0123][0124]
或l不存在,y是甲基,r5是cor8,并且r8是
‑
nh
‑
(亚烷基
‑
o)
n
‑
nh2;并且
[0125]
n、n'、n"、n'"以及n""各自独立地是大于或等于1的整数;
[0126]
其中式(xxxvii)对应于:
[0127][0128]
其中:
[0129]
a是任选的,并且当存在时是低碳亚烷基、经取代的低碳亚烷基、低碳亚烯基、经取代的低碳亚烯基、亚芳基、经取代的亚芳基、亚杂芳基、经取代的亚杂芳基、亚烷芳基、经取代的亚烷芳基、亚芳烷基或经取代的亚芳烷基;
[0130]
b是任选的,并且当存在时是选自由以下组成的群组的连接基团:低碳亚烷基、经取代的低碳亚烷基、低碳亚烯基、经取代的低碳亚烯基、
‑
o
‑
、
‑
o
‑
(亚烷基或经取代的亚烷基)
‑
、
‑
s
‑
、
‑
s
‑
(亚烷基或经取代的亚烷基)
‑
、
‑
s(o)
k
‑
(其中k是1、2或3)、
‑
s(o)
k
(亚烷基或经取代的亚烷基)
‑
、
‑
c(o)
‑
、
‑
c(o)
‑
(亚烷基或经取代的亚烷基)
‑
、
‑
c(s)
‑
、
‑
c(s)
‑
(亚烷基或经取代的亚烷基)
‑
、
‑
n(r')
‑
、
‑
nr'
‑
(亚烷基或经取代的亚烷基)
‑
、
‑
c(o)n(r')
‑
、
‑
con(r')
‑
(亚烷基或经取代的亚烷基)
‑
、
‑
csn(r')
‑
、
‑
csn(r')
‑
(亚烷基或经取代的亚烷基)
‑
、
‑
n(r')co
‑
(亚烷基或经取代的亚烷基)
‑
、
‑
n(r')c(o)o
‑
、
‑
s(o)
k
n(r')
‑
、
‑
n(r')c(o)n(r')
‑
、
‑
n(r')c(s)n(r')
‑
、
‑
n(r')s(o)
k
n(r')
‑
、
‑
n(r')
‑
n=、
‑
c(r')=n
‑
、
‑
c(r')=n
‑
n(r')
‑
、
‑
c(r')=n
‑
n=、
‑
c(r')2‑
n=n
‑
以及
‑
c(r')2‑
n(r')
‑
n(r')
‑
,其中每个r'独立地是h、烷基或经取代的烷基;
[0131]
每个r'独立地是h、烷基或经取代的烷基;
[0132]
k是
[0133]
r是h、烷基、经取代的烷基、环烷基或经取代的环烷基;
[0134]
r1是h、氨基保护基、树脂、至少一个氨基酸或多核苷酸;
[0135]
r2是oh、酯保护基、树脂、至少一个氨基酸或多核苷酸;以及
[0136]
r3和r4各自独立地是h、卤素、低碳烷基或经取代的低碳烷基,或r3和r4或两个r3基团任选地形成环烷基或杂环烷基。
[0137]
在一些实施例中,所衍生的海兔毒素类似物包含至少一个含肟氨基酸,具有式(viii)、(ix)、(x)、(xi)、(xii)或(xiii)的结构:
[0138]
[0139]
[0140][0141]
在特定实施例中,海兔毒素类似物与式(xxxvii)试剂在适度酸性条件下在水溶液中接触。
[0142]
本发明的某些实施例描述一种化合物,包含式(xxv)、(xxvi)、(xxvii)、(xxviii)、(xxix)或(xxx):
[0143]
[0144][0145]
其中:
[0146]
z具有以下结构:
[0147][0148]
r5是h、co2h、c1‑
c6烷基或噻唑;
[0149]
r6是oh或h;
[0150]
ar是苯基或吡啶;
[0151]
r1是h、氨基保护基、树脂、至少一个氨基酸、多肽或多核苷酸;
[0152]
r2是oh、酯保护基、树脂、至少一个氨基酸、多肽或多核苷酸;
[0153]
r4是h、卤素、低碳烷基或经取代的低碳烷基;
[0154]
r7是c1‑
c6烷基或氢;
[0155]
l、l1、l2、l3以及l4各自是选自由以下组成的群组的连接基团:一键、
‑
亚烷基
‑
、
‑
亚烷基
‑
c(o)
‑
、
‑
亚烷基
‑
j
‑
、
‑
(亚烷基
‑
o)
n
‑
亚烷基
‑
、
‑
(亚烷基
‑
o)
n
‑
亚烷基
‑
c(o)
‑
、
‑
(亚烷基
‑
o)
n
‑
j
‑
、
‑
(亚烷基
‑
o)
n
‑
j
‑
亚烷基
‑
、
‑
(亚烷基
‑
o)
n
‑
(ch2)
n'
‑
nhc(o)
‑
(ch2)
n”‑
c(me)2‑
s
‑
s
‑
(ch2)
n”'
‑
nhc(o)
‑
(亚烷基
‑
o)
n
””
‑
亚烷基
‑
、
‑
(亚烷基
‑
o)
n
‑
亚烷基
‑
w
‑
、
‑
亚烷基
‑
c(o)
‑
w
‑
、
‑
(亚烷基
‑
o)
n
‑
亚烷基
‑
j
‑
、
‑
亚烷基'
‑
j
‑
(亚烷基
‑
o)
n
‑
亚烷基
‑
、
‑
(亚烷基
‑
o)
n
‑
亚烷基
‑
j
‑
亚烷基'、
‑
j
‑
(亚烷基
‑
o)
n
‑
亚烷基
‑
、
‑
(亚烷基
‑
o)
n
‑
亚烷基
‑
j
‑
(亚烷基
‑
o)
n
'
‑
亚烷基
‑
j'
‑
、
‑
w
‑
、
‑
亚烷基
‑
w
‑
、亚烷基'
‑
j
‑
(亚烷基
‑
nme)
n
‑
亚烷基
‑
w
‑
、
‑
j
‑
(亚烷基
‑
nme)
n
‑
亚烷基
‑
w
‑
、
‑
(亚烷基
‑
o)
n
‑
亚烷基
‑
u
‑
亚烷基
‑
c(o)
‑
、
‑
(亚烷基
‑
o)
n
‑
亚烷基
‑
u
‑
亚烷基
‑
、
‑
j
‑
亚烷基
‑
nme
‑
亚烷基'
‑
nme
‑
亚烷基"
‑
w
‑
以及
‑
亚烷基
‑
j
‑
亚烷基'
‑
nme
‑
亚烷基"
‑
nme
‑
亚烷基'"
‑
w
‑
;
[0156]
w具有以下结构:
[0157][0158]
u具有以下结构:
[0159][0160]
j和j'各自独立地具有以下结构:
[0161][0162]
n和n'各自独立地是大于或等于1的整数;并且
[0163]
每个r
16
独立地选自由以下组成的群组:氢、卤素、烷基、no2、cn以及经取代的烷基。
[0164]
在一些实施例中,r1是多肽。在特定实施例中,所述多肽是抗体。在某些特定实施例中,所述抗体是赫赛汀。在其它实施例中,r2是多肽。在特定实施例中,所述多肽是抗体。在某些特定实施例中,所述抗体是赫赛汀。
[0165]
本发明的一些实施例描述一种化合物,包含式(xxxi)、(xxxii)、(xxxiii)、(xxxiv)、(xxxv)或(xxxvi):
[0166]
[0167][0168]
其中:
[0169]
z具有以下结构:
[0170][0171]
r5是h、co2h、c1‑
c6烷基或噻唑;
[0172]
r6是oh或h;
[0173]
ar是苯基或吡啶;
[0174]
r1是h、氨基保护基、树脂、至少一个氨基酸、多肽或多核苷酸;
[0175]
r2是oh、酯保护基、树脂、至少一个氨基酸、多肽或多核苷酸;
[0176]
r4是h、卤素、低碳烷基或经取代的低碳烷基;
[0177]
r7是c1‑
c6烷基或氢;
[0178]
l、l1、l2、l3以及l4各自是选自由以下组成的群组的连接基团:一键、
‑
亚烷基
‑
、
‑
亚烷基
‑
c(o)
‑
、
‑
亚烷基
‑
j
‑
、
‑
(亚烷基
‑
o)
n
‑
亚烷基
‑
、
‑
(亚烷基
‑
o)
n
‑
亚烷基
‑
c(o)
‑
、
‑
(亚烷基
‑
o)
n
‑
j
‑
、
‑
(亚烷基
‑
o)
n
‑
j
‑
亚烷基
‑
、
‑
(亚烷基
‑
o)
n
‑
(ch2)
n'
‑
nhc(o)
‑
(ch2)
n”‑
c(me)2‑
s
‑
s
‑
(ch2)
n”'
‑
nhc(o)
‑
(亚烷基
‑
o)
n
””
‑
亚烷基
‑
、
‑
(亚烷基
‑
o)
n
‑
亚烷基
‑
w
‑
、
‑
亚烷基
‑
c(o)
‑
w
‑
、
‑
(亚烷基
‑
o)
n
‑
亚烷基
‑
j
‑
、
‑
亚烷基'
‑
j
‑
(亚烷基
‑
o)
n
‑
亚烷基
‑
、
‑
(亚烷基
‑
o)
n
‑
亚烷基
‑
j
‑
亚烷基'、
‑
j
‑
(亚烷基
‑
o)
n
‑
亚烷基
‑
、
‑
(亚烷基
‑
o)
n
‑
亚烷基
‑
j
‑
(亚烷基
‑
o)
n
'
‑
亚烷基
‑
j'
‑
、
‑
w
‑
、
‑
亚烷基
‑
w
‑
、亚烷基'
‑
j
‑
(亚烷基
‑
nme)
n
‑
亚烷基
‑
w
‑
、
‑
j
‑
(亚烷基
‑
nme)
n
‑
亚烷基
‑
w
‑
、
‑
(亚烷基
‑
o)
n
‑
亚烷基
‑
u
‑
亚烷基
‑
c(o)
‑
、
‑
(亚烷基
‑
o)
n
‑
亚烷基
‑
u
‑
亚烷基
‑
、
‑
j
‑
亚烷基
‑
nme
‑
亚烷基'
‑
nme
‑
亚烷基"
‑
w
‑
以及
‑
亚烷基
‑
j
‑
亚烷基'
‑
nme
‑
亚烷基"
‑
nme
‑
亚烷基'"
‑
w
‑
;
[0179]
w具有以下结构:
[0180][0181]
u具有以下结构:
[0182][0183]
j和j'各自独立地具有以下结构:
[0184][0185]
n和n'各自独立地是大于或等于1的整数;
[0186]
d具有以下结构:
[0187][0188]
每个r
17
独立地选自由以下组成的群组:h、烷基、经取代的烷基、烯基、经取代的烯基、炔基、经取代的炔基、烷氧基、经取代的烷氧基、烷基烷氧基、经取代的烷基烷氧基、聚环氧烷、经取代的聚环氧烷、芳基、经取代的芳基、杂芳基、经取代的杂芳基、烷芳基、经取代的烷芳基、芳烷基、经取代的芳烷基、
‑
(亚烷基或经取代的亚烷基)
‑
on(r")2、
‑
(亚烷基或经取代的亚烷基)
‑
c(o)sr"、
‑
(亚烷基或经取代的亚烷基)
‑
s
‑
s
‑
(芳基或经取代的芳基)、
‑
c(o)r"、
‑
c(o)2r"或
‑
c(o)n(r")2,其中每个r"独立地是氢、烷基、经取代的烷基、烯基、经取代的烯基、烷氧基、经取代的烷氧基、芳基、经取代的芳基、杂芳基、烷芳基经取代的烷芳基、芳烷基或经取代的芳烷基;
[0189]
每个z1是一键、cr
17
r
17
、o、s、nr'、cr
17
r
17
‑
cr
17
r
17
、cr
17
r
17
‑
o、o
‑
cr
17
r
17
、cr
17
r
17
‑
s、s
‑
cr
17
r
17
、cr
17
r
17
‑
nr'或nr'
‑
cr
17
r
17
;
[0190]
每个r'是h、烷基或经取代的烷基;
[0191]
每个z2选自由以下组成的群组:一键、
‑
c(o)
‑
、
‑
c(s)
‑
、任选地经取代的c1‑
c3亚烷基、任选地经取代的c1‑
c3亚烯基以及任选地经取代的杂烷基;
[0192]
每个z3独立地选自由以下组成的群组:一键、任选地经取代的c1‑
c4亚烷基、任选地经取代的c1‑
c4亚烯基、任选地经取代的杂烷基、
‑
o
‑
、
‑
s
‑
、
‑
c(o)
‑
、
‑
c(s)
‑
以及
‑
n(r')
‑
;
[0193]
每个t3是一键、c(r")(r")、o或s;其条件是当t3是o或s时,r"不能是卤素;
[0194]
每个r”是h、卤素、烷基、经取代的烷基、环烷基或经取代的环烷基;
[0195]
m和p是0、1、2或3,只要m或p中的至少一个不是0即可;
[0196]
m2是是其中(a)指示键结到所述b基团并且(b)指示键结到所述杂环基团内的对应位置;
[0197]
m3是其中(a)指示键结到所述b基团并且(b)指示键结到所述杂环基团内的对应位置;
[0198]
m4是其中(a)指示键结到所述b基团并且(b)指示键结到所述杂环基团内的对应位置;
[0199]
每个r
19
独立地选自由以下组成的群组:c1‑
c6烷基、c1‑
c6烷氧基、酯、醚、硫醚、氨基烷基、卤素、烷基酯、芳基酯、酰胺、芳基酰胺、烷基卤化物、烷基胺、烷基磺酸、烷基硝基、硫酯、磺酰基酯、卤磺酰基、腈、烷基腈以及硝基;
[0200]
q是0、1、2、3、4、5、6、7、8、9、10或11;以及
[0201]
每个r
16
独立地选自由以下组成的群组:氢、卤素、烷基、no2、cn以及经取代的烷基。
[0202]
在一些实施例中,r1是多肽。在特定实施例中,所述多肽是抗体。在某些特定实施例中,所述抗体是赫赛汀。在其它实施例中,r2是多肽。在特定实施例中,所述多肽是抗体。在某些特定实施例中,所述抗体是赫赛汀。
[0203]
在一些实施例中,描述一种化合物,包含式(xxxi
‑
a):
[0204][0205]
在某些实施例中,提供一种医药组合物,它包含所描述的化合物中的任一种和医药学上可接受的载体、赋形剂或粘合剂。
[0206]
另外或替代实施例是检测患者中多肽的存在的方法,所述方法包含投与包含至少一个含杂环非天然氨基酸的多肽,并且所得含杂环非天然氨基酸多肽相对于同源天然存在的氨基酸多肽调节所述多肽的免疫原性。
[0207]
应理解本文所述的方法和组合物不限于本文所述的具体方法、方案、细胞系、构筑体以及试剂,并且因此可以变化。还应理解,本文所使用的术语只是出于描述特定实施例的目的,并且不打算限制本文所述的方法和组合物的范围,所述范围将仅受所附权利要求书限制。
[0208]
除非上下文另作明确指示,否则如本文和所附权利要求书中所使用,单数形式“一”和“所述”包括多个参考物。
[0209]
除非另作定义,否则本文所使用的所有技术和科学术语具有与本文所述的本发明所属领域的技术人员通常所理解相同的含义。尽管可以将与本文所述的方法、装置和材料
类似或相当的任何方法、装置和材料用于本文所述的本发明的实践或测试中,但是现仅对优选方法、装置和材料加以描述。
[0210]
本文所提及的所有公开案和专利都是以全文引用的方式并入本文中,以达到描述和披露例如所述公开案中描述的可能与当前所述的发明结合使用的构筑体和方法的目的。本文所讨论的公开案仅提供本技术案申请日期之前的披露内容。本文在任何方面都不应解释为承认本文所述的本发明人由于现有发明或任何其它原因而无权使所述披露内容的日期提前。
[0211]
术语“基于醇醛的键”或“基于混合醇醛的键”是指一种羰基化合物与可能相同或可能不同的另一种羰基化合物的烯醇酯/烯醇的酸或碱催化的缩合,从而产生β
‑
羟基羰基化合物(醇醛)。
[0212]
如本文所使用,术语“亲和标记”是指可逆或不可逆地结合另一分子以对其进行修饰、将其破坏或与其形成化合物的标记。举例来说,亲和标记包括酶和其底物,或者抗体和其抗原。
[0213]
术语“烷氧基”、“烷基氨基”和“烷硫基”(或硫代烷氧基)是以其常规含义使用,并且指分别通过氧原子、氨基或硫原子连接于分子的那些烷基。
[0214]“烷基”本身或作为另一分子的部分意思是指具有指定碳原子数量(即,c1‑
c
10
意思是1到10个碳)的直链或支链或环状烃基或其组合,其可以是完全饱和、单或多不饱和的并且可包括二价和多价基团。饱和烃基的实例包括(但不限于)如以下的基团:甲基、乙基、正丙基、异丙基、正丁基、叔丁基、异丁基、仲丁基、环己基、(环己基)甲基、环丙基甲基;例如正戊基、正己基、正庚基、正辛基的同系物和异构体等。不饱和烷基是具有一个或一个以上双键或三键的烷基。不饱和烷基的实例包括(但不限于)乙烯基、2
‑
丙烯基、巴豆基、2
‑
异戊烯基、2
‑
(丁二烯基)、2,4
‑
戊二烯基、3
‑
(1,4
‑
戊二烯基)、乙炔基、1
‑
丙炔基和3
‑
丙炔基、3
‑
丁炔基以及高级同系物和异构体。除非另作说明,否则术语“烷基”还意欲包括本文更为详细地定义的烷基衍生物,如“杂烷基”、“卤烷基”和“同系烷基(homoalkyl)”。
[0215]
术语“亚烷基”本身或作为另一分子的部分意思是指衍生自烷烃的二价基团,例如(
‑
ch2‑
)
n
,其中n可以是1到约24。仅举例来说,所述基团包括(但不限于)具有10个或10个以下碳原子的基团,如结构
‑
ch2ch2‑
和
‑
ch2ch2ch2ch2‑
。“低碳烷基”或“低碳亚烷基”是通常具有8个或8个以下碳原子的链较短的烷基或亚烷基。除非另作说明,否则术语“亚烷基”还意欲包括本文描述为“亚杂烷基”的基团。
[0216]
术语“氨基酸”是指天然存在的氨基酸和非天然氨基酸,以及以与天然存在的氨基酸类似的方式起作用的氨基酸类似物和氨基酸模拟物。天然编码的氨基酸是20种常见氨基酸(丙氨酸、精氨酸、天冬酰胺、天冬氨酸、半胱氨酸、谷氨酰胺、谷氨酸、甘氨酸、组氨酸、异亮氨酸、亮氨酸、赖氨酸、甲硫氨酸、苯丙氨酸、脯氨酸、丝氨酸、苏氨酸、色氨酸、酪氨酸和缬氨酸)和吡咯赖氨酸和硒代半胱氨酸。氨基酸类似物是指具有与天然存在的氨基酸相同的基础化学结构的化合物,所述基础化学结构仅举例来说是与氢、羧基、氨基和r基团结合的α碳。所述类似物可具有经修饰的r基团(例如,正亮氨酸)或者可具有经修饰的肽主链,同时仍保持与天然存在的氨基酸相同的基础化学结构。氨基酸类似物的非限制性实例包括高丝氨酸、正亮氨酸、甲硫氨酸亚砜、甲硫氨酸甲基锍。
[0217]
氨基酸可在本文中以其名称、其通常已知的三字母符号或iupac
‑
iub生物化学命
名委员会(biochemical nomenclature commission)所推荐的单字母符号提及。此外,核苷酸可通过其通常接受的单字母代码提及。
[0218]“氨基末端修饰基团”是指可与末端胺基连接的任何分子。举例来说,所述末端胺基可在聚合分子的末端处,其中所述聚合分子包括(但不限于)多肽、多核苷酸和多糖。末端修饰基团包括(但不限于)各种水溶性聚合物、肽或蛋白质。仅举例来说,末端修饰基团包括聚乙二醇或血清白蛋白。末端修饰基团可用于改变聚合分子的治疗特征,包括(但不限于)增加肽的血清半衰期。
[0219]“抗体片段”是指除全长形式外的抗体的任何形式。本文中的抗体片段包括作为存在于全长抗体内的较小组分的抗体,以及已经工程化的抗体。抗体片段包括(但不限于)fv、fc、fab和(fab')2、单链fv(scfv)、双链抗体、三链抗体、四链抗体、双功能性杂交抗体、cdr1、cdr2、cdr3、cdr的组合、可变区、框架区、恒定区、重链、轻链和可变区,以及替代支架非抗体分子、双特异性抗体等(梅纳德(maynard)和乔治乌(georgiou),2000,生物医学工程年评(annu.rev.biomed.eng.)2:339
‑
76;哈德逊(hudson),1998,生物技术新见(curr.opin.biotechnol.)9:395
‑
402)。另一功能性子结构是单链fv(scfv),其包含通过肽连接子共价连接的免疫球蛋白重链和轻链的可变区(胡s
‑
z(s
‑
z hu)等人,1996,癌症研究(cancer research),56,3055
‑
3061)。这些小(mr 25,000)蛋白质通常在单一多肽中保持对抗原的特异性和亲和性并且能够提供较大抗原特异性分子的便利构筑嵌段。除非另作明确指示,否则使用术语“抗体”的陈述和权利要求书中特别包括“抗体片段”。
[0220]
如本文所使用,“抗体
‑
药结合物”或“adc”是指共价键结于一个或一个以上生物活性分子的抗体分子或其片段。生物活性分子可通过连接基团、聚合物或其它共价键结合于抗体。
[0221]
如本文所使用,术语“芳香族”或“芳基”是指一种闭环结构,其具有至少一个具有共轭π电子系统的环并且包括碳环芳基和杂环芳基(或“杂芳基”或“杂芳香族”)。碳环或杂环芳香族基团可含有5到20个环原子。所述术语包括共价连接的单环或稠环多环(即,共用相邻碳原子对的环)基团。芳香族基团可以是未经取代的或经取代的。“芳香族”或“芳基”的非限制性实例包括苯基、1
‑
萘基、2
‑
萘基、4
‑
联苯基、蒽基和菲基。上述芳基和杂芳基环系统中的每一个的取代基选自本文所述的可接受取代基的群组。
[0222]
简言之为了简便起见,术语“芳香族”或“芳基”当与其它术语(包括(但不限于)芳氧基、芳硫氧基、芳烷基)组合使用时包括如上文所定义的芳基和杂芳基环。因此,术语“芳烷基”或“烷芳基”意欲包括芳基与烷基连接的基团(包括(但不限于)苯甲基、苯乙基、吡啶基甲基等),所述烷基包括碳原子(包括(但不限于)亚甲基)已经被杂原子(仅举例来说,氧原子)置换的烷基。所述芳基的实例包括(但不限于)苯氧基甲基、2
‑
吡啶氧基甲基、3
‑
(1
‑
萘氧基)丙基等。
[0223]
如本文所使用,术语“亚芳基”是指二价芳基。“亚芳基”的非限制性实例包括亚苯基、亚吡啶基、亚嘧啶基和亚噻吩基。亚芳基的取代基选自本文所述的可接受的取代基的群组。
[0224]“双官能聚合物”(也称为“双官能连接基团”)是指包含两个能够与其它部分特异性反应以形成共价或非共价键的官能团的聚合物。所述部分可包括(但不限于)天然或非天然氨基酸或者含有所述天然或非天然氨基酸的肽上的侧基。可连接于双官能连接基团或双
官能聚合物的其它部分可以是相同或不同的部分。仅举例来说,双官能连接基团可具有可与第一肽上的基团反应的官能团和可与第二肽上的基团反应的另一官能团,从而形成包括第一肽、双官能连接基团和第二肽的结合物。已知许多将各种化合物与肽连接的程序和连接分子。参见,例如欧洲专利申请案第188,256号、美国专利第4,671,958号、第4,659,839号、第4,414,148号、第4,699,784号、第4,680,338号和第4,569,789号,所述专利以全文引用的方式并入本文中。“多官能聚合物”(也称为“多官能连接基团”)是指包含两个或两个以上能够与其它部分反应的官能团的聚合物。所述部分可包括(但不限于)天然或非天然氨基酸或者含有所述天然或非天然氨基酸的肽上的侧基(包括(但不限于)氨基酸侧基)以形成共价或非共价键。双官能聚合物或多官能聚合物可以是任何所需长度或分子量,并且可经选择以在连接到化合物的一个或一个以上分子与其所结合的分子或化合物之间提供特定所需间隔或构象。
[0225]
如本文所使用,术语“生物可用性”是指物质或其活性部分自医药剂型传递并且在作用部位或在全身循环中变得可用的比率和程度。生物可用性增加是指使物质或其活性部分自医药剂型传递并且在作用部位或在全身循环中变得可用的比率和程度增加。举例来说,生物可用性的增加可指定为物质或其活性部分在与其它物质或活性部分相比时在血液中的浓度增加。评估生物可用性增加的方法的一个非限制性实例在实例21
‑
25中给出。此方法可用于评估任何多肽的生物可用性。
[0226]
术语“生物活性分子”、“生物活性部分”或“生物活性剂”当用于本文中时意思是指可影响涉及生物体(包括(但不限于)病毒、细菌、噬菌体、转座子、朊病毒、昆虫、真菌、植物、动物和人类)的生物系统、路径、分子或相互作用的任何物理或生物化学性质的任何物质。具体来说,如本文所使用,生物活性分子包括(但不限于)打算用于诊断、治愈、缓解、治疗或预防人类或其它动物的疾病或者以其它方式增强人类或动物的身体或精神健康状况的任何物质。生物活性分子的实例包括(但不限于)肽、蛋白质、酶、小分子药物、硬药、软药、前药、碳水化合物、无机原子或分子、染料、脂质、核苷、放射性核素、寡核苷酸、毒素、细胞、病毒、脂质体、微粒和胶束。适用于本文所述的方法和组合物的生物活性剂的种类包括(但不限于)药物、前药、放射性核素、显影剂、聚合物、抗生素、杀真菌剂、抗病毒剂、消炎剂、抗肿瘤剂、心血管剂、抗焦虑剂、激素、生长因子、类固醇剂、微生物来源的毒素等。
[0227]“调节生物活性”意思是指增加或减少多肽的反应性、改变多肽的选择性、增强或降低多肽的底物选择性。经改变的生物活性的分析可通过比较非天然多肽的生物活性与天然多肽的生物活性来进行。
[0228]
如本文所使用,术语“生物材料”是指生物来源的材料,包括(但不限于)由生物反应器和/或重组方法和技术获得的材料。
[0229]
如本文所使用,术语“生物物理探针”是指可检测或监测分子结构变化的探针。所述分子包括(但不限于)蛋白质,并且“生物物理探针”可用于检测或监测蛋白质与其它大分子的相互作用。生物物理探针的实例包括(但不限于)自旋标记、荧光团和可光活化的基团。
[0230]
如本文所使用,术语“生物合成”是指利用翻译系统(细胞或非细胞)的任何方法,所述方法包括使用以下组分中的至少一种:多核苷酸、密码子、trna和核糖体。举例来说,非天然氨基酸可使用本文“体内产生包含非天然氨基酸的多肽”和非限制性实例20中所述的方法和技术“以生物合成方式并入”非天然氨基酸多肽中。另外,选择可“以生物合成方式并
入”非天然氨基酸多肽中的适用非天然氨基酸的方法描述于非限制性实例20中。
[0231]
如本文所使用,术语“生物素类似物”(或也称为“生物素模拟物”)是除生物素外的任何分子,其以高亲和力与抗生物素蛋白和/或抗生物素蛋白链菌素结合。
[0232]
如本文所使用,术语“羰基”是指含于选自由
‑
c(o)
‑
、
‑
s(o)
‑
、
‑
s(o)2
‑
和
‑
c(s)
‑
组成的群组的部分处的基团,包括(但不限于)含有至少一个酮基、和/或至少一个醛基、和/或至少一个酯基、和/或至少一个羧酸基和/或至少一个硫酯基的基团。所述羰基包括酮、醛、羧酸、酯和硫酯。另外,所述基团可以是直链、支链或环状分子的一部分。
[0233]
术语“羧基末端修饰基团”是指可与末端羧基连接的任何分子。举例来说,所述末端羧基可在聚合分子的末端处,其中所述聚合分子包括(但不限于)多肽、多核苷酸和多糖。末端修饰基团包括(但不限于)各种水溶性聚合物、肽或蛋白质。仅举例来说,末端修饰基团包括聚乙二醇或血清白蛋白。末端修饰基团可用于改变聚合分子的治疗特征,包括(但不限于)增加肽的血清半衰期。
[0234]
如本文所使用,术语“可化学裂解的基团”(也称为“化学不稳定的”)是指当暴露于酸、碱、氧化剂、还原剂、化学引发剂或自由基引发剂时断裂或裂解的基团。
[0235]
如本文所使用,术语“化学发光基团”是指在不加热的情况下因化学反应而发光的基团。仅举例来说,鲁米诺(luminol)(5
‑
氨基
‑
2,3
‑
二氢
‑
1,4
‑
酞嗪二酮)与如过氧化氢(h2o2)的氧化剂在存在碱和金属催化剂的情况下反应,产生激发态产物(3
‑
氨基邻苯二甲酸根,3
‑
apa)。
[0236]
如本文所使用,术语“发色团”是指吸收可见波长、uv波长或ir波长的光的分子。
[0237]
如本文所使用,术语“辅因子”是指对大分子的作用至关重要的原子或分子。辅因子包括(但不限于)无机离子、辅酶、蛋白质或酶活性必需的一些其它因子。实例包括血色素中的血红素、叶绿素中的镁和蛋白质的金属离子。
[0238]
如本文所使用,“共折叠”是指使用至少两个分子的再折叠过程、反应或方法,所述分子彼此相互作用并且导致展开或不适当折叠的分子转化成适当折叠的分子。仅举例来说,“共折叠”使用至少两个多肽,其彼此相互作用并且导致展开或不适当折叠的多肽转化成自然、适当折叠的多肽。所述多肽可含有天然氨基酸和/或至少一个非天然氨基酸。
[0239]
如本文所使用,“比较窗”是指在最佳比对两个序列后用于将一种序列与具有相同数量邻近位置的参考序列相比较的邻近位置中任一个的区段。所述邻近位置包括(但不限于)由约20到约600个连续单元、包括约50到约200个连续单元和约100到约150个连续单元组成的群组。仅举例来说,所述序列包括多肽和含有非天然氨基酸的多肽,其中连续单元包括(但不限于)天然和非天然氨基酸。此外,仅举例来说,所述序列包括核苷酸是相应连续单元的多核苷酸。所属领域众所周知供比较的序列比对方法。可通过(包括(但不限于))史密斯(smith)和沃特曼(waterman)(1970)应用数学进展(adv.appl.math.)2:482c的局部同源性算法;尼德曼(needleman)和温施(wunsch)(1970)分子生物学杂志(j.mol.biol.)48:443的同源性比对算法;皮尔森(pearson)和李普曼(lipman)(1988)美国国家科学院院刊(proc.nat'l.acad.sci.usa)85:2444的相似性搜索方法;这些算法的计算机实施(威斯康星遗传学软件包(wisconsin genetics software package);威斯康星州麦迪逊科学车道575号的遗传计算机组(genetics computer group,575science dr.,madison,wi))中的gap、bestfit、fasta和tfasta);或者手工比对和目测(参见,例如奥苏伯尔(ausubel)等人,
分子生物学实验室指南(current protocols in molecular biology)(1995增补版))来进行供比较的序列的最佳比对。
[0240]
举例来说,可用于测定序列一致性和序列相似性百分比的算法是blast和blast2.0算法,其分别描述于阿特休尔(altschul)等人(1997)核酸研究(nuc.acids res.)25:3389
‑
3402和阿特休尔等人(1990)分子生物学杂志215:403
‑
410。进行blast分析的软件可通过美国生物技术信息中心(national center for biotechnology information)公共可用。blast算法参数w、t和x决定比对的灵敏性和速度。blastn程序(用于核苷酸序列)使用以下作为默认值:字长(w)是11,期望值(e)是10,m=5,n=
‑
4并比较两条链。对于氨基酸序列来说,blastp程序使用以下作为默认值:字长是3并且期望值(e)是10,和blosum62计分矩阵(参见亨尼科夫(henikoff)和亨尼科夫(1992)美国国家科学院院刊89:10915),比对值(b)是50,期望值(e)是10,m=5,n=
‑
4并比较两条链。在进行blast算法时通常关闭“低复杂度”筛选程序。
[0241]
blast算法也进行两个序列之间相似性的统计分析(参见,例如卡林(karlin)和阿特休尔(1993)美国国家科学院院刊90:5873
‑
5787)。blast算法所提供的一种相似性测量法是最小总和概率(p(n)),其提供对两个核苷酸或氨基酸序列之间将偶然发生匹配的概率的指示。举例来说,如果测试核酸与参考核酸的比较中最小总和概率小于约0.2、或小于约0.01或小于约0.001,那么认为核酸与参考序列相似。
[0242]
术语“保守修饰变体”适用于天然与非天然氨基酸以及天然与非天然核酸序列以及其组合。就特定核酸序列来说,“保守修饰变体”是指编码相同或基本上相同的天然和非天然氨基酸序列的天然和非天然核酸,或者当天然和非天然核酸不编码天然和非天然氨基酸序列时,是指基本上相同的序列。举例来说,由于遗传密码的简并性,大量功能相同的核酸将编码任何给定蛋白质。举例来说,密码子gca、gcc、gcg和gcu都编码氨基酸丙氨酸。因此,在密码子指定丙氨酸的每一位置处,密码子可在不改变所编码多肽的情况下变成任何相应的密码子。所述核酸变异是“沉默变异(silent variation)”,其是保守修饰变异的一种。因此,举例来说,编码天然或非天然多肽的本文中的每一天然或非天然核酸序列也描述天然或非天然核酸的每一可能的沉默变异。所属领域的技术人员将认识到,天然或非天然核酸中的每一密码子(通常是甲硫氨酸的唯一密码子的aug和通常是色氨酸的唯一密码子的tgg除外)可经修饰以得到功能相同的分子。因此,编码天然和非天然多肽的天然和非天然核酸的每一沉默变异是每一所述序列中所固有的。
[0243]
对于氨基酸序列来说,使所编码序列中单个天然和非天然氨基酸或一小部分天然和非天然氨基酸发生改变、添加或缺失的核酸、肽、多肽或蛋白质序列的个别取代、缺失或添加是“保守修饰变体”,其中所述改变导致氨基酸的缺失、氨基酸的添加或者化学上类似的氨基酸对天然和非天然氨基酸的取代。所属领域众所周知提供功能类似的天然氨基酸的保守取代表。所述保守修饰变体除了是多形态变体外并且不排除多形态变体,还是本文所述方法和组合物的种间同系物和等位基因。
[0244]
所属领域的技术人员已知提供功能相似的氨基酸的保守取代表。以下八个群组各自含有彼此互为保守取代的氨基酸:
[0245]
1)丙氨酸(a)、甘氨酸(g);
[0246]
2)天冬氨酸(d)、谷氨酸(e);
[0247]
3)天冬酰胺(n)、谷氨酰胺(q);
[0248]
4)精氨酸(r)、赖氨酸(k);
[0249]
5)异亮氨酸(i)、亮氨酸(l)、甲硫氨酸(m)、缬氨酸(v);
[0250]
6)苯丙氨酸(f)、酪氨酸(y)、色氨酸(w);
[0251]
7)丝氨酸(s)、苏氨酸(t);和
[0252]
8)半胱氨酸(c)、甲硫氨酸(m)
[0253]
(参见,例如克赖顿(creighton),蛋白质:结构和分子性质(proteins:structures and molecular properties)(w h弗里曼公司(w h freeman&co.);第2版(1993年12月))。
[0254]
除非另作说明,否则术语“环烷基”和“杂环烷基”本身或与其它术语组合时分别表示“烷基”和“杂烷基”的环状形式。因此,环烷基或杂环烷基包括饱和、部分不饱和以及完全不饱和的环键。此外,对于杂环烷基来说,杂原子可占据杂环与分子的剩余部分连接的位置。杂原子可包括(但不限于)氧、氮或硫。环烷基的实例包括(但不限于)环戊基、环己基、1
‑
环己烯基、3
‑
环己烯基、环庚基等。杂环烷基的实例包括(但不限于)1
‑
(1,2,5,6
‑
四氢吡啶基)、1
‑
哌啶基、2
‑
哌啶基、3
‑
哌啶基、4
‑
吗啉基、3
‑
吗啉基、四氢呋喃
‑2‑
基、四氢呋喃
‑3‑
基、四氢噻吩
‑2‑
基、四氢噻吩
‑3‑
基、1
‑
哌嗪基、2
‑
哌嗪基等。此外,所述术语涵盖多环结构,包括(但不限于)双环和三环结构。类似地,术语“亚杂环烷基”本身或作为另一分子的部分意思是指衍生自杂环烷基的二价基团,并且术语“亚环烷基”本身或作为另一分子的部分意思是指衍生自环烷基的二价基团。
[0255]
如本文所使用,术语“环糊精”是指在环形成过程中由至少6到8个葡萄糖分子组成的环状碳水化合物。环的外侧部分含有水溶性基团;在环中心处是能够容纳小分子的相对非极性腔。
[0256]
如本文所使用,术语“细胞毒性”是指危害细胞的化合物。
[0257]
如本文所使用,“变性剂(denaturing agent/denaturant)”是指将引起聚合物可逆展开的任何化合物或材料。仅举例来说,“变性剂”可引起蛋白质可逆展开。变性剂的强度将由特定变性剂的性质和浓度来决定。举例来说,变性剂包括(但不限于)离液剂、清洁剂、可与水混溶的有机溶剂、磷脂或其组合。离液剂的非限制性实例包括(但不限于)脲、胍和硫氰酸钠。清洁剂的非限制性实例可包括(但不限于)强清洁剂(如十二烷基硫酸钠或聚氧乙烯醚)(例如,tween或triton清洁剂)、月桂酰肌氨酸钠(sarkosyl)、温和的非离子清洁剂(例如,毛地黄皂苷)、温和的阳离子清洁剂(如,n
→
2,3
‑
(二油酰基氧基)
‑
丙基
‑
n,n,n
‑
三甲基铵)、温和的离子清洁剂(例如,胆酸钠或去氧胆酸钠)或两性离子清洁剂(包括(但不限于)硫代甜菜碱(两性洗涤剂)、3
‑
(3
‑
胆酰胺基丙基)二甲氨基
‑1‑
丙烷硫酸盐(chaps)和3
‑
(3
‑
胆酰胺基丙基)二甲氨基
‑2‑
羟基
‑1‑
丙烷磺酸盐(chapso))。可与水混溶的有机溶剂的非限制性实例包括(但不限于)乙腈、低碳烷醇(尤其c2
‑
c4烷醇,如乙醇或异丙醇)或低碳烷二醇(c2
‑
c4烷二醇,如乙二醇)可用作变性剂。磷脂的非限制性实例包括(但不限于)天然存在的磷脂,如磷脂酰乙醇胺、磷脂酰胆碱、磷脂酰丝氨酸和磷脂酰肌醇,或合成的磷脂衍生物或变体,如二己酰磷脂酰胆碱或二庚酰磷脂酰胆碱。
[0258]
如本文所使用,术语“所需功能性”是指选自以下的任何群组:标记、染料、聚合物、水溶性聚合物、聚乙二醇衍生物、光交联剂、细胞毒性化合物、药物、亲和标记、光亲和标记、反应性化合物、树脂、第二蛋白质或多肽或多肽类似物、抗体或抗体片段、金属螯合剂、辅因
子、脂肪酸、碳水化合物、多核苷酸、dna、rna、反义多核苷酸、糖、水溶性树突状聚合物、环糊精、生物材料、纳米粒子、自旋标记、荧光团、含金属部分、放射性部分、新颖官能团、与其它分子共价或非共价相互作用的基团、光笼蔽部分、光化辐射可激发部分、配体、可光异构化部分、生物素、生物素类似物、并有重原子的部分、可化学裂解基团、可光裂解基团、延长的侧链、碳连接糖、氧化还原活性剂、氨基硫代酸、毒性部分、同位素标记的部分、生物物理探针、磷光基团、化学发光基团、电子致密基团、磁性基团、插入基团、发色团、能量转移剂、生物活性剂(在所述情况下,生物活性剂可包括具有治疗学活性的药剂并且非天然氨基酸多肽或经修饰的非天然氨基酸可用于与连接的治疗剂作为共治疗剂或作为将治疗剂传递到生物体内所需位点的手段)、可检测标记、小分子、抑制性核糖核酸、放射性核苷酸、中子捕获剂、生物素衍生物、量子点、纳米递质、放射性递质、抗体酶、活化复合活化剂、病毒、佐剂、糖苷配基、过敏原、血管生成抑制素、抗激素、抗氧化剂、适体、向导rna、皂苷、穿梭载体、大分子、模拟表位、受体、反胶束和其任何组合。
[0259]
如本文所使用,术语“二胺”是指包含至少两个胺官能团的基团/分子,包括(但不限于)肼基团、脒基团、亚胺基团、1,1
‑
二胺基团、1,2
‑
二胺基团、1,3
‑
二胺基团和1,4
‑
二胺基团。另外,所述基团可以是直链、支链或环状分子的一部分。
[0260]
如本文所使用,术语“可检测标记”是指可使用分析技术观察的标记,包括(但不限于)荧光、化学发光、电子自旋共振、紫外/可见光吸收光谱、质谱、核磁共振、磁共振和电化学方法。
[0261]
如本文所使用,术语“二羰基”是指含有至少两个选自由
‑
c(o)
‑
、
‑
s(o)
‑
、
‑
s(o)2‑
和
‑
c(s)
‑
组成的群组的部分的基团,包括(但不限于)1,2
‑
二羰基、1,3
‑
二羰基和1,4
‑
二羰基;以及含有至少一个酮基和/或至少一个醛基和/或至少一个酯基和/或至少一个羧酸基和/或至少一个硫酯基的基团。所述二羰基包括二酮、酮醛、酮酸、酮酯和酮硫酯。此外,所述基团可以是直链、支链或环状分子的部分。二羰基中的两个部分可以是相同或不同的,并且可包括将在这两个部分中的任一个处仅产生例如酯、酮、醛、硫酯或酰胺的取代基。
[0262]
如本文所使用,术语“药物”是指用于预防、诊断、缓和、治疗或治愈疾病或病状的任何物质。
[0263]
如本文所使用,术语“染料”是指含有发色团的可溶性着色物质。
[0264]
如本文所使用,术语“有效量”是指所投与的药剂或化合物的充足量,其将在一定程度上缓解所治疗的疾病或病状的一种或一种以上症状。结果可以是疾病的病征、症状或病因的减轻和/或缓和,或者生物系统的任何其它所需改变。举例来说,所投与的药剂或化合物包括(但不限于)天然氨基酸多肽、非天然氨基酸多肽、经修饰的天然氨基酸多肽或经修饰的非天然氨基酸多肽。可投与含有所述天然氨基酸多肽、非天然氨基酸多肽、经修饰的天然氨基酸多肽或经修饰的非天然氨基酸多肽的组合物以用于预防性、增强性和/或治疗性治疗。任何个别情况中的适当“有效”量可使用如剂量增加研究的技术来确定。
[0265]
如本文所使用,术语“电子致密基团”是指当用电子束照射时散射电子的基团。所述基团包括(但不限于)钼酸铵、碱式硝酸、铋碘化镉(99%)、碳酰肼、六水合氯化铁、六亚甲基四胺(98.5%)、无水三氯化铟、硝酸镧、三水合乙酸铅、三水合柠檬酸铅、硝酸铅、高碘酸、磷钼酸、磷钨酸、铁氰化钾、亚铁氰化钾、钌红、硝酸银、蛋白银(ag分析:8.0
‑
8.5%)“强”、四苯基卟吩银(s
‑
tpps)、氯金酸钠、钨酸钠、硝酸铊、氨基硫脲(tsc)、乙酸双氧铀、硝酸双氧铀
和硫酸氧钒。
[0266]
如本文所使用,术语“能量转移剂”是指可向另一分子提供能量或从另一分子接受能量的分子。仅举例来说,荧光共振能量转移(fret)是偶极
‑
偶极偶合过程,通过所述过程荧光供体分子的激发态能量非辐射性地转移到未激发的受体分子,随后荧光性地以较长波长发射所提供的能量。
[0267]
术语“增强”意思是增加或延长所需作用的效力或持续时间。举例来说,“增强”治疗剂的作用是指增加或延长疾病、病症或病状的治疗过程中治疗剂作用的效力或持续时间的能力。如本文所使用,“增强有效量”是指足以增强疾病、病症或病状的治疗过程中治疗剂的作用的量。当用于患者时,用于此用途的有效量将视疾病、病症或病状的严重程度和病程、先前疗法、患者的健康状态和对药物的反应以及主治医生的判断而定。
[0268]
如本文所使用,术语“真核生物”是指属于系统发生真核领域的生物体,包括(但不限于)动物(包括(但不限于)哺乳动物、昆虫、爬行动物、鸟类等)、纤毛虫、植物(包括(但不限于)单子叶植物、双子叶植物和藻类)、真菌、酵母、鞭毛虫、小孢子虫和原生生物。
[0269]
如本文所使用,术语“脂肪酸”是指具有约c6或更长烃侧链的羧酸。
[0270]
如本文所使用,术语“荧光团”是指在激发后发射光子并且由此发荧光的分子。
[0271]
如本文所使用,术语“官能团”、“活性部分”、“活化基团”、“离去基团”、“反应位点”、“化学反应性基团”和“化学反应性部分”是指分子发生化学反应的部分或单元。所述术语在化学领域中于一定程度上同义,并且在本文中用于指示执行某种功能或活性并且可与其它分子反应的分子的部分。
[0272]
术语“卤素”包括氟、氯、碘和溴。
[0273]
如本文所使用,术语“卤酰基”是指含有卤素部分的酰基,包括(但不限于)
‑
c(o)ch3、
‑
c(o)cf3、
‑
c(o)ch2och3等。
[0274]
如本文所使用,术语“卤烷基”是指含有卤素部分的烷基,包括(但不限于)
‑
cf3和
‑
ch2cf3等。
[0275]
如本文所使用,术语“杂烷基”是指直链或支链或环状烃基或其组合,其是由烷基和至少一个选自由o、n、si和s组成的群组的杂原子组成,并且其中氮和硫原子可任选地被氧化并且氮杂原子可任选地被季铵化。杂原子o、n和s以及si可位于杂烷基的任何内部位置处或烷基与分子剩余部分连接的位置处。实例包括(但不限于)
‑
ch2‑
ch2‑
o
‑
ch3、
‑
ch2‑
ch2‑
nh
‑
ch3、
‑
ch2‑
ch2‑
n(ch3)
‑
ch3、
‑
ch2‑
s
‑
ch2‑
ch3、
‑
ch2‑
ch2、
‑
s(o)
‑
ch3、
‑
ch2‑
ch2‑
s(o)2‑
ch3、
‑
ch=ch
‑
o
‑
ch3、
‑
si(ch3)3、
‑
ch2‑
ch=n
‑
och3和
‑
ch=ch
‑
n(ch3)
‑
ch3。此外,最多两个杂原子可以是连续的,如
‑
ch2‑
nh
‑
och3和
‑
ch2‑
o
‑
si(ch3)3。
[0276]
术语“基于杂环的键”或“杂环键”是指由二羰基与二胺基团反应形成的部分。所得反应产物是杂环,包括杂芳基或杂环烷基。所得杂环基团充当非天然氨基酸或非天然氨基酸多肽与另一官能团之间的化学键。在一个实施例中,杂环键包括含氮杂环键,仅举例来说包括吡唑键、吡咯键、吲哚键、苯二氮卓键和吡唑啉酮键。
[0277]
类似地,术语“亚杂烷基”是指衍生自杂烷基的二价基团,例如(但不限于)
‑
ch2‑
ch2‑
s
‑
ch2‑
ch2‑
和
‑
ch2‑
s
‑
ch2‑
ch2‑
nh
‑
ch2‑
。对于亚杂烷基来说,相同或不同杂原子也可占据任一个或两个链末端(包括(但不限于)亚烷基氧基、亚烷基二氧基、亚烷基氨基、亚烷基二氨基、氨氧基亚烷基等)。另外,对于亚烷基和亚杂烷基连接基团来说,连接基团的化学式
所书写的方向并不表示连接基团的定向。举例来说,式
‑
c(o)2r'
‑
表示
‑
c(o)2r'
‑
和
‑
r'c(o)2‑
。
[0278]
如本文所使用,术语“杂芳基”或“杂芳香族”是指含有至少一个选自n、o和s的杂原子的芳基;其中氮和硫原子可任选地被氧化并且氮原子可被季铵化。杂芳基可被取代或不被取代。杂芳基可通过杂原子与分子的剩余部分连接。杂芳基的非限制性实例包括1
‑
吡咯基、2
‑
吡咯基、3
‑
吡咯基、3
‑
吡唑基、2
‑
咪唑基、4
‑
咪唑基、吡嗪基、2
‑
噁唑基、4
‑
噁唑基、2
‑
苯基
‑4‑
噁唑基、5
‑
噁唑基、3
‑
异噁唑基、4
‑
异噁唑基、5
‑
异噁唑基、2
‑
噻唑基、4
‑
噻唑基、5
‑
噻唑基、2
‑
呋喃基、3
‑
呋喃基、2
‑
噻吩基、3
‑
噻吩基、2
‑
吡啶基、3
‑
吡啶基、4
‑
吡啶基、2
‑
嘧啶基、4
‑
嘧啶基、5
‑
苯并噻唑基、嘌呤基、2
‑
苯并咪唑基、5
‑
吲哚基、1
‑
异喹啉基、5
‑
异喹啉基、2
‑
喹喔啉基、5
‑
喹喔啉基、3
‑
喹啉基和6
‑
喹啉基。
[0279]
如本文所使用,术语“均烷基(homoalkyl)”是指是烃基的烷基。
[0280]
如本文所使用,术语“一致”是指两个或两个以上序列或子序列相同。此外,如本文所使用,术语“实质上一致”是指当使用比较算法或通过手工比对和目测在比较窗或指定测量的区域上比较和比对最大相应性时,两个或两个以上具有相同的连续单元百分比的序列。仅举例来说,如果特定区域内的连续单元约60%一致、约65%一致、约70%一致、约75%一致、约80%一致、约85%一致、约90%一致或约95%一致,那么两个或两个以上序列可“实质上一致”。所述百分数用于描述两个或两个以上序列的“一致性百分比”。序列的一致性可存在于至少约75
‑
100个连续单元长的区域、约50个连续单元长的区域或(未指定时)整个序列内。此定义也是指测试序列的互补性。仅举例来说,当氨基酸残基相同时,两个或两个以上多肽序列一致;而如果指定区域内的氨基酸残基约60%一致、约65%一致、约70%一致、约75%一致、约80%一致、约85%一致、约90%一致或约95%一致,那么两个或两个以上多肽序列“实质上一致”。一致性可存在于至少约75到约100个氨基酸长的区域、约50个氨基酸长的区域或(未指定时)多肽序列的整个序列内。此外,仅举例来说,当核酸残基相同时,两个或两个以上多核苷酸序列一致;而如果指定区域内的核酸残基约60%一致、约65%一致、约70%一致、约75%一致、约80%一致、约85%一致、约90%一致或约95%一致,那么两个或两个以上多核苷酸序列“实质上一致”。一致性可存在于至少约75到约100个核酸长的区域、约50个核酸长的区域或(未指定时)多核苷酸序列的整个序列内。
[0281]
对于序列比较来说,通常一个序列充当与测试序列相比较的参考序列。当使用序列比较算法时,将测试序列和参考序列输入计算机内,必要时指定子序列坐标,并且指定序列算法程序参数。可使用默认程序参数,或者可指定替代参数。接着序列比较算法基于程序参数计算测试序列相对于参考序列的序列一致性百分比。
[0282]
如本文所使用,术语“免疫原性”是指对投与治疗药物的抗体反应。对治疗性非天然氨基酸多肽的免疫原性可使用供检测生物体液中抗非天然氨基酸多肽抗体用的定量和定性分析获得。所述分析包括(但不限于)放射免疫分析(ria)、酶联免疫吸附分析(elisa)、发光免疫分析(lia)和荧光免疫分析(fia)。对治疗性非天然氨基酸多肽的免疫原性分析涉及将投与治疗性非天然氨基酸多肽时的抗体反应与投与治疗性天然氨基酸多肽时的抗体反应比较。
[0283]
如本文所使用,术语“插入剂”(也称为“插入基团”)是指可插入分子的分子内间隙或者分子之间的分子间间隙的化学物质。仅举例来说,插入剂或基团可以是插入dna双螺旋
的堆叠碱基内的分子。
[0284]
如本文所使用,术语“分离”是指从非相关组分中分离并移出相关组分。分离物质可以是干燥状态或半干燥状态,或者是溶液(包括(但不限于)水溶液)的形式。分离组分可以是均质态,或分离组分可以是包含其它医药学上可接受的载体和/或赋形剂的医药组合物的一部分。可使用分析化学技术(包括(但不限于)聚丙烯酰胺凝胶电泳或高效液相色谱)测定纯度和均质性。此外,当分离出相关组分并且相关组分是制剂中存在的主要物质时,本文将所述组分描述为实质上经纯化。如本文所使用,术语“纯化”可指至少85%纯、至少90%纯、至少95%纯、至少99%纯或更纯的相关组分。仅举例来说,当核酸或蛋白质不含至少某些在天然状态下与其缔合的细胞组分或者已将核酸或蛋白质浓缩到高于其在体内或体外制造的浓度的水平时,所述核酸或蛋白质是“分离”的。同样,举例来说,当从与基因侧接并且编码除相关基因外的蛋白质的开放式阅读框分离时,基因是分离的。
[0285]
如本文所使用,术语“标记”是指并入化合物中并且易于检测,借此其物理分布可经检测和/或监测的物质。
[0286]
如本文所使用,术语“键”是指由连接基团的官能团与另一分子之间的化学反应形成的键结或化学部分。所述键结可包括(但不限于)共价键和非共价键,而所述化学部分可包括(但不限于)酯、碳酸酯、亚胺磷酸酯、腙、缩醛、原酸酯、肽键和寡核苷酸键。水解稳定的键意思是指所述键在水中实质上稳定并且在有用ph值下(包括(但不限于)在生理学条件下)一段较长时间内(可能甚至无限期)不与水反应。水解不稳定或可降解的键意思是所述键可在水或水溶液(包括例如血液)中降解。酶促不稳定或可降解的键意思是所述键可通过一种或一种以上酶降解。仅举例来说,peg和相关聚合物可在聚合物主链内或聚合物主链与聚合物分子的一个或一个以上末端官能团之间的连接基团中包括可降解键。所述可降解键包括(但不限于)由peg羧酸或活化peg羧酸与生物活性剂上的醇基反应而形成的酯键,其中所述酯基通常在生理学条件下水解以释放生物活性剂。其它水解可降解键包括(但不限于)碳酸酯键;由胺与醛反应产生的亚胺键;通过醇与磷酸基反应形成的磷酸酯键;作为酰肼与醛的反应产物的腙键;作为醛与醇的反应产物的缩醛键;作为甲酸酯与醇的反应产物的原酸酯键;由(包括(但不限于))聚合物(如peg)末端的胺基与肽的羧基形成的肽键;和由(包括(但不限于))聚合物末端的亚磷酰胺(phosphoramidite)基与寡核苷酸的5'羟基形成的寡核苷酸键。
[0287]
如本文所使用,术语“培养基(medium/media)”是指用于生长和收集细胞和/或所述细胞所表达和/或分泌的产物的任何培养基。所述“培养基”包括(但不限于)溶液、固体、半固体或刚性支撑物,其可支撑或含有任何宿主细胞,包括例如细菌宿主细胞、酵母宿主细胞、昆虫宿主细胞、植物宿主细胞、真核生物宿主细胞、哺乳动物宿主细胞、cho细胞、原核生物宿主细胞、大肠杆菌(e.coli)或假单胞菌(pseudomonas)宿主细胞和细胞内容物。所述“培养基”包括(但不限于)已生长宿主细胞、已分泌多肽的培养基,包括增殖步骤之前或之后的培养基。所述“培养基”还包括(但不限于)含有宿主细胞溶解产物(例如,细胞内产生的多肽)的缓冲液或试剂并且使宿主细胞溶解或破裂以释放多肽。
[0288]
如本文所使用,术语“代谢物”是指例如天然氨基酸多肽、非天然氨基酸多肽、经修饰的天然氨基酸多肽或经修饰的非天然氨基酸多肽的化合物的衍生物,其是在例如天然氨基酸多肽、非天然氨基酸多肽、经修饰的天然氨基酸多肽或经修饰的非天然氨基酸多肽的
化合物代谢时形成的。术语“医药学上活性代谢物”或“活性代谢物”是指例如天然氨基酸多肽、非天然氨基酸多肽、经修饰的天然氨基酸多肽或经修饰的非天然氨基酸多肽的化合物的生物活性衍生物,其是在例如天然氨基酸多肽、非天然氨基酸多肽、经修饰的天然氨基酸多肽或经修饰的非天然氨基酸多肽的所述化合物代谢时形成的。
[0289]
如本文所使用,术语“代谢”是指生物体改变特定物质的过程的统称。所述过程包括(但不限于)水解反应和酶催化的反应。有关代谢的其它信息可从治疗学的药理学基础(the pharmacological basis of therapeutics),第9版,麦格劳
‑
希尔(mcgraw
‑
hill)(1996)获得。仅举例来说,天然氨基酸多肽、非天然氨基酸多肽、经修饰的天然氨基酸多肽或经修饰的非天然氨基酸多肽的代谢物可通过以下方式来鉴别:对宿主投与天然氨基酸多肽、非天然氨基酸多肽、经修饰的天然氨基酸多肽或经修饰的非天然氨基酸多肽并分析来自宿主的组织样品;或者在体外孵育天然氨基酸多肽、非天然氨基酸多肽、经修饰的天然氨基酸多肽或经修饰的非天然氨基酸多肽与肝细胞并分析所得化合物。
[0290]
如本文所使用,术语“金属螯合剂”是指与金属离子形成金属络合物的分子。举例来说,所述分子可与中心金属离子形成两个或两个以上配位键并且可形成环结构。
[0291]
如本文所使用,术语“含金属部分”是指含有金属离子、原子或粒子的基团。所述部分包括(但不限于)顺铂(cisplatin)、螯合金属离子(如镍、铁和铂)和金属纳米粒子(如镍、铁和铂)。
[0292]
如本文所使用,术语“并有重原子的部分”是指并有通常比碳重的原子的离子的基团。所述离子或原子包括(但不限于)硅、钨、金、铅和铀。
[0293]
如本文所使用,术语“修饰”是指存在对天然氨基酸、非天然氨基酸、天然氨基酸多肽或非天然氨基酸多肽的改变。可通过天然氨基酸、非天然氨基酸、天然氨基酸多肽或非天然氨基酸多肽的合成后修饰或共翻译,或天然氨基酸、非天然氨基酸、天然氨基酸多肽或非天然氨基酸多肽的翻译后修饰来获得所述改变或修饰。形式“修饰或未修饰”意思指所讨论的天然氨基酸、非天然氨基酸、天然氨基酸多肽或非天然氨基酸多肽任选地经修饰,也就是说,所讨论的天然氨基酸、非天然氨基酸、天然氨基酸多肽或非天然氨基酸多肽可经修饰或不经修饰。
[0294]
如本文所使用,术语“经调节的血清半衰期”是指经修饰的生物活性分子相对于其未经修饰形式的循环半衰期的正或负改变。举例来说,经修饰的生物活性分子包括(但不限于)天然氨基酸、非天然氨基酸、天然氨基酸多肽或非天然氨基酸多肽。举例来说,通过在投与生物活性分子或经修饰的生物活性分子后各个时间点时取得血液样品,并且测定每个样品中所述分子的浓度来测量血清半衰期。血清浓度与时间的相关性允许计算血清半衰期。举例来说,经调节的血清半衰期可以是血清半衰期增加,其能够实现改进的给药方案或避免毒性作用。所述血清的增加可以是至少约2倍、至少约3倍、至少约5倍或至少约10倍。用于评估血清半衰期增加的方法的非限制性实例在实例33中给出。此方法可用于评估任何多肽的血清半衰期。
[0295]
如本文所使用,术语“经调节的治疗半衰期”是指治疗有效量的经修饰生物活性分子相对于其未经修饰形式的半衰期的正或负改变。举例来说,经修饰的生物活性分子包括(但不限于)天然氨基酸、非天然氨基酸、天然氨基酸多肽或非天然氨基酸多肽。举例来说,通过测量投药后各个时间点时分子的药物动力学和/或药效性质来测量治疗半衰期。增加
的治疗半衰期能够实现特别有益的给药方案、特别有益的总剂量或者避免不合需要的作用。举例来说,增加治疗半衰期可由增加效力、增加或降低经修饰分子与其标靶的结合、增加或降低未经修饰分子的另一参数或作用机制或者增加或降低酶(仅举例来说,蛋白酶)对分子的降解而引起。用于评估治疗半衰期增加的方法的非限制性实例在实例33中给出。此方法可用于评估任何多肽的治疗半衰期。
[0296]
如本文所使用,术语“纳米粒子”是指粒径介于约500nm到约1nm之间的粒子。
[0297]
如本文所使用,术语“近化学计量”是指参与化学反应的化合物的摩尔比是约0.75到约1.5。
[0298]
如本文所使用,术语“非真核生物”是指非真核生物体。举例来说,非真核生物体可属于真细菌(其包括(但不限于)大肠杆菌(escherichia coli)、极端嗜热菌(thermus thermophilius)或嗜热脂肪芽孢杆菌(bacillus stearothermophilus)、荧光假单胞杆菌(pseudomonas fluorescens)、铜绿假单胞菌(pseudomonas aeruginosa)、恶臭假单胞菌(pseudomonas putida))系统发生域;或古细菌(其包括(但不限于)詹氏甲烷球菌(methanococcus jannaschii)、嗜热自养甲烷杆菌(methanobacterium thermoautotrophicum)、闪烁古生球菌(archaeoglobus fulgidus)、激烈火球菌(pyrococcus furiosus)、堀越火球菌(pyrococcus horikoshii)、嗜热泉生古细菌(aeuropyrum pernix)或嗜盐菌(halobacterium)(如沃氏嗜盐富饶菌(haloferax volcanii)和嗜盐菌属nrc
‑
1(halobacterium species nrc
‑
1)))或系统发生域。
[0299]“非天然氨基酸”是指不是20种常见氨基酸或者吡咯赖氨酸或硒代半胱氨酸中的一种的氨基酸。可与术语“非天然氨基酸(non
‑
natural amino acid)”同义使用的其它术语是“非天然编码的氨基酸”、“非天然氨基酸(unnatural amino acid)”、“非天然存在的氨基酸”以及其各种以连字符连接和未用连字符连接的形式。术语“非天然氨基酸”包括(但不限于)通过修饰天然编码的氨基酸(包括(但不限于)20种常见氨基酸或吡咯赖氨酸和硒代半胱氨酸)而天然存在,但本身未通过翻译复合物并入生长的多肽链中的氨基酸。并非天然编码的天然存在的氨基酸的实例包括(但不限于)n
‑
乙酰氨基葡萄糖基
‑
l
‑
丝氨酸、n
‑
乙酰氨基葡萄糖基
‑
l
‑
苏氨酸和o
‑
磷酸酪氨酸。此外,术语“非天然氨基酸”包括(但不限于)天然不存在并且可以合成方式获得或者可通过修饰非天然氨基酸而获得的氨基酸。
[0300]
如本文所使用,术语“核酸”是指单链或双链形式的脱氧核糖核苷酸、脱氧核糖核苷、核糖核苷或核糖核苷酸以及其聚合物。仅举例来说,所述核酸和核酸聚合物包括(但不限于)(i)天然核苷酸的类似物,其具有与参考核酸相似的结合性质并且以与天然存在的核苷酸相似的方式代谢;(ii)寡核苷酸类似物,包括(但不限于)pna(肽基核酸)、用于反义技术中的dna类似物(硫代磷酸酯、氨基磷酸酯等);(iii)其保守修饰变体(包括(但不限于)简并密码子取代)和互补序列以及明确描述的序列。举例来说,可通过产生一个或一个以上(或所有)所选密码子的第三位被混合碱基和/或脱氧肌苷残基取代的序列来实现简并密码子取代(巴策尔(batzer)等人,核酸研究19:5081(1991);大冢(ohtsuka)等人,生物化学杂志(j.biol.chem.)260:2605
‑
2608(1985);和罗索利尼(rossolini)等人,分子细胞探针(mol.cell.probes)8:91
‑
98(1994))。
[0301]
如本文所使用,术语“氧化剂”是指能够从经氧化的化合物中去除电子的化合物或物质。举例来说,氧化剂包括(但不限于)经氧化的谷胱甘肽、胱氨酸、胱胺、经氧化的二硫苏
糖醇、经氧化的赤藓醇和氧。各种氧化剂适用于本文所述的方法和组合物。
[0302]
如本文所使用,术语“医药学上可接受的”是指包括(但不限于)盐、载体或稀释剂的物质,其不消除化合物的生物活性或性质并且相对无毒,即所述物质可投与个体而不引起不合需要的生物学作用或与含有其的组合物中的任何组分以有害方式相互作用。
[0303]
如本文所使用,术语“光亲和标记”是指具有当曝光时与标记对其具有亲和性的分子形成键的基团的标记。仅举例来说,所述键可以是共价键或非共价键。
[0304]
如本文所使用,术语“光笼蔽部分”是指当以某种波长照射时共价或非共价结合其它离子或分子的基团。
[0305]
如本文所使用,术语“可光裂解基团”是指当曝光时断裂的基团。
[0306]
如本文所使用,术语“光交联剂”是指包含两个或两个以上官能团的化合物,所述官能团可在曝光时反应并且与两个或两个以上单体或聚合分子形成共价或非共价键。
[0307]
如本文所使用,术语“可光异构化部分”是指光照时由一种异构形式变为另一种异构形式的基团。
[0308]
如本文所使用,术语“聚亚烷基二醇”是指线性或分支聚合的聚醚多元醇。所述聚亚烷基二醇包括(但不限于)聚乙二醇、聚丙二醇、聚丁二醇和其衍生物。其它例示性实施例列于例如商业供应商目录中,如希尔沃特公司(shearwater corporation)的目录“用于生物医学应用的聚乙二醇和衍生物(polyethylene glycol and derivatives for biomedical applications)”(2001)。仅举例来说,所述聚合聚醚多元醇具有介于约0.1kda到约100kda之间的平均分子量。举例来说,所述聚合聚醚多元醇包括(但不限于)介于约100da与约100,000da之间或100,000da以上。聚合物的分子量可介于约100da与约100,000da之间,包括(但不限于)约100,000da、约95,000da、约90,000da、约85,000da、约80,000da、约75,000da、约70,000da、约65,000da、约60,000da、约55,000da、约50,000da、约45,000da、约40,000da、约35,000da、约30,000da、约25,000da、约20,000da、约15,000da、约10,000da、约9,000da、约8,000da、约7,000da、约6,000da、约5,000da、约4,000da、约3,000da、约2,000da、约1,000da、约900da、约800da、约700da、约600da、约500da、400da、约300da、约200da和约100da。在一些实施例中,聚合物的分子量介于约100da与约50,000da之间。在一些实施例中,聚合物的分子量介于约100da与约40,000da之间。在一些实施例中,聚合物的分子量介于约1,000da与约40,000da之间。在一些实施例中,聚合物的分子量介于约2,000da与约50,000da之间。在一些实施例中,聚合物的分子量介于约5,000da与约40,000da之间。在一些实施例中,聚合物的分子量介于约10,000da与约40,000da之间。在一些实施例中,聚(乙二醇)分子是分支聚合物。支链peg的分子量可介于约1,000da与约100,000da之间,包括(但不限于)约100,000da、约95,000da、约90,000da、约85,000da、约80,000da、约75,000da、约70,000da、约65,000da、约60,000da、约55,000da、约50,000da、约45,000da、约40,000da、约35,000da、约30,000da、约25,000da、约20,000da、约15,000da、约10,000da、约9,000da、约8,000da、约7,000da、约6,000da、约5,000da、约4,000da、约3,000da、约2,000da和约1,000da。在一些实施例中,支链peg的分子量介于约1,000da与约50,000da之间。在一些实施例中,支链peg的分子量介于约1,000da与约40,000da之间。在一些实施例中,支链peg的分子量介于约5,000da与约40,000da之间。在一些实施例中,支链peg的分子量介于约5,000da与约20,000da之间。在其它实施例中,支链peg的分子量介于约2,000da与约50,
000da之间。
[0309]
如本文所使用,术语“聚合物”是指由重复亚单元构成的分子。所述分子包括(但不限于)多肽、多核苷酸或多糖或者聚亚烷基二醇。
[0310]
术语“多肽”、“肽”和“蛋白质”在本文中可互换使用以指代氨基酸残基的聚合物。也就是说,针对多肽的描述同样适用于肽的描述和蛋白质的描述,并且反之亦然。所述术语适用于天然存在的氨基酸聚合物以及一个或一个以上氨基酸残基是非天然氨基酸的氨基酸聚合物。此外,所述“多肽”、“肽”和“蛋白质”包括任何长度的氨基酸链,包括全长蛋白质,其中氨基酸残基是通过共价肽键连接。
[0311]
术语“翻译后修饰”是指在天然或非天然氨基酸已以翻译方式并入多肽链后发生的对所述氨基酸的任何修饰。所述修饰包括(但不限于)共翻译体内修饰、共翻译体外修饰(如在无细胞翻译系统中)、翻译后体内修饰和翻译后体外修饰。
[0312]
如本文所使用,术语“前药”或“医药学上可接受的前药”是指在体内或体外转化成母体药物的药剂,其中其不会消除药物的生物活性或性质并且相对无毒,即所述物质可投与个体而不引起不合需要的生物学作用或与含有其的组合物中的任何组分以有害方式相互作用。前药通常是药物前体,在投与个体和后续吸收之后,其通过一些过程转化成活性或更大活性的物质,如通过代谢路径转化。一些前药具有存在于前药上使所述前药活性较小和/或赋予药物溶解性或一些其它性质的化学基团。当所述化学基团自前药裂解和/或经修饰时,产生活性药物。前药在体内通过酶促或非酶促反应转化为活性药物。前药可提供改进的生理化学性质,如更好的溶解性、增强的传递特征(如特异性靶向特定细胞、组织、器官或配体)和改进的药物治疗学价值。所述前药的益处包括(但不限于)(i)与母体药物相比易于投药;(ii)前药可通过口服投与而为生物可利用的,但母体药物不行;和(iii)与母体药物相比,前药在医药组合物中还可具有改进的溶解性。前药包括药理学上无活性或活性降低的活性药物衍生物。前药可被设计成通过操控药物性质(如生理化学、生物医药或药物动力学性质)来调节到达所需作用位点的药物或生物活性分子的量。前药的一个实例(非限制性)将是以酯(“前药”)形式投与以促进跨细胞膜传送的非天然氨基酸多肽,在细胞膜中水溶性不利于移动性,但所述酯接着在进入水溶性有利的细胞内部后经代谢水解为羧酸(活性实体)。前药可设计为可逆的药物衍生物,作为调节剂用于增强药物转运到位点特异性组织。
[0313]
如本文所使用,术语“防治有效量”是指防治性地应用于患者的含有至少一个非天然氨基酸多肽或至少一个经修饰的非天然氨基酸多肽的组合物的量,其将在一定程度上缓解所治疗的疾病、病状或病症的一种或一种以上症状。在所述防治应用中,所述量可视患者的健康状态、体重等而定。所属领域的技术人员将充分考虑到,通过常规实验(包括(但不限于)剂量增加临床试验)可确定所述防治有效量。
[0314]
如本文所使用,术语“经保护的”是指存在防止化学反应性官能团在某些反应条件下反应的“保护基”或部分。保护基将视所保护的化学反应性基团的类型而变化。仅举例来说,(i)如果化学反应性基团是胺或酰肼,那么保护基可选自叔丁氧羰基(t
‑
boc)和9
‑
芴基甲氧基羰基(fmoc);(ii)如果化学反应性基团是硫醇,那么保护基可以是邻吡啶基二硫化物;并且(iii)如果化学反应性基团是羧酸(如丁酸或丙酸)或羟基,那么保护基可以是苯甲基或烷基(如甲基、乙基或叔丁基)。
[0315]
仅举例来说,阻断/保护基可选自:
[0316][0317]
此外,保护基包括(但不限于)包括光不稳定基团,如nvoc和menvoc以及所属领域已知的其它保护基。其它保护基描述于格林(greene)和伍兹(wuts),有机合成中的保护基(protective groups in organic synthesis),第3版,纽约州纽约的约翰威利父子公司(john wiley&sons,new york,ny),1999中,所述文献以全文引用的方式并入本文中。
[0318]
如本文所使用,术语“放射性部分”是指原子核自发地放出核辐射(如α、β或γ粒子)的基团;其中α粒子是氦核,β粒子是电子,并且γ粒子是高能光子。
[0319]
如本文所使用,术语“反应性化合物”是指在适当条件下对另一原子、分子或化合物具有反应性的化合物。
[0320]
术语“重组宿主细胞”(也称为“宿主细胞”)是指包括外源多核苷酸的细胞,其中用于将外源多核苷酸插入细胞中的方法包括(但不限于)直接摄取、转导、f配对或所属领域中已知的产生重组宿主细胞的其它方法。仅举例来说,所述外源多核苷酸可以是非整合载体,包括(但不限于)质粒;或可整合到宿主基因组中。
[0321]
如本文所使用,术语“氧化还原活性剂”是指氧化或还原另一分子的分子,由此氧化还原活性剂变成还原或氧化态。氧化还原活性剂的实例包括(但不限于)二茂铁、醌、ru
2 /3
络合物、co
2 /3
络合物和os
2 /3
络合物。
[0322]
如本文所使用,术语“还原剂”是指能够将电子加到所还原的化合物中的化合物或物质。举例来说,还原剂包括(但不限于)二硫苏糖醇(dtt)、2
‑
巯基乙醇、二硫赤藓醇、半胱氨酸、半胱胺(2
‑
氨基乙硫醇)和经还原的谷胱甘肽。所述还原剂可用于(仅举例来说)使巯基保持在还原态并且还原分子内或分子间二硫键。
[0323]
如本文所使用,“再折叠”描述将未适当折叠或展开状态转化成天然或适当折叠的构象的任何过程、反应或方法。仅举例来说,就二硫键来说,再折叠将含有二硫键的多肽由未适当折叠或展开状态转化成天然或适当折叠的构象。所述含有二硫键的多肽可以是天然氨基酸多肽或非天然氨基酸多肽。
[0324]
如本文所使用,术语“树脂”是指高分子量的不可溶聚合物珠粒。仅举例来说,所述珠粒可用作固相肽合成的支撑物或在纯化前连接分子的部位。
[0325]
如本文所使用,术语“糖”是指一系列碳水化合物,包括(但不限于)糖、单糖、寡糖和多糖。
[0326]
如本文所使用,术语“安全性”或“安全概況”是指相对于已投与药物的次数可能与药物投与有关的副作用。举例来说,已多次投与并且仅产生适度或无副作用的药物据称具有极佳安全概況。评估安全概況的方法的一个非限制性实例在实例26中给出。此方法可用于评估任何多肽的安全概況。
[0327]
如本文所使用,短语“与
……
选择性杂交”或“与
……
特异性杂交”是指当特定核苷酸序列存在于包括(但不限于)全细胞或者文库dna或rna的复杂混合物中时,一个分子与所述序列在严格杂交条件下结合、形成双链体或杂交。
[0328]
如本文所使用,术语“自旋标记”是指含有展现可通过电子自旋共振光谱检测的未配对电子自旋(即,稳定的顺磁性基团)的一个原子或一组原子并且可与另一分子连接的分子。所述自旋标记分子包括(但不限于)硝酰基和硝基氧并且可以是单自旋标记或双自旋标记。
[0329]
如本文所使用,术语“化学计量”是指参与化学反应的化合物的摩尔比是约0.9到约1.1。
[0330]
如本文所使用,术语“类化学计量”是指在反应条件改变时或者在存在添加剂的情况下变为化学计量或近化学计量的化学反应。所述反应条件的改变包括(但不限于)温度的增加或ph值的改变。所述添加剂包括(但不限于)加速剂。
[0331]
短语“严格杂交条件”是指dna、rna、pna或其它核酸模拟物或其组合的序列在低离子强度和高温条件下的杂交。举例来说,在严格条件下,探针将与其在核酸的复杂混合物(包括(但不限于)全细胞或文库dna或rna)中的靶序列杂交,但不与在复杂混合物中的其它序列杂交。严格条件是序列依赖性的并且将随不同环境而不同。举例来说,较长的序列在较高温度下特异性杂交。严格杂交条件包括(但不限于)(i)在指定离子强度和ph值下比特定序列的热熔点(tm)低约5
‑
10℃;(ii)在约ph 7.0到约ph 8.3下盐浓度是约0.01m到约1.0m,并且对于短探针(包括(但不限于)约10到约50个核苷酸)来说温度是至少约30℃,并且对于长探针(包括(但不限于)大于50个核苷酸)来说温度是至少约60℃;(iii)加入去稳定剂,包括(但不限于)甲酰胺;(iv)50%甲酰胺、5
×
ssc和1%sds,在42℃下孵育;或5
×
ssc、约1%sds,在65℃下孵育,并且在65℃下在0.2
×
ssc和约0.1%sds中洗涤,持续介于约5分钟到约120分钟之间的时间。仅举例来说,选择性或特异性杂交的检测包括(但不限于)至少两倍于背景的正信号。有关核酸杂交的广泛指导见于蒂森(tijssen),生物化学和分子生物学的实验室技术——与核酸探针杂交(laboratory techniques in biochemistry and molecular biology
‑‑
hybridization with nucleic probes),“杂交原理和核酸分子分析策略的综述(overview of principles of hybridization and the strategy of nucleic acid assays)”(1993)中。
[0332]
如本文所使用,术语“个体”是指作为治疗、观察或实验对象的动物。仅举例来说,个体可以是(但不限于)哺乳动物,包括(但不限于)人类。
[0333]
如本文所使用,术语“实质上经纯化”是指可实质上或基本上不含在纯化前通常伴随相关组分或与相关组分相互作用的其它组分的相关组分。仅举例来说,当相关组分的制剂含有小于约30%、小于约25%、小于约20%、小于约15%、小于约10%、小于约5%、小于约
4%、小于约3%、小于约2%或小于约1%(以干重计)污染组分时,相关组分可以是“实质上经纯化”的。因此,“实质上经纯化”的相关组分可具有约70%、约75%、约80%、约85%、约90%、约95%、约96%、约97%、约98%、约99%或更高的纯度水平。仅举例来说,可从天然细胞或在重组产生的天然氨基酸多肽或非天然氨基酸多肽的情况下从宿主细胞中纯化出天然氨基酸多肽或非天然氨基酸多肽。举例来说,当天然氨基酸多肽或非天然氨基酸多肽的制剂含有小于约30%、小于约25%、小于约20%、小于约15%、小于约10%、小于约5%、小于约4%、小于约3%、小于约2%或小于约1%(以干重计)污染物质时,所述制剂可以是“实质上经纯化”的。举例来说,当通过宿主细胞重组产生天然氨基酸多肽或非天然氨基酸多肽时,天然氨基酸多肽或非天然氨基酸多肽可以占细胞干重约30%、约25%、约20%、约15%、约10%、约5%、约4%、约3%、约2%或约1%或1%以下存在。举例来说,当通过宿主细胞重组产生天然氨基酸多肽或非天然氨基酸多肽时,天然氨基酸多肽或非天然氨基酸多肽可以占细胞干重约5g/l、约4g/l、约3g/l、约2g/l、约1g/l、约750mg/l、约500mg/l、约250mg/l、约100mg/l、约50mg/l、约10mg/l或约1mg/l或1mg/l以下存在于培养基中。举例来说,如通过适当方法(包括(但不限于)sds/page分析、rp
‑
hplc、sec和毛细管电泳)所测定,“实质上经纯化”的天然氨基酸多肽或非天然氨基酸多肽可具有约30%、约35%、约40%、约45%、约50%、约55%、约60%、约65%、约70%、约75%、约80%、约85%、约90%、约95%、约99%或更高的纯度水平。
[0334]
术语“取代基”(也称为“无干扰取代基”)是指可用于置换分子上的另一基团的基团。所述基团包括(但不限于)卤基、c1‑
c
10
烷基、c2‑
c
10
烯基、c2‑
c
10
炔基、c1‑
c
10
烷氧基、c5‑
c
12
芳烷基、c3‑
c
12
环烷基、c4‑
c
12
环烯基、苯基、经取代的苯基、甲苯酰基、二甲苯基、联苯基、c2‑
c
12
烷氧基烷基、c5‑
c
12
烷氧基芳基、c5‑
c
12
芳氧基烷基、c7‑
c
12
氧基芳基、c1‑
c6烷基亚磺酰基、c1‑
c
10
烷基磺酰基、
‑
(ch2)
m
‑
o
‑
(c1‑
c
10
烷基)(其中m是1到8)、芳基、经取代的芳基、经取代的烷氧基、氟烷基、杂环基、经取代的杂环基、硝基烷基、
‑
no2、
‑
cn、
‑
nrc(o)
‑
(c1‑
c
10
烷基)、
‑
c(o)
‑
(c1‑
c
10
烷基)、c2‑
c
10
烷硫基烷基、
‑
c(o)o
‑
(c1‑
c
10
烷基)、
‑
oh、
‑
so2、=s、
‑
cooh、
‑
nr2、羰基、
‑
c(o)
‑
(c1‑
c
10
烷基)
‑
cf3、
‑
c(o)
‑
cf3、
‑
c(o)nr2、
‑
(c1‑
c
10
芳基)
‑
s
‑
(c6‑
c
10
芳基)、
‑
c(o)
‑
(c6‑
c
10
芳基)、
‑
(ch2)
m
‑
o
‑
(ch2)
m
‑
o
‑
(c1‑
c
10
烷基)(其中每个m是1到8)、
‑
c(o)nr2、
‑
c(s)nr2、
‑
so2nr2、
‑
nrc(o)nr2、
‑
nrc(s)nr2、其盐等。前述清单中的每个r基团包括(但不限于)h、烷基或经取代的烷基、芳基或经取代的芳基或烷芳基。当通过从左向右书写的常规化学式说明取代基时,其同样涵盖由从右向左书写结构所得到的在化学上相同的取代基;例如,
‑
ch2o
‑
相当于
‑
och2‑
。
[0335]
仅举例来说,烷基和杂烷基(包括称为亚烷基、烯基、亚杂烷基、杂烯基、炔基、环烷基、杂环烷基、环烯基和杂环烯基的基团)的取代基包括(但不限于):
‑
or、=o、=nr、=n
‑
or、
‑
nr2、
‑
sr、
‑
卤素、
‑
sir3、
‑
oc(o)r、
‑
c(o)r、
‑
co2r、
‑
conr2、
‑
oc(o)nr2、
‑
nrc(o)r、
‑
nr
‑
c(o)nr2、
‑
nr(o)2r、
‑
nr
‑
c(nr2)=nr、
‑
s(o)r、
‑
s(o)2r、
‑
s(o)2nr2、
‑
nrso2r、
‑
cn和
‑
no2。前述清单中的每个r基团包括(但不限于)氢、经取代的或未经取代的杂烷基、经取代的或未经取代的芳基(包括(但不限于)被1
‑
3个卤素取代的芳基)、经取代的或未经取代的烷基、烷氧基或硫烷氧基或芳烷基。当将两个r基团连接到相同氮原子时,其可与氮原子组合形成5、6或7元环。举例来说,
‑
nr2意欲包括(但不限于)1
‑
吡咯烷基和4
‑
吗啉基。
[0336]
举例来说,芳基和杂芳基的取代基包括(但不限于)
‑
or、=o、=nr、=n
‑
or、
‑
nr2、
‑
sr、
‑
卤素、
‑
sir3、
‑
oc(o)r、
‑
c(o)r、
‑
co2r、
‑
conr2、
‑
oc(o)nr2、
‑
nrc(o)r、
‑
nr
‑
c(o)nr2、
‑
nr(o)2r、
‑
nr
‑
c(nr2)=nr、
‑
s(o)r、
‑
s(o)2r、
‑
s(o)2nr2、
‑
nrso2r、
‑
cn、
‑
no2、
‑
r、
‑
n3、
‑
ch(ph)2、氟(c1‑
c4)烷氧基和氟(c1‑
c4)烷基,其数量是零到芳香族环系统上开放价态的总数;并且其中前述清单中的每个r基团包括(但不限于)氢、烷基、杂烷基、芳基和杂芳基。
[0337]
如本文所使用,术语“治疗有效量”是指投与已罹患疾病、病状或病症的患者的含有至少一个非天然氨基酸多肽和/或至少一个经修饰的非天然氨基酸多肽的组合物的量,其足以治愈或至少部分遏制或在一定程度上缓解所治疗的疾病、病症或病状的一种或一种以上症状。所述组合物的效用视包括(但不限于)疾病、病症或病状的严重程度和病程、先前疗法、患者的健康状态和对药物的反应以及主治医生的判断的情况而定。仅举例来说,治疗有效量可通过常规实验(包括(但不限于)剂量增加临床试验)来确定。
[0338]
如本文所使用,术语“硫烷氧基”是指通过氧原子与分子连接的含硫烷基。
[0339]
术语“热熔点”或tm是平衡时50%与标靶互补的探针与靶序列杂交的温度(在指定离子强度、ph值和核酸浓度下)。
[0340]
如本文所使用,术语“毒性部分”或“毒性基团”是指可引起伤害、紊乱或死亡的化合物。毒性部分包括(但不限于)奥利斯坦(auristatin)、dna小沟结合剂、dna小沟烷化剂、烯二炔、来西托辛(lexitropsin)、倍癌霉素(duocarmycin)、紫杉烷(taxane)、嘌呤霉素(puromycin)、海兔毒素、类美登素(maytansinoid)、长春花生物碱(vinca alkaloid)、afp、mmaf、mmae、aeb、aevb、奥利斯坦e、太平洋紫杉醇(paclitaxel)、多烯紫杉醇(docetaxel)、cc
‑
1065、sn
‑
38、拓朴替康(topotecan)、n
‑
吗啉基
‑
阿霉素、根瘤菌素(rhizoxin)、氰基
‑
n
‑
吗啉基
‑
阿霉素、海兔毒素
‑
10、棘霉素(echinomycin)、康普立停(combretatstatin)、卡奇霉素(chalicheamicin)、美登素(maytansine)、dm
‑
1、纺锤菌素(netropsin)、鬼臼毒素(podophyllotoxin)(例如依托泊苷(etoposide)、替尼泊苷(teniposide)等)、浆果赤霉素和其衍生物、抗微管蛋白剂、奎托非辛(cryptophysin)、康普瑞汀(combretastatin)、奥利斯坦e、长春新碱(vincristine)、长春碱(vinblastine)、长春地辛(vindesine)、长春瑞滨(vinorelbine)、vp
‑
16、喜树碱(camptothecin)、艾普塞隆(epothilone)a、艾普塞隆b、诺考达唑(nocodazole)、秋水仙碱(colchicine)、秋水仙胺(colcemid)、雌莫司汀(estramustine)、西马多丁(cemadotin)、圆皮海绵内酯(discodermolide)、美登素、艾榴素(eleutherobin)、二氯甲基二乙胺(mechlorethamine)、环磷酰胺(cyclophosphamide)、美法仑(melphalan)、卡莫司汀(carmustine)、洛莫司汀(lomustine)、司莫司汀(semustine)、链脲菌素(streptozocin)、氯脲霉素(chlorozotocin)、尿嘧啶氮芥(uracil mustard)、氮芥(chlormethine)、异环磷酰胺(ifosfamide)、苯丁酸氮芥(chlorambucil)、哌泊溴烷(pipobroman)、三亚乙基三聚氰胺、三亚乙基硫代磷胺、白消安(busulfan)、达卡巴嗪(dacarbazine)和替莫唑胺(temozolomide)、阿糖胞苷(cytarabine)、胞嘧啶阿拉伯糖(cytosine arabinoside)、氟尿嘧啶(fluorouracil)、氮尿苷(floxuridine)、6
‑
硫鸟嘌呤、6
‑
巯基嘌呤、喷司他丁(pentostatin)、5
‑
氟尿嘧啶、甲氨喋呤(methotrexate)、10
‑
炔丙基
‑
5,8
‑
二氮杂叶酸、5,8
‑
二氮杂四氢叶酸、甲酰四氢叶酸(leucovorin)、磷酸氟达拉滨、喷司他丁、吉西他滨(gemcitabine)、ara
‑
c、太平洋紫杉醇、多烯紫杉醇、去氧柯福霉素(deoxycoformycin)、丝裂霉素(mitomycin)
‑
c、l
‑
天冬酰胺酶、硫唑嘌呤、布喹那(brequinar)、抗生素(例如蒽环霉素(anthracycline)、庆大霉素(gentamicin)、头孢噻吩
(cefalotin)、万古霉素(vancomycin)、特拉万星(telavancin)、达托霉素(daptomycin)、阿奇霉素(azithromycin)、红霉素(erythromycin)、罗红霉素(rocithromycin)、呋喃唑酮(furazolidone)、阿莫西林(amoxicillin)、氨苄青霉素(ampicillin)、羧苄青霉素(carbenicillin)、氟氯西林(flucloxacillin)、甲氧西林(methicillin)、青霉素(penicillin)、环丙沙星(ciprofloxacin)、莫西沙星(moxifloxacin)、氧氟沙星(ofloxacin)、多西环素(doxycycline)、米诺环素(minocycline)、氧四环素(oxytetracycline)、四环素(tetracycline)、链霉素(streptomycin)、利福布汀(rifabutin)、乙胺丁醇(ethambutol)、利福昔明(rifaximin)等)、抗病毒药物(例如阿巴卡韦(abacavir)、阿昔洛韦(acyclovir)、安普利根(ampligen)、西多福韦(cidofovir)、地拉韦啶(delavirdine)、去羟肌苷(didanosine)、依法韦仑(efavirenz)、因提弗(entecavir)、膦乙酸盐(fosfonet)、更昔洛韦(ganciclovir)、伊巴他滨(ibacitabine)、依莫诺维(imunovir)、碘苷(idoxuridine)、肌苷(inosine)、洛匹那韦(lopinavir)、美替沙腙(methisazone)、纳泽维尔(nexavir)、奈韦拉平(nevirapine)、奥司他韦(oseltamivir)、喷昔洛韦(penciclovir)、司他夫定(stavudine)、曲氟尿苷(trifluridine)、特鲁瓦达(truvada)、伐昔洛韦(valaciclovir)、扎那米韦(zanamivir)等)、盐酸道诺霉素(daunorubicin hydrochloride)、道诺霉素、柔红霉素(rubidomycin)、盐酸正定霉素(cerubidine)、艾达霉素(idarubicin)、阿霉素、表柔比星(epirubicin)和n
‑
吗啉基衍生物、吩噁嗪酮双环肽(例如放线菌素d(dactinomycin))、碱性糖肽(例如博莱霉素(bleomycin))、蒽醌糖苷(例如普卡霉素(plicamycin)、光神霉素(mithramycin))、蒽醌(例如米托蒽醌(mitoxantrone))、氮丙啶并吡咯并吲哚二酮(azirinopyrrolo indoledione)(例如丝裂霉素)、巨环免疫抑制剂(例如环孢素(cyclosporine)、fk
‑
506、他克莫司(tacrolimus)、普乐可复(prograf)、雷帕霉素(rapamycin)等)、诺维本(navelbene)、cpt
‑
11、阿那曲唑(anastrazole)、来曲唑(letrazole)、卡培他滨(capecitabine)、雷洛昔芬(reloxafine)、环磷酰胺、异环磷酰胺(ifosamide)、屈洛昔芬(droloxafine)、别秋水仙碱(allocolchicine)、软海绵素(halichondrin)b、秋水仙碱、秋水仙碱衍生物、美登素、根瘤菌素、太平洋紫杉醇、太平洋紫杉醇衍生物、多烯紫杉醇、硫代秋水仙碱、三苯甲基半胱氨酸、硫酸长春碱、硫酸长春新碱、顺铂、卡铂、羟基脲、n
‑
甲基肼、表叶毒素(epidophyllotoxin)、丙卡巴肼(procarbazine)、米托蒽醌、甲酰四氢叶酸和喃氟啶(tegafur)。“紫杉烷”包括太平洋紫杉醇以及任何活性紫杉烷衍生物或前药。
[0341]
如本文所使用,术语“治疗”包括缓和、减轻或改善疾病或病状的症状;预防其它症状;改善或预防症状的潜在代谢病因;抑制疾病或病状,例如使疾病或病状的发展停滞;缓解疾病或病状;引起疾病或病状的消退;缓解由疾病或病状引起的症象;或者停止疾病或病状的症状。术语“治疗”包括(但不限于)防治性和/或治疗性治疗。
[0342]
如本文所使用,术语“水溶性聚合物”是指可溶于水性溶剂的任何聚合物。所述水溶性聚合物包括(但不限于)聚乙二醇、聚乙二醇丙醛、其单c1‑
c
10
烷氧基或芳氧基衍生物(描述于美国专利第5,252,714号中,其以引用的方式并入本文中)、单甲氧基
‑
聚乙二醇、聚乙烯吡咯烷酮、聚乙烯醇、聚氨基酸、二乙烯基醚马来酸酐、n
‑
(2
‑
羟基丙基)
‑
甲基丙烯酰胺、葡聚糖、葡聚糖衍生物(包括硫酸葡聚糖)、聚丙二醇、聚环氧丙烷/环氧乙烷共聚物、聚氧乙基化多元醇、肝素、肝素片段、多糖、寡糖、聚糖、纤维素和纤维素衍生物(包括(但不限
于)甲基纤维素和羧甲基纤维素)、血清白蛋白、淀粉和淀粉衍生物、多肽、聚亚烷基二醇和其衍生物、聚亚烷基二醇共聚物和其衍生物、聚乙烯基乙基醚和α
‑
β
‑
聚[(2
‑
羟乙基)
‑
dl
‑
天冬酰胺等,或其混合物。仅举例来说,所述水溶性聚合物与天然氨基酸多肽或非天然多肽连接可导致改变,包括(但不限于)水溶性增加、血清半衰期增加或经调节、治疗半衰期相对于未经修饰的形式增加或经调节、生物可用性增加、生物活性经调节、循环时间延长、免疫原性经调节、物理缔合特征(包括(但不限于)聚集和多聚体形成)经调节、受体结合改变、与一个或一个以上结合搭配物的结合改变和受体二聚化或多聚化改变。此外,所述水溶性聚合物可具有或可不具有其自身的生物活性。
[0343]
除非另作说明,否则所属领域技术范围内的质谱、nmr、hplc、蛋白质化学、生物化学、重组dna技术和药理学的常规方法都可使用。
[0344]
本文所呈现的化合物(包括(但不限于)非天然氨基酸、非天然氨基酸多肽、经修饰的非天然氨基酸多肽以及制造上述化合物的试剂)包括同位素标记的化合物,其与本文所呈现的各个化学式和结构中所述者相同,除了一个或一个以上原子被原子质量或质量数与自然界常见的原子质量或质量数不同的原子置换这一事实外。可并入本发明的化合物中的同位素的实例包括氢、碳、氮、氧、氟和氯的同位素,分别如2h、3h、
13
c、
14
c、
15
n、
18
o、
17
o、
35
s、
18
f、
36
cl。本文所述的某些同位素标记的化合物(例如,并有如3h和
14
c的放射性同位素的化合物)适用于药物和/或基质组织分布分析中。此外,用同位素(如氘,即2h)取代可因较高的代谢稳定性(例如,增加的体内半衰期或降低的剂量需求)而提供某些治疗优势。
[0345]
本文中的一些化合物(包括(但不限于)非天然氨基酸、非天然氨基酸多肽和经修饰的非天然氨基酸多肽,以及制造上述化合物的试剂)具有不对称碳原子并且因此可以对映异构体或非对映异构体形式存在。可基于物理化学差异通过已知方法(例如,色谱法和/或分级结晶)将非对映异构体混合物分成其个别非对映异构体。可通过与适当的光学活性化合物(例如,醇)反应将对映异构体混合物转化成非对映异构体混合物,分离非对映异构体以及将个别非对映异构体转化(例如,水解)成相应的纯对映异构体,从而分离对映异构体。认为所有所述异构体(包括非对映异构体、对映异构体和其混合物)都是本文所述的组合物的部分。
[0346]
在额外或另外实施例中,将本文所述的化合物(包括(但不限于)非天然氨基酸、非天然氨基酸多肽和经修饰的非天然氨基酸多肽,以及制造上述化合物的试剂)以前药的形式使用。在额外或另外实施例中,本文所述的化合物((包括(但不限于)非天然氨基酸、非天然氨基酸多肽和经修饰的非天然氨基酸多肽,以及制造上述化合物的试剂)在投与有需要的生物体后代谢产生代谢物,所述代谢物接着用于产生所需作用,包括所需治疗作用。另外或额外实施例是非天然氨基酸和“经修饰或未经修饰”的非天然氨基酸多肽的活性代谢物。
[0347]
本文所述的方法和调配物包括使用非天然氨基酸、非天然氨基酸多肽和经修饰的非天然氨基酸多肽的n
‑
氧化物、结晶形式(也称为多晶形物)或医药学上可接受的盐。在某些实施例中,非天然氨基酸、非天然氨基酸多肽和经修饰的非天然氨基酸多肽可以互变异构体形式存在。所有互变异构体都包括在本文所呈现的非天然氨基酸、非天然氨基酸多肽和经修饰的非天然氨基酸多肽的范围内。此外,本文所述的非天然氨基酸、非天然氨基酸多肽和经修饰的非天然氨基酸多肽可以未溶剂化形式以及与医药学上可接受的溶剂(如水、乙醇等)形成的溶剂化形式存在。认为本文所呈现的非天然氨基酸、非天然氨基酸多肽和经
修饰的非天然氨基酸多肽的溶剂化形式也在本文中有所披露。
[0348]
本文中的一些化合物(包括(但不限于)非天然氨基酸、非天然氨基酸多肽和经修饰的非天然氨基酸多肽,以及制造上述化合物的试剂)可以若干互变异构形式存在。认为所有所述互变异构形式都是本文所述的组合物的部分。此外,例如认为本文中的任何化合物(包括(但不限于)非天然氨基酸、非天然氨基酸多肽和经修饰的非天然氨基酸多肽,以及制造上述化合物的试剂)的所有烯醇
‑
酮形式是本文所述的组合物的部分。
[0349]
本文中的一些化合物(包括(但不限于)非天然氨基酸、非天然氨基酸多肽和经修饰的非天然氨基酸多肽,以及制造上述化合物的试剂)是酸性并且可与医药学上可接受的阳离子形成盐。本文中的一些化合物(包括(但不限于)非天然氨基酸、非天然氨基酸多肽和经修饰的非天然氨基酸多肽,以及制造上述化合物的试剂)可以是碱性并且因此可与医药学上可接受的阴离子形成盐。所有所述盐(包括二盐)都在本文所述的组合物的范围内并且其可通过常规方法制备。举例来说,可通过使酸性和碱性实体在水性介质、非水性介质或部分水性介质中接触来制备盐。通过使用以下技术中的至少一种来回收盐:过滤、用非溶剂沉淀随后过滤、蒸发溶剂或在水溶液的情况下冻干。
[0350]
本文所披露的非天然氨基酸多肽的医药学上可接受的盐可在亲本非天然氨基酸多肽中存在的酸性质子被金属离子(例如碱金属离子、碱土金属离子或铝离子)置换或与有机碱配位时形成。另外,所披露的非天然氨基酸多肽的盐形式可使用起始物质或中间物的盐制备。本文所述的非天然氨基酸多肽可通过使本文所述的非天然氨基酸多肽的游离碱形式与医药学上可接受的无机或有机酸反应而以医药学上可接受的酸加成盐(其是一类医药学上可接受的盐)形式制备。或者,本文所述的非天然氨基酸多肽可通过使本文所述的非天然氨基酸多肽的游离酸形式与医药学上可接受的无机或有机碱反应而以医药学上可接受的碱加成盐(其是一类医药学上可接受的盐)形式制备。
[0351]
医药学上可接受的盐的类型包括(但不限于):(1)与无机酸形成的酸加成盐,所述无机酸如盐酸、氢溴酸、硫酸、硝酸、磷酸等;或与有机酸形成的酸加成盐,所述有机酸如乙酸、丙酸、己酸、环戊烷丙酸、乙醇酸、丙酮酸、乳酸、丙二酸、琥珀酸、苹果酸、马来酸、富马酸、酒石酸、柠檬酸、苯甲酸、3
‑
(4
‑
羟基苯甲酰基)苯甲酸、肉桂酸、扁桃酸、甲烷磺酸、乙烷磺酸、1,2
‑
乙烷二磺酸、2
‑
羟基乙烷磺酸、苯磺酸、2
‑
萘磺酸、4
‑
甲基双环
‑
[2.2.2]辛
‑2‑
烯
‑1‑
甲酸、葡庚糖酸、4,4'
‑
亚甲基双
‑
(3
‑
羟基
‑2‑
烯
‑1‑
甲酸)、3
‑
苯基丙酸、三甲基乙酸、叔丁基乙酸、月桂基硫酸、葡糖酸、谷氨酸、羟基萘甲酸、水杨酸、硬脂酸、粘康酸等;(2)当母体化合物中存在的酸性质子被金属离子(例如,碱金属离子、碱土金属离子或铝离子)置换或者与有机碱配位时所形成的盐。可接受的有机碱包括乙醇胺、二乙醇胺、三乙醇胺、氨丁三醇、n
‑
甲基葡糖胺等。可接受的无机碱包括氢氧化铝、氢氧化钙、氢氧化钾、碳酸钠、氢氧化钠等。
[0352]
非天然氨基酸多肽医药学上可接受的盐的相应相对离子可使用多种方法(包括(但不限于)离子交换色谱、离子色谱、毛细管电泳、电感耦合等离子体、原子吸收光谱、质谱或其任何组合)加以分析和鉴别。另外,所述非天然氨基酸多肽医药学上可接受的盐的治疗学活性可使用实例87
‑
91中所述的技术和方法测试。
[0353]
应了解,提到盐包括其溶剂加成形式或晶体形式,尤其是溶剂化物或多晶形物。溶剂化物含有化学计量或非化学计量的量的溶剂,并且通常是在结晶过程中与医药学上可接
受的溶剂(如水、乙醇等)形成。当溶剂是水时形成水合物,或当溶剂是醇时形成醇化物。多晶形物包括具有相同化合物元素组成的不同晶体装填排列。多晶形物通常具有不同的x射线衍射图案、红外光谱、熔点、密度、硬度、晶形、光学和电学性质、稳定性和溶解性。如再结晶溶剂、结晶速率和储存温度的各种因素可导致单晶形式占优势。
[0354]
非天然氨基酸多肽医药学上可接受的盐多晶型物和/或溶剂化物的筛选和表征可使用多种技术(包括(但不限于)热分析、x射线衍射、光谱法、蒸气吸附和显微术)实现。热分析方法解决热化学降解或热物理过程,包括(但不限于)多晶型转变,并且所述方法用于分析多晶型形式之间的关系、测定重量损失、发现玻璃转化温度或用于赋形剂相容性研究。所述方法包括(但不限于)差示扫描量热法(dsc)、调制式差示扫描量热法(mdcs)、热解重量分析(tga)和热解重量和红外线分析(tg/ir)。x射线衍射法包括(但不限于)单晶和粉末衍射仪和同步加速辐射源。所用多种分光技术包括(但不限于)拉曼法(raman)、ftir、uvis和nmr(液态和固态)。多种显微术技术包括(但不限于)偏振光显微术、扫描电子显微术(sem)与能量分散x射线分析(edx)、环境扫描电子显微术与edx(在气体或水蒸汽大气压中)、ir显微术和拉曼显微术。
附图说明
[0355]
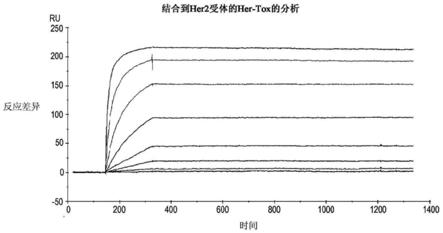
本发明的新颖特征详细阐述于所附权利要求书中。将通过参考以下阐述利用本发明原理的说明性实施例的具体实施方式以及随附图式获得对本发明特征和优势的更好理解,在所述随附图式中:
[0356]
图1呈现结合到her2受体的her
‑
tox的图解说明。
[0357]
图2呈现通过elisa分析测定的抗her2变体的表达的图解说明。
[0358]
图3呈现通过elisa分析测定的抗her2变体的表达的图解说明。
[0359]
图4呈现使用hcc 1954乳癌细胞系和海兔毒素连接基团衍生物的细胞增殖分析的图解说明。
[0360]
图5呈现使用hcc 1954乳癌细胞系和曲妥珠单抗
‑
tox结合物的细胞增殖分析的分析的图解说明。
[0361]
图6呈现使用skov
‑
3卵巢癌细胞系和海兔毒素连接基团衍生物的细胞增殖分析的分析的图解说明。
[0362]
图7呈现使用skov
‑
3卵巢癌细胞系和曲妥珠单抗
‑
tox结合物的细胞增殖分析的分析的图解说明。
[0363]
图8呈现使用mda
‑
mb
‑
468乳癌细胞系和海兔毒素连接基团衍生物的细胞增殖分析的分析的图解说明。
[0364]
图9呈现使用mda
‑
mb
‑
468乳癌系和曲妥珠单抗
‑
tox结合物的细胞增殖分析的分析的图解说明。
[0365]
图10呈现在曲妥珠单抗连接的海兔毒素衍生物的单次皮内剂量(3.3mg/kg、10mg/kg、20mg/kg)之后肿瘤体积测量(mm3)的图解说明。
[0366]
图11呈现用于测量sd大鼠血清中曲妥珠单抗连接的海兔毒素衍生物浓度的分析形式;左半部:(非选择性地)测量动物基质中her
‑
2抗体的总水平(非选择性),应用:her2 /-sm的pk概况非结合的抗体、结合的抗体;右半部:(选择性地)测量在每种药物两次或两
次以上有效负载情况下的完整her2
‑
adc水平,应用:全部ambrx adc( sm)的pk概况、评估连接基团稳定性、形式i的证实性分析。
[0367]
图12呈现在单次静脉内注射之后曲妥珠单抗连接的海兔毒素衍生物的血清浓度(ng/ml)的图解说明。
[0368]
图13呈现在单次静脉内注射之后曲妥珠单抗连接的海兔毒素衍生物的血清浓度(ng/ml)的图解说明。此分析检测结合到erbb2受体的抗体。
[0369]
图14呈现在静脉内注射之后曲妥珠单抗连接的海兔毒素衍生物的血清浓度(ng/ml)的图解说明。体内稳定性测量检测连接到曲妥珠单抗的至少两个海兔毒素衍生物。
[0370]
图15呈现在用曲妥珠单抗连接的海兔毒素衍生物处理之后大鼠体重和肿瘤体积变化的图解说明。
[0371]
图16呈现针对在scid
‑
bg小鼠中建立的hcc1954肿瘤的曲妥珠单抗、her2
‑
hs122
‑
ncd1和her2
‑
hs122/lk145
‑
hcd1的抗肿瘤功效的图解说明。在第1天投与小鼠单次静脉内注射(箭头)。数据点表示组平均肿瘤体积并且误差线表示平均值的标准误差(sem)。
[0372]
图17呈现mda361dyt2乳房(2 )异种移植模型中海兔毒素连接基团衍生物的抗肿瘤功效的图解说明。
[0373]
图18呈现mda361dyt2乳房(2 )异种移植模型中海兔毒素连接基团衍生物的抗肿瘤功效的图解说明。
具体实施方式
[0374]
虽然本文已展示并且描述本发明的优选实施例,但对于所属领域的技术人员来说所述实施例显而易见仅作为举例提供。在不脱离本发明的情况下,所属领域的技术人员现将进行多种变更、改变以及取代。应理解本文描述的本发明的实施例的不同替代方案均可以用于实施本发明。打算所附权利要求书定义本发明的范围并且由此涵盖这些权利要求范围内的方法和结构以及其等效物。
[0375]
i.引言
[0376]
近来已报导了蛋白质科学中的全新技术,其提供了克服与蛋白质位点特异性修饰相关的众多局限的前景。具体来说,已将新的组件加到原核生物大肠杆菌(escherichiacoli,e.coli)(例如王l(l.wang)等人,(2001),科学(science)292:498
‑
500)和真核生物酿酒酵母菌(sacchromyces cerevisia,s.cerevisiae)(例如秦j(j.chin)等人,科学301:964
‑
7(2003))的蛋白质生物合成机器中,所述机器能够在体内将非天然氨基酸并入蛋白质中。已使用这种方法响应琥珀密码子(tag)将多种具有新颖化学、物理或生物性质的新的氨基酸有效并且高保真地并入大肠杆菌和酵母的蛋白质中,所述新的氨基酸包括光亲和标记和可光异构化氨基酸、酮基氨基酸和糖基化氨基酸。参见,例如秦j.w.(j.w.chin)等人,(2002),美国化学学会志(journal of the american chemical society)124:9026
‑
9027(以其全文引用的方式并入);秦j.w.和舒尔茨p.g.(p.g.schultz),(2002),化学生物化学(chembiochem)3(11):1135
‑
1137(以其全文引用的方式并入);秦j.w.等人,(2002),美国国家科学院院刊(pnas united states of america)99(17):11020
‑
11024(以其全文引用的方式并入);以及王l.和舒尔茨p.g.,(2002),化学通讯(chem.comm.)1
‑
11(以其全文引用的方式并入)。这些研究已证实,有可能选择性并且常
规地引入未见于蛋白质中、对20种常见的基因编码的氨基酸中所见的所有官能团呈化学惰性并且可用于有效地并且选择性地反应形成稳定共价键的化学官能团。
[0377]
ii.综述
[0378]
在一个层面,本文描述用于产生和使用包含以下的海兔毒素连接基团衍生物或类似物的工具(方法、组合物、技术):至少一个羰基、二羰基、肟、羟胺、醛、经保护的醛、酮、经保护的酮、硫酯、酯、二羰基、肼、叠氮化物、脒、亚胺、二胺、酮
‑
胺、酮
‑
炔烃、炔烃、环炔烃或烯
‑
二酮。在另一层面,本文描述用于产生和使用包含以下的海兔毒素连接基团衍生物或类似物的工具(方法、组合物、技术):至少一个具有肟、芳香族胺、杂环(例如吲哚、喹喔啉、吩嗪、吡唑、三唑等)的非天然氨基酸或经修饰的非天然氨基酸。
[0379]
所述包含非天然氨基酸的海兔毒素连接基团衍生物可含有另一官能团,包括(但不限于)聚合物、水溶性聚合物、聚乙二醇衍生物、第二蛋白质或多肽或多肽类似物、抗体或抗体片段和其任何组合。应指出,各种上述官能团不意欲意指一个官能团的成员无法被归类为另一官能团的成员。实际上,视具体情况而定将存在重叠。仅举例来说,水溶性聚合物与聚乙二醇衍生物范围重叠,然而所述重叠不完全并且因此上文列举两个官能团。
[0380]
在一些实施例中,本文提供毒性基团连接基团衍生物,其包含羰基、二羰基、肟、羟胺、醛、经保护的醛、酮、经保护的酮、硫酯、酯、二羰基、肼、叠氮化物、脒、亚胺、二胺、酮
‑
胺、酮
‑
炔烃、炔烃、环炔烃或烯
‑
二酮。在一些实施例中,毒性基团衍生物包含本文所披露的连接基团中的任一个。在其它实施例中,本文描述用于产生和使用包含以下的毒性基团衍生物或类似物的工具(方法、组合物、技术):至少一个具有肟、芳香族胺、杂环(例如吲哚、喹喔啉、吩嗪、吡唑、三唑等)的非天然氨基酸或经修饰的非天然氨基酸。
[0381]
在一些实施例中,所述包含非天然氨基酸的毒性衍生物可含有另一官能团,包括(但不限于)聚合物、水溶性聚合物、聚乙二醇衍生物、第二蛋白质或多肽或多肽类似物、抗体或抗体片段和其任何组合。在特定实施例中,毒性基团是海兔毒素或奥利斯坦。在某些特定实施例中,毒性基团是海兔毒素
‑
10。应指出,各种上述官能团不意欲意指一个官能团的成员无法被归类为另一官能团的成员。实际上,视具体情况而定将存在重叠。仅举例来说,水溶性聚合物与聚乙二醇衍生物范围重叠,然而所述重叠不完全并且因此上文列举两个官能团。
[0382]
本发明的某些实施例描述制备具有连接基团的某些毒性部分,所述连接基团在体内使所述部分的毒性减小而毒性部分保留药理学活性。在一些实施例中,在投与动物或人类时,与游离毒性基团或包含不稳定键的毒性基团衍生物相比,连接的毒性基团的毒性减小或消除,同时保留药理学活性。在一些实施例中,连接的毒性基团(例如海兔毒素连接基团衍生物、非天然氨基酸连接的海兔毒素衍生物)的增加的剂量可以较大安全性投与动物或人类。在某些实施例中,连接到毒性部分(例如海兔毒素衍生物)的非天然氨基酸多肽提供体外和体内稳定性。在一些实施例中,连接到毒性部分(例如海兔毒素
‑
10衍生物)的非天然氨基酸多肽与游离毒性部分(例如海兔毒素
‑
10)相比有效并且毒性更小。
[0383]
iii.海兔毒素连接基团衍生物
[0384]
在一个层面,本文描述用于产生和使用包含以下的海兔毒素连接基团衍生物或类似物的工具(方法、组合物、技术):至少一个具有羰基、二羰基、肟或羟胺基团的非天然氨基酸或经修饰的非天然氨基酸。所述包含非天然氨基酸的海兔毒素连接基团衍生物可含有另
一官能团,包括(但不限于)聚合物、水溶性聚合物、聚乙二醇衍生物、第二蛋白质或多肽或多肽类似物、抗体或抗体片段和其任何组合。应指出,各种上述官能团不意欲意指一个官能团的成员无法被归类为另一官能团的成员。实际上,视具体情况而定将存在重叠。仅举例来说,水溶性聚合物与聚乙二醇衍生物范围重叠,然而所述重叠不完全并且因此上文列举两个官能团。
[0385]
一个方面是选择和设计待使用本文描述的方法、组合物和技术修饰的海兔毒素连接基团衍生物的方法。新的海兔毒素连接基团衍生物可重新(包括仅举例来说,作为高通量筛选过程的一部分(在所述情况下可设计、合成、表征和/或测试许多多肽)或基于研究者兴趣)进行设计。新的海兔毒素连接基团衍生物还可以基于已知或部分表征的多肽的结构进行设计。仅举例来说,海兔毒素已是科学界深入研究的主题;新型化合物可基于海兔毒素的结构设计。选择取代和/或修饰哪一个(哪些)氨基酸的原理单独描述于本文中。本文中还描述使用何种修饰的选择,并且所述选择可用于满足实验者或终端用户的需要。所述需要可包括(但不限于)操控多肽的治疗功效;改进多肽的安全概況;调节多肽的药物动力学、药理学和/或药效学,如(仅举例来说)增加水溶性、生物可用性,增加血清半衰期,增加治疗半衰期,调节免疫原性,调节生物活性或延长循环时间。此外,所述修饰包括(仅举例来说)向多肽提供其它官能团;并入抗体;和上述修饰的任何组合。
[0386]
本文还描述具有以下各者或可经修饰以含有以下各者的海兔毒素连接基团衍生物:肟、羰基、二羰基或羟胺基团。此方面包括用于产生、纯化、表征和使用所述海兔毒素连接基团衍生物的方法。
[0387]
海兔毒素连接基团衍生物可含有至少一个、至少两个、至少三个、至少四个、至少五个、至少六个、至少七个、至少八个、至少九个或者十个或十个以上羰基或二羰基、肟基、羟胺基团或其经保护的形式。海兔毒素连接基团衍生物可相同或不同,例如在包含1、2、3、4、5、6、7、8、9、10、11、12、13、14、15、16、17、18、19、20个或20个以上不同反应性基团的衍生物中存在1、2、3、4、5、6、7、8、9、10、11、12、13、14、15、16、17、18、19、20个或20个以上不同位点。
[0388]
a.海兔毒素连接基团衍生物的结构和合成:亲电子和亲核基团
[0389]
含有羟胺(也称为氨氧基)基团的具有连接基团的海兔毒素衍生物允许与多种亲电子基团发生反应以形成结合物(包括(但不限于)与peg或其它水溶性聚合物)。如肼、酰肼和氨基脲般,氨氧基增强的亲核性允许其有效地并且选择性地与各种含有羰基或二羰基的分子(包括(但不限于)酮、醛或具有相似化学反应性的其它官能团)反应。参见例如邵j.(shao,j.)和塔恩j.(tarn,j.),美国化学学会志(j.am.chem.soc.)117:3893
‑
3899(1995);航h.(h.hang)和贝尔托西c.(c.bertozzi),化学研究述评(ace.chem.res.)34(9):727
‑
736(2001)。尽管与肼基团发生反应的结果是相应腙,然而,肟通常由氨氧基与含羰基或二羰基的基团(如酮、醛或具有相似化学反应性的官能团)的反应产生。在一些实施例中,包含叠氮化物、炔烃或环炔烃的具有连接基团的海兔毒素衍生物允许通过环加成反应(例如1,3
‑
偶极环加成、叠氮化物
‑
炔烃胡伊斯根环加成(azide
‑
alkyne huisgen cycloaddition)等)连接分子。(描述在美国专利第7,807,619号中,其在关于反应的程度上以引用的方式并入本文中)。
[0390]
因此,本文所述的某些实施例是包含以下的具有连接基团的海兔毒素衍生物:羟
胺、醛、经保护的醛、酮、经保护的酮、硫酯、酯、二羰基、肼、脒、亚胺、二胺、酮
‑
胺、酮
‑
炔烃和烯
‑
二酮羟胺基团、羟胺样基团(其具有与羟胺基团类似的反应性并且在结构上与羟胺基团类似)、经遮蔽羟胺基团(其可易于转化为羟胺基团)或经保护的羟胺基团(其在脱除保护基后具有与羟胺基团类似的反应性)。在一些实施例中,具有连接基团的海兔毒素衍生物包含叠氮化物、炔烃或环炔烃。所述海兔毒素连接基团衍生物包括具有式(i)、(iii)、(iv)、(v)以及(vi)结构的化合物:
[0391]
[0392][0393]
其中:
[0394]
z具有以下结构:
[0395][0396]
r5是h、cor8、c1‑
c6烷基或噻唑;
[0397]
r8是oh或
‑
nh
‑
(亚烷基
‑
o)
n
‑
nh2;
[0398]
r6是oh或h;
[0399]
ar是苯基或吡啶;
[0400]
r7是c1‑
c6烷基或氢;
[0401]
y和v各自选自由以下组成的群组:羟胺、甲基、醛、经保护的醛、酮、经保护的酮、硫酯、酯、二羰基、肼、叠氮化物、脒、亚胺、二胺、酮基
‑
胺、酮基
‑
炔烃、炔烃、环炔烃以及烯
‑
二酮;
[0402]
l、l1、l2、l3以及l4各自是选自由以下组成的群组的连接基团:一键、
‑
亚烷基
‑
、
‑
亚烷基
‑
c(o)
‑
、
‑
亚烷基
‑
j
‑
、
‑
(亚烷基
‑
o)
n
‑
亚烷基
‑
、
‑
(亚烷基
‑
o)
n
‑
亚烷基
‑
c(o)
‑
、
‑
(亚烷基
‑
o)
n
‑
j
‑
、
‑
(亚烷基
‑
o)
n
‑
j
‑
亚烷基
‑
、
‑
(亚烷基
‑
o)
n
‑
(ch2)
n'
‑
nhc(o)
‑
(ch2)
n”‑
c(me)2‑
s
‑
s
‑
(ch2)
n”'
‑
nhc(o)
‑
(亚烷基
‑
o)
n
””
‑
亚烷基
‑
、
‑
(亚烷基
‑
o)
n
‑
亚烷基
‑
w
‑
、
‑
亚烷基
‑
c(o)
‑
w
‑
、
‑
(亚烷基
‑
o)
n
‑
亚烷基
‑
j
‑
、
‑
亚烷基'
‑
j
‑
(亚烷基
‑
o)
n
‑
亚烷基
‑
、
‑
(亚烷基
‑
o)
n
‑
亚烷基
‑
j
‑
亚烷基'、
‑
j
‑
(亚烷基
‑
o)
n
‑
亚烷基
‑
、
‑
(亚烷基
‑
o)
n
‑
亚烷基
‑
j
‑
(亚烷基
‑
o)
n
'
‑
亚烷基
‑
j'
‑
、
‑
w
‑
、
‑
亚烷基
‑
w
‑
、亚烷基'
‑
j
‑
(亚烷基
‑
nme)
n
‑
亚烷基
‑
w
‑
、
‑
j
‑
(亚烷基
‑
nme)
n
‑
亚烷基
‑
w
‑
、
‑
(亚烷基
‑
o)
n
‑
亚烷基
‑
u
‑
亚烷基
‑
c(o)
‑
、
‑
(亚烷基
‑
o)
n
‑
亚烷基
‑
u
‑
亚烷基
‑
、
‑
j
‑
亚烷基
‑
nme
‑
亚烷基'
‑
nme
‑
亚烷基"
‑
w
‑
以及
‑
亚烷基
‑
j
‑
亚烷基'
‑
nme
‑
亚烷基"
‑
nme
‑
亚烷基'"
‑
w
‑
;
[0403]
w具有以下结构:
[0404][0405]
u具有以下结构:
[0406][0407]
j和j'各自独立地具有以下结构:
[0408][0409]
n、n'、n"、n'"以及n""各自独立地是大于或等于1的整数;并且
[0410]
或l不存在,y是甲基,r5是cor8,并且r8是
‑
nh
‑
(亚烷基
‑
o)
n
‑
nh2。
[0411]
所述尾海兔素连接基团衍生物可以呈盐形式,或可并入非天然氨基酸多肽、聚合物、多糖或多核苷酸中并且任选地进行翻译后修饰。
[0412]
在式(i)、(iii)和(v)化合物的某些实施例中,r5是噻唑或羧酸。在式(i)、(iii)和(v)化合物的某些实施例中,r5是氢。在式(i)、(iii)和(v)化合物的某些实施例中,r5是甲基、乙基、丙基、异丙基、丁基、异丁基、仲丁基、叔丁基、戊基或己基。在式(i)、(iii)和(v)化合物的某些实施例中,r5是
‑
nh
‑
(亚烷基
‑
o)
n
‑
nh2,其中亚烷基是
‑
ch2‑
、
‑
ch2ch2‑
、
‑
ch2ch2ch2‑
、
‑
ch2ch2ch2ch2‑
、
‑
ch2ch2ch2ch2ch2‑
、
‑
ch2ch2ch2ch2ch2ch2‑
、
‑
ch2ch2ch2ch2ch2ch2ch2‑
、
‑
ch2ch2ch2ch2ch2ch2ch2ch2‑
、
‑
ch2ch2ch2ch2ch2ch2ch2ch2ch2‑
、
‑
ch2ch2ch2ch2ch2ch2ch2ch2ch2ch2‑
、
‑
ch2ch2ch2ch2ch2ch2ch2ch2ch2ch2ch2‑
或
‑
ch2ch2ch2ch2ch2ch2ch2ch2ch2ch2ch2ch2‑
。在式(iv)和(vi)化合物的某些实施例中,r5是
‑
nh
‑
(亚烷基
‑
o)
n
‑
nh2,其中n是0、1、2、3、4、5、6、7、8、9、10、11、12、13、14、15、16、17、18、19、20、21、22、23、24、25、26、27、28、29、30、31、32、33、34、35、36、37、38、39、40、41、42、43、44、45、46、47、48、49、50、51、52、53、54、55、56、57、58、59、60、61、62、63、64、65、66、67、68、69、70、71、72、73、74、75、76、77、78、79、80、81、82、83、84、85、86、87、88、89、90、91、92、93、94、95、96、97、98、99或100。
[0413]
在一些实施例中,y是叠氮化物。在其它实施例中,y是环炔烃。在特定实施例中,环辛炔具有以下结构:
[0414][0415]
每个r
19
独立地选自由以下组成的群组:c1‑
c6烷基、c1‑
c6烷氧基、酯、醚、硫醚、氨基烷基、卤素、烷基酯、芳基酯、酰胺、芳基酰胺、烷基卤化物、烷基胺、烷基磺酸、烷基硝基、硫酯、磺酰基酯、卤磺酰基、腈、烷基腈以及硝基;并且
[0416]
q是0、1、2、3、4、5、6、7、8、9、10或11。
[0417]
在式(i)、(iii)和(v)化合物的某些实施例中,r6是h。在式(i)、(iii)和(v)的化合物的一些实施例中,r6是羟基。
[0418]
在式(i)、(iii)和(v)化合物的某些实施例中,ar是苯基。
[0419]
在式(i)、(iii)、(iv)、(v)和(vi)化合物的某些实施例中,r7是甲基、乙基、丙基、异丙基、丁基、仲丁基、异丁基、叔丁基、戊基或己基。在式(i)、(iii)、(iv)、(v)和(vi)化合物的某些实施例中,r7是氢。
[0420]
在式(i)、(iii)和(v)化合物的某些实施例中,y是羟胺、醛、经保护的醛、酮、经保护的酮、硫酯、酯、二羰基、肼、脒、亚胺、二胺、酮基
‑
胺、酮基
‑
炔烃或烯
‑
二酮。
[0421]
在式(iv)和(vi)化合物的某些实施例中,v是羟胺、甲基、醛、经保护的醛、酮、经保护的酮、硫酯、酯、二羰基、肼、脒、亚胺、二胺、酮基
‑
胺、酮基
‑
炔烃以及烯
‑
二酮。
[0422]
在式(i)、(iii)、(iv)、(v)和(vi)化合物的某些实施例中,l、l1、l2、l3和l4各自独立地是可裂解连接基团或不可裂解连接基团。在式(i)、(iii)、(iv)、(v)和(vi)化合物的某些实施例中,l、l1、l2、l3和l4各自独立地是寡聚(乙二醇)衍生化的连接基团。
[0423]
在式(i)、(iii)、(iv)、(v)和(vi)化合物的某些实施例中,亚烷基、亚烷基'、亚烷基"和亚烷基'"各自独立地是
‑
ch2‑
、
‑
ch2ch2‑
、
‑
ch2ch2ch2‑
、
‑
ch2ch2ch2ch2‑
、
‑
ch2ch2ch2ch2ch2‑
、
‑
ch2ch2ch2ch2ch2ch2‑
、
‑
ch2ch2ch2ch2ch2ch2ch2‑
、
‑
ch2ch2ch2ch2ch2ch2ch2ch2‑
、
‑
ch2ch2ch2ch2ch2ch2ch2ch2ch2‑
、
‑
ch2ch2ch2ch2ch2ch2ch2ch2ch2ch2‑
、
‑
ch2ch2ch2ch2ch2ch2ch2ch2ch2ch2ch2‑
或
‑
ch2ch2ch2ch2ch2ch2ch2ch2ch2ch2ch2ch2‑
。在式(xiv)、(xv)、(xvi)、(xvii)和(xviii)化合物的某些实施例中,n、n'、n"、n'"和n""各自是0、1、2、3、4、5、6、7、8、9、10、11、12、13、14、15、16、17、18、19、
20、21、22、23、24、25、26、27、28、29、30、31、32、33、34、35、36、37、38、39、40、41、42、43、44、45、46、47、48、49、50、51、52、53、54、55、56、57、58、59、60、61、62、63、64、65、66、67、68、69、70、71、72、73、74、75、76、77、78、79、80、81、82、83、84、85、86、87、88、89、90、91、92、93、94、95、96、97、98、99或100。
[0424]
b.尾海兔素连接基团衍生物的结构和合成:羟胺基团
[0425]
因此,本文描述的某些实施例是包含以下的具有连接基团的海兔毒素衍生物:羟胺基团、羟胺类基团(其具有与羟胺基团类似的反应性并且在结构上与羟胺基团类似)、经遮蔽羟胺基团(其可易于转化为羟胺基团)或经保护的羟胺基团(其在脱除保护基后具有与羟胺基团类似的反应性)。所述尾海兔素连接基团衍生物包括具有式(i)结构的化合物:
[0426][0427]
其中:
[0428]
z具有以下结构:
[0429][0430]
r5是h、cor8、c1‑
c6烷基或噻唑;
[0431]
r8是oh或
‑
nh
‑
(亚烷基
‑
o)
n
‑
nh2;
[0432]
r6是oh或h;
[0433]
ar是苯基或吡啶;
[0434]
r7是c1‑
c6烷基或氢;
[0435]
y是nh2‑
o
‑
或甲基;
[0436]
l是选自由以下组成的群组的连接基团:
‑
亚烷基
‑
、
‑
亚烷基
‑
c(o)
‑
、
‑
(亚烷基
‑
o)
n
‑
亚烷基
‑
、
‑
(亚烷基
‑
o)
n
‑
亚烷基
‑
c(o)
‑
、
‑
(亚烷基
‑
o)
n
‑
(ch2)
n'
‑
nhc(o)
‑
(ch2)
n”‑
c(me)2‑
s
‑
s
‑
(ch2)
n”'
‑
nhc(o)
‑
(亚烷基
‑
o)
n
””
‑
亚烷基
‑
、
‑
(亚烷基
‑
o)
n
‑
亚烷基
‑
w
‑
、
‑
亚烷基
‑
c(o)
‑
w
‑
、
‑
(亚烷基
‑
o)
n
‑
亚烷基
‑
u
‑
亚烷基
‑
c(o)
‑
以及
‑
(亚烷基
‑
o)
n
‑
亚烷基
‑
u
‑
亚烷基
‑
;
[0437]
w具有以下结构:
[0438][0439]
u具有以下结构:
[0440][0441]
或l不存在,y是甲基,r5是cor8,并且r8是
‑
nh
‑
(亚烷基
‑
o)
n
‑
nh2;并且
[0442]
n、n'、n"、n'"和n""各自独立地是大于或等于1的整数。所述尾海兔素连接基团衍生物可以呈盐形式,或可并入非天然氨基酸多肽、聚合物、多糖或多核苷酸中并且任选地进行翻译后修饰。
[0443]
在式(i)化合物的某些实施例中,r5是噻唑。在式(i)化合物的某些实施例中,r5是氢。在式(i)化合物的某些实施例中,r5是甲基、乙基、丙基、异丙基、丁基、异丁基、仲丁基、叔丁基、戊基或己基。在式(i)化合物的某些实施例中,r5是
‑
nh
‑
(亚烷基
‑
o)
n
‑
nh2,其中亚烷基是
‑
ch2‑
、
‑
ch2ch2‑
、
‑
ch2ch2ch2‑
、
‑
ch2ch2ch2ch2‑
、
‑
ch2ch2ch2ch2ch2‑
、
‑
ch2ch2ch2ch2ch2ch2‑
、
‑
ch2ch2ch2ch2ch2ch2ch2‑
、
‑
ch2ch2ch2ch2ch2ch2ch2ch2‑
、
‑
ch2ch2ch2ch2ch2ch2ch2ch2ch2‑
、
‑
ch2ch2ch2ch2ch2ch2ch2ch2ch2ch2‑
、
‑
ch2ch2ch2ch2ch2ch2ch2ch2ch2ch2ch2‑
或
‑
ch2ch2ch2ch2ch2ch2ch2ch2ch2ch2ch2ch2‑
。在式(i)化合物的某些实施例中,r5是
‑
nh
‑
(亚烷基
‑
o)
n
‑
nh2,其中n是0、1、2、3、4、5、6、7、8、9、10、11、12、13、14、15、16、17、18、19、20、21、22、23、24、25、26、27、28、29、30、31、32、33、34、35、36、37、38、39、40、41、42、43、44、45、46、47、48、49、50、51、52、53、54、55、56、57、58、59、60、61、62、63、64、65、66、67、68、69、70、71、72、73、74、75、76、77、78、79、80、81、82、83、84、85、86、87、88、89、90、91、92、93、94、95、96、97、98、99或100。
[0444]
在式(i)化合物的某些实施例中,r6是h。在式(i)化合物的一些实施例中,r6是羟基。
[0445]
在式(i)化合物的某些实施例中,ar是苯基。
[0446]
在式(i)化合物的某些实施例中,r7是甲基、乙基、丙基、异丙基、丁基、仲丁基、异丁基、叔丁基、戊基或己基。在式(i)化合物的某些实施例中,r7是氢。
[0447]
在式(i)化合物的某些实施例中,y是羟胺、醛、经保护的醛、酮、经保护的酮、硫酯、酯、二羰基、肼、脒、亚胺、二胺、酮基
‑
胺、酮基
‑
炔烃或烯
‑
二酮。在式(i)化合物的某些实施例中,v是羟胺、甲基、醛、经保护的醛、酮、经保护的酮、硫酯、酯、二羰基、肼、脒、亚胺、二胺、酮基
‑
胺、酮基
‑
炔烃以及烯
‑
二酮。
[0448]
在式(i)化合物的某些实施例中,每个l独立地是可裂解连接基团或不可裂解连接基团。在式(i)化合物的某些实施例中,每个l独立地是寡聚(乙二醇)衍生化连接基团。
[0449]
在式(i)化合物的某些实施例中,亚烷基是
‑
ch2‑
、
‑
ch2ch2‑
、
‑
ch2ch2ch2‑
、
‑
ch2ch2ch2ch2‑
、
‑
ch2ch2ch2ch2ch2‑
、
‑
ch2ch2ch2ch2ch2ch2‑
、
‑
ch2ch2ch2ch2ch2ch2ch2‑
、
‑
ch2ch2ch2ch2ch2ch2ch2ch2‑
、
‑
ch2ch2ch2ch2ch2ch2ch2ch2ch2‑
、
‑
ch2ch2ch2ch2ch2ch2ch2ch2ch2ch2‑
、
‑
ch2ch2ch2ch2ch2ch2ch2ch2ch2ch2ch2‑
或
‑
ch2ch2ch2ch2ch2ch2ch2ch2ch2ch2ch2ch2‑
。在式(i)化合物的某些实施例中,n、n'、n"、n'"和n""各自是0、1、2、3、4、5、6、7、8、9、10、11、12、13、14、15、16、17、18、19、20、21、22、23、24、25、26、27、28、29、30、31、32、33、34、35、36、37、38、39、40、41、42、43、44、45、46、47、48、49、50、51、52、53、54、55、56、57、58、59、60、61、62、63、64、65、66、67、68、69、70、71、72、73、74、75、76、77、78、79、80、
81、82、83、84、85、86、87、88、89、90、91、92、93、94、95、96、97、98、99或100。
[0450]
在某些实施例中,尾海兔素连接基团衍生物包括具有式(ii)结构的化合物:
[0451][0452]
在式(ii)化合物的一些实施例中,l是
‑
(亚烷基
‑
o)
n
‑
亚烷基
‑
。在一些实施例中,每个亚烷基是
‑
ch2ch2‑
,n等于3,并且r7是甲基。在一些实施例中,l是
‑
亚烷基
‑
。在式(ii)化合物的一些实施例中,每个亚烷基是
‑
ch2ch2‑
并且r7是甲基或氢。在式(ii)化合物的一些实施例中,l是
‑
(亚烷基
‑
o)
n
‑
亚烷基
‑
c(o)
‑
。在式(ii)化合物的一些实施例中,每个亚烷基是
‑
ch2ch2‑
,n等于4,并且r7是甲基。在式(ii)化合物的一些实施例中,l是
‑
(亚烷基
‑
o)
n
‑
(ch2)
n'
‑
nhc(o)
‑
(ch2)
n”‑
c(me)2‑
s
‑
s
‑
(ch2)
n”'
‑
nhc(o)
‑
(亚烷基
‑
o)
n
””
‑
亚烷基
‑
。在式(ii)化合物的一些实施例中,每个亚烷基是
‑
ch2ch2‑
,n等于1,n'等于2,n"等于1,n'"等于2,n""等于4,并且r7是甲基。所述尾海兔素连接基团衍生物可以呈盐形式,或可并入非天然氨基酸多肽、聚合物、多糖或多核苷酸中并且任选地进行翻译后修饰。
[0453]
在式(ii)化合物的某些实施例中,每个l独立地是可裂解连接基团或不可裂解连接基团。在式(ii)化合物的某些实施例中,每个l独立地是寡聚(乙二醇)衍生化连接基团。
[0454]
在式(ii)化合物的某些实施例中,r7是甲基、乙基、丙基、异丙基、丁基、仲丁基、异丁基、叔丁基、戊基或己基。在式(ii)化合物的某些实施例中,r7是氢。
[0455]
在式(ii)化合物的某些实施例中,亚烷基是
‑
ch2‑
、
‑
ch2ch2‑
、
‑
ch2ch2ch2‑
、
‑
ch2ch2ch2ch2‑
、
‑
ch2ch2ch2ch2ch2‑
、
‑
ch2ch2ch2ch2ch2ch2‑
、
‑
ch2ch2ch2ch2ch2ch2ch2‑
、
‑
ch2ch2ch2ch2ch2ch2ch2ch2‑
、
‑
ch2ch2ch2ch2ch2ch2ch2ch2ch2‑
、
‑
ch2ch2ch2ch2ch2ch2ch2ch2ch2ch2‑
、
‑
ch2ch2ch2ch2ch2ch2ch2ch2ch2ch2ch2‑
或
‑
ch2ch2ch2ch2ch2ch2ch2ch2ch2ch2ch2ch2‑
。在式(ii)化合物的某些实施例中,n、n'、n"、n'"和n""各自是0、1、2、3、4、5、6、7、8、9、10、11、12、13、14、15、16、17、18、19、20、21、22、23、24、25、26、27、28、29、30、31、32、33、34、35、36、37、38、39、40、41、42、43、44、45、46、47、48、49、50、51、52、53、54、55、56、57、58、59、60、61、62、63、64、65、66、67、68、69、70、71、72、73、74、75、76、77、78、79、80、81、82、83、84、85、86、87、88、89、90、91、92、93、94、95、96、97、98、99或100。
[0456]
所述尾海兔素连接基团衍生物包括具有式(iii)、(iv)、(v)或(vi)结构的化合物:
[0457][0458]
[0459][0460]
其中:
[0461]
z具有以下结构:
[0462][0463]
r5是h、cor8、c1‑
c6烷基或噻唑;
[0464]
r8是oh;
[0465]
r6是oh或h;
[0466]
ar是苯基或吡啶;
[0467]
r7是c1‑
c6烷基或氢;
[0468]
y是nh2‑
o
‑
;
[0469]
v是
‑
o
‑
nh2;
[0470]
l1、l2、l3和l4各自是独立地选自由以下组成的群组的连接基团:一键、
‑
亚烷基
‑
、
‑
(亚烷基
‑
o)
n
‑
亚烷基
‑
j
‑
、
‑
亚烷基'
‑
j
‑
(亚烷基
‑
o)
n
‑
亚烷基
‑
、
‑
j
‑
(亚烷基
‑
o)
n
‑
亚烷基
‑
、
‑
(亚烷基
‑
o)
n
‑
亚烷基
‑
j
‑
(亚烷基
‑
o)
n
'
‑
亚烷基
‑
j'
‑
、
‑
(亚烷基
‑
o)
n
‑
亚烷基
‑
j
‑
亚烷基'
‑
、
‑
w
‑
、
‑
亚烷基
‑
w
‑
、亚烷基'
‑
j
‑
(亚烷基
‑
nme)
n
‑
亚烷基
‑
w
‑
、
‑
j
‑
(亚烷基
‑
nme)
n
‑
亚烷基
‑
w
‑
、
‑
j
‑
亚烷基
‑
nme
‑
亚烷基'
‑
nme
‑
亚烷基"
‑
w
‑
以及
‑
亚烷基
‑
j
‑
亚烷基'
‑
nme
‑
亚烷基"
‑
nme
‑
亚烷基'"
‑
w
‑
;
[0471]
w具有以下结构:
[0472][0473]
j和j'各自独立地具有以下结构:
[0474]
并且
[0475]
n和n'各自独立地是大于或等于1的整数。
[0476]
所述尾海兔素连接基团衍生物可以呈盐形式,或可并入非天然氨基酸多肽、聚合物、多糖或多核苷酸中并且任选地进行翻译后修饰。
[0477]
在式(iii)、(iv)、(v)或(vi)化合物的某些实施例中,r5是噻唑。在式(iii)、(iv)、(v)或(vi)化合物的某些实施例中,r6是h。在式(iii)、(iv)、(v)或(vi)化合物的某些实施例中,ar是苯基。在式(iii)、(iv)、(v)或(vi)化合物的某些实施例中,r7是甲基。在式(iii)、(iv)、(v)或(vi)化合物的某些实施例中,n和n'是0到20的整数。在式(iii)、(iv)、(v)或(vi)化合物的某些实施例中,n和n'是0到10的整数。在式(iii)、(iv)、(v)或(vi)化合物的某些实施例中,n和n'是0到5的整数。
[0478]
在式(iii)和(v)化合物的某些实施例中,r5是噻唑或羧酸。在式(iii)和(v)化合物的某些实施例中,r5是氢。在式(iii)和(v)化合物的某些实施例中,r5是甲基、乙基、丙基、异丙基、丁基、异丁基、仲丁基、叔丁基、戊基或己基。在式(iii)和(v)化合物的某些实施例中,r5是
‑
nh
‑
(亚烷基
‑
o)
n
‑
nh2,其中亚烷基是
‑
ch2‑
、
‑
ch2ch2‑
、
‑
ch2ch2ch2‑
、
‑
ch2ch2ch2ch2‑
、
‑
ch2ch2ch2ch2ch2‑
、
‑
ch2ch2ch2ch2ch2ch2‑
、
‑
ch2ch2ch2ch2ch2ch2ch2‑
、
‑
ch2ch2ch2ch2ch2ch2ch2ch2‑
、
‑
ch2ch2ch2ch2ch2ch2ch2ch2ch2‑
、
‑
ch2ch2ch2ch2ch2ch2ch2ch2ch2ch2‑
、
‑
ch2ch2ch2ch2ch2ch2ch2ch2ch2ch2ch2‑
或
‑
ch2ch2ch2ch2ch2ch2ch2ch2ch2ch2ch2ch2‑
。在式(iii)和(v)化合物的某些实施例中,r5是
‑
nh
‑
(亚烷基
‑
o)
n
‑
nh2,其中n是0、1、2、3、4、5、6、7、8、9、10、11、12、13、14、15、16、17、18、19、20、21、22、23、24、25、26、27、28、29、30、31、32、33、34、35、36、37、38、39、40、41、42、43、44、45、46、47、48、49、50、51、52、53、54、55、56、57、58、59、60、61、62、63、64、65、66、67、68、69、70、71、72、73、74、75、76、77、78、79、80、81、82、83、84、85、86、87、88、89、90、91、92、93、94、95、96、97、98、99或100。
[0479]
在式(iii)、(iv)、(v)和(vi)化合物的某些实施例中,r6是h。在式(iii)、(iv)、(v)和(vi)化合物的一些实施例中,r6是羟基。
[0480]
在式(iii)、(iv)、(v)和(vi)化合物的某些实施例中,ar是苯基。
[0481]
在式(iii)、(iv)、(v)和(vi)化合物的某些实施例中,r7是甲基、乙基、丙基、异丙基、丁基、仲丁基异丁基、叔丁基、戊基或己基。在式(iii)、(iv)、(v)和(vi)化合物的某些实施例中,r7是氢。
[0482]
在式(iii)和(v)化合物的某些实施例中,y是羟胺、醛、经保护的醛、酮、经保护的酮、硫酯、酯、二羰基、肼、脒、亚胺、二胺、酮基
‑
胺、酮基
‑
炔烃或烯
‑
二酮。在式(iv)和(vi)化合物的某些实施例中,v是羟胺、甲基、醛、经保护的醛、酮、经保护的酮、硫酯、酯、二羰基、肼、脒、亚胺、二胺、酮基
‑
胺、酮基
‑
炔烃以及烯
‑
二酮。
[0483]
在式(xiv)、(xv)、(xvi)、(xvii)和(xviii)化合物的某些实施例中,l、l1、l2、l3和l4各自独立地是可裂解连接基团或不可裂解连接基团。在式(xiv)、(xv)、(xvi)、(xvii)和(xviii)化合物的某些实施例中,l、l1、l2、l3和l4各自独立地是寡聚(乙二醇)衍生化连接基团。
[0484]
在式(iii)、(iv)、(v)和(vi)化合物的某些实施例中,亚烷基、亚烷基'、亚烷基"和亚烷基'"各自独立地
‑
ch2‑
、
‑
ch2ch2‑
、
‑
ch2ch2ch2‑
、
‑
ch2ch2ch2ch2‑
、
‑
ch2ch2ch2ch2ch2‑
、
‑
ch2ch2ch2ch2ch2ch2‑
、
‑
ch2ch2ch2ch2ch2ch2ch2‑
、
‑
ch2ch2ch2ch2ch2ch2ch2ch2‑
、
‑
ch2ch2ch2ch2ch2ch2ch2ch2ch2‑
、
‑
ch2ch2ch2ch2ch2ch2ch2ch2ch2ch2‑
、
‑
ch2ch2ch2ch2ch2ch2ch2ch2ch2ch2ch2‑
或
‑
ch2ch2ch2ch2ch2ch2ch2ch2ch2ch2ch2ch2‑
。在式(iii)、(iv)、(v)和(vi)化合物的某些实施例中,亚烷基是亚甲基、亚乙基、亚丙基、亚丁基、亚戊基、亚己基或亚庚基。
[0485]
在式(iii)、(iv)、(v)和(vi)化合物的某些实施例中,n和n'各自独立地是0、1、2、3、4、5、6、7、8、9、10、11、12、13、14、15、16、17、18、19、20、21、22、23、24、25、26、27、28、29、30、31、32、33、34、35、36、37、38、39、40、41、42、43、44、45、46、47、48、49、50、51、52、53、54、55、56、57、58、59、60、61、62、63、64、65、66、67、68、69、70、71、72、73、74、75、76、77、78、79、80、81、82、83、84、85、86、87、88、89、90、91、92、93、94、95、96、97、98、99或100。
[0486]
在某些实施例中,尾海兔素连接基团衍生物包括具有式(vii)结构的化合物:
[0487][0488]
在式(vii)化合物的某些实施例中,l1是
‑
(亚烷基
‑
o)
n
‑
亚烷基
‑
j
‑
,l2是
‑
亚烷基'
‑
j'
‑
(亚烷基
‑
o)
n
'
‑
亚烷基
‑
,l3是
‑
j"
‑
(亚烷基
‑
o)
n
"
‑
亚烷基
‑
,亚烷基是
‑
ch2ch2‑
,亚烷基'是
‑
(ch2)4‑
,n是1,n'和n"是3,j具有结构j'和j"具有结构并且r7是甲基。在式(vii)化合物的某些实施例中,l1是
‑
j
‑
(亚烷基
‑
o)
n
‑
亚烷基
‑
,l2是
‑
(亚烷基
‑
o)
n'
‑
亚烷基
‑
j'
‑
亚烷基'
‑
,l3是
‑
(亚烷基
‑
o)
n”‑
亚烷基
‑
j"
‑
,亚烷基是
‑
ch2ch2‑
,亚烷基'是
‑
(ch2)4‑
,n是1,n'和n"是4,并且j、j'和j"具有结构所述尾海兔素连接基团衍生物可以呈盐形式,或可并入非天然氨基酸多肽、聚合物、多糖或多核苷酸中并且任选地进行翻译后修饰。
[0489]
在某些实施例中,式(i)
‑
(vii)化合物在水溶液中在适度酸性条件下稳定至少1个月。在某些实施例中,式(i)
‑
(vii)化合物在适度酸性条件下稳定至少2周。在某些实施例中,式(i)
‑
(vii)化合物在适度酸性条件下稳定至少5天。在某些实施例中,所述酸性条件是ph 2到8。
[0490]
本文所提供和描述的方法和组合物包括包含尾海兔素连接基团衍生物的多肽,含有至少一个羰基或二羰基、肟基团、羟胺基团或其受保护或遮蔽形式。将至少一个反应性基团引入尾海兔素连接基团衍生物中能够允许应用涉及以下的结合化学物质:包括(但不限于)与一种或一种以上尾海兔素连接基团衍生物发生特异性化学反应但不与共同存在的氨基酸反应。在并入之后,尾海兔素连接基团衍生物侧链还可以通过使用本文所描述的或适用于尾海兔素连接基团衍生物中所存在的特定官能团或取代基的化学方法进行修饰。
[0491]
本文所描述的尾海兔素连接基团衍生方法和组合物提供了具有各种官能团、取代基或部分的物质与其它物质的结合物,包括(但不限于)聚合物、水溶性聚合物、聚乙二醇衍生物、第二蛋白质或多肽或多肽类似物、抗体或抗体片段和其任何组合。
[0492]
在某些实施例中,本文所描述的尾海兔素连接基团衍生物、连接基团和反应剂(包括式(i)
‑
(vii)化合物)在水溶液中在适度酸性条件(包括(但不限于)ph 2到8)下是稳定的。在其它实施例中,所述化合物在适度酸性条件下稳定至少一个月。在其它实施例中,所述化合物在适度酸性条件下稳定至少2周。在其它实施例中,所述化合物在适度酸性条件下稳定至少5天。
[0493]
本文所描述的组合物、方法、技术和策略的另一个方面是用于研究或使用上述“修饰或未修饰”的非天然氨基酸尾海兔素连接基团衍生物中的任一种的方法。仅举例来说,这方面包括将受益于包含“修饰或未修饰”的非天然氨基酸多肽或蛋白质的尾海兔素连接基团衍生物的治疗、诊断、基于分析的、工业、化妆品、植物生物学、环境、能量产生、消费者产品和/或军事用途。
[0494]
尾海兔素连接基团衍生物的非限制性实例包括:
[0495]
[0496]
[0497]
[0498]
[0499][0500]
以及
[0501][0502]
iv.非天然氨基酸衍生物
[0503]
本文所述的方法和组合物中使用的非天然氨基酸具有以下四种性质中的至少一种:(1)非天然氨基酸侧链上的至少一个官能团具有至少一种与20种常见的基因编码的氨基酸(即,丙氨酸、精氨酸、天冬酰胺、天冬氨酸、半胱氨酸、谷氨酰胺、谷氨酸、甘氨酸、组氨酸、异亮氨酸、亮氨酸、赖氨酸、甲硫氨酸、苯丙氨酸、脯氨酸、丝氨酸、苏氨酸、色氨酸、酪氨酸和缬氨酸)的化学反应性正交或者至少与存在于包括非天然氨基酸的多肽中的天然存在的氨基酸的化学反应性正交的特征和/或活性和/或反应性;(2)所引入的非天然氨基酸实质上在化学上对20种常见的基因编码的氨基酸呈惰性;(3)可将非天然氨基酸稳定地并入多肽中,优选具有与天然存在的氨基酸相当的稳定性或在典型生理条件下稳定,并且另外优选所述并入可通过体内系统发生;以及(4)非天然氨基酸包括肟官能团或可通过与试剂优选在不破坏包括非天然氨基酸的多肽的生物性质(当然,除非所述生物性质的破坏是修饰/转化的目的的情形)的条件下反应而转化成肟基团的官能团,或者其中所述转化可在水性条件下在介于约4与约8之间的ph值下发生,或其中非天然氨基酸上的反应性位点是亲电子位点。可将任何数量的非天然氨基酸引入多肽中。非天然氨基酸还可包括经保护的或经遮蔽的肟,或可在脱除保护基或除去遮蔽基团后转化成肟基团的经保护的或经遮蔽的基团。非天然氨基酸还可包括经保护的或经遮蔽的羰基或二羰基,其可在脱除保护基或去除遮蔽基团后转化成羰基或二羰基,并且由此可供用于与羟基胺或肟反应以形成肟基团。
[0504]
可用于本文所述的方法和组合物中的非天然氨基酸包括(但不限于):包含具有新颖官能团的氨基酸的氨基酸、与其它分子共价或非共价相互作用的氨基酸、糖基化氨基酸(如糖取代的丝氨酸)、其它碳水化合物修饰的氨基酸、含酮基氨基酸、含醛的氨基酸、包含聚乙二醇或其它聚醚的氨基酸、重原子取代的氨基酸、可化学裂解和/或可光裂解的氨基酸、与天然氨基酸相比具有延长的侧链的氨基酸(包括(但不限于)聚醚或长链烃,包括(但不限于)大于约5或大于约10个碳)、含碳连接糖的氨基酸、氧化还原活性氨基酸、含有氨基硫代酸的氨基酸和包含一个或一个以上毒性部分的氨基酸。
[0505]
在一些实施例中,非天然氨基酸包含糖部分。所述氨基酸的实例包括n
‑
乙酰基
‑
l
‑
葡糖氨基
‑
l
‑
丝氨酸、n
‑
乙酰基
‑
l
‑
半乳糖氨基
‑
l
‑
丝氨酸、n
‑
乙酰基
‑
l
‑
葡糖氨基
‑
l
‑
苏氨酸、n
‑
乙酰基
‑
l
‑
葡糖氨基
‑
l
‑
天冬酰胺和o
‑
甘露糖氨基
‑
l
‑
丝氨酸。所述氨基酸的实例还包
括氨基酸与糖之间的天然存在的n键或o键经自然界中不常见的共价键(包括(但不限于)烯、肟、硫醚、酰胺等)置换的实例。所述氨基酸的实例还包括天然存在的蛋白质中不常见的糖,如2
‑
脱氧
‑
葡萄糖、2
‑
脱氧半乳糖等。
[0506]
通过将非天然氨基酸并入多肽中而并入所述多肽的化学部分为多肽提供多种优势和操控。举例来说,羰基或二羰基官能团(包括酮官能团或醛官能团)的独特反应性允许在体内和体外用多种含肼或羟胺的试剂中的任一者选择性修饰蛋白质。举例来说,重原子非天然氨基酸可适用于定相x射线结构数据。使用非天然氨基酸位点特异性地引入重原子还为选择重原子的位置提供选择性和灵活性。光反应性非天然氨基酸(包括(但不限于)具有二苯甲酮和叠氮芳基(包括(但不限于)叠氮苯)侧链的氨基酸)例如允许在体内和体外有效地光交联多肽。光反应性非天然氨基酸的实例包括(但不限于)对叠氮基
‑
苯丙氨酸和对苯甲酰基
‑
苯丙氨酸。接着可通过激发提供光反应性基团的临时对照使具有光反应性非天然氨基酸的多肽随意交联。在一个非限制性实例中,非天然氨基酸的甲基可经作为局部结构和动力学探针(包括(但不限于)在使用核磁共振和振动光谱的情况下)的同位素标记的(包括(但不限于))甲基取代。
[0507]
a.非天然氨基酸衍生物的结构和合成:羰基、羰基样基团、经遮蔽羰基和经保护的羰基
[0508]
具有亲电子反应性基团的氨基酸允许通过多种化学反应(包括(但不限于)亲核加成反应)连接分子的多种反应。所述亲电子反应性基团包括羰基或二羰基(包括酮基或醛基)、羰基样或二羰基样基团(其具有与羰基或二羰基类似的反应性并且在结构上与羰基或二羰基类似)、经遮蔽羰基或经遮蔽二羰基(其可易于转化为羰基或二羰基)、或经保护的羰基或经保护的二羰基(其在脱除保护基后具有与羰基或二羰基类似的反应性)。所述氨基酸包括具有以下式(xxxvii)结构的氨基酸:
[0509][0510]
其中:
[0511]
a是任选的,并且当存在时是低碳亚烷基、经取代的低碳亚烷基、低碳亚环烷基、经取代的低碳亚环烷基、低碳亚烯基、经取代的低碳亚烯基、亚炔基、低碳亚杂烷基、经取代的亚杂烷基、低碳亚杂环烷基、经取代的低碳亚杂环烷基、亚芳基、经取代的亚芳基、亚杂芳基、经取代的亚杂芳基、亚烷芳基、经取代的亚烷芳基、亚芳烷基或经取代的亚芳烷基;
[0512]
b是任选的,并且当存在时是选自由以下组成的群组的连接基团:低碳亚烷基、经取代的低碳亚烷基、低碳亚烯基、经取代的低碳亚烯基、低碳亚杂烷基、经取代的低碳亚杂烷基、
‑
o
‑
、
‑
o
‑
(亚烷基或经取代的亚烷基)
‑
、
‑
s
‑
、
‑
s
‑
(亚烷基或经取代的亚烷基)
‑
、
‑
s(o)
k
‑
(其中k是1、2或3)、
‑
s(o)
k
(亚烷基或经取代的亚烷基)
‑
、
‑
c(o)
‑
、
‑
ns(o)2‑
、
‑
os(o)2‑
、
‑
c(o)
‑
(亚烷基或经取代的亚烷基)
‑
、
‑
c(s)
‑
、
‑
c(s)
‑
(亚烷基或经取代的亚烷基)
‑
、
‑
n(r')
‑
、
‑
nr'
‑
(亚烷基或经取代的亚烷基)
‑
、
‑
c(o)n(r')
‑
、
‑
con(r')
‑
(亚烷基或经取代的亚烷基)
‑
、
‑
csn(r')
‑
、
‑
csn(r')
‑
(亚烷基或经取代的亚烷基)
‑
、
‑
n(r')co
‑
(亚烷基或经取代的亚烷基)
‑
、
‑
n(r')c(o)o
‑
、
‑
s(o)
k
n(r')
‑
、
‑
n(r')c(o)n(r')
‑
、
‑
n(r')c(s)n
(r')
‑
、
‑
n(r')s(o)
k
n(r')
‑
、
‑
n(r')
‑
n=、
‑
c(r')=n
‑
、
‑
c(r')=n
‑
n(r')
‑
、
‑
c(r')=n
‑
n=、
‑
c(r')2‑
n=n
‑
和
‑
c(r')2‑
n(r')
‑
n(r')
‑
,其中每个r'独立地是h、烷基或经取代的烷基;
[0513]
k是
[0514]
r是h、烷基、经取代的烷基、环烷基或经取代的环烷基;
[0515]
每个r"独立地是h、烷基、经取代的烷基或保护基,或当存在一个以上r"基团时,两个r"任选地形成杂环烷基;
[0516]
r1是h、氨基保护基、树脂、氨基酸、多肽或多核苷酸;并且
[0517]
r2是oh、酯保护基、树脂、氨基酸、多肽或多核苷酸;
[0518]
r3和r4中的每一个独立地是h、卤素、低碳烷基或经取代的低碳烷基,或r3和r4或两个r3基团任选地形成环烷基或杂环烷基;
[0519]
或
‑
a
‑
b
‑
k
‑
r基团共同形成双环或三环环烷基或杂环烷基,其包含至少一个羰基(包括二羰基)、经保护的羰基(包括经保护的二羰基)或经遮蔽羰基(包括经遮蔽二羰基);
[0520]
或
‑
k
‑
r基团共同形成单环或双环环烷基或杂环烷基,其包含至少一个羰基(包括二羰基)、经保护的羰基(包括经保护的二羰基)或经遮蔽羰基(包括经遮蔽二羰基);
[0521]
其限制条件是当a是亚苯基并且每个r3是h时,b存在;并且当a是
‑
(ch2)4‑
并且每个r3是h时,b不是
‑
nhc(o)(ch2ch2)
‑
;并且当a和b不存在并且每个r3是h时,r不是甲基。所述非天然氨基酸可呈盐形式,或可并入非天然氨基酸多肽、聚合物、多糖或多核苷酸中并且任选地经翻译后修饰。
[0522]
在某些实施例中,式(xxxvii)化合物在水溶液中在适度酸性条件下稳定至少1个月。在某些实施例中,式(xxxvii)化合物在适度酸性条件下稳定至少2周。在某些实施例中,式(xxxvii)化合物在适度酸性条件下稳定至少5天。在某些实施例中,所述酸性条件是ph 2到8。
[0523]
在式(xxxvii)化合物的某些实施例中,b是低碳亚烷基、经取代的低碳亚烷基、
‑
o
‑
(亚烷基或经取代的亚烷基)
‑
、
‑
c(r')=n
‑
n(r')
‑
、
‑
n(r')co
‑
、
‑
c(o)
‑
、
‑
c(r')=n
‑
、
‑
c(o)
‑
(亚烷基或经取代的亚烷基)
‑
、
‑
con(r')
‑
(亚烷基或经取代的亚烷基)
‑
、
‑
s(亚烷基或经取代的亚烷基)
‑
、
‑
s(o)(亚烷基或经取代的亚烷基)
‑
或
‑
s(o)2(亚烷基或经取代的亚烷基)
‑
。在式(xxxvii)化合物的某些实施例中,b是
‑
o(ch2)
‑
、
‑
ch=n
‑
、
‑
ch=n
‑
nh
‑
、
‑
nhch2‑
、
‑
nhco
‑
、
‑
c(o)
‑
、
‑
c(o)
‑
(ch2)
‑
、
‑
conh
‑
(ch2)
‑
、
‑
sch2‑
、
‑
s(=o)ch2‑
或
‑
s(o)2ch2‑
。在式(xxxvii)化合物的某些实施例中,r是c1‑6烷基或环烷基。在式(xxxvii)化合物的某些实施例中,r是
‑
ch3、
‑
ch(ch3)2或环丙基。在式(xxxvii)化合物的某些实施例中,r1是h、叔丁氧羰基(boc)、9
‑
芴基甲氧基羰基(fmoc)、n
‑
乙酰基、四氟乙酰基(tfa)或苯甲氧羰基(cbz)。在式(xxxvii)化合物的某些实施例中,r1是树脂、氨基酸、多肽、抗体或多核苷酸。在式(xxxvii)化合物的某些实施例中,r2是oh、o
‑
甲基、o
‑
乙基或o
‑
叔丁基。在式(xxxvii)化合物的某些实施例中,r2是树脂、氨基酸、多肽、抗体或多核苷酸。在式(xxxvii)化合物的某些实施例中,r2是多核苷酸。在式(xxxvii)化合物的某些实施例中,r2是核糖核酸(rna)。
[0524]
在式(xxxvii)化合物的某些实施例中,是选自由以下组成的群组:
[0525]
(i)a是经取代的低碳亚烷基、c4‑
亚芳基、经取代的亚芳基、亚杂芳基、经取代的亚杂芳基、亚烷芳基、经取代的亚烷芳基、亚芳烷基或经取代的亚芳烷基;
[0526]
b是任选的,并且当存在时是选自由以下组成的群组的二价连接基团:低碳亚烷基、经取代的低碳亚烷基、低碳亚烯基、经取代的低碳亚烯基、
‑
o
‑
、
‑
o
‑
(亚烷基或经取代的亚烷基)
‑
、
‑
s
‑
、
‑
s(o)
‑
、
‑
s(o)2‑
、
‑
ns(o)2‑
、
‑
os(o)2‑
、
‑
c(o)
‑
、
‑
c(o)
‑
(亚烷基或经取代的亚烷基)
‑
、
‑
c(s)
‑
、
‑
n(r')
‑
、
‑
c(o)n(r')
‑
、
‑
con(r')
‑
(亚烷基或经取代的亚烷基)
‑
、
‑
csn(r')
‑
、
‑
n(r')co
‑
(亚烷基或经取代的亚烷基)
‑
、
‑
n(r')c(o)o
‑
、
‑
n(r')c(s)
‑
、
‑
s(o)n(r')、
‑
s(o)2n(r')、
‑
n(r')c(o)n(r')
‑
、
‑
n(r')c(s)n(r')
‑
、
‑
n(r')s(o)n(r')
‑
、
‑
n(r')s(o)2n(r')
‑
、
‑
n(r')
‑
n=、
‑
c(r')=n
‑
n(r')
‑
、
‑
c(r')=n
‑
n=、
‑
c(r')2‑
n=n
‑
和
‑
c(r')2‑
n(r')
‑
n(r')
‑
;
[0527]
(ii)a是任选的,并且当存在时是经取代的低碳亚烷基、c4‑
亚芳基、经取代的亚芳基、亚杂芳基、经取代的亚杂芳基、亚烷芳基、经取代的亚烷芳基、亚芳烷基或经取代的亚芳烷基;
[0528]
b是选自由以下组成的群组的二价连接基团:低碳亚烷基、经取代的低碳亚烷基、低碳亚烯基、经取代的低碳亚烯基、
‑
o
‑
、
‑
o
‑
(亚烷基或经取代的亚烷基)
‑
、
‑
s
‑
、
‑
s(o)
‑
、
‑
s(o)2‑
、
‑
ns(o)2‑
、
‑
os(o)2‑
、
‑
c(o)
‑
、
‑
c(o)
‑
(亚烷基或经取代的亚烷基)
‑
、
‑
c(s)
‑
、
‑
n(r')
‑
、
‑
c(o)n(r')
‑
、
‑
con(r')
‑
(亚烷基或经取代的亚烷基)
‑
、
‑
csn(r')
‑
、
‑
n(r')co
‑
(亚烷基或经取代的亚烷基)
‑
、
‑
n(r')c(o)o
‑
、
‑
n(r')c(s)
‑
、
‑
s(o)n(r')、
‑
s(o)2n(r')、
‑
n(r')c(o)n(r')
‑
、
‑
n(r')c(s)n(r')
‑
、
‑
n(r')s(o)n(r')
‑
、
‑
n(r')s(o)2n(r')
‑
、
‑
n(r')
‑
n=、
‑
c(r')=n
‑
n(r')
‑
、
‑
c(r')=n
‑
n=、
‑
c(r')2‑
n=n
‑
和
‑
c(r')2‑
n(r')
‑
n(r')
‑
;
[0529]
(iii)a是低碳亚烷基;
[0530]
b是任选的,并且当存在时是选自由以下组成的群组的二价连接基团:低碳亚烷基、经取代的低碳亚烷基、低碳亚烯基、经取代的低碳亚烯基、
‑
o
‑
、
‑
o
‑
(亚烷基或经取代的亚烷基)
‑
、
‑
s
‑
、
‑
s(o)
‑
、
‑
s(o)2‑
、
‑
ns(o)2‑
、
‑
os(o)2‑
、
‑
c(o)
‑
、
‑
c(o)
‑
(亚烷基或经取代的亚烷基)
‑
、
‑
c(s)
‑
、
‑
n(r')
‑
、
‑
c(o)n(r')
‑
、
‑
csn(r')
‑
、
‑
con(r')
‑
(亚烷基或经取代的亚烷基)
‑
、
‑
n(r')c(o)o
‑
、
‑
n(r')c(s)
‑
、
‑
s(o)n(r')、
‑
s(o)2n(r')、
‑
n(r')c(o)n(r')
‑
、
‑
n(r')c(s)n(r')
‑
、
‑
n(r')s(o)n(r')
‑
、
‑
n(r')s(o)2n(r')
‑
、
‑
n(r')
‑
n=、
‑
c(r')=n
‑
n(r')
‑
、
‑
c(r')=n
‑
n=、
‑
c(r')2‑
n=n
‑
和
‑
c(r')2‑
n(r')
‑
n(r');以及
[0531]
(iv)a是亚苯基;
[0532]
b是选自由以下组成的群组的二价连接基团:低碳亚烷基、经取代的低碳亚烷基、低碳亚烯基、经取代的低碳亚烯基、
‑
o
‑
、
‑
o
‑
(亚烷基或经取代的亚烷基)
‑
、
‑
s
‑
、
‑
s(o)
‑
、
‑
s(o)2‑
、
‑
ns(o)2‑
、
‑
os(o)2‑
、
‑
c(o)
‑
、
‑
c(o)
‑
(亚烷基或经取代的亚烷基)
‑
、
‑
c(s)
‑
、
‑
n(r')
‑
、
‑
c(o)n(r')
‑
、
‑
con(r')
‑
(亚烷基或经取代的亚烷基)
‑
、
‑
csn(r')
‑
、
‑
n(r')co
‑
(亚烷基或经取代的亚烷基)
‑
、
‑
n(r')c(o)o
‑
、
‑
n(r')c(s)
‑
、
‑
s(o)n(r')、
‑
s(o)2n(r')、
‑
n(r')c(o)n(r')
‑
、
‑
n(r')c(s)n(r')
‑
、
‑
n(r')s(o)n(r')
‑
、
‑
n(r')s(o)2n(r')
‑
、
‑
n(r')
‑
n=、
‑
c(r')=n
‑
n(r')
‑
、
‑
c(r')=n
‑
n=、
‑
c(r')2‑
n=n
‑
和
‑
c(r')2‑
n(r')
‑
n(r')
‑
;
[0533]
k是
[0534]
每个r'独立地是h、烷基或经取代的烷基;
[0535]
r1是任选的,并且当存在时是h、氨基保护基、树脂、氨基酸、多肽或多核苷酸;并且
[0536]
r2是任选的,并且当存在时是oh、酯保护基、树脂、氨基酸、多肽或多核苷酸;并且
[0537]
r3和r4各自独立地是h、卤素、低碳烷基或经取代的低碳烷基;
[0538]
r是h、烷基、经取代的烷基、环烷基或经取代的环烷基。
[0539]
另外,包括具有式(xxxviii)结构的氨基酸:
[0540][0541]
其中:
[0542]
a是任选的,并且当存在时是低碳亚烷基、经取代的低碳亚烷基、低碳亚环烷基、经取代的低碳亚环烷基、低碳亚烯基、经取代的低碳亚烯基、亚炔基、低碳亚杂烷基、经取代的亚杂烷基、低碳亚杂环烷基、经取代的低碳亚杂环烷基、亚芳基、经取代的亚芳基、亚杂芳基、经取代的亚杂芳基、亚烷芳基、经取代的亚烷芳基、亚芳烷基或经取代的亚芳烷基;
[0543]
b是任选的,并且当存在时是选自由以下组成的群组的连接基团:低碳亚烷基、经取代的低碳亚烷基、低碳亚烯基、经取代的低碳亚烯基、低碳亚杂烷基、经取代的低碳亚杂烷基、
‑
o
‑
、
‑
o
‑
(亚烷基或经取代的亚烷基)
‑
、
‑
s
‑
、
‑
s
‑
(亚烷基或经取代的亚烷基)
‑
、
‑
s(o)
k
‑
(其中k是1、2或3)、
‑
s(o)
k
(亚烷基或经取代的亚烷基)
‑
、
‑
c(o)
‑
、
‑
ns(o)2‑
、
‑
os(o)2‑
、
‑
c(o)
‑
(亚烷基或经取代的亚烷基)
‑
、
‑
c(s)
‑
、
‑
c(s)
‑
(亚烷基或经取代的亚烷基)
‑
、
‑
n(r')
‑
、
‑
nr'
‑
(亚烷基或经取代的亚烷基)
‑
、
‑
c(o)n(r')
‑
、
‑
con(r')
‑
(亚烷基或经取代的亚烷基)
‑
、
‑
csn(r')
‑
、
‑
csn(r')
‑
(亚烷基或经取代的亚烷基)
‑
、
‑
n(r')co
‑
(亚烷基或经取代的亚烷基)
‑
、
‑
n(r')c(o)o
‑
、
‑
s(o)
k
n(r')
‑
、
‑
n(r')c(o)n(r')
‑
、
‑
n(r')c(s)n(r')
‑
、
‑
n(r')s(o)
k
n(r')
‑
、
‑
n(r')
‑
n=、
‑
c(r')=n
‑
、
‑
c(r')=n
‑
n(r')
‑
、
‑
c(r')=n
‑
n=、
‑
c(r')2‑
n=n
‑
和
‑
c(r')2‑
n(r')
‑
n(r')
‑
,其中每个r'独立地是h、烷基或经取代的烷基;
[0544]
r是h、烷基、经取代的烷基、环烷基或经取代的环烷基;
[0545]
r1是h、氨基保护基、树脂、至少一个氨基酸、多肽或多核苷酸;并且
[0546]
r2是oh、酯保护基、树脂、至少一个氨基酸、多肽或多核苷酸;
[0547]
其限制条件是当a是亚苯基时,b存在;并且当a是
‑
(ch2)4‑
时,b不是
‑
nhc(o)(ch2ch2)
‑
;并且当a和b不存在时,r不是甲基。所述非天然氨基酸可呈盐形式,或可并入非天然氨基酸多肽、聚合物、多糖或多核苷酸中并且任选地经翻译后修饰。
[0548]
另外,包括具有式(xxxix)结构的氨基酸:
[0549]
[0550]
其中:
[0551]
b是选自由以下组成的群组的连接基团:低碳亚烷基、经取代的低碳亚烷基、低碳亚烯基、经取代的低碳亚烯基、低碳亚杂烷基、经取代的低碳亚杂烷基、
‑
o
‑
、
‑
o
‑
(亚烷基或经取代的亚烷基)
‑
、
‑
s
‑
、
‑
s
‑
(亚烷基或经取代的亚烷基)
‑
、
‑
s(o)
k
‑
(其中k是1、2或3)、
‑
s(o)
k
(亚烷基或经取代的亚烷基)
‑
、
‑
c(o)
‑
、
‑
ns(o)2‑
、
‑
os(o)2、
‑
c(o)
‑
(亚烷基或经取代的亚烷基)
‑
、
‑
c(s)
‑
、
‑
c(s)
‑
(亚烷基或经取代的亚烷基)
‑
、
‑
n(r')
‑
、
‑
nr'
‑
(亚烷基或经取代的亚烷基)
‑
、
‑
c(o)n(r')
‑
、
‑
con(r')
‑
(亚烷基或经取代的亚烷基)
‑
、
‑
csn(r')
‑
、
‑
csn(r')
‑
(亚烷基或经取代的亚烷基)
‑
、
‑
n(r')co
‑
(亚烷基或经取代的亚烷基)
‑
、
‑
n(r')c(o)o
‑
、
‑
s(o)
k
n(r')
‑
、
‑
n(r')c(o)n(r')
‑
、
‑
n(r')c(s)n(r')
‑
、
‑
n(r')s(o)
k
n(r')
‑
、
‑
n(r')
‑
n=、
‑
c(r')=n
‑
、
‑
c(r')=n
‑
n(r')
‑
、
‑
c(r')=n
‑
n=、
‑
c(r')2‑
n=n
‑
和
‑
c(r')2‑
n(r')
‑
n(r')
‑
,其中每个r'独立地是h、烷基或经取代的烷基;
[0552]
r是h、烷基、经取代的烷基、环烷基或经取代的环烷基;
[0553]
r1是h、氨基保护基、树脂、氨基酸、多肽或多核苷酸;并且
[0554]
r2是oh、酯保护基、树脂、氨基酸、多肽或多核苷酸;
[0555]
每个r
a
独立地选自由以下组成的群组:h、卤素、烷基、经取代的烷基、
‑
n(r')2、
‑
c(o)
k
r'(其中k是1、2或3)、
‑
c(o)n(r')2、
‑
or'和
‑
s(o)
k
r',其中每个r'独立地是h、烷基或经取代的烷基。所述非天然氨基酸可呈盐形式,或可并入非天然氨基酸多肽、聚合物、多糖或多核苷酸中并且任选地经翻译后修饰。
[0556]
另外,包括以下氨基酸:
[0557][0558]
以及
[0559]
所述非天然氨基酸可任选地是氨基保护基、羧基经保护的和/或呈盐形式,或可并入非天然氨基酸多肽、聚合物、多糖或多核苷酸中并且任选地经翻译后修饰。
[0560]
另外,包括以下具有式(xxxx)结构的氨基酸:
[0561][0562]
其中
[0563]
‑
ns(o)2‑
、
‑
os(o)2‑
任选的并且当存在时是选自由以下组成的群组的连接基团:低碳亚烷基、经取代的低碳亚烷基、低碳亚烯基、经取代的低碳亚烯基、低碳亚杂烷基、经取代
的低碳亚杂烷基、
‑
o
‑
、
‑
o
‑
(亚烷基或经取代的亚烷基)
‑
、
‑
s
‑
、
‑
s
‑
(亚烷基或经取代的亚烷基)
‑
、
‑
s(o)
k
‑
(其中k是1、2或3)、
‑
s(o)
k
(亚烷基或经取代的亚烷基)
‑
、
‑
c(o)
‑
、
‑
c(o)
‑
(亚烷基或经取代的亚烷基)
‑
、
‑
c(s)
‑
、
‑
c(s)
‑
(亚烷基或经取代的亚烷基)
‑
、
‑
n(r')
‑
、
‑
nr'
‑
(亚烷基或经取代的亚烷基)
‑
、
‑
c(o)n(r')
‑
、
‑
con(r')
‑
(亚烷基或经取代的亚烷基)
‑
、
‑
csn(r')
‑
、
‑
csn(r')
‑
(亚烷基或经取代的亚烷基)
‑
、
‑
n(r')co
‑
(亚烷基或经取代的亚烷基)
‑
、
‑
n(r')c(o)o
‑
、
‑
s(o)
k
n(r')
‑
、
‑
n(r')c(o)n(r')
‑
、
‑
n(r')c(s)n(r')
‑
、
‑
n(r')s(o)
k
n(r')
‑
、
‑
n(r')
‑
n=、
‑
c(r')=n
‑
、
‑
c(r')=n
‑
n(r')
‑
、
‑
c(r')=n
‑
n=、
‑
c(r')2‑
n=n
‑
和
‑
c(r')2‑
n(r')
‑
n(r')
‑
,其中每个r'独立地是h、烷基或经取代的烷基;
[0564]
r是h、烷基、经取代的烷基、环烷基或经取代的环烷基;
[0565]
r1是h、氨基保护基、树脂、氨基酸、多肽或多核苷酸;并且
[0566]
r2是oh、酯保护基、树脂、氨基酸、多肽或多核苷酸;
[0567]
每个r
a
独立地选自由以下组成的群组:h、卤素、烷基、经取代的烷基、
‑
n(r')2、
‑
c(o)
k
r'(其中k是1、2或3)、
‑
c(o)n(r')2、
‑
or'和
‑
s(o)
k
r',其中每个r'独立地是h、烷基或经取代的烷基;并且n是0到8;
[0568]
其限制条件是当a是
‑
(ch2)4‑
时,b不是
‑
nhc(o)(ch2ch2)
‑
。所述非天然氨基酸可呈盐形式,或可并入非天然氨基酸多肽、聚合物、多糖或多核苷酸中并且任选地经翻译后修饰。
[0569]
另外,包括以下氨基酸:
[0570][0571]
以及其中所述化合物任选地氨基经保护、任选地羧基经保护、任选地氨基经保护和羧基经保护,或是其盐,或可并入非天然氨基酸多肽、聚合物、多糖或多核苷酸中并且任选地经翻译后修饰。
[0572]
另外,包括以下具有式(xxxxi)结构的氨基酸:
[0573][0574]
其中,
[0575]
a是任选的,并且当存在时是低碳亚烷基、经取代的低碳亚烷基、低碳亚环烷基、经取代的低碳亚环烷基、低碳亚烯基、经取代的低碳亚烯基、亚炔基、低碳亚杂烷基、经取代的亚杂烷基、低碳亚杂环烷基、经取代的低碳亚杂环烷基、亚芳基、经取代的亚芳基、亚杂芳基、经取代的亚杂芳基、亚烷芳基、经取代的亚烷芳基、亚芳烷基或经取代的亚芳烷基;
[0576]
b是任选的,并且当存在时是选自由以下组成的群组的连接基团:低碳亚烷基、经取代的低碳亚烷基、低碳亚烯基、经取代的低碳亚烯基、低碳亚杂烷基、经取代的低碳亚杂烷基、
‑
o
‑
、
‑
o
‑
(亚烷基或经取代的亚烷基)
‑
、
‑
s
‑
、
‑
s
‑
(亚烷基或经取代的亚烷基)
‑
、
‑
s(o)
k
‑
(其中k是1、2或3)、
‑
s(o)
k
(亚烷基或经取代的亚烷基)
‑
、
‑
c(o)
‑
、
‑
ns(o)2‑
、
‑
os(o)2‑
、
‑
c(o)
‑
(亚烷基或经取代的亚烷基)
‑
、
‑
c(s)
‑
、
‑
c(s)
‑
(亚烷基或经取代的亚烷基)
‑
、
‑
n(r')
‑
、
‑
nr'
‑
(亚烷基或经取代的亚烷基)
‑
、
‑
c(o)n(r')
‑
、
‑
con(r')
‑
(亚烷基或经取代的亚烷基)
‑
、
‑
csn(r')
‑
、
‑
csn(r')
‑
(亚烷基或经取代的亚烷基)
‑
、
‑
n(r')co
‑
(亚烷基或经取代的亚烷基)
‑
、
‑
n(r')c(o)o
‑
、
‑
s(o)
k
n(r')
‑
、
‑
n(r')c(o)n(r')
‑
、
‑
n(r')c(s)n(r')
‑
、
‑
n(r')s(o)
k
n(r')
‑
、
‑
n(r')
‑
n=、
‑
c(r')=n
‑
、
‑
c(r')=n
‑
n(r')
‑
、
‑
c(r')=n
‑
n=、
‑
c(r')2‑
n=n
‑
和
‑
c(r')2‑
n(r')
‑
n(r')
‑
,其中每个r'独立地是h、烷基或经取代的烷基;
[0577]
r1是h、氨基保护基、树脂、氨基酸、多肽或多核苷酸;并且
[0578]
r2是oh、酯保护基、树脂、氨基酸、多肽或多核苷酸。
[0579]
所述非天然氨基酸可呈盐形式,或可并入非天然氨基酸多肽、聚合物、多糖或多核苷酸中并且任选地经翻译后修饰。
[0580]
另外,包括以下具有式(xxxxii)结构的氨基酸:
[0581][0582]
其中,
[0583]
b是任选的,并且当存在时是选自由以下组成的群组的连接基团:低碳亚烷基、经取代的低碳亚烷基、低碳亚烯基、经取代的低碳亚烯基、低碳亚杂烷基、经取代的低碳亚杂烷基、
‑
o
‑
、
‑
o
‑
(亚烷基或经取代的亚烷基)
‑
、
‑
s
‑
、
‑
s
‑
(亚烷基或经取代的亚烷基)
‑
、
‑
s(o)
k
‑
(其中k是1、2或3)、
‑
s(o)
k
(亚烷基或经取代的亚烷基)
‑
、
‑
c(o)
‑
、
‑
ns(o)2‑
、
‑
os(o)2‑
、
‑
c(o)
‑
(亚烷基或经取代的亚烷基)
‑
、
‑
c(s)
‑
、
‑
c(s)
‑
(亚烷基或经取代的亚烷基)
‑
、
‑
n(r')
‑
、
‑
nr'
‑
(亚烷基或经取代的亚烷基)
‑
、
‑
c(o)n(r')
‑
、
‑
con(r')
‑
(亚烷基或经取代的亚烷基)
‑
、
‑
csn(r')
‑
、
‑
csn(r')
‑
(亚烷基或经取代的亚烷基)
‑
、
‑
n(r')co
‑
(亚烷基
或经取代的亚烷基)
‑
、
‑
n(r')c(o)o
‑
、
‑
s(o)
k
n(r')
‑
、
‑
n(r')c(o)n(r')
‑
、
‑
n(r')c(s)n(r')
‑
、
‑
n(r')s(o)
k
n(r')
‑
、
‑
n(r')
‑
n=、
‑
c(r')=n
‑
、
‑
c(r')=n
‑
n(r')
‑
、
‑
c(r')=n
‑
n=、
‑
c(r')2‑
n=n
‑
和
‑
c(r')2‑
n(r')
‑
n(r')
‑
,其中每个r'独立地是h、烷基或经取代的烷基;
[0584]
r是h、烷基、经取代的烷基、环烷基或经取代的环烷基;
[0585]
r1是h、氨基保护基、树脂、氨基酸、多肽或多核苷酸;并且
[0586]
r2是oh、酯保护基、树脂、氨基酸、多肽或多核苷酸;
[0587]
其中每个r
a
独立地选自由以下组成的群组:h、卤素、烷基、经取代的烷基、
‑
n(r')2、
‑
c(o)
k
r'(其中k是1、2或3)、
‑
c(o)n(r')2、
‑
or'和
‑
s(o)
k
r',其中每个r'独立地是h、烷基或经取代的烷基。
[0588]
所述非天然氨基酸可呈盐形式,或可并入非天然氨基酸多肽、聚合物、多糖或多核苷酸中并且任选地经翻译后修饰。
[0589]
另外,包括以下氨基酸:
[0590][0591]
以及
[0592]
其中所述化合物任选地氨基经保护、任选地羧基经保护、任选地氨基经保护和羧基经保护,或是其盐,或可并入非天然氨基酸多肽、聚合物、多糖或多核苷酸中并且任选地经翻译后修饰。
[0593]
另外,包括以下具有式(xxxxiv)结构的氨基酸:
[0594][0595]
其中,
[0596]
b是任选的,并且当存在时是选自由以下组成的群组的连接基团:低碳亚烷基、经取代的低碳亚烷基、低碳亚烯基、经取代的低碳亚烯基、低碳亚杂烷基、经取代的低碳亚杂烷基、
‑
o
‑
、
‑
o
‑
(亚烷基或经取代的亚烷基)
‑
、
‑
s
‑
、
‑
s
‑
(亚烷基或经取代的亚烷基)
‑
、
‑
s(o)
k
‑
(其中k是1、2或3)、
‑
s(o)
k
(亚烷基或经取代的亚烷基)
‑
、
‑
c(o)
‑
、
‑
ns(o)2‑
、
‑
os(o)2‑
、
‑
c(o)
‑
(亚烷基或经取代的亚烷基)
‑
、
‑
c(s)
‑
、
‑
c(s)
‑
(亚烷基或经取代的亚烷基)
‑
、
‑
n(r')
‑
、
‑
nr'
‑
(亚烷基或经取代的亚烷基)
‑
、
‑
c(o)n(r')
‑
、
‑
con(r')
‑
(亚烷基或经取代的亚烷基)
‑
、
‑
csn(r')
‑
、
‑
csn(r')
‑
(亚烷基或经取代的亚烷基)
‑
、
‑
n(r')co
‑
(亚烷基或经取代的亚烷基)
‑
、
‑
n(r')c(o)o
‑
、
‑
s(o)
k
n(r')
‑
、
‑
n(r')c(o)n(r')
‑
、
‑
n(r')c(s)n
(r')
‑
、
‑
n(r')s(o)
k
n(r')
‑
、
‑
n(r')
‑
n=、
‑
c(r')=n
‑
、
‑
c(r')=n
‑
n(r')
‑
、
‑
c(r')=n
‑
n=、
‑
c(r')2‑
n=n
‑
和
‑
c(r')2‑
n(r')
‑
n(r')
‑
,其中每个r'独立地是h、烷基或经取代的烷基;
[0597]
r是h、烷基、经取代的烷基、环烷基或经取代的环烷基;
[0598]
r1是h、氨基保护基、树脂、氨基酸、多肽或多核苷酸;并且
[0599]
r2是oh、酯保护基、树脂、氨基酸、多肽或多核苷酸;
[0600]
每个r
a
独立地选自由以下组成的群组:h、卤素、烷基、经取代的烷基、
‑
n(r')2、
‑
c(o)
k
r'(其中k是1、2或3)、
‑
c(o)n(r')2、
‑
or'和
‑
s(o)
k
r',其中每个r'独立地是h、烷基或经取代的烷基;并且n是0到8。
[0601]
所述非天然氨基酸可呈盐形式,或可并入非天然氨基酸多肽、聚合物、多糖或多核苷酸中并且任选地经翻译后修饰。
[0602]
另外,包括以下氨基酸:
[0603]
以及
[0604][0605]
其中所述化合物任选地氨基经保护、任选地羧基经保护、任选地氨基经保护和羧基经保护,或是其盐,或可并入非天然氨基酸多肽、聚合物、多糖或多核苷酸中并且任选地经翻译后修饰。
[0606]
除单羰基结构以外,本文所述的非天然氨基酸可包括如二羰基、二羰基样基团、经遮蔽二羰基和经保护的二羰基。举例来说,包括以下具有式(xxxxv)结构的氨基酸:
[0607][0608]
其中,
[0609]
a是任选的,并且当存在时是低碳亚烷基、经取代的低碳亚烷基、低碳亚环烷基、经取代的低碳亚环烷基、低碳亚烯基、经取代的低碳亚烯基、亚炔基、低碳亚杂烷基、经取代的亚杂烷基、低碳亚杂环烷基、经取代的低碳亚杂环烷基、亚芳基、经取代的亚芳基、亚杂芳基、经取代的亚杂芳基、亚烷芳基、经取代的亚烷芳基、亚芳烷基或经取代的亚芳烷基;
[0610]
b是任选的,并且当存在时是选自由以下组成的群组的连接基团:低碳亚烷基、经取代的低碳亚烷基、低碳亚烯基、经取代的低碳亚烯基、低碳亚杂烷基、经取代的低碳亚杂烷基、
‑
o
‑
、
‑
o
‑
(亚烷基或经取代的亚烷基)
‑
、
‑
s
‑
、
‑
s
‑
(亚烷基或经取代的亚烷基)
‑
、
‑
s
(o)
k
‑
(其中k是1、2或3)、
‑
s(o)
k
(亚烷基或经取代的亚烷基)
‑
、
‑
c(o)
‑
、
‑
ns(o)2‑
、
‑
os(o)2‑
、
‑
c(o)
‑
(亚烷基或经取代的亚烷基)
‑
、
‑
c(s)
‑
、
‑
c(s)
‑
(亚烷基或经取代的亚烷基)
‑
、
‑
n(r')
‑
、
‑
nr'
‑
(亚烷基或经取代的亚烷基)
‑
、
‑
c(o)n(r')
‑
、
‑
con(r')
‑
(亚烷基或经取代的亚烷基)
‑
、
‑
csn(r')
‑
、
‑
csn(r')
‑
(亚烷基或经取代的亚烷基)
‑
、
‑
n(r')co
‑
(亚烷基或经取代的亚烷基)
‑
、
‑
n(r')c(o)o
‑
、
‑
s(o)
k
n(r')
‑
、
‑
n(r')c(o)n(r')
‑
、
‑
n(r')c(s)n(r')
‑
、
‑
n(r')s(o)
k
n(r')
‑
、
‑
n(r')
‑
n=、
‑
c(r')=n
‑
、
‑
c(r')=n
‑
n(r')
‑
、
‑
c(r')=n
‑
n=、
‑
c(r')2‑
n=n
‑
和
‑
c(r')2‑
n(r')
‑
n(r')
‑
,其中每个r'独立地是h、烷基或经取代的烷基;
[0611]
r是h、烷基、经取代的烷基、环烷基或经取代的环烷基;
[0612]
r1是h、氨基保护基、树脂、氨基酸、多肽或多核苷酸;并且
[0613]
r2是oh、酯保护基、树脂、氨基酸、多肽或多核苷酸。
[0614]
所述非天然氨基酸可呈盐形式,或可并入非天然氨基酸多肽、聚合物、多糖或多核苷酸中并且任选地经翻译后修饰。
[0615]
另外,包括以下具有式(xxxxvi)结构的氨基酸:
[0616][0617]
其中,
[0618]
b是任选的,并且当存在时是选自由以下组成的群组的连接基团:低碳亚烷基、经取代的低碳亚烷基、低碳亚烯基、经取代的低碳亚烯基、低碳亚杂烷基、经取代的低碳亚杂烷基、
‑
o
‑
、
‑
o
‑
(亚烷基或经取代的亚烷基)
‑
、
‑
s
‑
、
‑
s
‑
(亚烷基或经取代的亚烷基)
‑
、
‑
s(o)
k
‑
(其中k是1、2或3)、
‑
s(o)
k
(亚烷基或经取代的亚烷基)
‑
、
‑
c(o)
‑
、
‑
ns(o)2‑
、
‑
os(o)2‑
、
‑
c(o)
‑
(亚烷基或经取代的亚烷基)
‑
、
‑
c(s)
‑
、
‑
c(s)
‑
(亚烷基或经取代的亚烷基)
‑
、
‑
n(r')
‑
、
‑
nr'
‑
(亚烷基或经取代的亚烷基)
‑
、
‑
c(o)n(r')
‑
、
‑
con(r')
‑
(亚烷基或经取代的亚烷基)
‑
、
‑
csn(r')
‑
、
‑
csn(r')
‑
(亚烷基或经取代的亚烷基)
‑
、
‑
n(r')co
‑
(亚烷基或经取代的亚烷基)
‑
、
‑
n(r')c(o)o
‑
、
‑
s(o)
k
n(r')
‑
、
‑
n(r')c(o)n(r')
‑
、
‑
n(r')c(s)n(r')
‑
、
‑
n(r')s(o)
k
n(r')
‑
、
‑
n(r')
‑
n=、
‑
c(r')=n
‑
、
‑
c(r')=n
‑
n(r')
‑
、
‑
c(r')=n
‑
n=、
‑
c(r')2‑
n=n
‑
和
‑
c(r')2‑
n(r')
‑
n(r')
‑
,其中每个r'独立地是h、烷基或经取代的烷基;
[0619]
r是h、烷基、经取代的烷基、环烷基或经取代的环烷基;
[0620]
r1是h、氨基保护基、树脂、氨基酸、多肽或多核苷酸;并且
[0621]
r2是oh、酯保护基、树脂、氨基酸、多肽或多核苷酸;
[0622]
其中每个r
a
独立地选自由以下组成的群组:h、卤素、烷基、经取代的烷基、
‑
n(r')2、
‑
c(o)
k
r'(其中k是1、2或3)、
‑
c(o)n(r')2、
‑
or'和
‑
s(o)
k
r',其中每个r'独立地是h、烷基或经取代的烷基。
[0623]
所述非天然氨基酸可呈盐形式,或可并入非天然氨基酸多肽、聚合物、多糖或多核苷酸中并且任选地经翻译后修饰。
[0624]
另外,包括以下氨基酸:
[0625][0626]
其中所述化合物任选地氨基经保护和羧基经保护,或是其盐。所述非天然氨基酸可呈盐形式,或可并入非天然氨基酸多肽、聚合物、多糖或多核苷酸中并且任选地经翻译后修饰。
[0627]
另外,包括以下具有式(xxxxvii)结构的氨基酸:
[0628][0629]
其中,
[0630]
b是任选的,并且当存在时是选自由以下组成的群组的连接基团:低碳亚烷基、经取代的低碳亚烷基、低碳亚烯基、经取代的低碳亚烯基、低碳亚杂烷基、经取代的低碳亚杂烷基、
‑
o
‑
、
‑
o
‑
(亚烷基或经取代的亚烷基)
‑
、
‑
s
‑
、
‑
s
‑
(亚烷基或经取代的亚烷基)
‑
、
‑
s(o)
k
‑
(其中k是1、2或3)、
‑
s(o)
k
(亚烷基或经取代的亚烷基)
‑
、
‑
c(o)
‑
、
‑
ns(o)2‑
、
‑
os(o)2‑
、
‑
c(o)
‑
(亚烷基或经取代的亚烷基)
‑
、
‑
c(s)
‑
、
‑
c(s)
‑
(亚烷基或经取代的亚烷基)
‑
、
‑
n(r')
‑
、
‑
nr'
‑
(亚烷基或经取代的亚烷基)
‑
、
‑
c(o)n(r')
‑
、
‑
con(r')
‑
(亚烷基或经取代的亚烷基)
‑
、
‑
csn(r')
‑
、
‑
csn(r')
‑
(亚烷基或经取代的亚烷基)
‑
、
‑
n(r')co
‑
(亚烷基或经取代的亚烷基)
‑
、
‑
n(r')c(o)o
‑
、
‑
s(o)
k
n(r')
‑
、
‑
n(r')c(o)n(r')
‑
、
‑
n(r')c(s)n(r')
‑
、
‑
n(r')s(o)
k
n(r')
‑
、
‑
n(r')
‑
n=、
‑
c(r')=n
‑
、
‑
c(r')=n
‑
n(r')
‑
、
‑
c(r')=n
‑
n=、
‑
c(r')2‑
n=n
‑
和
‑
c(r')2‑
n(r')
‑
n(r')
‑
,其中每个r'独立地是h、烷基或经取代的烷基;
[0631]
r是h、烷基、经取代的烷基、环烷基或经取代的环烷基;
[0632]
r1是h、氨基保护基、树脂、氨基酸、多肽或多核苷酸;并且
[0633]
r2是oh、酯保护基、树脂、氨基酸、多肽或多核苷酸;
[0634]
每个r
a
独立地选自由以下组成的群组:h、卤素、烷基、经取代的烷基、
‑
n(r')2、
‑
c(o)
k
r'(其中k是1、2或3)、
‑
c(o)n(r')2、
‑
or'和
‑
s(o)
k
r',其中每个r'独立地是h、烷基或经取代的烷基;并且n是0到8。
[0635]
所述非天然氨基酸可呈盐形式,或可并入非天然氨基酸多肽、聚合物、多糖或多核苷酸中并且任选地经翻译后修饰。
[0636]
另外,包括以下氨基酸:
[0637][0637]
其中所述化合物任选地氨基经保护和羧基经保护,或是其盐,或可并入非天然氨基酸多肽、聚合物、多糖或多核苷酸中并且任选地经翻译后修饰。
[0638]
另外,包括以下具有式(xxxxviii)结构的氨基酸:
[0639][0640]
其中:
[0641]
a是任选的,并且当存在时是低碳亚烷基、经取代的低碳亚烷基、低碳亚环烷基、经取代的低碳亚环烷基、低碳亚烯基、经取代的低碳亚烯基、亚炔基、低碳亚杂烷基、经取代的亚杂烷基、低碳亚杂环烷基、经取代的低碳亚杂环烷基、亚芳基、经取代的亚芳基、亚杂芳基、经取代的亚杂芳基、亚烷芳基、经取代的亚烷芳基、亚芳烷基或经取代的亚芳烷基;
[0642]
r是h、烷基、经取代的烷基、环烷基或经取代的环烷基;
[0643]
r1是h、氨基保护基、树脂、氨基酸、多肽或多核苷酸;并且
[0644]
r2是oh、酯保护基、树脂、氨基酸、多肽或多核苷酸;
[0645]
x1是c、s或s(o);并且l是亚烷基、经取代的亚烷基、n(r')(亚烷基)或n(r')(经取代的亚烷基),其中r'是h、烷基、经取代的烷基、环烷基或经取代的环烷基。
[0646]
所述非天然氨基酸可呈盐形式,或可并入非天然氨基酸多肽、聚合物、多糖或多核苷酸中并且任选地经翻译后修饰。
[0647]
另外,包括以下具有式(xxxxix)结构的氨基酸:
[0648][0649]
其中:
[0650]
a是任选的,并且当存在时是低碳亚烷基、经取代的低碳亚烷基、低碳亚环烷基、经取代的低碳亚环烷基、低碳亚烯基、经取代的低碳亚烯基、亚炔基、低碳亚杂烷基、经取代的亚杂烷基、低碳亚杂环烷基、经取代的低碳亚杂环烷基、亚芳基、经取代的亚芳基、亚杂芳基、经取代的亚杂芳基、亚烷芳基、经取代的亚烷芳基、亚芳烷基或经取代的亚芳烷基;
[0651]
r是h、烷基、经取代的烷基、环烷基或经取代的环烷基;
[0652]
r1是h、氨基保护基、树脂、氨基酸、多肽或多核苷酸;并且
[0653]
r2是oh、酯保护基、树脂、氨基酸、多肽或多核苷酸;
[0654]
l是亚烷基、经取代的亚烷基、n(r')(亚烷基)或n(r')(经取代的亚烷基),其中r'是h、烷基、经取代的烷基、环烷基或经取代的环烷基。
[0655]
所述非天然氨基酸可呈盐形式,或可并入非天然氨基酸多肽、聚合物、多糖或多核苷酸中并且任选地经翻译后修饰。
[0656]
另外,包括以下具有式(xxxxx)结构的氨基酸:
[0657][0658]
其中:
[0659]
a是任选的,并且当存在时是低碳亚烷基、经取代的低碳亚烷基、低碳亚环烷基、经取代的低碳亚环烷基、低碳亚烯基、经取代的低碳亚烯基、亚炔基、低碳亚杂烷基、经取代的亚杂烷基、低碳亚杂环烷基、经取代的低碳亚杂环烷基、亚芳基、经取代的亚芳基、亚杂芳基、经取代的亚杂芳基、亚烷芳基、经取代的亚烷芳基、亚芳烷基或经取代的亚芳烷基;
[0660]
r是h、烷基、经取代的烷基、环烷基或经取代的环烷基;
[0661]
r1是h、氨基保护基、树脂、氨基酸、多肽或多核苷酸;并且
[0662]
r2是oh、酯保护基、树脂、氨基酸、多肽或多核苷酸;
[0663]
l是亚烷基、经取代的亚烷基、n(r')(亚烷基)或n(r')(经取代的亚烷基),其中r'是h、烷基、经取代的烷基、环烷基或经取代的环烷基。
[0664]
所述非天然氨基酸可呈盐形式,或可并入非天然氨基酸多肽、聚合物、多糖或多核苷酸中并且任选地经翻译后修饰。
[0665]
另外,包括以下具有式(xxxxxi)结构的氨基酸:
[0666][0667]
其中:
[0668]
a是任选的,并且当存在时是低碳亚烷基、经取代的低碳亚烷基、低碳亚环烷基、经取代的低碳亚环烷基、低碳亚烯基、经取代的低碳亚烯基、亚炔基、低碳亚杂烷基、经取代的亚杂烷基、低碳亚杂环烷基、经取代的低碳亚杂环烷基、亚芳基、经取代的亚芳基、亚杂芳基、经取代的亚杂芳基、亚烷芳基、经取代的亚烷芳基、亚芳烷基或经取代的亚芳烷基;
[0669]
r是h、烷基、经取代的烷基、环烷基或经取代的环烷基;
[0670]
r1是h、氨基保护基、树脂、氨基酸、多肽或多核苷酸;并且
[0671]
r2是oh、酯保护基、树脂、氨基酸、多肽或多核苷酸;
[0672]
x1是c、s或s(o);并且n是0、1、2、3、4或5;并且每个cr8r9基团上的r8和r9各自独立地选自由以下组成的群组:h、烷氧基、烷基胺、卤素、烷基、芳基,或任何r8和r9可共同形成=o或环烷基,或任一者与邻接r8基团可共同形成环烷基。
[0673]
所述非天然氨基酸可呈盐形式,或可并入非天然氨基酸多肽、聚合物、多糖或多核苷酸中并且任选地经翻译后修饰。
[0674]
另外,包括以下具有式(xxxxxii)结构的氨基酸:
[0675][0676]
其中:
[0677]
a是任选的,并且当存在时是低碳亚烷基、经取代的低碳亚烷基、低碳亚环烷基、经取代的低碳亚环烷基、低碳亚烯基、经取代的低碳亚烯基、亚炔基、低碳亚杂烷基、经取代的亚杂烷基、低碳亚杂环烷基、经取代的低碳亚杂环烷基、亚芳基、经取代的亚芳基、亚杂芳基、经取代的亚杂芳基、亚烷芳基、经取代的亚烷芳基、亚芳烷基或经取代的亚芳烷基;
[0678]
r是h、烷基、经取代的烷基、环烷基或经取代的环烷基;
[0679]
r1是h、氨基保护基、树脂、氨基酸、多肽或多核苷酸;并且
[0680]
r2是oh、酯保护基、树脂、氨基酸、多肽或多核苷酸;
[0681]
n是0、1、2、3、4或5;并且每个cr8r9基团上的r8和r9各自独立地选自由以下组成的群组:h、烷氧基、烷基胺、卤素、烷基、芳基,或任何r8和r9可共同形成=o或环烷基,或任一者与邻接r8基团可共同形成环烷基。
[0682]
所述非天然氨基酸可呈盐形式,或可并入非天然氨基酸多肽、聚合物、多糖或多核苷酸中并且任选地经翻译后修饰。
[0683]
另外,包括以下具有式(xxxxxiii)结构的氨基酸:
[0684][0685]
其中:
[0686]
a是任选的,并且当存在时是低碳亚烷基、经取代的低碳亚烷基、低碳亚环烷基、经取代的低碳亚环烷基、低碳亚烯基、经取代的低碳亚烯基、亚炔基、低碳亚杂烷基、经取代的亚杂烷基、低碳亚杂环烷基、经取代的低碳亚杂环烷基、亚芳基、经取代的亚芳基、亚杂芳基、经取代的亚杂芳基、亚烷芳基、经取代的亚烷芳基、亚芳烷基或经取代的亚芳烷基;
[0687]
r是h、烷基、经取代的烷基、环烷基或经取代的环烷基;
[0688]
r1是h、氨基保护基、树脂、氨基酸、多肽或多核苷酸;并且
[0689]
r2是oh、酯保护基、树脂、氨基酸、多肽或多核苷酸;
[0690]
n是0、1、2、3、4或5;并且每个cr8r9基团上的r8和r9各自独立地选自由以下组成的群组:h、烷氧基、烷基胺、卤素、烷基、芳基,或任何r8和r9可共同形成=o或环烷基,或任一者与邻接r8基团可共同形成环烷基。
[0691]
所述非天然氨基酸可呈盐形式,或可并入非天然氨基酸多肽、聚合物、多糖或多核苷酸中并且任选地经翻译后修饰。
[0692]
另外,包括以下具有式(xxxxxiv)结构的氨基酸:
[0693][0694]
其中:
[0695]
a是任选的,并且当存在时是低碳亚烷基、经取代的低碳亚烷基、低碳亚环烷基、经取代的低碳亚环烷基、低碳亚烯基、经取代的低碳亚烯基、亚炔基、低碳亚杂烷基、经取代的亚杂烷基、低碳亚杂环烷基、经取代的低碳亚杂环烷基、亚芳基、经取代的亚芳基、亚杂芳基、经取代的亚杂芳基、亚烷芳基、经取代的亚烷芳基、亚芳烷基或经取代的亚芳烷基;
[0696]
r是h、烷基、经取代的烷基、环烷基或经取代的环烷基;
[0697]
r1是h、氨基保护基、树脂、氨基酸、多肽或多核苷酸;并且
[0698]
r2是oh、酯保护基、树脂、氨基酸、多肽或多核苷酸;
[0699]
x1是c、s或s(o);并且l是亚烷基、经取代的亚烷基、n(r')(亚烷基)或n(r')(经取代的亚烷基),其中r'是h、烷基、经取代的烷基、环烷基或经取代的环烷基。
[0700]
所述非天然氨基酸可呈盐形式,或可并入非天然氨基酸多肽、聚合物、多糖或多核苷酸中并且任选地经翻译后修饰。
[0701]
另外,包括以下具有式(xxxxxv)结构的氨基酸:
[0702][0703]
其中:
[0704]
a是任选的,并且当存在时是低碳亚烷基、经取代的低碳亚烷基、低碳亚环烷基、经取代的低碳亚环烷基、低碳亚烯基、经取代的低碳亚烯基、亚炔基、低碳亚杂烷基、经取代的亚杂烷基、低碳亚杂环烷基、经取代的低碳亚杂环烷基、亚芳基、经取代的亚芳基、亚杂芳基、经取代的亚杂芳基、亚烷芳基、经取代的亚烷芳基、亚芳烷基或经取代的亚芳烷基;
[0705]
r是h、烷基、经取代的烷基、环烷基或经取代的环烷基;
[0706]
r1是h、氨基保护基、树脂、氨基酸、多肽或多核苷酸;并且
[0707]
r2是oh、酯保护基、树脂、氨基酸、多肽或多核苷酸;
[0708]
l是亚烷基、经取代的亚烷基、n(r')(亚烷基)或n(r')(经取代的亚烷基),其中r'是h、烷基、经取代的烷基、环烷基或经取代的环烷基。
[0709]
所述非天然氨基酸可呈盐形式,或可并入非天然氨基酸多肽、聚合物、多糖或多核苷酸中并且任选地经翻译后修饰。
[0710]
另外,包括以下具有式(xxxxxvi)结构的氨基酸:
[0711][0712]
其中:
[0713]
a是任选的,并且当存在时是低碳亚烷基、经取代的低碳亚烷基、低碳亚环烷基、经取代的低碳亚环烷基、低碳亚烯基、经取代的低碳亚烯基、亚炔基、低碳亚杂烷基、经取代的亚杂烷基、低碳亚杂环烷基、经取代的低碳亚杂环烷基、亚芳基、经取代的亚芳基、亚杂芳基、经取代的亚杂芳基、亚烷芳基、经取代的亚烷芳基、亚芳烷基或经取代的亚芳烷基;
[0714]
r是h、烷基、经取代的烷基、环烷基或经取代的环烷基;
[0715]
r1是h、氨基保护基、树脂、氨基酸、多肽或多核苷酸;并且
[0716]
r2是oh、酯保护基、树脂、氨基酸、多肽或多核苷酸;
[0717]
l是亚烷基、经取代的亚烷基、n(r')(亚烷基)或n(r')(经取代的亚烷基),其中r'是h、烷基、经取代的烷基、环烷基或经取代的环烷基。
[0718]
所述非天然氨基酸可呈盐形式,或可并入非天然氨基酸多肽、聚合物、多糖或多核苷酸中并且任选地经翻译后修饰。
[0719]
另外,包括具有式(xxxxxvii)结构的氨基酸:
[0720][0721]
其中:
[0722]
a是任选的,并且当存在时是低碳亚烷基、经取代的低碳亚烷基、低碳亚环烷基、经取代的低碳亚环烷基、低碳亚烯基、经取代的低碳亚烯基、亚炔基、低碳亚杂烷基、经取代的亚杂烷基、低碳亚杂环烷基、经取代的低碳亚杂环烷基、亚芳基、经取代的亚芳基、亚杂芳基、经取代的亚杂芳基、亚烷芳基、经取代的亚烷芳基、亚芳烷基或经取代的亚芳烷基;
[0723]
m是
‑
c(r3)
‑
、、其中(a)指示键结到a基团并且(b)指示键结到相应羰基,r3和r4独立地选自h、卤素、烷基、经取代的烷基、环烷基或经取代的环烷基,或r3和r4或两个r3基团或两个r4基团任选地形成环烷基或杂环烷基;
[0724]
r是h、卤素、烷基、经取代的烷基、环烷基或经取代的环烷基;
[0725]
t3是一键、c(r)(r)、o或s,并且r是h、卤素、烷基、经取代的烷基、环烷基或经取代的环烷基;
[0726]
r1是h、氨基保护基、树脂、氨基酸、多肽或多核苷酸;并且
[0727]
r2是oh、酯保护基、树脂、氨基酸、多肽或多核苷酸。
[0728]
所述非天然氨基酸可呈盐形式,或可并入非天然氨基酸多肽、聚合物、多糖或多核苷酸中并且任选地经翻译后修饰。
[0729]
另外,包括具有式(xxxxxviii)结构的氨基酸:
[0730][0731]
其中:
[0732]
m是
‑
c(r3)
‑
、
其中(a)指示键结到a基团并且(b)指示键结到相应羰基,r3和r4独立地选自h、卤素、烷基、经取代的烷基、环烷基或经取代的环烷基,或r3和r4或两个r3基团或两个r4基团任选地形成环烷基或杂环烷基;
[0733]
r是h、卤素、烷基、经取代的烷基、环烷基或经取代的环烷基;
[0734]
t3是一键、c(r)(r)、o或s,并且r是h、卤素、烷基、经取代的烷基、环烷基或经取代的环烷基;
[0735]
r1是h、氨基保护基、树脂、氨基酸、多肽或多核苷酸;并且
[0736]
r2是oh、酯保护基、树脂、氨基酸、多肽或多核苷酸;
[0737]
每个r
a
独立地选自由以下组成的群组:h、卤素、烷基、经取代的烷基、
‑
n(r')2、
‑
c(o)
k
r'(其中k是1、2或3)、
‑
c(o)n(r')2、
‑
or'和
‑
s(o)
k
r',其中每个r'独立地是h、烷基或经取代的烷基。
[0738]
所述非天然氨基酸可呈盐形式,或可并入非天然氨基酸多肽、聚合物、多糖或多核苷酸中并且任选地经翻译后修饰。
[0739]
另外,包括具有式(xxxxxix)结构的氨基酸:
[0740][0741]
其中:
[0742]
r是h、卤素、烷基、经取代的烷基、环烷基或经取代的环烷基;并且
[0743]
t3是o或s。
[0744]
所述非天然氨基酸可呈盐形式,或可并入非天然氨基酸多肽、聚合物、多糖或多核苷酸中并且任选地经翻译后修饰。
[0745]
另外,包括具有式(xxxxxx)结构的氨基酸:
[0746][0747]
其中:
[0748]
r是h、卤素、烷基、经取代的烷基、环烷基或经取代的环烷基。
[0749]
另外,包括以下具有式(xxxxxx)结构的氨基酸:
[0750][0751]
所述非天然氨基酸可呈盐形式,或可并入非天然氨基酸多肽、聚合物、多糖或多核苷酸中并且任选地经翻译后修饰。
[0752]
羰基或二羰基官能团可在温和条件下在水溶液中与含羟胺试剂选择性反应,从而形成在生理条件下稳定的相应肟键。参见,例如詹克斯w.p.(jencks,w.p.),美国化学学会志81,475
‑
481(1959);邵j.(shao,j.)和塔恩j.p.(tarn,j.p.),美国化学学会志117(14):3893
‑
3899(1995)。此外,羰基或二羰基的独特的反应性允许在其它氨基酸侧链存在下的选择性修饰。参见,例如科尼什v.w.(cornish,v.w.)等人,美国化学学会志118:8150
‑
8151(1996);盖根k.f.(geoghegan,k.f.)和斯特罗j.g.(stroh,j.g.),生物共轭化学(bioconjug.chem.)3:138
‑
146(1992);玛哈l.k.(mahal,l.k.)等人,科学276:1125
‑
1128(1997)。
[0753]
对乙酰基
‑
( /
‑
)
‑
苯丙氨酸和间乙酰基
‑
( /
‑
)
‑
苯丙氨酸的合成描述于张z.(zhang,z.)等人,生物化学(biochemistry)42:6735
‑
6746(2003)中,其以引用的方式并入。可类似地制备其它含羰基或二羰基的氨基酸。
[0754]
在一些实施例中,包含非天然氨基酸的多肽以化学方式修饰以产生反应性羰基或二羰基官能团。举例来说,适用于共轭反应的醛官能团可由具有邻接氨基和羟基的官能团产生。当生物活性分子是多肽时,举例来说,n端丝氨酸或苏氨酸(其可以是通常存在的或可通过化学或酶促消化暴露)可用于在适度氧化裂解条件下使用高碘酸盐产生醛官能团。参见,例如盖特纳(gaertner)等人,生物共轭化学3:262
‑
268(1992);盖根k.和斯特罗j.,生物共轭化学3:138
‑
146(1992);盖特纳等人,生物化学杂志269:7224
‑
7230(1994)。然而,所属领域已知的方法限于在肽或蛋白质的n端处的氨基酸。
[0755]
另外,例如携有邻接羟基和氨基的非天然氨基酸可作为“经遮蔽”醛官能团并入多肽中。举例来说,5
‑
羟赖氨酸携有邻近于ε胺的羟基。用于产生醛的反应条件通常涉及在温和条件下加入摩尔过量的偏高碘酸钠,从而避免多肽内其它位点处的氧化。氧化反应的ph值通常是约7.0。典型反应涉及向多肽的缓冲溶液中加入约1.5摩尔过量的偏高碘酸钠,随
后在黑暗中孵育约10分钟。参见,例如美国专利第6,423,685号。
[0756]
b.非天然氨基酸的结构和合成:二羰基、二羰基样基团、经遮蔽二羰基和经保护的二羰基
[0757]
具有亲电子反应性基团的氨基酸允许尤其通过亲核加成反应连接分子的多种反应。所述亲电子反应性基团包括二羰基(包括二酮基团、酮醛基团、酮酸基团、酮酯基团和酮硫酯基团)、二羰基样基团(其具有与二羰基类似的反应性并且在结构上与二羰基类似)、经遮蔽二羰基(其可易于转化为二羰基)、或经保护的二羰基(其在脱除保护基后具有与二羰基类似的反应性)。所述氨基酸包括具有以下式(xxxvii)结构的氨基酸:
[0758][0759]
其中:
[0760]
a是任选的,并且当存在时是低碳亚烷基、经取代的低碳亚烷基、低碳亚环烷基、经取代的低碳亚环烷基、低碳亚烯基、经取代的低碳亚烯基、亚炔基、低碳亚杂烷基、经取代的亚杂烷基、低碳亚杂环烷基、经取代的低碳亚杂环烷基、亚芳基、经取代的亚芳基、亚杂芳基、经取代的亚杂芳基、亚烷芳基、经取代的亚烷芳基、亚芳烷基或经取代的亚芳烷基;
[0761]
b是任选的,并且当存在时是在一端连接于含二胺部分的连接基团,所述连接基团选自由以下组成的群组:低碳亚烷基、经取代的低碳亚烷基、低碳亚烯基、经取代的低碳亚烯基、低碳亚杂烷基、经取代的低碳亚杂烷基、
‑
o
‑
(亚烷基或经取代的亚烷基)
‑
、
‑
s
‑
(亚烷基或经取代的亚烷基)
‑
、
‑
c(o)r"
‑
、
‑
s(o)
k
(亚烷基或经取代的亚烷基)
‑
(其中k是1、2或3)、
‑
c(o)
‑
(亚烷基或经取代的亚烷基)
‑
、
‑
c(s)
‑
(亚烷基或经取代的亚烷基)
‑
、
‑
nr"
‑
(亚烷基或经取代的亚烷基)
‑
、
‑
con(r")
‑
(亚烷基或经取代的亚烷基)
‑
、
‑
csn(r")
‑
(亚烷基或经取代的亚烷基)
‑
和
‑
n(r")co
‑
(亚烷基或经取代的亚烷基)
‑
,其中每个r"独立地是h、烷基或经取代的烷基;
[0762]
k是k是其中,
[0763]
t1是一键、任选经取代的c1‑
c4亚烷基、任选经取代的c1‑
c4亚烯基或任选经取代的杂烷基;
[0764]
其中每个任选的取代基独立地选自低碳亚烷基、经取代的低碳亚烷基、低碳亚环烷基、经取代的低碳亚环烷基、低碳亚烯基、经取代的低碳亚烯基、亚炔基、低碳亚杂烷基、经取代的亚杂烷基、低碳亚杂环烷基、经取代的低碳亚杂环烷基、亚芳基、经取代的亚芳基、亚杂芳基、经取代的亚杂芳基、亚烷芳基、经取代的亚烷芳基、亚芳烷基或经取代的亚芳烷
基;
[0765]
t2是选自由以下组成的群组:低碳亚烷基、经取代的低碳亚烷基、低碳亚烯基、经取代的低碳亚烯基、低碳亚杂烷基、经取代的低碳亚杂烷基、
‑
o
‑
、
‑
o
‑
(亚烷基或经取代的亚烷基)
‑
、
‑
s
‑
、
‑
s
‑
(亚烷基或经取代的亚烷基)
‑
、
‑
s(o)
k
‑
(其中k是1、2或3)、
‑
s(o)
k
(亚烷基或经取代的亚烷基)
‑
、
‑
c(o)
‑
、
‑
c(o)
‑
(亚烷基或经取代的亚烷基)
‑
、
‑
c(s)
‑
、
‑
c(s)
‑
(亚烷基或经取代的亚烷基)
‑
、
‑
n(r')
‑
、
‑
nr'
‑
(亚烷基或经取代的亚烷基)
‑
、
‑
c(o)n(r')
‑
、
‑
con(r')
‑
(亚烷基或经取代的亚烷基)
‑
、
‑
csn(r')
‑
、
‑
csn(r')
‑
(亚烷基或经取代的亚烷基)
‑
、
‑
n(r')co
‑
(亚烷基或经取代的亚烷基)
‑
、
‑
n(r')c(o)o
‑
、
‑
s(o)
k
n(r')
‑
、
‑
n(r')c(o)n(r')
‑
、
‑
n(r')c(s)n(r')
‑
、
‑
n(r')s(o)
k
n(r')
‑
、
‑
n(r')
‑
n=、
‑
c(r')=n
‑
、
‑
c(r')=n
‑
n(r')
‑
、
‑
c(r')=n
‑
n=、
‑
c(r')2‑
n=n
‑
和
‑
c(r')2‑
n(r')
‑
n(r')
‑
,其中每个r'独立地是h、烷基或经取代的烷基;
[0766]
t3是其中每个x1独立地选自由以下组成的群组:
‑
o
‑
、
‑
s
‑
、
‑
n(h)
‑
、
‑
n(r)
‑
、
‑
n(ac)
‑
和
‑
n(ome)
‑
;x2是
‑
or、
‑
oac、
‑
sr、
‑
n(r)2、
‑
n(r)(ac)、
‑
n(r)(ome)或n3,并且其中每个r'独立地是h、烷基或经取代的烷基;
[0767]
r是h、卤素、烷基、经取代的烷基、环烷基或经取代的环烷基;
[0768]
r1是h、氨基保护基、树脂、氨基酸、多肽或多核苷酸;并且
[0769]
r2是oh、酯保护基、树脂、氨基酸、多肽或多核苷酸;
[0770]
或
‑
a
‑
b
‑
k
‑
r基团共同形成双环或三环环烷基或杂环烷基,其包含至少一个羰基(包括二羰基)、经保护的羰基(包括经保护的二羰基)或经遮蔽羰基(包括经遮蔽二羰基);
[0771]
或
‑
k
‑
r基团共同形成单环或双环环烷基或杂环烷基,其包含至少一个羰基(包括二羰基)、经保护的羰基(包括经保护的二羰基)或经遮蔽羰基(包括经遮蔽二羰基)。
[0772]
具有式(xxxvii)结构的二羰基氨基酸的非限制性实例包括:
[0773][0774]
以及也包括具有式(xxxvii)结构的以下氨基酸:
[0775]
[0776][0777]
以及
[0778]
所述非天然氨基酸可呈盐形式,或可并入非天然氨基酸多肽、聚合物、多糖或多核苷酸中并且任选地经翻译后修饰。
[0779]
c.非天然氨基酸的结构和合成:酮炔烃、酮炔烃样、经遮蔽酮炔烃、经保护的酮炔烃基团、炔烃和环炔烃基团
[0780]
含有具有二羰基样反应性的反应性基团的氨基酸允许通过亲核加成反应连接分子。所述亲电子反应性基团包括酮炔烃基团、酮炔烃样基团(其具有与酮炔烃基团类似的反应性并且在结构上与酮炔烃基团类似)、经遮蔽酮炔烃基团(其可易于转化为酮炔烃基团)或经保护的酮炔烃基团(其在脱除保护基后具有与酮炔烃基团类似的反应性)。在一些实施例中,含有具有末端炔烃、内部炔烃或环炔烃的反应性基团的氨基酸允许通过环加成反应(例如1,3
‑
偶极环加成、叠氮化物
‑
炔烃胡伊斯根环加成等)连接分子。所述氨基酸包括具有式(xxxxxxi
‑
a)或(xxxxxxi
‑
b)结构的氨基酸:
[0781][0782]
其中:
[0783]
a是任选的,并且当存在时是低碳亚烷基、经取代的低碳亚烷基、低碳亚环烷基、经取代的低碳亚环烷基、低碳亚烯基、经取代的低碳亚烯基、亚炔基、低碳亚杂烷基、经取代的亚杂烷基、低碳亚杂环烷基、经取代的低碳亚杂环烷基、亚芳基、经取代的亚芳基、亚杂芳基、经取代的亚杂芳基、亚烷芳基、经取代的亚烷芳基、亚芳烷基或经取代的亚芳烷基;
[0784]
b是任选的,并且当存在时是在一端连接于含二胺部分的连接基团,所述连接基团选自由以下组成的群组:低碳亚烷基、经取代的低碳亚烷基、低碳亚烯基、经取代的低碳亚
烯基、低碳亚杂烷基、经取代的低碳亚杂烷基、
‑
o
‑
(亚烷基或经取代的亚烷基)
‑
、
‑
s
‑
(亚烷基或经取代的亚烷基)
‑
、
‑
c(o)r"
‑
、
‑
s(o)
k
(亚烷基或经取代的亚烷基)
‑
(其中k是1、2或3)、
‑
c(o)
‑
(亚烷基或经取代的亚烷基)
‑
、
‑
c(s)
‑
(亚烷基或经取代的亚烷基)
‑
、
‑
nr"
‑
(亚烷基或经取代的亚烷基)
‑
、
‑
con(r")
‑
(亚烷基或经取代的亚烷基)
‑
、
‑
csn(r")
‑
(亚烷基或经取代的亚烷基)
‑
和
‑
n(r")co
‑
(亚烷基或经取代的亚烷基)
‑
,其中每个r"独立地是h、烷基或经取代的烷基;
[0785]
g是任选的,并且当存在时是
[0786]
t4是羰基保护基,包括(但不限于)是羰基保护基,包括(但不限于)其中每个x1独立地选自由以下组成的群组:
‑
o
‑
、
‑
s
‑
、
‑
n(h)
‑
、
‑
n(r)
‑
、
‑
n(ac)
‑
和
‑
n(ome)
‑
;x2是
‑
or、
‑
oac、
‑
sr、
‑
n(r)2、
‑
n(r)(ac)、
‑
n(r)(ome)或n3,并且其中每个r'独立地是h、烷基或经取代的烷基;
[0787]
r是h、卤素、烷基、经取代的烷基、环烷基或经取代的环烷基;
[0788]
r1是h、氨基保护基、树脂、氨基酸、多肽或多核苷酸;
[0789]
r2是oh、酯保护基、树脂、氨基酸、多肽或多核苷酸;
[0790]
r3和r4中的每一个独立地是h、卤素、低碳烷基或经取代的低碳烷基,或r3和r4或两个r3基团任选地形成环烷基或杂环烷基;
[0791]
每个r
19
独立地选自由以下组成的群组:c1‑
c6烷基、c1‑
c6烷氧基、酯、醚、硫醚、氨基烷基、卤素、烷基酯、芳基酯、酰胺、芳基酰胺、烷基卤化物、烷基胺、烷基磺酸、烷基硝基、硫酯、磺酰基酯、卤磺酰基、腈、烷基腈以及硝基;并且
[0792]
q是0、1、2、3、4、5、6、7、8、9、10或11。
[0793]
d.非天然氨基酸的结构和合成:酮胺、酮胺样、经遮蔽酮胺和经保护的酮胺基团
[0794]
含有具有二羰基样反应性的反应性基团的氨基酸允许通过亲核加成反应连接分子。所述反应性基团包括酮胺基团、酮胺样基团(其具有与酮胺基团类似的反应性并且在结构上与酮胺基团类似)、经遮蔽酮胺基团(其可易于转化为酮胺基团)或经保护的酮胺基团(其在脱除保护基后具有与酮胺基团类似的反应性)。所述氨基酸包括具有式(xxxxxxii)结构的氨基酸:
[0795][0796]
其中:
[0797]
a是任选的,并且当存在时是低碳亚烷基、经取代的低碳亚烷基、低碳亚环烷基、经
取代的低碳亚环烷基、低碳亚烯基、经取代的低碳亚烯基、亚炔基、低碳亚杂烷基、经取代的亚杂烷基、低碳亚杂环烷基、经取代的低碳亚杂环烷基、亚芳基、经取代的亚芳基、亚杂芳基、经取代的亚杂芳基、亚烷芳基、经取代的亚烷芳基、亚芳烷基或经取代的亚芳烷基;
[0798]
b是任选的,并且当存在时是在一端连接于含二胺部分的连接基团,所述连接基团选自由以下组成的群组:低碳亚烷基、经取代的低碳亚烷基、低碳亚烯基、经取代的低碳亚烯基、低碳亚杂烷基、经取代的低碳亚杂烷基、
‑
o
‑
(亚烷基或经取代的亚烷基)
‑
、
‑
s
‑
(亚烷基或经取代的亚烷基)
‑
、
‑
c(o)r"
‑
、
‑
s(o)
k
(亚烷基或经取代的亚烷基)
‑
(其中k是1、2或3)、
‑
c(o)
‑
(亚烷基或经取代的亚烷基)
‑
、
‑
c(s)
‑
(亚烷基或经取代的亚烷基)
‑
、
‑
nr"
‑
(亚烷基或经取代的亚烷基)
‑
、
‑
con(r")
‑
(亚烷基或经取代的亚烷基)
‑
、
‑
csn(r")
‑
(亚烷基或经取代的亚烷基)
‑
和
‑
n(r")co
‑
(亚烷基或经取代的亚烷基)
‑
,其中每个r"独立地是h、烷基或经取代的烷基;
[0799]
g是
[0800]
t1是任选经取代的c1‑
c4亚烷基、任选经取代的c1‑
c4亚烯基或任选经取代的杂烷基;
[0801]
t4是羰基保护基,包括(但不限于)是羰基保护基,包括(但不限于)其中每个x1独立地选自由以下组成的群组:
‑
o
‑
、
‑
s
‑
、
‑
n(h)
‑
、
‑
n(r')
‑
、
‑
n(ac)
‑
和
‑
n(ome)
‑
;x2是
‑
or、
‑
oac、
‑
sr'、
‑
n(r')2、
‑
n(r')(ac)、
‑
n(r')(ome)或n3,并且其中每个r'独立地是h、烷基或经取代的烷基;
[0802]
r是h、卤素、烷基、经取代的烷基、环烷基或经取代的环烷基;
[0803]
r1是h、氨基保护基、树脂、氨基酸、多肽或多核苷酸;并且
[0804]
r2是oh、酯保护基、树脂、氨基酸、多肽或多核苷酸;
[0805]
r3和r4中的每一个独立地是h、卤素、低碳烷基或经取代的低碳烷基,或r3和r4或两个r3基团任选地形成环烷基或杂环烷基。
[0806]
具有式(xxxxxxii)结构的氨基酸包括具有式(xxxxxxiii)和式(xxxxxxiv)结构的氨基酸:
[0807][0808]
其中每个r
a
独立地选自由以下组成的群组:h、卤素、烷基、经取代的烷基、
‑
n(r')2、
‑
c(o)
k
r'(其中k是1、2或3)、
‑
c(o)n(r')2、
‑
or'和
‑
s(o)
k
r',其中每个r'独立地是h、
烷基或经取代的烷基。
[0809]
e.非天然氨基酸的结构和合成:二胺、二胺样、经遮蔽二胺、经保护的胺和叠氮化物
[0810]
具有亲核反应性基团的氨基酸允许尤其通过亲电加成反应连接分子的多种反应。所述亲核反应性基团包括二胺基团(包括肼基团、脒基团、亚胺基团、1,1
‑
二胺基团、1,2
‑
二胺基团、1,3
‑
二胺基团和1,4
‑
二胺基团)、二胺样基团(其具有与二胺基团类似的反应性并且在结构上与二胺基团类似)、经遮蔽二胺基团(其可易于转化为二胺基团)、经保护的二胺基团(其在脱除保护基后具有与二胺基团类似的反应性)。在一些实施例中,含有具有叠氮化物的反应性基团的氨基酸允许通过环加成反应(例如1,3
‑
偶极环加成、叠氮化物
‑
炔烃胡伊斯根环加成等)连接分子。
[0811]
另一方面是化学合成用于衍生化羰基取代的海兔毒素衍生物的肼取代的分子的方法。在一个实施例中,肼取代的分子可以是海兔毒素连接的衍生物。一个实施例是制备适于衍生化含有羰基的非天然氨基酸多肽(包括(仅举例来说)含酮或含醛的非天然氨基酸多肽)的肼取代的分子的方法。在一个另外或额外实施例中,非天然氨基酸在蛋白质体内翻译期间位点特异性地并入。在一个另外或额外实施例中,肼取代的海兔毒素衍生物允许通过亲核攻击每个羰基而使含羰基的非天然氨基酸位点特异性衍生化,从而以位点特异性方式形成杂环衍生的多肽,包括含氮杂环衍生的多肽。在一个另外或额外实施例中,制备肼取代的海兔毒素衍生物的方法提供得到多种位点特异性衍生化的多肽的方式。一个另外或额外实施例是合成肼官能化的聚乙二醇(peg)连接的海兔毒素衍生物的方法。
[0812]
所述氨基酸包括具有式(xxxvii
‑
a)或(xxxvii
‑
b)结构的氨基酸:
[0813][0814]
其中:
[0815]
a是任选的,并且当存在时是低碳亚烷基、经取代的低碳亚烷基、低碳亚环烷基、经取代的低碳亚环烷基、低碳亚烯基、经取代的低碳亚烯基、亚炔基、低碳亚杂烷基、经取代的亚杂烷基、低碳亚杂环烷基、经取代的低碳亚杂环烷基、亚芳基、经取代的亚芳基、亚杂芳基、经取代的亚杂芳基、亚烷芳基、经取代的亚烷芳基、亚芳烷基或经取代的亚芳烷基;
[0816]
b是任选的,并且当存在时是在一端连接于含二胺部分的连接基团,所述连接基团选自由以下组成的群组:低碳亚烷基、经取代的低碳亚烷基、低碳亚烯基、经取代的低碳亚烯基、低碳亚杂烷基、经取代的低碳亚杂烷基、
‑
o
‑
(亚烷基或经取代的亚烷基)
‑
、
‑
s
‑
(亚烷基或经取代的亚烷基)
‑
、
‑
c(o)r"
‑
、
‑
c(o)r"
‑
、
‑
s(o)
k
(亚烷基或经取代的亚烷基)
‑
(其中k是1、2或3)、
‑
c(o)
‑
(亚烷基或经取代的亚烷基)
‑
、
‑
c(s)
‑
(亚烷基或经取代的亚烷基)
‑
、
‑
nr"
‑
(亚烷基或经取代的亚烷基)
‑
、
‑
con(r")
‑
(亚烷基或经取代的亚烷基)
‑
、
‑
csn(r")
‑
(亚烷基或经取代的亚烷基)
‑
和
‑
n(r")co
‑
(亚烷基或经取代的亚烷基)
‑
,其中每个r"独立地是h、烷基或经取代的烷基;
[0817]
k是其中:
[0818]
r8和r9独立地选自h、烷基、经取代的烷基、环烷基、经取代的环烷基或胺保护基;
[0819]
t1是一键、任选经取代的c1‑
c4亚烷基、任选经取代的c1‑
c4亚烯基或任选经取代的杂烷基;
[0820]
t2是任选经取代的c1‑
c4亚烷基、任选经取代的c1‑
c4亚烯基、任选经取代的杂烷基、任选经取代的芳基或任选经取代的杂芳基;
[0821]
其中每个任选的取代基独立地选自低碳烷基、经取代的低碳烷基、低碳环烷基、经取代的低碳环烷基、低碳烯基、经取代的低碳烯基、炔基、低碳杂烷基、经取代的杂烷基、低碳杂环烷基、经取代的低碳杂环烷基、芳基、经取代的芳基、杂芳基、经取代的杂芳基、烷芳基、经取代的烷芳基、芳烷基或经取代的芳烷基;
[0822]
r是h、烷基、经取代的烷基、环烷基或经取代的环烷基;
[0823]
r1是h、氨基保护基、树脂、氨基酸、多肽或多核苷酸;并且
[0824]
r2是oh、酯保护基、树脂、氨基酸、多肽或多核苷酸;
[0825]
r3和r4中的每一个独立地是h、卤素、低碳烷基或经取代的低碳烷基,或r3和r4或两个r3基团任选地形成环烷基或杂环烷基;
[0826]
或
‑
a
‑
b
‑
k
‑
r基团共同形成双环或三环环烷基或杂环烷基,其包含至少一个二胺基团、经保护的二胺基团或经遮蔽二胺基团;
[0827]
或
‑
b
‑
k
‑
r基团共同形成双环或三环环烷基或环芳基或杂环烷基,其包含至少一个二胺基团、经保护的二胺基团或经遮蔽二胺基团;
[0828]
或
‑
k
‑
r基团共同形成单环或双环环烷基或杂环烷基,其包含至少一个二胺基团、经保护的二胺基团或经遮蔽二胺基团;
[0829]
其中
‑
a
‑
b
‑
k
‑
r上的至少一个胺基任选地是经保护的胺。
[0830]
一个方面是包含结构1或2的化合物:
[0831][0832]
其中:
[0833]
a是任选的,并且当存在时是低碳亚烷基、经取代的低碳亚烷基、低碳亚环烷基、经取代的低碳亚环烷基、低碳亚烯基、经取代的低碳亚烯基、亚炔基、低碳亚杂烷基、经取代的亚杂烷基、低碳亚杂环烷基、经取代的低碳亚杂环烷基、亚芳基、经取代的亚芳基、亚杂芳基、经取代的亚杂芳基、亚烷芳基、经取代的亚烷芳基、亚芳烷基或经取代的亚芳烷基;
[0834]
b是任选的,并且当存在时是在一端连接于含二胺部分的连接基团,所述连接基团选自由以下组成的群组:低碳亚烷基、经取代的低碳亚烷基、低碳亚烯基、经取代的低碳亚烯基、低碳亚杂烷基、经取代的低碳亚杂烷基、
‑
o
‑
(亚烷基或经取代的亚烷基)
‑
、
‑
s
‑
(亚烷
基或经取代的亚烷基)
‑
、
‑
c(o)r"
‑
、
‑
s(o)
k
(亚烷基或经取代的亚烷基)
‑
(其中k是1、2或3)、
‑
c(o)
‑
(亚烷基或经取代的亚烷基)
‑
、
‑
c(s)
‑
(亚烷基或经取代的亚烷基)
‑
、
‑
nr"
‑
(亚烷基或经取代的亚烷基)
‑
、
‑
con(r")
‑
(亚烷基或经取代的亚烷基)
‑
、
‑
csn(r")
‑
(亚烷基或经取代的亚烷基)
‑
和
‑
n(r")co
‑
(亚烷基或经取代的亚烷基)
‑
,其中每个r"独立地是h、烷基或经取代的烷基;
[0835]
t1是一键或ch2;并且t2是ch;
[0836]
其中每个任选的取代基独立地选自低碳烷基、经取代的低碳烷基、低碳环烷基、经取代的低碳环烷基、低碳烯基、经取代的低碳烯基、炔基、低碳杂烷基、经取代的杂烷基、低碳杂环烷基、经取代的低碳杂环烷基、芳基、经取代的芳基、杂芳基、经取代的杂芳基、烷芳基、经取代的烷芳基、芳烷基或经取代的芳烷基;
[0837]
r1是h、氨基保护基、树脂、氨基酸、多肽或多核苷酸;并且
[0838]
r2是oh、酯保护基、树脂、氨基酸、多肽或多核苷酸;
[0839]
r3和r4中的每一个独立地是h、卤素、低碳烷基或经取代的低碳烷基,或r3和r4或两个r3基团任选地形成环烷基或杂环烷基;
[0840]
或含有
‑
a
‑
b
‑
二胺的部分共同形成双环环烷基或杂环烷基,其包含至少一个二胺基团、经保护的二胺基团或经遮蔽二胺基团;
[0841]
或含有
‑
b
‑
二胺的部分基团共同形成双环或三环环烷基或环芳基或杂环烷基,其包含至少一个二胺基团、经保护的二胺基团或经遮蔽二胺基团;
[0842]
其中含有
‑
a
‑
b
‑
二胺的部分上的至少一个胺基任选地是经保护的胺;
[0843]
或其活性代谢物、盐或医药学上可接受的前药或溶剂化物。
[0844]
包括具有式(xxxvii)结构的氨基酸的以下非限制性实例:
[0845][0845][0846]
以及
[0847]
所述非天然氨基酸还可呈盐形式或可并入非天然氨基酸多肽、聚合物、多糖或多核苷酸和/或任选地经翻译后修饰。
[0848]
在某些实施例中,式(xxxvii)化合物在水溶液中在适度酸性条件下稳定至少1个月。在某些实施例中,式(xxxvii)化合物在适度酸性条件下稳定至少2周。在某些实施例中,式(xxxvii)化合物在适度酸性条件下稳定至少5天。在某些实施例中,所述酸性条件是ph值为约2到约8。
[0849]
在式(xxxvii)化合物的某些实施例中,b是低碳亚烷基、经取代的低碳亚烷基、o
‑
(亚烷基或经取代的亚烷基)
‑
、c(r')=nn(r')
‑
、
‑
n(r')co
‑
、c(o)
‑
、
‑
c(r')=n
‑
、c(o)
‑
(亚烷基或经取代的亚烷基)
‑
、con(r')(亚烷基或经取代的亚烷基)
‑
、
‑
s(亚烷基或经取代的亚烷基)
‑
、
‑
s(o)(亚烷基或经取代的亚烷基)
‑
或
‑
s(o)2(亚烷基或经取代的亚烷基)
‑
。在式(xxxvii)化合物的某些实施例中,b是
‑
o(ch2)
‑
、
‑
ch=n
‑
、ch=nnh
‑
、
‑
nhch2‑
、
‑
nhco
‑
、c(o)
‑
、c(o)(ch2)
‑
、conh(ch2)
‑
、
‑
sch2‑
、
‑
s(=o)ch2‑
或
‑
s(o)2ch2‑
。在式(xxxvii)化合物的某些实施例中,r是c1‑6烷基或环烷基。在式(xxxvii)化合物的某些实施例中,r是
‑
ch3、
‑
ch(ch3)2或环丙基。在式(xxxvii)化合物的某些实施例中,r1是h、叔丁氧羰基(boc)、9
‑
芴基甲氧基羰基(fmoc)、n
‑
乙酰基、四氟乙酰基(tfa)或苯甲氧羰基(cbz)。在式(xxxvii)化合物的某些实施例中,r1是树脂、氨基酸、多肽或多核苷酸。在式(xxxvii)化合物的某些实施例中,r1是抗体、抗体片段或单克隆抗体。在式(xxxvii)化合物的某些实施例中,r2是oh、o
‑
甲基、o
‑
乙基或o
‑
叔丁基。在式(xxxvii)化合物的某些实施例中,r2是树脂、至少一个氨基酸、多肽或多核苷酸。在式(xxxvii)化合物的某些实施例中,r2是抗体、抗体片段或单克隆抗体。
[0850]
还包括具有式(xxxvii)结构的氨基酸的以下非限制性实例:
[0851]
[0852]
以及
[0853]
具有式(xxxvii)结构的经保护的氨基酸的非限制性实例包括:
[0854]
以及
[0855][0856]
f.非天然氨基酸的结构和合成:芳香族胺
[0857]
具有亲核反应性基团(如(仅举例来说)芳香族胺基团(包括仲胺和叔胺基团)、经遮蔽芳香族胺基团(其可易于转化为芳香族胺基团)或经保护的芳香族胺基团(其在脱除保护基后具有与芳香族胺基团类似的反应性))的非天然氨基酸允许通过多种反应(包括(但不限于)与含醛的海兔毒素连接基团衍生物的还原性烷基化反应)连接分子的多种反应。所述含有芳香族胺的非天然氨基酸包括具有式(xxxxxxv)结构的氨基酸:
[0858][0859]
其中:
[0860]
是选自由以下组成的群组:单环芳基环、双环芳基环、多环芳基环、单环杂芳基环、双环杂芳基环和多环杂芳基环;
[0861]
a独立地是cr
a
或n;
[0862]
b独立地是cr
a
、n、o或s;
[0863]
每个r
a
独立地选自由以下组成的群组:h、卤素、烷基、
‑
no2、
‑
cn、经取代的烷基、
‑
n(r')2、
‑
c(o)
k
r'、
‑
c(o)n(r')2、
‑
or'和
‑
s(o)
k
r',其中k是1、2或3;并且n是0、1、2、3、4、5或6;
[0864]
r1是h、氨基保护基、树脂、至少一个氨基酸、多肽或多核苷酸;并且
[0865]
r2是oh、酯保护基、树脂、至少一个氨基酸、多肽或多核苷酸;
[0866]
r3和r4中的每一个独立地是h、卤素、低碳烷基或经取代的低碳烷基,或r3和r4或两
个r3基团任选地形成环烷基或杂环烷基;
[0867]
m是h或
‑
ch2r5;或m
‑
n
‑
c(r5)部分可形成4到7元环结构;
[0868]
r5是烷基、经取代的烷基、烯基、经取代的烯基、炔基、经取代的炔基、烷氧基、经取代的烷氧基、烷基烷氧基、经取代的烷基烷氧基、聚环氧烷、经取代的聚环氧烷、环烷基、经取代的环烷基、芳基、经取代的芳基、杂芳基、经取代的杂芳基、杂环、经取代的杂环、烷芳基、经取代的烷芳基、芳烷基、经取代的芳烷基、
‑
c(o)r"、
‑
c(o)or"、
‑
c(o)n(r")2、
‑
c(o)nhch(r")2、
‑
(亚烷基或经取代的亚烷基)
‑
n(r")2、
‑
(亚烯基或经取代的亚烯基)
‑
n(r")2、
‑
(亚烷基或经取代的亚烷基)
‑
(芳基或经取代的芳基)、
‑
(亚烯基或经取代的亚烯基)
‑
(芳基或经取代的芳基)、
‑
(亚烷基或经取代的亚烷基)
‑
on(r")2、
‑
(亚烷基或经取代的亚烷基)
‑
c(o)sr"、
‑
(亚烷基或经取代的亚烷基)
‑
s
‑
s
‑
(芳基或经取代的芳基),其中每个r"独立地是氢、烷基、经取代的烷基、烯基、经取代的烯基、烷氧基、经取代的烷氧基、芳基、经取代的芳基、杂芳基、经取代的杂芳基、杂环、经取代的杂环、烷芳基、经取代的烷芳基、芳烷基、经取代的芳烷基或
‑
c(o)or';
[0869]
或两个r5基团任选地形成环烷基或杂环烷基;
[0870]
或r5和任一r
a
任选地形成环烷基或杂环烷基;并且
[0871]
每个r'独立地是h、烷基或经取代的烷基。
[0872]
所述非天然氨基酸还可呈盐形式,或可并入非天然氨基酸多肽、聚合物、多糖或多核苷酸中并且任选地经还原性烷基化。
[0873]
结构(如在本文中所有实例中所呈现)不呈现“a”、“b”、“nh
‑
m”和“r
a”的相对定向;更确切地说此结构的这四个特征可以任何化学合理的方式(连同此结构的其它特征一起)定向,如由本文中实例所示出。
[0874]
含有具有式(a)结构的芳香族胺部分的非天然氨基酸包括具有以下结构的非天然氨基酸:
[0875]
以及其中,每个a'独立地选自cr
a
、n或并且最多两个a'可以是并且其余a'选自cr
a
或n。
[0876]
所述非天然氨基酸还可呈盐形式,或可并入非天然氨基酸多肽、聚合物、多糖或多
核苷酸中并且任选地经还原性烷基化。
[0877]
具有式(xxxxxxv)结构的含有芳香族胺部分的非天然氨基酸的非限制性实例包括具有式(xxxxxxvi)和式(xxxxxxvii)结构的非天然氨基酸,
[0878]
其中:g是胺保护基,包括(但不限于)
[0879][0880]
所述非天然氨基酸可呈盐形式,或可并入非天然氨基酸多肽、聚合物、多糖或多核苷酸中并且任选地经还原性烷基化。
[0881]
含有芳香族胺部分的非天然氨基酸具有以下结构:
[0882]
以及
[0883][0884]
其中每个r
a
独立地选自由以下组成的群组:h、卤素、烷基、
‑
no2、
‑
cn、经取代的烷基、
‑
n(r')2、
‑
c(o)
k
r'、
‑
c(o)n(r')2、
‑
or'和
‑
s(o)
k
r',其中k是1、2或3;
[0885]
m是h或
‑
ch2r5;或m
‑
n
‑
c(r5)部分可形成4到7元环结构;
[0886]
r1是h、氨基保护基、树脂、氨基酸、多肽或多核苷酸;
[0887]
r2是oh、酯保护基、树脂、氨基酸、多肽或多核苷酸;
[0888]
r5是烷基、经取代的烷基、烯基、经取代的烯基、炔基、经取代的炔基、烷氧基、经取代的烷氧基、烷基烷氧基、经取代的烷基烷氧基、聚环氧烷、经取代的聚环氧烷、环烷基、经取代的环烷基、芳基、经取代的芳基、杂芳基、经取代的杂芳基、杂环、经取代的杂环、烷芳基、经取代的烷芳基、芳烷基、经取代的芳烷基、
‑
c(o)r"、
‑
c(o)or"、
‑
c(o)n(r")2、
‑
c(o)nhch(r")2、
‑
(亚烷基或经取代的亚烷基)
‑
n(r")2、
‑
(亚烯基或经取代的亚烯基)
‑
n(r")2、
‑
(亚烷基或经取代的亚烷基)
‑
(芳基或经取代的芳基)、
‑
(亚烯基或经取代的亚烯基)
‑
(芳基或经取代的芳基)、
‑
(亚烷基或经取代的亚烷基)
‑
on(r")2、
‑
(亚烷基或经取代的亚烷基)
‑
c(o)sr"、
‑
(亚烷基或经取代的亚烷基)
‑
s
‑
s
‑
(芳基或经取代的芳基),其中每个r"独立地是氢、烷基、经取代的烷基、烯基、经取代的烯基、烷氧基、经取代的烷氧基、芳基、经取代的芳基、杂芳基、经取代的杂芳基、杂环、经取代的杂环、烷芳基、经取代的烷芳基、芳烷基、经取代的芳烷基或
‑
c(o)or';
[0889]
或r5和任一r
a
任选地形成环烷基或杂环烷基;并且
[0890]
每个r'独立地是h、烷基或经取代的烷基。所述非天然氨基酸还可呈盐形式,或可并入非天然氨基酸多肽、聚合物、多糖或多核苷酸中。
[0891]
所述式(xxxxxxv)非天然氨基酸可通过还原非天然氨基酸的芳香族部分上的经保护的或经遮蔽胺部分而形成。所述经保护的或经遮蔽胺部分包括(但不限于)亚胺、肼、硝基或叠氮化物取代基。用于还原所述经保护的或经遮蔽胺部分的还原剂包括(但不限于)tcep、na2s、na2s2o4、lialh4、nabh4或nabcnh3。
[0892]
v.非天然氨基酸连接的海兔毒素衍生物
[0893]
本文所述的另一方面是用于将至少一个所述海兔毒素连接基团衍生物并入非天然氨基酸中的方法、策略和技术。此方面还包括产生、纯化、表征和使用所述含有至少一个所述非天然氨基酸的海兔毒素连接基团衍生物的方法。此方面还包括产生、纯化、表征和使用寡核苷酸(包括dna和rna)的组合物和方法,所述寡核苷酸可用于至少部分产生含有至少一个非天然氨基酸的海兔毒素连接基团衍生物。此方面还包括产生、纯化、表征和使用细胞的组合物和方法,所述细胞可表达可用于至少部分产生含有至少一个非天然氨基酸的海兔毒素连接基团衍生物的所述寡核苷酸。
[0894]
因此,本文提供并描述包含至少一个具有羰基、二羰基、炔烃、环炔烃、叠氮化物、肟或羟胺基团的非天然氨基酸或经修饰的非天然氨基酸的海兔毒素连接基团衍生物。在某些实施例中,具有至少一个具有羰基、二羰基、炔烃、环炔烃、叠氮化物、肟或羟胺基团的非天然氨基酸或经修饰的非天然氨基酸的海兔毒素连接基团衍生物包括至少一个在多肽某个位置处的翻译后修饰。在一些实施例中,共翻译或翻译后修饰是通过细胞机器发生(例如糖基化、乙酰化、酰化、脂质修饰、棕榈酰化、棕榈酸盐加成、磷酸化、糖脂连接修饰等),在许多情况下,所述基于细胞机器的共翻译或翻译后修饰是在多肽上天然存在的氨基酸位点处发生,然而,在某些实施例中,基于细胞机器的共翻译或翻译后修饰是在多肽上的非天然氨基酸位点处发生。
[0895]
在其它实施例中,翻译后修饰不利用细胞机器,而是代之以利用本文所述的化学方法或适于特定反应性基团的其它方法通过将包含第二反应性基团的分子(聚合物、水溶性聚合物、聚乙二醇衍生物、第二蛋白质或多肽或多肽类似物、抗体或抗体片段、和其任何组合)与至少一个包含第一反应性基团的非天然氨基酸(包括(但不限于)含有酮、醛、缩醛、半缩醛、炔烃、环炔烃、叠氮化物、肟或羟胺官能团的非天然氨基酸)连接来提供官能团。在某些实施例中,共翻译或翻译后修饰是于真核细胞或非真核细胞中在体内进行。在某些实施例中,翻译后修饰不利用细胞机器在体外进行。此方面还包括产生、纯化、表征和使用所述含有至少一个所述经共翻译或翻译后修饰的非天然氨基酸的海兔毒素连接基团衍生物的方法。
[0896]
本文所述的方法、组合物、策略和技术的范围内还包括能够与作为多肽的一部分的海兔毒素连接基团衍生物(含有羰基或二羰基、肟基、炔烃、环炔烃、叠氮化物、羟胺基团或其经遮蔽或经保护的形式)反应从而产生上述翻译后修饰中的任一种的试剂。在某些实施例中,所得翻译后修饰的海兔毒素连接基团衍生物将含有至少一个肟基;所得经修饰的含肟海兔毒素连接基团衍生物可经历后续修饰反应。此方面还包括产生、纯化、表征和使用所述能够对所述海兔毒素连接基团衍生物进行任何所述翻译后修饰的试剂的方法。
[0897]
在某些实施例中,多肽或非天然氨基酸连接的海兔毒素衍生物包括至少一个在体内通过一个宿主细胞进行的共翻译或翻译后修饰,其中所述翻译后修饰通常不是由另一宿主细胞类型进行。在某些实施例中,多肽包括至少一个通过真核细胞在体内进行的共翻译或翻译后修饰,其中所述共翻译或翻译后修饰通常不是由非真核细胞进行。所述共翻译或翻译后修饰的实例包括(但不限于)糖基化、乙酰化、酰化、脂质修饰、棕榈酰化、棕榈酸盐加成、磷酸化、糖脂连接修饰等。在一个实施例中,共翻译或翻译后修饰包含通过glcnac
‑
天冬酰胺键将寡糖与天冬酰胺连接在一起(包括(但不限于)寡糖包含(glcnac
‑
man)2‑
man
‑
glcnac
‑
glcnac等的情形)。在另一实施例中,共翻译或翻译后修饰包含通过galnac
‑
丝氨酸、galnac
‑
苏氨酸、glcnac
‑
丝氨酸或glcnac
‑
苏氨酸键将寡糖(包括(但不限于)gal
‑
galnac、gal
‑
glcnac等)与丝氨酸或苏氨酸连接在一起。在某些实施例中,蛋白质或多肽可包含分泌或定位序列、抗原决定基标签、flag标签、聚组氨酸标签、gst融合体等。此方面还包括产生、纯化、表征和使用所述含有至少一个所述共翻译或翻译后修饰的多肽的方法。在其它实施例中,糖基化非天然氨基酸多肽是以非糖基化的形式产生。所述糖基化非天然氨基酸的非糖基化形式可通过包括以下的方法产生:从经过分离的或实质上经纯化或未经纯化的糖基化非天然氨基酸多肽中以化学或酶促方式去除寡糖基团;在不使所述非天然氨基酸多肽糖基化的宿主中产生非天然氨基酸(所述宿主包括经工程化或经突变而不使所述多肽糖基化的原核生物或真核生物);将糖基化抑制剂引入细胞培养基中,其中所述非天然氨基酸多肽是通过通常会使所述多肽糖基化的真核生物产生;或任何所述方法的组合。本文还描述所述通常糖基化的非天然氨基酸多肽(通常糖基化意思是指当在使天然存在的多肽糖基化的条件下产生时将糖基化的多肽)的非糖基化形式。当然,所述通常糖基化的非天然氨基酸多肽的非糖基化形式(或实际上本文中所述的任何多肽)可以呈未经纯化的形式、实质上经纯化的形式或经过分离的形式。
[0898]
在某些实施例中,非天然氨基酸多肽包括至少一个在加速剂存在下进行的翻译后修饰,其中所述翻译后修饰是化学计量、类化学计量或近化学计量的。在其它实施例中,多肽与式(xix)试剂在加速剂存在下接触。在其它实施例中,加速剂是选自由以下组成的群组:
[0899][0899]
以及
[0900]
a.非天然氨基酸连接的海兔毒素衍生物的化学合成:含肟连接的海兔毒素衍生物
[0901]
含有肟基的非天然氨基酸海兔毒素连接的衍生物允许与含有某些反应性羰基或二羰基(包括(但不限于)酮、醛或具有相似反应性的其它基团)的多种试剂反应以形成包含
新的肟基的新的非天然氨基酸。所述肟置换反应允许海兔毒素连接的衍生物的进一步官能化。另外,原始的含有肟基的海兔毒素连接的衍生物就其自身来说可适用,只要肟键在将氨基酸并入多肽(例如本文所述的体内、体外和化学合成方法)所必需的条件下是稳定的即可。
[0902]
因此,本文所述的某些实施例是具有侧链的非天然氨基酸海兔毒素连接的衍生物,所述侧链包含肟基、肟样基团(其具有与肟基类似的反应性并且在结构上与肟基类似)、经遮蔽肟基(其可易于转化为肟基)或经保护的肟基(其在脱除保护基后具有与肟基类似的反应性)。
[0903]
所述非天然氨基酸海兔毒素连接的衍生物包括具有式(viii)或(ix)结构的海兔毒素连接的衍生物:
[0904][0905]
其中:
[0906]
a是任选的,并且当存在时是低碳亚烷基、经取代的低碳亚烷基、低碳亚环烷基、经取代的低碳亚环烷基、低碳亚烯基、经取代的低碳亚烯基、亚炔基、低碳亚杂烷基、经取代的亚杂烷基、低碳亚杂环烷基、经取代的低碳亚杂环烷基、亚芳基、经取代的亚芳基、亚杂芳基、经取代的亚杂芳基、亚烷芳基、经取代的亚烷芳基、亚芳烷基或经取代的亚芳烷基;
[0907]
b是任选的,并且当存在时是选自由以下组成的群组的连接基团:低碳亚烷基、经取代的低碳亚烷基、低碳亚烯基、经取代的低碳亚烯基、低碳亚杂烷基、经取代的低碳亚杂烷基、
‑
o
‑
、
‑
o
‑
(亚烷基或经取代的亚烷基)
‑
、
‑
s
‑
、
‑
s
‑
(亚烷基或经取代的亚烷基)
‑
、
‑
s(o)
k
‑
(其中k是1、2或3)、
‑
s(o)
k
(亚烷基或经取代的亚烷基)
‑
、
‑
c(o)
‑
、
‑
c(o)
‑
(亚烷基或经取代的亚烷基)
‑
、
‑
c(s)
‑
、
‑
c(s)
‑
(亚烷基或经取代的亚烷基)
‑
、
‑
n(r')
‑
、
‑
nr'
‑
(亚烷基或经取代的亚烷基)
‑
、
‑
c(o)n(r')
‑
、
‑
con(r')
‑
(亚烷基或经取代的亚烷基)
‑
、
‑
csn(r')
‑
、
‑
csn(r')
‑
(亚烷基或经取代的亚烷基)
‑
、
‑
n(r')co
‑
(亚烷基或经取代的亚烷基)
‑
、
‑
n(r')c(o)o
‑
、
‑
s(o)
k
n(r')
‑
、
‑
n(r')c(o)n(r')
‑
、
‑
n(r')c(s)n(r')
‑
、
‑
n(r')s(o)
k
n(r')
‑
、
‑
n(r')
‑
n=、
‑
c(r')=n
‑
、
‑
c(r')=n
‑
n(r')
‑
、
‑
c(r')=n
‑
n=、
‑
c(r')2‑
n=n
‑
和
‑
c(r')2‑
n(r')
‑
n(r')
‑
,其中每个r'独立地是h、烷基或经取代的烷基;
[0908]
r是h、烷基、经取代的烷基、环烷基或经取代的环烷基;
[0909]
r1是h、氨基保护基、树脂、至少一个氨基酸、多肽或多核苷酸;
[0910]
r2是oh、酯保护基、树脂、至少一个氨基酸、多肽或多核苷酸;
[0911]
r3和r4各自独立地是h、卤素、低碳烷基或经取代的低碳烷基,或r3和r4或两个r3基团任选地形成环烷基或杂环烷基;
[0912]
z具有以下结构:
[0913][0914]
r5是h、cor8、c1‑
c6烷基或噻唑;
[0915]
r8是oh
[0916]
r6是oh或h;
[0917]
ar是苯基或吡啶;
[0918]
r7是c1‑
c6烷基或氢;
[0919]
l是选自由以下组成的群组的连接基团:
‑
亚烷基
‑
、
‑
亚烷基
‑
c(o)
‑
、
‑
(亚烷基
‑
o)
n
‑
亚烷基
‑
、
‑
(亚烷基
‑
o)
n
‑
亚烷基
‑
c(o)
‑
、
‑
(亚烷基
‑
o)
n
‑
(ch2)
n'
‑
nhc(o)
‑
(ch2)
n”‑
c(me)2‑
s
‑
s
‑
(ch2)
n”'
‑
nhc(o)
‑
(亚烷基
‑
o)
n
””
‑
亚烷基
‑
、
‑
(亚烷基
‑
o)
n
‑
亚烷基
‑
w
‑
、
‑
亚烷基
‑
c(o)
‑
w
‑
、
‑
(亚烷基
‑
o)
n
‑
亚烷基
‑
u
‑
亚烷基
‑
c(o)
‑
以及
‑
(亚烷基
‑
o)
n
‑
亚烷基
‑
u
‑
亚烷基
‑
;
[0920]
w具有以下结构:
[0921][0922]
u具有以下结构:
[0923]
并且
[0924]
n、n'、n"、n'"和n""各自独立地是大于或等于1的整数;
[0925]
或其活性代谢物或医药学上可接受的前药或溶剂化物。
[0926]
在式(viii)和(ix)化合物的某些实施例中,r5是噻唑。在式(viii)和(ix)化合物的某些实施例中,r6是h。在式(viii)和(ix)化合物的某些实施例中,ar是苯基。在式(viii)和(ix)化合物的某些实施例中,r7是甲基。在式(viii)和(ix)化合物的某些实施例中,n是0
到20的整数。在式(viii)和(ix)化合物的某些实施例中,n是0到10的整数。在式(viii)和(ix)化合物的某些实施例中,n是0到5的整数。
[0927]
在式(viii)和(ix)化合物的某些实施例中,r5是噻唑。在式(viii)和(ix)化合物的某些实施例中,r5是氢。在式(viii)和(ix)化合物的某些实施例中,r5是甲基、乙基、丙基、异丙基、丁基、异丁基、仲丁基、叔丁基、戊基或己基。在式(viii)和(ix)化合物的某些实施例中,r5是
‑
nh
‑
(亚烷基
‑
o)
n
‑
nh2,其中亚烷基是
‑
ch2‑
、
‑
ch2ch2‑
、
‑
ch2ch2ch2‑
、
‑
ch2ch2ch2ch2‑
、
‑
ch2ch2ch2ch2ch2‑
、
‑
ch2ch2ch2ch2ch2ch2‑
、
‑
ch2ch2ch2ch2ch2ch2ch2‑
、
‑
ch2ch2ch2ch2ch2ch2ch2ch2‑
、
‑
ch2ch2ch2ch2ch2ch2ch2ch2ch2‑
、
‑
ch2ch2ch2ch2ch2ch2ch2ch2ch2ch2‑
、
‑
ch2ch2ch2ch2ch2ch2ch2ch2ch2ch2ch2‑
或
‑
ch2ch2ch2ch2ch2ch2ch2ch2ch2ch2ch2ch2‑
。在式(viii)和(ix)的某些实施例中,亚烷基是亚甲基、亚乙基、亚丙基、亚丁基、亚戊基、亚己基或亚庚基。
[0928]
在式(viii)和(ix)化合物的某些实施例中,r5是
‑
nh
‑
(亚烷基
‑
o)
n
‑
nh2,其中n是0、1、2、3、4、5、6、7、8、9、10、11、12、13、14、15、16、17、18、19、20、21、22、23、24、25、26、27、28、29、30、31、32、33、34、35、36、37、38、39、40、41、42、43、44、45、46、47、48、49、50、51、52、53、54、55、56、57、58、59、60、61、62、63、64、65、66、67、68、69、70、71、72、73、74、75、76、77、78、79、80、81、82、83、84、85、86、87、88、89、90、91、92、93、94、95、96、97、98、99或100。
[0929]
在式(viii)和(ix)化合物的某些实施例中,r6是h。
[0930]
在式(viii)和(ix)化合物的某些实施例中,ar是苯基。
[0931]
在式(viii)和(ix)化合物的某些实施例中,r7是甲基、乙基、丙基、异丙基、丁基、仲丁基异丁基、叔丁基、戊基或己基。在式(viii)和(ix)化合物的某些实施例中,r7是氢。
[0932]
在式(viii)和(ix)化合物的某些实施例中,每个l独立地是可裂解连接基团或不可裂解连接基团。在式(viii)和(ix)化合物的某些实施例中,每个l独立地是寡聚(乙二醇)衍生化连接基团。
[0933]
在式(viii)和(ix)化合物的某些实施例中,亚烷基、亚烷基'、亚烷基"和亚烷基'"各自独立地是
‑
ch2‑
、
‑
ch2ch2‑
、
‑
ch2ch2ch2‑
、
‑
ch2ch2ch2ch2‑
、
‑
ch2ch2ch2ch2ch2‑
、
‑
ch2ch2ch2ch2ch2ch2‑
、
‑
ch2ch2ch2ch2ch2ch2ch2‑
、
‑
ch2ch2ch2ch2ch2ch2ch2ch2‑
、
‑
ch2ch2ch2ch2ch2ch2ch2ch2ch2‑
、
‑
ch2ch2ch2ch2ch2ch2ch2ch2ch2ch2‑
、
‑
ch2ch2ch2ch2ch2ch2ch2ch2ch2ch2ch2‑
或
‑
ch2ch2ch2ch2ch2ch2ch2ch2ch2ch2ch2ch2‑
。在式(viii)和(ix)化合物的某些实施例中,亚烷基是亚甲基、亚乙基、亚丙基、亚丁基、亚戊基、亚己基或亚庚基。
[0934]
在式(viii)和(ix)化合物的某些实施例中,n、n'、n"、n'"和n""各自独立地是0、1、2、3、4、5、6、7、8、9、10、11、12、13、14、15、16、17、18、19、20、21、22、23、24、25、26、27、28、29、30、31、32、33、34、35、36、37、38、39、40、41、42、43、44、45、46、47、48、49、50、51、52、53、54、55、56、57、58、59、60、61、62、63、64、65、66、67、68、69、70、71、72、73、74、75、76、77、78、79、80、81、82、83、84、85、86、87、88、89、90、91、92、93、94、95、96、97、98、99或100。
[0935]
在式(viii)或(ix)化合物的某些实施例中,r1是多肽。在式(viii)或(ix)化合物的某些实施例中,r2是多肽。在式(viii)或(ix)化合物的某些实施例中,所述多肽是抗体。在式(viii)或(ix)化合物的某些实施例中,所述抗体是赫赛汀。
[0936]
所述非天然氨基酸尾海兔素连接衍生物包括具有式(x)、(xi)、(xii)或(xiii)结构的尾海兔素连接衍生物:
[0937][0938][0939]
其中:
[0940]
a是任选的,并且当存在时是低碳亚烷基、经取代的低碳亚烷基、低碳亚环烷基、经取代的低碳亚环烷基、低碳亚烯基、经取代的低碳亚烯基、亚炔基、低碳亚杂烷基、经取代的亚杂烷基、低碳亚杂环烷基、经取代的低碳亚杂环烷基、亚芳基、经取代的亚芳基、亚杂芳基、经取代的亚杂芳基、亚烷芳基、经取代的亚烷芳基、亚芳烷基或经取代的亚芳烷基;
[0941]
b是任选的,并且当存在时是选自由以下组成的群组的连接基团:低碳亚烷基、经取代的低碳亚烷基、低碳亚烯基、经取代的低碳亚烯基、低碳亚杂烷基、经取代的低碳亚杂烷基、
‑
o
‑
、
‑
o
‑
(亚烷基或经取代的亚烷基)
‑
、
‑
s
‑
、
‑
s
‑
(亚烷基或经取代的亚烷基)
‑
、
‑
s(o)
k
‑
(其中k是1、2或3)、
‑
s(o)
k
(亚烷基或经取代的亚烷基)
‑
、
‑
c(o)
‑
、
‑
c(o)
‑
(亚烷基或经取代的亚烷基)
‑
、
‑
c(s)
‑
、
‑
c(s)
‑
(亚烷基或经取代的亚烷基)
‑
、
‑
n(r')
‑
、
‑
nr'
‑
(亚烷基或经取代的亚烷基)
‑
、
‑
c(o)n(r')
‑
、
‑
con(r')
‑
(亚烷基或经取代的亚烷基)
‑
、
‑
csn(r')
‑
、
‑
csn(r')
‑
(亚烷基或经取代的亚烷基)
‑
、
‑
n(r')co
‑
(亚烷基或经取代的亚烷基)
‑
、
‑
n(r')c(o)o
‑
、
‑
s(o)
k
n(r')
‑
、
‑
n(r')c(o)n(r')
‑
、
‑
n(r')c(s)n(r')
‑
、
‑
n(r')s(o)
k
n(r')
‑
、
‑
n(r')
‑
n=、
‑
c(r')=n
‑
、
‑
c(r')=n
‑
n(r')
‑
、
‑
c(r')=n
‑
n=、
‑
c(r')2‑
n=n
‑
以及
‑
c(r')2‑
n(r')
‑
n(r')
‑
,其中每个r'独立地是h、烷基或经取代的烷基;
[0942]
r是h、烷基、经取代的烷基、环烷基或经取代的环烷基;
[0943]
r1是h、氨基保护基、树脂、至少一个氨基酸、多肽或多核苷酸;
[0944]
r2是oh、酯保护基、树脂、至少一个氨基酸、多肽或多核苷酸;
[0945]
r3和r4各自独立地是h、卤素、低碳烷基或经取代的低碳烷基,或r3和r4或两个r3基团任选地形成环烷基或杂环烷基;
[0946]
z具有以下结构:
[0947][0948]
r5是h、co2h、c1‑
c6烷基或噻唑;
[0949]
r6是oh或h;
[0950]
ar是苯基或吡啶;
[0951]
r7是c1‑
c6烷基或氢;
[0952]
l1、l2、l3和l4各自是独立地选自由以下组成的群组的连接基团:一键、
‑
亚烷基
‑
、
‑
(亚烷基
‑
o)
n
‑
亚烷基
‑
j
‑
、
‑
亚烷基'
‑
j
‑
(亚烷基
‑
o)
n
‑
亚烷基
‑
、
‑
j
‑
(亚烷基
‑
o)
n
‑
亚烷基
‑
、
‑
(亚烷基
‑
o)
n
‑
亚烷基
‑
j
‑
(亚烷基
‑
o)
n
'
‑
亚烷基
‑
j'
‑
、
‑
(亚烷基
‑
o)
n
‑
亚烷基
‑
j
‑
亚烷基'
‑
、
‑
w
‑
、
‑
亚烷基
‑
w
‑
、亚烷基'
‑
j
‑
(亚烷基
‑
nme)
n
‑
亚烷基
‑
w
‑
、
‑
j
‑
(亚烷基
‑
nme)
n
‑
亚烷基
‑
w
‑
、
‑
j
‑
亚烷基
‑
nme
‑
亚烷基'
‑
nme
‑
亚烷基"
‑
w
‑
以及
‑
亚烷基
‑
j
‑
亚烷基'
‑
nme
‑
亚烷基"
‑
nme
‑
亚烷基'"
‑
w
‑
;
[0953]
w具有以下结构:
[0954][0955]
j和j'各自独立地具有以下结构:
[0956]
并且
[0957]
n和n'各自独立地是大于或等于1的整数。
[0958]
在式(x)、(xi)、(xii)或(xiii)化合物的某些实施例中,r5是噻唑或羧酸。在式(x)、(xi)、(xii)或(xiii)化合物的某些实施例中,r6是h。在式(x)、(xi)、(xii)或(xiii)化合物的某些实施例中,ar是苯基。在式(x)、(xi)、(xii)或(xiii)化合物的某些实施例中,r7是甲基。在式(x)、(xi)、(xii)或(xiii)化合物的某些实施例中,n和n'是0到20的整数。在式(x)、(xi)、(xii)或(xiii)化合物的某些实施例中,n和n'是0到10的整数。在式(x)、(xi)、(xii)或(xiii)化合物的某些实施例中,在式(x)、(xi)、(xii)或(xiii)化合物的某些实施例中,n和n'是0到5的整数。
[0959]
在式(x)、(xi)、(xii)或(xiii)化合物的某些实施例中,r5是噻唑。在式(x)、(xi)、(xii)或(xiii)化合物的某些实施例中,r5是氢。在式(x)、(xi)、(xii)或(xiii)化合物的某些实施例中,r5是甲基、乙基、丙基、异丙基、丁基、异丁基、仲丁基、叔丁基、戊基或己基。在式(x)、(xi)、(xii)或(xiii)化合物的某些实施例中,r5是
‑
nh
‑
(亚烷基
‑
o)
n
‑
nh2,其中亚烷基是
‑
ch2‑
、
‑
ch2ch2‑
、
‑
ch2ch2ch2‑
、
‑
ch2ch2ch2ch2‑
、
‑
ch2ch2ch2ch2ch2‑
、
‑
ch2ch2ch2ch2ch2ch2‑
、
‑
ch2ch2ch2ch2ch2ch2ch2‑
、
‑
ch2ch2ch2ch2ch2ch2ch2ch2‑
、
‑
ch2ch2ch2ch2ch2ch2ch2ch2ch2‑
、
‑
ch2ch2ch2ch2ch2ch2ch2ch2ch2ch2‑
、
‑
ch2ch2ch2ch2ch2ch2ch2ch2ch2ch2ch2‑
或
‑
ch2ch2ch2ch2ch2ch2ch2ch2ch2ch2ch2ch2‑
。在式(x)、(xi)、(xii)或(xiii)的某些实施例中,亚烷基是亚甲基、亚乙基、亚丙基、亚丁基、亚戊基、亚己基或亚庚基。
[0960]
在式(x)、(xi)、(xii)或(xiii)化合物的某些实施例中,r5是
‑
nh
‑
(亚烷基
‑
o)
n
‑
nh2,其中n是0、1、2、3、4、5、6、7、8、9、10、11、12、13、14、15、16、17、18、19、20、21、22、23、24、25、26、27、28、29、30、31、32、33、34、35、36、37、38、39、40、41、42、43、44、45、46、47、48、49、50、51、52、53、54、55、56、57、58、59、60、61、62、63、64、65、66、67、68、69、70、71、72、73、74、75、76、77、78、79、80、81、82、83、84、85、86、87、88、89、90、91、92、93、94、95、96、97、98、99或100。
[0961]
在式(x)、(xi)、(xii)或(xiii)化合物的某些实施例中,r6是h。在式(x)、(xi)、(xii)或(xiii)化合物的某些实施例中,r6是羟基。
[0962]
在式(x)、(xi)、(xii)或(xiii)化合物的某些实施例中,ar是苯基。
[0963]
在式(x)、(xi)、(xii)或(xiii)化合物的某些实施例中,r7是甲基、乙基、丙基、异丙基、丁基、仲丁基异丁基、叔丁基、戊基或己基。在式(x)、(xi)、(xii)或(xiii)化合物的某
些实施例中,r7是氢。
[0964]
在式(x)、(xi)、(xii)或(xiii)化合物的某些实施例中,l1、l2、l3和l4各自独立地是可裂解连接基团或不可裂解连接基团。在式(x)、(xi)、(xii)或(xiii)化合物的某些实施例中,l1、l2、l3和l4各自独立地是寡聚(乙二醇)衍生化连接基团。
[0965]
在式(x)、(xi)、(xii)或(xiii)化合物的某些实施例中,亚烷基、亚烷基'、亚烷基"和亚烷基'"各自独立地是
‑
ch2‑
、
‑
ch2ch2‑
、
‑
ch2ch2ch2‑
、
‑
ch2ch2ch2ch2‑
、
‑
ch2ch2ch2ch2ch2‑
、
‑
ch2ch2ch2ch2ch2ch2‑
、
‑
ch2ch2ch2ch2ch2ch2ch2‑
、
‑
ch2ch2ch2ch2ch2ch2ch2ch2‑
、
‑
ch2ch2ch2ch2ch2ch2ch2ch2ch2‑
、
‑
ch2ch2ch2ch2ch2ch2ch2ch2ch2ch2‑
、
‑
ch2ch2ch2ch2ch2ch2ch2ch2ch2ch2ch2‑
或
‑
ch2ch2ch2ch2ch2ch2ch2ch2ch2ch2ch2ch2‑
。在式(x)、(xi)、(xii)或(xiii)化合物的某些实施例中,亚烷基是亚甲基、亚乙基、亚丙基、亚丁基、亚戊基、亚己基或亚庚基。
[0966]
在式(x)、(xi)、(xii)或(xiii)化合物的某些实施例中,n和n'各自独立地是0、1、2、3、4、5、6、7、8、9、10、11、12、13、14、15、16、17、18、19、20、21、22、23、24、25、26、27、28、29、30、31、32、33、34、35、36、37、38、39、40、41、42、43、44、45、46、47、48、49、50、51、52、53、54、55、56、57、58、59、60、61、62、63、64、65、66、67、68、69、70、71、72、73、74、75、76、77、78、79、80、81、82、83、84、85、86、87、88、89、90、91、92、93、94、95、96、97、98、99或100。
[0967]
在式(x)、(xi)、(xii)或(xiii)化合物的某些实施例中,r1是多肽。在式(x)、(xi)、(xii)或(xiii)化合物的某些实施例中,r2是多肽。在式(x)、(xi)、(xii)或(xiii)化合物的某些实施例中,所述多肽是抗体。在式(x)、(xi)、(xii)或(xiii)化合物的某些实施例中,所述抗体是赫赛汀。
[0968]
在某些实施例中,式(x)、(xi)、(xii)或(xiii)化合物在水溶液中在适度酸性条件下稳定至少1个月。在某些实施例中,式(x)、(xi)、(xii)或(xiii)化合物在适度酸性条件下稳定至少2周。在某些实施例中,式(x)、(xi)、(xii)或(xiii)化合物在适度酸性条件下稳定至少5天。在某些实施例中,所述酸性条件是ph 2到8。所述非天然氨基酸可呈盐形式,或可并入非天然氨基酸多肽、聚合物、多糖或多核苷酸中并且任选地经翻译后修饰。
[0969]
基于肟的非天然氨基酸可通过所属领域中已描述的方法或通过本文中所述的方法合成,包括:(a)含羟胺的非天然氨基酸与含羰基或含二羰基的试剂反应;(b)含羰基或含二羰基的非天然氨基酸与含羟胺的试剂反应;或(c)含肟的非天然氨基酸与某些含羰基或含二羰基的试剂反应。
[0970]
b.非天然氨基酸连接的海兔毒素衍生物的化学结构和合成:烷基化芳香族胺连接的海兔毒素衍生物
[0971]
一个方面是基于芳香族胺基的反应性使非天然氨基酸化学衍生化的海兔毒素连接基团衍生物。在另外或额外实施例中,将至少一个上述非天然氨基酸并入海兔毒素连接基团衍生物中,即,所述实施例是非天然氨基酸连接的海兔毒素衍生物。在另外或额外实施例中,在海兔毒素连接基团衍生物的侧链上使其官能化,以致其与衍生化非天然氨基酸反应产生胺键。在另外或额外实施例中,海兔毒素连接基团衍生物是选自具有芳香族胺侧链的海兔毒素连接基团衍生物。在另外或额外实施例中,海兔毒素连接基团衍生物包含经遮蔽侧链(包括经遮蔽芳香族胺基团)。在另外或额外实施例中,非天然氨基酸是选自具有芳香族胺侧链的氨基酸。在另外或额外实施例中,非天然氨基酸包含经遮蔽侧链(包括经遮蔽
芳香族胺基团)。
[0972]
另一方面是基于胺键产生衍生化的非天然氨基酸多肽的羰基取代的海兔毒素连接基团衍生物,如醛和酮。另一实施例是醛取代的海兔毒素连接基团衍生物,其用于通过在衍生化海兔毒素连接基团与含芳香族胺的非天然氨基酸多肽之间形成胺键来使含芳香族胺的非天然氨基酸多肽衍生化。
[0973]
在另外或额外实施例中,非天然氨基酸包含芳香族胺侧链,其中芳香族胺是选自芳基胺或杂芳基胺。在另外或额外实施例中,非天然氨基酸在结构方面相似于天然氨基酸,但含有芳香族胺基团。在额外或另外实施例中,非天然氨基酸相似于苯丙氨酸或酪氨酸(芳香族氨基酸)。在一个实施例中,非天然氨基酸具有与天然氨基酸的性质不同的性质。在一个实施例中;所述不同性质是侧链的化学反应性;在另一实施例中;此不同的化学反应性允许非天然氨基酸的侧链在作为多肽的单元的同时经历反应,即使同一多肽中的天然存在的氨基酸单元的侧链不经历上述反应。在另一实施例中,非天然氨基酸的侧链具有与天然存在的氨基酸的侧链正交的化学性质。在另一实施例中,非天然氨基酸的侧链包含含亲核试剂部分;在另一实施例中,非天然氨基酸的侧链上的含亲核试剂部分可经历反应以产生胺连接的衍生的海兔毒素。在另一实施例中,非天然氨基酸的侧链包含含亲电子试剂部分;在另一实施例中,非天然氨基酸的侧链上的含亲电子试剂部分可经历亲核攻击以产生胺连接的衍生的海兔毒素。在此段落的任一上述实施例中,非天然氨基酸可作为单独分子存在或者可被并入任何长度的多肽中;如果是后者,那么多肽可另外并有天然存在的或非天然的氨基酸。
[0974]
使用还原性烷基化或还原性胺化反应修饰本文中所述的非天然氨基酸具有任一种或全部以下优势。第一,可在约4到约10的ph范围内(并且在某些实施例中,在约4到约7的ph范围内)用含羰基化合物(包括醛和酮)使芳香族胺还原烷基化以产生经取代的胺(包括仲胺和叔胺)键。第二,在这些反应条件下,由于天然存在的氨基酸的侧链无反应性,故化学物质对非天然氨基酸具选择性。这使得能够使已并入含有芳香族胺部分或经保护的醛部分的非天然氨基酸的多肽(包括例如重组蛋白质)得到位点特异性衍生化。所述衍生化多肽和蛋白质可由此作为定义的均质产物制备。第三,实现已并入多肽中的氨基酸上的芳香族胺部分与含醛试剂的反应所需的温和条件通常不会不可逆地破坏多肽的三级结构(当然,除反应目的是破坏所述三级结构的情形外)。类似地,实现已并入多肽中并且经去保护的氨基酸上的醛部分与含芳香族胺试剂的反应所需的温和条件通常不会不可逆地破坏多肽的三级结构(当然,除反应目的是破坏所述三级结构的情形外)。第四,反应在室温下迅速发生,这允许使用否则在较高温度下将不稳定的许多类型的多肽或试剂。第五,反应易于在水性条件下发生,这也允许使用与非水溶液不相容(在任何程度上)的多肽和试剂。第六,即使当多肽或氨基酸与试剂的比率是化学计量、类化学计量或近化学计量时,反应也易于发生,从而不需要加入过量的试剂或多肽来获得有用量的反应产物。第七,可视反应物中胺和羰基部分的设计而区域选择性和/或区域特异性地产生所得胺。最后,用含醛试剂使芳香族胺还原性烷基化以及用含芳香族胺试剂使醛还原性胺化会产生在生物条件下稳定的胺(包括仲胺和叔胺)键。
[0975]
具有亲核反应性基团(如(仅举例来说)芳香族胺基团(包括仲胺和叔胺基团)、经遮蔽芳香族胺基团(其可易于转化为芳香族胺基团)或经保护的芳香族胺基团(其在脱除保
护基后具有与芳香族胺基团类似的反应性))的非天然氨基酸允许通过多种反应(包括(但不限于)与含醛的海兔毒素连接的衍生物的还原性烷基化反应)连接分子的多种反应。所述烷基化非天然氨基酸连接的海兔毒素衍生物包括具有式(xxv)、(xxvi)、(xxvii)、(xxviii)、(xxix)或(xxx)结构的氨基酸:
[0976]
[0977][0978]
其中:
[0979]
z具有以下结构:
[0980][0981]
r5是h、co2h、c1‑
c6烷基或噻唑;
[0982]
r6是oh或h;
[0983]
ar是苯基或吡啶;
[0984]
r1是h、氨基保护基、树脂、至少一个氨基酸、多肽或多核苷酸;
[0985]
r2是oh、酯保护基、树脂、至少一个氨基酸、多肽或多核苷酸;
[0986]
r4是h、卤素、低碳烷基或经取代的低碳烷基;
[0987]
r7是c1‑
c6烷基或氢;
[0988]
l、l1、l2、l3和l4各自是选自由以下组成的群组的连接基团:一键、
‑
亚烷基
‑
、
‑
亚烷基
‑
c(o)
‑
、
‑
(亚烷基
‑
o)
n
‑
亚烷基
‑
、
‑
(亚烷基
‑
o)
n
‑
亚烷基
‑
c(o)
‑
、
‑
(亚烷基
‑
o)
n
‑
(ch2)
n'
‑
nhc(o)
‑
(ch2)
n”‑
c(me)2‑
s
‑
s
‑
(ch2)
n”'
‑
nhc(o)
‑
(亚烷基
‑
o)
n
””
‑
亚烷基
‑
、
‑
(亚烷基
‑
o)
n
‑
亚烷
基
‑
w
‑
、
‑
亚烷基
‑
c(o)
‑
w
‑
、
‑
(亚烷基
‑
o)
n
‑
亚烷基
‑
j
‑
、
‑
亚烷基'
‑
j
‑
(亚烷基
‑
o)
n
‑
亚烷基
‑
、
‑
(亚烷基
‑
o)
n
‑
亚烷基
‑
j
‑
亚烷基'、
‑
j
‑
(亚烷基
‑
o)
n
‑
亚烷基
‑
、
‑
(亚烷基
‑
o)
n
‑
亚烷基
‑
j
‑
(亚烷基
‑
o)
n
'
‑
亚烷基
‑
j'
‑
、
‑
w
‑
、
‑
亚烷基
‑
w
‑
、亚烷基'
‑
j
‑
(亚烷基
‑
nme)
n
‑
亚烷基
‑
w
‑
和j
‑
(亚烷基
‑
nme)
n
‑
亚烷基
‑
w
‑
、
‑
(亚烷基
‑
o)
n
‑
亚烷基
‑
u
‑
亚烷基
‑
c(o)
‑
、
‑
(亚烷基
‑
o)
n
‑
亚烷基
‑
u
‑
亚烷基
‑
、
‑
j
‑
亚烷基
‑
nme
‑
亚烷基'
‑
nme
‑
亚烷基"
‑
w
‑
以及
‑
亚烷基
‑
j
‑
亚烷基'
‑
nme
‑
亚烷基"
‑
nme
‑
亚烷基'"
‑
w
‑
;
[0989]
w具有以下结构:
[0990][0991]
u具有以下结构:
[0992][0993]
j和j'各自独立地具有以下结构:
[0994][0995]
n和n'各自独立地是大于或等于1的整数;并且
[0996]
每个r
16
独立地选自由以下组成的群组:氢、卤素、烷基、no2、cn以及经取代的烷基。
[0997]
所述烷基化非天然氨基酸连接的海兔毒素衍生物也可以呈盐形式,或可并入非天然氨基酸多肽、聚合物、多糖或多核苷酸中并且任选地经还原烷基化。
[0998]
在式(xxv)、(xxvi)、(xxvii)、(xxviii)、(xxix)或(xxx)化合物的某些实施例中,r5是噻唑或羧酸。在式(xxv)、(xxvi)、(xxvii)、(xxviii)、(xxix)或(xxx)化合物的某些实施例中,r6是h。在式(xxv)、(xxvi)、(xxvii)、(xxviii)、(xxix)或(xxx)化合物的某些实施例中,ar是苯基。在式(xxv)、(xxvi)、(xxvii)、(xxviii)、(xxix)或(xxx)化合物的某些实施例中,r7是甲基。在式(xxv)、(xxvi)、(xxvii)、(xxviii)、(xxix)或(xxx)化合物的某些实施例中,n是0到20的整数。在式(xxv)、(xxvi)、(xxvii)、(xxviii)、(xxix)或(xxx)化合物的某些实施例中,n是0到10的整数。在式(xxv)、(xxvi)、(xxvii)、(xxviii)、(xxix)或(xxx)或(xxiv)化合物的某些实施例中,n是0到5的整数。
[0999]
在式(xxv)、(xxvi)、(xxvii)、(xxviii)、(xxix)或(xxx)化合物的某些实施例中,r5是噻唑或羧酸。在式(xxv)、(xxvi)、(xxvii)、(xxviii)、(xxix)或(xxx)化合物的某些实施例中,r5是氢。在式(xxv)、(xxvi)、(xxvii)、(xxviii)、(xxix)或(xxx)化合物的某些实施例中,r5是甲基、乙基、丙基、异丙基、丁基、异丁基、仲丁基、叔丁基、戊基或己基。在式
(xxv)、(xxvi)、(xxvii)、(xxviii)、(xxix)或(xxx)化合物的某些实施例中,r5是
‑
nh
‑
(亚烷基
‑
o)
n
‑
nh2,其中亚烷基是
‑
ch2‑
、
‑
ch2ch2‑
、
‑
ch2ch2ch2‑
、
‑
ch2ch2ch2ch2‑
、
‑
ch2ch2ch2ch2ch2‑
、
‑
ch2ch2ch2ch2ch2ch2‑
、
‑
ch2ch2ch2ch2ch2ch2ch2‑
、
‑
ch2ch2ch2ch2ch2ch2ch2ch2‑
、
‑
ch2ch2ch2ch2ch2ch2ch2ch2ch2‑
、
‑
ch2ch2ch2ch2ch2ch2ch2ch2ch2ch2‑
、
‑
ch2ch2ch2ch2ch2ch2ch2ch2ch2ch2ch2‑
或
‑
ch2ch2ch2ch2ch2ch2ch2ch2ch2ch2ch2ch2‑
。在式(xxv)、(xxvi)、(xxvii)、(xxviii)、(xxix)或(xxx)化合物的某些实施例中,亚烷基是亚甲基、亚乙基、亚丙基、亚丁基、亚戊基、亚己基或亚庚基。
[1000]
在式(xxv)、(xxvi)、(xxvii)、(xxviii)、(xxix)或(xxx)化合物的某些实施例中,r5是
‑
nh
‑
(亚烷基
‑
o)
n
‑
nh2,其中n是0、1、2、3、4、5、6、7、8、9、10、11、12、13、14、15、16、17、18、19、20、21、22、23、24、25、26、27、28、29、30、31、32、33、34、35、36、37、38、39、40、41、42、43、44、45、46、47、48、49、50、51、52、53、54、55、56、57、58、59、60、61、62、63、64、65、66、67、68、69、70、71、72、73、74、75、76、77、78、79、80、81、82、83、84、85、86、87、88、89、90、91、92、93、94、95、96、97、98、99或100。
[1001]
在式(xxv)、(xxvi)、(xxvii)、(xxviii)、(xxix)或(xxx)化合物的某些实施例中,r6是h。在式(xxv)、(xxvi)、(xxvii)、(xxviii)、(xxix)或(xxx)化合物的一些实施例中,r6是羟基。
[1002]
在式(xxv)、(xxvi)、(xxvii)、(xxviii)、(xxix)或(xxx)化合物的某些实施例中,ar是苯基。
[1003]
在式(xxv)、(xxvi)、(xxvii)、(xxviii)、(xxix)或(xxx)化合物的某些实施例中,r7是甲基、乙基、丙基、异丙基、丁基、仲丁基异丁基、叔丁基、戊基或己基。在式(xxv)、(xxvi)、(xxvii)、(xxviii)、(xxix)或(xxx)化合物的某些实施例中,r7是氢。
[1004]
在式(xxv)、(xxvi)、(xxvii)、(xxviii)、(xxix)或(xxx)化合物的某些实施例中,l、l1、l2、l3和l4各自独立地是可裂解连接基团或不可裂解连接基团。在式(xxv)、(xxvi)、(xxvii)、(xxviii)、(xxix)或(xxx)化合物的某些实施例中,l、l1、l2、l3和l4各自独立地是寡聚(乙二醇)衍生化连接基团。
[1005]
在式(xxv)、(xxvi)、(xxvii)、(xxviii)、(xxix)或(xxx)化合物的某些实施例中,亚烷基、亚烷基'、亚烷基"和亚烷基'"各自独立地是
‑
ch2‑
、
‑
ch2ch2‑
、
‑
ch2ch2ch2‑
、
‑
ch2ch2ch2ch2‑
、
‑
ch2ch2ch2ch2ch2‑
、
‑
ch2ch2ch2ch2ch2ch2‑
、
‑
ch2ch2ch2ch2ch2ch2ch2‑
、
‑
ch2ch2ch2ch2ch2ch2ch2ch2‑
、
‑
ch2ch2ch2ch2ch2ch2ch2ch2ch2‑
、
‑
ch2ch2ch2ch2ch2ch2ch2ch2ch2ch2‑
、
‑
ch2ch2ch2ch2ch2ch2ch2ch2ch2ch2ch2‑
或
‑
ch2ch2ch2ch2ch2ch2ch2ch2ch2ch2ch2ch2‑
。在式(xix)、(xx)、(xxi)、(xxii)、(xxiii)或(xxiv)化合物的某些实施例中,亚烷基是亚甲基、亚乙基、亚丙基、亚丁基、亚戊基、亚己基或亚庚基。
[1006]
在式(xxv)、(xxvi)、(xxvii)、(xxviii)、(xxix)或(xxx)化合物的某些实施例中,n、n'、n"、n'"和n""各自独立地是0、1、2、3、4、5、6、7、8、9、10、11、12、13、14、15、16、17、18、19、20、21、22、23、24、25、26、27、28、29、30、31、32、33、34、35、36、37、38、39、40、41、42、43、44、45、46、47、48、49、50、51、52、53、54、55、56、57、58、59、60、61、62、63、64、65、66、67、68、69、70、71、72、73、74、75、76、77、78、79、80、81、82、83、84、85、86、87、88、89、90、91、92、93、94、95、96、97、98、99或100。
[1007]
在式(xxv)、(xxvi)、(xxvii)、(xxviii)、(xxix)或(xxx)化合物的某些实施例中,
r1是多肽。在式(xxv)、(xxvi)、(xxvii)、(xxviii)、(xxix)或(xxx)化合物的某些实施例中,r2是多肽。在式(xxv)、(xxvi)、(xxvii)、(xxviii)、(xxix)或(xxx)化合物的某些实施例中,所述多肽是抗体。在式(xxv)、(xxvi)、(xxvii)、(xxviii)、(xxix)或(xxx)化合物的某些实施例中,所述抗体是赫赛汀。
[1008]
式(xxv)、(xxvi)、(xxvii)、(xxviii)、(xxix)或(xxx)化合物可以通过芳香族胺化合物与含有羰基的试剂(如酮、酯、硫酯和醛)的还原性烷基化作用而形成。
[1009]
在一些实施例中,首先还原多肽中所含的非天然氨基酸的经遮蔽胺部分,得到并入非天然氨基酸多肽中的含有芳香族胺部分的非天然氨基酸。所述芳香族胺部分接着经上述含有羰基的试剂还原性烷基化,得到含有式(xxv)、(xxvi)、(xxvii)、(xxviii)、(xxix)或(xxx)非天然氨基酸的多肽。所述反应还可以应用于将非天然氨基酸并入合成聚合物、多糖或多核苷酸中。另外,所述反应可应用于未经并入的非天然氨基酸。举例来说,用于还原经遮蔽胺部分的还原剂包括(但不限于)tcep、na2s、na2s2o4、lialh4、b2h6和nabh4。仅举例来说,还原性烷基化可在ph值为约4到约7的水性缓冲液中并且使用温和还原剂(如(仅举例来说)氰基硼氢化钠(nabcnh3))发生。另外,其它还原剂可用于还原性烷基化,包括(但不限于)tcep、na2s、na2s2o4、lialh4、b2h6和nabh4。
[1010]
通过非天然氨基酸中所含的芳香族仲胺部分与上述含羰基试剂的还原性烷基化进行的含有式(xxv)、(xxvi)、(xxvii)、(xxviii)、(xxix)或(xxx)氨基酸的非天然氨基酸多肽的一个非限制性例示性合成。所述还原性烷基化得到含有具有芳香族叔胺部分的非天然氨基酸的多肽。所述反应还可以应用于将非天然氨基酸并入合成聚合物、多糖或多核苷酸中。另外,所述反应可应用于未经并入的非天然氨基酸。仅举例来说,还原性烷基化可在ph值为约4到约7的水性缓冲液中并且使用温和还原剂(如(仅举例来说)氰基硼氢化钠(nabcnh3))发生。另外,其它还原剂可用于还原性烷基化,包括(但不限于)tcep、na2s、na2s2o4、lialh4、b2h6和nabh4。
[1011]
c.非天然氨基酸连接的海兔毒素衍生物的化学合成:含杂芳基的连接的海兔毒素衍生物
[1012]
一个方面是基于二羰基(包括含有至少一个酮基、和/或至少一个醛基、和/或至少一个酯基、和/或至少一个羧酸和/或至少一个硫酯基的基团,并且其中所述二羰基可以是1,2
‑
二羰基、1,3
‑
二羰基或1,4
‑
二羰基)的反应性使海兔毒素连接的衍生物化学衍生化的非天然氨基酸。另外或额外方面是基于二胺基团(包括肼基团、脒基团、亚胺基团、1,1
‑
二胺基团、1,2
‑
二胺基团、1,3
‑
二胺基团和1,4
‑
二胺基团)的反应性使海兔毒素连接的衍生物化学衍生化的非天然氨基酸。在另外或额外实施例中,将至少一个上述非天然氨基酸并入海兔毒素连接的衍生物中,即,所述实施例是非天然氨基酸连接的海兔毒素衍生物。在另外或额外实施例中,非天然氨基酸的侧链经官能化使得其与衍生化分子发生反应产生一键,包括基于杂环(包括含氮杂环)的键,和/或基于醇醛的键。另外或额外实施例是非天然氨基酸多肽,其可与衍生化海兔毒素连接基团反应以产生含有以下的非天然氨基酸连接的海兔毒素衍生物:一键,包括基于杂环(包括含氮杂环)的键,和/或基于醇醛的键。在另外或额外实施例中,非天然氨基酸是选自具有二羰基和/或二胺侧链的氨基酸。在另外或额外实施例中,非天然氨基酸包含经遮蔽侧链,包括经遮蔽二胺基团和/或经遮蔽二羰基。在另外或额外实施例中,非天然氨基酸包含选自以下的基团:酮
‑
胺(即,含有酮和胺两者的基团);酮
‑
炔烃(即,含有酮和炔烃两者的基团);和烯
‑
二酮(即,含有二羰基和烯烃的基团)。
[1013]
在另外或额外实施例中,非天然氨基酸包含二羰基侧链,其中羰基是选自酮、醛、羧酸或酯,包括硫酯。另一实施例是非天然氨基酸,其含有在用适当官能化试剂处理时能够形成杂环(包括含氮杂环)的官能团。在另外或额外实施例中,非天然氨基酸在结构方面相似于天然氨基酸,但含有上述官能团中的一种。在额外或另外实施例中,非天然氨基酸相似于苯丙氨酸或酪氨酸(芳香族氨基酸);而在一个各别实施例中,非天然氨基酸相似于丙氨酸和亮氨酸(疏水性氨基酸)。在一个实施例中,非天然氨基酸具有与天然氨基酸的性质不同的性质。在一个实施例中,所述不同性质是侧链的化学反应性,在另一实施例中,此不同的化学反应性允许非天然氨基酸的侧链在作为多肽的单元的同时经历反应,即使同一多肽中的天然存在的氨基酸单元的侧链不经历上述反应。在另一实施例中,非天然氨基酸的侧链具有与天然存在的氨基酸的侧链正交的化学性质。在另一实施例中,非天然氨基酸的侧链包含含亲电子试剂部分;在另一实施例中,非天然氨基酸的侧链上的含亲电子试剂部分可经历亲核攻击以产生杂环衍生的蛋白质,包括含氮杂环衍生的蛋白质。在此段落的任一上述实施例中,非天然氨基酸可作为单独分子存在或者可被并入任何长度的多肽中;如果是后者,那么多肽可另外并有天然存在的或非天然的氨基酸。
[1014]
另一方面是基于杂环(包括含氮杂环)键产生衍生化非天然氨基酸连接的海兔毒素衍生物的二胺取代的分子,其中二胺基团是选自肼、脒、亚胺、1,1
‑
二胺、1,2
‑
二胺、1,3
‑
二胺和1,4
‑
二胺基团。另一实施例是二胺取代的海兔毒素衍生物,其用于通过在衍生化分子和含二羰基的非天然氨基酸多肽之间形成杂环(包括含氮杂环)键来衍生化含二羰基的非天然氨基酸多肽。在其它实施例中,上述含二羰基的非天然氨基酸多肽是含二酮的非天然氨基酸多肽。在另外或额外实施例中,含二羰基的非天然氨基酸包含侧链,其中羰基是选自酮、醛、羧酸或酯,包括硫酯。在另外或额外实施例中,二胺取代的分子包含选自所需官能团的基团。在另一实施例中,非天然氨基酸的侧链具有与天然存在的氨基酸的侧链正交的化学性质,其允许非天然氨基酸与二胺取代的分子选择性反应。在另一实施例中,非天然氨基酸的侧链包含与含二胺的分子选择性反应的含亲电子试剂的部分;在另一实施例中,非天然氨基酸的侧链上的含亲电子试剂的部分可经历亲核攻击以产生杂环衍生的蛋白质,包括含氮杂环衍生的蛋白质。与此段落中描述的实施例有关的另一方面是经修饰的非天然氨基酸多肽,其由衍生化分子与非天然氨基酸多肽的反应产生。其它实施例包括已经修饰的非天然氨基酸多肽的任何其它修饰。
[1015]
另一方面是基于杂环(包括含氮杂环)键产生衍生化非天然氨基酸多肽的二羰基取代的分子。另一实施例是二羰基取代的分子,其用于通过形成杂环(包括含氮杂环基团)来使含二胺的非天然氨基酸多肽衍生化。另一实施例是二羰基取代的分子,其可与含二胺的非天然氨基酸多肽在介于约4与约8之间的ph值范围内形成所述杂环(包括含氮杂环基团)。另一实施例是二羰基取代的分子,其用于通过在衍生化分子与含二胺的非天然氨基酸多肽之间形成杂环(包括含氮杂环)键来使含二胺的非天然氨基酸多肽衍生化。在另一实施例中,二羰基取代的分子是二酮取代的分子、在其它方面中是酮醛取代的分子、在其它方面中是酮酸取代的分子、在其它方面中是酮酯取代的分子(包括酮硫酯取代的分子)。在其它实施例中,二羰基取代的分子包含选自所需官能团的基团。在另外或额外实施例中,醛取代的分子是醛取代的聚乙二醇(peg)分子。在另一实施例中,非天然氨基酸的侧链具有与天然
存在的氨基酸的侧链正交的化学性质,其允许非天然氨基酸与羰基取代的分子选择性反应。在另一实施例中,非天然氨基酸的侧链包含与含二羰基的分子选择性反应的部分(例如二胺基团);在另一实施例中,非天然氨基酸的侧链上的亲核部分可经历亲电子攻击以产生杂环衍生的蛋白质,包括含氮杂环衍生的蛋白质。与此段落中描述的实施例有关的另一方面是经修饰非天然氨基酸多肽,其由衍生化分子与非天然氨基酸多肽的反应产生。其它实施例包括已经修饰的非天然氨基酸多肽的任何其它修饰。
[1016]
一个方面是通过羰基与肼反应物的反应以产生杂环衍生的蛋白质(包括含氮杂环衍生的海兔毒素)使蛋白质衍生化的方法。此方面内包括基于含羰基与含肼的反应物的缩合以产生杂环衍生的海兔毒素(包括含氮杂环衍生的海兔毒素)使海兔毒素连接基团衍生物衍生化的方法。额外或另外实施例是用肼官能化的非天然氨基酸使含酮海兔毒素衍生物或含醛海兔毒素衍生物衍生化的方法。在额外或另外方面中,肼取代的分子可包括蛋白质、其它聚合物和小分子。
[1017]
另一方面是化学合成用于衍生化羰基取代的海兔毒素衍生物的肼取代的分子的方法。在一个实施例中,肼取代的分子是海兔毒素连接的衍生物,其适于衍生化含有羰基的非天然氨基酸多肽(包括(仅举例来说)含酮或含醛的非天然氨基酸多肽)。
[1018]
一个方面是基于喹喔啉或吩嗪键使海兔毒素类似物化学衍生化的非天然氨基酸。在另外或额外实施例中,非天然氨基酸的侧链经官能化使得其与衍生化海兔毒素连接基团发生反应产生喹喔啉或吩嗪键。在另外或额外实施例中,非天然氨基酸是选自具有1,2
‑
二羰基或1,2
‑
芳基二胺侧链的氨基酸。在另外或额外实施例中,非天然氨基酸是选自具有经保护的或经遮蔽1,2
‑
二羰基或1,2
‑
芳基二胺侧链的氨基酸。进一步包括1,2
‑
二羰基侧链的等效物、或1,2
‑
二羰基侧链的经保护的或经遮蔽等效物。
[1019]
另一方面是基于喹喔啉或吩嗪键产生衍生化非天然氨基酸多肽的衍生化分子。一个实施例是1,2
‑
二羰基取代的海兔毒素连接基团衍生物,其用于使含1,2
‑
芳基二胺的非天然氨基酸多肽衍生化以形成喹喔啉或吩嗪键。另一实施例是1,2
‑
芳基二胺取代的海兔毒素连接基团衍生物,其用于使含1,2
‑
二羰基的非天然氨基酸多肽衍生化以形成喹喔啉或吩嗪键。与上文实施例有关的另一方面是经修饰非天然氨基酸多肽,其由衍生化海兔毒素连接基团与非天然氨基酸多肽的反应产生。一个实施例是含1,2
‑
芳基二胺的非天然氨基酸多肽,其用1,2
‑
二羰基取代的海兔毒素连接基团衍生物衍生化以形成喹喔啉或吩嗪键。另一实施例是含1,2
‑
二羰基的非天然氨基酸多肽,其用1,2
‑
芳基二胺取代的海兔毒素连接基团衍生物衍生化以形成喹喔啉或吩嗪键。
[1020]
本文在某些实施例中提供基于三唑键产生包含非天然氨基酸多肽的毒性化合物的衍生化分子。在一些实施例中,第一与第二反应性基团之间的反应可通过亲偶极反应进行。在某些实施例中,第一反应性基团可以是叠氮化物并且第二反应性基团可以是炔烃。在另外或替代性实施例中,第一反应性基团可以是炔烃并且第二反应性基团可以是叠氮化物。在一些实施例中,胡伊斯根环加成反应(参见,例如胡伊斯根,1,3
‑
偶极环加成化学作用(1,3
‑
dipolar cycloaddition chemistry),(帕德瓦a.(padwa,a.)编,1984),第1
‑
176页)使携有含叠氮化物和炔烃侧链的非天然编码氨基酸的并入允许所得多肽以极高选择性经修饰。在某些实施例中,叠氮化物和炔烃官能团对见于天然存在的多肽中的二十种常见氨基酸均是惰性的。然而,当达到紧密邻近时,叠氮化物和炔烃基团的“簧压(spring
‑
loaded)”性质得以披露,并且其通过胡伊斯根[3 2]环加成反应选择性并且有效地反应以产生相应三唑。参见,例如秦等人,科学301:964
‑
7(2003);王等人,美国化学学会志,125,3192
‑
3193(2003);秦等人,美国化学学会志,124:9026
‑
9027(2002)。涉及含有叠氮化物或炔烃的多肽的环加成反应可在室温下在水性条件下通过加入cu(ii)(例如呈催化量的cuso4形式)在用于以催化量将cu(ii)原位还原成cu(i)的还原剂存在下进行。参见,例如王等人,美国化学学会志125,3192
‑
3193(2003);托尔诺(tornoe)等人,有机化学杂志(j.org.chem.)67:3057
‑
3064(2002);罗斯托夫采夫(rostovtsev),应用化学国际版(angew.chem.int.ed.)41:2596
‑
2599(2002)。优选还原剂包括抗坏血酸盐、金属铜、奎宁、氢醌、维生素k、谷胱甘肽、半胱氨酸、fe2、co2和施加的电势。
[1021]
所述非天然氨基酸杂芳基连接的海兔毒素衍生物包括具有式(xxxi)、(xxxii)、(xxxiii)、(xxxiv)、(xxxv)或(xxxvi)结构的氨基酸:
[1022]
[1023][1024]
其中:
[1025]
z具有以下结构:
[1026][1027]
r5是h、co2h、c1‑
c6烷基或噻唑;
[1028]
r6是oh或h;
[1029]
ar是苯基或吡啶;
[1030]
r1是h、氨基保护基、树脂、至少一个氨基酸、多肽或多核苷酸;
[1031]
r2是oh、酯保护基、树脂、至少一个氨基酸、多肽或多核苷酸;
[1032]
r4是h、卤素、低碳烷基或经取代的低碳烷基;
[1033]
r7是c1‑
c6烷基或氢;
[1034]
l、l1、l2、l3和l4各自是选自由以下组成的群组的连接基团:一键、
‑
亚烷基
‑
、
‑
亚烷基
‑
c(o)
‑
、
‑
亚烷基
‑
j
‑
、
‑
(亚烷基
‑
o)
n
‑
亚烷基
‑
、
‑
(亚烷基
‑
o)
n
‑
亚烷基
‑
c(o)
‑
、
‑
(亚烷基
‑
o)
n
‑
j
‑
、
‑
(亚烷基
‑
o)
n
‑
j
‑
亚烷基
‑
、
‑
(亚烷基
‑
o)
n
‑
(ch2)
n'
‑
nhc(o)
‑
(ch2)
n”‑
c(me)2‑
s
‑
s
‑
(ch2)
n”'
‑
nhc(o)
‑
(亚烷基
‑
o)
n
””
‑
亚烷基
‑
、
‑
(亚烷基
‑
o)
n
‑
亚烷基
‑
w
‑
、
‑
亚烷基
‑
c(o)
‑
w
‑
、
‑
(亚烷基
‑
o)
n
‑
亚烷基
‑
j
‑
、
‑
亚烷基'
‑
j
‑
(亚烷基
‑
o)
n
‑
亚烷基
‑
、
‑
(亚烷基
‑
o)
n
‑
亚烷基
‑
j
‑
亚烷基'、
‑
j
‑
(亚烷基
‑
o)
n
‑
亚烷基
‑
、
‑
(亚烷基
‑
o)
n
‑
亚烷基
‑
j
‑
(亚烷基
‑
o)
n
'
‑
亚烷基
‑
j'
‑
、
‑
w
‑
、
‑
亚烷基
‑
w
‑
、亚烷基'
‑
j
‑
(亚烷基
‑
nme)
n
‑
亚烷基
‑
w
‑
、
‑
j
‑
(亚烷基
‑
nme)
n
‑
亚烷基
‑
w
‑
、
‑
(亚烷基
‑
o)
n
‑
亚烷基
‑
u
‑
亚烷基
‑
c(o)
‑
、
‑
(亚烷基
‑
o)
n
‑
亚烷基
‑
u
‑
亚烷基
‑
、
‑
j
‑
亚烷基
‑
nme
‑
亚烷基'
‑
nme
‑
亚烷基"
‑
w
‑
以及
‑
亚烷基
‑
j
‑
亚烷基'
‑
nme
‑
亚烷基"
‑
nme
‑
亚烷基'"
‑
w
‑
;
[1035]
w具有以下结构:
[1036][1037]
u具有以下结构:
[1038][1039]
j和j'各自独立地具有以下结构:
[1040][1041]
n和n'各自独立地是大于或等于1的整数;
[1042]
d具有以下结构:
[1043][1044]
[1045]
每个r
17
独立地选自由以下组成的群组:h、烷基、经取代的烷基、烯基、经取代的烯基、炔基、经取代的炔基、烷氧基、经取代的烷氧基、烷基烷氧基、经取代的烷基烷氧基、聚环氧烷、经取代的聚环氧烷、芳基、经取代的芳基、杂芳基、经取代的杂芳基、烷芳基、经取代的烷芳基、芳烷基、经取代的芳烷基、
‑
(亚烷基或经取代的亚烷基)
‑
on(r")2、
‑
(亚烷基或经取代的亚烷基)
‑
c(o)sr"、
‑
(亚烷基或经取代的亚烷基)
‑
s
‑
s
‑
(芳基或经取代的芳基)、
‑
c(o)r"、
‑
c(o)2r"或
‑
c(o)n(r")2,其中每个r"独立地是氢、烷基、经取代的烷基、烯基、经取代的烯基、烷氧基、经取代的烷氧基、芳基、经取代的芳基、杂芳基、烷芳基、经取代的烷芳基、芳烷基或经取代的芳烷基;
[1046]
每个z1是一键、cr
17
r
17
、o、s、nr'、cr
17
r
17
‑
cr
17
r
17
、cr
17
r
17
‑
o、o
‑
cr
17
r
17
、cr
17
r
17
‑
s、s
‑
cr
17
r
17
、cr
17
r
17
‑
nr'或nr'
‑
cr
17
r
17
;
[1047]
每个r'是h、烷基或经取代的烷基;
[1048]
每个z2选自由以下组成的群组:一键、
‑
c(o)
‑
、
‑
c(s)
‑
、任选经取代的c1‑
c3亚烷基、任选经取代的c1‑
c3亚烯基和任选经取代的杂烷基;
[1049]
每个z3独立地选自由以下组成的群组:一键、任选经取代的c1‑
c4亚烷基、任选经取代的c1‑
c4亚烯基、任选经取代的杂烷基、
‑
o
‑
、
‑
s
‑
、
‑
c(o)
‑
、
‑
c(s)
‑
和
‑
n(r')
‑
;
[1050]
每个t3是一键、c(r")(r")、o或s;其限制条件是当t3是o或s时,r"不可以是卤素;
[1051]
每个r”是h、卤素、烷基、经取代的烷基、环烷基或经取代的环烷基;
[1052]
m和p是0、1、2或3,其限制条件是m或p中的至少一个不是0;
[1053]
m2是是其中(a)指示键结到b基团并且(b)指示键结到杂环基团内的对应位置;
[1054]
m3是其中(a)指示键结到b基团并且(b)指示键结到杂环基团内的对应位置;
[1055]
m4是其中(a)指示键结到b基团并且(b)指示键结到杂环基团内的对应位置;
[1056]
每个r
19
独立地选自由以下组成的群组:c1‑
c6烷基、c1‑
c6烷氧基、酯、醚、硫醚、氨基烷基、卤素、烷基酯、芳基酯、酰胺、芳基酰胺、烷基卤化物、烷基胺、烷基磺酸、烷基硝基、硫
酯、磺酰基酯、卤磺酰基、腈、烷基腈以及硝基;
[1057]
q是0、1、2、3、4、5、6、7、8、9、10或11;并且
[1058]
每个r
16
独立地选自由以下组成的群组:氢、卤素、烷基、no2、cn和经取代的烷基。
[1059]
在一些实施例中,式(xxxi)化合物包括具有式(xxxi
‑
a)结构的化合物:
[1060][1061]
在式(xxxi)、(xxxii)、(xxxiii)、(xxxiv)、(xxxv)或(xxxvi)化合物的某些实施例中,r5是噻唑或羧酸。在式(xxxi)、(xxxii)、(xxxiii)、(xxxiv)、(xxxv)或(xxxvi)化合物的某些实施例中,r6是h。在式(xxxi)、(xxxii)、(xxxiii)、(xxxiv)、(xxxv)或(xxxvi)化合物的某些实施例中,ar是苯基。在式(xxxi)、(xxxii)、(xxxiii)、(xxxiv)、(xxxv)或(xxxvi)化合物的某些实施例中,r7是甲基。在式(xxxi)、(xxxii)、(xxxiii)、(xxxiv)、(xxxv)或(xxxvi)化合物的某些实施例中,n是0到20的整数。在式(xxxi)、(xxxii)、(xxxiii)、(xxxiv)、(xxxv)或(xxxvi)化合物的某些实施例中,n是0到10的整数。在式(xxxi)、(xxxii)、(xxxiii)、(xxxiv)、(xxxv)或(xxxvi)化合物的某些实施例中,n是0到5的整数。
[1062]
在式(xxxi)、(xxxii)、(xxxiii)、(xxxiv)、(xxxv)或(xxxvi)化合物的某些实施例中,r5是噻唑或羧酸。在式(xxxi)、(xxxii)、(xxxiii)、(xxxiv)、(xxxv)或(xxxvi)化合物的某些实施例中,r5是氢。在式(xxxi)、(xxxii)、(xxxiii)、(xxxiv)、(xxxv)或(xxxvi)化合物的某些实施例中,r5是甲基、乙基、丙基、异丙基、丁基、异丁基、仲丁基、叔丁基、戊基或己基。在式(xxxi)、(xxxii)、(xxxiii)、(xxxiv)、(xxxv)或(xxxvi)化合物的某些实施例中,r5是
‑
nh
‑
(亚烷基
‑
o)
n
‑
nh2,其中亚烷基是
‑
ch2‑
、
‑
ch2ch2‑
、
‑
ch2ch2ch2‑
、
‑
ch2ch2ch2ch2‑
、
‑
ch2ch2ch2ch2ch2‑
、
‑
ch2ch2ch2ch2ch2ch2‑
、
‑
ch2ch2ch2ch2ch2ch2ch2‑
、
‑
ch2ch2ch2ch2ch2ch2ch2ch2‑
、
‑
ch2ch2ch2ch2ch2ch2ch2ch2ch2‑
、
‑
ch2ch2ch2ch2ch2ch2ch2ch2ch2ch2‑
、
‑
ch2ch2ch2ch2ch2ch2ch2ch2ch2ch2ch2‑
或
‑
ch2ch2ch2ch2ch2ch2ch2ch2ch2ch2ch2ch2‑
。在式(xxxi)、(xxxii)、(xxxiii)、(xxxiv)、(xxxv)或(xxxvi)的某些实施例中,亚烷基是亚甲基、亚乙基、亚丙基、亚丁基、亚戊基、亚己基或亚庚基。
[1063]
在式(xxxi)、(xxxii)、(xxxiii)、(xxxiv)、(xxxv)或(xxxvi)化合物的某些实施例中,r5是
‑
nh
‑
(亚烷基
‑
o)
n
‑
nh2,其中n是0、l、2、3、4、5、6、7、8、9、10、11、12、13、14、15、16、17、18、19、20、21、22、23、24、25、26、27、28、29、30、31、32、33、34、35、36、37、38、39、40、41、42、43、44、45、46、47、48、49、50、51、52、53、54、55、56、57、58、59、60、61、62、63、64、65、66、67、68、69、70、71、72、73、74、75、76、77、78、79、80、81、82、83、84、85、86、87、88、89、90、91、92、93、94、95、96、97、98、99或100。
[1064]
在式(xxxi)、(xxxii)、(xxxiii)、(xxxiv)、(xxxv)或(xxxvi)化合物的某些实施例中,r6是h。在式(xxxi)、(xxxii)、(xxxiii)、(xxxiv)、(xxxv)或(xxxvi)化合物的一些实施例中,r6是羟基。
[1065]
在式(xxxi)、(xxxii)、(xxxiii)、(xxxiv)、(xxxv)或(xxxvi)化合物的某些实施例中,ar是苯基。
[1066]
在式(xxxi)、(xxxii)、(xxxiii)、(xxxiv)、(xxxv)或(xxxvi)化合物的某些实施例中,r7是甲基、乙基、丙基、异丙基、丁基、仲丁基异丁基、叔丁基、戊基或己基。在式(xxxi)、(xxxii)、(xxxiii)、(xxxiv)、(xxxv)或(xxxvi)化合物的某些实施例中,r7是氢。
[1067]
在式(xxxi)、(xxxii)、(xxxiii)、(xxxiv)、(xxxv)或(xxxvi)化合物的某些实施例中,l、l1、l2、l3和l4各自独立地是可裂解连接基团或不可裂解连接基团。在式(xxxi)、(xxxii)、(xxxiii)、(xxxiv)、(xxxv)或(xxxvi)化合物的某些实施例中,l、l1、l2、l3和l4各自独立地是寡聚(乙二醇)衍生化连接基团。
[1068]
在式(xxxi)、(xxxii)、(xxxiii)、(xxxiv)、(xxxv)或(xxxvi)化合物的某些实施例中,亚烷基、亚烷基'、亚烷基"和亚烷基'"各自独立地是
‑
ch2‑
、
‑
ch2ch2‑
、
‑
ch2ch2ch2‑
、
‑
ch2ch2ch2ch2‑
、
‑
ch2ch2ch2ch2ch2‑
、
‑
ch2ch2ch2ch2ch2ch2‑
、
‑
ch2ch2ch2ch2ch2ch2ch2‑
、
‑
ch2ch2ch2ch2ch2ch2ch2ch2‑
、
‑
ch2ch2ch2ch2ch2ch2ch2ch2ch2‑
、
‑
ch2ch2ch2ch2ch2ch2ch2ch2ch2ch2‑
、
‑
ch2ch2ch2ch2ch2ch2ch2ch2ch2ch2ch2‑
或
‑
ch2ch2ch2ch2ch2ch2ch2ch2ch2ch2ch2ch2‑
。在式(xxxi)、(xxxii)、(xxxiii)、(xxxiv)、(xxxv)或(xxxvi)化合物的某些实施例中,亚烷基是亚甲基、亚乙基、亚丙基、亚丁基、亚戊基、亚己基或亚庚基。
[1069]
在式(xxxi)、(xxxii)、(xxxiii)、(xxxiv)、(xxxv)或(xxxvi)化合物的某些实施例中,n、n'、n"、n'"和n""各自独立地是0、1、2、3、4、5、6、7、8、9、10、11、12、13、14、15、16、17、18、19、20、21、22、23、24、25、26、27、28、29、30、31、32、33、34、35、36、37、38、39、40、41、42、43、44、45、46、47、48、49、50、51、52、53、54、55、56、57、58、59、60、61、62、63、64、65、66、67、68、69、70、71、72、73、74、75、76、77、78、79、80、81、82、83、84、85、86、87、88、89、90、91、92、93、94、95、96、97、98、99或100。
[1070]
在式(xxxi)、(xxxii)、(xxxiii)、(xxxiv)、(xxxv)或(xxxvi)化合物的某些实施例中,r1是多肽。在式(xxxi)、(xxxii)、(xxxiii)、(xxxiv)、(xxxv)或(xxxvi)化合物的某些实施例中,r2是多肽。在式(xxxi)、(xxxii)、(xxxiii)、(xxxiv)、(xxxv)或(xxxvi)化合物的某些实施例中,所述多肽是抗体。在式(xxxi)、(xxxii)、(xxxiii)、(xxxiv)、(xxxv)或(xxxvi)化合物的某些实施例中,所述抗体是赫赛汀。
[1071]
式(xxxi)、(xxxii)、(xxxiii)、(xxxiv)、(xxxv)或(xxxvi)化合物可通过用含羰基的反应剂(例如酮、酯、硫酯和醛)使芳香族胺化合物还原烷基化而形成。
[1072]
所述具有式(xxxi)、(xxxii)、(xxxiii)、(xxxiv)、(xxxv)或(xxxvi)结构的非天然氨基酸杂环连接的海兔毒素衍生物的形成包括(但不限于)(i)含二胺的非天然氨基酸与含二羰基的海兔毒素连接的衍生物反应或含二胺的非天然氨基酸与含酮炔烃的海兔毒素连接的衍生物反应,(ii)含二羰基的非天然氨基酸与含二胺的海兔毒素连接的衍生物反应或含二羰基的非天然氨基酸与含酮胺的海兔毒素连接的衍生物反应,(iii)含酮炔烃的非天然氨基酸与含二胺的海兔毒素连接的衍生物反应,或(iv)含酮胺的非天然氨基酸与含二羰基的v反应。
[1073]
使用所述反应修饰本文所述的海兔毒素连接的衍生物具有任一种或全部以下优势。第一,二胺在约5到约8的ph值范围内(并且在其它实施例中在约4到约10的ph值范围内,在其它实施例中在约3到约8的ph值范围内,在其它实施例中在约4到约9的ph值范围内,并
且在其它实施例中在约4到约9的ph值范围内,在其它实施例中约4的ph值,并且在另一实施例中约8的ph值)与含二羰基的化合物经历缩合,产生杂环(其包括含氮杂环)键。在这些条件下,天然存在的氨基酸的侧链无反应性。第二,所述选择性化学过程使得有可能对重组蛋白质进行位点特异性衍生化:衍生化蛋白质现可以定义的均质产物形式制备。第三,实现本文所述的二胺与本文中所述的含有二羰基的多肽反应所需的温和条件通常不会不可逆地破坏多肽的三级结构(当然,除反应目的是破坏所述三级结构的情形外)。第四,反应在室温下迅速发生,这允许使用将在较高温度下不稳定的许多类型的多肽或试剂。第五,反应易于在水性条件下发生,这也允许使用与非水溶液不相容(在任何程度上)的多肽和试剂。第六,即使当多肽或氨基酸与试剂的比率是化学计量、近化学计量或类化学计量时,反应也易于发生,从而不需要加入过量的试剂或多肽来获得有用量的反应产物。第七,可视反应物中二胺和二羰基部分的设计而区域选择性和/或区域特异性地产生所得杂环。最后,二胺与含二羰基的分子的缩合会产生在生物条件下稳定的杂环(包括含氮杂环)键。
[1074]
vi.海兔毒素连接基团衍生物中非天然氨基酸的定位
[1075]
本文所述的方法和组合物包括将一个或一个以上非天然氨基酸并入海兔毒素连接基团衍生物中。可将一个或一个以上非天然氨基酸并入一个或一个以上不破坏海兔毒素连接基团衍生物活性的特定位置处。这可以通过进行“保守”取代实现,包括(但不限于)用非天然或天然疏水性氨基酸取代疏水性氨基酸;用非天然或天然庞大氨基酸取代庞大氨基酸;用非天然或天然亲水性氨基酸取代亲水性氨基酸;和/或将非天然氨基酸插入活性不需要的位置中。
[1076]
可使用多种生物化学和结构方法来选择海兔毒素连接基团衍生物内供非天然氨基酸取代的所需位点。在一些实施例中,非天然氨基酸连接在海兔毒素衍生物的c端处。在其它实施例中,非天然氨基酸连接在海兔毒素衍生物的n端处。海兔毒素连接基团衍生物的任何位置都适用于选择以并入非天然氨基酸,并且选择可基于合理设计或者通过随机选择以实现任何或并非特别需要的目的。所需位点的选择可基于产生具有任何所需性质或活性的非天然氨基酸多肽(其可经进一步修饰或保持未经修饰),包括(但不限于)受体结合调节剂、受体活性调节剂、与结合搭配物结合的调节剂、结合搭配物活性调节剂、结合搭配物构象调节剂;二聚体或多聚体形成;与天然分子相比活性或性质无改变;或者操控多肽的任何物理或化学性质(如溶解性、聚集或稳定性)。或者,经鉴别是对生物活性至关重要的位点也可视对于多肽所寻求的所需活性而为供非天然氨基酸取代的良好候选物。另一替代方案将是在多肽链上的每个位置中利用非天然氨基酸简单地进行连续取代并且观察对多肽活性的影响。选择用于将非天然氨基酸取代到任何多肽中的位置的任何方式、技术或方法都适用于本文所述的方法、技术和组合物。
[1077]
也可检查多肽的含有缺失的天然存在突变体的结构和活性以确定很可能耐受非天然氨基酸的取代的蛋白质区域。在已消除可能无法耐受非天然氨基酸的取代的残基后,可使用包括(但不限于)相关多肽以及任何缔合的配体或结合蛋白的三维结构的方法检查所推荐的取代在各剩余位置处的影响。许多多肽的x射线结晶学和nmr结构都可从蛋白质数据库(protein data bank,pdb;www.rcsb.org)得到,pdb是含有蛋白质和核酸大分子的三维结构数据的中央数据库,其可用于鉴别可经非天然氨基酸取代的氨基酸位置。此外,如果无法得到三维结构数据,那么可制造研究多肽二级结构和三级结构的模型。因此,可容易地
获得可经非天然氨基酸取代的氨基酸位置的鉴别。
[1078]
并入非天然氨基酸的例示性位点包括(但不限于):不包括在潜在受体结合区域或用于与结合蛋白或配体结合的区域中的位点;可完全或部分暴露于溶剂的位点;与邻近残基具有最小或无氢键相互作用的位点;可最低限度暴露于邻近反应性残基的位点;和/或可在如通过特定多肽与其缔合受体、配体或结合蛋白的三维晶体结构所预计的高度可弯曲的区域中的位点。
[1079]
多种非天然氨基酸可取代多肽的给定位置或并入多肽的给定位置中。举例来说,基于多肽与其缔合配体、受体和/或结合蛋白的三维晶体结构的检查来选择供并入的特定非天然氨基酸,优选保守取代。
[1080]
在一个实施例中,本文中所述的方法包括并入海兔毒素连接基团衍生物中,其中所述海兔毒素连接基团衍生物包含第一反应性基团;和使所述海兔毒素连接基团衍生物与包含第二反应性基团的分子(包括(但不限于)第二蛋白质或多肽或多肽类似物;抗体或抗体片段;和其任何组合)接触。在某些实施例中,第一反应性基团是羟胺部分并且第二反应性基团是羰基或二羰基部分,由此形成肟键。在某些实施例中,第一反应性基团是羰基或二羰基部分并且第二反应性基团是羟胺部分,由此形成肟键。在某些实施例中,第一反应性基团是羰基或二羰基部分并且第二反应性基团是肟部分,由此发生肟交换反应。在某些实施例中,第一反应性基团是肟部分并且第二反应性基团是羰基或二羰基部分,由此发生肟交换反应。
[1081]
在一些情况下,将海兔毒素连接基团衍生物并入与多肽内的其它添加、取代或缺失组合以影响其它化学、物理、药理学和/或生物学特性。在一些情况下,所述其它添加、取代或缺失可增加多肽的稳定性(包括(但不限于)对蛋白水解降解的抗性)或增加多肽对其适当受体、配体和/或结合蛋白的亲和力。在一些情况下,所述其它添加、取代或缺失可增加多肽的溶解性(包括(但不限于)当在大肠杆菌或其它宿主细胞中表达时)。在一些实施例中,出于增加多肽溶解性的目的,在大肠杆菌或其它重组宿主细胞中表达后,选择除并入非天然氨基酸的另一位点外的位点以供天然编码或非天然氨基酸取代。
[1082]
在一些实施例中,多肽包含另一添加、取代或缺失,其调节对缔合配体、结合蛋白和/或受体的亲和力;调节(包括(但不限于)增加或降低)受体二聚化;使受体二聚体稳定;调节循环半衰期;调节释放或生物可用性;利于纯化;或者改进或改变特定投药途径。类似地,非天然氨基酸多肽可包含化学或酶裂解序列、蛋白酶裂解序列、反应性基团、抗体结合域(包括(但不限于)flag或多聚组氨酸)或其它基于亲和力的序列(包括(但不限于)flag、多聚组氨酸、gst等)或连接分子(包括(但不限于)生物素),其改进检测(包括(但不限于)gfp)、纯化、转运穿过组织或细胞膜、前药释放或活化、尺寸减小或多肽的其它特性。
[1083]
vii.作为范例的her2基因
[1084]
本文所述的方法、组合物、策略和技术不限于特定类型、种类或家族的多肽或蛋白质。事实上,几乎任何多肽都可经设计或经修饰以包括本文所述的含有至少一个“经修饰或未经修饰”的非天然氨基酸的海兔毒素连接基团衍生物。仅举例来说,多肽可与选自由以下组成的群组的治疗性蛋白质同源:α
‑
1抗胰蛋白酶、血管生成抑制素、抗溶血因子、抗体、抗体片段、单克隆抗体(例如贝伐单抗(bevacizumab)、西妥昔单抗(cetuximab)、帕尼单抗(panitumumab)、英利昔单抗(infliximab)、阿达木单抗(adalimumab)、巴利昔单抗
(basiliximab)、达利珠单抗(daclizumab)、奥马珠单抗(omalizumab)、优特克单抗(ustekinumab)、依那西普(etanercept)、吉妥珠单抗(gemtuzumab)、阿仑单抗(alemtuzumab)、利妥昔单抗(rituximab)、曲妥珠单抗(trastuzumab)、尼妥珠单抗(nimotuzumab)、帕利珠单抗(palivizumab)和阿昔单抗(abciximab))、载脂蛋白(apolipoprotein)、脱辅基蛋白(apoprotein)、心房利钠因子、心房利钠多肽、心房肽、c
‑
x
‑
c趋化因子、t39765、nap
‑
2、ena
‑
78、gro
‑
a、gro
‑
b、gro
‑
c、ip
‑
10、gcp
‑
2、nap
‑
4、sdf
‑
1、pf4、mig、降钙素、c
‑
kit配体、细胞因子、cc趋化因子、单核细胞趋化蛋白
‑
1、单核细胞趋化蛋白
‑
2、单核细胞趋化蛋白
‑
3、单核细胞炎症蛋白
‑
1α、单核细胞炎症蛋白
‑
iβ、rantes、1309、r83915、r91733、hcc1、t58847、d31065、t64262、cd40、cd40配体、c
‑
kit配体、胶原蛋白、群落刺激因子(csf)、补体因子5a、补体抑制剂、补体受体1、细胞因子、上皮嗜中性粒细胞活化肽
‑
78、mip
‑
16、mcp
‑
1、表皮生长因子(egf)、上皮嗜中性粒细胞活化肽、促红细胞生成素(epo)、脱落毒素、因子ix、因子vii、因子viii、因子x、成纤维细胞生长因子(fgf)、纤维蛋白原、纤维结合蛋白、四螺旋束蛋白、g
‑
csf、glp
‑
1、gm
‑
csf、葡糖脑苷脂酶、促性腺激素、生长因子、生长因子受体、grf、刺猬蛋白、血红蛋白、肝细胞生长因子(hgf)、水蛭素(hirudin)、人类生长激素(hgh)、人血清白蛋白、icam
‑
1、icam
‑
1受体、lfa
‑
1、lfa
‑
1受体、胰岛素、胰岛素样生长因子(igf)、igf
‑
i、igf
‑
ii、干扰素(ifn)、ifn
‑
α、ifn
‑
β、ifn
‑
γ、白细胞介素(il)、il
‑
1、il
‑
2、il
‑
3、il
‑
4、il
‑
5、il
‑
6、il
‑
7、il
‑
8、il
‑
9、il
‑
10、il
‑
11、il
‑
12、角质化细胞生长因子(kgf)、乳铁蛋白、白血病抑制因子、荧光素酶、神经秩蛋白(neurturin)、嗜中性粒细胞抑制因子(nif)、抑瘤素m(oncostatin m)、成骨蛋白、癌基因产物、paracitonin、甲状旁腺激素、pd
‑
ecsf、pdgf、肽激素、多效生长因子(pleiotropin)、蛋白质a、蛋白质g、pth、致热性外毒素a、致热性外毒素b、致热性外毒素c、pyy、松驰素、肾素、scf、小生物合成蛋白、可溶性补体受体i、可溶性i
‑
cam 1、可溶性白细胞介素受体、可溶性tnf受体、生长调节素(somatomedin)、生长抑素(somatostatin)、生长激素(somatotropin)、链激酶、超抗原(superantigen)、葡萄球菌肠毒素(staphylococcal enterotoxin)、sea、seb、sec1、sec2、sec3、sed、see、类固醇激素受体、超氧化物歧化酶、中毒性休克综合症毒素、胸腺肽α1、组织型纤溶酶原活化剂、肿瘤生长因子(tgf)、肿瘤坏死因子、肿瘤坏死因子α、肿瘤坏死因子β、肿瘤坏死因子受体(tnfr)、vla
‑
4蛋白、vcam
‑
1蛋白、血管内皮生长因子(vegf)、尿激酶、mos、ras、raf、met、p53、tat、fos、myc、jun、myb、rel、雌激素受体、孕酮受体、睾酮受体、醛固酮受体、ldl受体和皮质酮。
[1085]
一个实施例是一种治疗过度表达her
‑
2的实体肿瘤的方法,所述实体肿瘤选自由以下组成的群组:乳癌、小细胞肺癌、卵巢癌、前列腺癌、胃癌、子宫颈癌、食道癌和结肠癌。在另一实施例中,实体肿瘤是乳癌。在另一实施例中,实体肿瘤是卵巢癌。
[1086]
因此,提供以下曲妥珠单抗的说明以用于说明性目的,并且仅举例来说不作为对本文所述的方法、组合物、策略和技术的范围的限制。另外,在本技术案中提及曲妥珠单抗打算使用通用术语作为任何抗体的一个实例。因此,应理解在提及曲妥珠单抗情况下本文所述的修饰和化学作用可同样地应用于任何抗体或单克隆抗体,包括本文中特别列出的那些。
[1087]
曲妥珠单抗是人类化单克隆抗体,其结合于her2/neu受体的胞外区段的域iv。her2基因(也称为her2/neu和erbb2基因)在20%到30%的早期乳癌中扩增,由此使其过度
表达。此外,在癌症中,her2可在有丝分裂原没有到达并结合于任何受体的情况下发送信号,使其过度活跃。
[1088]
her2穿过细胞膜延伸,并将信号从细胞外部携带到内部。在健康人群中,称为有丝分裂原的信号传导化合物到达细胞膜,并结合于her受体家族的其它成员的外部部分。那些结合的受体接着与her2连接(二聚),将其活化。her2接着向细胞内部发送信号。信号通过不同生物化学路径。此路径包括pi3k/akt路径和mapk路径。这些信号促进细胞的侵袭、存活和血管生长(血管生成)。
[1089]
用曲妥珠单抗处理的细胞在细胞周期的g1期期间经历停滞,因此增殖减少。已提出曲妥珠单抗通过以下方式诱导一些其作用:下调her2/neu,引起受体二聚化的破坏并且信号传导通过下游pi3k级联。p27kip1接着不经磷酸化并且能够进入细胞核并且抑制cdk2活性,引起细胞周期停滞。此外,曲妥珠单抗通过诱导抗血管生成因子和抑制促血管生成因子两者来抑制血管生成。据认为在癌症中观察到的对未经调节的生长的贡献可归因于引起胞外域释放的her2/neu的蛋白水解裂解。曲妥珠单抗已展示在乳癌细胞中抑制her2/neu胞外域裂解。
[1090]
viii.非天然氨基酸的细胞摄取
[1091]
真核细胞对非天然氨基酸的摄取是在设计和选择(包括(但不限于))用于并入蛋白质中的非天然氨基酸时通常所考虑的一个问题。举例来说,α
‑
氨基酸的高电荷密度表明,这些化合物不可能渗透细胞。通过一系列基于蛋白质的转运系统将天然氨基酸吸收到真核细胞中。可进行评估哪些非天然氨基酸(如果存在)被细胞吸收的快速筛选(本文中实例15和16说明可在非天然氨基酸上进行的测试的非限制性实例)。参见,例如,例如名为“蛋白质阵列(protein arrays)”的美国专利公开案第2004/198637号(其以全文引用的方式并入本文中)以及刘d.r.(liu,d.r.)和舒尔茨p.g.(schultz,p.g.)(1999)关于具有扩展遗传代码的生物体的进化的进展(progress toward the evolution of an organism with an expanded genetic code).美国国家科学院院刊(pnas united states)96:4780
‑
4785中的毒性分析。尽管易于利用各种分析来分析摄取,但设计适用于细胞摄取路径的非天然氨基酸的替代方案是提供生物合成路径以在体内产生氨基酸。
[1092]
通常,如本文所述通过细胞摄取产生的非天然氨基酸以足以进行有效蛋白质生物合成(包括(但不限于)天然细胞量)但未达到影响其它氨基酸的浓度或耗尽细胞资源的程度的浓度来产生。以此方式产生的典型浓度是约10mm到约0.05mm。
[1093]
ix.非天然氨基酸的生物合成
[1094]
许多生物合成路径已存在于细胞中以供产生氨基酸和其它化合物。虽然特定非天然氨基酸的生物合成方法可能不存在于自然界(包括(但不限于)细胞)中,但本文所述的方法和组合物提供此类方法。举例来说,可在宿主细胞中通过加入新的酶或改变现存的宿主细胞路径来产生非天然氨基酸的生物合成路径。其它新的酶包括天然存在的酶或人工开发的酶。举例来说,对氨基苯丙氨酸的生物合成(如名为“非天然氨基酸的体内并入(in vivo incorporation of unnatural amino acids)”的wo 2002/085923中的一个实例所呈现)依赖于加入来自其它生物体的已知酶的组合。这些酶的基因可通过用包含所述基因的质粒转化细胞来引入真核细胞中。当在细胞中表达时,所述基因提供合成所需化合物的酶促路径。本文提供任选地加入的酶类型的实例。其它酶序列见于例如genbank中。人工开发的酶可以
相同方式加入细胞中。以此方式,操控细胞机器和细胞资源产生非天然氨基酸。
[1095]
多种方法可用于产生用于生物合成路径或发展现存路径的新颖酶。举例来说,可将(包括(但不限于))如麦克西金公司(maxygen,inc.)所开发的递归重组(recursive recombination)(可在万维网www.maxygen.com上获得)用于开发新颖酶和路径。参见,例如斯泰莫(stemmer)(1994),通过dna改组使蛋白质体外快速进化(rapid evolution of a protein in vitro by dna shuffling),自然(nature)370(4):389
‑
391;和斯泰莫,(1994),通过随机片段化和重新装配进行dna改组:分子进化的体外重组(dna shuffling by random fragmentation and reassembly:in vitro recombination for molecular evolution),美国国家科学院院刊,91:10747
‑
10751。类似地,任选地将杰能科(genencor)所开发的designpath
tm
(可在万维网genencor.com上获得)用于代谢路径工程化,包括(但不限于)使路径工程化以在细胞中产生非天然氨基酸。这项技术使用新基因(包括(但不限于)通过功能性基因组学、分子进化和设计所鉴别的基因)的组合在宿主生物体中重建现存路径。达维萨公司(diversa corporation;可在万维网diversa.com上获得)也提供迅速筛选基因文库和基因路径的技术,包括(但不限于)建立新路径以用于以生物合成方式产生非天然氨基酸。
[1096]
通常,用如本文所述的经工程化的生物合成路径所产生的非天然氨基酸是以足以进行有效蛋白质生物合成(包括(但不限于)天然细胞量)但未达到影响其它氨基酸的浓度或耗尽细胞资源的程度的浓度来产生。以此方式在体内所产生的典型浓度是约10mm到约0.05mm。在用包含用于产生特定路径所需的酶的基因的质粒转化细胞并且产生非天然氨基酸后,任选地使用体内选择以针对核糖体蛋白质合成和细胞生长两者进一步优化非天然氨基酸产生。
[1097]
x.其它合成方法
[1098]
可使用所属领域中所述的方法或使用本文所述的技术或通过其组合来合成本文所述的非天然氨基酸。作为辅助,下表提供可组合产生所需官能团的各种起始亲电子试剂和亲核试剂。所提供的信息意欲说明而非限制本文所述的合成技术。
[1099]
表1:共价键和其前体的实例
[1100][1101][1102]
一般来说,碳亲电子试剂易于受包括碳亲核试剂的互补亲核试剂攻击,其中攻击性亲核试剂将电子对运送到碳亲电子试剂,以便在亲核试剂与碳亲电子试剂之间形成新
键。
[1103]
碳亲核试剂的非限制性实例包括(但不限于)烷基、烯基、芳基和炔基格林纳试剂(grignard);有机锂;有机锌;烷基、烯基、芳基和炔基锡试剂(有机锡烷);烷基、烯基、芳基和炔基硼烷试剂(有机硼烷和有机硼酸盐);这些碳亲核试剂具有在水或极性有机溶剂中动力学稳定的优势。碳亲核试剂的其它非限制性实例包括磷内鎓盐、烯醇和烯醇化物试剂;这些碳亲核试剂具有相对易于由合成有机化学领域技术人员众所周知的前体产生的优势。当与碳亲电子试剂组合使用时,碳亲核试剂在碳亲核试剂与碳亲电子试剂之间产生新的碳
‑
碳键。
[1104]
适于与碳亲电子试剂偶合的非碳亲核试剂的非限制性实例包括(但不限于)伯胺和仲胺、硫醇、硫醇盐和硫醚、醇、醇盐、叠氮化物、氨基脲等。当与碳亲电子试剂结合使用时,这些非碳亲核试剂通常产生杂原子键(c
‑
x
‑
c),其中x是杂原子,包括(但不限于)氧、硫或氮。
[1105]
实例
[1106]
实例1:合成化合物1
[1107]
流程1
[1108][1109]
化合物1
‑
3:在0℃下将四(乙二醇)1
‑
1(10g,51.5mmol)、n
‑
羟基邻苯二甲酰亚胺1
‑
2(8.4g,51.15mmol)和三苯膦(17.6g,67mmol)溶解于300ml四氢呋喃中,随后加入diad(12.8ml,61.78mmol)。在室温下搅拌所得溶液过夜,接着浓缩到干燥。残余物通过快速柱色谱纯化,得到5.47g(31%)化合物1
‑
3。
[1110]
化合物1
‑
4:向化合物1
‑
3(200mg,0.59mmol)于15ml二氯甲烷中的溶液中加入戴斯
‑
马丁高碘烷(dess
‑
martin periodinane)(300mg,0.71mmol)。在环境温度下搅拌反应混
合物过夜。用亚硫酸氢钠于15ml饱和碳酸氢钠中的溶液淬灭反应物。分离混合物。有机层用饱和碳酸氢钠、盐水洗涤,经硫酸钠干燥,过滤并且在真空中浓缩。残余物通过快速柱色谱纯化,得到150mg(75%)化合物1
‑
4。
[1111]
化合物1
‑
6:向单甲基海兔毒素盐酸盐1
‑
5(50mg,0.062mmol)于1ml dmf中的溶液中加入化合物1
‑
4(63mg,0.186mmol)和70μl乙酸,随后加入8mg氰基硼氢化钠。在环境温度下搅拌所得混合物2小时。反应混合物用水稀释并且通过hplc纯化,得到60mg(80%)化合物1
‑
6。ms(esi)m/z 547[m 2h],1092[m h]。
[1112]
化合物1:将化合物1
‑
6(60mg,0.05mmol)溶解于1ml dmf中。加入32μl肼。在环境温度下搅拌所得溶液1小时。用1n盐酸溶液淬灭反应物。反应混合物通过hplc纯化,得到33mg(55%)化合物1。ms(esi)m/z 482[m 2h],962[m h]。
[1113]
实例2:合成化合物2
[1114]
流程2
[1115][1116]
化合物2通过与如实例1中所述类似的合成途径合成。ms(esi)m/z 460[m 2h],918[m h]。
[1117]
实例3:合成化合物3
[1118]
流程3
[1119][1120]
化合物3通过与实例1类似的合成途径合成。ms(esi)m/z 438[m 2h],974[m h]。
[1121]
实例4:合成化合物4
[1122]
化合物4
‑
2:向val(otbu)
‑
oh.hcl 4
‑
1(1g,4.77mmol)和溴乙醇(304.7μl,4.3mmol)于10ml dmf中的溶液中加入1.68ml diea。在室温下搅拌反应混合物2天。向反应混合物中相继加入4.8mmol boc2o和0.84ml diea。在室温下搅拌反应混合物2天。反应混合物在真空中浓缩并且用乙酸乙酯萃取,并且用水、盐水洗涤,经硫酸钠干燥并且在真空中浓缩。残余物通过快速柱色谱纯化,得到0.66g化合物4
‑
2。
[1123]
流程4
[1124][1125]
化合物4
‑
3:在0℃下,向化合物4
‑
2(500mg,1.58mmol)、n
‑
羟基邻苯二甲酰亚胺(261mg,1.6mmol)和三苯膦(538mg,2.05mmol)于15ml thf中的溶液中加入diad(394μl,1.9mmol)。在室温下搅拌所得溶液过夜,接着在真空中浓缩。残余物通过快速柱色谱纯化,得到0.68g化合物4
‑
3。
[1126]
化合物4
‑
4:将化合物4
‑
3溶解于15ml 4n hcl/二噁烷中。在室温下搅拌反应混合物2天并且在真空中浓缩。将残余物溶解于dmf中并且用boc2o(230μl,1mmol)和diea(352μl,2mmol)处理。在室温下搅拌反应混合物2天。反应混合物通过hplc纯化,得到100mg化合物4
‑
4。
[1127]
化合物4
‑
5:向化合物boc
‑
val
‑
dil
‑
甲基dap
‑
oh于dmf中的溶液中加入phe(otbu)
‑
oh.hcl、hatu和n
‑
甲基吗啉。在室温下搅拌反应混合物4小时。在真空中浓缩反应混合物并且用乙酸乙酯(100ml
×
1,50ml
×
2)萃取。合并有机层并用盐水洗涤,经硫酸钠干燥并且在真空中浓缩。残余物通过快速色谱纯化。所得化合物用hcl/etoac处理,得到化合物4
‑
5。
[1128]
化合物4
‑
6:向化合物4
‑
5于dmf中的溶液中加入化合物4
‑
4、hatu和diea。在室温下
搅拌反应混合物4小时。在真空中浓缩反应混合物并用乙酸乙酯(100ml
×
1,50ml
×
2)萃取。合并有机层并用盐水洗涤,经硫酸钠干燥并且在真空中浓缩。残余物通过快速色谱纯化,得到化合物4
‑
6。
[1129]
化合物4
‑
7:将化合物4
‑
6溶解于15ml 4n hcl/二噁烷中。在室温下搅拌反应混合物2小时并且在真空中浓缩,得到化合物4
‑
7。
[1130]
化合物4
‑
8:向化合物4
‑
7于1ml dmf中的溶液中相继加入甲醛和乙酸以及氰基硼氢化钠。在环境温度下搅拌所得混合物2小时。反应混合物用水稀释并通过hplc纯化,得到化合物4
‑
8。
[1131]
化合物4:将化合物4
‑
8溶解于1ml dmf中。加入肼。在环境温度下搅拌所得溶液1小时。用1n盐酸溶液淬灭反应物。反应混合物通过hplc纯化,得到化合物4。
[1132]
实例5:合成化合物5
[1133]
将化合物4
‑
7溶解于1ml dmf中。加入肼。在环境温度下搅拌所得溶液1小时。用1n盐酸溶液淬灭反应物。反应混合物通过hplc纯化,得到化合物5。
[1134]
实例6:合成化合物6
[1135]
流程6
[1136][1137]
化合物6
‑
2:向化合物6
‑
1(500mg,0.875mmol)于3ml dmf中的溶液中加入283mg苯丙氨酸盐酸盐、433mg hatu和581μl n
‑
甲基吗啉。在室温下搅拌反应混合物4小时。在真空中浓缩反应混合物并且用乙酸乙酯(100ml
×
1,50ml
×
2)萃取。合并有机层并用盐水洗涤,经硫酸钠干燥并且在真空中浓缩。残余物通过快速色谱纯化,得到560mg(76%)化合物6
‑
2。
[1138]
化合物6
‑
3:将化合物6
‑
2溶解于15ml 4n hcl/二噁烷中。在室温下搅拌反应混合物2小时并且在真空中浓缩,得到511mg化合物6
‑
3。
[1139]
化合物6
‑
4:向化合物6
‑
3(368mg,0.55mmol)于3ml dmf中的溶液中加入255mg boc
‑
n
‑
甲基缬氨酸、314mg hatu和303μl n
‑
甲基吗啉。在室温下搅拌反应混合物4小时。在真空中浓缩反应混合物并用乙酸乙酯(100ml
×
1,50ml
×
2)萃取。合并有机层并用盐水洗涤,经硫酸钠干燥并且在真空中浓缩。残余物通过快速色谱纯化,得到370mg(79%)化合物
6
‑
4。
[1140]
化合物6
‑
5:向化合物6
‑
4(170mg)于10ml meoh中的溶液中加入5当量1n lioh。在室温下搅拌反应混合物2小时。反应混合物利用1n hcl酸化并且用乙酸乙酯萃取,用盐水洗涤,经硫酸钠干燥并且在真空中浓缩,得到150mg(90%)化合物6
‑
5。
[1141]
化合物6
‑
6:将化合物6
‑
5溶解于4n hcl/二噁烷中。在室温下搅拌反应混合物2小时并且在真空中浓缩,并且通过hplc纯化,得到150mg化合物6
‑
6。
[1142]
化合物6
‑
7:向化合物6
‑
6(50mg,0.062mmol)于1ml dmf中的溶液中相继加入化合物1
‑
4(63mg,0.186mmol)和70μl乙酸以及8mg氰基硼氢化钠。在环境温度下搅拌所得混合物2小时。反应混合物用水稀释并且通过hplc纯化,得到60mg(80%)化合物6
‑
7。
[1143]
化合物6:将化合物6
‑
7(60mg,0.05mmol)溶解于1ml dmf中。加入32μl肼。在环境温度下搅拌所得溶液1小时。用1n盐酸溶液淬灭反应物。反应混合物通过hplc纯化,得到33mg(55%)化合物6。
[1144]
实例7:合成化合物7
[1145]
流程7
[1146][1147]
化合物7通过与化合物1类似的合成途径合成。ms(esi)m/z 440[m 2h],879[m h]。
[1148]
实例8:合成化合物8
[1149]
流程8
[1150][1151]
化合物8通过与化合物1类似的合成途径合成。ms(esi)m/z 418[m 2h],835[m h]。
[1152]
实例9:合成化合物9
[1153]
流程9
[1154][1155]
化合物9
‑
1:向化合物boc
‑
val
‑
dil
‑
甲基dap
‑
oh于dmf中的溶液中加入4
‑
(2
‑
氨基乙基)吡啶、hatu和n
‑
甲基吗啉。在室温下搅拌反应混合物4小时。在真空中浓缩反应混合物
并用乙酸乙酯(100ml
×
1,50ml
×
2)萃取。合并有机层并用盐水洗涤,经硫酸钠干燥并且在真空中浓缩。残余物通过快速色谱纯化。所得化合物用hcl/etoac处理,得到化合物9
‑
1。
[1156]
化合物9
‑
2:向化合物9
‑
1于dmf中的溶液中加入化合物4
‑
4、hatu和diea。在室温下搅拌反应混合物4小时。在真空中浓缩反应混合物并且用乙酸乙酯(100ml
×
1,50ml
×
2)萃取。合并有机层并用盐水洗涤,经硫酸钠干燥并且在真空中浓缩。残余物通过快速色谱纯化,得到化合物9
‑
2。
[1157]
化合物9
‑
3:将化合物9
‑
2溶解于15ml 4n hcl/二噁烷中。在室温下搅拌反应混合物2小时并且在真空中浓缩,得到化合物9
‑
3。
[1158]
化合物9
‑
4:向化合物9
‑
3于1ml dmf中的溶液中相继加入甲醛和乙酸以及氰基硼氢化钠。在环境温度下搅拌所得混合物2小时。反应混合物用水稀释并通过hplc纯化,得到化合物9
‑
4。
[1159]
化合物9:将化合物9
‑
4溶解于1ml dmf中。加入肼。在环境温度下搅拌所得溶液1小时。用1n盐酸溶液淬灭反应物。反应混合物通过hplc纯化,得到化合物9。
[1160]
实例10:合成化合物10
[1161]
流程10
[1162][1163]
化合物10:将化合物9
‑
3溶解于1ml dmf中。加入肼。在环境温度下搅拌所得溶液1小时。用1n盐酸溶液淬灭反应物。反应混合物通过hplc纯化,得到实例10。
[1164]
实例11:合成化合物11
[1165]
流程11
[1166][1167]
化合物11
‑
3:向四(乙二醇)11
‑
1(40.6ml,235mmol)于100ml四氢呋喃中的溶液中加入47mg钠。在钠溶解之后加入12ml丙烯酸叔丁酯。在室温下搅拌反应混合物24小时。在真空中浓缩反应混合物并且用2ml 1n hcl淬灭。将残余物悬浮于盐水中并且用乙酸乙酯(100ml
×
1,50
×
2)萃取。合并有机层并且用盐水洗涤,经硫酸钠干燥并且在真空中浓缩,得到6.4g(23%)化合物11
‑
3。
[1168]
化合物11
‑
5:在0℃下,将化合物11
‑
3(1.0g,3.12mmol)、n
‑
羟基邻苯二甲酰亚胺11
‑
4(611mg,3.744mmol)和三苯膦(1.23g,4.68mmol)溶解于20ml四氢呋喃中,接着加入diad(0.84ml,4.06mmol)。在室温下搅拌所得溶液过夜,接着浓缩到干燥。通过快速柱色谱,使用siliasep滤筒(80g),用0
‑
100%乙酸乙酯/己烷洗脱来纯化残余物,得到1.0g(100%)化合物11
‑
5。
[1169]
化合物11
‑
6:将化合物11
‑
5溶解于15ml 4n hcl/二噁烷中。在室温下搅拌反应混合物2小时并且在真空中浓缩,得到1.0g化合物11
‑
6。
[1170]
化合物11
‑
8:向30mg(0.0372mmol)单甲基海兔毒素盐酸盐、31mg(0.0744mmol)化合物11
‑
6和38.2mg(0.082mmol)pybrop于1ml dmf中的溶液中加入33μl(0.186mmol)二异丙基乙胺。在室温下搅拌反应混合物5小时。通过hplc纯化反应混合物,得到28mg(65%)化合物11
‑
8。ms(esi)m/z 785[m 2h],1164[m h]。
[1171]
化合物11:将化合物11
‑
8(28mg,0.024mmol)溶解于1ml dmf中。加入23μl(0.72mmol)无水肼。在室温下搅拌所得溶液1小时。用1n盐酸溶液淬灭反应物。通过制备型hplc,在254nm下用20
‑
70%ch3cn/h2o洗脱20分钟来纯化反应混合物,得到20mg(66%)化合物11。ms(esi)m/z 518[m 2h],1034[m h]。
[1172]
实例12:合成化合物12
[1173]
流程12
[1174][1175]
化合物12
‑
2:向化合物12
‑
1(500mg,0.875mmol)于3ml dmf中的溶液中加入283mg苯丙氨酸盐酸盐、433mg hatu和581μl n
‑
甲基吗啉。在室温下搅拌反应混合物4小时。在真空中浓缩反应混合物并且用乙酸乙酯(100ml
×
1,50ml
×
2)萃取。合并有机层并且用盐水洗涤,经硫酸钠干燥并且在真空中浓缩。通过快速色谱纯化残余物,得到560mg(76%)化合物12
‑
2。
[1176]
化合物12
‑
3:将化合物12
‑
2溶解于15ml 4n hcl/二噁烷中。在室温下搅拌反应混合物2小时并且在真空中浓缩,得到511mg化合物12
‑
3。
[1177]
化合物12
‑
4:向化合物12
‑
3(368mg,0.55mmol)于3ml dmf中的溶液中加入255mg boc
‑
n
‑
甲基缬氨酸、314mg hatu和303μl n
‑
甲基吗啉。在室温下搅拌反应混合物4小时。在真空中浓缩反应混合物并且用乙酸乙酯(100ml
×
1,50ml
×
2)萃取。合并有机层并且用盐水洗涤,经硫酸钠干燥并且在真空中浓缩。通过快速色谱纯化残余物,得到370mg(79%)化合物12
‑
4。
[1178]
化合物12
‑
5:向化合物12
‑
4(170mg)于10ml meoh中的溶液中加入5当量1n lioh。在室温下搅拌反应混合物2小时。反应混合物用1n hcl酸化并用乙酸乙酯萃取,用盐水洗涤,经硫酸钠干燥并且在真空中浓缩,得到150mg(90%)化合物12
‑
5。
[1179]
化合物12
‑
6:将化合物12
‑
5溶解于4n hcl/二噁烷中。在室温下搅拌反应混合物2小时并且在真空中浓缩和通过hplc纯化,得到150mg化合物12
‑
6。
[1180]
化合物12
‑
7:向化合物12
‑
6于dmf中的溶液中相继加入甲醛(3当量)和20当量乙酸以及2当量氰基硼氢化钠。在环境温度下搅拌所得混合物2小时。反应混合物用水稀释并且通过hplc纯化,得到化合物12
‑
7。
[1181]
化合物12
‑
10:在0℃下,将2
‑
(2
‑
羟基乙氧基)乙基氨基甲酸叔丁酯(2.05g,10mmol)、n
‑
羟基邻苯二甲酰亚胺(1.8g,11mmol)和三苯膦(3.67g,14mmol)溶解于100ml四氢呋喃中,接着加入diad(2.48ml,12mmol)。在室温下搅拌所得溶液过夜,接着浓缩到干燥。
用50ml 4n hcl/二噁烷处理残余物。在室温下搅拌混合物2小时。在真空中去除溶剂。残余物用乙醚处理,过滤,用醚洗涤并且在真空中干燥,得到2.6g(91%)化合物12
‑
10。ms(esi)m/z 251[m h]。
[1182]
化合物12
‑
11:向化合物12
‑
10(20mg,0.026mmol)于1ml dmf中的溶液中加入11.2mg化合物12
‑
10、15mg hatu和23μl diea。在室温下搅拌反应混合物2小时。通过hplc纯化反应混合物,得到20mg(70%)化合物12
‑
4。ms(esi)m/z 490[m 2h],978[m h]。
[1183]
化合物12:将化合物12
‑
11(20mg,0.0183mmol)溶解于1ml dmf中。加入18μl(0.56mmol)无水肼。在室温下搅拌所得溶液1小时。用1n盐酸溶液淬灭反应物。通过制备型hplc,在254nm下用20
‑
70%ch3cn/h2o洗脱20分钟纯化反应混合物,得到14mg(72%)化合物12。ms(esi)m/z 425[m 2h],848[m h]。
[1184]
实例13:合成化合物13
[1185][1186]
化合物13
‑
2:在0℃下,将6
‑
羟基己酸叔丁酯13
‑
1(1.5g,1.97mmol)、n
‑
羟基邻苯二甲酰亚胺(1.42g,8.76mmol)和三苯膦(2.82g,10.76mmol)溶解于50ml四氢呋喃中,接着加入diad(2ml,9.564mmol)。在室温下搅拌所得溶液过夜,接着浓缩到干燥。通过快速柱色谱纯化残余物,得到2.5g(95%)化合物13
‑
2。
[1187]
化合物13
‑
3:用15ml 4n hcl的二噁烷溶液处理化合物13
‑
2。在环境温度下搅拌反应混合物12小时并在真空中浓缩到干燥,得到900mg(100%)化合物13
‑
3。
[1188]
化合物13
‑
4:向化合物13
‑
3(900mg,3.0mmol)于10ml thf中的溶液中相继加入397mg n
‑
羟基琥珀酰亚胺、669mg dcc。在环境温度下搅拌反应混合物过夜并过滤。浓缩滤液并用10ml dcm处理。使dcm溶液在环境温度下静置1小时并过滤。浓缩滤液并通过快速柱色谱纯化,得到800mg(71%)化合物13
‑
4。
[1189]
化合物13
‑
6:在环境温度下搅拌化合物13
‑
4(435mg,1.16mmol)和val
‑
cit
‑
paboh13
‑
5(400mg,1.054mmol)于12ml dmf中的混合物24小时。在真空中去除溶剂。残余物用乙醚处理、过滤并用乙醚洗涤。在真空中干燥固体,得到660mg(98%)化合物13
‑
6。
[1190]
化合物13
‑
7:向化合物13
‑
6(200mg,0.313mmol)于6ml dmf中的溶液中相继加入双(对硝基苯基)碳酸酯(286mg,0.94mmol)、110.2μl diea。在环境温度下搅拌反应混合物5小时并浓缩。用乙醚处理残余物并过滤。所收集的固体用乙醚、5%柠檬酸、水、乙醚洗涤并且在真空中干燥,得到210mg(83%)化合物13
‑
7。
[1191]
化合物13
‑
9:向单甲基奥利斯坦盐酸盐13
‑
8(100mg,0.1325mmol)于2ml dmf中的溶液中相继加入化合物13
‑
7(159mg,0.2mmol)和10mg hobt以及35.2μl diea。在环境温度下搅拌所得混合物2天。用水稀释反应混合物并且通过hplc纯化,得到93mg(51%)化合物13
‑
9。ms(esi)m/z 692[m 2h],1382[m h]。
[1192]
化合物13:将化合物13
‑
9(50mg,0.036mmol)溶解于1ml dmf中。加入23μl肼。在环境温度下搅拌所得溶液3小时。用1n盐酸溶液淬灭反应物。通过hplc纯化反应混合物,得到32mg(65%)化合物13。ms(esi)m/z 638.5[m na 2h],1253.3[m h],1275.8[m na]。
[1193]
实例14:合成化合物14
[1194]
流程14
[1195][1196]
化合物14
‑
3:向四(乙二醇)14
‑
1(40.6ml,235mmol)于100ml四氢呋喃中的溶液中
加入47mg钠。在钠溶解之后加入12ml丙烯酸叔丁酯。在室温下搅拌反应混合物24小时。在真空中浓缩反应混合物并且用2ml 1n hcl淬灭。将残余物悬浮于盐水中并且用乙酸乙酯(100ml
×
1,50ml
×
2)萃取。合并有机层并用盐水洗涤,经硫酸钠干燥并且在真空中浓缩,得到6.4g(23%)化合物14
‑
3。
[1197]
化合物14
‑
5:在0℃下,将化合物14
‑
3(1.0g,3.12mmol)、n
‑
羟基邻苯二甲酰亚胺14
‑
4(611mg,3.744mmol)和三苯膦(1.23g,4.68mmol)溶解于20ml四氢呋喃中,接着加入diad(0.84ml,4.06mmol)。在室温下搅拌所得溶液过夜,接着浓缩到干燥。通过快速柱色谱,使用siliasep滤筒(80g),用0
‑
100%乙酸乙酯/己烷洗脱来纯化残余物,得到1.0g(100%)化合物14
‑
5。
[1198]
化合物14
‑
6:将化合物14
‑
5溶解于15ml 4n hcl/二噁烷中。在室温下搅拌反应混合物2小时并且在真空中浓缩,得到1.0g化合物14
‑
6。
[1199]
化合物14
‑
7:向化合物6(1.93g,4.68mmol)和n
‑
羟基琥珀酰亚胺(646mg,5.616mmol)于20ml四氢呋喃中的溶液中加入1.062g(5.148mmol)dcc。在室温下搅拌反应混合物过夜并过滤。浓缩滤液并且通过快速柱色谱,使用siliasep滤筒(80g),用0
‑
100%乙酸乙酯/己烷洗脱来纯化,得到2.37g(100%)化合物14
‑
7。
[1200]
化合物14
‑
8:根据文献(生物共轭化学.2002,13(4),855
‑
869)制造化合物14
‑
8。
[1201]
化合物14
‑
9:向化合物14
‑
8(200mg,0.527mmol)于2ml dmf中的溶液中加入295mg(0.58mmol)化合物14
‑
7。在室温下搅拌反应混合物过夜并且在真空中浓缩。用乙醚处理残余物,过滤,用乙醚洗涤并且在真空中干燥,得到402mg(98%)化合物14
‑
9。
[1202]
化合物14
‑
10:向化合物14
‑
9(406mg,0.527mmol)和双(对硝基苯酚)碳酸酯(481mg,1.58mmol)于10ml dmf中的溶液中加入0.186ml(1.054mmol)二异丙基乙胺。在室温下搅拌反应混合物5小时。在真空中去除溶剂。用乙醚处理残余物,过滤,用乙醚、5%柠檬酸、水、乙醚洗涤并且在真空中干燥,得到350mg(72%)化合物14
‑
10。
[1203]
化合物14
‑
11:向50mg(0.062mmol)单甲基海兔毒素盐酸盐、87.2mg(0.093mmol)化合物14
‑
10和4.7mg(0.031mmol)hobt于1ml dmf中的溶液中加入22μl(0.124mmol)二异丙基乙胺。在室温下搅拌反应混合物16小时。通过hplc纯化反应混合物,得到41mg(42%)化合物14
‑
11。ms(esi)m/z 785[m 2h]。
[1204]
化合物14:将化合物14
‑
11(41mg,0.026mmol)溶解于1ml dmf中。加入17μl(0.52mmol)无水肼。在室温下搅拌所得溶液1小时。用1n盐酸溶液淬灭反应物。通过制备型hplc,在254nm下用20
‑
70%ch3cn/h2o洗脱20分钟来纯化反应混合物,得到22mg(58%)化合物14。ms(esi)m/z 720[m 2h]。
[1205]
实例15:合成化合物15
[1206]
流程15
[1207][1208]
化合物15
‑
2:向50mg(0.062mmol)单甲基海兔毒素盐酸盐、75mg(0.093mmol)化合物13
‑
7和4.7mg(0.031mmol)hobt于1ml dmf中的溶液中加入22μl(0.124mmol)二异丙基乙胺。在室温下搅拌反应混合物16小时。通过hplc纯化反应混合物,得到41mg(42%)化合物15
‑
2。ms(esi)m/z 718[m 2h],1435[m h]。
[1209]
化合物15
‑
2:将化合物15
‑
2(41mg,0.026mmol)溶解于1ml dmf中。加入17μl(0.52mmol)无水肼。在室温下搅拌所得溶液1小时。用1n盐酸溶液淬灭反应物。通过制备型hplc,在254nm下用20
‑
70%ch3cn/h2o洗脱20分钟来纯化反应混合物,得到22mg(58%)实例15。ms(esi)m/z 653[m 2h],1305[m h]。
[1210]
实例16:合成化合物16
[1211]
流程16
[1212][1213]
化合物16
‑
3:向乙二醇16
‑
1(13.1ml,235mmol)于100ml四氢呋喃中的溶液中加入47mg钠。在钠溶解之后加入12ml丙烯酸叔丁酯。在室温下搅拌反应混合物24小时。在真空中浓缩反应混合物并且用2ml 1n hcl淬灭。将残余物悬浮于盐水中并且用乙酸乙酯(100ml
×
1,50ml
×
2)萃取。合并有机层并且用盐水洗涤,经硫酸钠干燥并且在真空中浓缩。通过快速柱色谱纯化残余物,得到5.2g(24%)化合物16
‑
3。
[1214]
化合物16
‑
5:在0℃下,将化合物16
‑
3(2.0g,10.5mmol)、n
‑
羟基邻苯二甲酰亚胺(2.05g,12.6mmol)和三苯膦(3.58g,13.65mmol)溶解于50ml四氢呋喃中,接着加入diad
(3.26ml,15.75mmol)。在室温下搅拌所得溶液过夜,接着浓缩到干燥。通过快速柱色谱纯化残余物,得到化合物16
‑
5。
[1215]
化合物16
‑
6:将化合物16
‑
5溶解于15ml 4n hcl/二噁烷中。在室温下搅拌反应混合物2小时并且在真空中浓缩,得到化合物16
‑
6。
[1216]
化合物16
‑
7:向化合物16
‑
6(5.16mmol)和n
‑
羟基琥珀酰亚胺(722mg,6.7mmol)于20ml四氢呋喃中的溶液中加入1.28g(6.2mmol)dcc。在室温下搅拌反应混合物过夜并过滤。浓缩滤液并且通过快速柱色谱纯化,得到500mg化合物16
‑
7。
[1217]
化合物16
‑
8:根据文献(生物共轭化学.2002,13(4),855
‑
869)制造化合物16
‑
8。
[1218]
化合物16
‑
9:向化合物16
‑
8(5.0g,8.3mmol)和双(对硝基苯酚)碳酸酯(7.6g,25mmol)于100ml dmf中的溶液中加入2.92ml(16.6mmol)二异丙基乙胺。在室温下搅拌反应混合物16小时。在真空中去除溶剂。用乙醚处理残余物,过滤,用乙醚、5%柠檬酸、水、乙醚洗涤并且在真空中干燥,得到5.0g(81%)化合物16
‑
9。
[1219]
化合物16
‑
10:向1.0g(1.24mmol)单甲基海兔毒素盐酸盐、1.42g(1.8575mmol)化合物16
‑
9和95mg(0.62mmol)hobt于10ml dmf中的溶液中加入437μl(2.48mmol)二异丙基乙胺。在室温下搅拌反应混合物16小时。通过hplc纯化反应混合物,得到1.0g(58%)化合物16
‑
10。ms(esi)m/z 700[m 2h],1398[m h]。
[1220]
化合物16
‑
11:向化合物16
‑
10(1.0g,0.715mmol)于15ml四氢呋喃中的溶液中加入5ml(48mmol)二乙胺。在室温下搅拌反应混合物1.5小时并且在真空中浓缩。将残余物溶解于20ml dcm中,用200ml乙醚处理并过滤,用乙醚洗涤并且在真空中干燥,得到860mg化合物16
‑
11。ms(esi)m/z 589[m 2h],1176[m h]。
[1221]
化合物16:向50mg(0.0425mmol)化合物16
‑
11于1ml dmf中的溶液中加入32mg(0.085mmol)化合物16
‑
7。在室温下搅拌反应混合物16小时。hplc和ms显示反应完成。向反应混合物中加入27.2μl(0.85mmol)无水肼。2小时内反应完成。用1n hcl酸化反应混合物并且通过hplc纯化,得到40mg(66%)化合物16。ms(esi)m/z 654[m 2h],1307[m h]。
[1222]
实例17:合成化合物17
[1223]
流程17
[1224][1225]
化合物17
‑
2:向化合物17
‑
1(1.0g,4.52mmol)和n
‑
羟基琥珀酰亚胺(572mg,4.97mmol)于20ml四氢呋喃中的溶液中加入1.12g(5.424mmol)dcc。在室温下搅拌反应混合物过夜并过滤。浓缩滤液,得到化合物17
‑
2。
[1226]
化合物17:向50mg(0.0425mmol)化合物16
‑
11于1ml dmf中的溶液中加入41mg(0.1275mmol)化合物17
‑
2。在室温下搅拌反应混合物16小时。hplc和ms显示反应完成。向反应混合物中加入20μl(0.625mmol)无水肼。2小时内反应完成。用1n hcl酸化反应混合物并且通过hplc纯化,得到35mg(60%)化合物17。ms(esi)m/z 625[m 2h],1249[m h]。
[1227]
实例18:合成化合物18
[1228]
流程18
[1229][1230]
化合物18
‑
1:向化合物6
‑
6、mg(0.062mmol)化合物14
‑
10和hobt于1ml dmf中的溶液中加入二异丙基乙胺。在室温下搅拌反应混合物16小时。通过hplc纯化反应混合物,得到化合物18
‑
1。
[1231]
化合物18:将化合物18
‑
1溶解于1ml dmf中。加入无水肼。在室温下搅拌所得溶液1小时。用1n盐酸溶液淬灭反应物。通过制备型hplc,在254nm下用20
‑
70%ch3cn/h2o洗脱20分钟来纯化反应混合物,得到化合物18。
[1232]
实例19:合成化合物19
[1233]
流程19
[1234][1235]
化合物19
‑
2:在0℃下,将2
‑
(2
‑
羟基乙氧基)乙基氨基甲酸叔丁酯13(2.05g,10mmol)、n
‑
羟基邻苯二甲酰亚胺(1.8g,11mmol)和三苯膦(3.67g,14mmol)溶解于100ml四氢呋喃中,接着加入diad(2.48ml,12mmol)。在室温下搅拌所得溶液过夜,接着浓缩到干燥。用50ml 4n hcl/二噁烷处理残余物。在室温下搅拌混合物2小时。在真空中去除溶剂。用乙醚处理残余物,过滤,用乙醚洗涤并且在真空中干燥,得到2.6g(91%)化合物19
‑
2。ms(esi)m/z 251[m h]。
[1236]
化合物19
‑
3:向化合物19
‑
2(315mg,1.1mmol)、boc
‑
lys(boc)
‑
oh(365mg,1mmol)、edc(382mg,2mmol)和hobt(306mg,2mmol)于10ml dcm中的混合物中加入1.056ml(6mmol)二异丙基乙胺。在室温下搅拌反应混合物3小时并且用乙酸乙酯萃取,用5%柠檬酸、饱和碳酸氢钠、盐水洗涤,经硫酸钠干燥,过滤并且在真空中浓缩。通过快速柱色谱,使用siliasep滤筒(40g),用0
‑
100%乙酸乙酯/己烷洗脱来纯化残余物,得到405mg(70%)化合物19
‑
3。
[1237]
化合物19
‑
4:将化合物19
‑
3溶解于15ml 4n hcl/二噁烷中。在室温下搅拌反应混合物2小时并且在真空中浓缩,得到315mg(98%)化合物19
‑
4。ms(esi)m/z 379[m h]。
[1238]
化合物19
‑
5:向化合物14
‑
3(322mg,1mmol)于20ml二氯甲烷中的溶液中加入戴斯
‑
马丁高碘烷(636mg,1.5mmol)。在室温下搅拌反应混合物3小时。用含硫代硫酸钠(1.4g,8.85mmol)的15ml饱和碳酸氢钠溶液淬灭反应物。分离混合物。用饱和碳酸氢钠、盐水洗涤有机层,经硫酸钠干燥,过滤并且在真空中浓缩。通过快速柱色谱,使用siliasep滤筒
(40g),用0
‑
100%乙酸乙酯/己烷洗脱来纯化残余物,得到170mg(53%)化合物19
‑
5。
[1239]
化合物19
‑
6:向单甲基海兔毒素盐酸盐1.0g(1.24mmol)于20ml dmf中的溶液中相继加入1.19g(3.72mmol)化合物17、1.4ml(24.8mmol)乙酸和156mg(2.48mmol)氰基硼氢化钠。在室温下搅拌所得混合物2小时。在真空中去除溶剂。通过碳酸氢钠将残余物调节到ph 8并且用dcm萃取,用盐水洗涤,经硫酸钠干燥,过滤并且在真空中浓缩。通过快速柱色谱,使用siliasep滤筒(40g),用0
‑
5%甲醇/dcm洗脱来纯化残余物,得到680mg(51%)化合物19
‑
6。ms(esi)m/z 538[m 2h],1075[m h]。
[1240]
化合物19
‑
7:向化合物19
‑
6(680mg,0.632mmol)于5ml dcm中的溶液中加入20ml 4n hcl/二噁烷。在室温下搅拌反应混合物2小时并且在真空中浓缩。用乙醚处理残余物,过滤,用乙醚洗涤并且在真空中干燥,得到660mg(98%)化合物19
‑
7。ms(esi)m/z 510[m 2h],1019[m h]。
[1241]
化合物19
‑
8:向化合物19
‑
7(280mg,0.257mmol)、化合物19
‑
4(38mg,0.0857mmol)和n
‑
甲基吗啉(0.283ml,2.57mmol)于5ml n
‑
甲基吡咯烷酮中的溶液中加入98mg(0.257mmol)hatu。在室温下搅拌反应混合物1小时。通过hplc纯化反应混合物,得到160mg(71%)化合物19
‑
8。ms(esi)m/z 596[m 4h],794[m 3h],1191[m 2h]。
[1242]
化合物19:将化合物19
‑
8(160mg,0.0613mmol)溶解于1.5ml dmf中。加入20μl(0.613mmol)无水肼。在室温下搅拌所得溶液1小时。用1n盐酸溶液淬灭反应物。通过制备型hplc,在254nm下用20
‑
70%ch3cn/h2o洗脱20分钟来纯化反应混合物,得到120mg(75%)化合物19。ms(esi)m/z 451[m 5h],563[m 4h],751[m 3h],1126[m 2h]。
[1243]
实例20:合成化合物20
[1244]
流程20
[1245][1246]
化合物20
‑
2:在0℃下,向四(乙二醇)20
‑
1(8.0g,41.2mmol)于100ml四氢呋喃中的溶液中加入1.65g氢化钠。在室温下搅拌反应混合物30分钟。向此溶液中加入6.21g tbs
‑
cl。在室温下搅拌反应混合物过夜。在真空中浓缩反应混合物并且用2ml 1n hcl淬灭。将残余物悬浮于盐水中并且用乙酸乙酯(100ml
×
1,50ml
×
2)萃取。合并有机层并且用盐水洗涤,经硫酸钠干燥并且在真空中浓缩。通过快速柱色谱纯化残余物,得到5.7g化合物20
‑
2。
[1247]
化合物20
‑
3:向化合物20
‑
2(500mg,1.62mmol)于30ml二氯甲烷中的溶液中加入戴斯
‑
马丁高碘烷(1.03g,2.43mmol)。在室温下搅拌反应混合物3小时。用含硫代硫酸钠(1.4g,8.85mmol)的15ml饱和碳酸氢钠溶液淬灭反应物。分离混合物。用饱和碳酸氢钠、盐水洗涤有机层,经硫酸钠干燥,过滤并且在真空中浓缩。通过快速柱色谱纯化残余物,得到400mg化合物20
‑
3。
[1248]
化合物20
‑
4:向单甲基海兔毒素盐酸盐213mg(0.263mmol)于4ml dmf中的溶液中相继加入245mg(0.75mmol)化合物20
‑
3、0.303ml(5mmol)乙酸和34mg(0.5mmol)氰基硼氢化钠。在室温下搅拌所得混合物2小时。在真空中去除溶剂。在0℃下,相继加入3ml 60%乙腈、0.2ml hf.吡啶。在室温下搅拌所得溶液2小时。在真空中去除有机溶剂。通过碳酸氢钠将残
余物调整到ph 8并且用dcm萃取,用盐水洗涤,经硫酸钠干燥,过滤并且在真空中浓缩。通过快速柱色谱纯化残余物,得到160mg化合物20
‑
4。ms(esi)m/z 474[m 2h],947[m h]。
[1249]
化合物20
‑
5:在0℃下,向化合物20
‑
4(50mg,0.062mmol)于4ml dcm中的溶液中加入0.3ml光气/甲苯。在0℃下搅拌反应混合物3小时并且在真空中浓缩,不经纯化即用于下一步骤。
[1250]
化合物20
‑
6:向化合物19
‑
4(7.6mg,0.017mmol)和化合物20
‑
5(0.062mmol)的溶液中加入25μl二异丙基乙胺。在室温下搅拌反应混合物1小时。通过hplc,在254nm下用20
‑
70%ch3cn/h2o洗脱20分钟来纯化反应混合物,得到33mg化合物20
‑
6。ms(esi)m/z 582[m 4h],775[m 3h],1163[m 2h]。
[1251]
化合物20:将化合物20
‑
6(33mg,0.014mmol)溶解于1ml dmf中。加入14μl(0.43mmol)无水肼。在室温下搅拌所得溶液1小时。用1n盐酸溶液淬灭反应物。通过制备型hplc,在254nm下用20
‑
70%ch3cn/h2o洗脱20分钟来纯化反应混合物,得到10mg化合物20。ms(esi)m/z 549[m 4h],732[m 3h],1098[m 2h]。
[1252]
实例21:合成化合物21
[1253]
流程21
[1254]
[1255]
化合物21
‑
2:使n,n'
‑
二亚甲基二胺21
‑
1(5ml,46.5mmol)和丙烯酸叔丁酯13ml(116mmol)的混合物在85℃下加热1小时。再加入13ml(116mmol)丙烯酸叔丁酯。使反应混合物在85℃下连续加热1小时并且在室温下搅拌过夜。在真空中浓缩反应混合物。用己烷稀释残余物并且通过快速柱色谱,使用siliasep滤筒(120g),用0
‑
5%甲醇/dcm洗脱来纯化,得到10.1g(62%)化合物21
‑
2。ms(esi)m/z 345[m h]。
[1256]
化合物21
‑
3:向化合物21
‑
2(5.0g,14.5mmol)于50ml dcm中的溶液中加入40ml 4n hcl/二噁烷。在室温下搅拌反应混合物2天并且在真空中浓缩。用乙醚处理残余物,过滤,用乙醚洗涤并且在真空中干燥,得到4.3g(97%)化合物21
‑
3。
[1257]
化合物21
‑
4:向166mg(0.544mmol)化合物21
‑
3和0.15ml n
‑
甲基吗啉于10ml n
‑
甲基吡咯烷酮中的溶液中相继加入160mg化合物16
‑
11、0.068ml(0.408mmol)decp。在室温下搅拌反应混合物1小时。通过制备型hplc,在254nm下用35
‑
70%ch3cn/h2o洗脱20分钟来纯化反应混合物,得到100mg(50%)化合物21
‑
4。ms(esi)m/z 464[m 3h],696[m 2h],1391[m h]。
[1258]
化合物21
‑
5:向化合物19
‑
4(11mg,0.025mmol)、化合物21
‑
4(115mg,0.077mmol)和n
‑
甲基吗啉(0.028ml,0.25mmol)于1.5ml n
‑
甲基吡咯烷酮中的溶液中加入29.3mg(0.077mmol)hatu。在室温下搅拌反应混合物1小时。通过hplc,在254nm下用20
‑
70%ch3cn/h2o洗脱20分钟来纯化反应混合物,得到60mg(67%)化合物21
‑
5。ms(esi)m/z 625[m 5h],781[m 4h],1041[m 3h]。
[1259]
化合物21:将化合物21
‑
5(60mg,0.014mmol)溶解于1ml dmf中。加入7μl(0.21mmol)无水肼。在室温下搅拌所得溶液1小时。用1n盐酸溶液淬灭反应物。通过制备型hplc,在254nm下用20
‑
70%ch3cn/h2o洗脱20分钟来纯化反应混合物,得到29mg(58%)化合物21。ms(esi)m/z 599[m 5h],749[m 4h],998[m 3h]。
[1260]
实例22:合成化合物22
[1261]
流程22
[1262][1263]
化合物22
‑
1:向化合物19
‑
4(7.6mg,0.017mmol)、化合物12
‑
7(40mg,0.051mmol)和diea(0.030ml,0.17mmol)于2ml dmf中的溶液中加入32mg(0.085mmol)hatu。在室温下搅拌反应混合物2小时。通过hplc,在254nm下用20
‑
70%ch3cn/h2o洗脱20分钟来纯化反应混合物,得到24mg(68%)化合物22
‑
1。ms(esi)m/z 612[m 3h],917[m 2h],1834[m h]。
[1264]
化合物22:将化合物22
‑
1(24mg,0.012mmol)溶解于1ml dmf中。加入12μl(0.36mmol)无水肼。在室温下搅拌所得溶液1小时。用1n盐酸溶液淬灭反应物。通过制备型hplc,在254nm下用20
‑
70%ch3cn/h2o洗脱20分钟来纯化反应混合物,得到15mg(58%)实例21。ms(esi)m/z 569[m 3h],852[m 2h],1726[m 2h]。
[1265]
实例23:合成化合物23
[1266]
流程23
497[m 2h],993[m h]。
[1273]
化合物23
‑
6:向化合物19
‑
4(7.6mg,0.017mmol)、化合物23
‑
6(52mg,0.051mmol)和diea(0.030ml,0.17mmol)于2ml dmf中的溶液中加入32mg(0.085mmol)hatu。在室温下搅拌反应混合物2小时。通过hplc,在254nm下用20
‑
70%ch3cn/h2o洗脱20分钟来纯化反应混合物,得到26mg(61%)化合物23
‑
6。ms(esi)m/z 583[m 4h],777[m 3h],1165[m 2h]。
[1274]
化合物23:将化合物23
‑
6(26mg,0.01mmol)溶解于1ml dmf中。加入10μl(0.31mmol)无水肼。在室温下搅拌所得溶液1小时。用1n盐酸溶液淬灭反应物。通过制备型hplc,在254nm下用20
‑
70%ch3cn/h2o洗脱20分钟来纯化反应混合物,得到10mg(40%)实例23。ms(esi)m/z 550[m 4h],733[m 3h],1100[m 2h]。
[1275]
表1.化合物1
‑
23的结构
[1276]
[1277]
[1278]
[1279][1280]
实例24:结合到her2受体的her
‑
tox的分析
[1281]
将her2
‑
fc固定在cm5芯片上达到约280ru的密度。用hbs
‑
ep作为缓冲液将流速调整到50μl/min。注射hertox变体持续3分钟,其中有15个解离阶段。30秒20mm hcl的脉冲用于再生。利用二价分析物模型来拟合数据(图1)。数据分析指示hertox ha121
‑
nc2d:kd约60pm(chi2=4)和hertox ha121
‑
nc1d:kd约300pm(chi2=14)。
[1282]
实例25:瞬时转染
[1283]
转染前约16小时将cho
‑
s培养物以0.75
×
106个/毫升接种于freestyle cho培养基中。当细胞计数已达到1.4
‑
1.6
×
106个/毫升时,细胞准备好次日转染。当细胞达到目标计数时,将400mm paf储备液加入到1.4mm最终培养物浓度。如下所述制备pei/dna复合物:将dna(1.42微克/1
×
106个细胞)溶解于rpmi(总培养物体积的5%(v/v))中,将dna/rpmi混合物在室温下孵育2分钟,将pei储备液(1mg/ml)以3:1比率(ml pei/μg dna)加入dna溶液中,并且将混合物在室温下孵育5分钟。将培养物轻轻加入混合物中并且涡旋。将烧瓶转移到32℃孵育箱。在转染后第6天,进行西方印迹分析(western blot analysis)。在转染后第7天,收集上清液。
[1284]
实例26:抗her2变体表达测试
[1285]
使用freestyle培养基中的30ml振荡器培养物cho
‑
s、含56μg dna的pei试剂。还使用1.5mm paf。在第6天,收集上清液。通过fc elisa测定滴度。(图2和3)
[1286]
实例27:体外抑制增殖分析
[1287]
在第1天,接种细胞。吸出培养基,并且用30ml pbs
‑
/冲洗细胞的t
‑
225培养烧瓶。吸出pbs,并且将6ml 0.25%胰蛋白酶
‑
edta加入每个烧瓶中。将烧瓶在37℃、5%co2下孵育2
‑
5分钟。通过击打烧瓶来移出附着性细胞,并且通过加入14ml培养基来中和胰蛋白酶。将细胞悬浮液混合并且转移到50ml锥形管中。细胞在室温下以1200rpm旋转下降5分钟。将所得细胞沉淀再悬浮于12ml培养基中。在血细胞计数器中计数细胞。细胞以适当细胞密度接种到96孔平底透明板中并且在37℃、5%co2下孵育过夜以允许细胞附着。接种体积是80微升/孔。将80微升/孔培养基用作“无细胞”对照。
[1288]
细胞接种密度实例包括:
[1289]
bt474(高her2)
‑
20,000个细胞/孔于f12k/dmem(50/50)、10%fbs、p/s中
[1290]
mda
‑
mb
‑
468(her2阴性)
‑
6,000个细胞/孔于f12k/dmem(50/50)、10%fbs、p/s中
[1291]
hcc1954
‑
5,000个细胞/孔于rpmi 1640、10%fbs、p/s中
[1292]
skov
‑3‑
6,000个细胞/孔于rpmi 1640、10%fbs、p/s中
[1293]
ht29
‑
20,000个细胞/孔于麦克考伊氏5a(mccoy's 5a)、10%fbs、p/s中
[1294]
在第2天,将测试样品加入细胞中。在圆底96孔板的第2列中将测试样品在培养基中稀释到9
×
储备液浓度。用多通道移液器从第2列到第11列制得3
×
连续稀释液。将10微升/孔的以上样品一式两份地加入接种板的适当孔中。孔中的总体积是约90微升/孔。加入10微升/孔的培养基以避免样品孔的边缘效应。内部孔中包括未加入样品(仅10微升/孔培养基)的欲用于增殖计算的培养基对照孔。将板在37℃、5%co2下孵育72小时。
[1295]
在第5天,进行增殖读数。为了检测细胞增殖,将10微升/孔的wst
‑
8试剂加入(细胞计数试剂盒
‑
8(cell counting kit
‑
8),目录号ck04
‑
20,同仁实验室(dojindo labs))所有孔中。将板在37℃、5%co2下孵育4小时。在od 450nm下针对吸光度对板进行测量。计算测试样品的增殖抑制:从所有孔的od450值中减去“无细胞对照”od450值;计算培养基对照(未经处理的)孔的平均值;使用下式计算每个样品的培养基对照值%:(od450样品/od450平均培养基对照%)
×
100;计算每个样品的一式两份的培养基对照值%的平均值、标准偏差和cv%;将每个样品平均培养基对照值%针对样品浓度作图;使用4参数逻辑拟合回归分析(logistic fit regression analysis)计算ic50值以测定测试样品的效力。
[1296]
图4和图5说明来自使用海兔毒素连接基团衍生物和乳癌系hcc1954(her2 )的体外增殖分析的结果。图6和7说明来自使用海兔毒素连接基团衍生物和卵巢癌系skov
‑
3(her2 )的体外增殖分析的结果。图8和9说明来自使用海兔毒素连接基团衍生物和乳癌系mds
‑
mb
‑
468(her2阴性)的体外增殖分析的结果。
[1297]
表2.her
‑
tox增殖分析汇总:72小时药物处理之后的ic
50
值[nm]
[1298][1299]
river laboratories)。将hcc1954细胞(人类,乳癌,atcc,#crl
‑
2338)与matrigel(马萨诸塞州贝德福德bd生物科学(bd biosciences,bedford ma))1:1混合并且皮下注射到小鼠中。当肿瘤达到100
‑
200mm3的平均大小时,将小鼠分选到每组9
‑
10只小鼠的组中。每周两次进行卡尺测量直到研究结束为止。为了估算肿瘤体积,用卡尺测量两个正交直径并且将值输入下式:(l
×
w
×
w)/2=v,(其中w=最短直径,l=最长直径并且v=体积),从而获得估算的体积。在excel数据文件中通过假定1mm3=1mg而将肿瘤体积转化成肿瘤重量。端点是基于肿瘤生长抑制(tgi)的研究设计。当对照组的平均肿瘤体积达到约1,000mm3时或第28天(无论何者在先),使所有小鼠安乐死。
[1306]
在给药的第1天给予小鼠单次静脉内注射(尾静脉)。将测试物品以4mg/ml、2mg/ml和0.66mg/ml溶解,并且以5ml/kg的剂量体积投与以传递20mg/kg、10mg/kg和3.3mg/kg。测试物品是:临床级(曲妥珠单抗)、her2
‑
hs122
‑
ncd1(抗体:药物比=1:2,不可裂解的连接基团)和her2
‑
hs122/lk145
‑
hcd1(抗体:药物比=1:4,可裂解的连接基团)参见图16。
[1307]
实例29:her2
‑
海兔毒素连接的衍生物的体内研究
[1308]
将hcc1954细胞用于此研究,其中将含107个细胞/小鼠的matrigel皮下注射于右侧腹。小鼠是4
‑
8周的雌性scid
‑
bg。在细胞植入后第5天(肿瘤约100mm3)进行分组:分成11组,每组10只小鼠。在给药的第1天用每个化合物以3个剂量水平(20mg/kg、10mg/kg和3.3mg/kg)给予单次静脉内剂量。监测肿瘤体积直到达到端点(1,000mm3或60天)为止。(图10)将太平洋紫杉醇(25mg/kg,静脉内,qod
×
5)用作对照化学疗法。媒剂=50mm组胺、0.1m nacl、5%海藻糖,ph 6。测试临床级(曲妥珠单抗)、her2
‑
hs122
‑
ncd1(不可裂解的连接基团)和her2
‑
hs122/lk145
‑
hcd1(可裂解的连接基团)。(图11和12)
[1309]
表4.在第28天针对hcc1954研究计算t/c(经处理/对照)
[1310][1311]
实例30:药物动力学研究
[1312]
进行检测结合到erbb2受体的抗体的分析。(图13)进行检测连接到抗体的至少两个海兔毒素的分析(图14)。
[1313]
图15。
[1314]
实例31:针对乳癌的治疗
[1315]
用于乳癌疗法的曲妥珠单抗连接的海兔毒素衍生物的安全性和/或功效的人类临
床试验
[1316]
目的:为了比较所投与的包含曲妥珠单抗连接的海兔毒素衍生物的组合物的安全性和药物动力学。
[1317]
研究设计:此研究将是在乳癌患者中相继进行的i期、单一中心、开放标记、随机化剂量增加研究和ii期研究。患者在研究登记之前不应暴露于曲妥珠单抗连接的海兔毒素衍生物。患者在开始试验的2周内不能接受针对其癌症的治疗。治疗包括使用化学疗法、造血生长因子和生物疗法(如单克隆抗体)。患者必须已从与先前治疗相关的所有毒性恢复(达到0级或1级)。针对安全性评估所有个体,并且如期收集用于药物动力学分析的所有血液收集物。所有研究均在机构伦理委员会批准和患者同意的情况下进行。
[1318]
i期:患者在每个28天周期的第1天、第8天和第15天静脉内接受曲妥珠单抗连接的海兔毒素衍生物。曲妥珠单抗连接的海兔毒素衍生物的剂量可基于如下汇总的评估针对毒性保持或修改。治疗在不存在不可接受的毒性的情况下每28天重复。3
‑
6个患者的群组接受增加剂量的曲妥珠单抗连接的海兔毒素衍生物直到测定曲妥珠单抗连接的海兔毒素衍生物的最大耐受剂量(mtd)为止。mtd被定义为3个患者中的2个或6个患者中的2个经历剂量限制性毒性之前的剂量。剂量限制性毒性根据由国家癌症研究所(national cancer institute;nci)通用不良事件术语(common terminology for adverse events;ctcae)第3.0版(2006年8月9日)设定的定义和标准测定。
[1319]
ii期:患者以i期中测定的mtd如在i期中般接受曲妥珠单抗连接的海兔毒素衍生物。治疗在不存在疾病进展或不可接受的毒性的情况下每4周重复持续2
‑
6个疗程。在完成2个疗程的研究疗法之后,实现完全或部分反应的患者可再接受4个疗程。在完成6个疗程的研究疗法之后维持稳定疾病超过2个月的患者可在疾病进展时再接受6个疗程,只要其满足原始资格准则即可。
[1320]
血液采样在投与曲妥珠单抗连接的海兔毒素衍生物之前和之后,通过直接静脉穿刺抽取连续血液。在给药前约10分钟和在给药后的大致以下时间:第1天、第8天和第15天,获得用于测定血清浓度的静脉血样品(5ml)。每个血清样品分成两个等分试样。所有血清样品均储存在
‑
20℃下。血清样品在干冰上运输。
[1321]
药物动力学:患者在开始治疗之前和在第1天、第8天和第15天经历血浆/血清样品收集以用于药物动力学评估。药物动力学参数通过模型无关的方法在数字设备公司(digital equipment corporation)vax 8600计算机系统上使用最新版本的bioavl软件进行计算。测定以下药物动力学参数:峰值血清浓度(c
max
);达到峰值血清浓度的时间(t
max
);借助于线性梯形法则计算的从时间零点到最后血液采样时间(auc0‑
72
)的浓度
‑
时间曲线下区域(auc);和由消除速度常数计算的终末消除半衰期(t
1/2
)。消除速度常数通过对数
‑
线性浓度
‑
时间图的末端线性区域中的连续数据点的线性回归进行估算。针对每个治疗计算药物动力学参数的平均值、标准偏差(sd)和变异系数(cv)。计算参数平均值(保存的调配物/非保存的调配物)的比率。
[1322]
患者对组合疗法的反应:患者反应通过用x射线、ct扫描和mri来评估,并且在研究开始之前和在第一周期结束时进行成像,并且每四周或在后续周期结束时再进行成像。成像模态基于癌症类型和可行性/可利用性选择,并且针对相似癌症类型以及贯穿每个患者的研究疗程始终使用相同的成像模态。反应率使用recist准则测定。(特拉萨(therasse)等
人,美国国立癌症研究所杂志(j.natl.cancer inst.)2000年2月2日;92(3):205
‑
16;http://ctep.cancer.gov/forms/therasserecistjnci.pdf)。患者还经历癌症/肿瘤活检,从而通过流式细胞术、西方印迹法和ihc评估祖代癌细胞表型的变化和克隆源性生长并且通过fish评估细胞遗传学的变化。在完成研究治疗之后,周期性跟踪患者持续4周。
[1323]
实例32:针对乳癌的治疗
[1324]
用于乳癌疗法的曲妥珠单抗连接的海兔毒素衍生物的安全性和功效的人类临床试验
[1325]
目的:在患有her2过度表达性转移性乳癌的女性中通过组合曲妥珠单抗和太平洋紫杉醇相对于第一线组合曲妥珠单抗和太平洋紫杉醇来比较在疾病进展时跟踪的单独曲妥珠单抗连接的海兔毒素衍生物的功效和毒性。
[1326]
研究设计:此研究是随机化的多中心研究。根据以下各项对患者进行分级:her2/neu
‑
过度表达程度(2 相对于3 )、先前含蒽环霉素的辅助治疗(无先前治疗相对于不伴有对左侧胸壁的放射疗法的先前治疗相对于伴有对左侧胸壁的放射疗法的先前治疗)、雌激素受体状态(阳性相对于阴性相对于未知)、先前疗法(第一线相对于第二/第三线)和中心。将患者随机分到两个治疗组中的一个中。组i:患者每周在30
‑
90分钟内接受曲妥珠单抗连接的海兔毒素衍生物。在疾病进展时,患者如组ii中般接受组合曲妥珠单抗连接的海兔毒素衍生物(静脉内)和太平洋紫杉醇(静脉内)。组ii:患者每周在30
‑
90分钟内接受曲妥珠单抗连接的海兔毒素衍生物。太平洋紫杉醇每周在1小时内静脉内投与,持续3周,随后休息1周。
[1327]
治疗在不存在疾病进展或不可接受的毒性的情况下在两个组中持续。在第2疗程、第3疗程、第4疗程、第5疗程、第6疗程、第8疗程、第10疗程和第12疗程的基线和第1天评估生活质量。在1个月、3个月和6个月并且接着此后每6个月跟踪患者。
[1328]
实例33:针对膀胱癌的治疗
[1329]
目的:在已经历针对膀胱的肌肉侵袭性移行细胞癌的先前经尿道膀胱切除术的患者中在使用或不使用本文所描述的海兔毒素衍生物的情况下测定太平洋紫杉醇和放射疗法的急性毒性。
[1330]
疾病特征:组织学上或细胞学上证实是膀胱的原发性移行细胞癌(tcc);固有肌层侵袭的组织迹象;满足以下阶段准则中的1个:阶段t2
‑
4a;nx、n0或n1;和m0疾病或临床阶段t1,3/3级疾病并且需要确定的局部疗法;允许尿道前列腺部的肿瘤涉及,只要满足以下准则即可:肿瘤明显被完全切除;无前列腺基质侵袭迹象,通过胸部x射线或ct扫描和腹部/骨盆ct扫描无远端转移迹象;在过去的3
‑
8周内已经历经尿道的膀胱切除术(如判断安全可能般彻底),包括使用肿瘤测绘的双手检查;对于her2/neu分析足够可利用的肿瘤组织;并非根治性膀胱切除术的候选人。
[1331]
研究设计:此研究是非随机化的多中心研究。根据her2/neu状态将患者分配到2个治疗组中的1个中(her2/neu 2 或3 染色[第1组]相对于her2/neu 0或1 染色[第2组])。
[1332]
第1组:患者在第1天、第8天、第15天、第22天、第29天、第36天和第43天在1小时内静脉内接受太平洋紫杉醇,并且在第1天在90分钟内并且接着在第8天、第15天、第22天、第29天、第36天和第43天在30分钟内静脉内接受本文所描述的海兔毒素衍生物。患者还在第1
‑
5天、第8
‑
12天、第15
‑
19天、第22
‑
26天、第29
‑
33天、第36
‑
40天、第43
‑
47天和第50天每日
经历放射疗法一次。治疗在不存在疾病进展或不可接受的毒性的情况下持续。
[1333]
第2组:患者如在第1组中般接受太平洋紫杉醇并且经历放射疗法。在完成研究治疗之后,在4
‑
5周、每3个月持续1年、每4个月持续1年、每6个月持续3年、接着此后每年地跟踪患者。
[1334]
实例34:针对卵巢癌的治疗
[1335]
针对卵巢癌疗法的本文所述的海兔毒素衍生物的安全性和功效的人类临床试验
[1336]
目的:在患有her2过度表达性卵巢癌的女性中评估包含本文所述的海兔毒素衍生物的组合物的四周(每周一次)静脉内剂量的安全性和功效。
[1337]
研究设计:此研究是非随机化、开放标记、11周、多中心研究。此研究将评估曲妥珠单抗连接的海兔毒素衍生物的四个每周一次的静脉内剂量的安全概況、mtd、pk和免疫原性。将患者分配到单一组中。患者每周一次接受一个剂量的曲妥珠单抗连接的海兔毒素衍生物,持续4周。曲妥珠单抗连接的海兔毒素衍生物将在研究第1天、第8天、第15天和第22天通过静脉内输注投与。将在第1天和第22天采集尿样品。
[1338]
血液采样在投与海兔毒素衍生物之前和之后,通过直接静脉穿刺抽取连续血液。在给药前约10分钟和在给药后的大致以下时间:第1天、第2天、第4天、第5天、第8天、第15天、第22天、第36天、第43天和第50天,获得用于测定血清浓度的静脉血样品(5ml)。每个血清样品分成两个等分试样。所有血清样品均储存在
‑
20℃下。血清样品在干冰上运输。
[1339]
治疗在不存在疾病进展或不可接受的毒性的情况下持续。在第2疗程、第3疗程、第4疗程、第5疗程、第6疗程、第8疗程、第10疗程和第12疗程的基线和第1天评估生活质量。在第29天、第36天、第43天和第50天跟踪患者。患者将被问及不良事件。患者将进行成像扫描和ecg以评估肿瘤大小和心脏功能(第43天)。在研究结束时,患者将进行身体检查(第50天)。具有疾病消退迹象的患者可继续接受疗法直到记录疾病进展的迹象为止。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。

