一种具有aie特性且克服缺氧的光敏剂及其制备方法与应用
技术领域
1.本发明涉及肿瘤治疗技术领域,尤其涉及荧光成像引导的光动力疗法技术。
背景技术:
2.荧光成像引导的光动力疗法(pdt)由于具有较高的时空分辨率、微创手术等优点,有望在未来的肿瘤精确治疗中发挥重要作用。作为pdt的重要组成部分,光敏剂(pss)应具有生物相容性好、光毒性大、亮度高、发射波长长等优良特性。目前,越来越多的有机pss被报道成为抑制肿瘤增殖的有效药物。但随之而来的问题,如荧光聚集引起的猝灭(acq)效应和肿瘤微环境缺氧,导致荧光成像引导的pdt可视化差,疗效降低。具有先进的聚集诱导发射(aie)特性的荧光团在聚集时发出明亮的荧光,但在溶液中荧光很弱或消失,这为解决acq问题提供了很好的启发。近年来,新发现了具有独特aie特性的pss可以用作新的荧光成像引导的pdt,特别是明确指导设计aie活性pss的分子方法,具有独特aie特性的pss在提供丰富的高亮度pss方面发挥了重要作用。然而,大多数报道的aie活性pss在光触发后产生ii单线态氧(1o2),也就是说需要足够的氧气来支持pdt中的1o2的产生。遗憾的是,癌细胞的异常增殖和凋亡以及扭曲的肿瘤血管导致严重的肿瘤缺氧,这已经成为许多抗肿瘤方案限制治疗结果的重要因素之一。虽然已经提出了许多新的增氧方案,如高压氧、肿瘤自补氧系统,但仍不能取得满意的效果,甚至常常产生不良的副作用,创造低氧依赖性的pss更有希望克服肿瘤缺氧。
3.如图1a所示,ros(reactive oxygen species活性氧)可以明确地分为两类,一种是能量转移到o2,产生type ii 1
o2,另一种是电子转移获得type
ⅰꢀ
ros,如自由基(oh
·
和1o2‑
·
)和过氧化氢(h2o2)。通常,typeⅰros被认为是pdt中毒性最强的氧化剂,它可以引发复杂的歧化反应形成o2,使o2在这些级联生物反应中可循环利用,这对提高抗缺氧性能具有重要意义。目前,大多数产生i型ros的光敏剂都是含金属的配合物(e.g,tio
2 and zno),生物降解性差,且可能产生副作用。酞菁类、氯类和二苯并噻嗪类等有机材料在生理环境下荧光效率较差,因为它们的疏水刚性结构通常会导致acq问题。除此之外,在传统pss中,严重的聚集导致ros生成能力减弱,导致pdt结果不理想。近年来,如图1b所示,新型激活型pss因其强大的固体荧光和较好的pdt效率而受到越来越多的关注。丰富的aie活性i型pss材料体系有利于开发荧光成像引导肿瘤pdt治疗的发展。在i型光敏剂中引入aie特性来获得明亮的光敏剂,可以同时抑制acq效应和肿瘤缺氧。然而,由于在这两个紧密竞争的过程中,ii型过程占主导地位,具有aie性质的i型pss的可行分子策略很少。
4.结构
‑
性质关系研究对于创造新材料非常重要。我们认为,在含有重原子的富电子aie材料中增强分子内电荷转移(ict)效应对于设计明亮的i型光敏剂至关重要。吩噻嗪(phe)作为一种富电子分子核,含有重原子(s和n),据前期研究,由于其蝶状结构,通常被用于设计具有独特aie性质和良好生物相容性的高亮度荧光团。phe基发光体在光催化剂、有机光发射二极管、压致变色材料中都具有很好的应用潜力。除了这些应用外,由于典型的重原子效应,phe有望作为一种潜在的分子骨架用于设计具有aie活性pss,以促进系统间的交
叉过程,从而提高三重态能量。
技术实现要素:
5.本发明的目的在于提供一种具有aie特性且克服缺氧的光敏剂及其制备方法与应用,以解决现有技术中光敏剂聚集诱导猝灭效应(acq)和肿瘤缺氧微环境导致荧光成像能力差、疗效低等问题。
6.为了达到上述目的本发明采用如下技术方案:
7.一种具有aie特性且克服缺氧的光敏剂,通式如下:
[0008][0009]
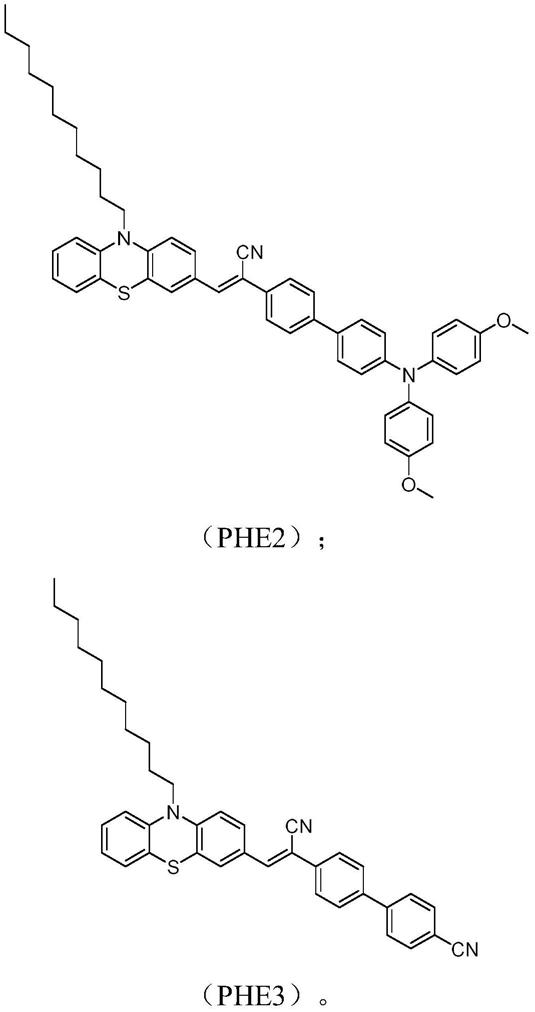
进一步地,通式(ⅰ)选自如下结构:
[0010]
[0011][0012]
一种具有aie特性且克服缺氧的光敏剂的制备方法,步骤包括:将nah加入到含吩噻嗪的二甲基甲酰胺溶液中,在n2条件下搅拌,将1
‑
溴癸烷的二甲基甲酰胺溶液加入并搅拌;加入pocl3和clch2ch2cl进行反应,最后淬灭反应,萃取所得混合物,得到化合物1;
[0013]
将化合物1和苯乙腈溶于无水乙醇中;在无水乙醇中加入几滴tba h溶液,回流;反应后冷却,析出固体粉末;过滤并在乙醇中重结晶得到粗产物,得到phe1。
[0014]
一种具有aie特性且克服缺氧的光敏剂的制备方法,步骤包括:将nah加入到含吩噻嗪的二甲基甲酰胺溶液中,在n2条件下搅拌,将1
‑
溴癸烷的二甲基甲酰胺溶液加入并搅拌;加入pocl3和clch2ch2cl进行反应,最后淬灭反应,萃取混合物,得到化合物1;
[0015]
将化合物1和4
‑
溴苯乙腈溶于无水乙醇中;在上述乙醇中加入几滴tba h溶液,回流;反应后冷却至室温,析出一些固体粉末;过滤、在乙醇中重结晶得到粗产物;过滤得到化合物2;
[0016]
将4
‑
(二苯氨基)苯硼酸,化合物2和pd(pph3)4溶解在干燥的脱气thf溶剂中;将k2co3水溶液注入上述thf中并回流反应;在n2环境下反应,将混合物冷却后,淬灭反应;萃取混合物,得到phe2。
[0017]
一种具有aie特性且克服缺氧的光敏剂的制备方法,步骤包括:将nah加入到含吩噻嗪的二甲基甲酰胺溶液中,在n2条件下搅拌,将1
‑
溴癸烷的二甲基甲酰胺溶液加入并搅拌;加入pocl3和clch2ch2cl进行反应,最后淬灭反应,萃取混合物,得到化合物1;
[0018]
将化合物1和4
‑
溴苯乙腈溶于无水乙醇中,在上述乙醇中加入几滴tba h溶液,回流一夜;反应后冷却至室温,析出一些固体粉末;过滤、在乙醇中重结晶得到粗产物;过滤,得到化合物2;
[0019]
将4
‑
氰基苯硼酸,化合物2和pd(pph3)4溶解在干燥的脱气thf溶剂中;将k2co3水溶液注入上述thf中并回流;在n2下进行;将混合物冷却后,淬灭反应;萃取混合物,得到phe3。
[0020]
一种具有aie特性且克服缺氧的光敏剂在制备治疗肿瘤药物中的应用。
[0021]
本发明与现有技术相比具有以下优点:
[0022]
通过一种可行的分子工程设计出能产生i型ros的aie光敏剂,它在产生i型ros的过程中具有明亮的聚集荧光特性和低的o2依赖性。在这个含有典型重原子的具有aie性质的富电子分子中,当频繁增强分子内电荷转移(ict)效应时,系间交叉(isc)通道被激活,从而确保产生足够的三重态能量来产生i型ros。体外荧光成像和光毒性评价均表明,本发明提供的新型aie光敏剂是一种很有应用前景的荧光成像引导光动力疗法候选材料。
附图说明
[0023]
图1a.现有技术有机pss中ros的产生机制;
[0024]
图1b.最近报道的i型pss的化学结构;
[0025]
图2.用b3lyp/6
‑
31g(d,p)水平计算phe1
‑
3的化学结构及其在前沿轨道上的电子分布结构图;
[0026]
图3a.phe1
‑
3的紫外
‑
可见吸收光谱;
[0027]
图3b.phe1
‑
3在thf溶液中的荧光光谱(10
‑
5m);
[0028]
图4a.基态phe1在具有不同极性的不同溶剂中的吸收光谱;
[0029]
图4b.基态phe2在具有不同极性的不同溶剂中的吸收光谱;
[0030]
图4c.基态phe3在具有不同极性的不同溶剂中的吸收光谱;
[0031]
图5a.激发态phe1在不同极性有机溶剂中的荧光光谱;
[0032]
图5b.激发态phe2在不同极性有机溶剂中的荧光光谱;
[0033]
图5c.激发态phe3在不同极性有机溶剂中的荧光光谱;
[0034]
图5d.溶剂极性参数与斯托克斯位移的相关性;
[0035]
图6a.具有不同的fw的在dmso/h2o的混合物中phe3的pl谱;
[0036]
图6b.发射最大值和相对发射强度(i/i0))与phe1
‑
3的水性混合物组成的关系图;
[0037]
图7a.具有不同fw的dmso/h2o混合物中phe1的pl光谱;
[0038]
图7b.具有不同fw的dmso/h2o混合物中phe2的pl光谱;
[0039]
图8a.在dmso溶液中包含h2dcfh
‑
da指示剂(a)的phe1、phe2、phe3溶液的最大发射量和相对发射强度(i/i0)与照射时间的关系图;
[0040]
图8b.dmso/h2o混合物(v/v=1:99)测试phe1、phe2、phe3的aie特性;
[0041]
图8c.phe1、phe2、phe3在含有abda染料的dmso/h2o混合液中进行激光照射的后吸收最大值和相对吸收强度比(a/a0);
[0042]
图8d.dhr123在光(白光:50mwcm
‑2)触发后phe3和/或vc存在下的pl光谱;
[0043]
图8e.按m062x/6
‑
31g(d,p)的水平进行理论计算phe2和phe3的s1,t1,t2示意图;
[0044]
图8f.i型ros产生示意图;
[0045]
图9a.单独的abda在8分钟内进行白光:50mw cm
‑2辐照后的abda的吸收光谱;
[0046]
图9b.abda phe1在8分钟内进行白光:50mw cm
‑2辐照后的abda的吸收光谱;
[0047]
图9c.abda phe2在8分钟内进行白光:50mw cm
‑2辐照后的abda的吸收光谱;
[0048]
图9d.abda phe3在8分钟内进行白光:50mw cm
‑2辐照后的abda的吸收光谱;
[0049]
图10a.在8分钟内触发光(白光:50mw cm
‑2)后,dhr123 phe1的pl光谱;
[0050]
图10b.在8分钟内触发光(白光:50mw cm
‑2)后,dhr123 phe2的pl光谱;
[0051]
图10c.在8分钟内触发光(白光:50mw cm
‑2)后,dhr123 phe3的pl光谱;
[0052]
图11a.dhr123在光(白光:50mw cm
‑2)触发后在phe1和vc存在下的pl光谱:
[0053]
图11b.dhr123在光(白光:50mw cm
‑2)触发后在phe2和vc存在下的pl光谱;
[0054]
图12.分别与phe1,phe2,phe3孵育后hepg2细胞的clsm图像。其中(a,d,g):亮场,(b,e,h):用405nm激光激发,(c,f,i):鸟场和激发场的合并图像。标尺=100μm;
[0055]
图13.培养phe3的细胞的clsm图像,随后共孵育h2dc fda(10μm,30分钟),然后(a)无激光,(b)10%激光功率在543nm处孵育2分钟,标尺=20μm;在(c)不同激光功率和(d)激光功率为50mw cm
‑2的常氧/缺氧条件下,hepg2细胞在phe3浓度范围内不受光照射的活力持续30分钟。
具体实施方式
[0056]
下面将结合附图以及具体实施例来详细说明本发明,在此以本发明的示意性实施例及说明用来解释本发明,但并不作为对本发明的限定。
[0057]
1.合成和测量
[0058]
首先制备化合物phe1、phe2、phe3,然后在bruker av400光谱仪上测量相关的1h nmr谱。使用ltq orbit rap xl仪器进行高分辨率质谱(ms)检测。确认成功制备了三种phe基化合物。
[0059]
其次,用b3lyp/6
‑
31g(d,p)水平计算目标化合物化学结构及其在最外层轨道上的电子分布。在岛津紫外
‑
2600分光光度计上测定紫外
‑
可见吸收光谱。在horibafluoromax
‑
4荧光仪上记录pl光谱。用hamamatsu绝对pl量子产率光谱仪c11347quantaurus_qy测量荧光量子产率。在奥林巴斯fv1000
‑
ix81共聚焦激光扫描显微镜上进行共聚焦激光扫描显微镜(clsm)图像。用b3lyp/6
‑
31g(d,p)水平计算目标化合物化学结构及其在最外层轨道上的电子分布。
[0060]
1.1化合物1的合成
[0061]
将nah(10mol,240mg)加入到含吩噻嗪(2mol,4.00g)的二甲基甲酰胺(dmf)溶液(30ml)中,在n2条件下搅拌2小时,将1
‑
溴癸烷(2mol,470mg)的dmf(10ml)溶液逐步加入并搅拌过夜;加入pocl3和clch2ch2cl进行反应,最后加入冰水以淬灭反应,混合物用二氯甲烷
(dcm)萃取3次。通过色谱法纯化纯产物,使用乙酸乙酯(ea)/石油作为洗脱剂,得到白色液体化合物1。产率:76%。1h nmr(500mhz,cd2cl2):δ
h
9.77(s,1h),7.64(d,j=10.5hz,1h),7.56(d,j=2.0hz,1h),7.19
‑
7.16(t,j=15.0hz,1h),7.12(d,j=5.0hz,1h),6.98(m,j=5.0hz,3h),3.91(t,j=10.0hz,2h),1.25(m,18h),0.90(t,j=10.0hz,3h),
13
c nmr(126mhz,cd2cl2):δ
c
191.1,152.0,144.9,132.4,144.9,132.4,131.4,129.2,128.9,128.7,126.2,125.0,124.8,117.4,116.2,49.3,33.2,30.9,30.8,30.7,30.5,28.0,28.0,24.0,15.2.
[0062]
1.2化合物2的合成
[0063]
将化合物1(3mmol,1.14g)和4
‑
溴苯乙腈(3.5mmol,0.69g)溶于无水乙醇(20ml)中。在上述乙醇中加入几滴tba h溶液,回流一夜。反应后冷却至室温,析出一些固体粉末。过滤、在乙醇中重结晶得到粗产物。过滤得纯橙粉化合物2。产率:75%。1h nmr(cd2cl2):δ
h
7.78
‑
7.76(d,j=10.0hz,1h),7.60
‑
7.53(m,5h),7.38(s,1h),7.17(t,j=5.0hz,1h),7.10(d,j=5.0hz,1h),6.96(m,j=10.0hz,3h),3.89(t,j=10.0hz,2h),1.28
‑
1.25(m,18h),0.88(t,j=10.0hz,3h)。
13
c nmr(126mhz,cd2cl2):δ
c 147.9,144.3,141.5,134.4,132.8,131.0,129.4,128.5,128.1,127.9,127.7,125.1,123.9,118.4,116.1,115.6,107.7,48.1,32.3,30.0,30.1,29.8,27.2,23.1,14.3.
[0064]
1.3合成phe1
[0065]
将化合物1(3mmol,1.14g)和苯乙腈(3.5mmol,0.41g)溶于无水乙醇(20ml)中。在无水乙醇中加入几滴tba h溶液,回流一夜。反应后冷却至室温,析出固体粉末。过滤并在乙醇中重结晶得到粗产物。得到纯橙粉末phe1。产率:78%。1h nmr(500mhz,cd2cl2)δ7.91
‑
7.89(d,j=10.0hz,1h),7.71
‑
7.69(d,j=10.0hz,1h),7.66
‑
7.60(m,j=10.0hz,2h),7.49
‑
7.41(m,5h),7.17(t,j=5.0hz,1h),7.12(d,j=5.0hz,1h),6.96
‑
6.90(m,j=5.0hz,2h),3.90(t,j=10.0hz,2h),1.28
‑
1.25(m,18h),0.89(t,j=10.0hz,3h),
13
c nmr(126mhz,cd2cl2),δ=142.9,141.4,135.5,131.1,129.7,128.0,126.3,123.6,119.0,116.3,115.8,109.2,48.3,32.5,31.2,30.3,30.2,30.0,29.8,27.4,23.3,14.5,hrms(c32h36n2s):m/z 480.2569[m]
(calcd for c
32
h
36
n2s,480.2599).
[0066]
1.4合成phe2
[0067]
将4
‑
(二苯氨基)苯硼酸(1.5mmol,434mg),化合物2(1mmol,558mg)和pd(pph3)4(0.05mmol,60mg)溶解在干燥的脱气thf溶剂(20ml)中。将k2co3水溶液(2m,12ml)注入上述thf中并回流。在90℃、n2环境下反应8小时。将混合物冷却后,加入饱和硫代硫酸钠水溶液以淬灭反应。将混合物用dcm萃取3次。通过色谱法纯化纯产物,使用乙酸乙酯(ea)/石油作为洗脱剂,得到橙色粉末phe2。产率:92%。1h nmr(500mhz,cd2cl2):δ
h
7.80
‑
7.78(d,j=10.0hz,1h),7.69
‑
7.67(d,j=10.0hz,2h),7.64
‑
7.62(m,j=10.0hz,3h),7.46
‑
7.43(m,j=15.0hz,3h),7.19
‑
6.85(m,15h),3.90(t,j=10.0hz,2h),3.79(s,6h),1.28
‑
1.25(m,18h),0.86(t,j=10.0hz,3h),
13
c nmr(126mhz,cdcl2):δ
c 147.1,144.0,128.8,128.4,128.0,127.5,127.3,124.6,123.6,123.0,115.7,115.2,55.4,47.7,31.9,29.69,29.6,29.2,26.8,22.7,13.9.hrms(c
52
h
53
n3o2s):m/z 783.3885[m ,calcd 783.3858].
[0068]
1.5合成phe3
[0069]
phe3的合成过程参照phe2的合成过程。不同的是原料4
‑
(二苯基氨基)苯硼酸被4
‑
氰基苯硼酸取代。采用色谱法得到纯产物,以乙酸乙酯(ea)/石油为洗脱剂,得到橙红色粉末phe3。产率:89%。1h nmr(cd2cl2)δ7.82(d,j=10.0hz,1h),7.78
‑
7.76(t,j=10.0hz,6h),7.73
‑
7.70(t,j=15.0hz,2h),7.64(d,j=2.0hz,1h),7.48(s,1h),7.20
‑
7.16(t,j=20.0hz,1h),7.13
‑
7.11(d,j=10.0hz,1h),6.93(m,j=3.0hz,3h),3.90(t,j=10.0hz,2h),1.28
‑
1.26(m,18h),0.86(t,j=10.0hz,3h),
13
c nmr(126mhz,cdcl2),δ=148.8,145.6,145.2,142.4,140.6,136.5,134.2,130.4,129.4,129.3,129.2,129.1,128.9,128.7,127.6,126.00,125.4,124.4,120.1,119.5,117.1,116.5,112.6,108.9,49.1,33.3,31.0,30.9,30.7,28.1,28.0,24.0,15.2.hrms(c
39
h
39
n3s):m/z 581.2863[m ,calcd 581.2865].
[0070]
上述各步骤合成路线如下:
[0071][0072]
2.结果和讨论
[0073]
2.1光物理特性
[0074]
本发明以高产率合成目标产物,
[0075]
首先,利用理论计算来证明上文制备得到的三种phe基化合物各自的电子在前沿轨道上的分布。如图2所示,在最高占据分子轨道(homo)上,phe1的电子分布在整个共轭分子骨架上,但在氰基二苯乙烯块上的最低未占据分子轨道(lumo)则显示出明显的局部激发(le)和电荷转移(ct)杂化状态。
[0076]
与phe1相比,引入富电子的含甲氧基的三苯胺(mtpa)单元后,phe2的有效共轭效应明显改善,homo分散在phe和mtpa共轭骨架上,而lumo上mtpa部分的电子消失,表现出显
著的ict效应。当mtpa被苯甲腈基团取代制备phe3时,由于phe与苯甲腈之间的电子转移更为显著,ict效应将进一步改善。有趣的是,它们在homo和lumo之间都有较大的电子重叠,预测可能具有更高的荧光效率。为了验证理论模拟,还对实验光物理结果进行了表征。如图3a所示,测定得到紫外
‑
可见吸收光谱中,phe1的吸收峰为420nm,比phe3(429nm)短。在这三种化合物中,phe2的吸收峰最短,为414nm,因为ct从mtpa转移到氰基二苯乙烯块和分段phe,表明phe的电子供体能力比mtpa单元强。这些弱吸收峰有助于ct的转变。le吸收是320nm附近的较强吸收峰。荧光光谱能较好地反映其激发特性。图3b表明,荧光光谱中,phe3的最长荧光峰为608nm,phe1和phe2的最长荧光峰分别为581和578nm,表明phe3应具有比phe1和phe2更强的ict效应。
[0077]
用荧光光谱的溶剂化效应比较它们的ict效应。首先,测试了phe1、phe2、phe3的吸收光谱,以反映基态的光学性质,结果如图4所示。phe1、phe2、phe3均表现出相似的吸收光谱,不同溶剂中的吸收峰变化很小,表明基态的光学性质对环境极性不敏感。然而,激发态的光学性质对溶剂极性非常敏感。如图5a所示,当溶剂极性改善时,phe1的红移发射明显。例如,在低极性正己烷溶液中,phe1的发射峰为520nm,但在高极性dmso中红移至612nm,红移范围92nm。phe2也表现出相似的溶剂化效应,但区别在于,如图5b所示,phe2比phe1具有更宽的红移范围,达到94nm。如图5c所示,由于dmso中的发射波长(631nm)较长,红移范围(96nm)大于其他两种,phe3的ict效应最强。此外,如图5d所示,phe3的斜率计算为7577.8cm
‑2,进一步高于phe2(7197.4cm
‑2)和phe1(5569.7cm
‑2),证明了由于高度极化的激发态,phe3的ict特性比phe1、phe2更强。
[0078]
其次,还测量了聚集时的光学性质。phe1、phe2、phe3具有良好的疏水性,通过将不良溶剂(h2o)添加到含有phe1、phe2、phe3的dmso溶液中可以形成纳米颗粒。如图6a所示,以phe3为例,phe3能很好地溶于634nm弱荧光的dmso溶剂中。当水被添加到水含量体积分数(fw)为20%时荧光强度降低,说明荧光强度与增强的环境极性相关。高极性溶液中扭曲的d
‑
a构型在激发的能量耗散过程中引起了主要的非辐射衰减过程。当fw提高到30%,荧光强度开始增强并发现蓝移发射,这可能是有助于聚集的形成。fw进一步增加达到70%以上,由于聚集时激发能的非辐射通道受到限制,荧光强度最高,证实了其独特的aie特性。如图7所示,phe1、phe2也具有明显的aie特性,并且由于引入了转子型mtpa,如图6b所示,phe2由于其较高的αaie而具有更明显的aie特性。此外,phe2粉末的plqy为42%,高于phe1(32%)和phe3(28%),表明转子型mtpa能有效地抑制聚集时的分子间堆积相互作用。
[0079]
2.2ros检测
[0080]
ict的增强有利于加速系统间交叉(isc)通道,该通道在产生三重态能量以促进ros的产生方面发挥了非常重要的作用。为了检测phe1、phe2、phe3的ros生成效率,首先使用荧光指示剂2’,7
’‑
二氯二氢荧光素二乙酸酯(h2dcf
‑
da)来评价总ros的产生。如图8a所示。在光触发后,在不同的dmso溶剂中分别加入phe1、phe2、phe3时,h2dcfda的荧光强度几乎没有变化,表明在单分子状态下几乎没有ros的产生。然而,如图8b所示,当phe1、phe2、phe3在dmso/h2o的混合物(v/v=1:99)中形成纳米粒子时,一旦遇到白光,h2dcfda的荧光强度迅速增强,体现了phe1、phe2、phe3聚集诱导ros生成的aie特性。此外,phe3的ros生成效率明显优于其他两种,这证实了ict效应的增强对ros的产生非常有利。为进一步区分ros,首先使用了9,10
‑
蒽基
‑
双(亚甲基)
‑
丁醛酸(abda)这种特别的1o2荧光指示剂。如图8c、
图9所示,在光触发后,在phe1、phe2、phe3存在下,abda染料的吸光度几乎没有变化,表明没有产生ii型1o2。吸收强度略有降低,应归因于abda指示剂自身产生的1o2的较少。
[0081]
因此,应考虑其他类型的ros。用荧光探针二氢罗丹明123(dhr123)检测i型1o2‑
·
。如图10所示,当在光触发后分别与phe1、phe2、phe3相互作用时,dhr123的荧光强度逐渐增强,这表明phe1、phe2、phe3均可产生i型ros而不是ii型1o2。此外,如图8d和图11所示,维生素c(vc)作为还原剂,能有效地猝灭dhr123由i型1o2‑
·
引发的荧光,它也可以用来间接证明phe1、phe2、phe3的1o2‑
·
生成。
[0082]
用理论计算证明的isc进程。如图8e所示,phe2的最低单重激发态(s1)的能级为2.00ev,低于第二个三重态(t2,2.11ev),但远高于最低三重激发态(t1,1.48ev))。因此,计算出s1和t2之间的能量分配(δest)约为0.11ev,这对于促进isc渠道是有利的。有趣的是,当提高ict效果时,phe3中的δest进一步降低了(0.01ev),有可能在phe3中可以进行更快的isc处理,这可以解释为phe3比phe2更有效地产生ros。
[0083]
由于在s1和t2之间出现小的δest,如图8f所示,我们推测3个pss中的ros产生机制经历了三个步骤:1)isc过程将s1平台上的一部分激发能转化为t2能级,2)通过内部转换(ic)过程迅速衰减到t1的水平,3)3o2从t1的能量中获取电子以形成1o2‑
·
[0084]
2.3荧光成像
[0085]
phe1、phe2、phe3都具有明显的aie特性,在细胞中表现出更好的生物成像效果。在含有5%co2的潮湿环境中,于37℃在含有10%胎牛血清的dmem培养基中培养hepg2细胞。将hepg2细胞分别与phe1、phe2、phe3(浓度均为5μm)培养4小时后,用pbs溶液分别洗涤多余的phe1、phe2、phe3,为评价其体外细胞摄取行为,采用共聚焦激光扫描显微镜(clsm)观察。结果如图12所示,phe1、phe2、phe3在hepg2细胞中显示孵育4h后细胞细胞质中明亮的橙色荧光。phe1的荧光信号比其他两个更亮,与其在聚集时较高的plqy有关。此外,添加上述3种光敏剂的细胞与未添加任何光敏剂的细胞均仍保持正常的生长形态,表明phe1、phe2、phe3具有很大的生物相容性。因此,phe1、phe2、phe3在生物成像中具有广阔的应用前景。
[0086]
2.4细胞活力
[0087]
由于phe3在这三种pss中产生的i型ros产量最高,我们采用phe3化合物来评价pdt的体外效率。首先,应验证phe3在hepg2细胞中的ros生成能力。当hepg2细胞与phe3和h2dcfhda探针在不受光照射的情况下孵育时,如图13a所示,可以观察到无荧光,但如图13b所示,光照射后出现强烈的绿色荧光。表明在光触发后,hepg2细胞中会产生有效的ros。然后,用cck
‑
8法测定phe3的细胞毒性。分别用0、2、4、6、8、10μm phe3与hepg2细胞孵育,结果如图13c所示,当不经光照射将phe3孵育浓度提高到10μm时,细胞活力仍超过90%,反映了可忽略的暗毒性。当用50mw cm
‑2的白光照射时,可以观察到明显的光毒性,并且当孵育浓度为10μm时,几乎所有细胞都死亡。此外,提高光功率时,细胞死亡率将加快。在缺氧环境下,i型ros可表现出更好的pdt结果,为了证明这一点,本发明测试了phe3在缺氧条件下的光毒性(o2含量:4%)。结果如图13d所示,当phe3浓度达到8μm、10μm时,hepg2细胞可被有效杀死,这表示在缺氧条件下phe3的pdt结果更好。因此,在常氧/缺氧条件下,phe3的荧光成像效果好,pdt效果更好,这表明其在荧光成像指导的pdt技术中具有很大的潜力。
[0088]
3.结论
[0089]
总之,提出了一种可行的分子方法来制备具有新型aie特性的i型ros光敏剂。提高
含有有重原子的富电子aie材料中的ict效应对于开发产生i型ros的光敏剂至关重要。理论结果表明,较强的ict效应导致s1和t2之间的能量分配较小,这加速了isc的通道促进ros的产生。其中phe3光敏的ros生成效率最高,由于其最强的ict作用,因此获得了三个pss。三种aie活性光敏剂均具有较高的plqy,以保证良好的体外荧光成像效率。phe3在常氧和缺氧环境下的pdt效果显著,证明在荧光成像引导的pdt中具有广阔的应用前景。
[0090]
当增加与红移发射伴随的ict效应时,i型ros的产生效率得到提高。phe31、phe2、phe3在聚集时的光致发光量子产率(plqys)都较高,为28
‑
47%,使它们在细胞中具有很好的荧光成像能力。另一方面,由于i型ros生成,phe3在常氧和缺氧环境下具有良好的pdt结果。本发明将在设计aie活性产生i型ros的光敏剂方面发挥重要作用,克服传统pdt的缺点。
[0091]
以上对本发明实施例所提供的技术方案进行了详细介绍,本文中应用了具体个例对本发明实施例的原理以及实施方式进行了阐述,以上实施例的说明只适用于帮助理解本发明实施例的原理;同时,对于本领域的一般技术人员,依据本发明实施例,在具体实施方式以及应用范围上均会有改变之处,综上所述,本说明书内容不应理解为对本发明的限制。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。

