一种fes
x
电极及制备方法、fes
x
协同微生物矿化固定cr(vi)的装置及方法
技术领域
1.本发明属于危险废物无害化技术领域,具体涉及一种fes
x
电极及制备方法、fes
x
协同微生物矿化固定cr(vi)的装置及方法。
背景技术:
2.近年来,随着工矿业的迅速发展,环境中重金属的污染已日益严重。其中,铬和铬盐作为重要的化工原料,主要用于化工、冶金、制革和电镀等行业,且这些工业部门分布点多而广,在上述行业的生产过程中导致了大量含铬废水、废渣的产生。在环境中,铬主要有cr(
ⅵ
)和cr(ⅲ)两种存在形式。 cr(
ⅵ
)剧毒且致癌,在环境介质中具有很高的迁移性,极易随水淋溶迁移。明确将cr(
ⅵ
)列为亟需治理的5种重金属之一。因此,cr(
ⅵ
)治理已成为我国环境领域关注的焦点问题。
3.目前,国内外对于含铬废水和废渣综合处理处置已有大量的研究报道,通常主要通过物理、化学和生物的方法将剧毒且溶解性较高的cr(
ⅵ
)还原为微毒且溶解性较低的cr(ⅲ)后固定下来,且对铬渣处理后的产物进行堆存或填埋。然而,长期堆存或填埋到土壤中的铬渣处理后的产物及土壤中广泛存在的稳定相的含铬矿物(最为常见的是铬铁矿
‑
fe[cr2o4]),因人类活动中的人为因素或环境中大量存在的强氧化性物质,在环境长期氧化条件下都容易被氧化活化成cr(
ⅵ
),对土壤环境造成污染。那么,针对土壤中剧毒且迁移性很高的cr(
ⅵ
)如何使其回归到稳定的矿物相,成为世界范围内的科学难题,并且在相关方面的研究非常缺失。因此,迫切需求一种可以有效还原土壤中 cr(
ⅵ
),且能同步实现cr(ⅲ)矿化固定的方法。
[0004]
因土壤环境中广泛存在着各种土著微生物,采用微生物还原法,利用其对 cr(
ⅵ
)的还原性,且微生物还原cr(
ⅵ
)产生cr(ⅲ)同环境中或外加离子等物质进一步进行矿化转化,形成难溶、稳定的杂化晶体形态的矿物,实现对土壤环境介质中铬的固定,且有效地避免了稳定相固态含铬矿物被重新释放到环境中。相关方面的研究,自从romanenko和koren’ken首次报道利用微生物可将cr(
ⅵ
)还原为cr(ⅲ)后,紧跟着国内外就有许多关于微生物对cr(vi)还原的研究报道。其中,绝大多数菌株是在厌氧条件下,以乙酸盐、葡萄糖、腐殖酸等外源有机物作为电子供体,cr(
ⅵ
)为呼吸链中最终的电子受体,利用细菌中特定的代谢途径将cr(
ⅵ
)还原为cr(ⅲ),如芽孢杆菌(bacillus sp.)等。然而,微生物还原铬过程中,总是需要添加外源碳源作为电子供体。微生物通过接收电子供体获得能量,增强自身的活性,并将电子最终传输到电子受体,进而提高cr(vi)还原效率,但未消耗完的带
‑
cooh和
‑
nh2可溶性的外源有机物和细菌表面固定cr(iii)的官能团起到了竞争性配位效应,导致了大量还原后的cr(iii)以可溶性有机铬[organo
‑
cr(iii)]形式存在。在后续的研究中,hai
‑
kun zhang等人通过外加醌类物质的电子供体,可以加速六价铬的还原速率,提高cr(iii)的固定化效率。但其还原产物并没有成矿,并且可能是通过被疏水性的脂类包裹,从而脱离水体。并且,kim等人提出了使用希瓦氏菌(s.oneidensis mr
‑
1)细菌还原cr(vi)时,通过外
加te(iv),虽然可以促使还原后的cr(iii)在细菌的表面形成无定形的cr(iii)
‑
te(iv)纳米粒子,但其过程依然受限于外源电子供体(主要是有机物)的供给。电子供体受限于外源有机物严重地影响了微生物处理cr(vi)方面的应用。
技术实现要素:
[0005]
生物电化学系统(bioelectrochemicalsystem,bes)三电极装置的阳极能够通过微生物氧化底物释放电子并将电子直接传递给电极,然后电子通过闭合外电路传递到生物阴极,进而被阴极电子受体接受,从而将阴极重金属离子还原。利用生物阴极提供的电子,间接促进重金属离子的还原。利用bes三电极技术可为微生物对重金属cr(vi)的处理中提供清洁电子供体,实现异位的电子补偿,强化了cr(vi)的去除,也为cr(iii)的有效固定及进一步矿化的提供了一种新的解决方法。
[0006]
本发明提供了一种在碳布上原位可控地制备纳米fes
x
的方法。
[0007]
本发明利用bes三电极技术,提供一种在fes
x
电极上构建三维杂化复合生物电极(3dfes
x
/s.oneidensismr
‑
1/cc)的方法。
[0008]
本发明针对微生物处理cr(vi)中所存在的铬的固定和矿化难的问题,利用bes三电极技术提供的清洁的电子供体,使用发明内容2所制备的复合生物膜电极,建立一种微生物基于外源电子还原cr(vi)成矿的方法。
[0009]
本发明基于fes
x
可以介导微生物胞外电子的双向传输的原理,首先,通过水热的方法,优化反应物浓度、反应溶剂的比例,最终在碳布上原位可控地合成了不同物相的fes
x
;利用bes三电极装置,构建成由fes
x
和s.oneidensismr
‑
1组成的3dfes
x
/s.oneidensismr
‑
1/cc;仅有s.oneidensismr
‑
1时,称为3ds.oneidensismr
‑
1/cc,并对其驯化;进一步将3dfes
x
/s.oneidensismr
‑
1/cc和3ds.oneidensismr
‑
1/cc电极发生反转,从向电极输送电子,变成从电极吸收电子,使之具有双向电子传输的电活性电极生物膜;并将吸收的电子传递给胞外变价cr(vi)电子受体,建立一种微生物基于外源电子还原cr(vi)成矿过程的系统;电子介导下,在微生物对cr(vi)还原的同时,利用fes2对cr(vi)还原的协同作用,实现对cr(vi)还原,并强化对还原产物cr(iii)的有效固定和进一步矿化。
[0010]
本发明目的通过以下技术方案予以实现:
[0011]
一种fes
x
电极的制备方法,包括以下步骤:
[0012]
(1)将六水三氯化铁和硫脲溶于水和乙醇的混合液中,然后加入碳布,搅拌;140~160℃水热反应3
‑
6,得到亚稳定相的fes
x
;
[0013]
(2)将步骤(1)所述亚稳定相的fes
x
洗涤、真空干燥;然后惰性气氛中,400~600℃热处理2
‑
4h,得到fes
x
电极。
[0014]
优选的,步骤(1)所述六水三氯化铁和硫脲的摩尔比为4
‑
7:5
‑
10;
[0015]
优选的,所述水和乙醇的体积比为1:5
‑
6;
[0016]
优选的,所述碳布的尺寸为2~4
×
4~6cm;
[0017]
优选的,所述搅拌的时间为30~60min。
[0018]
优选的,步骤(2)所述惰性气氛为氩气;
[0019]
优选的,所述洗涤为用无水乙醇洗涤;
[0020]
优选的,所述真空干燥的温度为40~60℃,真空干燥的时间为8
‑
12h。
[0021]
上述制备方法制备的fes
x
电极,所述x取值为1~2。
[0022]
一种电子介导下fes
x
协同微生物矿化固定cr(vi)的装置,包括三电极体系、质子交换膜、i室、ii室;所述的三电极体系包括工作电极、对电极及参比电极;所述i室和ii室通过质子交换膜隔开;所述工作电极和参比电极置于 i室,所述对电极置于ii室;所述工作电极为上述fes
x
电极和希瓦氏菌制备的复合生物膜电极。
[0023]
优选的,所述参比电极为饱和甘汞电极;
[0024]
优选的,所述对电极为铂片电极;
[0025]
优选的,所述质子交换膜为n117;
[0026]
优选的,所述i室的体系包括有矿物元素、混合维生素、希瓦氏菌、乳酸钠的磷酸缓冲液;所述ii室的体系为与i室相同浓度的pbs缓冲溶液;进一步优选的,所述磷酸缓冲液的浓度为50~60mm。
[0027]
优选的,所述复合生物膜电极的制备包括以下步骤:
[0028]
①
电极的组装:将fes
x
电极、参比电极置于i室,对电极置于ii室;并连接恒电位仪;i室加入有矿物元素、混合维生素、希瓦氏菌、乳酸钠的磷酸缓冲液,ii室加入磷酸缓冲液;
[0029]
②
电极的驯化:对fes
x
电极施加正电压,待乳酸钠消耗完时,更换新的电解液,直至电流稳定输出三个周期,形成复合生物膜电极。
[0030]
进一步优选的,步骤
①
所述fes
x
电极的规格为1
‑2×1‑
4cm;步骤
②
所述正电压为 200~300mv。
[0031]
使用上述的装置在电子介导下fes
x
协同微生物矿化固定cr(vi)的方法,包括如下步骤:
[0032]
i室加入有矿物元素、混合维生素、希瓦氏菌、乳酸钠和铬盐的磷酸缓冲液,ii室加入磷酸缓冲液,连接恒电位仪,对工作电极施加负电压,促进复合生物膜电极对cr(vi)去除及cr(iii)的有效固定。
[0033]
优选的,所述i室中铬盐的浓度为80~120mg/l;所述工作电极施加负电压的范围为:0~
‑
400mv。
[0034]
本发明提供一种电子介导下fes
x
协同微生物矿化固定cr(vi)方法,其原理如下:
[0035]
bes三电极装置能够通过微生物氧化底物释放电子并将电子直接传递给电极,然后电子通过闭合外电路传递到电极生物膜,进而被电子受体接受,从而将阴重金属离子还原。利用bes三电极装置提供的清洁电子供体,微生物获得了生长,间接促进重金属离子的还原。在本发明中,所使用的电活性微生物(s.oneidensis mr
‑
1),其电子的传输通道是可逆的,即作为阳极时可以将电子传递到电极,将其反转到阴极也可以实现电子的逆向传递—从电极向微生物细胞。另外,所制备的fes
x
电极在本发明中扮演着多重角色,一方面可以介导s.oneidensismr
‑
1的胞外电子的输出和输入。另外,fes
x
是cr(
ⅵ
) 的有效还原剂,还可以协同微生物还原阴极室中的cr(vi),且还原cr(vi)过程中生成的fe(ⅲ),可以和cr(ⅲ)进一步形成[fe,cr](oh)3。
[0036]
本发明相对于现有技术,具有如下的优点及效果:
[0037]
(1)本发明制备fes
x
电极的方法简单、高效。
[0038]
(2)本发明中使用fes
x
电极所组装的复合膜和生物膜电极
‑
具有双向电子传输的
高活性电化学性能。
[0039]
(3)本发明使用bes系统提供的电子供体,清洁、高效、可操作性强,解决微生物还原铬过程中电子供体受限于外源有机物的问题,同时避免了传统有机物作为电子供体时,形成有机铬的问题。
[0040]
(4)本发明所建立微生物基于外源电子还原cr(vi)成矿过程的系统,强化了cr(vi)的还原和固定,解决了cr(vi)还原后成矿难的瓶颈问题。
附图说明
[0041]
图1为本发明实施例1制备的fes2/cc和fe3s4/cc电极材料的x射线粉末衍射图;
[0042]
图2为本发明实施例1制备的fes2/cc和fe3s4/cc电极材料的扫描电镜图;
[0043]
图3为本发明实施例1制备的fes2电极材料中fe 2p的x射线光电子能谱;
[0044]
图4为本发明实施例1制备的fes2电极材料中s 2p的x射线光电子能谱;
[0045]
图5为本发明实施例1制备的fes2/cc、fe3s4/cc电极和纯碳布(cc)电极的循环伏安曲线图;
[0046]
图6为本发明实施例1制备的fes2/cc、fe3s4/cc电极和cc电极电化学阻抗曲线图;
[0047]
图7为本发明实施例5组装复合生物电极和生物电极的bes装置示意图;其中,we为工作电极、ref为参比电极、ce为对电极、pem为质子交换膜;
[0048]
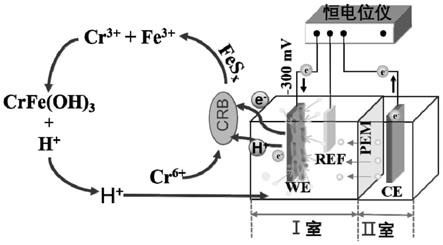
图8为本发明实施例5微生物基于外源电子还原cr(vi)成矿过程系统装置示意图;其中,we为工作电极、ref为参比电极、ce为对电极、pem为质子交换膜、crb为希瓦氏菌;
[0049]
图9为本发明实施例5复合生物膜和生物膜电极的循环伏安曲线图;
[0050]
图10为本发明实施例6对比复合生物膜和生物膜电极对cr(vi)的去除率;
[0051]
图11为本发明实施例6cr(ⅲ)在复合生物膜和生物膜电极上的成矿的扫描电极图。
具体实施方式
[0052]
以下结合实施例和附图来进一步解释本发明,但实施例并不对本发明做任何形式的限定。
[0053]
实施例1
[0054]
fes
x
/cc电极的制备
[0055]
1、fes2/cc电极的制备
[0056]
将fecl3·
6h2o(0.005mol)和硫脲(0.015mol)溶于60ml乙醇和水的混合液中(v:v=5:1),然后加入2*4cm的碳布(cc),搅拌30min后。将其置于100 ml的反应釜内衬中,140℃,反应6h。待反应结束,自然冷却后,用乙醇反复清洗所得产物,烘干后。将其置于管式炉中,在惰性气氛中,600℃,热处理2h,即得到fes
x
/cc电极。产品的x射线衍射图(xrd)见图1a。
[0057]
2、fe3s4/cc电极的制备
[0058]
将fecl3·
6h2o(0.005mol)和硫脲(0.015mol)溶于60ml乙醇和水的混合液中(v:v=5:1),然后加入2*4cm的碳布(cc),搅拌30min后。将其置于100 ml的反应釜内衬中,140℃,反应3h。待反应结束,自然冷却后,用乙醇反复清洗所得产物,烘干后。将其置于管式炉
中,在惰性气氛中,600℃,热处理2h,即得到fes
x
/cc电极。产品的x射线衍射图(xrd)见图1b。
[0059]
通过对fes2/cc和fe3s4/cc电极的xrd结果分析,可以得知,fes2/cc和fe3s4/cc电极除了在25
°
和43
°
处展示了两个主要的碳基底的衍射峰外,其余的一些尖锐的衍射峰与fes2的标准卡片(pdf99
‑
0076)和fe3s4的标准卡片pdf#16
‑
0713非常一致。
[0060]
实施例2
[0061]
实施例1所得fes2/cc和fe3s4/cc电极微观和宏观形貌的表征
[0062]
实施例1中所得fes2/cc和fe3s4/cc电极裁剪部分进行扫描电极的表征和分析,该电极的扫描图见图2a和图2b所示。图2a和图2b的sem数据表明了fes2和fe3s4纳米粒子成功地负载在碳布电极的上,将有利于微生物的附着和生物膜的形成。
[0063]
实施例3
[0064]
实施例1所得fes2电极的元素组成和价态信息的分析
[0065]
实施例1中所得fes2电极裁剪部分进行x射线光电子能谱的表征和分析,其结果见图3和图4。图3和图4分别为fe2p和s2p高分辨xps图谱。从图3中fe2p的xps结果可知,对于得到的fes2/c电极而言,fe可以分为两个峰:结合能在709.3evand705.3ev处的峰,分别为fe2p1/2和fe2p3/2。然而,对于s在fes2中的化学态,结合能在162.9evand163.9ev,对应于s2p1/2和s2p3/2。
[0066]
实施例4
[0067]
实施例1所得fes2/cc和fe3s4/cc电极的电化学性能的评价
[0068]
实施例1中所得fes2和fe3s4电极作为工作电极,铂线和甘汞电极分别作为对电极和参比电极。使用以上三电极体系对fes2/cc和fe3s4/cc电极的循环伏安法(cyclicvoltammetry,cv)和电化学交流阻抗法(electrochemicalimpedancespectroscopy,eis)进行测试和分析,其结果见图5和图6。图5是fes2/cc、fe3s4/cc和纯cc的cvs曲线图。如图5所示,fes2/cc和fe3s4/cc电极的cvs曲线的面积明显大于碳布的,依次顺序为:fes2/cc﹥fe3s4/cc﹥cc。并且,在阳极上没有附着生物膜之前,任何一个阳极都没有明显的电活性希瓦氏菌的氧化还原峰,说明fes2/cc、fe3s4/cc和cc电极在富集生物膜之前,没有对乳酸钠催化氧化特征。图6为fes2/cc、fe3s4/cc和cc电极的eis。如图6所示,相比于cc,fes2/cc、fe3s4/cc电极具有较小的欧姆电阻(r
s
)、较低的电荷转移电阻(r
ct
)。其中,fes2/cc和fe3s4/cc电极的r
ct
分别为23.82ω和36.43ω,低于cc的55.25ω的电荷转移电阻,说明制备纳米fes2的电极在电极/电解质界面上具有较快的电荷转移过程。
[0069]
实施例5
[0070]
双向电子传输的3dfes
x
/s.oneidensismr
‑
1/cc和3ds.oneidensismr
‑
1/cc电极的组装
[0071]
①
使用立方型双室微生物电解池(如下图7所示),采用三电极生物电化学系统,其中三电极体系由工作电极(1
×
2cm碳布、实例1所制备的1
×
2cmfes
x
电极),参比电极(饱和甘汞电极)及对电极(1
×
2cm铂片电极)构成。两室中间通过质子交换膜(n117)将i室(工作电极、参比电极)与ii室(对电极)隔开。i室的体系中为100ml、50mm的磷酸缓冲液(pbs)的混合液,具体包含有矿物元素(12.5ml
·
l
‑1)、混合维生素(10ml
·
l
‑1)、2ml电活性希瓦氏菌、20mm乳酸钠;ii室由相同浓度的pbs缓冲溶液组成。以上使用的溶液通过n2爆气20min,以去
除其中的溶解氧。所有的实验过程均在30℃下进行。
[0072]
其中,矿物元素、混合维生素的组成和具体配制过程如下所示。
[0073]
1l矿物元素溶液的配制:
[0074]
首先,将1.5g次氮基三乙酸溶解到大约0.5l的蒸馏水中,然后用1m的 koh溶液将其ph调到6.5;其次,依次向上述溶液中加入以下药品, mgso4·
7h2o(3.0g)、mnso4·
h2o(0.5g)、nacl(1.0g)、feso4·
7h2o(0.1g)、 cocl2·
6h2o(0.1g)、cacl2(0.1g)、znso4·
7h2o(0.1g)、cuso4·
5h2o(0.01 g)、alk(so4)2·
12h2o(0.1g)、h3bo3(0.01g)以及和na2moo4·
2h2o(0.01 g)。然后将溶液稀释至1000ml,过滤、灭菌消毒,待用。
[0075]
1l混合维生素的配制:
[0076]
分别称取以下维生素:维生素h(又称生物素,2.0mg)、维生素b9(又称叶酸,2.0mg)、盐酸吡哆醇(10.0mg)、维生素b1(又称盐酸硫胺素,5.0mg)、维生素b2(又称核黄素,5.0mg)、尼克酸(5.0mg)、d
‑
( )泛酸钙(5.0mg)、维生素b12(又称钴胺素,0.1mg)、对氨基苯甲酸(5.0mg)和硫辛酸(5.0mg)到烧杯中,加入灭菌水使其溶解后,转移至容量瓶中,定容1000ml,备用。
[0077]
②
用导线将三电极生物电化学系统与多通道恒电位器相连接起来,施加正电压( 200mv),工作电极3d fes
x
上形成了复合生物膜,称为3d fes
x
/ s.oneidensis mr
‑
1/cc(3d fes2/s.oneidensis mr
‑
1/cc和3d fe3s4/s.oneidensismr
‑
1/cc)。其他条件不变的情况下,仅有电活性铬还原菌时,工作电极碳布上形成的膜为3d s.oneidensis mr
‑
1/cc。该系统的电流在线采集并自动记录,待其底物乳酸钠消耗完时,更换新的电解液。电流稳定输出三个周期,表明复合生物膜和生物膜电极构建成功,以供后续使用。
[0078]
③
电极的反转:将孵化好的复合生物膜和生物膜电极反转,如图8所示。在导线接通之前,取铬盐加入该装置的i室中配置100mg/l铬盐溶液,i室和 ii室其他条件不变;然后,工作电极被施加不同恒电位(0,
‑
200,
‑
400mv) 后,促进复合生物膜电极对cr(vi)去除及cr(iii)的有效固定。
[0079]
按照图8的装置图,进一步将3d fes
x
/s.oneidensis mr
‑
1/cc和3ds.oneidensis mr
‑
1/cc电极进行反转,即得到双向电子传输的复合生物膜和生物膜电极。进一步对电极上生物膜活性cvs的测试,其结果如图9所示。在扫速为5mv
·
s
‑1,乳酸钠存在的条件下,3d fes
x
/s.oneidensis mr
‑
1/cc和3ds.oneidensis mr
‑
1/cc电极上的生物膜展示了典型希瓦氏菌的s形循环伏安图的特征,这说明了在这些生物阳极上产电菌的活性。
[0080]
实施例6
[0081]
微生物基于外源电子还原cr(vi)成矿的方法
[0082]
按照上述图8的装置中,取铬盐加入该装置的i室中配置100mg/l铬盐溶液,i室和ii室其他条件不变,工作电极施加
‑
300mv电压,分析不同电极对迁移态铬的还原效率,其结果如图10所示。如图10所示,设定电位为
‑
300 mv时,初始cr(vi)浓度为100mg时,相比于3d s.oneidensis mr
‑
1/cc生物电极(13.00mg/l d),3d fes2/s.oneidensis mr
‑
1/cc和3d fe3s4/s.oneidensismr
‑
1/cc复合生物电极在第一个周期内cr(vi)还原率分别为49.97mg/l d和32.40mg/l d。并且随着循环周期的增加,3d fes2/s.oneidensis mr
‑
1/cc生物电极对铬的还原率先增加再降低,在第5个周期达到了峰值,其还原速率为 29.00mg/l d。而3d fes2/s.oneidensis mr
‑
1/cc和3d fe3s4/s.oneidensismr
‑
1/cc复合生物电极对铬的还原
速率是持续增加。到第8个周期时,3dfes2/s.oneidensis mr
‑
1/cc和3d fe3s4/s.oneidensis mr
‑
1/cc复合生物电极对 cr(vi)去除速率达到最大,分别为87mg/l d和62.00mg/l d,且随着循环周期的增加保持不变。3d fes2/s.oneidensis mr
‑
1/cc和3d fe3s4/s.oneidensismr
‑
1/cc复合生物电极对cr(vi)还原速率的不再增加被认为是由于相对较高的cr(vi)浓度和/或累积的cr(iii)抑制所致。
[0083]
不同工作电极对铬还原后产物固定的分析,其结果如图11所示。由图11 (a)可知,对于纯的cc电极形成的生物膜,其表面十分光滑,整个菌体较为饱满。然后,对于3d fes2/s.oneidensis mr
‑
1/cc,从图11(b)可以看出细菌表面以及它周围的区域产生了大量颗粒物。
[0084]
以上实施例为本发明较佳的实施方式,但本发明的实施方式并不受上述实施例的限制,其他的任何未背离本发明的精神实质与原理下所作的改变、修饰、替代、组合、简化,均应为等效的置换方式,都包含在本发明的保护范围之内。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。