da)的次要蛋白成分时,将组合物与一种或多种药学上可接受的赋形剂合并以制备药用组合物。
6.在方法的各个方面:所制备的药用组合物包含28
‑
32 mg/ml的抗体,所述抗体包含含有seq id no:2的氨基酸序列的重链和含有seq id no:1的氨基酸序列的轻链;所制备的药用组合物包含9
‑
11 mg/ml的抗体,所述抗体包含含有seq id no:2的氨基酸序列的重链和含有seq id no:1的氨基酸序列的轻链;所述方法进一步包括仅当主要成分为按组合物中蛋白的重量计至少90%和次要成分为按组合物中蛋白的重量计至少3%时,将组合物与一种或多种药学上可接受的赋形剂合并以制备药用组合物;确定步骤包括电泳或色谱法;和提供步骤包括培养表达所述重链和所述轻链的细胞。
7.除非另外定义,否则本文所用的所有技术和科学术语具有与本发明所属领域的普通技术人员通常理解的相同含义。本文描述用于本发明的方法和材料;也可使用本领域已知的其他合适的方法和材料。材料、方法和实例仅为说明性的而不旨在限制。本文提及的所有出版物、专利申请、专利、序列、数据库条目和其他参考文献通过参考以其全部结合。在冲突的情况下,以本说明书(包括定义)为准。
8.根据以下详细描述和附图以及根据权利要求,本发明的其他特征和优点将为显而易见的。
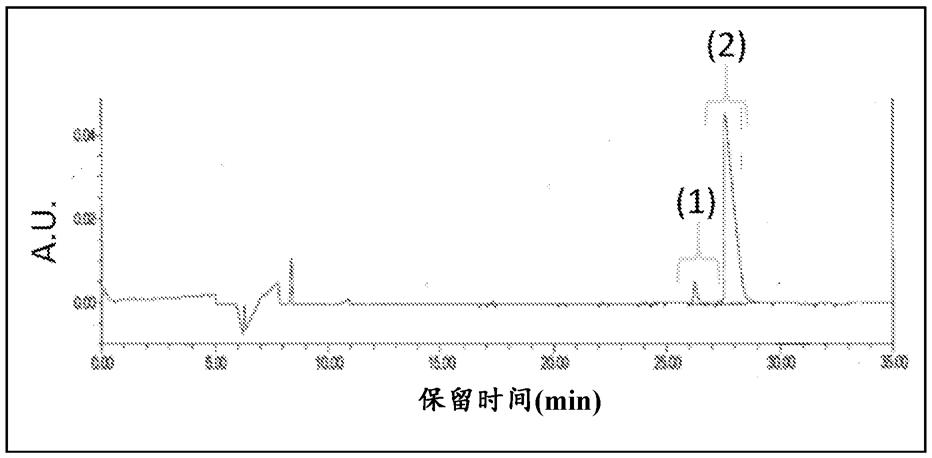
9.附图描述图1显示在非还原性条件下测量的m281组合物的代表性毛细管电泳(ce
‑
sds)电泳图谱;主要的完整igg标记为(2)和大小变体标记为(1)。
10.图2显示通过亲水相互作用液相色谱
‑
质谱联用(hilic lc
‑
ms)分析的m281组合物的代表性数据;(a) 通过亲水相互作用液相色谱分析的m281组合物的uv色谱图,其中主要的轻
‑
重
‑
重
‑
轻链标记为(2)和大小变体标记为(1);(b) 来自质谱的基峰色谱图,其中主要的轻
‑
重
‑
重
‑
轻链标记为(2)和大小变体标记为(1a,保留时间12.42分钟;1b,保留时间12.68分钟)。
11.图3a
‑
3b显示通过亲水相互作用液相色谱分离的选定级分的代表性质谱结果;(a) 显示包含图2 (1a)的级分的质谱结果;(b) 显示包含图2 (1b)的级分的质谱结果。
12.图4显示含有二硫键的肽的草图示意图,所述肽暴露于胰蛋白酶消化,并然后在存在加热或还原的情况下进行β
‑
消除。
13.图5显示m281组合物的代表性电荷电泳图谱(ce);主要同种型在3.03
‑
3.13分钟之间洗脱和次要同种型在3.23
‑
3.31分钟之间洗脱。
14.图6显示在通过具有直接电喷雾电离质谱的微芯片区带电泳分离进行分析后,包含次要同种型(图5所示,级分在3.23
‑
3.31分钟之间洗脱)的分离的样品的代表性质量。
15.图7显示方法的流程图,所述方法包括通过sds
‑
page凝胶电泳分离组合物,通过切割sds
‑
page凝胶版面而分离每种组合物中选定的大小变体,用胰蛋白酶消化分离的大小变体,并通过nano
‑
lc
‑
ms方法分析分离和胰蛋白酶消化的大小变体的质量分布。
16.图8显示由胰蛋白酶消化(a) 轻
‑
重
‑
重
‑
轻链(lc
‑
hc
‑
hc
‑
lc);(b) 重
‑
重
‑
轻链(hc
‑
hc
‑
lc);(c) 用脱氢丙氨酸取代未配对重链上的cys219的重
‑
重
‑
轻链产生的预期肽的化学表示和分子量。
17.图9显示对含有lc
‑
hc
‑
lc
‑
hc、cys
‑
a、deha
‑
a和cys
‑
hc
‑
hc的分离的组合物评估的
lc
‑
hc
‑
hc
‑
lc (数据以蓝色显示)和hc
‑
hc
‑
lc (数据以橙色显示)的链间二硫键量化。
18.详述本发明的特征在于包含靶向人类新生儿fc受体(fcrn)的抗体的新颖组合物。这些组合物可用于例如在受试者中促进自身抗体的清除,在受试者中抑制抗原呈递,阻断免疫应答(例如在受试者中阻断免疫应答的基于免疫复合物的激活)或治疗受试者的免疫性疾病(例如自身免疫性疾病)。本文中,公开了含有上述分离的抗体和一种或多种大小变体的组合物,其中最终组合物含有总蛋白含量的至少80%,其包含分子量为约140000
‑
143000 (例如141750
‑
141800) da的完全组装的轻
‑
重
‑
重
‑
轻链(lc
‑
hc
‑
hc
‑
lc);和总蛋白含量的最多5% (45、3%、2%、1%、0.8%),其包含较低分子量(例如118000
‑
120000 da)的选定大小变体。
19.抗fcrn抗体可如本文所述配制的抗体包括具有轻链序列qsaltqpasvsgspgqsitisctgtgsdvgsynlvswyqqhpgkapklmiygdserpsgvsnrfsgsksgntasltisglqaedeadyycssyagsgiyvfgtgtkvtvlgqpkaapsvtlfppsseelqankatlvclisdfypgavtvawkadsspvkagvetttpskqsnnkyaassylsltpeqwkshksyscqvthegstvektvaptecs (seq id no: 1)和重链序列evqllesggglvqpggslrlscaasgftfstyamgwvrqapgkglewvssigasgsqtryadsvkgrftisrdnskntlylqmnslraedtavyycarlaigdsywgqgtmvtvssastkgpsvfplapsskstsggtaalgclvkdyfpepvtvswnsgaltsgvhtfpavlqssglyslssvvtvpssslgtqtyicnvnhkpsntkvdkkvepkscdkthtcppcpapellggpsvflfppkpkdtlmisrtpevtcvvvdvshedpevkfnwyvdgvevhnaktkpreeqyastyrvvsvltvlhqdwlngkeykckvsnkalpapiektiskakgqprepqvytlppsreemtknqvsltclvkgfypsdiavewesngqpennykttppvldsdgsfflyskltvdksrwqqgnvfscsvmhealhnhytqkslslspg (seq id no: 2)的抗体。
20.该抗体的变体也可如本文所述进行配制。这种变体包括:具有拥有1
‑
5个单个氨基酸取代或缺失的seq id no:1的变体的轻链序列(并且优选地包含seq id no: 3
‑
5的cdr序列)和拥有1
‑
5个单个氨基酸取代或缺失的seq id no:24的变体的重链序列(并且优选地包含seq id no: 6
‑
8的cdr序列)的抗体。由seq id no:1的变体和seq id no:4的变体组成的抗体优选地保留m281的cdr序列:tgtgsdvgsynlvs (轻链cdr1;seq id no: 3);gdserps (轻链cdr2;seq id no: 4);ssyagsgiyv (轻链cdr3;seq id no: 5);tyamg (重链cdr1;seq id no: 6);sigasgsqtryads (重链cdr2;seq id no: 7);和laigdsy (重链cdr3;seq id no: 8)。
21.在某些情况下,轻链的序列与以下具有至少90%、95%或98%的同一性:qsaltqpasvsgspgqsitisctgtgsdvgsynlvswyqqhpgkapklmiygdserpsgvsnrfsgsksgntasltisglqaedeadyycssyagsgiyvfgtgtkvtvlgqpkaapsvtlfppsseelqankatlvclisdfypgavtvawkadsspvkagvetttpskqsnnkyaassylsltpeqwkshksyscqvthegstvektvaptecs (seq id no: 1)。
22.在某些情况下,重链的序列与以下具有至少90%、95%或98%的同一性:evqllesggglvqpggslrlscaasgftfstyamgwvrqapgkglewvssigasgsqtryadsvkgrftisrdnskntlylqmnslraedtavyycarlaigdsywgqgtmvtvssastkgpsvfplapsskstsggtaalgclvkdyfpepvtvswnsgaltsgvhtfpavlqssglyslssvvtvpssslgtqtyicnvnhkpsntkvdkkvepkscdkthtcppcpapellggpsvflfppkpkdtlmisrtpevtcvvvdvshedpevkfnwyvdgvevhnaktkpreeqyastyrvvsvltvlhqdwlngkeykckvsnkalpapiektiskakgqprepqvytlppsreemtknqvsltclvkgfy
psdiavewesngqpennykttppvldsdgsfflyskltvdksrwqqgnvfscsvmhealhnhytqkslslspg (seq id no: 2)。
23.在某些情况下,抗体在抗体的恒定区(例如fc区)中包含氨基酸取代、添加和/或缺失,其例如导致效应子功能降低,例如降低的补体依赖性细胞溶解(cdc)、抗体依赖性细胞介导的细胞溶解(adcc)和/或抗体依赖性细胞介导的吞噬作用(adcp)和/或降低的b细胞杀伤。恒定区不直接参与抗体与其靶标的结合,而是表现出多种效应子功能,比如抗体参与抗体依赖性细胞毒性。在某些情况下,抗体的特征为与自然杀伤(nk)细胞上的人类补体因子c1q和/或人类fc受体的结合减少(即没有结合)。在其他情况下,抗体的特征为与人类fcγri、fcγriia和/或fcγriiia的结合减少(即没有结合)。为了改变或减少抗体依赖性效应子功能,比如cdc、adcc、adcp和/或b细胞杀伤,抗体可属于igg类,并含有一个或多个氨基酸取代e233、l234、g236、d265、d270、e318、k320、k322、a327、a330、p331和/或p329 (自始至终为eu编号(edelman et al., proc. natl. acad. usa, 63:78
‑
85 (1969)),除非另外指明)。在某些情况下,抗体具有突变l234a/l235a或d265a/n297a。在某些情况下,相对于seq id no: 2的序列,抗体含有氨基酸取代a297n,使得抗体变为糖基化形式。预期在氨基酸n297处具有糖基化的抗体会结合补体或fc受体(即补体c1q结合),而预期具有n297a的抗体(例如seq id no:2)则与补体或fc受体的结合(即补体c1q结合)非常少,表明cdc的潜力低。在其他情况下,相对于seq id no: 2,m281确实在残基446处含有c
‑
末端赖氨酸。在某些情况下,轻链上的氨基末端gln为pyrogln。
24.载体、宿主细胞和抗体产生抗fcrn抗体可从宿主细胞中产生。宿主细胞是指媒介物,所述媒介物包含从其相应的核酸表达本文所述的多肽和构建体所需的必要细胞组件,例如细胞器。核酸可包含在核酸载体中,核酸载体可通过本领域已知的常规技术(例如转化、转染、电穿孔、磷酸钙沉淀、直接显微注射、感染等)引入到宿主细胞中。核酸载体的选择部分地取决于要使用的宿主细胞。通常,优选的宿主细胞具有原核(例如细菌)或真核(例如哺乳动物)来源。
25.核酸载体的构建和宿主细胞可通过本领域已知的多种方法来制备编码抗fcrn抗体的氨基酸序列的核酸序列。这些方法包括(但不限于)寡核苷酸介导的(或定点的)诱变和pcr诱变。可使用标准技术(例如基因合成)获得编码抗fcrn抗体的核酸分子。或者,可使用本领域的标准技术,例如quikchange
tm
诱变,将编码野生型抗fcrn抗体的核酸分子突变为含有特定的氨基酸取代。可使用核苷酸合成仪或pcr技术合成核酸分子。
26.可将编码抗fcrn抗体的核酸序列插入到能够在原核或真核宿主细胞中复制和表达核酸分子的载体中。许多载体为本领域可获得的并且可以使用。每个载体可含有可被调节和优化以与特定宿主细胞相容的各种组件。例如,载体组件可包括(但不限于)复制起点、选择标记基因、启动子、核糖体结合位点、信号序列、编码目标蛋白的核酸序列和转录终止序列。
27.哺乳动物细胞可用作宿主细胞。哺乳动物细胞类型的实例包括(但不限于)人类胚胎肾(hek) (例如hek293、hek 293f)、中国仓鼠卵巢(cho)、hela、cos、pc3、vero、mc3t3、ns0、sp2/0、very、bhk、mdck、w138、bt483、hs578t、htb2、bt20、t47d、ns0 (不会内源性地产生任何免疫球蛋白链的鼠骨髓瘤细胞系)、crl7o3o和hss78bst细胞。在其他可能(can)中,
大肠杆菌细胞可用作宿主细胞。大肠杆菌菌株的实例包括(但不限于)大肠杆菌294 (atcc
® 31446)、大肠杆菌λ 1776 (atcc
® 31537)、大肠杆菌bl21 (de3) (atcc
® baa
‑
1025)和大肠杆菌rv308 (atcc
® 31608)。不同的宿主细胞具有蛋白产物的翻译后加工和修饰的特征性和特定机制。可选择适当的细胞系或宿主系统以确保表达的抗fcrn抗体的正确修饰和加工。可使用本领域的常规技术,例如转化、转染、电穿孔、磷酸钙沉淀和直接显微注射,将上述表达载体引入到合适的宿主细胞中。一旦将载体引入到宿主细胞中以产生蛋白,就将宿主细胞在常规营养培养基中进行培养,所述营养培养基视情况进行修饰以诱导启动子、选择转化体或扩增编码所需序列的基因。用于表达治疗性蛋白的方法为本领域已知的,参见例如paulina balbas, argelialorence (eds.) recombinant gene expression: reviews and protocols (methods in molecular biology), humana press; 2nd ed. 2004 (2004年7月20日)和vladimir voynov和justin a. caravella (eds.) therapeutic proteins: methods and protocols (methods in molecular biology) humana press; 2nd ed. 2012 (2012年6月28日)。
28.蛋白产生、回收和纯化用于产生抗fcrn抗体的宿主细胞可在本领域已知并且适合于所选宿主细胞的培养的培养基中生长。适用于哺乳动物宿主细胞的培养基的实例包括最小必需培养基(mem)、dulbecco改良的eagle培养基(dmem)、expi293
™
表达培养基、补充有胎牛血清(fbs)的dmem和rpmi
‑
1640。适用于细菌宿主细胞的培养基的实例包括luria肉汤(lb)加上必要的补充剂,比如选择剂,例如氨苄西林。在合适的温度(比如约20℃
‑
约39℃,例如25℃
‑
约37℃,优选地37℃)和co2水平比如5
‑
10% (优选地8%)下培养宿主细胞。培养基的ph通常为约6.8
‑
7.4,例如7.0,这主要取决于宿主生物体。如果在表达载体中使用诱导型启动子,则在适合于启动子激活的条件下诱导蛋白表达。
29.蛋白回收一般地涉及使宿主细胞破裂,通常通过方法比如渗透压休克、超声处理或裂解。一旦细胞破裂,可通过离心或过滤去除细胞碎片。蛋白可进一步纯化。抗fcrn抗体可通过蛋白纯化领域中已知的任何方法来纯化,例如通过蛋白a亲和力、其他色谱(例如离子交换、亲和力和尺寸排阻柱色谱)、离心、差异溶解度或通过用于纯化蛋白的任何其他标准技术。(参见process scale purification of antibodies, uwe gottschalk (ed.) john wiley & sons, inc., 2009)。在某些情况下,可将抗fcrn抗体缀合于标记序列(比如肽)以促进纯化。标记氨基酸序列的实例为六聚组氨酸肽(his标签),其以微摩尔亲和力结合于镍官能化的琼脂糖亲和柱。可用于纯化的其他肽标签包括(但不限于)血凝素“ha”标签,其对应于源自流感血凝素蛋白的表位。
30.治疗方法和适应症通过本文所述的含有抗fcrn抗体的药用组合物对人类fcrn的阻断在由igg自身抗体驱动的疾病中可能具有治疗益处。fcrn阻断以诱导总体igg分解代谢并去除多种自身抗体、小的循环代谢物或脂蛋白的能力,提供一种方法以将自身抗体去除策略的效用和可及性扩大至具有自身抗体驱动的自身免疫性疾病病理学的患者。不受任何理论的束缚,抗fcrn抗体的主要作用机制可能是增加循环中病原性自身抗体的分解代谢和减少自身抗体和免疫复合物在受影响组织中的沉积。
31.药用组合物可用于在受试者中促进病原性抗体(例如igg和igg自身抗体)的分解
代谢和清除,以减少免疫应答,例如在受试者中阻断免疫应答的基于免疫复合物的激活和治疗受试者的免疫性病症或疾病。特别地,药用组合物可用于减少或治疗急性或慢性免疫应答的基于免疫复合物的激活。急性免疫应答可由选自以下的医学病症激活:寻常型天疱疮、狼疮性肾炎、重症肌无力、格林
‑
巴利综合征(guillain
‑
barr
éꢀ
syndrome)、抗体介导的排斥、抗磷脂抗体综合征(例如灾难性抗磷脂抗体综合征)、免疫复合物介导的血管炎、肾小球炎、离子通道病、视神经脊髓炎、自身免疫性听力损失、特发性血小板减少性紫癜(itp)、自身免疫性溶血性贫血(aiha)、免疫性嗜中性粒细胞减少症、扩张型心肌病和血清病。慢性免疫应答可由选自以下的医学病症激活:慢性炎性脱髓鞘性多神经病(cidp)、系统性狼疮、指示进行急性治疗的障碍的慢性形式、反应性关节病、原发性胆汁性肝硬化、溃疡性结肠炎和抗中性粒细胞胞浆抗体(anca)相关的血管炎。
32.在某些情况下,药用组合物可用于减少或治疗由自身免疫性疾病激活的免疫应答。自身免疫性疾病可选自斑秃、强直性脊柱炎、抗磷脂综合征、阿狄森氏病(addison's disease)、溶血性贫血、自身免疫性肝炎、肝炎、贝切特病(behcet’s disease)、大疱性类天疱疮、心肌病、口炎性腹泻
‑
皮炎(celiac sprue
‑
dermatitis)、慢性疲劳免疫功能障碍综合征、慢性炎性脱髓鞘性多神经病、churg
‑
strauss综合征、瘢痕性类天疱疮、局限性硬皮病(crest综合征)、冷凝集素病、克罗恩病(crohn's disease)、皮肌炎、盘状狼疮、特发性混合型冷沉淀球蛋白血症、纤维肌痛、纤维肌炎、格雷夫斯病(graves' disease)、桥本氏甲状腺炎(hashimoto's thyroiditis)、甲状腺功能减退症、炎症性肠病、自身免疫性淋巴细胞增生综合征、特发性肺纤维化、iga肾病、胰岛素依赖型糖尿病、幼年型关节炎、扁平苔藓、狼疮、梅尼埃病(m
é
ni
è
re's disease)、混合性结缔组织病、多发性硬化、恶性贫血、结节性多动脉炎、多软骨炎、多腺体综合征、风湿性多肌痛、多肌炎、原发性无丙种球蛋白血症、原发性胆汁性肝硬化、银屑病、雷诺现象(raynaud's phenomenon)、莱特尔综合征(reiter's syndrome)、风湿热、类风湿性关节炎、结节病、硬皮病、干燥综合征(sj
ö
gren's syndrome)、僵人综合征、大动脉炎(takayasu arteritis)、颞动脉炎、溃疡性结肠炎、葡萄膜炎、白癜风和韦格纳肉芽肿病(wegener's granulomatosis)。
33.特别地,药用组合物可用于减少或治疗由系统性红斑狼疮、抗磷脂综合征、寻常型天疱疮/大疱性类天疱疮、抗中性粒细胞胞浆抗体(anca)相关的血管炎、重症肌无力或视神经脊髓炎激活的免疫应答。
34.在某些情况下,药用组合物可用于降低胎儿贫血的风险或降低胎儿发生贫血的风险。在某些情况下,药用组合物可用于减少或消除对iut (宫内输血)的需要。在某些情况下,药用组合物和方法可用于减少或消除对产前pp ivig、产后输血、ivig和/或光疗的需要。
35.在某些情况下,药用组合物可用于减少或治疗由自身免疫性疾病激活的免疫应答。自身免疫性疾病可选自斑秃、强直性脊柱炎、抗磷脂综合征、阿狄森氏病、溶血性贫血、自身免疫性肝炎、肝炎、贝切特病、大疱性类天疱疮、心肌病、口炎性腹泻
‑
皮炎、慢性疲劳免疫功能障碍综合征、慢性炎性脱髓鞘性多神经病、churg
‑
strauss综合征、瘢痕性类天疱疮、局限性硬皮病(crest综合征)、冷凝集素病、克罗恩病、皮肌炎、盘状狼疮、特发性混合型冷沉淀球蛋白血症、纤维肌痛、纤维肌炎、格雷夫斯病、桥本氏甲状腺炎、甲状腺功能减退症、炎症性肠病、自身免疫性淋巴细胞增生综合征、特发性肺纤维化、iga肾病、胰岛素依赖型糖
尿病、幼年型关节炎、扁平苔藓、狼疮、梅尼埃病、混合性结缔组织病、多发性硬化、恶性贫血、结节性多动脉炎、多软骨炎、多腺体综合征、风湿性多肌痛、多肌炎、原发性无丙种球蛋白血症、原发性胆汁性肝硬化、银屑病、雷诺现象、莱特尔综合征、风湿热、类风湿性关节炎、结节病、硬皮病、干燥综合征、僵人综合征、大动脉炎、颞动脉炎、溃疡性结肠炎、葡萄膜炎、白癜风和韦格纳肉芽肿病。
36.在某些情况下,药用组合物可用于减少或治疗胎儿或新生儿的免疫应答。在某些情况下,药用组合物和方法可用于减少或治疗由怀孕母亲的自身免疫性疾病激活的胎儿或新生儿的免疫应答。
37.特别地,药用组合物可用于减少或治疗由系统性红斑狼疮、抗磷脂综合征、寻常型天疱疮/大疱性类天疱疮、抗中性粒细胞胞浆抗体(anca)相关的血管炎、重症肌无力或视神经脊髓炎激活的免疫应答。在某些情况下,药用组合物可用于减少或治疗胎儿或新生儿的免疫应答。在某些情况下,药用组合物和方法可用于减少或治疗由怀孕母亲的系统性红斑狼疮、抗磷脂综合征、寻常型天疱疮/大疱性类天疱疮、抗中性粒细胞胞浆抗体(anca)相关的血管炎、重症肌无力或视神经脊髓炎激活的免疫应答。
38.药用组合物可用于通过给予怀孕受试者与人类fcrn结合的分离的抗体来减少病原性抗体穿过怀孕受试者的胎盘的转运(例如病原性母体igg抗体转运),增加怀孕受试者体内的病原性抗体分解代谢以及治疗胎儿或新生儿的抗体介导的病毒性疾病的增强的方法中。可从本文所述的药用组合物的fcrn抑制中受益的疾病和障碍包括由母体病原体抗体(例如母体病原性igg抗体)从怀孕受试者穿过胎盘转移至胎儿和/或新生儿引起的胎儿和/或新生儿的疾病和障碍。
39.在某些情况下,可从用本文所述的药用组合物治疗中受益的疾病和障碍为胎儿和新生儿同种免疫和/或自身免疫性障碍。胎儿和新生儿的同种免疫性障碍为由怀孕受试者体内的病原性抗体引起的胎儿和/或新生儿的障碍。怀孕受试者体内的病原性抗体可攻击胎儿的抗原(例如胎儿从胎儿父亲那里遗传的抗原),从而导致胎儿或新生儿患有胎儿和新生儿的同种免疫和/或自身免疫性障碍。
40.可治疗的胎儿和新生儿的同种免疫和/或自身免疫性障碍的实例包括(但不限于)胎儿和新生儿同种免疫性血小板减少症(fnait)、胎儿和新生儿的溶血性疾病(hdfn)、同种免疫性泛血小板减少症(alloimmune pan
‑
thrombocytopenia)、先天性心脏传导阻滞、胎儿关节弯曲、新生儿重症肌无力、新生儿自身免疫性溶血性贫血、新生儿抗磷脂综合征、新生儿多肌炎、皮肌炎、新生儿狼疮、新生儿硬皮病、贝切特病、新生儿格雷夫斯病、新生儿川崎病(neonatal kawasaki disease)、新生儿自身免疫性甲状腺疾病和新生儿i型糖尿病。
41.在某些情况下,可从用本文所述的药用组合物治疗中受益的疾病和障碍为其中抗体促进病毒进入宿主细胞,导致细胞中的感染性增加或增强,例如抗体介导的病毒性疾病增强的病毒性疾病。在某些情况下,抗体可结合于病毒表面蛋白,并且抗体/病毒复合物可通过抗体与受体之间的相互作用而与细胞表面上的fcrn结合。随后,抗体/病毒复合物可被内化到细胞中。例如,病毒可通过与母体igg抗体形成复合物而进入胎儿的细胞和/或组织中。母体igg抗体可与病毒表面蛋白结合,并且igg/病毒复合物可与胎盘合体滋养层中的fcrn结合,其然后将复合物转移到胎儿中。
42.在某些情况下,本文所述的药用组合物可用于治疗抗体介导的病毒性疾病的增
强。在某些情况下,由病原性抗体(例如病原性igg抗体)增强的病毒性疾病包括(但不限于)由以下引起的病毒性疾病:甲病毒(alpha virus)感染、黄病毒(flavivirus)感染、寨卡病毒(zika virus)感染、基孔肯雅病毒(chikungunya virus)感染、罗斯河病毒(ross river virus)感染、严重急性呼吸综合征冠状病毒(severe acute respiratory syndrome coronavirus)感染、中东呼吸综合征(middle east respiratory syndrome)、禽流感(avian influenza)感染、流感病毒(influenza virus)感染、人类呼吸道合胞病毒(human respiratory syncytial virus)感染、埃博拉病毒(ebola virus)感染、黄热病毒(yellow fever virus)感染、登革病毒(dengue virus)感染、人类免疫缺陷病毒(human immunodeficiency virus)感染、呼吸道合胞病毒(respiratory syncytial virus)感染、汉坦病毒(hantavirus)感染、格塔病毒(getah virus)感染、辛德毕斯病毒(sindbis virus)感染、布尼亚病毒(bunyamwera virus)感染、西尼罗河病毒(west nile virus)感染、日本乙型脑炎病毒(japanese encephalitis virus b)感染、兔痘病毒(rabbitpox virus)感染、乳酸脱氢酶升高病毒(lactate dehydrogenase elevating virus)感染、呼肠孤病毒(reovirus)感染、狂犬病毒(rabies virus)感染、口蹄疫病毒(foot
‑
and
‑
mouth disease virus)感染、猪繁殖与呼吸综合征病毒(porcine reproductive and respiratory syndrome virus)感染、猴出血热病毒(simian hemorrhagic fever virus)感染、马传染性贫血病毒(equine infectious anemia virus)感染、山羊关节炎病毒(caprine arthritis virus)感染、非洲猪瘟病毒(african swine fever virus)感染、慢病毒(lentivirus)感染、bk乳多空病毒(bk papovavirus)感染、墨累谷脑炎病毒(murray valley encephalitis virus)感染、肠道病毒(enterovirus)感染、巨细胞病毒(cytomegalovirus)感染、肺炎病毒(pneumovirus)感染、麻疹病毒(morbillivirus)感染和麻疹病毒(measles virus)感染。
43.抗fcrn抗体对人类fcrn的阻断在由病原性抗体(例如病原性igg抗体)驱动的疾病中可具有治疗益处。fcrn阻断以诱导总体病原性抗体分解代谢并去除多种病原性抗体而不会干扰血清白蛋白、小的循环代谢物或脂蛋白的能力,提供一种方法以将病原性抗体去除策略的效用和可及性扩大至具有病原性抗体驱动的自身免疫性疾病病理学的患者。尽管不受理论的束缚,但抗fcrn抗体的主要作用机制可能是增加循环中病原性抗体的分解代谢和减少病原性抗体和免疫复合物在受影响组织中的沉积。
44.本文所述的药用组合物可给予患有在怀孕受试者中激活免疫应答的医学病症或处于患有该医学病症的风险下的怀孕受试者。在某些情况下,怀孕受试者可能在过去曾患有在怀孕受试者中激活免疫应答的医学病症。在某些情况下,怀孕受试者具有曾怀有患有胎儿和新生儿的同种免疫和/或自身免疫性障碍的先前胎儿或新生儿的病史。在某些情况下,如果在从怀孕受试者获得的生物样品(例如血液或尿液样品)中检测到与免疫性疾病相关的病原性抗体,则可将本文所述的抗fcrn抗体给予怀孕受试者。在某些情况下,已知在怀孕受试者的生物样品中检测到的病原性抗体会与来自怀孕受试者胎儿的抗原(例如胎儿从胎儿父亲那里遗传的抗原)结合。
45.在某些情况下,可将药用组合物给予正在计划怀孕并且患有在怀孕受试者中激活免疫应答的医学病症或处于患有该医学病症的风险下和/或在过去曾患有在怀孕受试者中激活免疫应答的医学病症的受试者。在某些情况下,受试者正在计划怀孕并且具有曾怀有
患有胎儿和新生儿的同种免疫和/或自身免疫性障碍的先前胎儿或新生儿的病史。在某些情况下,本文所述的抗fcrn抗体可给予正在计划怀孕并且其生物样品含有与免疫性疾病相关的病原性抗体的受试者。
46.在某些情况下,本文所述的药用组合物可给予受试者(例如怀孕受试者)以在受试者中减少或治疗急性或慢性免疫应答的基于免疫复合物的激活。急性免疫应答可由医学病症(例如寻常型天疱疮、狼疮性肾炎、重症肌无力、格林
‑
巴利综合征、抗体介导的排斥、灾难性抗磷脂抗体综合征、免疫复合物介导的血管炎、肾小球炎、离子通道病、视神经脊髓炎、自身免疫性听力损失、特发性血小板减少性紫癜、自身免疫性溶血性贫血、免疫性嗜中性粒细胞减少症、扩张型心肌病、血清病、慢性炎性脱髓鞘性多神经病、系统性狼疮、反应性关节病、原发性胆汁性肝硬化、溃疡性结肠炎或抗中性粒细胞胞浆抗体(anca)相关的血管炎)激活。
47.在某些情况下,本文所述的制剂可给予受试者(例如怀孕受试者)以减少或治疗由自身免疫性疾病激活的免疫应答。自身免疫性疾病可为例如斑秃、强直性脊柱炎、抗磷脂综合征(例如抗磷脂抗体综合征)、大疱性表皮松解症、膜性肾病、阿狄森氏病、溶血性贫血、温抗体型自身免疫性溶血性贫血(warm autoimmune hemolytic anemia) (waiha)、抗因子抗体、肝素诱导性血小板减少症(hict)、致敏性移植、自身免疫性肝炎、肝炎、贝切特病、大疱性类天疱疮、心肌病、口炎性腹泻
‑
皮炎、慢性疲劳免疫功能障碍综合征、慢性炎性脱髓鞘性多神经病、churg
‑
strauss综合征、瘢痕性类天疱疮、局限性硬皮病(crest综合征)、冷凝集素病、克罗恩病、皮肌炎、盘状狼疮、特发性混合型冷沉淀球蛋白血症、纤维肌痛、纤维肌炎、格雷夫斯病、桥本氏甲状腺炎、甲状腺功能减退症、炎症性肠病、自身免疫性淋巴细胞增生综合征、特发性肺纤维化、iga肾病、胰岛素依赖型糖尿病、幼年型关节炎、扁平苔藓、狼疮、梅尼埃病、混合性结缔组织病、多发性硬化、恶性贫血、结节性多动脉炎、多软骨炎、多腺体综合征、风湿性多肌痛、多肌炎、原发性无丙种球蛋白血症、原发性胆汁性肝硬化、银屑病、雷诺现象、莱特尔综合征、风湿热、类风湿性关节炎、结节病、硬皮病、干燥综合征、僵人综合征、大动脉炎、颞动脉炎、溃疡性结肠炎、葡萄膜炎、白癜风或韦格纳肉芽肿病。
实施例
48.在以下实施例中进一步描述本发明,这些实施例不限制权利要求中描述的本发明的范围。
49.在本文阐述的实施例中使用以下材料和方法。
50.材料m281的产生:通过离心和过滤澄清产生轻链和重链的细胞培养物,然后用去污剂处理进行病毒灭活。病毒灭活后,将材料应用于蛋白a柱上以去除过程相关的杂质(例如宿主细胞蛋白(hcp)、dna和培养基添加剂)。将洗脱液应用于阴离子交换柱和病毒去除过滤器。在病毒去除后和在使用25 mm磷酸钠和25 mm氯化钠的缓冲液(ph 6.5)的浓缩和渗滤之前,在标称分子量截留值为30 kda的聚醚砜膜上进行进一步过滤。通过添加海藻糖至最终浓度为8.7% w/w和添加聚山梨酯80至最终浓度为0.01%重量/体积(w/v)来配制材料。用配方缓冲液(25 mm磷酸钠、25 mm氯化钠、8.7%海藻糖、0.01% w/v聚山梨酯80,ph 6.5)将m281稀释至目标值为30 mg/ml (范围27
‑
33 mg/ml)。
51.实施例1. 大小变体种类的检测在使用本文所述的方法产生并含有m281抗体的通过具有sds的非还原性毛细管电泳(nr ce
‑
sds)分析的组合物中可重复地检测到大小变体种类。
52.结果制备m281的组合物并通过nr ce
‑
sds进行分析。通过nr ce
‑
sds分析的m281组合物的电泳图谱读出显示两个单独的峰——一个峰的保留时间为26
‑
27分钟和另一个峰的保留时间为27.5
‑
29分钟(图1)。后一个峰对应于完全组装的轻
‑
重
‑
重
‑
轻链(lc
‑
hc
‑
hc
‑
lc),而前一个峰对应于与重
‑
重
‑
轻链(称为hc
‑
hc
‑
lc或hhl)相比较重量更低的大小变体分子。在所有下游加工步骤(gmp ds和dp批次)期间以及稳定性研究期间(数据未显示),如通过nr ce
‑
sds检测到的大小变体分子的水平保持在总蛋白含量的约4.0
‑
4.5%。另外,在从250 l试验水平放大至gmp 2000 l规模期间,如通过nr ce
‑
sds检测到的该大小变体的水平没有明显变化。该大小变体的水平。当在样品制备期间或在进行ce
‑
sds分析之前组合物暴露于变性条件,比如温育温度升高(例如从37℃至70℃)时,m281组合物中大小变体的形成增加。
53.实施例2. 在m281组合物中检测到的大小变体种类的分子量表征为了确定m281组合物中大小变体种类的分子量,通过3种方法分析了m281组合物,所述方法包括亲水相互作用液相色谱
‑
质谱联用(hilic lc
‑
ms)、具有直接电喷雾电离质谱的微芯片区带电泳分离以及先后通过凝胶电泳和纳米液相色谱
‑
质谱联用分离的蛋白的非还原性胰蛋白酶消化。
54.结果通过hilic lc
‑
ms对m281组合物进行的分析显示,在hilic分离的uv色谱图上,峰集中在保留时间为12.5分钟处(图2a),该峰通过质谱解析为两种:一个峰集中在保留时间为12.42分钟处和另一个集中在保留时间为12.68分钟处(图2b)。通过对两个峰进行质谱的去卷积来确定在12.42分钟和12.68分钟保留时间峰中的分子量分布。对保留时间12.42分钟处峰中种类的质谱进行去卷积显示多种大小变体,其中包括119277 da的主要种类(图3a)。119277 da的上述主要种类与以脱氢丙氨酸替代未配对的重链中219位处的半胱氨酸的重
‑
重
‑
轻链(称为hc
‑
hc
‑
lc或hhl)(一种来自二硫键β
‑
消除的预期产物(图4))的119177 da理论质量接近。对保留时间为12.68分钟处峰中种类的质谱进行去卷积显示多种大小变体,其中包括119329 da的主要种类(图3b)。119329 da的上述主要种类与具有半胱氨酸化的未配对重链的重
‑
重
‑
轻链(称为hc
‑
hc
‑
lc或hhl)的119329 da理论质量接近。
55.为了进一步表征m281组合物中大小变体种类的分子量,通过具有直接电喷雾电离质谱(esi
‑
ms)的微芯片区带电泳(mze)分离分析m281组合物。mze分离的电泳图谱显示有少量酸性种类,迁移时间为约3.23分钟(图5)。对在约3.23分钟洗脱的峰中种类的质谱进行去卷积显示多种大小变体,其中包括分子量为119178 da和119332 da的两种主要种类。上述主要种类分别与以脱氢丙氨酸替代未配对的重链中219位处的半胱氨酸的重
‑
重
‑
轻链(hhl)的119177 da理论质量和具有半胱氨酸化的未配对重链的重
‑
重
‑
轻链(称为hc
‑
hc
‑
lc或hhl)的119329 da理论质量接近。
56.为了进一步表征m281组合物中大小变体种类的分子量,通过sds
‑
page凝胶电泳分离m281组合物,并从凝胶上切下对应于轻
‑
重
‑
重
‑
轻链和重
‑
重
‑
轻链的两条谱带(如图7所详示的)。对分离的凝胶片段进行非还原性凝胶内胰蛋白酶消化,并通过纳米液相色谱
‑
质
谱联用分析所得的消化片段(如图7所详示的)。对于轻
‑
重
‑
重
‑
轻链、具有半胱氨酸化的未配对的重链的重
‑
重
‑
轻链和以脱氢丙氨酸取代未配对的重链中(seq id no:2的)219位处的半胱氨酸的重
‑
重
‑
轻链,预期的胰蛋白酶消化的肽和分子量如图8所示。在对应于重
‑
重
‑
轻链的sds
‑
page凝胶电泳的谱带中,检测到对应于后两个种类的胰蛋白酶消化的肽作为主要种类,并在对应于轻
‑
重
‑
重
‑
轻链谱带的sds
‑
page凝胶电泳的谱带中检测到对应于后两个种类的胰蛋白酶消化的肽作为次要种类(表1和图9)。
57.表1. 每个单个特征性肽的提取离子色谱图(eic)峰面积相对于所有检测到的特征性肽的总eic峰的百分比总之,3种分析方法将m281组合物中的大小变体种类鉴定为具有与半胱氨酸化的重
‑
重
‑
轻链和脱氢丙氨酸重
‑
重
‑
轻链相似的分子量。
58.在另一个实例中,制备了m281制剂,并在5
±
3℃下储存后进行了稳定性测试。蛋白的重量百分比在119150
‑
119350 da范围内(hhl如表2所示)。
59.表2. 蛋白119150
‑
119350 da的重量百分比
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。