基于四芯光纤光操控的动态散斑荧光显微成像方法和系统
(一)技术领域
1.本发明涉及的是一种基于四芯光纤光操控的动态散斑荧光显微成像方法和系统,通过一根四芯光纤稳定捕获并精准操控活体单细胞的旋转角度,实现动态散斑宽场照明的快速扫描,可用于活体单细胞的捕获与控制和三维结构的高时间分辨率、高空间分辨率成像,属于生物光镊、生物成像领域。
(二)
背景技术:
2.细胞是组成有机体形态和功能的基本单位,自身又是由许多部分构成的。所以关于细胞结构的研究不仅要知道它是由哪些部分构成的,而且要进一步搞清每个部分的组成。相应地,关于功能不仅要知道细胞作为一个整体的功能,而且要了解各个部分在功能上的相互关系。
3.有机体的生理功能和一切生命现象都是以细胞为基础表达的。因此,不论对有机体的遗传、发育以及生理机能的了解,还是对于作为医疗基础的病理学、药理学等以及农业的育种等,对单个细胞的观察都至关重要。
4.怎样保持细胞生理特性的情况下研究细胞是揭示生命奥妙,攻克疾病的关键。通过对活细胞的研究,不仅可以观测到特别的现象,也有助于从细胞层面看待病理特征,这就对细胞活性提出了要求。为了更好的解析细胞表面特性,创造一种保持细胞活性的系统十分关键。
5.绝大多数细胞都非常微小,超出人的视力极限,观察细胞必须用显微镜。近年来,基于荧光显微成像技术、激光扫描共焦显微镜结构光照明成像技术已经成为研究细胞的重要工具。
5.使用透射式电子显微镜(transmission electron microscope,tem)在真空中观察经固定、脱水处理的细胞精细切片,获得细胞内部的高分辨精细结构图像。单细胞质谱分析技术(mass spectrometry,ms)和质谱流式细胞分析技术 (mass cytometry,mc)利用金属同位素对细胞进行标记,通过质谱分析方法实现单细胞成分的快速检测和定量分析。但是上述分析方法均无法实现活细胞的成分分析,因此无法准确揭示生物分子在细胞的生命周期中的功能和作用。
6.近年来,基于荧光标记技术的荧光光谱分析和显微成像技术已经成为单细胞研究的重要工具。流式细胞分析技术(flow cytometry,fcm)是一种用于对荧光标记的大量细胞进行高速定量分析和筛选的细胞分析技术。通过对大量细胞进行测量,可以得到一个细胞群体很好的统计分析结果,但是无法区分待测样品中少量的特异性细胞个体,无法实现单一特异性细胞的物理化学特性的深入分析和研究。
7.荧光显微成像技术利用生物体的自体荧光或引入外源荧光标记提供化学特异性和成像对比度,是目前单细胞分析与成像的主要研究手段,具有高特异性,高时间和高空间分辨率,以及三维层析成像能力。但是外源荧光标记必然会影响细胞的自身性质和生命活动过程,甚至会产生光致毒性,荧光团自身的光致漂白都是荧光显微成像技术无法回避的
问题。
8.具有层析分辨能力光学显微镜的出现对显微镜成像技术的发展具有划时代的意义,该技术的实现使得组织和细胞的光学连续切片和三维结构重建能够得以实现,对研究细胞各种现象提供了重要的工具。激光扫描共焦荧光显微镜与普通的宽场荧光显微成像方法相比,它的优点在于能够获得一定厚度样品的三维层析图像,可提供较高的时间和空间分辨率。但是这种显微成像方法需要对一个或多个照明点进行扫描,需要三维扫描系统,从而使得改显微镜成像速度慢、系统复杂、造价昂贵。
9.为了提高成像速度,人们提出了多种非扫描的宽场显微成像技术,比如结构光照明显微成像技术。但是在结构光照明显微成像技术中,由于样品对结构光的散射会降低图像的对比度,所以结构光显微成像技术不太适合用于对厚组织成像。
10.近年来,动态散斑照明的显微成像得到了普遍的使用。该成像技术不仅有深层层析分辨能力,而且采用宽场的成像方法,不需要复杂的装置,因此,成像速度快、结构简单、成本低廉。
11.以往,在宽场显微成像技术中,为了获得不同层面的层析图像,仍需要改变成像系统的位置以便获得多层面的图像。本发明则是利用不断调整细胞的位置来实现多层面的层析图像,而实现此目标需要用到光镊来作为工具。
12.光镊技术是一种可以稳定捕获待测活体单细胞,并对其实现操控的有力工具。基于光纤实现的光纤光操控技术对基片材料或厚度没有任何要求,可以灵活地在介质中任意移动,且体积小、可操作性强,具有很高的可集成度。近年来, 基于光纤的光操控技术已经实现了对细胞的捕获、移动、旋转和运输,这些技术被广泛应用在细胞分析、疾病诊断等过程中。
13.将动态散斑照明的宽场荧光显微成像方法与光镊(optical tweezers,ots) 技术有机地结合在一起,使研究人员从对活细胞进行被动的观察转而成为主动的操控,为解决上述问题提供了一种有效的途径。ots技术利用光场的力学效应,可以在不影响细胞内部及周围环境的条件下,以非接触、无损伤的方式稳定捕捉、精准操控和快速筛选单个病毒、细胞甚至生物大分子,为长时间观察处于液态环境中的活细胞获取其内部结构,进而深入研究细胞生命活动过程的生物调控机制等打开了大门。
14.本发明涉及的是一种基于四芯光纤光操控的动态散斑荧光显微成像方法和系统。利用四条特殊设计的单模光纤精准操控细胞,使其绕特定轴线旋转。当细胞旋转至每一个角度并达到稳定状态后,使用动态散斑照明的宽场荧光显微成像技术获取细胞的层析图像。通过获得不同角度上的细胞层析图像,最终重构细胞整体的三维结构图像。
(三)
技术实现要素:
15.本发明的目的在于提供一种成像速度快、分辨率高、结构简单等成像优点的一种基于四芯光纤光操控的动态散斑荧光显微成像方法和系统
16.在动态变化的散斑图案照明的宽场荧光显微系统中,当激光束通过一个不断改变的散射体时,在会复消色差显微物镜25的后焦面形成一系列随机变化的散斑图案,这些散斑图案用来照明待测细胞17。待测细胞17受激发后产生的荧光信号分为两个来源,一个是来自复消色差显微物镜25视场焦平面上的荧光信号,另一个则是来自于复消色差显微物镜
25视场焦平面以外的背景荧光信号。随着照明散斑图案的改变,散斑照明产生的散粒状分布的荧光强度在复消色差显微物镜25焦平面内发生剧烈变化,而在视场焦平面外的地方却变化缓慢,这种信号特征是实现层析成像的基础。通过cmos相机29记录待测细胞17特定层上一系列变化的散斑图案,利用特殊的算法能够提取该层面的荧光信号,从而具有层析成像功能。式中,n为图像序列中图像数,i
i
为第i幅图像的强度,i
rms
为采集得到n幅图像的均方根图像,也就是层析成像,n一般取80
‑
90就可以得到比较清晰的荧光层析图像。
17.动态散斑照明宽场荧光显微成像系统主要由激光光源18;透镜19、20、 23、24;散射体22;微位移台21;复消色差显微物镜25;双色镜26;滤光片 27;待测细胞17;成像镜头28;cmos相机29组成。所述系统中激光光源18 发出的激光光束经透镜19和20扩束后投射到散射体22上形成散斑图案,再经过透镜23和24扩束,经双色镜26反射后在复消色差显微物镜25后焦平面上形成散斑图案的像,经复消色差显微物镜25在待测细胞17上形成全场照明。当待测细胞17在光场控制下旋转至特定角度并达到稳定状态时,通过移动微位移台 21来改变散射体22的位置,使投射在待测细胞17上的散斑图案发生变化。不同散斑图案激发产生的荧光信号由复消色差显微物镜25收集,经双色镜26和滤光片27消除背景噪声,由成像镜头28和cmos相机29同步记录多幅荧光图像。由于散斑照明条件下,焦平面附近激发产生的荧光信号变化最剧烈,利用均方根算法即可提取焦平面附近的荧光层析图像。通过改变光场强度分布控制细胞17 绕轴线连续旋转,从而获取整个待测细胞17的三维结构荧光图像。
18.光操控系统主要由激光光源1;光纤分束器2、5、6;强度调制器11、 12;单模光纤3、4、7、8、9、10、13、14;光纤耦合器15;频率调制器30;时间延迟器31组成。所述光操控装置是一条固定在放置待测细胞的培养皿内,输出端加工成特定角度锥台的四芯光纤16。其中两个纤芯与水平面平行,另两个纤芯垂直于水平面。激光光源1输出的激光束通过光纤传输后,经光纤分束器 2按7:3的比例分成两束。其中一束强度较小的激光经单模光纤3传输后,经光纤分束器5分为强度相等的两束。两束激光经单模光纤7和8传输后,由光纤耦合器15耦合进输出端加工成特定角度锥台的四芯光纤中水平位置的两根纤芯。经纤芯传输后在输出端形成聚焦光场,作为捕获光以稳定捕获待测细胞17。另一束强度较大的激光经单模光纤4传输后,经频率调制器30调制产生具有一定重复频率的激光脉冲。激光脉冲经光纤分束器6按7:3的比例分为两束,分别耦合进单模光纤9、10。通过强度调制器11、12调节两束激光脉冲的强度,时间延迟器31调节两束激光脉冲之间的时间间隔。两束激光脉冲经光纤耦合器 15耦合进四芯光纤垂直位置的两根纤芯,经纤芯传输后在加工成特定角度锥台的光纤输出具有一定时间延迟的激光脉冲,分别作用在被捕获的待测细胞17两端,分别作为推动细胞17转动的推动脉冲和停止细胞转动的制动脉冲。由于水平位置的两个纤芯到光纤中心距离大于垂直位置的两个纤芯到光纤中心距离。因此,被捕获的待测细胞17在作用在细胞一端的推动光脉冲的作用下,绕捕获光形成的转动轴转动。当转动一个角度时,具有一定时间延迟的制动光脉冲作用在细胞的另一端,从而对细胞的转动施加制动力。通过改变推动光脉
冲和制动光脉冲的强度和两者之间的时间延迟,从而对细胞转动角度进行稳定而精准的主动光操控。
(四)附图说明
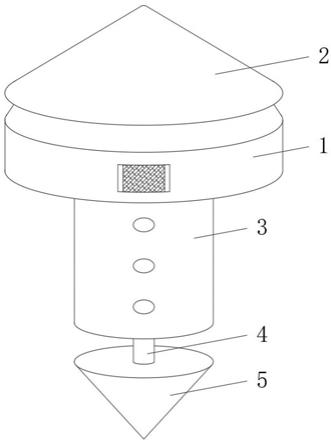
19.图1是一种基于四芯光纤光操控的动态散斑荧光显微成像方法和系统的结构示意图。
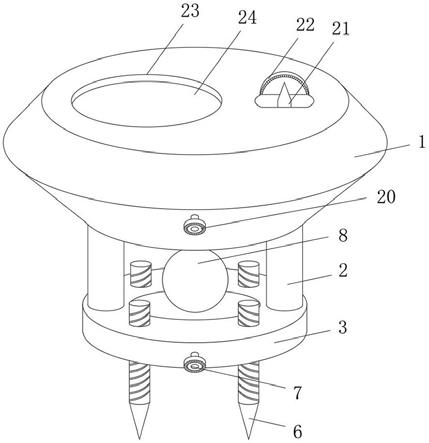
20.图2是光操控系统结构示意图(a)和动态散斑荧光显微方法(b)示意图。
21.图3是细胞三维结构成像的原理示意图。细胞每旋转至特定角度并达到稳定状态后,利用动态散斑照明宽场荧光显微技术获取活体单细胞的高分辨率层析结构图像,通过不断地旋转细胞来恢复出细胞的三维结构图像。
22.图4是接入装置的信号功率示意图。
23.附图标记说明:1
‑
激光光源;2
‑
光纤分束器;3
‑
单模光纤;4
‑
单模光纤; 5
‑
光纤分束器;6
‑
光纤分束器;7
‑
单模光纤;8
‑
单模光纤;9
‑
单模光纤;10
‑
单模光纤;11
‑
强度调制器;12
‑
强度调制器;13
‑
单模光纤;14
‑
单模光纤;15
‑
光纤耦合器;16
‑
四芯光纤;17
‑
待测细胞;18
‑
激光光源;19
‑
透镜;20
‑
透镜;21
‑
微位移台;22
‑
透镜;23
‑
透镜;24
‑
透镜;25
‑
复消色差显微物镜;26
‑
双色镜;27
‑
滤光片; 28
‑
物镜;29
‑
cmos相机;30
‑
频率调制器;31
‑
时间延迟器。
(五)具体实施方式
24.下面结合实例对本发明进行进一步的详细说明,以令本领域的技术人员参照说明书文字能够据以实施。
25.应当理解,本文所使用的诸如“具有”、“包含”以及“包括”术语并不排除一个或多个其它元件或其组合的存在或添加。
26.一种基于四芯光纤光操控的动态散斑荧光显微成像方法和系统,其特征是:所述系统由动态散斑照明宽场荧光显微成像系统和光操控系统两部分组成。所述系统主要由激光器1、18;光纤分束器2、5、6;强度调制器11、12;光纤耦合器15;待测细胞17;透镜19、20、23、24;微位移台21;散射体22;复消色差显微物镜25;双色镜26;滤光片27;成像镜头28;cmos相机29;单模光纤3、4、7、8、9、10、13、14;四芯光纤16;频率调制器30;时间延迟器31组成。激光器1输出的激光光束耦合进一根输出端加工成特定角度锥台的四芯光纤16的各纤芯。四芯光纤16固定在放置待测细胞的培养皿内,其中两束激光光束经水平位置两个纤芯传输后,在加工成锥台的输出端形成聚焦光场,实现稳定捕获待测细胞17。另外两束激光光束经调制后,形成具有一定时间间隔和重复频率的两束激光脉冲。两束激光脉冲经垂直位置的两个纤芯传输后,在输出端输出的光场分别作用在被捕获的细胞两端,施加方向相反的周期性的光推动脉冲和制动脉冲,从而实现对被捕获的待测细胞17转动角度进行稳定而精准的主动光操控。当待测细胞17转动至一个角度并稳定后,激光光源18输出的激光束经由扩束整形后,耦合进复消色差显微物镜25形成动态散斑照明照射到被捕获的待测细胞17上。激发动态散斑照明层面内的荧光物质产生的荧光信号经复消色差显微物镜25收集,由cmos相机29记录一副荧光层析图像。通过细胞转动角度的连续精准主动光操控,实现动态散斑在细胞的快速扫描,获取细胞的高空间分辨率三维结构图像。
27.系统中,激光光源18发出的激光光束经透镜19和20扩束后投射到散射体22上形成
散斑图案,再经过透镜23和24扩束,经双色镜26反射后在复消色差显微物镜25后焦平面上形成散斑图案的像,经复消色差显微物镜25在待测细胞17上形成全场照明。当待测细胞17在光场控制下旋转至特定角度并达到稳定状态时,通过移动微位移台21来改变散射体22的位置,使投射在待测细胞 17上的散斑图案发生变化。不同散斑图案激发产生的荧光信号由复消色差显微物镜25收集,经双色镜26和滤光片27消除背景噪声,由成像镜头28和cmos 相机29同步记录多幅荧光图像。由于散斑照明条件下,焦平面附近激发产生的荧光信号变化最剧烈,利用均方根算法即可提取焦平面附近的荧光层析图像。通过改变光场强度分布控制细胞17绕轴线连续旋转,从而获取整个待测细胞17 的三维结构荧光图像。
28.系统中,光操控装置是一条固定在放置待测细胞的培养皿内,输出端加工成特定角度锥台的四芯光纤16。其中两个纤芯与水平面平行,另两个纤芯垂直于水平面。激光光源1输出的激光束通过光纤传输后,经光纤分束器2按7: 3的比例分成两束。其中一束强度较小的激光经单模光纤3传输后,经光纤分束器5分为强度相等的两束。两束激光经单模光纤7和8传输后,由光纤耦合器 15耦合进输出端加工成特定角度锥台的四芯光纤中水平位置的两根纤芯。经纤芯传输后在输出端形成聚焦光场,作为捕获光以稳定捕获待测细胞17。另一束强度较大的激光经单模光纤4传输后,经频率调制器30调制产生具有一定重复频率的激光脉冲。激光脉冲经光纤分束器6按7:3的比例分为两束,分别耦合进单模光纤9、10。通过强度调制器11、12调节两束激光脉冲的强度,时间延迟器31调节两束激光脉冲之间的时间间隔。两束激光脉冲经光纤耦合器15耦合进四芯光纤垂直位置的两根纤芯,经纤芯传输后在加工成特定角度锥台的光纤输出具有一定时间延迟的激光脉冲,分别作用在被捕获的待测细胞17两端,分别作为推动细胞17转动的推动脉冲和停止细胞转动的制动脉冲。由于水平位置的两个纤芯到光纤中心距离大于垂直位置的两个纤芯到光纤中心距离。因此,被捕获的待测细胞17在作用在细胞一端的推动光脉冲的作用下,绕捕获光形成的转动轴转动。当转动一个角度时,具有一定时间延迟的制动光脉冲作用在细胞的另一端,从而对细胞的转动施加制动力。通过改变推动光脉冲和制动光脉冲的强度和两者之间的时间延迟,从而对细胞转动角度进行稳定而精准的主动光操控。
29.提供以上实例仅仅是为了描述本发明的目的,而并非限制本发明的范围。本发明的范围由所附权利要求限定。不脱离本发明的精神和原理而做出的各种等同替换和修改均应涵盖在本发明的范围内。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。