1.本发明涉及茵陈蒿用于制备治疗肺纤维化药物的用途。
背景技术:
2.肺纤维化是一种原因不明的慢性炎症间质性肺疾病,如间质性肺炎、结缔组织引发的肺部疾病都会导致肺纤维化。近年来肺纤维化的发病率呈逐渐上升趋势,致死率高,对人类健康危害严重,正引起全世界的广泛关注。肺纤维化患者临床主要表现为进行性呼吸困难,最终发展为低氧血症和呼吸衰竭而死亡,确诊后平均存活时间为3年。肺纤维化发病原因复杂,机制不明,尚缺乏有效的治疗药物。目前临床上治疗肺纤维化以免疫抑制类和糖皮质激素类药物为主,但疗效不明显且毒副作用。
3.茵陈蒿(学名:artemisia capillaris thunb.)是菊科,蒿属半灌木状草本植物,植株有浓烈的香气。茵陈蒿富含维生素及人体所需的多种微量元素和20余种氨基酸,具有很好的保健功能。茵陈蒿治病,最出名的就是茵陈蒿汤。在《伤寒论》中,茵陈蒿汤主要被用来治疗阳明病“瘀热在里”的“发黄”,而在《金匮要略方论》中,则被用来治疗黄疸病的“谷疸”。后世的医疗世家主要将茵陈蒿汤用来治疗湿热黄疸。而如今,茵陈蒿汤则更多的被用来治疗传染性肝炎,并在本方的基础上,时常增减药材,广泛运用于肝胆疾病的临床治疗。
4.还有研究报道,茵陈蒿与其他中药联合使用用于治疗肺癌。cn108524841a公开了一种治疗肺癌的药物。包括鱼腥草、牡丹皮、夏枯草、仙鹤草、紫草、牡蛎、前胡、女贞子、莪术、菟丝子、白花蛇舌草、川楝子、北沙参、茵陈蒿、百部、麦冬、葶苈子、百合、橘核、山药、紫菀、芦根、海藻、桑白皮、白茅根、阿胶、徐长卿、王不留行按一定重量配比制备而成。
5.茵陈为菊科植物滨蒿artemisia scoparia waldst.et kit.或茵陈蒿artemisia capillaris thunb.的干燥幼苗。茵陈最早记载于《神农本草经》。“主风湿寒热邪气,热结黄疸”蒙药阿荣目前收载于《内蒙古蒙药材标准》,也被称为茵陈。阿荣可单方用药,也可与其他蒙药配伍用药。单用可清肺、止咳、燥肺脓。
6.cn102552663a公开了一种用于治疗百草枯中毒的中药复方,包括蛤蚧、虫草、八角莲、川贝、茵陈、节菖蒲、桂枝、白芍、丝瓜络、旱莲草、乌梅、人参、阿胶、灶心土。虽然该专利文献提到中药复方以活血化瘀、去腐生肌、养肺通络、保肝护肾等中医治疗理论为支持,可以提高脏器自我修复能力和运化功能,抵抗肺纤维化的形成,但该专利文献是利用中药复方的协同作用来治疗百草枯中毒。
7.综上可知,未见茵陈蒿作为主要活性成分用于制备治疗肺纤维化的药物的相关报道。
技术实现要素:
8.本发明的目的在于提供一种茵陈蒿用于制备治疗肺纤维化药物的用途。茵陈蒿能够显著提高sod的含量,显著降低mda的含量,并一定程度上可以提高gsh的含量。本发明的目的是通过如下技术方案实现的。
9.本发明提供茵陈蒿用于制备治疗肺纤维化药物的用途。
10.根据本发明所述的用途,优选地,所述茵陈蒿为茵陈蒿药材粉末或茵陈蒿提取物。
11.根据本发明所述的用途,优选地,所述茵陈蒿为茵陈蒿提取物。
12.根据本发明所述的用途,优选地,所述药物形成治疗肺纤维化的药物制剂,所述药物制剂包含茵陈蒿,还包含药学上可接受的辅料。
13.根据本发明所述的用途,优选地,所述茵陈蒿为所述治疗肺纤维化药物中的唯一活性成分。
14.根据本发明所述的用途,优选地,所述药物形成用于提高血清中的sod的含量的药物制剂。
15.根据本发明所述的用途,优选地,所述药物形成用于降低血清中的mda的含量的药物制剂。
16.根据本发明所述的用途,优选地,所述茵陈蒿提取物由包括以下的步骤制备而得:
17.将过筛后的茵陈蒿药材粉末用水浸泡,加热回流提取2~5次,合并水提取液,固液分离,浓缩,得茵陈蒿提取物;其中,每次水的用量为过筛后的茵陈蒿药材粉末质量的8~16倍,每次浸泡的时间为2~6h,每次提取的时间为2~6h。
18.根据本发明所述的用途,优选地,单位剂量的药物制剂中,茵陈蒿提取物的用量为0.89~4.6g。
19.根据本发明所述的用途,优选地,茵陈蒿提取物的用量为1.8~4.3g。
20.本发明的茵陈蒿用于制备治疗肺纤维化药物,本发明研究发现茵陈蒿可以对气管滴注博来霉素建立的大鼠肺纤维化模型进行干预。茵陈蒿给药后炎症细胞浸润、肺泡间隔增厚、成纤维细胞增生和胶原沉积均有所改善。茵陈蒿能够显著提高sod的含量,显著降低mda的含量,并一定程度上可以提高gsh的含量。
附图说明
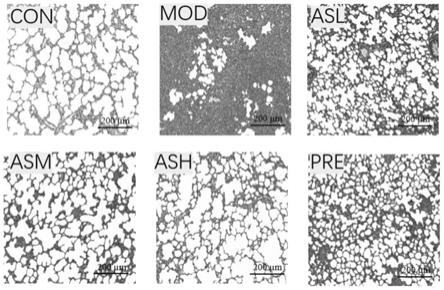
21.图1为不同用量的茵陈蒿对博来霉素诱导的肺纤维化大鼠he染色的影响结果。
22.图2为不同用量的茵陈蒿对博来霉素诱导的肺纤维化大鼠masson染色的影响结果。
23.图3为检测各个组别中大鼠血清中sod的含量结果。
24.图4为检测各个组别中大鼠血清中gsh的含量结果。
25.图5为检测各个组别中大鼠血清中mda的含量结果。
26.图1~图5中,con代表正常对照组,mod代表模型对照组,asl代表茵陈蒿低剂量组(100mg/kg),asm代表茵陈蒿中剂量组(200mg/kg),ash代表茵陈蒿高剂量组(400mg/kg),pre代表阳性对照组。
具体实施方式
27.下面结合具体实施例对本发明作进一步的说明,但本发明的保护范围并不限于此。
28.本发明的茵陈蒿用于制备治疗肺纤维化药物的用途。
29.在本发明中,茵陈蒿可以为茵陈蒿药材,比如茵陈蒿药材粉末。茵陈蒿可以为茵陈
蒿提取物。
30.根据本发明优选的一个实施方式,茵陈蒿为茵陈蒿提取物。
31.茵陈蒿提取物的制备方法没有特别限制。根据本发明的一个实施方式,茵陈蒿提取物由包括以下的步骤制备而得:将过筛后的茵陈蒿药材粉末用水加热回流提取2~5次,合并水提取液,固液分离,浓缩,得茵陈蒿提取物;其中,每次水的用量为过筛后的茵陈蒿药材粉末质量的8~16倍,每次提取的时间为2~6h。
32.在本发明中,可以加热回流提取2~5次,优选为加热回流提取2~4次,更优选为3~4次。每次提取时,水的用量可以为过筛后的茵陈蒿药材粉末质量的8~16倍,优选为8~13倍,更优选为9~11倍。每次提取的时间可以为2~6h,优选为3~6h,更优选为2~5h。
33.在本发明中,可以先将所述茵陈蒿药材碾碎后过2号筛。每次提取前,先用水浸泡过筛后的茵陈蒿药材粉末2~6h,优选为3~6h,更优选为3~5h。这样有利于更大程度地提取所需的茵陈蒿提取物。根据本发明的一个具体的实施方式,将茵陈蒿药材碾碎过2号筛,将过筛后的茵陈蒿药材粉末用水浸泡,加热回流提取2~5次,固液分离;合并水提取液并浓缩,得茵陈蒿提取物;其中,每次水的用量为过筛后的茵陈蒿药材粉末质量的8~16倍,每次浸泡的时间为2~6h,每次提取的时间为2~6h。在本发明中,固液分离可以为过滤,过滤时可以采用多层纱布进行,比如三层纱布。在本发明中,所得的茵陈蒿提取物基本不含水。将所得的茵陈蒿提取物放入4~6℃下冷藏,使用时可以加水稀释溶解。
34.在本发明中,药物形成治疗肺纤维化的药物制剂,所述药物制剂包含茵陈蒿,还包含药学上可接受的辅料。
35.本发明中,茵陈蒿可以为所述治疗肺纤维化药物中的唯一活性成分。在某些实施方案中,治疗肺纤维化药物以茵陈蒿为唯一活性成分。在另一些实施方案中,治疗肺纤维化药物也可以包含其他具有治疗肺纤维化作用的活性成分,或者包含本身不具有治疗肺纤维化作用、但能够辅助茵陈蒿发挥治疗肺纤维化作用的活性成分。
36.本发明的药物可以形成用于显著提高血清中的sod的含量的药物制剂,一定程度上提高血清中的gsh含量。而且,本发明的药物形成用于降低血清中的mda的含量的药物制剂。sod是超氧化物歧化酶。gsh是还原型谷胱甘肽。mda是丙二醛。
37.sod是生物体内存在的一种抗氧化金属酶,它能够催化超氧阴离子自由基歧化生成氧和过氧化氢,在机体氧化与抗氧化平衡中起到至关重要的作用。gsh,化学名称为n
‑
(n
‑
l
‑
γ
‑
谷氨酰基
‑
l
‑
半胱氨酰基)甘氨酸,分子式为c
10
h
17
n3o6s,分子量为307.33。mda作为过氧化脂质的降解产物,其含量可体现机体内脂质过氧化的程度,间接反映细胞或机体受损伤的轻重程度。
38.本发明中,所述治疗肺纤维化药物可以为原料药,也可以为制剂。所述制剂的剂型可以为任意药用剂型,不做特别限制。优选地,所述剂型为口服剂型。所述口服剂型可以为缓释或控释剂型,例如缓释胶囊剂、缓释片剂等。例如,所述剂型为片剂、丸剂、胶囊剂、颗粒剂、混悬剂等。
39.在某些实施方案中,所述治疗肺纤维化药物可以包含药学上可接受的辅料。所述药学上可接受的辅料的种类不做限制。当所述药物为口服制剂时,所述辅料可以选自稀释剂、粘合剂、崩解剂和润滑剂中的一种或多种。所述稀释剂包括但不限于甘露醇、微晶纤维素、乳糖、蔗糖、预胶化淀粉或糊精中的一种或多种,优选为微晶纤维素、乳糖或糊精中的一
种或多种。所述黏合剂选自甲基纤维素、羧甲基纤维素钠、乙基纤维素、羟丙基纤维素、羟丙基甲基纤维素、明胶、聚维酮或聚乙二醇中的一种或多种,优选为羧甲基纤维素钠、明胶或聚维酮中的一种或多种。所述崩解剂包括但不限于羧甲基淀粉钠、交联羧甲基纤维素钠、交联聚维酮中的一种或多种。所述润滑剂选自聚乙二醇、十二烷基硫酸钠、滑石粉或硬脂酸镁中的一种或多种,优选为交联聚维酮或交联羧甲基纤维素钠。根据本发明一个实施方式,所述药物中的辅料包含微晶纤维素、羧甲基纤维素钠以及交联聚维酮。
40.本发明中,单位剂量的药物制剂中,茵陈蒿提取物的用量为0.89~4.6g,优选为1.8~4.3g,更优选为1.95~4.1g。根据本发明的一个具体的实施方式,单位剂量的药物制剂中,茵陈蒿提取物的用量为1.92~3.9g。制备的治疗肺纤维化药物中,茵陈蒿的用量在上述范围时,便于服用和发挥功效,并减少副作用。
41.本发明中的治疗肺纤维化药物的功效可以减少间质内胶原纤维。能够显著提高sod的含量,显著降低mda的含量,一定程度上提高gsh的含量。
42.制备例
43.将茵陈蒿药材碾碎后过2号筛,得到过筛后的茵陈蒿药材粉末;将100g过筛后的茵陈蒿药材粉末用水浸泡,加热回流提取3次;每次水的用量为1000ml,每次浸泡5h,每次加热回流提取4h;合并提取液过滤,减压浓缩,得19.1g茵陈蒿提取物。放入4℃冰箱冷藏,使用时加水稀释溶解。茵陈蒿药材由内蒙古通辽内蒙古民族大学附属医院提供。
44.实施例1
45.1、动物造模及实验方法
46.动物采用健康sd大鼠,体重300~350g,购于长春市亿斯实验动物技术有限责任公司。
47.将大鼠随机分为正常对照组、博来霉素模型对照组(模型对照组)、茵陈蒿给药组(低中高三种剂量,茵陈蒿提取物的用量分别为100mg/kg、200mg/kg、400mg/kg,茵陈蒿提取物为制备例所得)及盐酸泼尼松阳性对照组(5mg/kg),共6组,每组10只。各组均灌胃给药相应受试药,每天1次,直至处死,模型对照组和正常对照组灌胃蒸馏水。除正常对照组外,其余各组通过向气管内一次性注入博来霉素5mg/kg构建大鼠肺纤维化模型;正常对照组采取向气管内一次性注入同体积生理盐水,每组大鼠分别在建模后第14天处死大鼠,取肺组织和血液进行后续实验。
48.2、观测指标及其测定方法
49.肺组织进行he、masson染色:将大鼠右肺后叶置于中性福尔马林液中固定,常规石蜡包埋切片进行he染色和masson染色以评价肺组织的损伤和肺纤维化程度。
50.2.1组织石蜡包埋和切片
51.2.1.1分别取出各组的右肺后叶在4%的多聚甲醛中固定24h;
52.2.1.2吸走多聚甲醛,加入pbs溶液(磷酸盐缓冲液)浸泡,每间隔8小时更换一次,连续72h,4℃保存;
53.2.1.3打开烘箱,将温度设定在62℃,溶解石蜡;
54.2.1.4将各个肺组织切成0.2~0.3cm的小块,然后用酒精梯度进行脱水(酒精的浓度为30%、50%、70%、80%、90%、95%、100%),每隔30min更换一次;
55.2.1.5放入50%酒精 50%二甲苯溶液30min后取出,然后放入二甲苯中注意观察
肺组织块至透明;
56.2.1.6放入预融50%酒精 50%二甲苯30min,然后分别放入预融的石蜡两次,每次2h;
57.2.1.7放入预融100%石蜡纸盒内凝固,4℃存放;
58.2.1.8用切片机将组织切成5~10μm厚的连续切片,将切片平展放置于平板上,光面朝上;
59.2.1.9将石蜡薄切片放于水面上(水温40℃),使其伸展,然后贴在预先处理好的玻片上;
60.2.1.10 40℃烘烤,过夜,以备染色。
61.2.2he染色步骤
62.2.2.1烤片:80℃恒温箱中放置1h;
63.2.2.2脱蜡:二甲苯i脱蜡10min、二甲苯ii脱蜡20min;
64.2.2.3脱水:100%乙醇5min脱水2次,95%乙醇5min脱水2次,85%乙醇中放置约1min,75%乙醇中放置约1min,以吸水纸吸干液体;
65.2.2.4冲洗:蒸馏水冲洗2min,冲洗两次;
66.2.2.5染色:苏木素染色5min;
67.2.2.6用自来水稍微冲洗;
68.2.2.7分化:1%盐酸酒精溶液浸润5~10s(观察切片由蓝变红);
69.2.2.8返蓝:自来水洗25min左右;
70.2.2.9 0.5%伊红染色2min;
71.2.2.10 95%乙醇5min脱水2次,用吸水纸吸干液体;
72.2.2.11 100%乙醇5min脱水2次,用吸水纸吸干液体;
73.2.2.12二甲苯中透明5min两次,用吸水纸吸干液体;
74.2.2.13中性树胶封固、镜下观察。
75.2.3masson染色步骤
76.2.3.1肺组织切片常规脱蜡至水;
77.2.3.2masson复合染液染色5~10min;
78.2.3.3置于2%冰醋酸水溶液浸洗片刻;
79.2.3.4置于1%磷酸水溶液中3~5min后甩干;
80.2.3.5用苯胺蓝水溶液染色5min;
81.2.3.6酒精梯度脱水,二甲苯i、ii透明,中性树胶封片。
82.2.4血清中mda含量检测(硫代巴比妥酸法)
83.2.4.1测试原理:mda(丙二醛)可与硫代巴比妥酸(tba)相结合而形成红色产物。该产物于532nm处有最大吸收峰。由于该反应的底物为tba,所以该检测方法也称为tba法。
84.2.4.2操作步骤:
85.(1)设定空白管、标准管、测定管,空白管中加入100μl无水乙醇,标准管中加入100μl标准品(四乙氧基丙烷10nmol/ml),测定管中加入100μl待测样品。
86.(2)加入100μl试剂一,涡旋混匀1min。
87.(3)分别加入1.5ml试剂二和试剂三涡旋混匀。
88.(4)95%恒温水浴40min,取出试管以流水冷却,在室温3500rpm离心10min吸取上清液加入96孔板,每孔200μl,每个样本设置3个复孔。532nm处测定od值,取均值作为测定od值。
89.以双蒸水调零。
90.*因样本不存在溶血、脂血现象,故标准管及空白管每批只做2个样本,同时以空白管来代替对照管。该操作步骤中,采用试剂盒进行检测,该试剂盒购自南京建成生物工程研究所,型号为a003
‑1‑
2。
91.2.5血清中sod含量检测(wst
‑
1法)
92.2.5.1操作步骤
93.(1)设定对照空、对照空白孔、测定孔和测定空白孔,对照孔和对照空白孔中加入20μl双蒸水,测定孔和测定空白孔中加入20μl待测样品。
94.(2)在对照空白孔和测定空白孔中加入20μl酶稀释液,在对照孔和测定空中加入20μl酶工作液。
95.(3)加入200μl底物应用液,涡旋混匀,37℃孵育20min,450nm处测定od值。
96.该操作步骤中,采用试剂盒进行检测,该试剂盒购自南京建成生物工程研究所,型号为a001
‑3‑
2。
97.2.6血清中gsh含量检测(比色法)
98.2.6.1操作步骤
99.(1)设定空白孔、标准孔和测定孔,空白孔加入100μl试剂一(贮备液),标准孔中加入100μl标准品(20μm gsh标准溶液),测定孔中加入100μl待测样品(上清液)。
100.(2)分别加入100μl试剂二和25μl的试剂三。
101.(3)混匀,静置5min,405nm处酶标仪测定各孔吸光度值。
102.该操作步骤中,采用试剂盒进行检测,该试剂盒购自南京建成生物工程研究所,型号为a006
‑2‑
1。
103.3、实验结果
104.3.1利用肺组织he染色评价茵陈蒿对肺纤维化大鼠的改善作用
105.图1为不同浓度的茵陈蒿对博来霉素诱导的肺纤维化大鼠he染色的影响结果。如图1所示,正常对照组大鼠肺泡形态正常,壁纤细,未见肺间质中有炎症细胞浸润。模型对照组中,博来霉素给药后即出现肺泡间隔增厚,可见炎细胞浸润;可见片状实变,实变区有较多炎细胞浸润、成纤维细胞增生和胶原沉积。茵陈蒿给药组(茵陈蒿低剂量组、中剂量组和高剂量组)中,可以看出茵陈蒿给药后炎症细胞浸润、肺泡间隔增厚、成纤维细胞增生和胶原沉积均有所改善。
106.3.2利用肺组织masson染色评价茵陈蒿对肺纤维化大鼠的改善作用
107.图2为不同浓度的茵陈蒿对博来霉素诱导的肺纤维化大鼠masson染色的影响结果。
108.如图2所示,正常对照组大鼠肺组织肺泡结构基本正常。模型对照组中,博来霉素造模后的各组出现不同程度的肺组织纤维化,其中以模型对照组肺组织肺泡塌陷、融合,肺泡壁增宽,间质内胶原纤维增多明显。茵陈蒿给药组(茵陈蒿低剂量组、茵陈蒿中剂量组和茵陈蒿高剂量组)的肺泡结构部分破坏,肺泡壁增宽增厚,胶原纤维增多均有所改善。茵陈
蒿给药组与模型对照组相比,间质内胶原纤维增加较少。茵陈蒿低剂量组、茵陈蒿中剂量组和茵陈蒿高剂量组的都能够明显改善博来霉素造模诱导的肺纤维化,与阳性对照组相比,茵陈蒿中剂量给药组效果更好。
109.3.3检测大鼠血清中sod、gsh和mda的含量
110.图3为检测各个组别中大鼠血清中sod的含量结果。图4为检测各个组别中大鼠血清中gsh的含量结果。图5为检测各个组别中大鼠血清中mda的含量结果。各个组别指的是正常对照组、模型对照组、茵陈蒿低剂量组、茵陈蒿中剂量组、茵陈蒿高剂量组和阳性对照组。
111.图3、图4和图5中##代表正常组和模型组有显著性差异,p<0.01,#代表正常组和模型组有显著性差异,p<0.05,**给药组与模型组有显著性差异,p<0.01。
112.当机体受损时,系统会产生大量氧自由基。这些氧自由基进而攻击生物膜中的多不饱和脂肪酸引起脂质过氧化,形成脂质过氧化物及新的氧自由基等,造成组织细胞的损伤。mda作为过氧化脂质的降解产物,其含量可体现机体内脂质过氧化的程度,间接反映细胞或机体受损伤的轻重程度。
113.抗氧化剂也被运用于肺间质纤维化的治疗中。
114.sod具有抗自由基损伤的能力,其活力的高低可间接反映机体清除氧自由基的能力及组织氧化反应的严重程度。gsh(谷胱甘肽)是体内存在的一种清除自由基的系统,在一些病理状况下谷胱甘肽过氧化物酶的活力会发生明显变化。
115.由图3可知,茵陈蒿低剂量组、中剂量组和高剂量组均能明显提高sod的含量。其中,茵陈蒿中剂量组和高剂量组对提高sod含量的效果超过了阳性对照组。
116.由图4可知,茵陈蒿低剂量组、中剂量组和高剂量组能够略微提高gsh的含量,明显不如阳性对照组的效果好。
117.由图5可知,茵陈蒿中剂量组能够显著降低mda的含量。茵陈蒿低剂量组几乎无法降低mda的含量,茵陈蒿高剂量组仅能稍微降低mda的含量,低中高剂量组并未表现明显的量效关系,可能与高剂量的剂量高有关,药物剂量过高可能使对mda的作用降低。
118.以上结果说明茵陈蒿能够改善博来霉素诱导的肺纤维化程度,而且我们初步推断其改善肺纤维化的机制可能与抗氧化有关。并且茵陈蒿高剂量组在提高sod含量方面的效果最优,超过了阳性对照组的结果。茵陈蒿中剂量组在降低mda含量方面效果最优。
119.本发明并不限于上述实施方式,在不背离本发明的实质内容的情况下,本领域技术人员可以想到的任何变形、改进、替换均落入本发明的范围。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。