1.本发明属于生物医药领域,具体地说,涉及一种口腔癌诊断标志物制备口腔癌早期诊断产品中的应用。
背景技术:
2.口腔癌是指发生于口腔的恶性肿瘤,包括唇部、颊黏膜以及舌前的2/3,还有就是硬腭、牙龈以及口底等,其中病理类型以黏膜上皮来源的鳞状细胞癌最为多见。国内的文献报道,口腔癌的发病率为1.06/100000
‑
1.69/100000,口腔癌占全身恶性肿瘤1.9%
‑
3.5%,占头颈部恶性肿瘤的4.7%
‑
20.3%。印度和东南亚,为口腔癌的高发区,发病率男性高于女性约2倍,患病的高峰年龄为50
‑
60岁。
3.目前,对于口腔癌的发病因素,并不完全明确,但是认为与病毒感染以及嚼槟榔、吸烟等有一定的关系。
4.2016年全球疾病负担(global burden of disease,gbd)最新统计结果表明,全球共有130多万人患口腔癌,死亡人数约为17.6万人,在一些口腔癌的高发地域,每年的新发病例高达男性恶性肿瘤的1/4。
5.近年来,口腔癌发病率有增高及明显年轻化的趋势,严重危害患者的生命和生存质量。虽然有很多肿瘤的诊治效果取得了很大的进展,但口腔癌的5年生存率一直在50%左右。口腔癌治疗后常使患者丧失一些关键的脏器功能,对患者的生活质量造成严重影响。
6.因此,口腔癌的早期诊断具有十分重要的意义。
7.口腔癌的发生被公认为一个多阶段、多步骤的过程。多数口腔癌经历了正常组织、癌前病变、癌前状态、癌的发展过程。口腔癌疗效的关键在于早发现、早诊断、早治疗。如果能及早发现早期口腔癌,即原位癌和早期浸润癌,通过手术治疗即可获得比较理想的效果。
8.因此,如何从大量口腔癌前病变、癌前状态患者中发现早期癌变,提高口腔癌早期诊断的准确率,这对提高口腔癌患者5年存活率和生存质量具有非常重要的意义。目前,用于检测早期口腔癌方法主要包括临床检查、组织学检查、细胞学检查、活体组织染色、免疫组织化学、光学检测系统、血液学、影像学等。然而现有诊断方法受创伤性、特异性、敏感性等局限,致使口腔癌的诊断特别是早期诊断效果不够理想。
技术实现要素:
9.本发明的目的是提供了一种口腔癌诊断标志物制备口腔癌早期诊断产品中的应用,本发明的标志物可以单独或两种或两种以上组合用于制备口腔癌早期诊断产品。
10.为了实现上述目的,本发明采用以下技术方案:
11.一种口腔癌诊断标志物制备口腔癌早期诊断产品中的应用,包括多个标志物,所述标志物作为检出靶标,所述标志物的核苷酸探针序列分别如seq id no.1
‑
seq id no.11所示。
12.作为本发明的一种优选方案,口腔癌早期诊断产品包括试剂盒、芯片或检测平台。
13.作为本发明的一种优选方案,口腔癌早期诊断产品包含检测所述一种或多种标志物的试剂,所述试剂用于检测受试者口腔组织标本中所述一种或多种标志物的浓度。
14.其中,所述试剂是基于基因芯片检测或pcr检测所述一种或多种标志物浓度时所需的试剂。
15.作为本发明的一种优选方案,所述标志物中的一种或几种在口腔癌组织和唾液中表达与正常组织和唾液中表达相比显著增高。
16.作为本发明的一种优选方案,所述标志物中的一种或几种在口腔癌组织和唾液中表达与正常组织和唾液中表达相比显著降低。
17.作为本发明的一种优选方案,所述试剂盒包括:reaction mix、enzyme mix、negative ctrl与positive ctrl,其中,reaction mix由反应混合液,含检测目标和内参基因的引物探针,dntp,mg
2
与h20组成。
18.作为本发明的一种优选方案,所述标志物为plau、krt15、spp1、il1rn、hopx、krt13、tgm3、mal、emp1、nmu和mmp1中的一种或几种。
19.作为本发明的一种优选方案,所述标志物为plau、spp1、mmp1、emp1、mal和krt13中的一种或几种。
20.作为本发明的一种优选方案,所述口腔癌的发展阶段是指口腔癌早期诊断产品可以判断待检测细胞为正常、口腔炎症、癌前病变、口腔癌和术后阶段。
21.作为本发明的一种优选方案,口腔癌早期诊断产品应用时,标本是口腔组织和唾液。
22.与现有技术相比,本发明可以获得包括以下技术效果:
23.本发明的目的是筛选口腔癌检测的分子指标。通过对临床口腔癌组织样本转录组检测和临床数据的整合与挖掘,结合差异表达与roc曲线分析,本发明筛选了11个可以用于鉴定口腔癌的分子标志物。这11个基因的曲线下面积(auc)均大于0.9,具有较高的灵敏度与特异性,提示其准确性与敏感度均达到90%以上。其中plau、spp1、emp1、mal和krt13的auc大于0.95。本发明的结果表明可利用这些基因的mrna表达水平进行定量检测,同时结合临床诊断结果,判断这些分子标志物作为口腔癌早期筛选的理想肿瘤标志物的可行性。探讨口腔脱落细胞中肿瘤标志物基因表达含量变化的机制,以及在预后判断上的临床价值。
附图说明
24.图1为口腔癌和正常癌旁组织关键基因spp1表达情况图。
25.图2为口腔癌和正常癌旁组织关键基因mmp1表达情况图。
26.图3为口腔癌和正常癌旁组织关键基因plau表达情况图。
27.图4为口腔癌和正常癌旁组织关键基因emp1表达情况图。
28.图5为口腔癌和正常癌旁组织关键基因mal表达情况图。
29.图6为口腔癌和正常癌旁组织关键基因krt13表达情况图。
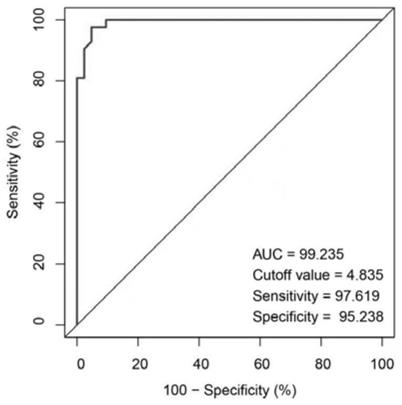
30.图7为口腔癌和正常癌旁数据每个标志物诊断效能的roc曲线。
31.所有标志物的表达差异具有统计学意义,p<0.01。
具体实施方式
32.下面将结合本发明实施例,对本发明实施例中的技术方案进行清楚、完整地描述,显然,所描述的实施例仅仅是本发明一部分实施例,而不是全部的实施例。基于本发明中的实施例,本领域普通技术人员在没有做出创造性劳动前提下所获得的所有其他实施例,都属于本发明保护的范围。
33.实施例1:
34.口腔癌诊断标志物:
35.本发明提供的口腔癌诊断标志物共11种,这类标志物可以单独或两种或两种以上组合来进行口腔癌的诊断;包括:aplau、krt15、spp1、il1rn、hopx、krt13、tgm3、mal、emp1、nmu和mmp1中的一种或几种。
36.其核苷酸探针序列如seq id no.1
‑
seq id no.11所示,具体如表1所示。
37.表1.核苷酸探针序列
38.seq id no.1tggcttgtccttcaggacatccacgtaseq id no.2ccgagacaagtgccgctaccacgcaseq id no.3cccacggctgtcccaatcagacgtcseq id no.4ccatcgctgtcagaggaaccaaccacseq id no.5cggattccaccacgctgtgcctcatgaseq id no.6tgaggaggccgccatcacaagcatcseq id no.7cctccagctccagcacaagseq id no.8caccaccaccttgatcatcctctaseq id no.9aacgcagtatcaccacggctatatseq id no.10tgctgaccttcttccattccgcgseq id no.11tctgacattcaccaaggtctctatc
39.实施例2
40.研究对象:包括100例患病组患者和30例正常健康人作为对照组。
41.患病组:2015~2020年在上海交通大学附属第九人民医院口腔科就诊的患者中选取100例患者,其中炎症20例、癌前损伤(白斑)20例,口腔癌30例、术后30例(所有病例均手术扩大切除原发灶,炎症组多为牙周炎和口底蜂窝织炎),癌前损伤组为白斑和口腔良性肿瘤,口腔癌多为舌鳞癌、颊癌、颌骨癌、牙龈癌,患者临床诊断均由病理诊断证实为口腔鳞状细胞癌,全身检查无其他恶性肿瘤,患者年龄平均57岁。
42.对照组:30例正常健康人作为正常对照组,他们均来自经口腔检查无牙周病、无炎症、无溃疡,全身检查无全身疾病的志愿者。
43.trizol法提取样本中的rna:使用trizol试剂从组织样本中提取总rna。
44.用剪刀将组织剪碎,加入1ml trizol,振荡器上震荡1min;常温放置10min,使核蛋白完全分解。加入200μl三氯甲烷(氯仿),盖紧管盖,剧烈震荡15s,常温静置10min。然后4℃,11000rpm离心15min。将水样层转移到一个新的离心管中,加入500μl异丙醇;颠倒混匀后,常温静置10min后4℃,11000rpm,离心15min。用枪小心吸走液体,留沉淀在管底,加入1ml 75%的乙醇,在振荡器上震荡5s,洗涤沉淀一次;然后4℃,8000rpm,离心5min,将上清小心去掉,干燥沉淀10min,加入适量的水溶解沉淀10min。
45.qrt
‑
pcr检测
46.根据本发明设计的靶基因序列,合成相应引物探针,配置qrt
‑
pcr检测试剂盒。
47.试剂组成:
48.reaction mix,反应混合液,含检测目标和内参基因的引物探针以及dntp、mg
2
、h20;
49.enzyme mix,含有rt酶、dna聚合酶、udg酶等;
50.negative ctrl,正常人口试子保存液样本;
51.positive ctrl,阳性对照(pc),含有目标基因与人内参基因片段
52.反应液配置
53.使用前请彻底融化试剂并离心甩至管底。根据样品数和对照数确定反应管数,每管按下列方法配制25μl反应体系。
54.18μl reaction mix,2μl enzyme mix,每反应按20μl分管,5μl标本/pc/nc。
55.扩增检测
56.本发明的试剂盒拥有极高的扩增效率,建议高速扩增以获得较高的灵敏度,若仪器不支持请选用标准程序。
57.高速扩增程序(全程约55min):50℃10min;95℃30sec;5cycles:95℃5sec,55℃30sec;40cycles:95℃3sec,60℃10sec(read)。
58.标准扩增(全程约1.2h):50℃10min;95℃30sec;45cycles:95℃10sec,55℃30sec(read)。
59.设计了2个试剂盒分别为oc1试剂盒,oc2试剂盒。
60.试剂盒oc1检测通道:plau:fam,mmp1:hex/vic,spp1:rox,ic:cy5。
61.试剂盒oc2检测通道:emp1:fam,mal:hex/vic,krt13:rox,ic:cy5。
62.注:abi机器参考荧光请设为none;请将淬灭基因均设为none;全程检测时间因不同仪器而略有差异。
63.质量控制
64.pc(包括内参基因)扩增且ct<30示实验成立,否则无效,需重做。
65.标本内参基因ic<30示实验可接受,>30为不可接受,宜重新采样检测。
66.内参ic以人类管家基因为目标(cy5为检测通道),来自人体的有效标均应阳性,使用ic可考察人源性标本的采集质量以及样品中是否存在过量pcr抑制物。若排除采样质量问题,示存在过强反应抑制可能,提示标本需经核酸纯化去除抑制物再行检测。
67.结果判定:
68.通过对临床样本delta ct(目标基因扩增ct值与内参基因扩增ct值)与阴性对照delta ct值(目标基因扩增ct值与内参基因扩增ct值)差异。
69.内参基因ct<35且样本delta ct与阴性对照delta ct值差异值绝对值》3为目标基因扩增阳性。目标基因扩增阳性基因位点数量》4,则临床样本判断为阳性样本。
70.临床样本内参基因ct<35,且目标基因扩增delta ct与阴性对照delta ct值差异值绝对值<3为目标基因扩增阴性。目标基因扩增阴性的基因位点数量》3,则临床样本判断为阴性样本。
71.【临床参考值】临床样本内参基因ct<35,且目标基因扩增delta ct与阴性对照
delta ct值差异值绝对值<3。
72.【方法局限性】
73.检测结果受样本中的细胞载量(过高或过低)、样本的采集质量和本身特殊组分、试剂的运输与保存条件、实验的环境状况(是否污染)、人员的操作情况(是否失误)、仪器的运行状态(是否良好)等因素影响,可能会出现假阴性或假阳性。本试剂盒的质量控制措施有利于发现假阴性,但不能完全排除假阴性或假阳性,因此,本试剂盒检测结果用于诊断时需结合临床或流调资料,不能单独作为诊断或排除诊断之依据。
74.从图1可见,优化的6个基因标志物预测曲线下面积(auc)均大于0.9。因此,从图1
‑
6可以看出本发明提供的口腔癌诊断标志物具有灵敏度高,精确度高的特点。
75.所述6种口腔癌标志物在口腔癌组织与正常组织中的详细变化见附图7。
76.从图1
‑
图6可知,这6个口腔癌诊断标志物在正常组织和肿瘤组织中具有显著的差异性,并且具有较好的预测精度。
77.以上所述,仅为本发明的较佳实施例,并非对本发明任何形式上和实质上的限制,应当指出,对于本技术领域的普通技术人员,在不脱离本发明方法的前提下,还将可以做出若干改进和补充,这些改进和补充也应视为本发明的保护范围。凡熟悉本专业的技术人员,在不脱离本发明的精神和范围的情况下,当可利用以上所揭示的技术内容而做出的些许更动、修饰与演变的等同变化,均为本发明的等效实施例;同时,凡依据本发明的实质技术对上述实施例所作的任何等同变化的更动、修饰与演变,均仍属于本发明的技术方案的范围内。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。