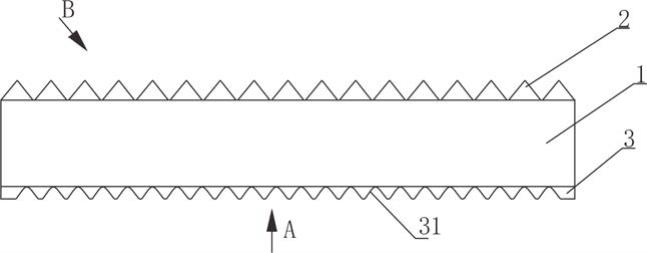
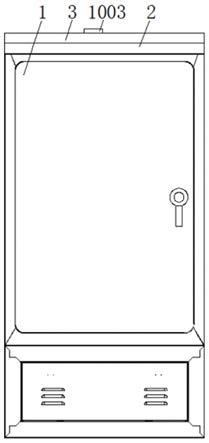
用于水产养殖的益生菌饲料
1.相关申请的交叉引用
2.本技术要求2018年12月24日提交的英国专利申请1821191.2的优先权。
技术领域
3.本发明涉及一种用于水产养殖的益生菌饲料组合物,以及一种水产养殖方法,该方法包括将此饲料供应给养殖的水产动物。
背景技术:
4.众所周知,鲍鱼和棘皮动物等海洋动物的水产养殖非常困难。鲍鱼因其高营养成分和独特的质地、风味和外观感官特性而成为备受追捧的海鲜商品。因此,鲍鱼在国际市场上的价格很高,尤其是在亚洲,它是一种非常珍贵的美食。过度捕捞和偷猎已使野生鲍鱼的数量减少到受到威胁的程度,目前养殖鲍鱼供应了大部分鲍鱼肉的消耗。
5.虽然成年鲍鱼在室外水道中养殖,但鲍鱼发育阶段(图1)从配子融合到后期幼体后期(post
‑
larval)阶段(通常在定居后约三个月)发生在室内孵化设施中。在产卵过程中,性成熟的成年亲鱼将配子释放到单独的产卵容器中。然后将自由游动的精子轻轻倒入受精容器中,而负浮力的卵子则通过虹吸作用被添加到受精容器中。雌雄配子融合后,受精卵沉入容器底部。收集受精卵并在不同的容器中分开,胚胎发育发生在一夜之间。在这个过程中,胚胎经历反复的分裂,形成游动到水层顶部的担轮幼虫。受精后约24小时,担轮幼虫发育完成。此后,顶部70
‑
80%的养殖水被虹吸到幼虫养殖容器中,担轮幼虫在这里孵化成自由游动的浮游幼虫。鲍鱼会在幼虫阶段停留数天(对于南非鲍(h.midae)在20℃下大约5天,在17.5℃下大约7天),之后它们就会有能力定居。在这个阶段,有能力的幼虫以所需的沉降密度分配到准备好的沉降池中。在商业孵化场,沉降表面通常是垂直悬挂在大型流通池中的扁平或波纹塑料板。在幼虫加入前大约三周,这些沉降表面在流通池中通过被动播种(即进入的海水提供定殖微生物)和光照进行“调节”。这个调节期促进了生物膜的生长。生物膜通常被称为微生物群落,它们定居在液体或空气表面界面,并被包裹在eps(细胞外聚合物)基质中。在孵化场培养中,生物膜的特征是微藻尤其是底栖硅藻和海洋细菌的异质种群。这些生物膜是幼体后期鲍鱼的主要食物源,直到它们在幼年期开始时戒断到人工饲料或大型藻类。
6.不幸的是,限制南非鲍最佳商业生产的主要因素之一是常在生产孵化阶段遇到的性能不佳。孵化场经常受到低成活率和低增长率的困扰,这威胁到养殖过程中养成阶段的优质幼鱼的正常供应。
7.众所周知,上述硅藻生物膜的发展难以管理,因为这些生物膜在质量和数量方面往往变化很大,因此,它们通常不能充分满足幼体后期鲍鱼的能量需求或特定营养需求。这种无法为幼体后期发育提供始终如一的营养饮食已被认为是导致低存活率和低生长率的主要因素,这威胁到鲍鱼养殖养成阶段优质幼鱼的正常供应。
8.因此,许多研究工作都集中在人工配方的开发上,这些配方可以为幼体后期鲍鱼
提供营养全面的饮食。例如,幼虫后期生产系统(pps)包括基于藻酸盐的饮食,其中包含蛋白质、碳水化合物和营养混合物。这种人造微粒饮食被涂在硬质波纹塑料板上。据报道,这种饮食可以提高总体存活率但没有提高生长速度。饮食还需要每隔一天重新涂抹一次。另一种人工饲料,称为斯托特(stott’s)幼体后期鲍鱼生产系统(sapps),依赖于琼脂的温度相关凝固特性(0.5
‑
1.0%)。这些琼脂配方与人工微量饮食混合并喷洒在硬质波纹塑料板上。sapps饮食改善了幼体后期鲍鱼的生长和存活,但仍然需要每1
‑
2天对板重新喷洒一次。由于在鲍鱼养殖面上配制和维持上述饲料需要大量的劳动力和高昂的成本,它们并不适合鲍鱼的大规模生产。
9.因此,虽然人工饲料的开发代表了当前孵化场饲养技术的有前途的可选方案,但该领域几乎没有取得任何进展,并且仍然需要一种在商业环境中经济可行的替代策略。
技术实现要素:
10.根据本发明的第一实施方案,提供了一种水生动物的水产养殖方法,该方法包括向水生动物至少供应弧菌sy9(vibrio midae sy9)作为食物源,从而使水生动物生长。
11.所述的弧菌sy9可以在薄膜上或薄膜内提供给水生动物。
12.所述的膜可以在支撑物上形成。
13.所述的膜可包含碳水化合物粘合剂,例如藻酸盐。
14.所述的膜上或膜内的弧菌sy9的浓度可以是至少108个细胞/cm2。
15.所述的方法还可包括向水生动物供应硅藻作为额外的食物源。
16.所述的硅藻可以在与弧菌sy9相同的薄膜上或薄膜内被提供。
17.所述的薄膜中硅藻浓度至少可为106个细胞/cm2。
18.或者,所述的方法可以在不向水生动物供应硅藻作为食物源的情况下进行。
19.所述的方法还可包括在5天或5天以上后更换薄膜的步骤。
20.所述的水生动物可以是咸水动物,例如鲍鱼和棘皮动物(例如海胆、海参等)。
21.根据本发明的第二个实施方案,提供了一种配制用于喂养水生动物的饲料组合物,该饲料组合物包括弧菌sy9作为食物源。
22.所述的弧菌sy9可涂覆在薄膜上或封装在薄膜内。
23.所述的膜可在平面上形成。
24.所述的膜可由碳水化合物粘合剂形成,例如藻酸盐。
25.所述的饲料组合物中弧菌sy9的浓度可以是至少109个细胞/cm2。
26.所述的饲料组合物还可包括硅藻作为幼体鲍鱼的额外食物源。
27.所述的饲料组合物中硅藻的浓度可至少是107个细胞/cm2。
28.所述的饲料组合物可在水性组合物中稳定5天或5天以上。
29.所述的水生动物可以是咸水动物,例如鲍鱼和棘皮动物(例如海胆、海参等)。
附图说明
30.图1显示了鲍鱼(haliotis spp)的生命周期(重绘自http://oceanlink island.net/conservation/abalone/bhcap/development.html)。
31.图2显示了由益生菌弧菌k811(v.midae k811)、卵形藻(cocconeis sp.)的任一种
或益生菌和卵形藻的混合物组成的人工生物膜喂食25天的南非鲍幼体后期(post
‑
larval h.midae)的存活率,在三个独立的实验中进行的测试。每个水箱的初始放养密度为150只鲍鱼。
具体实施方式
32.本文描述了一种水产养殖方法,包括向养殖的水生动物提供弧菌sy9以及包含弧菌sy9的饲料组合物作为食物源。
33.水生动物通常是以藻类为食的海洋动物,特别是在其生命周期中具有自由游动幼体阶段的动物。幼体定居在适当的基质上并变形。这些动物包括鲍鱼和棘皮动物,如海胆、海参、海星、脆星、沙钱和海百合。在一种实施方式中,将弧菌sy9提供给处于幼体后期的这些动物。
34.鲍鱼是鲍科(haliotidae)任何一类海洋腹足类软体动物的通用名称。其他常见名称是耳壳(ear shells)、海耳(sea ears)、羊肉鱼(muttonfish)、羊肉壳(muttonshells)、ormer(蠕虫)和保阿(p
ā
ua)。全世界公认的物种数量在30到130之间,南非最大的鲍鱼是南非鲍(haliotis midae)。在世界各地养殖的其他具有商业价值的鲍鱼品种包括九孔鲍(haliotis diversicolor)、澳大利亚黑鲍(haliotis rubra)、皱纹盘鲍(haliotis discus hannai)和红鲍(haliotis rufescens)。
35.术语“幼体后期”描述了在游动的幼体从水柱沉降到固体、水下表面并经历变态之后发生的生命周期的一部分(图1)。
36.如本文所用,益生菌被定义为活微生物补充剂,其通过改善宿主动物的肠道平衡而有益地影响宿主动物。
37.幼体后期的鲍鱼通过肌肉发达的足部在固体表面上活动,并以底栖硅藻和细菌的生物膜为食,时间大约为三个月。一旦幼体后期的鲍鱼长得足够长(壳长5
‑
10毫米),它就会变成幼鲍,从以底栖硅藻为食到戒断,以大型藻类(海藻)为食。
38.研究表明,益生菌具有改善幼鲍和成鲍养殖结果的潜力。然而,关于益生菌对鲍鱼(以及一般的水生物种)早期发育阶段的影响知之甚少。
39.申请人现在已经表明,在没有底栖硅藻定植生物膜的情况下,弧菌sy9可以改善幼体后期南非鲍的生长和存活。
40.弧菌sy9可以在基质(或表面)上或在膜(或生物膜)上或膜内提供给动物,通常在支撑物上形成。支撑物可以是固体表面,例如由玻璃或塑料材料制成的片材或板。在一个示例中,支撑物是平的,而在另一示例中,支撑物是波纹状的等等。固体表面可包含网状织物以提高膜的粘附性。或者,支撑物可以是网、纱布或网状材料,其可位于框架内。薄膜可以由粘合剂形成,例如藻酸盐、淀粉或琼脂等碳水化合物粘合剂。
41.弧菌sy9细胞可以是提供给动物的基本或主要营养物。可以选择提供硅藻作为额外的食物源。硅藻是具有二氧化硅细胞壁的单细胞藻类。虽然底栖硅藻的生物膜是从流入的海水中自发产生的,但用于幼体后期鲍鱼培养首选的常见硅藻物种有舟形藻(navicula)、两栖藻(amphiprora)和卵形藻(cocconeis)。该方法也可以在不提供硅藻作为食物源的情况下进行,特别是不引入在饲养动物的水箱中未自发发育的硅藻。
42.膜中弧菌sy9的浓度可至少为108个细胞/cm2,并且如果存在这样的浓度,硅藻的浓
度可至少为106个细胞/cm2。
43.该薄膜通常每5天更换一次,以确保持续供应相对较高浓度的益生菌。然而,可以设法改变薄膜的配方致使更换期延长,例如延长至10天或10天以上。
44.在三个独立的实验室规模实验中,给幼体后期南非鲍(平均壳长2.7毫米)喂食三种不同的人工生物膜饲料,这些饲料由藻酸盐和推定的益生菌弧菌sy9组成(饲料1),由底栖硅藻卵形藻和弧菌sy9 k811的混合物(饲料2)或仅由卵形藻(硅藻控制饲料)组成。在25天内监测鲍鱼的存活率,并通过测量鲍鱼壳长度来量化生长。结果证实,弧菌sy9通过显著提高存活率和促使生长速度三倍增长来对幼体后期的南非鲍具有益生菌效果。这些结果表明幼体后期的南非鲍可以在缺乏硅藻细胞的细菌薄膜饲料中存活和生长。因此,细菌可以取代硅藻成为南非鲍幼体后期的主要食物源。本研究中描述的益生菌饲料可为幼体后期鲍鱼提供更可靠和一致的营养来源,对商业鲍鱼养殖场具有重要的经济意义。改善幼体后期的生长和存活可以大大提高养殖场的生产力,并提高鲍鱼养殖的经济潜力。
45.据申请人所知,这是第一次描述使用益生菌微生物作为幼体后期鲍鱼和海胆的直接食物源。
46.现在将通过以下非限制性实施例更详细地描述本发明,其中鲍鱼用作示例性水产养殖动物并且弧菌sy9用作示例性益生菌。
47.实施例
48.材料和方法
49.微生物和生长培养基
50.弧菌sy9(bccm登录号mucl 54982)先前是从南非鲍成鲍(macey&coyne,2005)的胃肠道中分离出来的。在本研究中使用了一种基因修饰的弧菌sy9菌株,命名为k811菌株,以允许对人工饲料配方中的这种细菌进行量化。弧菌k811(v.midae k811)对链霉素具有抗性,并含有生物发光质粒pkluxcat。该质粒是paklux2的衍生物,包含来自发光杆菌(photorhabdus luminescens,karsi and lawrence 2007)的lux操纵子(luxcdabe)。添加tn9氯霉素乙酰转移酶(cat)基因对paklux2进行修饰,以便能够对转接合子进行抗生素选择(未公开的数据)。弧菌k811在补充有120μg/ml链霉素和15μ5/ml氯霉素的胰蛋白胨大豆肉汤(30g/l nacl、17g/l胰蛋白胨、6g/l蛋白胨、2.5g/l葡萄糖、2.5g/l k2hpo4、ph7.8)中常规生长,并在定轨振荡器中以150rpm和25℃温育。
51.之所以在此研究中选择卵形藻,是因为该属的成员是鲍鱼幼虫(壳长>0.8毫米)生物膜喂食的主要食物源。卵形藻是一种单藻但非无菌培养的藻类,由林业和渔业部(daff)研究水族馆(南非开普敦)提供。培养物在补充有1ml/l偏硅酸钠(40g/l na2sio3无水储备溶液)和20ml/l吉拉德(guillard's f/2)培养基(奥德里奇,sigma
‑
aldrich)的无菌人工海水(24.7g/l nacl、4.7g/l mgcl2·
6h2o、1.9g/l cacl2·
2h2o、6.3g/l mgso4·
7h2o、0.66g/l kcl、0.18g/l nahco3、ph 7.8)中生长。培养物在15℃于光照:无光=12h:12h的周期(光强4.91μmol/sec/m2)下培养,并通过悬挂空气软管给每个培养物提供通风。
52.人工生物膜饲料准备
53.制备了三种基于藻酸盐的生物膜饲料:仅由益生菌弧菌k811组成的薄膜(饲料1),由弧菌k811和卵形藻组合的混合生物膜(饲料2)和仅由卵形藻组成的生物膜(硅藻控制饮食)。在每个25天的生长实验过程中,每3天制备新鲜的生物膜或薄膜。
54.玻璃板的制备
55.使用海洋硅胶将几张蚊帐网状织物(11cm x 19cm)粘附在玻璃板(11cm x 19cm,3mm厚)的边缘。制备含有30g/l海藻酸钠(sigma
‑
aldrich)的人工海水(asw)溶液,并以0.05ml/cm2的容量添加到准备的表面上。使用l形玻璃涂布器将混合物均匀地分散在表面。之后将藻酸盐涂覆的表面在25℃下干燥24小时,再于
‑
20℃下储存直至需要。弧菌k811细胞悬浮液的制备
56.对于每组新的生物膜,弧菌k811的培养物在标准条件下生长4小时至od600=1.0,相当于大约5x108个益生菌细胞/ml。每种培养物的细胞通过离心(10 000xg,10℃,10分钟)分别获得。弃去上清液,每个细菌细胞沉淀用100ml的asw洗涤两次。此后,将每个细菌沉淀悬浮在10ml的asw中,以达到大约5x109个细胞/ml的浓度。益生菌细胞悬液用于制备仅有弧菌k811(饲料1)组成的单一物种生物膜。
57.卵形藻的细胞悬浮液的制备
58.对于每组新的生物膜,适当体积的卵形藻培养物在标准条件下生长五天直至大约107个细胞/ml的浓度。每种培养物的生物质通过离心(10 000xg,10℃,10分钟)分别获得。弃去上清液,每个生物质样品用100ml的asw洗涤两次。对于仅由卵形藻组成的生物膜,将硅藻细胞团悬浮在10ml的asw中以达到大约5x107个细胞/ml的浓度。硅藻细胞悬浮液用于制备仅由卵形藻组成的单一物种生物膜。它代表了本研究中的对照饲料。
59.混合物种细胞悬浮液的制备
60.卵形藻的颗粒细胞不是悬浮在asw中,而是悬浮在弧菌k811(如上所述制备)中。这产生了由两种微生物组成的混合物种细胞悬浮液,最终浓度约为5x109个益生菌细胞/ml和约5x107个细胞/ml的硅藻。这些混合物种细胞悬浮液用于制备混合物种生物膜(饲料2)。
61.生物膜的制备
62.将各自的细胞悬浮液以每40平方厘米1毫升的体积加入到准备的玻璃板中。使用l形玻璃涂布器将微生物均匀地分散在表面上。将所有板在室温(约25℃)下孵育20分钟,使细胞附着在藻酸盐包被的表面上,然后浸入asw中以去除附着较弱的细胞。
63.生物膜成分的定量
64.使用允许在体内同时检测发光和/或荧光的ivisx流量ii成像系统(xenogen ivis
‑
iilumina ii)观察所有生物膜,并使用生存镜像(living image)软件捕获图像。用于检测发光(弧菌k811)的采集参数包括10秒曝光、小分档、光圈值1(f/stop 1)、开放式过滤器和12.5cm视场(fov)。用于检测荧光(卵形藻)的采集参数包括10秒曝光、小分档、光圈值8(f/stop 8)、695
‑
770nm激发滤光片、cy5.5发射滤光片、12.5cm fov。使用光子通量测量记录的所有数据,光子通量代表每秒曝光捕获的光子数(p/s)。
65.为了量化每个时间点生物膜中存在的微生物细胞数量,将记录的通量(p/s)数据与绘制通量(p/s)对微生物细胞/cm2构建的校准曲线进行比较。使用活菌落计数(cfu/ml)对弧菌k811的细胞进行定量,而使用计数室(改良纽巴(neubauer),尺寸:0.0025mm
2 x 0.01mm)对卵形藻的细胞定量。发现在体内准确检测发光和荧光所需的发光弧菌k811细胞的最小数量分别约为104个细胞/ml(弧菌k811)和105个细胞/ml(卵形藻)。
66.三种人工生物膜在标准条件下用于实验室培养幼体后期鲍鱼的验证
67.准备了六个玻璃水箱(底部20x25厘米,高20厘米,玻璃厚度2毫米),以重复测试三
种不同生物膜饲料的水稳定性,并使用标准的幼体后期鲍鱼的饲养条件(如上所述)。两个含有相同成分的生物膜水平放置在每个玻璃水箱的底部,在那里共孵育五天。每24小时从罐中移除生物膜,并且弧菌k811和/或卵形藻残留在生物膜中的浓度如前所述进行量化。
68.幼体后期南非鲍的生长实验
69.在南非开普敦大学分子和细胞生物学实验室进行的三个独立的生长实验中,评估了三种不同的生物膜饲料对幼体后期南非鲍生长的影响。每个生长实验持续时间为25天。
70.玻璃水箱的规格
71.准备六个单独的玻璃壳体水箱(底座20x25厘米,高度20厘米,玻璃厚度2毫米),对于每个生长实验,以一式两份测试三种不同的生物膜饲料中的每一种。使用了封闭的再循环水系统。所有水箱都用过滤的(0.22μm)天然海水(nsw)填充至15厘米的深度。每4
‑
5天通过虹吸进行换水(50%)以保持良好的水质。此外,每个水箱都装有一个在整个生长实验中连续运行的小型潜水滤水器(boyu,型号sp
‑
6011)。每个水箱都通过悬挂空气软管进行充气,由空气压缩机(boyu,型号acq
‑
007)供气,并用空气石终止。环境温度保持在15℃。遵循12h:12h的亮:暗的光周期。每个水箱的顶部都覆盖着黑色塑料布,以限制水分蒸发以及鲍鱼所经历的光照强度,鲍鱼更喜欢低光照条件。在实验1中,水箱直接安装在顶置空气调节装置的下方。然而,在实验2和3中,为了限制水的蒸发,水箱被安置在距离空气调节装置2米的地方,这可能会影响实验1中获得的结果。
72.幼体后期南非鲍
73.雅各布湾(jacobsbaai)海产品(雅各布湾,南非)捐赠了三批不同批次的幼体后期南非鲍(源自同一亲鱼)。此前,鲍鱼在商业孵化场内的天然硅藻生物膜上定居和生长。在孵化场收集期间,使用大而柔软的画笔将动物从塑料沉降板表面刷掉,然后转移到塑料容器(底部22x26厘米,高10厘米)中。此容器里装了一半的海水,密封好,放在冷藏箱中的冷冻冰袋之间,以便运送到我们的实验室。从养殖场的表面取出鲍鱼至转移到实验槽之间的时间不超过3小时。使用小而软的油漆刷,将150只鲍鱼单独转移到6个玻璃水箱中的每一个。在每个实验开始时,鲍鱼被脚朝下单独放置,每天检查它们的方向。如有必要,可以使用软毛刷将鲍鱼脚朝下翻转。在生长试验开始之前,动物没有适应环境或饥饿。实验期间的死亡率要去除并量化。
74.喂养方式
75.鲍鱼是按照接力式的方式喂食的。在试验开始时,用塑料衣夹固定的玻璃隔板(20厘米x20厘米,2毫米厚)将每个装有nsw深度为15厘米的水箱分成两等份。此后,一个仅有益生菌菌株k811(饲料1)、两种微生物的混合物(饲料2)或仅有卵形藻(硅藻控制)的生物膜水平放置在每个水箱底部的一半。然后将鲍鱼添加到这半水箱中,在试验的前三天它们是被限制使用的。在第3天,将新鲜的生物膜放置在每个水箱的剩余一半中并移除玻璃隔板,从而允许鲍鱼在两个生物膜之间自由移动。在试验的前三天将动物限制在水箱的一半,确保当第二个生物膜添加到系统中时鲍鱼不会被困在水箱的玻璃底部。在第六天,第一层生物膜被移除并更换新鲜的生物膜。同样,在第9天,移除并更换第二个生物膜。以这种方式继续喂食,每三天向鲍鱼提供一层新鲜的生物膜,并在喂养六天后去除老化的生物膜。在生物膜制备以及鲍鱼喂养六天后立即对粘附在每个板上的细胞生物量进行定量。
76.鲍鱼生长的量化
77.在每个实验开始时,从最初的动物群中随机抽取50只鲍鱼,并使用电子游标卡尺测量其壳长,精确到0.01毫米。在25天的实验期后,测量了从每个水箱中这随机选择的50只动物的壳长。计算了喂食不同饲料的鲍鱼壳长度增加的百分比以及日增长率(μμ/天)。
78.统计分析
79.在适用的情况下,数据表示为平均值和标准误差(se)。为了验证生物膜水中的稳定性,使用学生t
‑
检测(student’s t
‑
test)在t
20min
,t
24hr
和t
120hr
(在每个时间点,n=4个生物膜)进行两组之间的统计比较。使用单向方差分析(anova)确定益生菌膳食补充剂对鲍鱼幼体生长和存活的影响。为了确定饲料对鲍鱼幼体最终平均壳长(slt25)的影响,在每个实验中单独考虑每个水箱的数据,以便单个鲍鱼作为重复(每个罐n=50)。对于%存活率(以及%sl增加和每日增长率)的统计分析,所有三个实验的%存活率数据(或%sl增加/每日增长率数据)按饲料分组(即,n=6种不同的饮食)。在p<0.05处建立统计学显著差异。当anova的影响显著时,使用用于多重比较的图基事后多重比较法(post
‑
hoc tukey test)来检验样本平均值之间的显著差异。所有分析均使用r版本3.0.1(r development core team,2014)进行。
80.结果
81.三种人工饲料在典型鲍鱼饲养条件下的表现
82.弧菌k811(表1)的t
20min
浓度在细菌生物膜(饲料1)和混合物种生物膜(饲料2)之间没有显著差异(p=0.162)。平均而言,这些生物膜中弧菌k811的初始浓度为1.20x108个细胞/cm2。类似地,卵形藻的t
20min
浓度(表1)在硅藻对照饲料和混合物种生物膜(饮食2)之间没有显著差异(p=0.107)。平均而言,这些生物膜中卵形藻的浓度为2.56x106个细胞/cm2。随后将生物膜在含有nsw的玻璃水族箱中培养,由于通气和过滤设备,nsw具有相当大的水流。在五天内监测来自不同制备下的微生物细胞的损失。在整个实验中的单一和混合物种生物膜之间卵形藻和弧菌k811的浓度没有显著差异。
83.总体而言,该实验的结果表明,即使在nsw延长孵育时间后,每种微生物成分的浓度在不同生物膜之间也是相当的。尽管在五天的过程中生物膜中的微生物成分丢失,但在nsw中浸泡5天后,大约105个益生菌细胞/cm2和5x105个硅藻细胞/cm2的留在生物膜中。
84.幼体后期南非鲍生长实验
85.为了确保在整个试验过程中保持充足的食物供应,随着时间的推移监测和量化细胞生物膜成分的浓度。所有含有弧菌k811或卵形藻的生物膜分别具有大约108个益生菌细胞/cm2或106个藻类细胞/cm2的起始浓度。鲍鱼喂养六天后,每个菌株的浓度下降到大约105个益生菌细胞/cm2的和105个藻类细胞/cm2(数据未显示)。
86.由仅由弧菌k811的生物膜(饲料1)或与卵形藻的混合物(饲料2)喂食的鲍鱼分别显示68%和74%的存活率。仅由卵形藻喂食的对照组的鲍鱼存活率约49%(表2)。饲料对幼体后期的存活有显著影响(单向anova,f=5.51,df=2,p=0.016)。当鲍鱼被喂食由弧菌k811和卵形藻组成的混合物(饲料2)时,存活率显著高于被喂食对照饲料的鲍鱼(p=0.016)。与对照饲料相比,当仅由益生菌组成的饲料(饲料1)喂食鲍鱼时,存活率没有显著提高(p=0.068)。此外,由纯益生菌饲料(饲料1)和混合饲料(饲料2)喂食的鲍鱼的存活率没有显著差异(p=0.744)。
87.表1:在装有通气和水过滤装置的玻璃水箱中培养的三种不同人工生物膜的水稳
定性。
88.结果表示为平均浓度(细胞/cm2)
±
se(每个生物膜n=4)。
[0089][0090]
表2:在三个独立的25天生长实验中,鲍鱼以三种不同的人工生物膜饲料喂养后存活的幼体后期南非鲍的数量和相应的存活率百分比(%)。每种饲料的影响一式两份进行测
试,初始饲养密度为每个水箱150只。
[0091][0092]
在所有三个实验中,存活鲍鱼的数量在每个25天的实验期间都在下降(图2)。然而,在每个实验结束时,当动物喂食益生菌饲料(饲料1和2)时,存活率始终较高。在实验1中,第4天,在一个由卵形藻对照饲料喂食的重复水箱中发生了高死亡率事件(67只死亡)。
此外,在第18天,第二个由卵形藻对照饲料喂食的重复水箱中(25只死亡)以及在一个仅由益生菌饲料喂养的重复水箱中(饲料1,22只死亡)也看到了高死亡率。这意味着在实验结束时,有两个水箱(对照水箱1和纯益生菌水箱1)记录的壳长度测量值少于50个(分别为40和47个鲍鱼)。实验2和3中没有发生大的死亡事件,并且实验1中的鲍鱼可能受到了压力(在第一个实验中,所有玻璃外壳水箱都直接安置在空气调节装置的顶下,这可能会增加水蒸发,进而水的盐度增加)。
[0093]
对于实验1、2和3,幼体后期的初始平均壳长度(sl
t0
)分别为3.04(
±
0.10)mm、2.06(
±
0.04)mm和3.1(
±
0.04)mm。在所有三个实验中,饲料对鲍鱼的sl
t25
有显著影响(单向anova,p<0.05)。在实验1中,混合饲料喂食的幼体后期的平均sl
t25
显著高于卵形藻饲料喂食的幼体后期的平均sl
t25
(p<0.05)。然而,在实验2和3中,与对照饲料相比,两种益生菌饲料(饲料1和2)都显著提高了幼体后期的平均sl
t25
(p<0.05)。无论益生菌是单独存在还是与卵形藻混合存在,益生菌生物膜饲料喂养的鲍鱼的sl
t25
之间没有显著差异。(数据未展示)。
[0094]
仅由弧菌k811(饲料1)或弧菌k811和卵形藻的混合物(饲料2)组成的益生菌生物膜饲料喂食的鲍鱼的壳长度平均增加了21.3%和23.0%,增长率分别约为29.7μm/天和33.1μm/天(表3)。由卵形藻组成的对照饲料(对照饲料)喂食的鲍鱼的平均壳长仅提高了8.3%,这些鲍鱼的生长速度为11.6μm/天。总的来说,这些结果表明益生菌饲料可以使幼体后期南非鲍的生长速度增加三倍。
[0095]
表3:在三个独立的25天生长实验中,喂食三种不同的人工生物膜饮食后,鲍鱼的最终平均壳长(mm)、壳长增加百分比(%)和日生长率(gr)(μm/天)。在每个实验中,每种饲料一式两份进行测试。
[0096][0097]
尽管幼体后期的初始平均壳长(sl
t0
)存在差异(实验1、2和3分别为3.04毫米、2.06毫米和3.1毫米),但在所有三个实验中喂食益生菌饲料(饲料1和2)的动物壳长的百分比增加和日增长率数据都相当一致(表3)。例如,在实验1、2和3中,喂食纯益生菌饲料(饲料1)的鲍鱼的平均sl增加分别为18.3%、22.9%和22.8%,而喂食混合饲料(饲料2)的鲍鱼的平均
sl增加为分别为24.9%、22%和22.3%。然而,喂食对照饲料的鲍鱼所获得的结果一致性较差,在实验1、2和3中,动物的平均sl增加分别在16.7%、1.0%和7.5%之间变化。此外,在实验1、2和3中由卵形藻组成的饲料喂食的鲍鱼的平均增长率分别为24.4μm/天、0.8μm/天和9.6μm/天。
[0098]
饲料对鲍鱼的%sl增加有显著影响(单向anova,f=13.69,df=2,p<0.001)。与硅藻对照饲料相比,当用益生菌饲料(饲料1和2)喂食鲍鱼时,幼体后期的%sl增加得到显著改善(p<0.05)。仅用由弧菌k811组成的饲料(饲料1)喂食的鲍鱼和混合生物膜喂食的鲍鱼(饲料2)之间的%sl增加没有显著差异(p=0.845)。饲料对鲍鱼的生长速度也有显著影响(单向anova,f=8.71,df=2,p=0.003)。与硅藻对照饲料相比,当用益生菌饲料(饲料1和2)喂食鲍鱼时,幼体后期的生长速度显著提高(p<0.05)。用仅由弧菌k811组成的饲料(饲料1)喂食的鲍鱼和用由弧菌k811和卵形藻组成的混合生物膜(饲料2)喂食的鲍鱼之间的生长速度没有显著差异(p=0.814)。
[0099]
讨论
[0100]
在当前的研究中,进行了三个独立的饲养实验,以确定推定的益生菌弧菌sy9为人工生物膜饲料的主要成分提供时,其对幼体后期南非鲍(haliotis midae)的存活和生长的影响。结果表明,幼体后期南非鲍喂食益生菌(饲料1和2)和对照饲料的存活率分别为71%和49%,只有混合饲料(饲料2)显著提高了鲍鱼的存活率。此外,在所有三个实验中,益生菌饮食对鲍鱼后期的sl
t25
都有显著影响,与对照饲料喂食的动物相比,益生菌饲料喂食的幼体后期鲍鱼的sl增加百分比和生长率显著更高。总的来说,这些结果证实了弧菌sy9在发育的幼体后期阶段对南非鲍具有益生菌作用。
[0101]
当前研究的生长和存活结果超过了先前研究中观察到的结果,这些研究测试了基于藻酸盐的人工饲料对幼体后期发育的影响(stott et al.2002;2003a,b)。例如,目前的研究中,在三个单独的实验里,藻酸盐益生菌饲料(饲料1和2)喂食的幼体后期南非鲍的平均增长率分别为29.7μm/天和33.1μm/天,这显著高于幼体后期喂食硅藻对照饲料的平均增长率11.6μm/天。斯托特(stott)等人(2003a)报导,用藻酸盐饲料喂食三天大的黑鲍(h.discus supertexta)幼体后期,并补充商业饲料sf
‑
15或sf
‑
15[t],平均增长率分别为每种饲料27.5μm/天和28.6μm/天。天然硅藻对照饲料喂食的幼体后期的增长率为18.6μm/天。与目前的研究相反,该研究表明,与喂食硅藻对照饲料(49%的存活率)相比,喂食益生菌饲料(饲料1和2的平均存活率为71%)幼体后期南非鲍的存活率更高。然而,据斯托特(stott)等人(2003a)报导,与硅藻对照饲料(12.9%)相比,人工饲料的幼体后期存活率更低(sf
‑
15和sf
‑
15[t]分别为5.3%和7.8%)。这表明,与之前研究中描述的藻酸盐饲料相比,益生菌饲料可以为幼体鲍鱼提供更好的喂养。
[0102]
尽管据报道卵形藻这种硅藻很容易被幼体后期鲍鱼(>800μm sl)消化,但它似乎不是适合幼体后期南非鲍的硅藻。目前的研究表明,当鲍鱼被喂食仅由卵形藻组成的对照饲料时,幼体后期的生长率存在很大差异(表2)。总体而言,这些结果突出了与使用硅藻作为幼体后期鲍鱼的主要食物源相关的挑战。使用为幼体后期发育提供持续营养供应的配方饲料代替它们将是有利的。
[0103]
该研究表明,当以细菌作为主要食物源时,幼体后期南非鲍可以生长和存活。结果表明,当鲍鱼喂食不同的益生菌饲料(饲料1和2)时,其生长和存活率没有显着差异。这表示
仅基于藻酸盐和细菌益生菌的人工饲料可能会排除用硅藻生物膜对幼体后期鲍鱼进行商业养殖的需要。
[0104]
当幼体后期南非鲍喂食混合生物膜(饲料2)时,观察到幼虫后期存活率和生长率的最大改善,这表明卵形藻可能提供单独弧菌k811无法完全提供的营养益处。
[0105]
微生物沉积细节
[0106]
根据国际承认用于专利程序目的的微生物保藏的布达佩斯条约(budapest treaty),本说明书中描述的弧菌sy9菌株于2013年7月1日在比利时微生物协调保藏中心(bccm)保藏,登记号lmg p
‑
27727。
[0107]
参考文献
[0108]
karsi,a.and lawrence,m.l.,2007.broad host range fluorescence and bioluminescence expression vectors for gram
‑
negative bacteria.plasmid,57(3),pp.286
‑
295.
[0109]
macey,b.m.and coyne,v.e.,2005.improved growth rate and disease resistance in farmed haliotis midae through probiotic treatment.aquaculture,245(1),pp.249
‑
261.
[0110]
stott,a.e.,takeuchi,t.,koike,y.,yamakawa,h.and imada,o.,2002.using micro particle diets to replace diatoms for feeding postlarval abalone haliotis discus discus(reeve.).fish.sci.68(5),pp.1088
‑
1093.
[0111]
stott,a.e.,takeuchi,t.,koike,y.and imada,o.,2003a.settling and raising postlarval abalone haliotis diversicolor supertexta(lischke)on microparticulate diets embedded in a layer of alginate.aquac.res.34(7),pp.561
‑
567.
[0112]
stott,a.e.,takeuchi,t.,koike,y.,and imada,o.,2003b.the effect of three different application methods for an artificial microparticle diet on the survival and growth rate of post
‑
larval abalone haliotis discus discus(reeve).suisanzoshoku,51(2),pp.197
‑
203.
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。