1.本发明属于医药化工领域,涉及喹诺酮羧酸衍生物或二氮杂萘酮羧酸衍生物的制备方法,具体涉及7-取代-3-喹诺酮羧酸衍生物或7-取代-1,5-二氮杂萘酮羧酸衍生物的制备方法。
背景技术:
2.7-取代-3-喹诺酮羧酸衍生物属于喹诺酮类抗菌药(quinolone antibiotics),又称吡酮酸类抗菌药(pyridonecarboxylic acid antibiotics),是一类人工合成的具有1,4二氢-4-氧代喹啉-3-羧酸结构的化合物。该类药物目前已经发展到第四代喹诺酮药物,占据了抗菌药的第二大市场份额。
3.[0004][0005]
如上所述,喹诺酮药物多数具有如下结构:
[0006][0007]
这些高效抗菌的喹诺酮羧酸通常是在喹诺酮羧酸的7-位上具有杂单环或杂双环胺基团。这些环胺基团一般可通过相应的7-卤代-喹诺酮羧酸与相应的胺进行亲核取代来制备。
[0008]
迄今为止,已经发现了各种喹诺酮羧酸衍生物的合成方法。
[0009]
ep0350733中采用直接偶联策略,化合物v在碱的作用下与任意的环状仲胺iii直接偶联,生成取代的衍生物i
[0010][0011]
在该方案中,由于6-位卤素与7-f存在竞争性的亲核取代反应,因而会导致6-位异构体杂质vi的生成,产品往往需要柱层析纯化,增加了生产成本且不利于工业化生产。同时,当8-位上有一个-och3供电子基,7位的反应性降低,在温和的反应条件下,只能得到极低量8-烷氧基喹诺酮羧酸的衍生物。而且,当使反应条件剧烈时,8位上的烷氧基发生去烷基化,变成羟基,因此不能得到高纯度的目的产物。
[0012]
v的3-位羧基和4-位羰基能够与硼形成络合物ii,增加7-位碳原子的电负性,提高7-f的反应选择性,可以减少6-位异构体杂质的生成。日本专利公开昭63-198664中介绍了如下改进方法,
[0013][0014]
如上所示,该方法利用二氟化硼螯合物进行,可以增强7-位碳原子上的碳正性,增加反应的活性和选择性,所以可以得到高产量的目标化合物。但是氟硼酸价格较贵,会导致生产成本变高。而且由于制备该中间体时氟化氢作为副产物生成,难以用常规生产设备生产。
[0015]
日本专利jph0778065b2中使用其二(乙酸酯-o)-硼酸酯代替二氟化硼螯合物来解决上述问题,使用此螯合化合物可得到高产量、高纯度的目的产物。因为在合成该螯合物的时候不产生能腐蚀反应釜的副产物氟化氢,因此该螯合物适合工业生产。此外,该螯合物制备成本比昭63-198664公开的方法便宜得多。
[0016][0017]
但上述合成方法仍然存在一些弊端。首先,反应中生成的一分子hf需要过量的碱来中和,过量碱的存在导致ph过高,硼螯合物iib在碱性条件下容易降解,重新生成化合物v,导致反应收率的降低,同时仍然会有部分位置异构体杂质vi的生成。
[0018][0019]
其次,当8-位存在甲氧基等给电子基时,譬如第四代喹诺酮药物莫西沙星、加替沙星、巴洛沙星等,8-位上会发生去甲基化反应,同时侧链仲胺氮原子会发生甲基化反应。以莫西沙星为例,kumar等人在莫西沙星的合成中发现两个影响产品质量的关键杂质,8-oh莫西沙星和n-甲基莫西沙星(j pharmaceut biomed,2004,34(5):1125-1129)。专利ep1832587a1中提出反应中生成的氟离子的脱甲基作用会导致8-oh莫西沙星杂质的生成,
同时生成的甲基正离子会对侧链仲胺氮原子进行甲基化,导致杂质n-甲基莫西沙星的生成。由于这两种杂质与莫西沙星在结构上极为接近,需要多次重结晶才能除去,导致生产成本的提高和三废的增加。
[0020][0021]
上述两种合成方案本质上均为氟代芳烃的c-n偶联反应,遵循s
n
ar反应机理,反应过程中氟离子的生成无法避免。
[0022]
因此,化学工作者在努力寻求一种反应时间短、成本低廉、底物转化彻底、原料不易降解的喹诺酮羧酸衍生物或二氮杂萘酮羧酸的制备方法。
技术实现要素:
[0023]
为了克服现有技术的缺陷,本发明提供了一种7-取代-3-喹诺酮羧酸衍生物的制备方法,该方法要具有反应时间短、成本低廉、底物转化彻底、原料不易降解以及氟离子所致杂质显著减少等优点。
[0024]
本发明利用有机硅化合物取代传统方法中使用的碱,来捕捉反应中生成的氢氟酸,既能降低反应体系的碱性,减少螯合物的降解,同时也显著减少了氟离子导致的杂质,提高了产品纯度和收率,克服了现有技术方案存在的上述不足。
[0025]
具体地说,在本发明的实施方案中,本发明提供了一种7-取代-3-喹诺酮羧酸衍生物或7-取代-1,5-二氮杂萘酮羧酸衍生物(i)的制备方法,包括如下步骤:
[0026]
(1)在有机溶剂中,将硼螯合物ii与有机胺iii在有机硅化合物下发生偶联反应,得到化合物iv;
[0027][0028]
(2)将化合物iv与盐酸混合,随后过滤分离沉淀的化合物i;
[0029][0030]
其中,
[0031]
x为卤素;
[0032]
y为c、ch或n;当y为n时r3不存在;
[0033]
r1为氢、c3-c6环烷基、c1-c6烷基、苯基、苄基,所述的c1-c6烷基、苯基可以被c1-c4烷基、卤素取代;
[0034]
r2为氢、c1-c6烷基、c1-c6烷氧基、氨基或硝基;
[0035]
r3为氢、c1-c6烷基、c1-c6烷氧基、或者r1与r3相连使r
1-n-c-c-r3构成六元环,所述的六元环可以被c1-c4烷基取代;
[0036]
r4、r5与它们键合的氮原子一起形成一个5-10元单杂环或双环杂环,所述的单杂环或双环杂环中还可以含有n、o或s的杂原子;所述的单杂环或双环杂环可以被一个或多个羟基、氨基、卤素、c1-c6烷基取代;
[0037]
r6为卤素、c2-c6脂肪族羧基或c7-c11的芳香族酸基。
[0038]
进一步地,
[0039]
x为卤素;
[0040]
y为c、ch;
[0041]
r1为氢、c3-c6环烷基、c1-c4烷基、苯基、苄基,所述的c1-c4烷基、苯基可以被c1-c4烷基、卤素取代;
[0042]
r2为氢、c1-c4烷基、c1-c4烷氧基;
[0043]
r3为氢、c1-c4烷基、c1-c4烷氧基、或者r1与r3相连使r
1-n-c-c-r3构成所述的可以被c1-c4取代;
[0044]
r4、r5与它们键合的氮原子一起形成
[0045][0046]
更进一步地,
[0047]
化合物i可以为盐酸莫西沙星、n-甲基莫西沙星、8-羟基莫西沙星、盐酸加替沙星、盐酸巴洛沙星、盐酸左氧氟沙星、盐酸沙拉沙星、盐酸双氟沙星、盐酸替马沙星、盐酸环丙沙星、盐酸诺氟沙星、盐酸培氟沙星或盐酸恩诺沙星。
[0048]
在本发明的实施方案中,
[0049]
步骤(1)中有机溶剂为c1-c4的一元醇或二元醇、乙腈、四氢呋喃、1,4-二氧六环、乙酸乙酯、n,n-二甲酰胺、二甲基亚砜、乙醚、甲基叔丁基醚等中的一种或任意多种的混合溶剂,优选溶剂为乙腈、乙醇或二者的混合溶剂。
[0050]
步骤(1)中反应温度控制在-20℃~100℃,优选10~50℃,更优选20~30℃。
[0051]
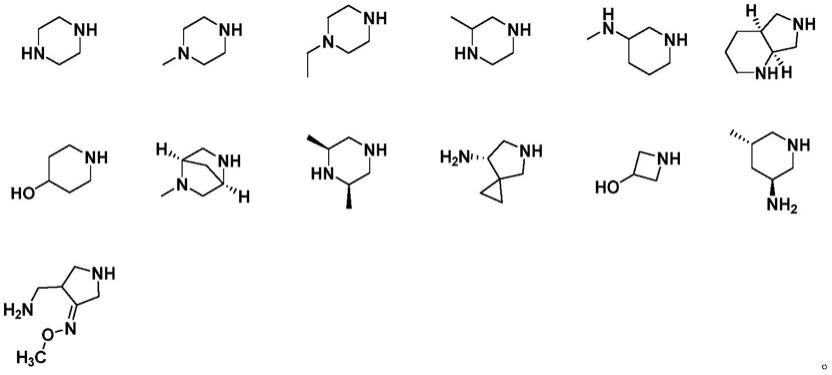
步骤(1)中所述的有机胺iii为仲胺,优选为步骤(1)中所述的有机胺iii为仲胺,优选为中的一种;
[0052]
步骤(1)中所述的有机硅化合物为c4-c20硅氧烷、c4-c10硅氮烷、c4-c10硅醚等;
[0053]
所述的硼螯合物ii、有机硅化合物(以硅摩尔量计算)、有机胺iii的摩尔比为1:(1~5):(1~2);
[0054]
进一步地,有机硅化合物(以硅摩尔量计算)与硼螯合物ii的摩尔比优选为(1~3):1。
[0055]
进一步地,有机胺iii与硼螯合物ii的摩尔比优选为(1~1.5):1。
[0056]
更进一步地,步骤(1)中所述的硅氧烷是指含si-o-si键构成主链结构的聚合物,包括但不限于如下结构:
[0057][0058]
更进一步地,步骤(1)中所述的硅醚是指具有si-o-c链的一类化合物,包括但不限于如下结构:
[0059][0060]
优选的硅醚为tmsome和tmsoet。
[0061]
步骤(2)中反应混合物与盐酸混合,调节ph<1。
[0062]
本发明的方法能够具有反应时间短、成本低廉、底物转化彻底、原料不易降解以及氟离子所致杂质显著减少、收率高、纯度高的优点。
具体实施方式:
[0063]
下面详细描述本发明的实施例。下面描述的实施例是示例性的,旨在用于解释本发明,而不能理解为对本发明的限制。
[0064]
以下实施例阐述了喹诺酮药物的制备步骤,
[0065]
实施例1
[0066][0067]
向50ml反应瓶中,依次投入2g化合物iic(4.73mmol)、13ml乙腈和三甲基乙氧基硅烷(tmsoet,1.68g,14.2mmol),不断搅拌至完全溶解,向反应瓶中加入0.66g(s,s)-2,8-二氮杂双环[4.3.0]壬烷(化合物iiic),室温反应至tlc监测反应完全。降温至0℃,在搅拌下向反应液中滴加浓盐酸调节ph<1,继续保温搅拌4h,有黄色固体生成。抽滤,滤饼用2ml乙醇洗涤两次,干燥,得到黄色固体粉末,收率96.5%,hplc纯度99.91%,n-甲基莫西沙星含量0.0161%。ms(esi)m/z:计算值401.44实测值402.1[m h]
、803.3[2m h]
.1h nmr(400mhz,dmso-d6)δ15.12(s,1h),10.18(d,j=8.6hz,1h),9.07
–
8.83(br,1h),8.66(s,1h),7.67(d,j=14.2hz,1h),4.15(tt,j=7.4,4.1hz,1h),4.07(dd,j=12.2,5.4hz,1h),3.93
–
3.83(m,2h),3.80
–
3.72(m,1h),3.60(s,3h),3.18(d,j=12.4hz,1h),2.92(d,j=10.8hz,1h),
1.92
–
1.60(m,4h),1.26
–
1.13(m,1h),1.17
–
1.05(m,1h),1.08
–
0.97(m,1h),0.94
–
0.82(m,1h).
13
c nmr(101mhz,dmso-d6)δ176.43(d,j=3.2hz),166.28,151.68,150.78,140.80(d,j=7.3hz),137.11(d,j=10.4hz),134.96,117.73(d,j=8.8hz),107.10,106.86,62.33,54.92(d,j=4.4hz),54.52,52.36(d,j=9.7hz),41.90,41.07,34.59(d,j=2.6hz),20.99,17.99,10.04,8.84.
[0068]
实施例2
[0069][0070]
向100ml单口瓶中加入莫西沙星(5g,12.45mmol)、20ml甲酸和30ml 37%的甲醛水溶液,搅拌下回流反应4h。待反应结束后,减压浓缩溶剂,加入20ml水,用10%naoh溶液调节ph至中性,用50ml二氯甲烷萃取3次,合并二氯甲烷相,并用饱和食盐水洗涤,有机相加入无水na2so4干燥过夜。次日抽滤,滤液减压浓缩得淡黄色固体,用30ml乙腈重结晶,抽滤,滤饼于50℃减压干燥,得4.5g白色固体为杂质g,收率为87.0%,纯度为99.98%。ms(esi)m/z:计算值415.47,实测值416.3[m h] 。1h nmr(400mhz,chloroform-d)δ15.13(s,1h),8.75(s,1h),7.74(d,j=13.9hz,1h),4.02(tt,j=7.3,4.0hz,1h),3.89(td,j=9.7,3.1hz,1h),3.83
–
3.68(m,2h),3.58(s,3h),3.52
–
3.40(m,1h),2.86
–
2.68(m,2h),2.43(dq,j=8.9,4.7hz,1h),2.28(s,3h),2.18(td,j=12.8,11.4,2.3hz,1h),1.94
–
1.81(m,1h),1.79
–
1.67(m,2h),1.67
–
1.55(m,1h),1.31
–
1.20(m,1h),1.19
–
1.02(m,2h),0.96
–
0.85(m,1h).
13
c nmr(101mhz,chloroform-d)δ176.68(d,j=3.2hz),167.16,154.82,152.33,149.41,140.29(d,j=7.4hz),137.61(d,j=11.1hz),134.52,117.77(d,j=8.9hz),107.61(d,j=24.0hz),64.44(d,j=1.9hz),61.01,54.38(d,j=6.5hz),54.24,53.20(d,j=6.4hz),44.17,40.50,37.63(d,j=1.6hz),23.16,22.00,10.09,8.86.
[0071]
实施例3
[0072][0073]
向100ml单口瓶中加入30ml 40%hbr溶液和盐酸莫西沙星(3g,6.6mmol),升温至90-100℃并回流搅拌反应12h。待反应结束后,将反应液冷却至室温,再用10%的naoh水溶液调ph值至中性,用50ml二氯甲烷萃取3次,合并有机层,用150ml饱和食盐水洗涤,有机相加无水硫酸钠干燥过夜。次日抽滤除去无水硫酸钠,滤液减压浓缩,残余物经柱层析分离纯化(展开剂为meoh:dcm:acoh=1:40:1),得灰白色固体0.5g即为杂质e。将其溶于乙醇,滴加浓盐酸使其ph值至1,有淡黄色固体析出,抽滤,干燥,得到0.4g杂质e的盐酸盐,收率为14.3%,纯度为97.97%。ms(esi)m/z calc.for c
20
h
22
fn3o4[m-h]-:387.41,found 386.1.1h nmr(400mhz,dmso-d6)δ14.97(s,1h),9.92(s,1h),9.58(d,j=9.2hz,1h),9.21
–
8.98(m,1h),8.67(s,1h),7.52(d,j=12.1hz,1h),4.33(ddd,j=11.0,6.9,4.6hz,1h),3.87
–
3.80(m,1h),3.80
–
3.72(m,1h),3.61(t,j=9.8hz,1h),3.30(t,j=12.8hz,2h),3.17(t,j=9.7hz,1h),3.00
–
2.72(m,2h),2.11
–
1.52(m,4h),1.23
–
1.01(m,4h).13c nmr(101mhz,dmso-d6)δ176.86(d,j=2.9hz),166.22,157.96(d,j=249.9hz),150.18,147.19(d,j=6.6hz),130.09(d,j=13.6hz),129.75,123.88(d,j=9.9hz),106.54,102.05(d,j=22.5hz),56.51,55.68(d,j=7.2hz),51.98,42.52,42.29,35.19,21.23,17.14,9.77(d,j=34.4hz).
[0074]
实施例4
[0075][0076]
向50ml反应瓶中,依次投入2g化合物iic(4.73mmol)、13ml乙腈和三乙胺(et3n,0.55g,5.44mmol),不断搅拌至完全溶解,向反应瓶中加入0.69g(s,s)-2,8-二氮杂双环[4.3.0]壬烷(化合物iiic),室温反应至tlc监测反应完全。降温至0℃,在搅拌下向反应液中滴加浓盐酸调节ph<1,继续保温搅拌4h,有黄色固体生成。抽滤,滤饼用2ml乙醇洗涤两次,干燥,得到黄色固体粉末,收率85.1%,hplc纯度99.52%,n-甲基莫西沙星含量0.1504%。
[0077]
实施例5
[0078][0079]
向50ml反应瓶中,依次投入2.0g化合物iic(4.73mmol)、13ml乙腈和0.56g三甲基乙氧基硅烷(tmsoet),不断搅拌至完全溶解,向反应瓶中加入2-甲基哌嗪iiid(0.54g,5.44mmol),室温反应至tlc监测反应完全。降温至0℃,在搅拌下向反应液中滴加浓盐酸调节ph<1,继续保温搅拌4h,有黄色固体生成。抽滤,滤饼用2ml乙醇洗涤两次,干燥,得到黄色固体,即盐酸加替沙星,收率93.2%,纯度99.67%。ms(esi)m/z calc.for c
19
h
22
fn3o4[m h]
:375.16,found 376.2.1h nmr(400mhz,d2o)δ8.50(s,1h),6.71(d,j=11.8hz,1h),4.24
–
3.95(m,1h),3.73(s,3h),3.68
–
3.43(m,5h),3.41
–
3.18(m,2h),1.35(d,j=6.3hz,3h),1.20(d,j=7.1hz,2h),0.92(d,j=2.8hz,2h).
13
c nmr(101mhz,deuterium oxide)δ175.63,168.15,157.09,154.59,150.50,146.15(d,j=4.9hz),138.60(d,j=12.2hz),133.82,120.82(d,j=9.7hz),106.12(d,j=21.5hz),105.16,62.80,53.48,51.89,46.61,43.80,41.30,15.15,8.93.
[0080]
实施例6
[0081][0082]
向50ml反应瓶中,依次投入2.0g化合物iic(4.73mmol)、13ml乙腈和0.56g三甲基乙氧基硅烷(tmsoet),不断搅拌至完全溶解,向反应瓶中加入iiie(0.62g,5.44mmol),室温反应至tlc监测反应完全。降温至0℃,在搅拌下向反应液中滴加浓盐酸调节ph<1,继续保温搅拌4h,有黄色固体生成。抽滤,滤饼用2ml乙醇洗涤两次,干燥,得到黄色固体,即盐酸巴洛沙星,收率94.1%,纯度99.96%。ms(esi)m/z calc.for c
20
h
24
fn3o4[m h]
:389.18,found 390.23.1h nmr(600mhz,dmso-d6)δ14.87(s,1h),9.37(s,2h),8.71(s,1h),7.75(s,1h),4.18(s,1h),3.78(s,4h),3.51
–
3.22(m,4h),3.10(s,1h),2.57(s,3h),2.24(s,1h),1.89(s,1h),1.81
–
1.54(m,2h),1.15(s,2h),1.05(s,2h).
13
c nmr(151mhz,dmso-d6)δ176.28,165.49,155.72(d,j=249.0hz),150.55,146.36,138.89(d,j=12.3hz),133.98,121.50(d,j=9.3hz),106.65,106.45(d,j=22.4hz),63.10,54.47,52.58
–
51.51(m),50.65,40.72,29.61,25.88,23.67,8.95(d,j=19.2hz).
[0083]
实施例7
[0084][0085]
向50ml反应瓶中,依次投入2.0g化合物iid(4.89mmol)、13ml乙腈和1.16g三甲基乙氧基硅烷(tmsoet),不断搅拌至完全溶解,向反应瓶中加入iiif(0.56g,5.62mmol),室温反应至tlc监测反应完全。降温至0℃,在搅拌下向反应液中滴加浓盐酸调节ph<1,继续保温搅拌4h,有黄色固体生成。抽滤,滤饼用2ml乙醇洗涤两次,干燥,得到黄色固体,即盐酸左氧氟沙星,收率90.5%,纯度99.95%。ms(esi)m/z calc.for c
18
h
20
fn3o4[m h]
:361.14,found 362.19.1h nmr(600mhz,dmso-d6)δ15.11(s,1h),11.18(s,1h),9.00(s,1h),7.62(d,j=11.9hz,1h),4.95(d,j=6.7hz,1h),4.61(d,j=11.1hz,1h),4.41(d,j=9.9hz,1h),3.71
–
3.54(m,4h),3.45(d,j=10.3hz,2h),3.16(s,2h),2.82(s,3h),1.46(d,j=6.8hz,3h).
13
c nmr(151mhz,dmso-d6)δ176.35(d,j=3.1hz),165.87,155.29(d,j=246.7hz),146.35,140.58(d,j=6.0hz),130.40(d,j=14.6hz),124.74,120.55(d,j=9.5hz),106.86,103.18(d,j=23.6hz),68.28,54.81,53.03,48.35
–
45.57(m),42.27,17.90.
[0086]
实施例8
[0087][0088]
向50ml反应瓶中,依次投入2.0g化合物iie(4.47mmol)、13ml乙腈和1.06g三甲基乙氧基硅烷,不断搅拌至完全溶解,向反应瓶中加入哌嗪iiig(0.44g,5.14mmol),室温反应至tlc监测反应完全。降温至0℃,在搅拌下向反应液中滴加浓盐酸调节ph<1,继续保温搅拌4h,有黄色固体生成。抽滤,滤饼用2ml乙醇洗涤两次,干燥,得到黄色固体,即盐酸沙拉沙星,收率95.40%,纯度99.95%。ms(esi)m/z calc.for c
20
h
17
f2n3o3[m h]
:385.12,found 386.20.1h nmr(600mhz,dmso-d6)δ8.67(s,1h),8.05(d,j=14.1hz,1h,),7.80(s,2h),6.42(s,2h),3.34(s,8h).
13
c nmr(151mhz,dmso-d6)δ
[0089]
实施例9
[0090][0091]
向50ml反应瓶中,依次投入2.0g化合物iie(4.47mmol)、13ml乙腈和1.06g三甲基乙氧基硅烷,不断搅拌至完全溶解,向反应瓶中加入n-甲基哌嗪iiif(0.52g,5.14mmol),室温反应至tlc监测反应完全。降温至0℃,在搅拌下向反应液中滴加浓盐酸调节ph<1,继续保温搅拌4h,有黄色固体生成。抽滤,滤饼用2ml乙醇洗涤两次,干燥,得到黄色固体,即盐酸双氟沙星,收率96.30%,hplc纯度99.95%。ms(esi)m/z calc.for c
21
h
19
f2n3o3[m h]
:399.14,found 400.21。1h nmr(600mhz,dmso-d6)δ15.01(s,1h),11.21(s,1h),8.67(s,1h),8.05(d,j=12.8hz,1h),7.91
–
7.69(m,2h),7.55(t,j=8.3hz,2h),6.44(d,j=6.9hz,1h),3.58(s,2h),3.44(s,2h),3.15(s,4h),2.77(s,3h).
13
c nmr(151mhz,dmso-d6)δ176.70,165.57,161.70,152.79(d,j=249.2hz),148.95,143.86(d,j=10.6hz),138.99,136.09,129.87(d,j=9.5hz),119.42(d,j=7.6hz),117.28(d,j=23.4hz),111.28(d,j=23.3hz),107.53,107.10,51.74,45.97,41.89.
[0092]
实施例10
[0093][0094]
向50ml反应瓶中,依次投入2.0g化合物iif(4.30mmol)、13ml乙腈和1.02g三甲基乙氧基硅烷,不断搅拌至完全溶解,向反应瓶中加入iiid(0.49g,4.95mmol),室温反应至tlc监测反应完全。降温至0℃,在搅拌下向反应液中滴加浓盐酸调节ph<1,继续保温搅拌4h,有黄色固体生成。抽滤,滤饼用2ml乙醇洗涤两次,干燥,得到黄色固体,即盐酸替马沙星,收率94.7%,hplc纯度99.03%。ms(esi)m/z calc.for c
21
h
18
f3n3o3[m h]
:417.13,found 418.21。1h nmr(600mhz,chloroform-d)δ9.14(s,1h),8.42(t,j=8.4hz,1h),7.77(q,j=8.4hz,1h),7.32(t,j=7.8hz,1h),7.29
–
7.23(m,1h),7.10(dd,j=9.6,6.2hz,1h),2.08(s,6h).
13
c nmr(151mhz,chloroform-d)δ173.25(d,j=83.7hz),171.76(d,j=2.9hz),165.57(d,j=11.2hz),159.32,150.29,139.00(d,j=9.6hz),130.13(d,j=9.9hz),122.79(d,j=13.4hz),119.24(d,j=7.2hz),114.36(d,j=3.0hz),114.31(d,j=4.0hz),114.26
–
114.20(m),114.15(d,j=3.7hz),110.48,106.99(d,j=23.0hz),106.65(d,j=4.4hz),106.65(d,j=48.9hz),23.08.
[0095]
实施例11
[0096][0097]
向50ml反应瓶中,依次投入2.0g化合物iig(5.09mmol)、13ml乙腈和1.20g三甲基乙氧基硅烷,搅拌下向反应瓶中加入iiig(0.50g,5.85mmol),室温反应至tlc监测反应完全。降温至0℃,在搅拌下向反应液中滴加浓盐酸调节ph<1,继续保温搅拌4h,有黄色固体生成。抽滤,滤饼用2ml乙醇洗涤两次,干燥,得到黄色固体,即盐酸环丙沙星,收率92.4%,纯度99.86%。ms(esi)m/z calc.for c
17
h
18
fn3o3[m h]
:331.13,found 332.18。1h nmr(600mhz,deuterium oxide)δ8.32(s,1h),7.27(d,j=7.0hz,1h),7.02(d,j=12.8hz,1h),3.54
–
3.50(m,5h),3.48
–
3.42(m,4h),1.35(d,j=6.6hz,2h),1.05(s,2h).
13
c nmr(151mhz,deuterium oxide)δ175.34,168.36,153.09(d,j=251.5hz),147.89,144.51(d,j=10.1hz),138.70,118.23(d,j=7.5hz),110.39(d,j=23.6hz),106.33,105.38,46.28(d,j=5.0hz),43.24,40.41,7.52.
[0098]
实施例12
[0099][0100]
向50ml反应瓶中,依次投入2.0g化合物iih(5.25mmol)、13ml乙腈和1.24g三甲基乙氧基硅烷,搅拌下向反应瓶中加入iiig(0.52g,6.04mmol),室温反应至tlc监测反应完全。降温至0℃,在搅拌下向反应液中滴加浓盐酸调节ph<1,继续保温搅拌4h,有黄色固体生成。抽滤,滤饼用2ml乙醇洗涤两次,干燥,得到黄色固体,即盐酸环丙沙星,收率95.0%,hplc纯度99.95%。ms(esi)m/z calc.for c
16
h
18
fn3o3[m h]
:319.13,found 320.20。1h nmr(600mhz,deuterium oxide)δ8.28(s,1h),7.00(d,j=12.7hz,1h),6.75(d,j=6.9hz,1h),4.20(d,j=7.2hz,2h),3.50
–
3.46(m,4h),3.45
–
3.40(m,4h),1.36(t,j=7.2hz,3h).
13
c nmr(151mhz,deuterium oxide)δ174.99,168.42,152.83(d,j=251.7hz),147.34,144.67(d,j=10.2hz),136.82,118.69(d,j=7.9hz),110.68(d,j=93.0hz),105.49(d,j=32.8hz),50.25,46.34,43.22,40.40,13.73.
[0101]
实施例13
[0102][0103]
向50ml反应瓶中,依次投入2.0g化合物iih(5.25mmol)、13ml乙腈和1.24g三甲基乙氧基硅烷,搅拌下向反应瓶中加入iiif(0.60g,6.04mmol),室温反应至tlc监测反应完全。降温至0℃,在搅拌下向反应液中滴加浓盐酸调节ph<1,继续保温搅拌4h,有黄色固体生成。抽滤,滤饼用2ml乙醇洗涤两次,干燥,得到黄色固体,即盐酸培氟沙星,收率91.8%,纯度99.83%。ms(esi)m/z calc.for c
17
h
20
fn3o3[m h]
:333.15,found 334.22。1h nmr(600mhz,deuterium oxide)δ8.42
–
8.26(m,1h),7.20
–
7.02(m,1h),6.90
–
6.74(m,1h),4.23(s,2h),3.80(s,2h),3.66(d,j=10.3hz,2h),3.41
–
3.16(m,4h),2.99(s,3h),1.39(d,j=3.6hz,3h).
13
c nmr(151mhz,d2o)δ175.05,168.45,152.84(d,j=251.7hz),147.42,144.25(d,j=9.9hz),136.84,118.89,110.79(d,j=23.2hz),105.60(d,j=16.5hz),99.99,53.13,50.27,46.59,43.03,13.73.
[0104]
实施例14
[0105]
[0106]
向50ml反应瓶中,依次投入2.0g化合物iig(5.09mmol)、13ml乙腈和1.20g三甲基乙氧基硅烷,搅拌下向反应瓶中加入iiih(0.67g,5.85mmol),室温反应至tlc监测反应完全。降温至0℃,在搅拌下向反应液中滴加浓盐酸调节ph<1,继续保温搅拌4h,有黄色固体生成。抽滤,滤饼用2ml乙醇洗涤两次,干燥,得到黄色固体,即盐酸恩诺沙星,收率92.4%,hplc纯度99.81%。ms(esi)m/z calc.for c
19
h
22
fn3o3[m h] :359.16,found 360.23。1h nmr(600mhz,deuterium oxide)δ8.36(s,1h),7.28(s,1h),7.14(s,1h),3.81(s,2h),3.65(s,2h),3.52(s,1h),3.24(s,6h),1.29(s,5h),1.03(s,2h).
13
c nmr(151mhz,deuterium oxide)δ175.70(d,j=9.0hz),168.67,153.25(d,j=252.2hz),148.16,144.18,138.86,118.63(d,j=7.1hz),110.72,106.55,105.59,52.32,50.93,46.53,36.17,8.63,7.53.
[0107]
实施例15
[0108][0109]
向50ml反应瓶中,依次投入2g化合物iic(4.73mmol)、13ml乙腈和三甲基甲氧基硅烷(tmsome,1.48g,14.2mmol),不断搅拌至完全溶解,向反应瓶中加入0.69g(s,s)-2,8-二氮杂双环[4.3.0]壬烷(化合物iiic),室温反应至tlc监测反应完全。降温至0℃,在搅拌下向反应液中滴加浓盐酸调节ph<1,继续保温搅拌4h,有黄色固体生成。抽滤,滤饼用2ml乙醇洗涤两次,干燥,得到黄色固体粉末,收率95.2%,hplc纯度99.87%,n-甲基莫西沙星含量0.0473%。
[0110]
实施例16
[0111][0112]
向50ml反应瓶中,依次投入2g化合物iic(4.73mmol)、13ml乙腈和三甲基丙氧基硅烷(tmsopr,1.87g,14.2mmol),不断搅拌至完全溶解,向反应瓶中加入0.69g(s,s)-2,8-二氮杂双环[4.3.0]壬烷(化合物iiic),室温反应至tlc监测反应完全。降温至0℃,在搅拌下向反应液中滴加浓盐酸调节ph<1,继续保温搅拌4h,有黄色固体生成。抽滤,滤饼用2ml乙醇洗涤两次,干燥,得到黄色固体粉末,收率90.1%,hplc纯度99.80%,n-甲基莫西沙星含量0.0494%。
[0113]
实施例17
[0114][0115]
向50ml反应瓶中,依次投入2g化合物iic(4.73mmol)、13ml乙腈和六甲基二硅氮烷(hmds,1.87g,14.2mmol),不断搅拌至完全溶解,向反应瓶中加入0.69g(s,s)-2,8-二氮杂双环[4.3.0]壬烷(化合物iiic),室温反应至tlc监测反应完全。降温至0℃,在搅拌下向反应液中滴加浓盐酸调节ph<1,继续保温搅拌4h,有黄色固体生成。抽滤,滤饼用2ml乙醇洗涤两次,干燥,得到黄色固体粉末,收率94.7%,hplc纯度99.75%,n-甲基莫西沙星含量0.0340%。
[0116]
实施例18
[0117][0118]
向50ml反应瓶中,依次投入2g化合物iic(4.73mmol)、13ml乙腈和六甲基环三硅氧烷(d3,1.05g,4.37mmol),不断搅拌至完全溶解,向反应瓶中加入0.69g(s,s)-2,8-二氮杂双环[4.3.0]壬烷(化合物iiic),室温反应至tlc监测反应完全。降温至0℃,在搅拌下向反应液中滴加浓盐酸调节ph<1,继续保温搅拌4h,有黄色固体生成。抽滤,滤饼用2ml乙醇洗涤两次,干燥,得到黄色固体粉末,收率85.2%,hplc纯度99.79%,n-甲基莫西沙星含量0.0458%。
[0119]
实施例19
[0120][0121]
向50ml反应瓶中,依次投入2g化合物iic(4.73mmol)、13ml乙腈和八甲基环四硅氧烷(d4,1.05g,3.55mmol),不断搅拌至完全溶解,向反应瓶中加入0.69g(s,s)-2,8-二氮杂双环[4.3.0]壬烷(化合物iiic),室温反应至tlc监测反应完全。降温至0℃,在搅拌下向反应液中滴加浓盐酸调节ph<1,继续保温搅拌4h,有黄色固体生成。抽滤,滤饼用2ml乙醇洗涤两次,干燥,得到黄色固体粉末,收率87.1%,hplc纯度99.80%,n-甲基莫西沙星含量0.0441%。
[0122]
实施例20
[0123][0124]
向50ml反应瓶中,依次投入2g化合物iic(4.73mmol)、13ml乙腈和十甲基环五硅氧烷(d5,1.05g,2.84mmol),不断搅拌至完全溶解,向反应瓶中加入0.69g(s,s)-2,8-二氮杂双环[4.3.0]壬烷(化合物iiic),室温反应至tlc监测反应完全。降温至0℃,在搅拌下向反应液中滴加浓盐酸调节ph<1,继续保温搅拌4h,有黄色固体生成。抽滤,滤饼用2ml乙醇洗涤两次,干燥,得到黄色固体粉末,收率89.8%,hplc纯度99.80%,n-甲基莫西沙星含量0.0295%。
[0125]
实施例21
[0126][0127]
向50ml反应瓶中,依次投入2g化合物iic(4.73mmol)、13ml乙腈和聚二甲基硅氧烷(pmds,1.05g),不断搅拌至完全溶解,向反应瓶中加入0.69g(s,s)-2,8-二氮杂双环[4.3.0]壬烷(化合物iiic),室温反应至tlc监测反应完全。降温至0℃,在搅拌下向反应液中滴加浓盐酸调节ph<1,继续保温搅拌4h,有黄色固体生成。抽滤,滤饼用2ml乙醇洗涤两次,干燥,得到黄色固体粉末,收率72.1%,hplc纯度99.71%,n-甲基莫西沙星含量0.0362%。
[0128]
实施例22
[0129][0130]
向50ml反应瓶中,依次投入2g化合物iic(4.73mmol)、13ml乙腈和六甲基二硅氧烷(hmdso,1.15g,7.10mmol),不断搅拌至完全溶解,向反应瓶中加入0.69g(s,s)-2,8-二氮杂双环[4.3.0]壬烷(化合物iiic),室温反应至tlc监测反应完全。降温至0℃,在搅拌下向反应液中滴加浓盐酸调节ph<1,继续保温搅拌4h,有黄色固体生成。抽滤,滤饼用2ml乙醇洗涤两次,干燥,得到黄色固体粉末,收率75.3%,纯度99.27%,n-甲基莫西沙星含量0.5400%。
[0131]
实施例23
[0132][0133]
向50ml反应瓶中,依次投入2g化合物iic(4.73mmol)、13ml乙腈和三乙基甲氧基硅烷(tesome,2.08g,14.20mmol),不断搅拌至完全溶解,向反应瓶中加入0.69g(s,s)-2,8-二氮杂双环[4.3.0]壬烷(化合物iiic),室温反应至tlc监测反应完全。降温至0℃,在搅拌下向反应液中滴加浓盐酸调节ph<1,继续保温搅拌4h,有黄色固体生成。抽滤,滤饼用2ml乙醇洗涤两次,干燥,得到黄色固体粉末,收率88.7%,hplc纯度99.59%,n-甲基莫西沙星含量0.1439%。
[0134]
实施例24
[0135][0136]
向50ml反应瓶中,依次投入2g化合物iic(4.73mmol)、13ml乙腈和叔丁基二甲基甲氧基硅烷(tbsome,2.08g,14.20mmol),不断搅拌至完全溶解,向反应瓶中加入0.69g(s,s)-2,8-二氮杂双环[4.3.0]壬烷(化合物iiic),室温反应至tlc监测反应完全。降温至0℃,在搅拌下向反应液中滴加浓盐酸调节ph<1,继续保温搅拌4h,有黄色固体生成。抽滤,滤饼用2ml乙醇洗涤两次,干燥,得到黄色固体粉末,收率86.1%,hplc纯度99.52%,n-甲基莫西沙星含量0.1555%。
[0137]
实施例25
[0138][0139]
向50ml反应瓶中,依次投入2g化合物iic(0.091mol)、13ml四氢呋喃和三甲基乙氧基硅烷(tmsoet,1.68g,14.2mmol),不断搅拌至完全溶解,向反应瓶中加入0.66g(s,s)-2,8-二氮杂双环[4.3.0]壬烷(化合物iiic),室温反应至tlc监测反应完全。降温至0℃,在搅拌下向反应液中滴加浓盐酸调节ph<1,继续保温搅拌4h。抽滤,滤饼用2ml乙醇洗涤两次,干燥,得到黄色固体粉末,收率68.9%,hplc纯度99.83%,n-甲基莫西沙星含量0.048%。
[0140]
实施例26
[0141][0142]
向50ml反应瓶中,依次投入2g化合物iic(0.091mol)、13ml无水乙醇和三甲基乙氧基硅烷(tmsoet,1.68g,14.2mmol),不断搅拌至完全溶解,向反应瓶中加入0.66g(s,s)-2,8-二氮杂双环[4.3.0]壬烷(化合物iiic),室温反应至tlc监测反应完全。降温至0℃,在搅拌下向反应液中滴加浓盐酸调节ph<1,继续保温搅拌4h。抽滤,滤饼用2ml乙醇洗涤两次,干燥,得到黄色固体粉末,收率83.1%,hplc纯度99.7774%,n-甲基莫西沙星含量0.0996%。
[0143]
实施例27
[0144][0145]
向50ml反应瓶中,依次投入2g化合物iic(0.091mol)、13ml无水甲醇和三甲基乙氧基硅烷(tmsoet,1.68g,14.2mmol),不断搅拌至完全溶解,向反应瓶中加入0.66g(s,s)-2,8-二氮杂双环[4.3.0]壬烷(化合物iiic),室温反应至tlc监测反应完全。降温至0℃,在搅拌下向反应液中滴加浓盐酸调节ph<1,继续保温搅拌4h。抽滤,滤饼用2ml乙醇洗涤两次,干燥,得到黄色固体粉末,收率78.5%,hplc纯度99.8841%,n-甲基莫西沙星含量0.0404%。
[0146]
实施例28
[0147][0148]
向50ml反应瓶中,依次投入2g化合物iic(0.091mol)、13ml1,4-二氧六环和三甲基乙氧基硅烷(tmsoet,1.68g,14.2mmol),不断搅拌至完全溶解,向反应瓶中加入0.66g(s,s)-2,8-二氮杂双环[4.3.0]壬烷(化合物iiic),室温反应至tlc监测反应完全。降温至0℃,在搅拌下向反应液中滴加浓盐酸调节ph<1,继续保温搅拌4h。抽滤,滤饼用2ml乙醇洗涤两次,干燥,得到黄色固体粉末,收率73.2%,hplc纯度99.8824%,n-甲基莫西沙星含量0.0339%。
[0149]
实施例29
[0150][0151]
向50ml反应瓶中,依次投入2g化合物iic(4.73mmol)、13ml乙腈和三甲基乙氧基硅烷(tmsoet,0.70g,5.91mmol),不断搅拌至完全溶解,向反应瓶中加入0.66g(s,s)-2,8-二氮杂双环[4.3.0]壬烷(化合物iiic),室温反应至tlc监测反应完全。降温至0℃,在搅拌下向反应液中滴加浓盐酸调节ph<1,继续保温搅拌4h,有黄色固体生成。抽滤,滤饼用2ml乙醇洗涤两次,干燥,得到黄色固体粉末,收率91.4%,hplc纯度99.7835%,n-甲基莫西沙星含量0.0256%。
[0152]
实施例30
[0153][0154]
向50ml反应瓶中,依次投入2g化合物iic(4.73mmol)、13ml乙腈和三甲基乙氧基硅烷(tmsoet,0.84g,7.10mmol),不断搅拌至完全溶解,向反应瓶中加入0.66g(s,s)-2,8-二氮杂双环[4.3.0]壬烷(化合物iiic),室温反应至tlc监测反应完全。降温至0℃,在搅拌下向反应液中滴加浓盐酸调节ph<1,继续保温搅拌4h,有黄色固体生成。抽滤,滤饼用2ml乙醇洗涤两次,干燥,得到黄色固体粉末,收率96.0%,hplc纯度99.7976%,n-甲基莫西沙星含量0.0223%。
[0155]
实施例31
[0156][0157]
向50ml反应瓶中,依次投入2g化合物iic(4.73mmol)、13ml乙腈和三甲基乙氧基硅烷(tmsoet,0.98g,8.28mmol),不断搅拌至完全溶解,向反应瓶中加入0.66g(s,s)-2,8-二氮杂双环[4.3.0]壬烷(化合物iiic),室温反应至tlc监测反应完全。降温至0℃,在搅拌下向反应液中滴加浓盐酸调节ph<1,继续保温搅拌4h,有黄色固体生成。抽滤,滤饼用2ml乙醇洗涤两次,干燥,得到黄色固体粉末,收率95.1%,hplc纯度99.8177%,n-甲基莫西沙星含量0.0302%。
[0158]
实施例32
[0159][0160]
向50ml反应瓶中,依次投入2g化合物iic(4.73mmol)、13ml乙腈和三甲基乙氧基硅烷(tmsoet,1.12g,9.46mmol),不断搅拌至完全溶解,向反应瓶中加入0.66g(s,s)-2,8-二氮杂双环[4.3.0]壬烷(化合物iiic),室温反应至tlc监测反应完全。降温至0℃,在搅拌下向反应液中滴加浓盐酸调节ph<1,继续保温搅拌4h,有黄色固体生成。抽滤,滤饼用2ml乙醇洗涤两次,干燥,得到黄色固体粉末,收率96.5%,hplc纯99.9063%,n-甲基莫西沙星含量0.0161%。
[0161]
实施例33
[0162][0163]
向50ml反应瓶中,依次投入2g化合物iic(4.73mmol)、13ml乙腈和三甲基乙氧基硅烷(tmsoet,1.40g,11.83mmol),不断搅拌至完全溶解,向反应瓶中加入0.66g(s,s)-2,8-二氮杂双环[4.3.0]壬烷(化合物iiic),室温反应至tlc监测反应完全。降温至0℃,在搅拌下向反应液中滴加浓盐酸调节ph<1,继续保温搅拌4h,有黄色固体生成。抽滤,滤饼用2ml乙醇洗涤两次,干燥,得到黄色固体粉末,收率94.3%,hplc纯99.8526%,n-甲基莫西沙星含量0.0179%。
[0164]
实施例34
[0165][0166]
向50ml反应瓶中,依次投入2.0g化合物iic(4.73mmol)、13ml乙腈和三甲基乙氧基硅烷(tmsoet,1.68g,14.2mmol),不断搅拌至完全溶解,向反应瓶中加入0.66g(s,s)-2,8-二氮杂双环[4.3.0]壬烷(化合物iiic),0℃反应至tlc监测反应完全。保温在搅拌下向反应液中滴加浓盐酸调节ph<1,继续保温搅拌4h,有黄色固体生成。抽滤,滤饼用2ml乙醇洗涤两次,干燥,得到黄色固体粉末,收率94.7%,hplc纯度99.8037%,n-甲基莫西沙星含量
0.0400%。
[0167]
实施例35
[0168][0169]
向50ml反应瓶中,依次投入2.0g化合物iic(4.73mmol)、13ml乙腈和三甲基乙氧基硅烷(tmsoet,1.68g,14.2mmol),不断搅拌至完全溶解,向反应瓶中加入0.66g(s,s)-2,8-二氮杂双环[4.3.0]壬烷(化合物iiic),-10℃反应至tlc监测反应完全。保温在搅拌下向反应液中滴加浓盐酸调节ph<1,继续保温搅拌4h,有黄色固体生成。抽滤,滤饼用2ml乙醇洗涤两次,干燥,得到黄色固体粉末,收率92.3%,hplc纯度99.7581%,n-甲基莫西沙星含量0.0395%。
[0170]
实施例36
[0171][0172]
向50ml反应瓶中,依次投入2.0g化合物iic(4.73mmol)、13ml乙腈和三甲基乙氧基硅烷(tmsoet,1.68g,14.2mmol),不断搅拌至完全溶解,向反应瓶中加入0.66g(s,s)-2,8-二氮杂双环[4.3.0]壬烷(化合物iiic),50℃反应至tlc监测反应完全。保温在搅拌下向反应液中滴加浓盐酸调节ph<1,继续保温搅拌4h,有黄色固体生成。抽滤,滤饼用2ml乙醇洗涤两次,干燥,得到黄色固体粉末,收率89.7%,hplc纯度99.7934%,n-甲基莫西沙星含量0.0443%。
[0173]
实施例37
[0174][0175]
向50ml反应瓶中,依次投入2.0g化合物iic(4.73mmol)、13ml乙腈和三甲基乙氧基硅烷(tmsoet,1.68g,14.2mmol),不断搅拌至完全溶解,向反应瓶中加入0.66g(s,s)-2,8-二氮杂双环[4.3.0]壬烷(化合物iiic),70℃反应至tlc监测反应完全。保温在搅拌下向反应液中滴加浓盐酸调节ph<1,继续保温搅拌4h,有黄色固体生成。抽滤,滤饼用2ml乙醇洗涤两次,干燥,得到黄色固体粉末,收率91.0%,hplc纯度99.7109%,n-甲基莫西沙星含量0.1047%。
[0176]
实施例38
[0177][0178]
向50ml反应瓶中,依次投入2.0g化合物iic(4.73mmol)、13ml乙腈和三甲基乙氧基硅烷(tmsoet,1.68g,14.2mmol),不断搅拌至完全溶解,向反应瓶中加入0.66g(s,s)-2,8-二氮杂双环[4.3.0]壬烷(化合物iiic),回流反应至tlc监测反应完全。保温在搅拌下向反应液中滴加浓盐酸调节ph<1,继续保温搅拌4h,有黄色固体生成。抽滤,滤饼用2ml乙醇洗涤两次,干燥,得到黄色固体粉末,收率85.3%,hplc纯度99.6809%,n-甲基莫西沙星含量0.1360%。本技术实施例所得产物收率如下表:
[0179]
[0180][0181]
可见使用本技术的7-取代-3-喹诺酮羧酸衍生物制备方法,可以得到收率较高的胺化物。相较于传统方法,该方法反应条件温和、绿色环保、收率高、副产物少。
[0182]
以上仅为本发明的优选实施例而已,并不用于限制本发明,对于本领域的技术人员来说,本发明可以有各种更改和变化。凡在本发明的精神和原则之内,所作的任何修改、等同替换、改进等,均应包含在本发明的保护范围之内。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。

