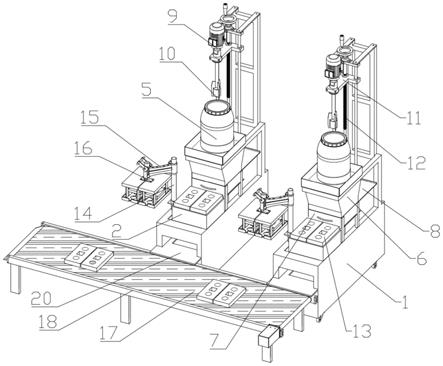
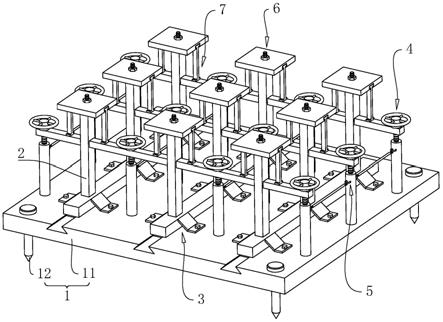
1.本发明涉及消毒剂技术领域,尤其涉及一种含低浓度过氧化氢的医用抗病毒消毒剂。
背景技术:
2.消毒剂是用于杀灭传播媒介上病原微生物的药物,其将病原微生物消灭于人体之外,切断传染病的传播途径,达到控制传染病的目的,新冠肺炎疫情防控形势依然严峻复杂,除去戴口罩,勤洗手外,对生活环境消毒也是控制疫情非常有效的手段。
3.国家卫健委在诊疗方案中明确说“新冠状病毒对紫外线和热敏感,56℃30分钟、乙醚、75%乙醇、含氯消毒剂、过氧乙酸和氯仿等脂溶剂均可有效灭活病毒,氯己定不能有效灭活病毒”,其中,乙醚、乙醇、酒精易燃,使用时需远离明火,禁止以喷雾的方式使用,应采取擦拭的方式,酒精消毒剂主要推荐用于手部,环境消毒建议采用其他消毒剂,以免留下消防安全隐患,含氯消毒剂产品有一定刺激性和腐蚀性,必须稀释后才能使用,使用时戴手套。
4.过氧化氢水溶液又称双氧水,属强氧化剂,高浓度的过氧化氢虽然杀菌效果强,但是对皮肤刺激性也大,不太适合用于家庭环境消毒,但低浓度过氧化氢的稳定性很差,而且浓度越低,杀菌效能越弱,过氧化氢分子中有两个氢原子和两个氧原子,在水中能缓慢释放出异常活泼的新生态氧原子,新生态的氧原子一旦接触到微生物,就会破坏微生物蛋白结构,使得微生物的蛋白变性,从而导致微生物死亡,达到灭活微生物效果。
5.季铵盐是良好的清洁剂,被广泛用作医疗保健环境中非关键环境表面的消毒,季铵盐因具有良好的表面活性,可高度聚集与微生物菌体周围,改变微生物细胞的渗透性,使得微生物菌体物质外渗阻碍其代谢而使细菌死亡。
6.但是,根据文献资料得知低浓度的过氧化氢不能灭活没有脂质包膜亲水病毒(脊髓灰质炎病毒),季铵盐也不能灭活没有脂质包膜亲水病毒(脊髓灰质炎病毒),因此,本发明提供了一种含低浓度的过氧化氢与季铵盐复配消毒剂,该复配消毒剂能够灭活没有脂质包膜亲水病毒(脊髓灰质炎病毒),可用于家庭环境以及医院环境的高效杀菌。
技术实现要素:
7.为了解决上述背景技术中所提到的技术问题,而提出的一种含低浓度过氧化氢的医用抗病毒消毒剂。
8.为了实现上述目的,本发明采用了如下技术方案:
9.一种含低浓度过氧化氢的医用抗病毒消毒剂,所述消毒剂的总重量按照100wt%计,包括0.3
‑
3.0%过氧化氢、0.1
‑
5.0%表面活性剂、1.0
‑
5.0%杀菌增效剂,0.3
‑
1.0%稳定剂、0.01%
‑
1.0%金属抑蚀剂、0.1
‑
1.0%酸碱调节剂和86
‑
98.19%纯化水;
10.在10
‑
25℃和1个大气压的条件下,所述消毒剂的具体制备方法包括以下步骤:
11.s1、先在配料桶中加入56
‑
68.19%的纯化水,再将稳定剂加入配料桶中搅拌
10min,直至完全溶解为止;
12.s2、将表面活性剂、杀菌增效剂、金属抑蚀剂和酸碱调节剂依次加入步骤s1的溶液中,搅拌10min直至完全溶解为止;
13.s3、将过氧化氢以及剩余30%的纯化水加入步骤s2的溶液中,搅拌10
‑
15min,直至混合均匀,静置30min,得到澄清透明溶液,溶液ph值3.5
‑
4.5。
14.作为上述技术方案的进一步描述:
15.所述稳定剂包括己二胺四亚甲基膦酸、二乙烯三胺五亚甲基膦酸、氨基三亚甲基膦酸和羟基亚乙基二膦酸中的至少一种。
16.作为上述技术方案的进一步描述:
17.所述表面活性剂包括月桂基二甲基氧化胺、椰油酰胺二甲基氧化胺、十二烷基硫酸钠、十二烷基磺酸钠、十二烷基苯环酸钠和十二烷基苯磺酸中的至少一种。
18.作为上述技术方案的进一步描述:
19.所述杀菌增效剂包括苯扎氯铵、双癸基二甲基氯化铵和乙醇中的至少一种。
20.作为上述技术方案的进一步描述:
21.所述金属抑蚀剂包括三乙醇胺、二乙醇胺、苯甲酸钠和苯并三氮唑中的至少一种。
22.作为上述技术方案的进一步描述:
23.所述酸碱调节剂包括磷酸二氢钾、磷酸钾和三聚磷酸钠中的至少一种。
24.综上所述,由于采用了上述技术方案,本发明的有益效果是:
25.1、本发明中,低浓度过氧化氢复配季铵盐消毒剂的制备工艺简单,产品性质稳定,可采用喷雾的方式也可采取擦拭的方式对环境表面进行消毒,低含量的过氧化氢对皮肤无刺激,对各类环境表面无腐蚀,使用时无需稀释,且杀菌作用快速,对脊髓灰质炎病毒1min能达到杀灭效果,是一款理想的用于家庭及医院环境消毒的消毒产品。
26.2、本发明中,消毒剂中季铵盐大大提升了过氧化氢的杀菌效率,季铵盐的烷基链具有亲脂性,能够与微生物中磷脂和蛋白质结合,固定微生物,使得溶液中过氧化氢释放活性氧原子更易接触微生物,使得微生物蛋白更易变性,达到协同灭活微生物的效果。
具体实施方式
27.下面对本发明实施例中的技术方案进行清楚、完整地描述,显然,所描述的实施例仅仅是本发明一部分实施例,而不是全部的实施例。基于本发明中的实施例,本领域普通技术人员在没有作出创造性劳动前提下所获得的所有其它实施例,都属于本发明保护的范围。
28.实施例一
29.具体的,本发明提供一种技术方案:一种含低浓度过氧化氢的医用抗病毒消毒剂,消毒剂的总重量按照100wt%计,包括0.3
‑
3.0%过氧化氢、0.1
‑
5.0%表面活性剂、1.0
‑
5.0%杀菌增效剂,0.3
‑
1.0%稳定剂、0.01%
‑
1.0%金属抑蚀剂、0.1
‑
1.0%酸碱调节剂和86
‑
98.19%纯化水;
30.具体的,稳定剂包括己二胺四亚甲基膦酸、二乙烯三胺五亚甲基膦酸、氨基三亚甲基膦酸和羟基亚乙基二膦酸中的至少一种,表面活性剂包括月桂基二甲基氧化胺、椰油酰胺二甲基氧化胺、十二烷基硫酸钠、十二烷基磺酸钠、十二烷基苯环酸钠和十二烷基苯磺酸
中的至少一种,杀菌增效剂包括苯扎氯铵、双癸基二甲基氯化铵和乙醇中的至少一种,金属抑蚀剂包括三乙醇胺、二乙醇胺、苯甲酸钠和苯并三氮唑中的至少一种,酸碱调节剂包括磷酸二氢钾、磷酸钾和三聚磷酸钠中的至少一种;
31.在10
‑
25℃和1个大气压的条件下,消毒剂的具体制备方法包括以下步骤:
32.s1、先在配料桶中加入60g的纯化水,再将0.25g己二胺四亚甲基磷酸加入配料桶中搅拌10min,直至完全溶解为止;
33.s2、将0.5g月桂基二甲基氧化胺、0.25g苯扎氯铵、0.2g三乙醇胺和0.11g磷酸氢二钾依次加入步骤s1的溶液中,搅拌10min直至完全溶解为止;
34.s3、将0.5g过氧化氢加入步骤s2的溶液后,再加入纯化水至100g,搅拌10
‑
15min,直至混合均匀,静置30min,得到澄清透明溶液,溶液ph值3.5
‑
4.5。
35.实施例二
36.在10
‑
25℃和1个大气压的条件下,消毒剂的具体制备方法包括以下步骤:
37.s1、先在配料桶中加入60g的纯化水,再将0.25g己二胺四亚甲基磷酸加入配料桶中搅拌10min,直至完全溶解为止;
38.s2、将0.5g月桂基二甲基氧化胺、0.25g双癸基二甲基氯化铵、0.2g三乙醇胺和0.11g磷酸氢二钾依次加入步骤s1的溶液中,搅拌10min直至完全溶解为止;
39.s3、将0.5g过氧化氢加入步骤s2的溶液后,再加入纯化水至100g,搅拌10
‑
15min,直至混合均匀,静置30min,得到澄清透明溶液,溶液ph值3.5
‑
4.5。
40.实施例三
41.在10
‑
25℃和1个大气压的条件下,消毒剂的具体制备方法包括以下步骤:
42.s1、先在配料桶中加入60g的纯化水,再将0.25g己二胺四亚甲基磷酸加入配料桶中搅拌10min,直至完全溶解为止;
43.s2、将0.5g月桂基二甲基氧化胺、0.15g苯扎氯铵、0.1g双癸基二甲基氯化铵、0.1g三乙醇胺和0.11g磷酸氢二钾依次加入步骤s1的溶液中,搅拌10min直至完全溶解为止;
44.s3、将0.5g过氧化氢加入步骤s2的溶液后,再加入纯化水至100g,搅拌10
‑
15min,直至混合均匀,静置30min,得到澄清透明溶液,溶液ph值3.5
‑
4.5。
45.实施例四
46.在10
‑
25℃和1个大气压的条件下,消毒剂的具体制备方法包括以下步骤:
47.s1、先在配料桶中加入60g的纯化水,再将0.25g己二胺四亚甲基磷酸加入配料桶中搅拌10min,直至完全溶解为止;
48.s2、将0.5g月桂基二甲基氧化胺、0.25g苯扎氯铵、0.05g苯并三氮唑和0.2g三乙醇胺依次加入步骤s1的溶液中,搅拌10min直至完全溶解为止;
49.s3、将1.0g过氧化氢加入步骤s2的溶液后,再加入纯化水至100g,搅拌10
‑
15min,直至混合均匀,静置30min,得到澄清透明溶液,溶液ph值3.5
‑
4.5。
50.实施例五
51.在10
‑
25℃和1个大气压的条件下,消毒剂的具体制备方法包括以下步骤:
52.s1、先在配料桶中加入60g的纯化水,再将0.25g己二胺四亚甲基磷酸加入配料桶中搅拌10min,直至完全溶解为止;
53.s2、将0.5g月桂基二甲基氧化胺、0.25g苯扎氯铵、0.05g苯并三氮唑和0.2g磷酸氢
二钾依次加入步骤s1的溶液中,搅拌10min直至完全溶解为止;
54.s3、将3.0g过氧化氢加入步骤s2的溶液后,再加入纯化水至100g,搅拌10
‑
15min,直至混合均匀,静置30min,得到澄清透明溶液,溶液ph值3.5
‑
4.5。
55.实施例六
56.在10
‑
25℃和1个大气压的条件下,消毒剂的具体制备方法包括以下步骤:
57.s1、先在配料桶中加入60g的纯化水,再将0.25g氨基三亚甲基膦酸加入配料桶中搅拌10min,直至完全溶解为止;
58.s2、将0.5g椰油酰胺二甲基氧化胺、0.15g苯扎氯铵、0.1g双癸基二甲基氯化铵、0.2g三乙醇胺和0.11g磷酸氢二钾依次加入步骤s1的溶液中,搅拌10min直至完全溶解为止;
59.s3、将0.5g过氧化氢加入步骤s2的溶液后,再加入纯化水至100g,搅拌10
‑
15min,直至混合均匀,静置30min,得到澄清透明溶液,溶液ph值3.5
‑
4.5。
60.实施例七
61.在10
‑
25℃和1个大气压的条件下,消毒剂的具体制备方法包括以下步骤:
62.s1、先在配料桶中加入60g的纯化水,再将0.25g羟基亚乙基二膦酸加入配料桶中搅拌10min,直至完全溶解为止;
63.s2、将0.5g椰油酰胺二甲基氧化胺、0.15g苯扎氯铵、0.1g双癸基二甲基氯化铵、0.03g苯并三氮唑和0.2g三乙醇胺依次加入步骤s1的溶液中,搅拌10min直至完全溶解为止;
64.s3、将0.5g过氧化氢加入步骤s2的溶液后,再加入纯化水至100g,搅拌10
‑
15min,直至混合均匀,静置30min,得到澄清透明溶液,溶液ph值3.5
‑
4.5。
65.实施例八
66.在10
‑
25℃和1个大气压的条件下,消毒剂的具体制备方法包括以下步骤:
67.s1、先在配料桶中加入60g的纯化水,再将0.3g羟基亚乙基二膦酸加入配料桶中搅拌10min,直至完全溶解为止;
68.s2、将0.5g椰油酰胺二甲基氧化胺、0.15g苯扎氯铵、0.1g双癸基二甲基氯化铵、0.03g苯并三氮唑、0.2g磷酸氢二钾依次加入步骤s1的溶液中,搅拌10min直至完全溶解为止;
69.s3、将0.5g过氧化氢加入步骤s2的溶液后,再加入纯化水至100g,搅拌10
‑
15min,直至混合均匀,静置30min,得到澄清透明溶液,溶液ph值3.5
‑
4.5。
70.对比例一
71.在10
‑
25℃和1个大气压的条件下,消毒剂的具体制备方法包括以下步骤:
72.s1、先在配料桶中加入60g的纯化水,再将0.1g氨基三亚甲基膦酸加入配料桶中搅拌10min,直至完全溶解为止;
73.s2、将0.5g椰油酰胺二甲基氧化胺、0.25g苯扎氯铵、0.05g三乙醇胺和0.2g磷酸氢二钾依次加入步骤s1的溶液中,搅拌10min直至完全溶解为止;
74.s3、将1.0g过氧化氢加入步骤s2的溶液后,再加入纯化水至100g,搅拌10
‑
15min,直至混合均匀,静置30min,得到澄清透明溶液,溶液ph值3.5
‑
4.5。
75.对比例二
76.在10
‑
25℃和1个大气压的条件下,消毒剂的具体制备方法包括以下步骤:
77.s1、先在配料桶中加入60g的纯化水,再将0.25g己二胺四亚甲基膦酸加入配料桶中搅拌10min,直至完全溶解为止;
78.s2、将0.5g月桂基二甲基氧化胺、0.03g苯并三氮唑和0.2g三乙醇胺依次加入步骤s1的溶液中,搅拌10min直至完全溶解为止;
79.s3、将1.0g过氧化氢加入步骤s2的溶液后,再加入纯化水至100g,搅拌10
‑
15min,直至混合均匀,静置30min,得到澄清透明溶液,溶液ph值3.5
‑
4.5。
80.按照实施例一~八和对比例一、二的制备方法配置不同的消毒剂,并对该十种消毒剂分别进行“病毒灭活实验”、“稳定性测试”和“金属腐蚀性测试”。
81.具体的,脊髓灰质炎悬液定量灭活试验操作包括以下步骤:
82.(1)从液氮中取出冻存的试验宿主细胞,在37℃温水中迅速融化,并用细胞维持液洗涤两次后,转种于加有10ml完全培养基培养瓶中,逐日观察细胞生长情况,在细胞长满单层时,用于消毒试验;
83.(2)取出低温冻存的脊髓灰质炎
‑
1毒株,37℃水浴融化,用细胞维持液作10倍稀释,然后接种于含已经长满单层细胞的细胞瓶内,置37℃温箱中,使与细胞吸附、生长,逐日观察病变,待3/4细胞出现病变时,收获病毒,收获时,将培养液取出,用超声波或反复冻融破碎宿主细胞,尽快离心,并将含病毒的上清液按每管1.0ml分装于无菌离心管(1.5ml)中,冷冻保存于
‑
80℃备用;
84.(3)取待测的消毒剂,用灭菌硬水稀释至所需浓度的1.25倍,于20℃
±
1℃水浴中备用;
85.(4)取100μl有机干扰物质与100μl病毒原液混合,于20℃
±
1℃水浴中作用5min,加入0.8ml待检消毒剂,立即混匀并记时,作用规定时间,立即取出0.1ml,加入中和剂中混匀,或用经鉴定合格的除药方法处理;
86.(5)阳性(病毒)对照组试验中,用无菌去离子水代替消毒剂;
87.(6)各组分别进行病毒滴度测定,可采用终点稀释法或噬斑法进行;
88.具体的,终点稀释法操作步骤:先用细胞维持培养液对待滴定样本做10倍系列稀释,然后在96孔培养板上滴定各稀释度样本中残留的病毒量,每个稀释度做4孔(各孔中应该已经长满单层的宿主细胞),在37℃,放置1h~2h,以确保残留病毒全部吸附在细胞上,取出培养板,更换细胞维持培养液,继续放入二氧化碳培养箱中(37℃,5%co2)培养,逐日在显微镜下观察细胞病变,连续观察3d,逐孔观察并记录细胞病变情况,其中,终点稀释法病毒感染滴度的计算:以半数细胞感染剂量(tcid50)表示;
89.具体的,噬斑法操作步骤:先用细胞维持培养液对待滴定样本做10倍系列稀释,然后接种于细胞培养瓶中,滴定各稀释度样本中残留的病毒量,接种细胞前,将生长致密的单层细胞中的培养液倾出,加入1ml待测样品,放置37℃吸附1h~2h,倾出样液,加入含0.8%琼脂的细胞维持液3ml,冷却后翻转细胞瓶,放置37℃培养48h~72h,然后每瓶细胞加入2ml甲醛溶液固定数分钟,用自来水冲洗后加结晶紫溶液染色数分钟,冲洗干净后计数,细胞瓶内圆形不着色的透明区即为一个蚀斑单位,每毫升测试样品中的病毒含量计算:pfu/ml=平板平均蚀斑数
×
稀释倍数,为了便于计数,病毒蚀斑数一般控制在每细胞瓶10pfu~30pfu;
90.具体的,平均灭活对数值按下式计算:设阳性(病毒)对照组平均病毒感染滴度(tcid50或pfu)的为n0,试验(消毒)组平均病毒感染滴度(tcid50或pfu)为n
x
,平均灭活对数值=log n0‑
log n
x
;
91.(7)试验重复3次。
92.脊灰病毒灭活试验可用于评价医疗器械、食具、物体表面和皮肤用化学消毒剂对病毒的灭活效果,病毒的灭活滴度,应达到4个对数值,其次,在正常情况下,3次试验的平均灭活对数值≥4.00,可判为对脊髓灰质炎病毒污染物消毒的实验室试验合格,同时,阳性对照组病毒滴度对数值应在5~7之间。
93.具体的,稳定性测试采用加速试验法,包括以下步骤:取包装好的消毒剂,置37℃(对粉剂、片剂要求相对湿度>75%)恒温箱内3个月,或54℃恒温箱内14d,于放置前、后分别测定消毒剂杀菌有效成分含量,每次检测样品为三批,每批样品重复测2次,取其平均值即可。
94.加速试验法结果评价以有效成分下降率超过10%为不符合要求,经54℃存放14d者,杀菌有效成分下降率≤10%,则贮存有效期可定为1年。
95.具体的,金属腐蚀性测试的步骤包括:
96.(1)在有表面活性作用的清洁剂中浸泡10min,充分去油,洗净,亦可用氧化镁糊剂涂抹除油后洗净,以120号粒度水砂纸磨去金属片两面和周边表面的氧化层,再用自来水冲净,测量片的直径、厚度、孔径(精确至0.1mm),用无水丙酮或无水乙醇再次脱脂,置50℃恒温箱中干燥1h,待其温度降至室温后称重(每金属片待天平回零后称重3次,精确至0.1mg),取其平均值作为试验前重量,称重时,应戴洁净手套,勿以手直接接触样片;
97.(2)按消毒剂最高使用浓度配制试验用消毒剂,用以浸泡试验样片,浸泡时,每一金属片需浸泡在200ml消毒剂中;
98.(3)金属样片用塑料线系以标签,编号和注明日期,悬挂于消毒剂中,一次性浸泡72h,易挥发性或有效成分不稳定的消毒剂,根据情况酌情定时更换消毒剂,直至浸泡72h;
99.(4)每种金属每次试验放置3片样片,浸泡时,若同种金属每一样片相隔1cm以上,可在同一容器内(含600ml消毒剂)进行;
100.(5)浸泡到规定时间后,取出金属片,先用自来水冲洗,再用毛刷或其它软性器具去除腐蚀产物,如仍有清除不掉的腐蚀产物,可按gb 10124
‑
88所介绍的下列方法清除:铜片:在室温下浸泡于盐酸溶液(500ml 36%~38%盐酸加蒸馏水至1000ml,盐酸比重为1.19)中1min~3min;碳钢片:置含锌粉200g/l的氢氧化钠溶液中,煮沸5min~30min;铝片:浸泡于三氧化铬磷酸溶液(三氧化铬20g,磷酸500ml,加蒸馏水至1000ml,磷酸比重为1.69)中,升温至80℃,持续5min~10min,如还未清除干净,可在室温浸于硝酸(比重1.42)溶液中1min;不锈钢:浸泡于60℃硝酸溶液(66%~68%硝酸100ml加蒸馏水至1000ml)20min。或浸于70℃柠檬酸铵溶液(柠檬酸铵150g加蒸馏水至1000ml)中10min~60min;
101.(6)金属样片除去腐蚀产物并清洗后,用粗滤纸吸干水分,置于垫有滤纸的平皿中,放入50℃温箱,干燥1h,用镊子夹取,待其温度降至室温后分别在天平上称重,天平回零后称3次,以其平均值作为试验后重量,称重时,与试验前相同,应戴洁净手套,勿以手直接接触样片(下同);
102.(7)样片在用化学法去除腐蚀物时,需设相应空白对照以校正误差,空白对照样片
与试验组样片同样进行表面处理、洗净和称重,但不经消毒剂浸泡,事后随同试验组样片用相同方法进行化学处理、水冲洗、干燥、称重,并计算其平均失重值;
103.(8)试验的全过程应同时设不锈钢片浸泡蒸馏水的对照,浸泡前后的重量差应<0.3mg,否则,在找出原因后,全部试验重做;
104.(9)试验结果,观察与纪录金属片颜色变化,并以金属腐蚀速率(r)平均值表达,在计算时应减去空白对照组样片的失重值。计算公式如下:
[0105][0106]
其中,r—为腐蚀速率,mm/a(毫米/年);
[0107]
m—试验前金属片重量,g;
[0108]
m
t
—试验后金属片重量,g;
[0109]
m
k
—化学处理去除腐蚀产物样片失重值,g,试验中未进行化学清除
[0110]
处理者,计算时在公式中删去m
k
值;
[0111]
s—金属片的表面积总值,cm2;
[0112]
t—试验时间,h;
[0113]
d—金属材料密度,kg/m3。
[0114]
具体的,金属腐蚀性分级标准如以下表1所示:
[0115]
表1金属腐蚀性分级标准表
[0116]
腐蚀速率r(mm/a)级别<0.0100基本无腐蚀0.0100~<0.100轻度腐蚀0.100~<1.00中度腐蚀≥1.00重度腐蚀
[0117]
实施例一~八和对比例一、二的稳定性、脊髓灰质炎病毒灭活效果即碳钢腐蚀性如以下表2、3所示:
[0118]
表2实施例一~五的稳定性、腐蚀性和病毒灭活效果数据表
[0119][0120]
表3实施例六~八和对比例一、二的稳定性、腐蚀性和病毒灭活效果数据表
[0121][0122]
通过表2和表3可知,实施例四~七中,含低浓度过氧化氢复配季胺盐消毒剂产品性能稳定,低含量的过氧化氢及季铵盐对皮肤无刺激,对各类环境表面无腐蚀,对脊髓灰质病毒1min能达到杀灭效果,杀菌快速。
[0123]
以上所述,仅为本发明较佳的具体实施方式,但本发明的保护范围并不局限于此,任何熟悉本技术领域的技术人员在本发明揭露的技术范围内,根据本发明的技术方案及其发明构思加以等同替换或改变,都应涵盖在本发明的保护范围之内。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。