相关申请的交叉引用
本专利申请要求于2018年12月20日提交的意大利专利申请号102018000020419的优先权,将其整个公开内容通过引用结合于此。
本发明涉及一种包含至少一种二噻吩基吡啶噻二唑(dithienylpyridinethiadiazole,或称为二噻吩基吡啶并噻二唑)化合物的发光太阳能集中器(luminescentsolarconcentrator,lsc)。
更特别地,本发明涉及一种发光太阳能集中器(lsc),其包含至少一种具有以下报告的特定通式(i)或(ii)的二噻吩基吡啶噻二唑化合物。
本发明还涉及至少一种具有以下报告的特定通式(i)或(ii)的二噻吩基吡啶噻二唑化合物在构建发光太阳能集中器(lsc)中的用途。
所述发光太阳能集中器(lsc)可以有利地用于在刚性支架和柔性支架上构建例如选自光伏电池(或太阳能电池)、光伏模块(或太阳能模块)的光伏装置(或太阳能装置)。
因此,本发明还涉及一种光伏装置(或太阳能装置),其包括至少一个光伏电池(或太阳能电池)以及至少一个包含至少一种具有以下报告的特定通式(i)或(ii)的二噻吩基吡啶噻二唑化合物的发光太阳能集中器(lsc)。
应当注意的是,具有特定通式(i)或(ii)的二噻吩基吡啶噻二唑化合物中的一些是新的。因此,所述具有特定通式(i)或(ii)的二噻吩基吡啶噻二唑化合物是本发明的另一个目的。
背景技术:
在现有技术中,利用太阳辐射能量的主要限制之一表现为光伏装置(或太阳能装置)仅最佳地吸收波长落在窄光谱范围内的辐射的能力。
对于从大约300nm的波长扩展到约2500nm的波长的太阳辐射的光谱范围,例如基于晶体硅的光伏电池(或太阳能电池)具有在900nm-1100nm范围内的最佳吸收区(有效光谱),而聚合物光伏电池(或太阳能电池)如果暴露于波长低于约500nm的辐射,则易于损坏,这是由于在低于此限值时变得显著的诱导光降解现象所致。典型地,现有技术的光伏装置(或太阳能装置)的效率在570nm和680nm(黄色-橙色)之间的光谱区域中最大。
上述缺点涉及光伏装置(或太阳能装置)的有限外量子效率(eqe),其被定义为在光伏装置(或太阳能装置)的半导体材料中产生的电子-空穴对的数量与在所述光伏器件(或太阳能器件)上的入射光子数量之间的比率。
为了提高光伏装置(或太阳能装置)的外量子效率(eqe),已经开发出插入在光辐射源(太阳)和光伏装置(或太阳能装置)之间的工具,其选择性地吸收波长在所述光伏装置(或太阳能装置)的有效光谱外部的入射辐射,从而以包括在有效光谱中的波长的光子的形式发射所吸收的能量。所述仪器称为发光太阳能集中器(lsc)。当由发光太阳能集中器(lsc)发射的光子的能量高于入射光子的能量时,光致发光过程(包括吸收太阳辐射和随后以较短波长发射光子)也称为上转换过程。相反,当由发光太阳能集中器(lsc)发射的光子的能量低于入射光子的能量时,光致发光过程称为“下转换”过程(或“下移”)。
通常,所述发光太阳能集中器(lsc)由对太阳辐射透明的材料(例如,聚合物或无机玻璃)的大片组成,在该发光太阳能集中器内充当光谱转换器的荧光化合物分散或化学连接至所述材料。由于全反射的光学现象,所以由荧光化合物发射的辐射被“引导”朝向片的薄边缘,在那里它集中到放置在其上的光伏电池(或太阳能电池)上。以这种方式,低成本材料(光致发光片)的大表面可以用于将光集中在高成本材料[光伏电池(或太阳能电池)]的小表面上。
荧光化合物可以以薄膜的形式沉积在玻璃支架上,或者如在聚合物材料的情况下,它们可以分散在聚合物基体内。可选地,聚合物基体可以直接用荧光发色团进行官能化。
理想情况下,为了用于构建发光太阳能集中器(lsc),荧光化合物必须具有以下特性:
-高发光量子效率(φ),所述发光量子效率(φ)根据以下报告的公式(1)定义为每单位时间发射的光子数与被发光分子吸收的光子数之间的比率,并且其最大值为1:
(φ)=发射的光子数/吸收的光子数(1);
-在其中光伏装置(或太阳能装置)效率低下的光谱区域中的宽吸收带;
-高吸收系数;
-在其中光伏装置(或太阳能装置)效率更高的光谱区域中的窄发射带;
-良好分离的吸收和发射带以避免或最小化自吸收现象。
已知的是,一些苯并噻二唑化合物,特别是4,7-二-(噻吩-2'-基)-2,1,3-苯并噻二唑(dtb),是可用于构建发光太阳能集中器(lsc)的荧光化合物。例如,在以申请人名义的国际专利申请wo2011/048458中已经描述了这种类型的化合物。
4,7-二-(噻吩-2'-基)-2,1,3-苯并噻二唑(dtb)的特征在于集中在579nm周围的发射,该值对应于远高于光伏电池(或太阳能电池)的操作的最低阈值的能量,该阈值例如对于最常见的硅基光伏电池(或太阳能电池)对应于约1100nm的波长。此外,其对光辐射的吸收强,并且在相对较宽的波长范围(包括指示性地介于550nm(绿色辐射的波长)和紫外线之间)内扩展。最后,4,7-二-(噻吩-2'-基)-2,1,3-苯并噻二唑(dtb)在二氯甲烷溶液中具有等于134nm的斯托克斯位移(stokes'shift),这远高于迄今为止提议用于发光太阳能集中器(lsc)的大多数商业产品的斯托克斯位移。
由于这些原因,使用4,7-二-(噻吩-2'-基)-2,1,3-苯并噻二唑(dtb)使得可以制造出优异品质的发光太阳能集中器(lsc)。
然而,4,7-二-(噻吩-2'-基)-2,1,3-苯并噻二唑(dtb)虽然吸收太阳光谱的很大一部分,但是在太阳光谱的更大波长区域(对应于黄色和红色辐射)中显示出适度的吸收,因此不能将其转换为被光伏电池(或太阳能电池)更有效利用的其他辐射。
二噻吩基吡啶噻二唑化合物也是已知的。
例如,bathulac.等人在“journaloffluorescence”(2016),第26卷,第3期,第1045-1052页中报告了具有下式(a)的4,7-双[(4-(2-乙基己基)-噻吩-2-基]-[1,2,5]噻二唑[3,4-c]吡啶:
其作为用于合成基于噻二唑[3,4-c]吡啶的共聚物的共聚单体,该共聚物可用于有机电子设备领域,例如用于有机场效应晶体管(“有机发光二极管”-oled)。
welchg.c.等人在“journalofmaterialschemistry”(2011),第21卷,第12700-12709页中报告了包含噻二唑[3,4-c]吡啶的有机分子,其包括具有式(6)的化合物:
以及它们在有机光伏电池中作为电子给体材料的用途,所述有机光伏电池具有通过溶液中的工艺获得的被称为本体异质结的结构。所述包含噻二唑[3,4-c]吡啶的有机分子(包括具有式(6)的化合物),以及它们作为电子给体材料在有机光伏电池中的用途(所述有机光伏电池具有借助于溶液中的工艺获得的被称为本体异质结的结构)也在美国专利申请us2014/0167002中描述。
bazang.c.等人在“journaloftheamericanchemicalsociety”(2013),第135(6)卷,第2298-2305页中报告了合成可用于有机电子设备领域中的包括噻二唑[3,4-c]吡啶的两种有机分子,即具有式(b)的化合物和具有式(c)的化合物:
因此,申请人已提出了寻找这样的化合物的问题,该化合物能够在具有较长波长(对应于黄色和红色辐射)的太阳光谱区域中具有良好吸收,并且因此相对于已知的苯并噻二唑化合物,特别是与4,7-二-(噻吩-2'-基)-2,1,3-苯并噻二唑(dtb)相比,能够提供相当或甚至更高的性能,特别是在由其中使用它们的光伏装置(或太阳能装置)产生的功率方面。
技术实现要素:
申请人现在已发现了具有特定通式[即具有以下报告的通式(i)或(ii)]的二噻吩基吡啶噻二唑化合物,其可以有利地用于构建发光太阳能集中器(lsc)。所述发光太阳能集中器(lsc)又可以有利地例如与光伏电池(或太阳能电池)一起用于构建光伏装置(或太阳能装置)。与已知的苯并噻二唑类化合物相比,特别是相对于4,7-二-(噻吩-2'-基)-2,1,3-苯并噻二唑(dtb),所述二噻吩基吡啶噻二唑化合物能够提供相当或甚至更高的性能,特别是在由其中使用它们的光伏装置产生的功率方面。
因此,本发明的一个目的是一种发光太阳能集中器(lsc),其包含至少一种具有通式(i)或(ii)的二噻吩基吡啶噻二唑化合物:
其中:
-r1、r2、r3、r4、r5和r6彼此相同或不同,表示氢原子;或它们选自直链或支链的、饱和或不饱和的c1-c20、优选c1-c8烷基(任选地含有杂原子)、任选取代的芳基、任选取代的杂芳基;
-r7彼此相同或不同,表示氢原子;或它们选自直链或支链的、饱和或不饱和的c1-c20、优选c1-c8烷基(任选地含有杂原子)、任选取代的芳基、任选取代的杂芳基、任选取代的苯氧基;
-或r1和r2或r2和r3和/或r4和r5或r5和r6可以任选地连接在一起以便与它们所连接的碳原子一起形成饱和的、不饱和的或芳族的环或多环体系(含有3至14个碳原子,优选4至6个碳原子),该环或多环体系任选地含有一个或多个杂原子诸如例如氧、硫、氮、硅、磷、硒;
-y表示含有一个或多个芳族或杂芳族环的二价环或多环基团,所述芳族或杂芳族环被任选取代;
-n为0或1;
-p为0或1。
如上所述的,具有特定通式(i)或(ii)的二噻吩基吡啶噻二唑化合物中的一些是新的。特别地,具有其中彼此相同或不同的取代基r1和r6选自任选取代的芳基的通式(i)或(ii)的化合物是新的。
因此,本发明的另一个目的是一种具有通式(i)或(ii)的二噻吩基吡啶噻二唑化合物:
其中:
-r2、r3、r4和r5彼此相同或不同,表示氢原子;或它们选自直链或支链的、饱和或不饱和的c1-c20、优选c1-c8烷基(任选地含有杂原子)、任选取代的芳基、任选取代的杂芳基;
-r7彼此相同或不同,表示氢原子;或它们选自直链或支链的、饱和或不饱和的c1-c20、优选c1-c8烷基(任选地含有杂原子)、任选取代的芳基、任选取代的杂芳基、任选取代的苯氧基;
-r1和r6彼此相同或不同,选自任选取代的芳基、任选取代的杂芳基;
-或r2和r3和/或r4和r5可以任选地连接在一起以便与它们所连接的碳原子一起形成含有3至14个碳原子,优选4至6个碳原子的饱和的、不饱和的或芳族的环或多环体系,所述环或多环体系任选地含有一个或多个杂原子诸如例如氧、硫、氮、硅、磷、硒;
-y表示含有一个或多个芳族或杂芳族环的二价环或多环基团,所述芳族或杂芳族环被任选取代;
-n为0或1;
-p为0或1。
出于本说明书和所附权利要求的目的,除非另有说明,数字区间的定义始终包括极值。
出于本说明书和所附权利要求的目的,术语"包括"也包括术语"其基本上由……组成"或"其由……组成"。
出于本说明书和所附权利要求的目的,术语"c1-c20烷基"是指直链或支链的、饱和或不饱和的具有1至20个碳原子的烷基。c1-c20烷基的具体实例是:甲基、乙基、正丙基、异丙基、正丁基、异丁基、叔丁基、戊基、2-乙基-己基、己基、庚基、辛基、壬基、癸基、十二烷基。
出于本说明书和所附权利要求的目的,术语"任选地含有杂原子的c1-c20烷基"是指其中氢原子中的至少一个被杂原子取代的直链或支链的、饱和或不饱和的具有1至20个碳原子的烷基,所述杂原子选自:卤素,诸如例如氟、氯,优选氟;氮;硫;氧。任选地含有杂原子的c1-c20烷基的具体实例是:氟甲基、二氟甲基、三氟甲基、三氯甲基、2,2,2-三氟乙基、2,2,2-三氯乙基、2,2,3,3-四氟丙基、2,2,3,3,3-五氟丙基、全氟戊基、全氟辛基、全氟癸基、甲氧基、乙氧基、丁氧基甲硫基、乙硫基、二甲氨基、丙氨基、二辛氨基、甲硫醚、乙硫醚、丁硫醚。
出于本说明书和所附权利要求的目的,术语"芳基"是指芳族碳环基团。所述芳基可以任选地被一个或多个基团取代,所述一个或多个基团彼此相同或不同,选自:卤素原子诸如例如氟、氯,优选氟;羟基;c1-c20烷基;c1-c20烷氧基;氰基;氨基;硝基;芳基;苯氧基;酯基;硫醚基团。芳基的具体实例是:苯基、甲基苯基、二甲基苯基、三甲基苯基、二-异丙基苯基、叔丁基苯基、甲氧基苯基、羟基苯基、苯氧基苯基、氟苯基、五氟苯基、氯苯基、硝基苯基、二苯氨基、二甲氨基苯基、二苯氨基苯基、萘基、苯基萘基、菲、蒽、苯硫醚、苄硫醚、2-苯氧基苯基、4-苯氧基苯基、2,4-二苯氧基苯基、2,6-二苯氧基苯基、2,4,6-三苯氧基苯基。
出于本说明书和所附权利要求的目的,术语"杂芳基"是指含有4至60个碳原子和1至4个杂原子的杂环芳族的五原子或六原子基团,也是苯并稠合的或杂二环的,所述杂原子选自氮、氧、硫、硅、硒、磷。所述杂芳基可以任选地被一个或多个基团取代,该一个或多个基团彼此相同或不同,选自:卤素原子诸如例如氟、氯、溴,优选氟;羟基;c1-c12烷基;c1-c12烷氧基;c1-c12硫代烷氧基;c3-c24三烷基硅烷基;c3-c24三烷氧基硅烷基;聚乙烯氧基;氰基;氨基;c1-c12单-或二-烷基胺基团;硝基。杂芳基的具体实例是:吡啶、甲基吡啶、甲氧基吡啶、苯基吡啶、氟吡啶、嘧啶、哒嗪、吡嗪、三嗪、四嗪、喹啉、喹喔啉、喹唑啉、呋喃、噻吩、己基噻吩、溴噻吩、二溴噻吩、吡咯、噁唑、噻唑、异噻唑、噁二唑、噻二唑、吡唑、咪唑、三唑、四唑、吲哚、苯并呋喃、苯并噻吩、苯并噁唑、苯并噻唑、苯并噁二唑、苯并噻二唑、苯并吡唑、苯并咪唑、苯并三唑、三唑吡啶(triazolepyridine)、香豆素。
出于本说明书和所附权利要求的目的,术语"任选取代的苯氧基"是指任选地被一个或多个基团取代的c6h5o苯氧基,该一个或多个基团彼此相同或不同,选自:卤素原子诸如例如氟、氯,优选氟;c1-c20烷基;c1-c20烷氧基;氰基;氨基;硝基。c6h5o苯氧基的具体实例是:苯氧基、4-硝基-苯氧基、2,4-二-硝基苯氧基、2-氯-4-硝基苯氧基、2-氟-4-硝基苯氧基、3-氟-4-硝基苯氧基、5-氟-2-硝基苯氧基、2-氨基苯氧基。
出于本说明书和所附权利要求的目的,术语"环或多环体系"是指饱和或不饱和的含有一个或多个含有3至14个碳原子的环的体系,所述体系任选地含有选自氮、氧、硫、硅、硒、磷的杂原子。环或多环体系的具体实例是:噻吩并[3,2-b]噻吩、噻二唑、苯并噻吩、喹喔啉、吡啶。
出于本说明书和所附权利要求的目的,术语"含有一个或多个芳族或杂芳族环的二价环或多环基团"是指含有一个任选取代的芳族环或任选取代的杂芳族环的基团,或者含有多个任选取代的芳族环或多个任选取代的杂芳族环的基团,所述芳族或杂芳族环通过单键或通过配体基团稠合或连接在一起。含有一个或多个芳族或杂芳族环的环或多环基团的具体实例是:噻吩、吡咯、呋喃、磷杂环戊二烯(phosphol)、苯并二噻吩、螺芴、螺噻吩、联噻吩、叔噻吩、噻吩并噻吩、二噻吩并噻吩、苯并噻吩、异苯并噻吩、苯并二噻吩、环戊二烯并二噻吩、硅杂环戊二烯、硅杂环戊二烯联噻吩、吲哚、苯、萘、蒽、苝、茚、芴、芘、甘菊环、吡啶、噁唑、噻唑、噻嗪、嘧啶、吡嗪、咪唑、苯并噁唑、苯并噁二唑、苯并噻唑、苯并咪唑、苯并呋喃、异苯并呋喃、噻二唑、二噻吩并吡咯、二硫代磷杂环戊二烯(dithiophosphol)、二噻吩并噻吩、噻吩并[3,2-b]噻吩、咔唑-9,9-rr′-9h-芴、9-r-9h-咔唑、3,3′-rr′-亚甲硅烷基-2,2′-联噻吩、3,3′-rr′-环戊二烯并[2,1-b:3,4-b′]-二噻吩,其中r和r′彼此相同或不同,表示直链或支链的c1-c30烷基或c6-c30芳基。
根据本发明的一个优选实施方案,在所述通式(i)中:
-r1、r2、r3、r4、r5、r6和r7彼此相同,表示氢原子;n和p为0;或
-r2、r3、r4、r5和r7彼此相同,表示氢原子;r1和r6彼此相同,选自任选取代的芳基,优选它们是2,5-二甲基苯基;n和p为0;或
-r2、r3、r4、r5和r7彼此相同,表示氢原子;r1和r6彼此相同,选自任选取代的芳基,优选它们是2,6-二甲基苯基;n和p为0;或
-r2、r3、r4、r5和r7彼此相同,表示氢原子;r1和r6彼此相同,选自任选取代的芳基,优选它们是2-苯氧基苯基;n和p为0;或
-r2、r3、r4、r5、r6和r7彼此相同,表示氢原子;r1选自任选取代的芳基,优选它是2-苯氧基苯基;n和p为0;或
-r2、r3、r4、r5和r7彼此相同,表示氢原子;r1和r6选自任选取代的芳基,优选它们是2,4,6-三苯氧基苯基;n和p为0。
可用于本发明目的的具有通式(i)的二噻吩基吡啶噻二唑化合物的具体实例在表1中报告。
表1
具有通式(i)或(ii)的二噻吩基吡啶噻二唑化合物可以根据本领域已知的方法获得。例如,所述具有通式(i)或(ii)的二噻吩基吡啶噻二唑化合物可以如例如由leclercm.等人在“journaloftheamericanchemicalsociety”(2008)第130(2)卷第732-742页中;或由jena.k.-y.在“journalofmaterialschemistry”(2011)第21卷第13247-13255页中;或由welchg.c.等人在“journaloftheamericanchemicalsociety”(2011)第133(12)卷第4632-4644页中;或在以申请人名义并通过引用结合于本文的意大利专利申请mi2018000000667中所描述进行操作而获得。与用于制备所述具有通式(i)或(ii)的二噻吩基吡啶噻二唑化合物的方法相关的进一步细节可以在以下实施例中找到。
本发明的另一个目的是至少一种具有通式(i)或(ii)的二噻吩基吡啶噻二唑化合物在构建发光太阳能集中器(lsc)中的用途。
具有通式(i)或(ii)的二噻吩基吡啶噻二唑化合物可以以以下形式用于所述发光太阳能集中器(lsc):分散在聚合物中或在玻璃中,化学地连接至聚合物或玻璃,以溶液,以凝胶的形式。
例如,发光太阳能集中器(lsc)可以含有透明基体,其中术语透明基体是指以载体、粘结剂或其中分散或掺入了至少一种具有通式(i)或(ii)的二噻吩基吡啶噻二唑化合物的材料的形式使用的任何透明材料。因此用于基体的材料对于感兴趣的辐射是透明的,并且特别是对于具有包含在其中使用它的光伏装置(或太阳能装置)诸如例如光伏电池(或太阳能电池)的有效光谱中的频率的辐射是透明的。因此,适用于本发明目的的材料可以选自至少在波长范围为250nm至1100nm的辐射下的透明材料。
可以用于本发明目的的透明基体可以选自例如聚合物材料或玻璃质材料。所述基体的特征在于关于热和光的高透明度和高持续时间。可以有利地用于本发明目的的聚合物材料是例如聚甲基丙烯酸甲酯(pmma)、环氧树脂、有机硅树脂、聚对苯二甲酸亚烷基酯、聚碳酸酯、聚苯乙烯、聚丙烯。可以有利地用于本发明目的的玻璃质材料是例如二氧化硅类。
在其中基体为聚合物类型的情况下,可以通过例如熔融分散和随后形成包含所述聚合物和所述至少一种具有通式(i)或(ii)的二噻吩基吡啶噻二唑化合物的片(例如根据所谓的“浇铸”技术进行操作),将所述至少一种具有通式(i)或(ii)的二噻吩基吡啶噻二唑化合物分散在所述基体的聚合物中。可选地,所述至少一种具有通式(i)或(ii)的二噻吩基吡啶噻二唑化合物和所述基体的聚合物可以溶解在至少一种溶剂中,获得一种溶液,该溶液沉积在所述聚合物的片上,形成包含所述至少一种具有通式(i)或(ii)的二噻吩基吡啶噻二唑化合物和所述聚合物的膜(例如通过使用“刮刀”涂膜器进行操作:随后,使所述溶剂蒸发)。
在其中基体为玻璃质类型的情况下,所述至少一种具有通式(i)或(ii)的二噻吩基吡啶噻二唑化合物可以溶解在至少一种溶剂中,获得一种溶液,该溶液沉积在所述玻璃质类型的基体的片上,形成包含所述至少一种具有通式(i)或(ii)的二噻吩基吡啶噻二唑化合物的膜(例如通过使用“刮刀”涂膜器进行操作:随后使所述溶剂蒸发)。
本发明的另一个目的是一种光伏装置(或太阳能装置),其包括至少一个光伏电池(或太阳能电池)和至少一个包含至少一种具有通式(i)或(ii)的二噻吩基吡啶噻二唑化合物的发光太阳能集中器(lsc)。
所述光伏装置(或太阳能装置)例如可以通过将上述发光太阳能集中器与至少一个光伏电池(或太阳能电池)进行组装而获得。
根据本发明的一个优选实施方案,上述太阳能集中器可以以透明片的形式制得,该透明片通过以下方式获得:将所述至少一种具有通式(i)或(ii)的二噻吩基吡啶噻二唑化合物和聚合物类型的基体的聚合物溶解在至少一种溶剂中,获得一种溶液,将该溶液沉积在所述聚合物的片上,从而形成包含所述至少一种具有通式(i)或(ii)的二噻吩基吡啶噻二唑化合物和所述聚合物的膜(例如,通过使用“刮刀”涂膜器进行操作:随后,使所述溶剂蒸发)。在所述光伏装置(或太阳能装置)中,所述片然后可以联接至光伏电池(或太阳能电池)。
具体实施方式
为了更好地理解本发明并将其付诸实践,以下报告了本发明的一些说明性且非限制性的实施例。
实施例1
4,7-二噻吩基[1,2,5]噻二唑[3,4-c]吡啶(dtp)的合成
在50ml微波管中,在氮气流下,装入二溴吡啶噻二唑(aldrich)(0.37g;1.25毫摩尔)、二甲基甲酰胺(dmf)(aldrich)(14ml)、2-三丁基锡烷基噻吩(aldrich)(0.97g;825μl;2.6毫摩尔)和四(三苯基膦)钯(0)(aldrich)(0.008g;6.9×10-3毫摩尔):在室温(25℃)下,在氮气流下,将管在搅拌下保持30秒。然后将管密封并在搅拌下在微波中加热,设定温度斜坡(temperatureramp)如下:在2分钟内从室温(25℃)到120℃;在120℃下保持2分钟;在2分钟内从120℃到140℃,在140℃下保持2分钟;在2分钟内从140℃到170℃;在170℃下保持36分钟。随后,将整体倒入蒸馏水(40ml)中并用二氯甲烷(aldrich)(3×20ml)萃取:获得的有机相用蒸馏水(3×25ml)洗涤至中性并且随后在硫酸钠(aldrich)上干燥。在通过减压下蒸馏除去了大部分残留溶剂之后,将获得的残留物逐滴加入到50ml的甲醇(aldrich)中,获得沉淀物,该沉淀物通过过滤回收并且随后通过在硅胶色谱柱上洗脱[洗脱剂:以9/1(v/v)比率的正庚烷(aldrich)/二氯甲烷(aldrich)的混合物]进行纯化,获得0.21g的4,7-二噻吩基[1,2,5]噻二唑[3,4-c]吡啶(dtp)(收率=92%)。
实施例2
4,7-二(5-(1-(2,5-二甲基)苯基)噻吩-2-基)-[1,2,5]噻二唑[3,4-c]吡啶(ppdtp)的合成
(1)2-(2,5-二甲基苯基)噻吩(a)的合成
在惰性气氛中,在装配有磁力搅拌、温度计和冷却剂的100ml烧瓶中,将溶解在蒸馏水(10ml)中的2,5-二甲基苯基硼酸(aldrich)(1.1g;7.3毫摩尔)和碳酸钾(aldrich)(3.4g;24.6毫摩尔)加入到2-溴噻吩(aldrich)(1g;6.13毫摩尔)在二噁烷(aldrich)(30ml)中的溶液中。在通过3个真空/氮气循环除去存在的空气之后,加入四(三苯基膦)钯(0)(aldrich)(0.14g;0.12毫摩尔),获得反应混合物,将该反应混合物浸入到预加热至85℃的浴中并在搅拌下在所述温度保持16小时。随后,在加入饱和氯化钠水溶液(aldrich)(50ml)之后,将获得的反应混合物用乙醚(aldrich)(3×20ml)萃取:获得的有机相用蒸馏水(3×25ml)洗涤至中性并且随后在硫酸钠(aldrich)上干燥。在通过在减压下蒸馏除去溶剂之后,将获得的残留物通过在硅胶色谱柱上洗脱[洗脱剂:正庚烷(aldrich)]进行纯化,获得1g的2-(2,5-二甲基苯基)噻吩(a)(收率=87%)。
(2)4,7-二(5-(1-(2,5-二甲基)苯基)噻吩-2-基)-[1,2,5]-噻二唑[3,4-c]吡啶(ppdtp)的合成
在惰性气氛中,在装配有磁力搅拌、温度计和冷却剂的100ml烧瓶中,在-78℃下将正丁基锂(aldrich)[在己烷(aldrich)中的1.6m溶液](2.5ml;4毫摩尔)逐滴加入到如上所述获得的2-(2,5-二甲基苯基)噻吩(a)(0.67g,3.6毫摩尔)在无水四氢呋喃(thf)(aldrich)(15ml)中的溶液中:将获得的反应混合物在搅拌下保持并且使温度在3小时内达到-55℃。随后,在将烧瓶放置在-78℃下的含有丙酮(aldrich)和干冰的浴中之后,逐滴加入氯化三丁基锡(aldrich)(1.4g;1.17ml;4.32毫摩尔)。在15分钟之后,将烧瓶从浴中移出,使温度升高至20℃并且将反应混合物在搅拌下在所述温度保持12小时。随后,在加入饱和碳酸氢钠溶液(aldrich)(20ml)之后,将反应混合物用乙醚(aldrich)(2×20ml)萃取:获得的有机相用饱和碳酸氢钠溶液(aldrich)(25ml)洗涤并且随后在硫酸钠(aldrich)上干燥。在通过在减压下蒸馏除去残留溶剂之后,将所获得的包含2-(2,5-二甲基苯基)-5-三丁基锡烷基噻吩(b)的残留物如下使用:
在50ml微波管中,在氮气流下,装入二溴吡啶噻二唑(aldrich)(0.42g;1.4毫摩尔)、二甲基甲酰胺(dmf)(aldrich)(15ml)、如上所述获得的包含2-(2,5-二甲基苯基)-5-三丁基锡烷基噻吩(b)的残留物和四(三苯基膦)钯(0)(aldrich)(0.011g;9.5×10-3毫摩尔):在室温(25℃)下,在氮气流下,将管在搅拌下保持30秒。然后将管密封并在搅拌下在微波中加热,设定温度斜坡如下:在2分钟内从室温(25℃)到120℃;在120℃下保持2分钟;在2分钟内从120℃到140℃,在140℃下保持2分钟;在2分钟内从140℃到170℃;在170℃下保持36分钟。随后,将整体倒入蒸馏水(40ml)中并用二氯甲烷(aldrich)(3×20ml)萃取:获得的有机相用蒸馏水(3×25ml)洗涤至中性并且随后在硫酸钠(aldrich)上干燥。在通过减压下蒸馏除去了大部分残留溶剂之后,将获得的残留物逐滴加入到50ml的甲醇(aldrich),获得沉淀物,该沉淀物通过过滤回收并且随后通过在硅胶色谱柱上洗脱[洗脱剂:以9/1(v/v)比率的正庚烷(aldrich)/二氯甲烷(aldrich)的混合物]进行纯化,获得0.6g的4,7-二(5-(1-(2,5-二甲基)苯基)噻吩-2-基)-[1,2,5]噻二唑[3,4-c]吡啶(ppdtp)(收率=84%)。
实施例3
4,7-二(5-(1-(2,6-二甲基)苯基)噻吩-2-基)-[1,2,5]噻二唑-[3,4-c]吡啶(mpdtp)的合成
(1)2-(2,6-二甲基苯基)噻吩(c)的合成
在惰性气氛中,在装配有磁力搅拌、温度计和冷却剂的100ml烧瓶中,将溶解在蒸馏水(10ml)中的2,6-二甲基苯基硼酸(aldrich)(1.1g;7.3毫摩尔)和碳酸钾(aldrich)(3.4g;24.6毫摩尔)加入到2-溴噻吩(aldrich)(1g;6.13毫摩尔)在二噁烷(aldrich)(30ml)中的溶液中。在通过3个真空/氮气循环除去存在的空气之后,加入四(三苯基膦)钯(0)(aldrich)(0.14g;0.12毫摩尔),获得反应混合物,将该反应混合物浸入到预加热至85℃的浴中并在搅拌下在所述温度保持16小时。随后,在加入饱和氯化钠水溶液(aldrich)(50ml)之后,将获得的反应混合物用乙醚(aldrich)(3×50ml)萃取:获得的有机相用蒸馏水(3×25ml)洗涤至中性并且随后在硫酸钠(aldrich)上干燥。在通过在减压下蒸馏除去溶剂之后,将获得的残留物通过在硅胶色谱柱上洗脱[洗脱剂:正庚烷(aldrich)]进行纯化,获得0.95g的2-(2,6-二甲基苯基)噻吩(c)(收率=83%)。
(2)4,7-二(5-(1-(2,6-二甲基)苯基)噻吩-2-基)-[1,2,5]噻二唑[3,4-c]吡啶(mpdtp)的合成
在惰性气氛中,在装配有磁力搅拌、温度计和冷却剂的100ml烧瓶中,在-78℃下将正丁基锂(aldrich)[在己烷(aldrich)中的1.6m溶液](2.5ml;4毫摩尔)逐滴加入到如上所述获得的2-(2,6-二甲基苯基)噻吩(c)(0.67g,3.6毫摩尔)在无水四氢呋喃(thf)(aldrich)(15ml)中的溶液中:将获得的反应混合物在搅拌下保持并且使温度在3小时内达到-55℃。随后,在将烧瓶放置在-78℃下的含有丙酮(aldrich)和干冰的浴中之后,逐滴加入氯化三丁基锡(aldrich)(1.4g;1.17ml;4.32毫摩尔)。在15分钟之后,将烧瓶从浴中移出,使温度升高至20℃并且将反应混合物在搅拌下在所述温度保持12小时。随后,在加入饱和碳酸氢钠溶液(aldrich)(20ml)之后,将反应混合物用乙醚(aldrich)(2×20ml)萃取:获得的有机相用饱和碳酸氢钠溶液(aldrich)(25ml)洗涤并且随后在硫酸钠(aldrich)上干燥。在通过在减压下蒸馏除去残留溶剂之后,所获得的包含2-(2,6-二甲基苯基)-5-三丁基锡烷基噻吩(d)的残留物如下使用:
在50ml微波管中,在氮气流下,装入二溴吡啶噻二唑(aldrich)(0.42g;1.4毫摩尔)、二甲基甲酰胺(dmf)(aldrich)(15ml)、如上所述获得的包含2-(2,6-二甲基苯基)-5-三丁基锡烷基噻吩(d)的残留物和四(三苯基膦)钯(0)(aldrich)(0.011g;9.5×10-3毫摩尔):在室温(25℃)下,在氮气流下,将管在搅拌下保持30秒。然后将管密封并在搅拌下在微波中加热,设定温度斜坡如下:在2分钟内从室温(25℃)到120℃;在120℃下保持2分钟;在2分钟内从120℃到140℃,在140℃下保持2分钟;在2分钟内从140℃到170℃;在170℃下保持36分钟。随后,将整体倒入蒸馏水(40ml)中并用二氯甲烷(aldrich)(3×20ml)萃取:获得的有机相用中性水(3×25ml)洗涤并且随后在硫酸钠(aldrich)上干燥。在通过减压下蒸馏除去了大部分残留溶剂之后,将获得的残留物逐滴加入到50ml的甲醇(aldrich),获得沉淀物,该沉淀物通过过滤回收并且随后通过在硅胶色谱柱上洗脱[洗脱剂:以9/1(v/v)比率的正庚烷(aldrich)/二氯甲烷(aldrich)的混合物]进行纯化,获得0.6g的4,7-二(5-(1-(2,6-二甲基)苯基)噻吩-2-基)-[1,2,5]噻二唑[3,4-c]吡啶(mpdtp)(收率=95%)。
实施例4
4,7-二(5-(1-(2-苯氧基)苯基)噻吩-2-基)-[1,2,5]噻二唑[3,4-c]吡啶(popdtp)的合成
(1)2-(2-苯氧基苯基)噻吩(e)的合成
在惰性气氛中,在装配有磁力搅拌、温度计和冷却剂的100ml烧瓶中,将溶解在蒸馏水(10ml)中的2-苯氧基苯基硼酸(aldrich)(1.6g;7.3毫摩尔)和碳酸钾(aldrich)(3.4g;24.6毫摩尔)加入到2-溴噻吩(aldrich)(1g;6.13毫摩尔)在二噁烷(aldrich)(30ml)中的溶液中。在通过3个真空/氮气循环除去存在的空气之后,加入四(三苯基膦)钯(0)(aldrich)(0.14g;0.12毫摩尔),获得反应混合物,将该反应混合物浸入到预加热至85℃的浴中并在搅拌下在所述温度保持16小时。随后,在加入饱和氯化钠水溶液(aldrich)(50ml)之后,将获得的反应混合物用乙醚(aldrich)(3×25ml)萃取:获得的有机相用蒸馏水(3×25ml)洗涤至中性并且随后在硫酸钠(aldrich)上干燥。在通过在减压下蒸馏除去溶剂之后,将获得的残留物通过在硅胶色谱柱上洗脱[洗脱剂:正庚烷(aldrich)]进行纯化,获得1.4g的2-(2-苯氧基苯基)噻吩(e)(收率=91%)。
(2)4,7-二(5-(1-(2-苯氧基)苯基)噻吩-2-基)-[1,2,5]噻二唑[3,4-c]吡啶(popdtp)的合成
在惰性气氛中,在装配有磁力搅拌、温度计和冷却剂的100ml烧瓶中,在-78℃下将正丁基锂(aldrich)[在己烷(aldrich)中的1.6m溶液](1.3ml;2.1毫摩尔)逐滴加入到如上所述获得的2-(2-苯氧基苯基)噻吩(e)(0.48g,1.9毫摩尔)在无水四氢呋喃(thf)(aldrich)(15ml)中的溶液中:将获得的反应混合物在搅拌下保持并且使温度在3小时内达到-55℃。随后,在将烧瓶放置在-78℃下的含有丙酮(aldrich)和干冰的浴中之后,逐滴加入氯化三丁基锡(aldrich)(0.74g;0.62ml;2.3毫摩尔)。在15分钟之后,将烧瓶从浴中移出,使温度升高至20℃并且将反应混合物在搅拌下在所述温度保持12小时。随后,在加入饱和碳酸氢钠溶液(aldrich)(20ml)之后,将反应混合物用乙醚(aldrich)(2×20ml)萃取:获得的有机相用饱和碳酸氢钠溶液(aldrich)(25ml)洗涤并且随后在硫酸钠(aldrich)上干燥。在通过在减压下蒸馏除去残留溶剂之后,所获得的包含2-(2-苯氧基苯基)-5-三丁基锡烷基噻吩(f)的残留物如下使用:
在50ml微波管中,在氮气流下,装入二溴吡啶噻二唑(aldrich)(0.225g;0.76毫摩尔)、二甲基甲酰胺(dmf)(aldrich)(10ml)、如上所述获得的包含2-(2-苯氧基苯基)-5-三丁基锡烷基噻吩(f)的残留物和四(三苯基膦)钯(0)(aldrich)(0.0061g;5.3×10-3毫摩尔):在室温(25℃)下,在氮气流下,将管在搅拌下保持30秒。然后将管密封并在搅拌下在微波中加热,设定温度斜坡如下:在2分钟内从室温(25℃)到120℃;在120℃下保持2分钟;在2分钟内从120℃到140℃,在140℃下保持2分钟;在2分钟内从140℃到170℃;在170℃下保持36分钟。随后,将整体倒入蒸馏水(40ml)中并用二氯甲烷(aldrich)(3×20ml)萃取:获得的有机相用蒸馏水(3×25ml)洗涤至中性并且随后在硫酸钠(aldrich)上干燥。在通过减压下蒸馏除去了大部分残留溶剂之后,将获得的残留物逐滴加入到50ml的甲醇(aldrich),获得沉淀物,该沉淀物通过过滤回收并且随后通过在硅胶色谱柱上洗脱[洗脱剂:以9/1(v/v)比率的正庚烷(aldrich)/二氯甲烷(aldrich)的混合物]进行纯化,获得0.2g的4,7-二(5-(1-(2-苯氧基)苯基)噻吩-2-基)-[1,2,5]噻二唑[3,4-c]吡啶(popdtp)(收率=46%)。
实施例5
4(5-(1-(2-苯氧基)苯基)噻吩-2-基)-7-(噻吩-2-基)[1,2,5]噻二唑[3,4-c]吡啶(monopopdtp)的合成
(1)4(5-(1-(2-溴)苯基)噻吩-2-基)-7-(噻吩-2-基)[1,2,5]噻二唑[3,4-c]吡啶(g)的合成
在惰性气氛中,在装配有磁力搅拌、温度计和冷却剂的100ml烧瓶中,将n-溴代琥珀酰亚胺(aldrich)(0.694g;3.92毫摩尔)加入到如实施例1中所述获得的4,7-二噻吩基[1,2,5]噻二唑[3,4-c]吡啶(dtp)(0.53g;1.76毫摩尔)在氯仿(aldrich)(13.2ml)中的溶液中:将所获得的混合物在搅拌下在黑暗中在室温(25℃)下留置12小时。随后,在加入50ml的蒸馏水之后,获得沉淀物,将该沉淀物通过过滤回收,用甲醇(aldrich)(200ml)洗涤并且从混合物正庚烷(aldrich)/二氯甲烷(aldrich)[比率9/1(v/v)]中重结晶,获得0.549g的4(5-(1-(2-溴)苯基)噻吩-2-基)-7-(噻吩-2-基)[1,2,5]噻二唑[3,4-c]吡啶(g)(收率=89%)。
(2)4(5-(1-(2-苯氧基)苯基)噻吩-2-基)-7-(噻吩-2-基)[1,2,5]噻二唑[3,4-c]吡啶(monopopdtp)的合成
在惰性气氛中,在装配有磁力搅拌、温度计和冷却剂的100ml烧瓶中,将溶解在蒸馏水(5ml)中的2-苯氧基苯基硼酸(aldrich)(0.749g;3.5毫摩尔)和碳酸钾(aldrich)(1.4g;10.3毫摩尔)加入到如上所述获得的4(5-(1-(2-溴)苯基)噻吩-2-基)-7-(噻吩-2-基)[1,2,5]噻二唑[3,4-c]吡啶(g)(0.549g;1.56毫摩尔)在二噁烷(aldrich)(30ml)中的溶液中。在通过3个真空/氮气循环除去存在的空气之后,加入四(三苯基膦)钯(0)(aldrich)(0.072g;0.07毫摩尔),获得反应混合物,将该反应混合物浸入到预加热至85℃的浴中并在搅拌下在所述温度保持16小时。随后,在加入饱和氯化钠水溶液(aldrich)(30ml)之后,将获得的反应混合物用乙醚(aldrich)(3×20ml)萃取:获得的有机相用蒸馏水(3×25ml)洗涤至中性并且随后在硫酸钠(aldrich)上干燥。在通过在减压下蒸馏除去溶剂之后,将获得的残留物通过在硅胶色谱柱上洗脱[洗脱剂:正庚烷(aldrich)]进行纯化,获得0.5g的4(5-(1-(2-苯氧基)苯基)噻吩-2-基)-7-(噻吩-2-基)[1,2,5]噻二唑[3,4-c]吡啶(monopopdtp)(收率=83%)。
实施例6
4,7-二(5-(1-(2,4,6-三苯氧基)苯基)噻吩-2-基)-7-(噻吩-2-基)[1,2,5]噻二唑[3,4-c]吡啶(tripopdtp)的合成
(1)2,4,6-三苯氧基-1-溴苯(h)的合成
在50ml微波管中,在氮气流下,装入2,4,6-三氟-1-溴苯(aldrich)(1.6g;0.9毫摩尔)、苯酚(aldrich)(3.2ml)、碳酸钾(aldrich)(5g;36.3毫摩尔)和n-甲基吡咯烷酮(aldrich)(26ml):将该管在氮气流下在搅拌下在室温(25℃)保持60秒。然后将管密封并在搅拌下在微波中加热,设定温度斜坡如下:在4分钟内从室温(25℃)到220℃;在220℃下保持3小时。随后,将整体倒入蒸馏水(50ml)中并用乙醚(aldrich)(3×25ml)萃取:获得的有机相用蒸馏水(3×25ml)洗涤至中性并且随后在硫酸钠(aldrich)上干燥。在通过减压下蒸馏除去了大部分残留溶剂之后,将获得的残留物逐滴加入到50ml的甲醇(aldrich),获得沉淀物,该沉淀物通过过滤回收并且随后通过在硅胶色谱柱上洗脱[洗脱剂:正庚烷(aldrich)]进行纯化,获得2.3g的2,4,6-三苯氧基-1-溴苯(h)(收率=70%)。
(2)2,4,6-三苯氧基-1-(2-噻吩基)苯(i)的合成
在惰性气氛中,在装配有磁力搅拌、温度计和冷却剂的100ml烧瓶中,将2-三丁基锡烷基噻吩(aldrich)(1.5g;1.3ml;4.2毫摩尔)加入到如上所述获得的2,4,6-三苯氧基-1-溴-苯(h)(1.5g;3.5毫摩尔)在无水甲苯(aldrich)(13.2ml)中的0.1m溶液中。在通过3个真空/氮气循环除去存在的空气之后,加入三-二亚苄基丙酮二钯(aldrich)(0.048g;0.05毫摩尔)和三-邻甲苯基膦(aldrich),获得反应混合物,将该反应混合物浸入到在110℃下预加热的浴中并且在搅拌下在所述温度保持12小时。随后,将反应混合物倒入蒸馏水(50ml)中并用二氯甲烷(aldrich)(3×25ml)萃取:获得的有机相用蒸馏水(3×25ml)洗涤至中性并且随后在硫酸钠(aldrich)上干燥。在通过减压下蒸馏除去了大部分残留溶剂之后,将获得的残留物逐滴加入到50ml的甲醇(aldrich),获得沉淀物,该沉淀物通过过滤回收并且随后通过在硅胶色谱柱上洗脱[洗脱剂:正庚烷(aldrich)]进行纯化,获得1.1g的2,4,6-三苯氧基-1-(2-噻吩基)苯(i)(收率=72%)。
(3)4,7-二(5-(1-(2,4,6-三苯氧基)苯基)噻吩-2-基)-7-(噻吩-2-基)[1,2,5]噻二唑[3,4-c]吡啶(tripopdtp)的合成
在惰性气氛中,在装配有磁力搅拌、温度计和冷却剂的100ml烧瓶中,在-78℃下将正丁基锂(aldrich)[在己烷(aldrich)中的1.6m溶液](0.8ml;1.3毫摩尔)逐滴加入到如上所述获得的2,4,6-三苯氧基-1-(2-噻吩基)苯(i)(0.5g;1.15毫摩尔)在无水四氢呋喃(thf)(aldrich)(11ml)中的0.1m溶液中:将所获得的反应混合物在搅拌下保持并且使温度在3小时内达到-55℃。随后,在将烧瓶放置在-78℃下的含有丙酮(aldrich)和干冰的浴中之后,逐滴加入氯化三丁基锡(aldrich)(0.5g;0.4ml;1.4毫摩尔)。在15分钟之后,将烧瓶从浴中移出,使温度升高至20℃并且将反应混合物在搅拌下在所述温度保持12小时。随后,在加入饱和碳酸氢钠溶液(aldrich)(30ml)之后,将反应混合物用乙醚(aldrich)(2×25ml)萃取:获得的有机相用饱和碳酸氢钠溶液(aldrich)(25ml)洗涤并且随后在硫酸钠(aldrich)上干燥。在通过在减压下蒸馏除去残留溶剂之后,所获得的包含2,4,6-三苯氧基-1-[2'(5'-三丁基锡烷基)噻吩基]苯(l)的残留物如下使用:
在50ml微波管中,在氮气流下,装入二溴吡啶噻二唑(aldrich)(0.15g;0.5毫摩尔)、二甲基甲酰胺(dmf)(aldrich)(10ml)、如上所述获得的包含2,4,6-三苯氧基-1-[2'(5'-三丁基锡烷基)噻吩基]苯(l)的残留物和四(三苯基膦)钯(0)(aldrich)(0.004g;3.4×10-3毫摩尔):在室温(25℃)下,在氮气流下,将管在搅拌下保持30秒。然后将管密封并在搅拌下在微波中加热,设定温度斜坡如下:在2分钟内从室温(25℃)到120℃;在120℃下保持2分钟;在2分钟内从120℃到140℃,在140℃下保持2分钟;在2分钟内从140℃到170℃;在170℃下保持36分钟。随后,将整体倒入蒸馏水(30ml)中并用二氯甲烷(aldrich)(3×20ml)萃取:获得的有机相用蒸馏水(3×25ml)洗涤至中性并且随后在硫酸钠(aldrich)上干燥。在通过减压下蒸馏除去了大部分残留溶剂之后,将获得的残留物逐滴加入到30ml的甲醇(aldrich),获得沉淀物,该沉淀物通过过滤回收并且随后通过在硅胶色谱柱上洗脱[洗脱剂:以9/1(v/v)比率的正庚烷(aldrich)/二氯甲烷(aldrich)的混合物]进行纯化,获得0.35g的4,7-二(5-(1-(2,4,6-三苯氧基)-苯基)噻吩-2-基)-7-(噻吩-2-基)[1,2,5]-噻二唑-[3,4-c]吡啶(tripopdtp)(收率=70%)。
实施例7(比较)
将6g的聚甲基丙烯酸甲酯(pmma)altuglasvsuvt100(arkema)和49.5mg的如在以申请人名义的国际专利申请wo2012/007834的实施例1中所述获得的4,7-二-(噻吩-2'-基)-2,1,3-苯并噻二唑(dtb)溶解在30ml的1,2-二氯苯(aldrich)中。随后使用“刮刀”涂膜器,将所获得的溶液均匀地沉积在聚甲基丙烯酸甲酯(pmma)片(尺寸为300mm×90mm×6mm)上,并在轻轻的空气流中使溶剂在室温(25℃)下蒸发24小时。结果是由发现厚度在100μm至50μm之间的膜向其赋予了橙色的透明片。
然后将表面积为1.2cm2的ixys-kxob22-12光伏电池施加于聚合物片的边缘之一。
因此,聚合物片的主面[涂覆有含有4,7-二-(噻吩-2'-基)-2,1,3-苯并噻二唑(dtb)的薄膜]用功率等于1个太阳光强(sun)(1000w/m2)的光源照射,并且测量由照明产生的电功率。
功率测量(p)通过照射尺寸等于100mm×90mm的片的一部分来进行,其中照射距离(d)从其上固定有光伏电池的边缘开始增加。这些以距光伏电池的可变距离的测量允许对波导、边缘、扩散和自吸收效应的贡献进行定量。
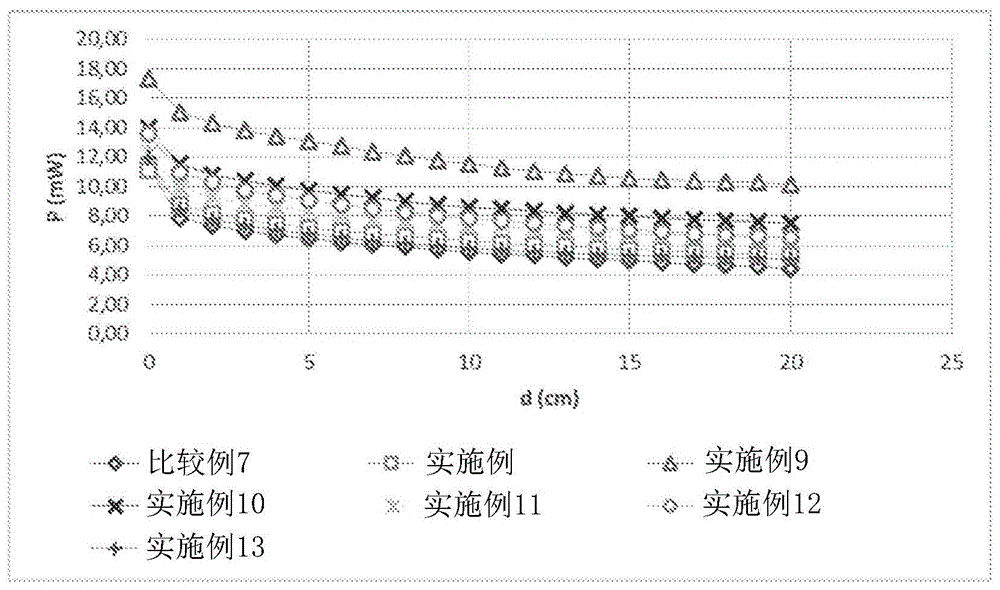
图1示出了根据以cm表示的距其上固定有光伏电池的边缘的距离(d)(在横坐标上报告),与以mw表示的所产生的功率值(p)(在纵坐标上报告)相关的曲线。
可以看出如何,在没有板效应(boardeffect)的情况下,平均产生的功率等于5.69mw(图1)。
图2示出了所获得的以mw表示的所产生的功率值(p)(在纵坐标上报告)(实施例的编号在横坐标上示出)。
实施例8(发明)
将6g的聚甲基丙烯酸甲酯(pmma)altuglasvsuvt100(arkema)和55.3mg的如实施例1中所述获得的4,7-二噻吩基[1,2,5]噻二唑[3,4-c]吡啶(dtp)溶解在30ml的1,2-二氯苯(aldrich)中。随后使用“刮刀”涂膜器,将所获得的溶液均匀地沉积在聚甲基丙烯酸甲酯(pmma)片(尺寸为300mm×90mm×6mm)上,并在轻轻的空气流中使溶剂在室温(25℃)下蒸发24小时。结果是由发现厚度在100μm至50μm之间的膜向其赋予了橙色的透明片。
然后将表面积为1.2cm2的ixys-kxob22-12光伏电池施加于聚合物片的边缘之一。
然后聚合物片的主面[涂覆有含有4,7-二噻吩基[1,2,5]噻二唑[3,4-c]吡啶(dtp)的薄膜]用功率等于1个太阳光强(1000w/m2)的光源照射,并且测量由于照明产生的电功率。
功率测量(p)通过照射尺寸等于100mm×90mm的片的一部分来进行,其中照射距离(d)从其上固定有光伏电池的边缘开始增加。这些以距光伏电池的可变距离的测量允许对波导、边缘、扩散和自吸收效应的贡献进行定量。
图1示出了根据以cm表示的距其上固定有光伏电池的边缘的距离(d)(在横坐标上报告),与以mw表示的所产生的功率值(p)(在纵坐标上报告)相关的曲线。
可以看出如何,在没有电路板效应的情况下,平均产生的功率等于6.47mw(图1)。
图2示出了所获得的以mw表示的所产生的功率值(p)(在纵坐标上报告)(实施例的编号在横坐标上示出)。
实施例9(发明)
将6g的聚甲基丙烯酸甲酯(pmma)altuglasvsuvt100(arkema)和89.6mg的如在实施例3中所述获得的4,7-二(5-(1-(2,6-二甲基)苯基)噻吩-2-基)-[1,2,5]噻二唑[3,4-c]吡啶(mpdtp)溶解在30ml的1,2-二氯苯(aldrich)中。随后使用“刮刀”涂膜器,将所获得的溶液均匀地沉积在聚甲基丙烯酸甲酯(pmma)片(尺寸为300mm×90mm×6mm)上,并在轻轻的空气流中使溶剂在室温(25℃)下蒸发24小时。结果是由发现厚度在100μm至50μm之间的膜向其赋予了橙色的透明片。
然后将表面积为1.2cm2的ixys-kxob22-12光伏电池施加于聚合物片的边缘之一。
聚合物片的主面[涂覆有含有4,7-二(5-(1-(2,6-二甲基)苯基)噻吩-2-基)-[1,2,5]噻二唑[3,4-c]-吡啶(mpdtp)的薄膜]用功率等于1个太阳光强(1000w/m2)的光源照射,并且测量由于照明产生的电功率。
功率测量(p)通过照射尺寸等于100mm×90mm的片的一部分来进行,其中照射距离(d)从其上固定有光伏电池的边缘开始增加。这些以距光伏电池的可变距离的测量允许对波导、边缘、扩散和自吸收效应的贡献进行定量。
图1示出了根据以cm表示的距其上固定有光伏电池的边缘的距离(d)(在横坐标上报告),与以mw表示的所产生的功率值(p)(在纵坐标上报告)相关的曲线。
可以看出如何,在没有板效应的情况下,平均产生的功率等于11.81mw(图1)。
图2示出了所获得的以mw表示的所产生的功率值(p)(在纵坐标上报告)(实施例的编号在横坐标上示出)。
实施例10(发明)
将6g的聚甲基丙烯酸甲酯(pmma)altuglasvsuvt100(arkema)和45mg的如在实施例2中所述获得的4,7-二(5-(1-(2,5-二甲基)苯基)噻吩-2-基)-[1,2,5]噻二唑[3,4-c]吡啶(ppdtp)溶解在30ml的1,2-二氯苯(aldrich)中。随后使用“刮刀”涂膜器,将所获得的溶液均匀地沉积在聚甲基丙烯酸甲酯(pmma)片(尺寸为300mm×90mm×6mm)上,并在轻轻的空气流中使溶剂在室温(25℃)下蒸发24小时。结果是由发现厚度在100μm至50μm之间的膜向其赋予了橙色的透明片。
然后将表面积为1.2cm2的ixys-kxob22-12光伏电池施加于聚合物片的边缘之一。
聚合物片的主面[涂覆有含有4,7-二(5-(1-(2,5-二甲基)苯基)噻吩-2-基)-[1,2,5]噻二唑[3,4-c]-吡啶(ppdtp)的薄膜]用功率等于1个太阳光强(1000w/m2)的光源照射,并且测量由于照明产生的电功率。
功率测量(p)通过照射尺寸等于100mm×90mm的片的一部分来进行,其中照射距离(d)从其上固定有光伏电池的边缘开始增加。这些以距光伏电池的可变距离的测量允许对波导、边缘、扩散和自吸收效应的贡献进行定量。
图1示出了根据以cm表示的距其上固定有光伏电池的边缘的距离(d)(在横坐标上报告),与以mw表示的所产生的功率值(p)(在纵坐标上报告)相关的曲线。
可以看出如何,在没有板效应的情况下,平均产生的功率等于8.85mw(图1)。
图2示出了所获得的以mw表示的所产生的功率值(p)(在纵坐标上报告)(实施例的编号在横坐标上示出)。
实施例11(发明)
将6g的聚甲基丙烯酸甲酯(pmma)altuglasvsuvt100(arkema)和85.4mg的如在实施例4中所述获得的4,7-二(5-(1-(2-苯氧基)苯基)噻吩-2-基)-[1,2,5]-噻二唑[3,4-c]吡啶(popdtp)溶解在30ml的1,2-二氯苯(aldrich)中。随后使用“刮刀”涂膜器,将所获得的溶液均匀地沉积在聚甲基丙烯酸甲酯(pmma)片(尺寸为300mm×90mm×6mm)上,并在轻轻的空气流中使溶剂在室温(25℃)下蒸发24小时。结果是由发现厚度在100μm至50μm之间的膜向其赋予了橙色的透明片。
然后将表面积为1.2cm2的ixys-kxob22-12光伏电池施加于聚合物片的边缘之一。
聚合物片的主面[涂覆有含有4,7-二(5-(1-(2-苯氧基)苯基)噻吩-2-基)-[1,2,5]噻二唑[3,4-c]吡啶(popdtp)的薄膜]用功率等于1个太阳光强(1000w/m2)的光源照射,并且测量由照明产生的电功率。
功率测量(p)通过照射尺寸等于100mm×90mm的片的一部分来进行,其中照射距离(d)从其上固定有光伏电池的边缘开始增加。这些以距光伏电池的可变距离的测量允许对波导、边缘、扩散和自吸收效应的贡献进行定量。
图1示出了根据以cm表示的距其上固定有光伏电池的边缘的距离(d)(在横坐标上报告),与以mw表示的所产生的功率值(p)(在纵坐标上报告)相关的曲线。
可以看出如何,在没有板效应的情况下,平均产生的功率等于7.57mw(图1)。
图2示出了所获得的以mw表示的所产生的功率值(p)(在纵坐标上报告)(实施例的编号在横坐标上示出)。
实施例12(发明)
将6g的聚甲基丙烯酸甲酯(pmma)altuglasvsuvt100(arkema)和60.1mg的如在实施例4中所述获得的4,7-二(5-(1-(2-苯氧基)苯基)噻吩-2-基)[1,2,5]-噻二唑[3,4-c]吡啶(popdtp)溶解在30ml的1,2-二氯苯(aldrich)中。随后使用“刮刀”涂膜器,将所获得的溶液均匀地沉积在聚甲基丙烯酸甲酯(pmma)片(尺寸为300mm×90mm×6mm)上,并在轻轻的空气流中使溶剂在室温(25℃)下蒸发24小时。结果是由发现厚度在100μm至50μm之间的膜向其赋予了橙色的透明片。
然后将表面积为1.2cm2的ixys-kxob22-12光伏电池施加于聚合物片的边缘之一。
聚合物片的主面[涂覆有含有4,7-二(5-(1-(2-苯氧基)苯基)噻吩-2-基)[1,2,5]噻二唑[3,4-c]吡啶(popdtp)的薄膜]用功率等于1个太阳光强(1000w/m2)的光源照射,并且测量由照明产生的电功率。
功率测量(p)通过照射尺寸等于100mm×90mm的片的一部分来进行,其中照射距离(d)从其上固定有光伏电池的边缘开始增加。这些以距光伏电池的可变距离的测量允许对波导、边缘、扩散和自吸收效应的贡献进行定量。
图1示出了根据以cm表示的距其上固定有光伏电池的边缘的距离(d)(在横坐标上报告),与以mw表示的所产生的功率值(p)(在纵坐标上报告)相关的曲线。
可以看出如何,在没有板效应的情况下,平均产生的功率等于8.06mw(图1)。
图2示出了所获得的以mw表示的所产生的功率值(p)(在纵坐标上报告)(实施例的编号在横坐标上显示)。
实施例13(发明)
将6g的聚甲基丙烯酸甲酯(pmma)altuglasvsuvt100(arkema)和168.3mg的如在实施例6中所述获得的4,7-二(5-(1-(2,4,6-三苯氧基)苯基)噻吩-2-基)-7-(噻吩-2-基)[1,2,5]噻二唑[3,4-c]吡啶(tripopdtp)溶解在30ml的1,2-二氯苯(aldrich)中。随后使用“刮刀”涂膜器,将所获得的溶液均匀地沉积在聚甲基丙烯酸甲酯(pmma)片(尺寸为300mm×90mm×6mm)上,并在轻轻的空气流中使溶剂在室温(25℃)下蒸发24小时。结果是由厚度在100μm至50μm之间的膜向其赋予了橙色的透明片。
然后将表面积为1.2cm2的ixys-kxob22-12光伏电池施加于聚合物片的边缘之一。
聚合物片的主面[涂覆有含有4,7-二(5-(1-(2,4,6-三苯氧基)苯基)噻吩-2-基)-7-(噻吩-2-基)[1,2,5]-噻二唑[3,4-c]吡啶(tripopdtp)的薄膜]用功率等于1个太阳光强(1000w/m2)的光源照射,并且测量由照明产生的电功率。
功率测量(p)通过照射尺寸等于100mm×90mm的片的一部分来进行,其中照射距离(d)从其上固定有光伏电池的边缘开始增加。这些以距光伏电池的可变距离的测量允许对波导、边缘、扩散和自吸收效应的贡献进行定量。
图1示出了根据以cm表示的距其上固定有光伏电池的边缘的距离(d)(在横坐标上报告),与以mw表示的所产生的功率值(p)(在纵坐标上报告)相关的曲线。
可以看出如何,在没有板效应的情况下,平均产生的功率等于6.08mw(图1)。
图2示出了所获得的以mw表示的所产生的功率值(p)(在纵坐标上报告)(实施例的编号在横坐标上示出)。
本文用于企业家、创业者技术爱好者查询,结果仅供参考。