1.本发明属于生物医学技术领域,具体涉及鼻咽癌标志物及其应用。
背景技术:
2.随着社会的发展,人们生活环境及饮食习惯等的变迁,恶性肿瘤已经成为人类健康的头号杀手之一,近年来在全球范围内患病人数不断增加,为全球经济和人类社会的发展带来了沉重的负担。
3.肿瘤精准治疗是目前肿瘤诊断、治疗的发展趋势。目前分子标志物在多种肿瘤中用于诊断和作为治疗靶点,让肿瘤患者受益。例如针对cml的融合基因bcr
‑
abl设计的分子靶向药物imatinib/gleevec已经在临床得到应用,同样地临床前及临床1期、2期数据表明alk激酶抑制剂对治疗eml4
‑
alk阳性病人有效。但是,目前缺乏诊断和预测鼻咽癌预后的分子标志物,而且鼻咽癌尚未发现较好的治疗靶点。
技术实现要素:
4.本发明的目的在于提供一种用于鼻咽癌诊断及预后预测的分子标志物,也可以用于鼻咽癌靶向治疗的分子靶点。
5.本发明所采取的技术方案是:
6.本发明的第一方面,提供检测上皮细胞标志物和免疫细胞标志物的试剂在制备鼻咽癌诊断和/或预后评估产品中的应用。
7.在本发明的一些实施方式中,所述上皮细胞标志物为epcam和/或pan
‑
ck。
8.在本发明的一些实施方式中,所述免疫细胞标志物为ifitm3、tnfsf10、cxcl10、bst2、isg15、hla
‑
drb1和hla
‑
dr中的至少一种。
9.在本发明的一些实施方式中,所述试剂为检测标志物基因表达水平的试剂。
10.在本发明的一些优选实施方式中,所述检测标志物基因表达水平包括通过测序技术、核酸杂交技术、核酸扩增技术或免疫测定的方法检测标志物基因表达水平的试剂。
11.在本发明的一些实施方式中,所述试剂为检测标志物基因编码的蛋白质表达水平的试剂,所述检测标志物基因编码的蛋白质表达水平的试剂包括免疫组化、western
‑
blot、蛋白免疫印迹、酶联免疫吸附(elisa)、流式细胞术、紫外分光光度法
‑
近红外光谱法、高效液相色谱法、比色法和质谱鉴定中的至少一种方法检测蛋白表达水平的试剂。
12.本发明人通过单细胞转录组测序,通过生物信息学分析,鉴定发现一种“上皮
‑
免疫”双阳性细胞,通过详细的实验研究发现,上皮
‑
免疫细胞的检测,可用于鼻咽癌预后诊断以及预后。
13.本发明的第二个方面,提供一种鼻咽癌诊断和/或预后评估试剂盒,包括本发明第一方面所述试剂。
14.本发明还提供上述试剂盒的使用方法,包括以下步骤:
15.(1)获取待测样品;
16.(2)检测待测样品中所述标志物的表达水平,与参考水平进行比较。
17.在本发明的一些实施方式中,当待测样品中所述标志物的表达水平高于参考水平表明患有鼻咽癌的几率高。
18.在本发明的一些实施方式中,所述待测样品可以为肿瘤组织样品。
19.在本发明的一些实施方式中,所述参考水平为非鼻咽癌患者中所述标志物的表达水平。
20.本发明的试剂盒可以用来检测标志物的表达水平,通过检测标志物的表达,有助于判断受试者是否存在患鼻咽癌的高风险,为临床辅助诊断及预后评估鼻咽癌提供了可能。
21.本发明的第三方面,提供上皮细胞标志物和免疫细胞标志物在制备用于预防和/或治疗鼻咽癌的药物中的应用。
22.在本发明的一些实施方式中,所述上皮细胞标志物为epcam和/或pan
‑
ck。
23.在本发明的一些实施方式中,所述免疫细胞标志物为ifitm3、tnfsf10、cxcl10、bst2、isg15、hla
‑
drb1和hla
‑
dr中的至少一种。
24.在本发明的一些实施方式中,所述药物为特异性抑制标志物表达的小分子物质、标志物的特异性抗体、靶向标志物的sirna和反义rna中的至少一种。
25.本发明的第四方面,提供上皮细胞标志物和免疫细胞标志物在筛选用于预防和/或治疗鼻咽癌的药物中的应用。
26.在本发明的一些实施方式中,所述上皮细胞标志物为epcam和/或pan
‑
ck。
27.在本发明的一些实施方式中,所述免疫细胞标志物为ifitm3、tnfsf10、cxcl10、bst2、isg15、hla
‑
drb1和hla
‑
dr中的至少一种。
28.在本发明的一些实施方式中,所述药物为特异性抑制标志物表达的小分子物质、标志物的特异性抗体、靶向标志物的sirna和反义rna中的至少一种。
29.本发明的第五方面,提供一种评估鼻咽癌预后的方法,具体为检测待测样品的本发明第一方面所述标志物的表达量,根据表达量预测鼻咽癌预后风险。
30.在本发明的一些实施方式中,所述根据表达量预测鼻咽癌预后风险具体为与参考水平进行比较。
31.在本发明的一些实施方式中,当待测样品中所述标志物的表达水平高于参考水平表明患有鼻咽癌的几率高。
32.在本发明的一些实施方式中,所述待测样品可以为肿瘤组织样品。
33.在本发明的一些实施方式中,所述参考水平为非鼻咽癌患者中所述标志物的表达水平。
34.在本发明的一些实施方式中,通过检测标志物的表达,有助于判断受试者是否存在患鼻咽癌的高风险以及预后风险。
35.本发明的第六个方面,提供一种筛选药物的方法,通过检测给药前后本发明第一方面所述标志物的表达量。
36.在本发明的一些实施方式中,通过检测给药前后标志物的表达,有助于判断药物是否有效。
37.本发明的有益效果是:
38.本发明通过单细胞转录组测序方法、多重免疫组化、流式细胞术鉴定发现一种“上皮
‑
免疫”肿瘤细胞,其中上皮标志为epcam或pan
‑
ck,免疫标志为ifitm3、tnfsf10、cxcl10、bst2、isg15、hla
‑
drb1或hla
‑
dr。通过检测上述标志物鉴定“上皮
‑
免疫”双阳性细胞数量,可用于鼻咽癌的早期诊断,以及为鼻咽癌患者的预后判断提供依据,也可作为分子靶点进行靶向治疗,从而进行个体化治疗,延长患者生存期,改善患者生活质量。
附图说明
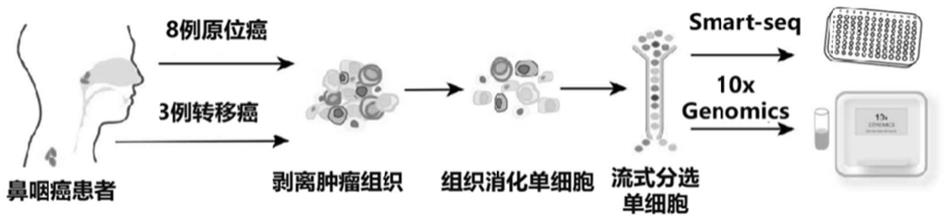
39.图1为鼻咽癌单细胞转录组流程示意图。
40.图2为单细胞转录组结果。
41.图3为免疫荧光结果。
42.图4为4例鼻咽癌组织的流式细胞术检测epcam和hla
‑
dr表达结果。
43.图5为实施例4中的免疫荧光结果。
44.图6为生存分析曲线。
45.图7为上皮
‑
免疫双阳性epcam
/hla
‑
dr
high
和上皮阳性epcam
/hla
‑
dr
low
鼻咽癌细胞的体内外增殖实验。其中图7a为使用流式分选技术,分选“上皮
‑
免疫”双阳性epcam
/hla
‑
dr
hi
和“上皮”单阳性epcam
/hla
‑
dr
low
鼻咽癌细胞,进行体内外增殖实验;图7b为裸鼠皮下成瘤实验,“上皮
‑
免疫”双阳性epcam
/hla
‑
dr
hi
和“上皮”单阳性epcam
/hla
‑
dr
low
鼻咽癌肿瘤重量增长;图7c为裸鼠皮下成瘤实验,“上皮
‑
免疫”双阳性epcam
/hla
‑
dr
hi
和“上皮”单阳性epcam
/hla
‑
dr
low
鼻咽癌肿瘤体积增长情况。
具体实施方式
46.以下将结合实施例对本发明的构思及产生的技术效果进行清楚、完整地描述,以充分地理解本发明的目的、特征和效果。显然,所描述的实施例只是本发明的一部分实施例,而不是全部实施例,基于本发明的实施例,本领域的技术人员在不付出创造性劳动的前提下所获得的其他实施例,均属于本发明保护的范围。
47.实施例1
48.本实施例单细胞转录组测序技术检测鼻咽癌“上皮
‑
免疫”细胞,操作如模式图1所示,具体包含以下步骤:
49.1)获取鼻咽癌新鲜组织;机械切碎至1
‑
2mm3。
50.2)胰酶消化【100μg/ml liberasetm research grade(roche,cat#5401127001)和5u/μldnase i(neb,cat#m0303l)于5ml pbs中】,50rpm震荡,37℃,20分钟。
51.3)用70μm细胞筛过滤;过滤后的细胞加入5ml lympholyte
‑
h(cedar lane labs,cat#cl5020)用于去除红细胞、碎片等。
52.4)流式分选活细胞、然后使用10x genomics gemcode平台,进行活力检测并进行测序。
53.5)使用cellranger进行单细胞转录组测序分析。
54.6)通过对数据进行生物信息学分析,根据细胞表达情况,区分细胞类型,并分析鼻咽癌细胞表达谱。
55.结果见图2,可以看到存在一群“上皮
‑
免疫”双阳性细胞,“上皮
‑
免疫”双阳性细胞
表达“上皮”标志物epcam,同时表达“免疫”标志物ifitm3、tnfsf10、cxcl10、bst2、isg5。
56.实施例2
57.本实施例通过多重免疫组化,检测鼻咽癌“上皮
‑
免疫”细胞。
58.具体步骤如下:
59.1)获取鼻咽癌石蜡包埋组织样品。
60.2)将4μm石蜡包埋组织切片浸于柠檬酸抗原提取溶液(ph 6.0)中,微波煮沸2.5分钟。
61.3)切片中加入hla
‑
drb1抗体(1:600浓度稀释,abcam,货号ab92511)、pan
‑
ck(zhongshan biotechnology,货号zm
‑
0069)4℃孵育过夜。
62.4)洗3次后,切片中加入荧光二抗,置湿盒内,37℃恒温箱孵育30分钟。
63.5)使用dapi(sigma,货号d9524)染色10分钟。
64.最后使用anti
‑
fade进行封皮,并使用olympus fv1000 confocal系统进行拍照。
65.结果见图3,可以看到,使用多重免疫组化,检测上皮标志物pan
‑
ck和免疫标志物hla
‑
drb1,结果明确鼻咽癌组织中存在“上皮
‑
免疫”双阳性细胞。
66.实施例3
67.本实施例通过流式细胞术,检测鼻咽癌“上皮
‑
免疫”细胞。
68.1)获取鼻咽癌新鲜组织;机械切碎至1
‑
2mm3。
69.2)胰酶消化【100μg/ml liberasetm research grade(roche,cat#5401127001)和5u/μldnase i(neb,cat#m0303l)于5ml pbs中】,50rpm震荡,37℃,20分钟。
70.3)用70μm细胞筛过滤;过滤后的细胞加入5ml lympholyte
‑
h(cedar lane labs,cat#cl5020)用于去除红细胞、碎片等。
71.4)然后加入epcam(abcam,货号ab112068)和hla
‑
dr(bd,货号560651)进行室温孵育30分钟。
72.5)然后进行流式细胞检测。
73.结果见图4,可以看出使用流式细胞术,检测鼻咽癌肿瘤组织中,上皮标志物epcam和免疫标志hla
‑
dr的表达情况,结果明确鼻咽癌组织中存在“上皮
‑
免疫”双阳性细胞。
74.实施例4
75.本实施通过免疫组化,检测鼻咽癌细胞中“免疫”标志hla
‑
dr表达水平。
76.1)获取鼻咽癌石蜡包埋组织样品。
77.2)将4μm石蜡包埋组织切片浸于柠檬酸抗原提取溶液(ph 6.0)中,微波煮沸2.5分钟。
78.3)切片中加入hla
‑
dr抗体(1:600浓度稀释,abcam,货号ab92511)孵育。
79.4)切片中加入二抗,置湿盒内,37℃恒温箱孵育30分钟。
80.5)3,3'
‑
二氨基联苯胺染色2分钟。
81.6)mayer苏木精复染使胞核着色。
82.7)切片脱水固定。
83.8)免疫反应性由两位病理学家独立进行评分,且两位病理学家均不了解此样本来源的患者信息。
84.9)根据肿瘤细胞显色反应强度评分如下:无染色0分,低度染色1分,中度染色2分,
强染色3分。
85.10)根据染色肿瘤细胞数占总细胞数比例评分如下:0%为0分,1%
–
10%为1分,11%
–
50%为2分,51%
–
80%为3分,81%
–
100%为4分。
86.11)两位病理学家评分的平均值作为最终得分,强度分数
×
百分比分数为ihc得分,根据肿瘤细胞中hla
‑
dr免疫染色的中值,可将鼻咽癌患者分为hla
‑
dr高表达及低表达组(图5)。
87.结合患者预后情况,进行生存分析。结果发现在鼻咽癌细胞中,高表达“免疫”标志hla
‑
dr,与鼻咽癌预后不良相关(图6)。
88.实施例5
89.功能实验:
90.1)使用流式分选技术,分选“上皮
‑
免疫”双阳性epcam
/hla
‑
dr
hi
和“上皮”单阳性epcam
/hla
‑
dr
low
鼻咽癌细胞,进行体内外增殖实验,“上皮
‑
免疫”双阳性epcam
/hla
‑
dr
hi
细胞增长更快(图7a)。
91.2)进行裸鼠皮下成瘤实验,结果显示,“上皮
‑
免疫”双阳性epcam /hla
‑
drhi细胞肿瘤增长更快(图7b
‑
图7c)。
92.综上所述,使用单细胞转录组、多重免疫组化、流式细胞术,检测“上皮
‑
免疫”双阳性数量,可以有效预测鼻咽癌预后,并可以用于鼻咽癌诊断。
93.上述具体实施方式对本发明作了详细说明,但是本发明不限于上述实施例,在所属技术领域普通技术人员所具备的知识范围内,还可以在不脱离本发明宗旨的前提下作出各种变化。此外,在不冲突的情况下,本发明的实施例及实施例中的特征可以相互组合。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。