1.本发明涉及一种利用激光的磷灰石粉末合成方法,具体涉及将基板浸渍于磷灰石形成用前体溶液并照射激光以形成磷灰石粉末的方法。
背景技术:
2.作为最为广泛使用的医用金属材料,钛基合金具有低弹性模量和突出的生物相容性,并且耐腐蚀性等比以往所使用的生物金属更加优秀。然而,因其具有生物惰性而无法直接诱导骨形成,需要相当长的治疗时间来实现骨结合,并且自然形成的氧化粉末的厚度薄,会很快消失,从而无法引导邻近的骨组织的再生。
3.因此,正在通过种植体表面处理来赋予生物活性度,以解决上述种植体无法直接与骨骼结合的问题,并解决为了缩短骨结合期间而松弛的问题。正在以物理、化学方法对用作种植体的主要材料的钛的表面实施表面处理以进一步提高生物活性,从而缩短种将植体植入人体后的愈合期,并且正在持续地进行关于更加有效的表面处理的研究。
4.此时,使用羟基磷灰石作为对钛的表面进行表面处理的材料。作为构成人体的硬组织的基本组分,羟基磷灰石(hydroxyapatite)还被用作骨组织移植或骨再生材料。羟基磷灰石的化学结构为ca
10
(po4)6(oh)2,人体的牙釉质中的羟基磷灰石主要分布于约1~2mm厚度的最外层牙釉质。这种羟基磷灰石能够体现再矿化效果,因此,具有填补脱钙牙釉质的微小空隙的功能。
5.除上述种植体表面处理以外,还要求磷灰石根据不同应用领域具备适合的粒子组分和粒径,以提供与用途相应的特征。以往主要采用固相反应法和水热合成法,以制备针状或板状的磷灰石粒子。然而,这些现有的方法存在诸多问题。
6.固相反应法的问题在于,热处理温度约为800℃~1200℃的高温,因此,所制备的粒子会增大至数十微米,并且在反应之后需要介入混合、煅烧、粉碎等复杂的后期工序,因此,无法成为在工业上有利的方法。
7.另一方面,水热合成法通常是利用非晶质的已沉淀的磷酸钙(calcium phosphate)在高压釜中以约150~250℃的温度范围进行反应的方法,需要沉淀和水热合成两步工序,并且需要混合多种添加剂,工艺本身复杂,因此,在大量生产上存在问题。
技术实现要素:
8.技术问题
9.本发明旨在解决上述多个问题,其目的在于,提供一种利用激光的磷灰石粉末合成方法,其向浸渍于磷灰石形成用前体溶液中的基材的表面照射激光以合成磷灰石粉末。
10.然而,这一技术问题是示例性的,本发明的范围不限于此。
11.技术方案
12.根据用于达成上述目的的本发明的一观点,提供一种利用激光的磷灰石粉末合成方法,其包括如下步骤:(a)将基板浸渍于磷灰石形成用前体溶液中;(b)向浸渍于所述磷灰
石形成用前体溶液中的基板上的区域照射激光束;以及(c)获得在所述磷灰石形成用前体溶液中生成的磷灰石粉末。
13.另外,根据本发明的一实施例,能够在所述步骤(c)中合成由化学式1表示的磷灰石粉末。
14.化学式1:
15.(m1)
a
(m2)
10-a
(zo4)6(x)216.其中,m1、m2分别是选自ca
2
、pb
2
、sr
2
、mg
2
、fe
2
、mn
2
、cd
2
、ba
2
、co
2
、ni
2
、cu
2
、zn
2
、sn
2
、eu
2
、na
、k
、li
、rb
、nh
4
、la
3
、ce
3
、sm
3
、eu
3
、y
3
、bi
3
、cr
3
、th
4
、u
4
以及u
6
中的一种,
17.zo4是选自po
43
‑
、aso
43
‑
、sio
44
‑
、vo
43
‑
、cro
43
‑
、cro
42
‑
、mno
43
‑
、so
42
‑
、seo
42
‑
、bef
42
‑
、geo
44
‑
、reo
53
‑
、sbo3f4‑
、sion5‑
、bo
45
‑
、bo
33
‑
以及co
32
‑
中的一种,
18.x是选自f
‑
、oh
‑
、cl
‑
、o2‑
、o3‑
、nco
‑
、bo2‑
、br
‑
、i
‑
、no2‑
、no3‑
、co
32
‑
、o
22
‑
、o2‑
、s2‑
、ncn2‑
以及no
22
‑
中的一种,
19.a是0~10之间的实数。
20.另外,根据本发明的一实施例,在所述步骤(a)中,所述磷灰石形成用前体溶液中可以溶解有m1离子、m2离子以及zo4离子。
21.另外,根据本发明的一实施例,当所述磷灰石形成用前体溶液包含ca
2
离子和po
43
‑
离子时,能够在所述步骤(c)中形成羟基磷灰石粉末。
22.另外,根据本发明的一实施例,当所述磷灰石形成用前体溶液包含mg
2
离子时,能够在所述步骤(c)中形成羟基磷灰石、含mg磷灰石、白磷钙石(whitlockite)以及它们的组合中的一种磷灰石粉末。
23.另外,根据本发明的一实施例,可通过调节所述磷灰石形成用前体溶液的浓度来控制所述磷灰石粉末的尺寸。
24.另外,根据本发明的一实施例,所述步骤(b)可以包括调节激光束照射时间以控制所生成的磷灰石粉末的尺寸的步骤。
25.另外,根据本发明的一实施例,所述步骤(b)可以包括调节激光束输出功率以控制所生成的磷灰石粉末的尺寸的步骤。
26.另外,根据本发明的一实施例,可通过调节所述磷灰石形成用前体溶液的组分来控制所述磷灰石粉末的组分。另外,根据本发明的一实施例,可通过调节所述磷灰石形成用前体溶液的浓度来控制所述磷灰石粉末的(m1 m2)/zo4比。
27.另外,根据本发明的一实施例,可通过调节所述激光束的功率来控制磷灰石粉末的结晶度。
28.另外,根据本发明的一实施例,可通过调节所述激光束的脉宽来控制磷灰石粉末的结晶度。
29.有益效果
30.根据上述本发明的一实施例,具有能够向浸渍于磷灰石形成用前体溶液中的基材的表面照射激光以合成组分和尺寸经调节的磷灰石粉末的效果。
31.然而,上述问题仅仅是示例,本发明的范围不限于此。
附图说明
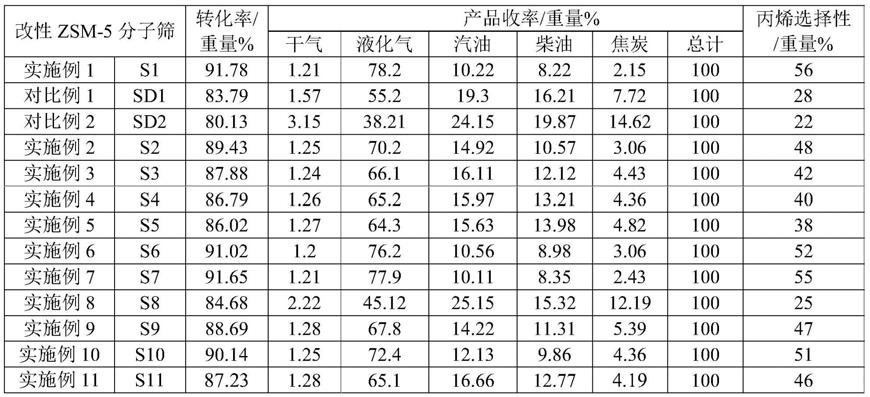
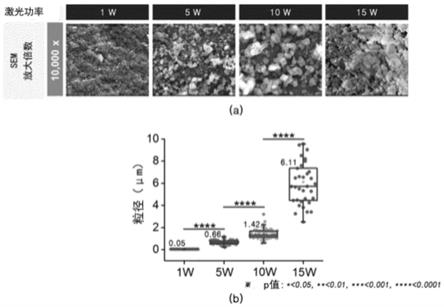
32.图1是根据一实施例的激光功率形成的磷灰石粉末的sem图像,以及所形成的磷灰石粉末的尺寸随激光功率而变的图。
33.图2是示出根据一实施例的磷灰石形成用前体溶液的浓度和激光照射时间而形成的磷灰石的尺寸的图。
34.图3是根据一实施例生成的白磷钙石(whitlockite)结晶的sem图像。
35.图4是根据一实施例和比较例生成的磷灰石结晶的sem图像。
36.图5是示出根据一实施例和比较例生成的磷灰石结晶的尺寸和生长率的图。
37.图6是根据一实施例生成的含mg磷灰石结晶的sem图像以及mg含量分析结果。
38.图7至图9是一实施例的磷灰石的电子显微镜及xrd测量结果。
39.图10是根据一实施例生成磷灰石之后的eds测量结果。
40.图11是在一实施例中调节激光功率以合成的磷灰石粉末的xrd和电子显微镜测量结果。
41.图12是在一实施例中调节激光脉宽以合成的磷灰石粉末的xrd和电子显微镜测量结果。
具体实施方式
42.后述的对于本发明的详细说明将参照附图,该附图将能够实施本发明的特定实施例作为示例示出。充分说明这些实施例,以使本领域技术人员能够实施本发明。应当理解本发明的多个实施例彼此不同但不必互斥。例如,记载于此的特定形状、结构以及特性,与一实施例相关联,在不脱离本发明的精神以及范围内,能够实现为其他实施例。另外,应当理解各个公开的实施例内的各个构成要素的位置或配置在不脱离本发明的精神以及范围内,能够进行变更。因此,后述的详细说明不是限定性的,只要恰当地说明,本发明的范围仅由其权利要求及其等同范围限定。附图中的相似的附图标记在各个方面指代相同或相似的功能,并且为了方便起见,能够进行夸张的表达。
43.以下,参照附图对本发明的多个优选实施例进行详细说明,以使本领域技术人员能够容易地实施本发明。
44.本发明的一实施例的磷灰石粉末合成方法包括如下步骤:(a)将基板浸渍于磷灰石形成用前体溶液中;(b)向浸渍于所述磷灰石形成用前体溶液中的基板上的区域照射激光束;以及(c)获得在所述磷灰石形成用前体溶液中生成的磷灰石粉末。
45.基板作为表面形成磷灰石膜的材料,例如,可以是生物金属。例如,所述基板可以使用选自钛、钛合金、镁以及镁合金中的任一种。除此之外,作为金属材料或陶瓷材料,可以使用需要形成磷灰石膜的材料。
46.本发明通过激光照射来形成含有所述磷灰石形成用前体溶液中所包含的离子的磷灰石粉末,因此,磷灰石形成用前体溶液中包含的离子的种类不受特别的限定。在一实施例中,作为供给用于生成磷灰石的原料的溶液,磷灰石形成用前体溶液可以包含选自ca
2
、pb
2
、sr
2
、mg
2
、fe
2
、mn
2
、cd
2
、ba
2
、co
2
、ni
2
、cu
2
、zn
2
、sn
2
、eu
2
、na
、k
、li
、rb
、nh
4
、la
3
、ce
3
、sm
3
、eu
3
、y
3
、bi
3
、cr
3
、th
4
、u
4
以及u
6
中的阳离子和选自po
43
‑
、aso
43
‑
、sio
44
‑
、vo
43
‑
、cro
43
‑
、cro
42
‑
、mno
43
‑
、so
42
‑
、seo
42
‑
、bef
42
‑
、geo
44
‑
、reo
53
‑
、sbo3f4‑
、sion5‑
、bo
45
‑
、bo
33
‑
以
及co
32
‑
中的阴离子。附加地,可以进一步包含选自f
‑
、oh
‑
、cl
‑
、o2‑
、o3‑
、nco
‑
、bo2‑
、br
‑
、i
‑
、no2‑
、no3‑
、co
32
‑
、o
22
‑
、o2‑
、s2‑
、ncn2‑
以及no
22
‑
中的离子。当使用包含上述离子的磷灰石形成用前体溶液时,能够在磷灰石形成用前体溶液中合成由化学式1表示的磷灰石粉末。
47.化学式1:
48.(m1)
a
(m2)
10-a
(zo4)6(x)249.其中,m1、m2分别是选自ca
2
、pb
2
、sr
2
、mg
2
、fe
2
、mn
2
、cd
2
、ba
2
、co
2
、ni
2
、cu
2
、zn
2
、sn
2
、eu
2
、na
、k
、li
、rb
、nh
4
、la
3
、ce
3
、sm
3
、eu
3
、y
3
、bi
3
、cr
3
、th
4
、u
4
以及u
6
中的一种,zo4是选自po
43
‑
、aso
43
‑
、sio
44
‑
、vo
43
‑
、cro
43
‑
、cro
42
‑
、mno
43
‑
、so
42
‑
、seo
42
‑
、bef
42
‑
、geo
44
‑
、reo
53
‑
、sbo3f4‑
、sion5‑
、bo
45
‑
、bo
33
‑
以及co
32
‑
中的一种,x是选自f
‑
、oh
‑
、cl
‑
、o2‑
、o3‑
、nco
‑
、bo2‑
、br
‑
、i
‑
、no2‑
、no3‑
、co
32
‑
、o
22
‑
、o2‑
、s2‑
、ncn2‑
以及no
22
‑
中的一种,a是0~10之间的实数。即,能够通过激光照射在溶液中形成含有溶解于所述磷灰石形成用前体溶液中的离子的磷灰石粉末。
50.以下,作为用于生成磷灰石的前体溶液的一例,对包含ca
2
离子和po
43
‑
离子的前体溶液进行更加详细说明。例如,包含ca
2
离子和po
43
‑
离子的前体溶液可以是选自包含dmem(杜尔贝科改良伊格尔培养基:dulbecco modified eagle medium)、hbss(hank's平衡盐溶液:hank's balanced salt solution)、hbp(人体血浆:human blood plasma)的无机组分的溶液以及sbf(模拟体液:simulated body fluid)中的一种。可以将所述磷灰石形成用前体溶液的ca
2
离子和po
43
‑
离子的浓度提高1倍~400倍后使用,以促进磷灰石的形成。然而,本发明不限于此,只要能够根据合成目的来调节前体溶液的浓度即可。
51.当向浸渍于磷灰石形成用前体溶液中的基材的表面照射具有高能量的激光束时,能够使前体溶液中的ca
2
离子与po
43
‑
离子的反应活化,从而形成磷灰石粉末。随后,可以通过将生成的磷灰石粉末与溶液分离并进行固化等的方式来形成成型体。
52.以往需经过固相合成、液相合成、气相合成、水热合成等方法来合成磷灰石粉末,现有方法的问题在于,工艺复杂且需经高温热处理。与此不同地,根据本发明的实施例,能够向前体溶液中的基板上的区域照射激光束,以在基板上形成磷灰石膜,同时在溶液中形成磷灰石粉末。能够将如此生成的磷灰石粉末分离并进行干燥,通过随后的成型来制造多种形状的产品,因此,与形成为镀膜时相比,利用率更高。
53.作为供给用于形成磷灰石的能量的能量供给源,激光发生器可以使用,例如,镱纳秒脉冲激光(ytterbium nanosecond pulsed)发生器或飞秒脉冲激光(femtosecond laser)发生器。此时,纳秒激光表示脉冲时间为数纳秒的具有10
‑9秒的短的脉宽的激光,飞秒激光表示具有10
‑
15
秒的非常短的脉宽的激光。然而,本发明不限于此,只要是能够对前体溶液施加充分的能量以生成磷灰石的激光即可。
54.能够控制磷灰石形成用前体溶液的浓度、激光束的条件,例如,激光束的功率、照射时间等,以改变生成的磷灰石粉末的尺寸。
55.能够调节磷灰石形成用前体溶液的组分、浓度,以改变磷灰石粉末的组分。例如,当磷灰石形成用前体溶液包含mg
2
离子时,能够根据mg
2
离子的含量来形成羟基磷灰石、含mg磷灰石、白磷钙石(whitlockite)以及它们的组合中的任一种磷灰石粉末。作为另一例,还能够通过调节磷灰石形成用前体溶液的浓度,以控制磷灰石粉末的(m1 m2)/zo4比。
56.根据本发明的实施例,能够通过控制激光束照射条件,例如,激光的功率、脉宽、波
长、脉冲能量、重复率、照射时间等,以调节磷灰石粉末的结晶度(crystallinity)。
57.以下,对多个实施例进行说明,所述实施例用于帮助理解本发明。只是,以下多个实施例仅用于帮助理解本发明,本发明不仅限于以下多个实施例。
58.实施例
59.基板使用钛或镁。向位于固定有基板的pdms模板上部的前体溶液浸渍部投入浓度被提高为100倍~400倍的dmem。然后,利用镱纳秒脉冲激光(ytterbium pulsed fiber laser)向基板的表面照射激光束以形成磷灰石粉末。激光束的功率从1w~15w范围中选择,照射时间从15分钟~30分钟范围中选择。
60.实验例
61.图1是对于根据激光功率所合成的磷灰石粉末尺寸进行分析的结果,能够确认当功率为1w~15w时,所合成的粉末的尺寸约为50nm~6000nm。能够确认激光照射能量越高,所生成的磷灰石粉末的尺寸越大。
62.图2是示出根据磷灰石形成用前体溶液浓度和激光照射时间而形成的磷灰石的尺寸的图。能够确认前体溶液浓度越浓,激光照射时间越长,所形成的磷灰石粉末的尺寸越大。与钛基板相比,当对镁基板照射激光时,所形成的磷灰石粉末的尺寸更小。因此,能够预料到即便照射相同能量的激光,温度上升程度也会根据基板而不同。
63.图3是由含有mg离子的磷灰石形成用前体溶液生成的白磷钙石(whitlockite)结晶的sem图像。由此能够确认利用激光生成了磷灰石结晶。
64.图4和图5是示出根据一实施例和比较例生成的磷灰石结晶的图像和结晶尺寸的图。图4的(a)、(b)是将白磷钙石(whitlockite)通过水热合成法合成而形成的结晶和结晶经两周生长的电子显微镜图像(参考文献:jang,hae lin,et al."phase transformation from hydroxyapatite to the secondary bone mineral,whitlockite."journal of materials chemistry b 3.7(2015):1342
‑
1349),其中,所述白磷钙石为含有mg离子的磷灰石。图4的(c)是将白磷钙石(whitlockite)通过激光照射合成而形成的结晶的电子显微镜图像,其中,白磷钙石为含有mg离子的磷灰石。
65.在图5的(a)中,通过水热合成法合成的白磷钙石(whitlockite)结晶的尺寸约为87nm,经两周生长的尺寸约为212nm,然而利用激光经15分钟合成的白磷钙石(whitlockite)结晶的尺寸约为1759nm,这表示能够形成最小约8倍、最大20倍尺寸的结晶。图5的(b)示出了结晶尺寸除以反应时间而得到的“结晶生长速度(生长率)”,与利用水热合成法的结晶生长速度相比,利用激光的方法具有快约11147倍的速度。
66.图6是所生成的含mg磷灰石结晶的sem图像以及mg含量分析结果。这表示能够调节反应溶液的离子组分以调节所合成的粉末的组分。
67.图7和图8是实施例的磷灰石的电子显微镜及xrd测量结果。作为改变激光的脉宽(pulse width)和功率以合成的粉末的相分析结果,在所有激光条件下均观察到了纯羟基磷灰石(hydroxyapatite)相。这表示即便激光条件(脉宽、功率)改变,也能够在不发生相变化的情况下稳定地合成粉末。
68.图9示出了能够通过调节前体溶液的组分来合成纯羟基磷灰石、含有mg组分的磷灰石以及具有白磷钙石(whitlockite)相的粉末。
69.图10是根据实施例生成磷灰石之后测量的eds的结果。示出了当利用组分经调节
的磷灰石形成用前体溶液以合成粉末时所合成的粉末的ca与p的组分含量之比,示出了能够合成ca/p之比经调节的粉末。
70.图11是示出当利用激光合成磷灰石粉末时根据激光功率所合成的粉末的结晶度变化的结果。图11的(a)是磷灰石粉末的xrd测量结果,结晶度越高,峰(peak)的厚度越薄,而高度越高。在激光的功率为1w时,显示相对较高的结晶度。图11的(b)是利用sem、tem、tem
‑
sad观察磷灰石粉末的结果。结晶度越高,在tem
‑
sad中越显示为白色的点状,且在激光功率为1w时,显示相对较高的结晶度。
71.图12是示出当利用激光合成磷灰石粉末时根据激光脉宽而合成的粉末的结晶度变化的结果。参照图12,在激光的脉宽为4ns时,结晶度相对较高,在200ns时,结晶度相对较低。
72.总结图11以及图12的结果,能够改变激光的功率、脉宽以调节所合成的磷灰石粉末的结晶度。
73.综上所述,根据本发明的实施例,能够在形成磷灰石膜的同时,形成磷灰石粉末粒子,因此,粉末制备方法简单,并且能够通过随后的粉末成型来制造多种尺寸和形状的产品,因此,利用率高。
74.利用多个优选实施例对本发明进行了说明,但本发明不限于所述实施例,本领域技术人员能够在不脱离本发明的精神的范围内进行多种变形和变更。这些变形例和变更例应当被视为属于本发明和所附权利要求的范围内。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。