固态纳米孔
‑
荧光共振能量转移复合检测方法及系统
技术领域
1.本发明属于单分子检测技术,特别是涉及一种用于单分子构象检测的固态纳米孔
‑
荧光共振能量转移复合检测方法及系统。
背景技术:
2.固态纳米孔作为一种单分子平台可以检测生物分子的构象变化,对于研究其结构和功能有重要意义。固态纳米孔是电泳单分子传感器,由纳米级别的超薄绝缘膜以及被该绝缘膜分隔开来的两个含有离子溶液的纳米级腔室组成。当两侧腔室施加合适的电压、压力或渗透压时,纳米孔可以利用检测通过孔的离子电流来探测带电的生物分子(例如dna、rna、蛋白质等),当分析物占据纳米孔中的一部分体积时,孔内溶液电导率会受到改变,从而导致离子电流的可测量变化。分析物不同的构象可以呈现出不同幅度或不同形状的电流信号,电流变化的持续时间也有所不同。然而,传统纳米孔只能对物质的在孔内部分的轮廓、体积信息进行分辨。溶液中生物分子的构象差异往往复杂多变,一些细小的变化可能具有重要的生物学意义,受纳米孔分辨率的影响,这些局部细微的构象改变无法通过离子电流区分开来。
3.荧光共振能量转移是指在两个不同的荧光基团中,当一个供体荧光分子的荧光光谱与另一个受体荧光分子的激发光谱具有重叠时,供体荧光分子的激发能诱发受体分子发出荧光,同时供体荧光分子自身的荧光强度衰减。荧光共振能量转移的强度和供体、受体的间隔距离的6次方呈反比,因而可以极为灵敏地检测分子间或分子内部不同结构域的纳米级尺度的距离变化。
4.目前未见固态纳米孔平台单分子检测和荧光共振能量转移技术的结合研究及应用。
技术实现要素:
5.发明目的:针对上述现有技术中存在的技术问题,本发明提供了一种固态纳米孔
‑
荧光共振能量转移复合检测方法即系统。
6.技术方案:本发明所述的一种固态纳米孔
‑
荧光共振能量转移复合检测方法,首先采用荧光显微镜聚焦于固态纳米孔所在的平面,然后用成对的荧光基团同时标记待分析物分子,在待分析物分子通过纳米孔时,采集待分析物分子过孔电流信号以及标记荧光基团间的荧光共振能量转移信号强度,在时间上匹配特征光、电信号,复合解析分子构象信息。
7.本发明所用的固态纳米孔检测装置可以为:包括氮化硅固态纳米孔芯片、ag电极、膜片钳设备axon 200b,ag电极与膜片钳系统电极夹持装置相连接,从而可以在纳米孔芯片的两次施加电压。
8.所述纳米孔芯片孔径大小根据分析物分子的大小,可供选择的范围为2nm
‑
350nm。
9.使用纳米孔芯片前需要用氧plasma等离子体清洗仪处理三分钟。对于ag/agcl电极,要用砂纸打磨去除表面氧化物,再在氯化铁溶液中浸泡,用纯水冲洗干净后晾干。
10.分析物与荧光团混合孵育后离心,过葡聚糖凝胶洗柱,用pbs洗脱。用注射器缓慢地将用荧光团标记后的样品推入纳米孔芯片一侧腔室中。ag电极与溶液接触并固定,与膜片钳系统相连,包括膜片钳放大器、数模/模数信号转换器和数据分析系统,分析物通过纳米孔的信号由电流幅度变化的形式呈现。
11.一般的,将固态纳米孔装置固定于共聚焦显微镜物镜下部,激发光系统根据分析物所用的荧光团来选择,共聚焦显微镜中的激光照明源发出的光束经二向色镜反射,通过光纤耦合器连接到扫描单元,通过扩束器使薄激光束能够完全填充物镜后孔径,然后由透镜系统聚焦到焦平面上的一个非常小的光斑,照明点的大小范围为直径的大约0.25到0.8微米,并且在最亮的强度下的深度为0.5到1.5微米。位于光电倍增管正前方的共轭平面上的针孔充当空间滤波器,激发的二次荧光穿过二向色镜和滤光片到达针孔。在物镜焦平面上方和下方发生的大量荧光发射与针孔不共焦,这些离焦光束在孔径平面中形成扩展的艾里斑,大部分杂散光都被针孔光圈消除。只有一小部分离焦荧光发射是通过针孔孔传递的,所以光电倍增管检测不到大部分这种外来光,也不会对产生的图像产生影响。通过针孔的荧光发射被光电倍增管转换成具有连续变化的电压(对应于荧光强度)的模拟电信号。模拟信号被周期性地采样,并通过安装在扫描单元或随附的电子柜中的模拟
‑
数字(a/d)转换器转换成像素。图像信息临时存储在计算机中的图像帧缓冲卡中并显示在监视器上。
12.在应用本发明方法时,采用的固态纳米孔材质为石墨烯、二硫化钼、氮化硅、二氧化硅中的一种或多种构成。可由湿法刻蚀、电介质击穿法、聚焦离子束刻蚀、电子束刻蚀法制备获得。使用的纳米孔大小根据被测分析物尺寸设计,为了兼容共聚焦显微镜的光学系统,其等效孔径范围为20nm
‑
350nm。不同材质和方法制备而成的固态纳米孔在尺寸结构和电学性质上有所差异,但都适用于本方法。
13.荧光团可以单独使用,也可作为一个功能系统搭配使用,在本方法中,单次检测中使用的荧光团种类为2种或2种以上,不同荧光团之间的发射波长和激发波长峰值相差10nm以上,且光谱之间存在交叠。当一个荧光团的激发光谱和另一个荧光团的发射光谱具有重叠时,且二者位于合适的距离和取向时发生荧光共振能量转移。所述用于标记分析物分子的荧光团可以是蛋白质和肽类或小分子有机化合物,如绿色荧光蛋白、黄色荧光蛋白、红色荧光蛋白等,核酸染料如dapi、溴化乙锭等。该方法通用性强,所述分析物分子是仅由同类分子组成或是由多种类能发生结构上相互作用的分子共同组成,可以检测蛋白质、dna、rna等生物分子自身多变的构象,或是分子间相互作用导致的相对位置和构象的变化,一些纳米尺度的带电粒子也可以应用于该方法。
14.分子由于自由扩散,或者受到纳米孔两侧电势差、渗透压差、压力差中的至少一种驱动力,在溶液环境中通过纳米孔。当分子受力驱动通过纳米孔时,主要受力单元既可以是分子本身,也可以是标记基团。采集电信号时,至少2个金属检测电极分别位于纳米孔两侧,将电极之间产生的电流信号导入膜片钳、电化学工作站或其他电流检测装置,并记录电流信号信息。检测电极之间可以预置电势差,也可以没有电势差。用于发生荧光共振能量转移的激光系统波长范围为300nm
‑
800nm,通过光学系统采集到各个荧光基团荧光信号,经由光电倍增管或感光成像元件转化为电信号,并经过计算得到荧光共振能量转移强度。将分析物通过固态纳米孔的电信号与fret强度的光信号进行按照时间进行对准,并通过计算机检测采集两种信号同时产生波动的事件。利用荧光共振能量转移得到待测分析物的标记位点
之间的距离信息、利用过孔电信号得到分析物轮廓信息。
15.所述待分析物分子由同类分子组成,或由多种类能发生结构上相互作用的分子共同组成。纳米孔两侧的溶液中除待测分析物分子外的其他物质包括无机盐、水、三羟甲基氨基甲烷、不与待测分析物分子发生反应或结合的有机分子。
16.有益效果:本发明将荧光共振能量转移技术和固态纳米孔平台结合,固态纳米孔平台单分子检测的特性,使得分析物中的异质性群体得以定量统计和分析,同时,相对于单独的不依靠光学的固态纳米孔检测方法,能够更有效地进一步区分生物分子内部或生物分子之间细微构象差异。光信号与电信号结合可以研究人员更加精确地探索分析物的构象改变及其功能意义。该方法适用于多种分析物单独检测和不同的分析物混合检测,并可以根据分析物特性选择不同的荧光团。
附图说明
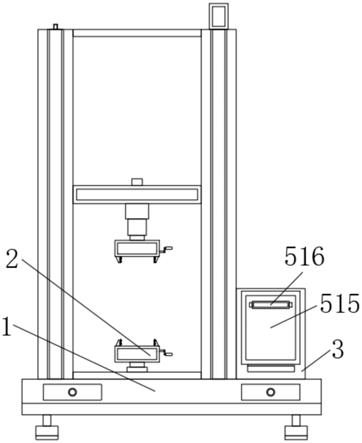
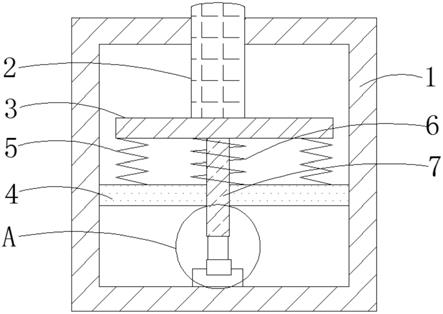
17.图1为实施例1中搭建的结合固态纳米孔和共聚焦显微镜同时检测纳米孔电信号和荧光共振能量转移光信号的平台示意图;
18.图2为实施例2中检测钙调蛋白采集的fret信号和纳米孔电流变化;
19.图3为实施例3中检测klenow大片段采集的fret信号和纳米孔电流变化。
具体实施方式
20.下面结合具体实施例对本发明方法进行进一步说明。
21.实施例1
22.氮化硅固态纳米孔芯片的制备,其通过在氮化硅自支撑薄膜上钻出纳米级小孔的过程,包括以下步骤:
23.(1)对于一面敷有二氧化硅的硅晶圆,在其二氧化硅面进行负性光刻。在二氧化硅一面的光刻完成后,将其浸入氢氟酸中去除二氧化硅层,露出中间的硅基体;随后采用四甲基氢氧化铵溶液在加热的条件下刻蚀硅基体从而得到悬空的氮化硅薄膜。
24.(2)使用球差矫正透射电子显微镜在悬空的氮化硅薄膜上制备了纳米孔。将上述氮化硅自支撑薄膜芯片装夹入透射电镜样品杆(带有悬空氮化硅的一面朝下放置),放入腔体并抽真空;随后通过视觉的反馈寻找并定位至悬空薄膜区域,并调节焦平面位置,确定最适焦平面,计算悬空区域中心点;第三步在悬空薄膜区域原位放大,细调聚焦,电子束辐照,持续观察纳米孔的生成。
25.(3)将纳米孔芯片放用食人鱼溶液(98%浓硫酸和30%过氧化氢按体积比3:1混合)中,水浴加热,待芯片冷却后,用去离子水洗净放入50%的乙醇溶液中保存,直至使用。
26.将纳米孔芯片悬空置于橡胶垫片上,橡胶垫片置于载玻片上,下方空隙为顺式侧,容纳顺式腔室溶液;纳米孔上方可滴注反式侧溶液。两个银电极直接固定两侧溶液中,经过放大器放大信号并与膜片钳系统(膜片钳设备axon 200b)相连。整个载玻片放置于共聚焦显微镜物镜下方,纳米孔芯片与共聚焦显微镜工作距离小于0.17mm,通过二向色镜和小孔等元件使得激光能聚焦于固态纳米孔所在的平面,从而能够检测到通过该平面的分子的荧光共振能量转移信号。供体荧光基团和受体荧光基团的激发光分别经由两个光电倍增管检测器检测并转换为电信号。待测分析物分子的荧光共振能量转移信号与其通过固态纳米孔
的电信号被数据采集系统采集并处理,根据对应的采集时间来匹配特征光、电信号,由此联合搭建了将固态纳米孔单分子检测技术和荧光共振能量转移技术相结合的平台。整个平台如图1所示,将固态纳米孔单分子检测技术和荧光共振能量转移技术相结合,从而可以复合解析出待测分析物分子的构象信息。
27.实施例2
28.按照实施例1搭建的平台检测钙调蛋白不同构象态。在顺式室滴入氯化钾溶液,钙调蛋白的c端和n端结构域分别用荧光探针cy3(荧光供体,标注为d)和cy5(荧光受体,标注为a)标记,并分散于氯化钾溶液中,滴入反式侧。cam是一种钙结合后能够发生构象变化的典型蛋白质,与ca
2
结合后,cam发生构型上的变化,其构象会从闭合状态变换到打开的状态,同时暴露疏水区,疏水区表面能够与调控的目标分子结合,从而对代谢过程的调控起到至关重要的作用。当钙调蛋白构象发生变化时,fret值显著变化。对固态纳米孔芯片的反式侧施加正压,驱动钙调蛋白通过纳米孔移动向另一腔室,在膜片钳系统中信号采集软件上呈现显著的离子电流幅值变化。同时,使用532nm激光器激发供体荧光团,以40毫秒的时间分辨率获取数据,收集540nm至750nm之间的荧光发射。使用的成像溶液含有tris碱(50mm,ph 7.5)、2mm trolox、0.8mg/ml葡萄糖、0.1mg/ml牛血清白蛋白、1mm dtt、0.1mg/ml葡萄糖氧化酶、0.02mg/ml过氧化氢酶、5mm mgcl2和150mm kcl。两种幅值的阻塞电流可以被观察到,通过在时间上与fret值配对,观察到低fret值与低电流幅值相对应,高fret值与高电流幅值对应,结果如图2所示。根据图示可见,低fret值表示了钙调蛋白c端、n端距离增加,对应于展开构象的钙调蛋白,其通过纳米孔的阻塞电流较小,说明展开构象的钙调蛋白具有较低的水合半径;高fret值表示了钙调蛋白c端、n端的靠近,对应于折叠构象的钙调蛋白,其通过纳米孔的阻塞电流更大,说明折叠构象的钙调蛋白具有更高的水合半径。因此,该固态纳米孔
‑
荧光共振能量转移复合检测方法能够结合fret信号强度和纳米孔阻塞电流大小解析待分析物分子在固态纳米孔中的体积信息。
29.实施例3
30.按照实施例1的方法,检测了klenow大片段与dna的结合。晶体结构表明,klenow大片段结合dna底物时,拇指域会发生构象变化,前后变化了约1.2nm。设计了如下标记有cy3b供体荧光团(标记为d)和cy5受体荧光团(标记为a)的klenow大片段。用550nm的激光器激发供体荧光团,以50毫秒的时间分辨率收集560nm至750nm之间的荧光发射。成像缓冲液含有50mm tris(ph 7.5)、10mm mgcl2、100mm nacl、100μg/ml bsa、5%甘油、1mm dtt、1mm trolox、1%葡萄糖氧化酶。将fret信号与纳米孔阻塞信号在时间上对应,结果如图3所示,根据图示可见,当klenow大片段与dna形成聚合物,拇指域的构象变化使得cy3b和cy5距离减小,显示较高fret值,其对应的过孔电流信号具有更长的过孔时间,说明形成聚合物后与孔壁之间的相互作用增大;较低的fret值代表了单独的klenow大片段,与快速的过孔事件相对应;未观察到荧光共振能量转移现象的过孔事件则是由dna分子通过纳米孔产生的。因此,该固态纳米孔
‑
荧光共振能量转移复合检测方法能够结合fret信号强度和纳米孔阻塞电流时长解析多个待分析物分子通过固态纳米孔时的结构。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。