1.本发明属于医疗机器人领域,涉及一种微型医疗机器人的施药技术,具体涉及一种磁控双驱动施药胶囊机器人。
背景技术:
2.微型机器人有关技术正飞速发展,其应用范围正持续扩大,应用程度也不断深入,目前,微型机器人在医疗领域发挥的作用正日益显著。医疗领域中,一直以来采用的传统人工内窥镜方法进行检测时,如果内窥镜在患者胃肠道中移动的幅度较大,则患者身体会对仪器反应出不适感,有时仪器甚至会存在对患者身体造成损伤的可能,因此使其更适合患者的身体是极其重要的;倘若角度控制得太小,则可能会使得图像质量下降,甚至可能会无法获得所需区域的影像;同时同时传统人工内窥镜工作效率低,医生的治疗、施药难度高,种种缺点使得医疗机构开始渐渐开始考虑使用磁控胶囊机器人取代人工进行图像获取、施药。因此十分有必要研发出现体积足够小、对患者身体不会造成过大负担的微型医疗机器人,部分医疗机构将微型胶囊机器人放入人体内进行检测、治疗,微型胶囊机器人体积小,病人的异物感小。目前在微型医疗机器人领域,科学家正致力于开发检测和轻伤的治疗技术。现如今生活中的内窥镜胶囊机器人已经可以实现普通胃肠镜的检测功能,却还无法实现在指定部位施药的功能,微型医疗机器人领域此后会更好地开发具有定点施药功能的内窥镜胶囊机器人。
技术实现要素:
3.鉴于上述现有技术的不足,本发明的目的在于一种磁控双驱动施药胶囊机器人,具有在目标位置定点施药的功能,使得胶囊机器人不仅能完成内窥镜的功能,而且能完成进一步的诊断及定点治疗任务。
4.为了解决上述技术问题,本发明采用的技术方案是:
5.一种磁控双驱动施药胶囊机器人,其特征在于:包括胶囊壳体和安装在胶囊壳体内的磁驱装置、内窥镜装置及施药装置;其中,
6.所述磁驱装置用于配合外界磁场驱动整个施药胶囊运动;
7.所述内窥镜装置用于对进行检测和施药环境观测;
8.所述施药装置包括施药微针、触发柱、固化压缩弹簧、设于胶囊壳体内的导向筒和设于胶囊壳体外的施药窗口;
9.所述施药微针位于施药窗口内,施药微针包括基底和设于基底上的微针阵列,所述施药窗口外侧还设有一层将施药微针保护起来的薄膜;
10.所述导向筒有两个,两个导向筒设于与施药窗口相对一侧的胶囊壳体内壁上,所述触发柱有两个,两个触发柱一端与施药微针的基底抵靠或者相连,另一端分别安装在两个导向筒内,两个触发柱中部通过连接板横向相连;所述固化压缩弹簧有两个,分别安装在两个导向筒内,且位于相应触发柱的端部和导向筒内底部之间;
11.所述固化压缩弹簧为通过可溶于体液的固化材料固化的压缩弹簧,安装固化压缩弹簧区域的导向筒侧壁设有与胶囊壳体外界相通的溶解孔,当施药胶囊处于人体使用环境时,体液通过溶解孔进入导向筒内将固化压缩弹簧的可溶于体液的固化材料融化,压缩弹簧释放,通过触发柱驱动施药微针向外伸出,刺破薄膜后与人体接触,进行微针施药。
12.进一步地,所述胶囊壳体为由承载壳体和施药壳体组合形成的圆柱形壳体,所述导向筒设置于承载壳体内壁,所述施药窗口设置于施药壳体外部。
13.进一步地,所述内窥镜装置包括内窥镜镜头、镜片以及电路板,其中所述内窥镜镜头设于胶囊壳体前进方向的前端。
14.进一步地,所述可溶于体液的固化材料包括明胶、淀粉和海藻酸钠中的任意一种或几种。
15.进一步地,设于施药窗口的薄膜为乳胶膜或者生物薄膜,所述薄膜还可以为无毒的塑料膜、橡胶膜等等。
16.进一步地,所述施药微针是使用pdms模具制造的微针阵列补丁,微针中含有所需药物。
17.进一步地,所述微针为圆锥状,每个微针底面直径为200
‑
400μm。
18.进一步地,两个导向筒平行设置,所述微针阵列的基底为弧形基底,每个微针均与弧形基底表面垂直。
19.进一步地,所述磁驱装置为设于胶囊壳体内同轴设置的环形永磁铁。
20.进一步地,所述导向筒设置与胶囊壳体尾部,且胶囊壳体尾部设置为便于体液进入溶解孔的开放式端口。
21.进一步地,所述微针是使用pdms模具制造的微针阵列补丁的过程制成,针中含有药物,基底不含有药物,所述微针为圆锥状,每个微针底面直径仅为300μm左右。
22.进一步地,所述承载壳体内安装有所述磁体,使得施药过程中,所述的磁控双驱动施药胶囊机器人可以通过磁控引导运动到指定的施药区。
23.进一步地,所述内窥镜镜片位于相对于施药装置的另一侧顶部,所述内窥镜装置通过无线与外界通信及数据传输。
24.进一步地,所述承载壳体与所述施药壳体之间通过倒扣与扣钩相互作用,牢固结合。
25.进一步地,所述内窥镜及所述内窥镜电路板均采用柔性线控制,该柔性线同时还作为磁控胶囊的牵引线。
26.进一步地,所述胶囊壳体整体为柱体结构,轴向剖切面为椭圆形。
27.本发明的有益效果是:
28.1、采用微型电路板控制,占用空间小、结构更紧凑,胶囊系统稳定性强;
29.2、本发明结构简单,机构动力传动效率高,没有引入复杂的机械结构,动作运行成功率较高。
30.2、胶囊机器人尾部线控能提供充足能量,可长时间多次在体内执行任务;
31.3、能额外满足胶囊机器人施药功能要求。
32.4、本发明通过设置两个触发柱和两个导向筒使得固化压缩弹簧被释放后,能根据均匀的对施药微针施加推力,从而使得施药均匀,防止施药微针顶歪,导致部分微针接触到
人体组织,而部分微针没有接触,降低施药效果。
附图说明
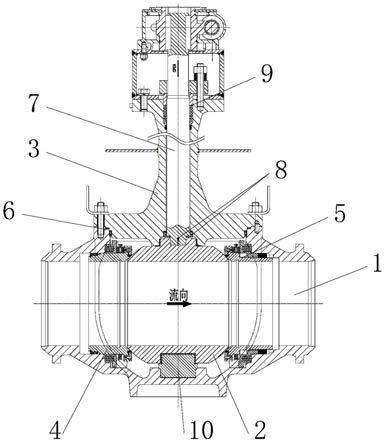
33.图1是本发明磁控双驱动施药胶囊机器人外部结构示意图。
34.图2是本发明磁控双驱动施药胶囊机器人去掉施药窗口上的薄膜示意图。
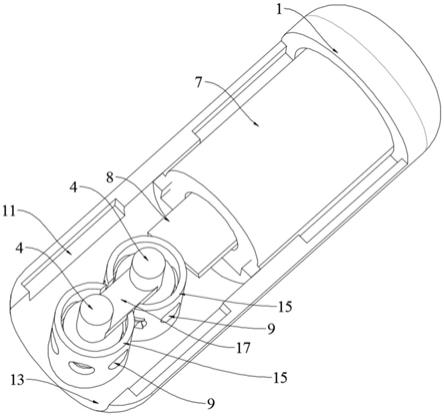
35.图3是本发明磁控双驱动施药胶囊机器人去掉施药壳体以及微针内部结构示意图。
36.图4是本发明弹簧压缩状态下内部结构剖视图。
37.图5是本发明弹簧复位状态下施药装置放大示意图。
38.图6是图中5中a
‑
a剖视图。
39.其中,1
‑
承载壳体,2
‑
施药壳体,3
‑
施药微针,31
‑
微针,32
‑
基底,4
‑
触发柱,5
‑
压缩弹簧,6
‑
内窥镜镜片,7
‑
环形永磁铁,8
‑
内窥镜电路板,9
‑
溶解孔,10
‑
扣钩,11
‑
倒扣,12
‑
固化材料,13
‑
开放式端口,14
‑
薄膜,15
‑
导向筒,16
‑
施药窗口,17
‑
连接板。
具体实施方式
40.下面结合附图和实施例来对本发明提供的一种磁控双驱动施药胶囊机器人进行详细说明,所述是对本发明的解释而不是限定。
41.如图1至图6所示,一种磁控双驱动施药胶囊机器人,包括胶囊壳体和安装在胶囊壳体内的磁驱装置、内窥镜装置及施药装置;其中,为了便于制造和组装,所述胶囊壳体为由承载壳体1和施药壳体2组合形成的圆柱形壳体,承载壳体1和施药壳体2之间通过扣钩10和倒扣11可拆卸相连。
42.所述磁驱装置用于配合外界磁场驱动整个施药胶囊运动;
43.所述内窥镜装置用于对进行检测和施药环境观测;
44.所述施药装置包括施药微针3、触发柱4、固化压缩弹簧、设于胶囊壳体内的导向筒15和设于胶囊壳体外的施药窗口16;
45.所述施药微针3位于施药窗口16内,施药微针3包括基底32和设于基底32上的由微针31组成的微针阵列,所述施药窗口16外侧还设有一层将施药微针3保护起来的薄膜14;
46.所述导向筒15有两个,两个导向筒15设于与施药窗口16相对一侧的胶囊壳体内壁上,所述触发柱4有两个,两个触发柱4一端与施药微针3的基底32抵靠或者相连,另一端分别安装在两个导向筒15内,两个触发柱4中部通过连接板17横向相连;所述固化压缩弹簧有两个,分别安装在两个导向筒15内,且位于相应触发柱4的端部和导向筒15内底部之间;
47.所述固化压缩弹簧为通过可溶于体液的固化材料12固化的压缩弹簧5,安装固化压缩弹簧区域的导向筒15侧壁设有与胶囊壳体外界相通的溶解孔9,当施药胶囊处于人体使用环境时,体液通过溶解孔9进入导向筒15内将固化压缩弹簧的可溶于体液的固化材料12融化,压缩弹簧5释放,通过触发柱4驱动施药微针3向外伸出,刺破薄膜14后与人体接触,进行微针31施药。
48.如图4和图5所示,借助可溶解的固化压缩弹簧控制触发柱4弹出微针31实现穿刺施药。所述固化压缩弹簧为通过可溶于体液的固化材料12固化的压缩弹簧5,具体的制造方式为:将弹簧压缩后保存压缩状态置于圆柱形模具内,然后往模具中灌注含有包括但不仅
限于明胶,淀粉,海藻酸钠等可溶于体液的固化材料12成分的溶液,等溶液风干后,拆模得到固化压缩弹簧。明胶,淀粉,海藻酸钠等成分在特定溶液或人体环境下的溶解,失去对压缩弹簧5的固化作用,弹簧伸展释放,产生施药动力,通过选择材料种类和圆柱形模具大小,使得固化压缩弹簧内固化态的材料在20
‑
30分钟作用能被体液溶解,从而释放压缩弹簧5,选择该时间长度是因为在该时间长度下,足以使得磁控微针31穿刺施药胶囊运动到人体任何可以达到的地方,并且稍作停留达到溶解时间后,压缩弹簧5自行释放,达到自动施药的目的,并且还不用在磁控双驱动施药胶囊机器人设置复杂的动力机构,实际上在微小的胶囊内设置微型电机不仅技术复杂,而且成本高昂,不具有实用性,而本发明通过巧妙结构设计,无需使用超微型电机,即可完成施药,大幅度降低使用和制造成本,当施药完成后取出微胶囊,只需要更换固化压缩弹簧后可以再次使用,达到重复使用的目的,而固化压缩弹簧无论是制造工艺还是材料都是常规材料和工艺,成本低廉,适合大规模推广应用。所述固化压缩弹簧复原方法包括但不仅限于通过溶解孔9流入液体逐步溶解的方式来实现。当胶囊运动到目标位置之后,固化材料12自动进行溶解,无需外界操作,简洁高效。
49.本发明通过设置两个触发柱4和两个导向筒15使得固化压缩弹簧被释放后,能根据均匀的对施药微针3施加推力,从而使得施药均匀,防止施药微针3顶歪,导致部分微针31接触到人体组织,而部分微针31没有接触,降低施药效果。
50.如图3所示,所述承载壳体1内安装有所述环形永磁铁7,使得施药过程中,所述的磁控双驱动施药胶囊机器人可以通过磁控引导运动到指定的施药区进行进一步操作。
51.如图3和图4所示,本发明内窥镜电路板8固定在环形永磁铁7内,内窥镜镜片6安装在承载壳体1前端端部,所述内窥镜镜片6及所述内窥镜电路板8均采用柔性线通讯控制,该柔性线同时还作为磁控胶囊机器人的牵引线。
52.如图2所示,所述施药微针3是使用pdms模具制造的微针阵列补丁,施药时,针尖表面含有药物,基底32不含有药物,所述微针31为圆锥状,每个微针31底面直径仅为300μm左右。测试施药有效性时,可用荧光试剂代替药物,对猪肠进行试验,观察荧光物质来判断施药的有效性,本发明施药微针3的具体制造工艺可以参考本发明人前期研究成果cn108837299b所公开技术。
53.如图4所示,所述内窥镜镜片6位于相对于施药装置的另一侧的胶囊壳体顶部,所述内窥镜装置通过无线与外界通信及数据传输,信息传输方式包含wifi但不仅限wifi。
54.如图5和图6所示,所述承载壳体1与所述施药壳体2之间通过倒扣11与扣钩10相互卡合相连,以保证能快速拆卸的牢固结合,具体的,承载壳体1上设有两个相对的凹槽,形成两个倒扣11,施药壳体2沿着轴线两侧各设有一个外侧切边的凸起,形成两个扣钩10,两个扣钩10外部之间距离略大于两个倒扣11内侧之间距离,施药壳体2本身具有一定的弹性,安装时,通过外力挤压施药壳体2两侧,使得施药壳体2变形,两个扣钩10外部之间距离小于两个倒扣11内侧之间距离,然后将两个扣钩10安装在两个倒扣11之间,释放外力,两个扣钩10在施药壳体2恢复形变的情况下向两侧伸展,抵靠在两个倒扣11内壁上,从而将承载壳体1与所述施药壳体2牢固的可拆卸固定在一起,拆卸过程完全相反,实际外力挤压施药壳体2使其变形即可,需要注意的是,两个扣钩10所需变形量不大,因此,正常情况下施药壳体2采用塑料或者金属材料制成都能满足要求。
55.如图2所示,所述胶囊壳体整体为柱体结构,轴向剖切面为椭圆形。
56.需要说明的是,本发明内窥镜装置及磁控胶囊其他常规结构并非本发明关键发明点,本发明没有详细公开的部分采用公知常识即可,比如为了配合图像采集装置,承载壳体1前端开设有拍摄孔或者胶囊壳体设置为透明罩。
57.本发明工作原理:
58.本发明所述承载壳体1内安装有磁性混合材料制成的环形永磁铁7,能在外部磁场驱动下在人体内移动及调整角度,具体的参照现有技术中的磁控胶囊技术;所述内窥镜装置能够完成图像采集功能,磁控双驱动施药胶囊机器人移动时,施药微针被薄膜覆盖,不会与人体组织接触,在到达指定位置后,只需等待所述固化压缩弹簧在体内或者溶液中,固化材料12逐渐溶解,所述压缩弹簧5复原,从而将所述含有治疗药物的微针31与所述触发柱4顶出,就能完成施药功能。
59.本发明中所述的内窥镜装置可全程记录摄录图像视频,当磁控胶囊执行任务完成后医生通过控制线将胶囊从患者体内拉出,以便开展后续的检测治疗工作。
60.以上实施方式仅用于说明本发明,而非对本发明的限制。尽管参照实施例对本发明进行了详细说明,本领域的普通技术人员应当理解,对本发明的技术方案进行各种组合、修改或者等同替换,都不脱离本发明技术方案的精神和范围,均应涵盖在本发明的权利要求范围当中。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。