基因编辑以改善关节功能
1.与相关申请的交叉引用
2.本技术要求2019年1月18日提交的美国临时专利申请号62/794,340、2019年8月30日提交的美国临时专利申请号62/894,184和2019年10月14日提交的美国临时专利申请号62/914,635的优先权,所述临时专利申请整体通过参考并入本文。
技术领域
3.本文中描述了用于治疗滑膜关节功能障碍的组合物和方法。此外,本文中公开了对滑膜细胞(synovial cells和/或synoviocytes)、软骨细胞、滑膜巨噬细胞和滑膜成纤维细胞进行基因编辑的方法,以及基因编辑过的滑膜细胞(synovial cells和/或synoviocytes)、软骨细胞、滑膜巨噬细胞和滑膜成纤维细胞在治疗诸如骨关节炎的疾病中的用途。
背景技术:
4.骨关节炎、退行性关节疾病和其他关节功能障碍的治疗是复杂的,并且对于症状缓解或恢复关节功能来说几乎没有长期选项。骨关节炎(oa)是由疼痛造成的残疾的主要原因。neogi,osteoarthritis cartilage2013;21:1145
‑
53。所有哺乳动物物种均受影响:取决于疾病进展的程度,工作动物、驯养宠物及其主人都会遭受与oa相关的不适、疼痛和残疾。
5.oa是一种以渐进性的残疾过程为特征的复杂疾病。系统性炎症与oa和oa疾病进展相关。炎症由促炎性细胞因子的水平升高驱动。迫切需要治疗这种疾病的新方法和组合物。本文公开了可用于治疗oa以及其他炎性关节障碍的组合物和方法。
6.对“序列表”、表格或在光盘上提交的计算机程序列表附录的引用
7.包含在名为“sequence_listing_123994
‑
5001
‑
wo.txt”的文件中并具有17.1kb大小的序列表已通过efs
‑
web以电子方式在此提交,所述txt文件的内容整体通过参考并入本文。
技术实现要素:
8.本发明提供了用于治疗以炎性成分为特征的关节障碍的组合物和方法。在某些情况下,所述组合物和方法用于在哺乳动物关节中预防骨关节炎和其他关节炎的进展和治疗骨关节炎和其他关节炎。根据示例性实施方式,至少一部分所述关节滑膜细胞和/或滑膜细胞、软骨细胞、滑膜巨噬细胞或滑膜成纤维细胞被基因编辑,以降低炎性细胞因子的表达。在某些情况下,至少一部分所述关节滑膜细胞和/或滑膜细胞、软骨细胞、滑膜巨噬细胞或滑膜成纤维细胞被基因编辑,以降低il
‑
1α、il
‑
1β或il
‑
1α与il
‑
1β两个的表达。
9.在某些实施方式中,所述基因编辑使在包含哺乳动物关节的至少一部分细胞中一个或多个细胞因子和/或生长因子基因的表达被沉默或降低。在某些情况下,所述细胞是滑膜细胞(synovial cells和/或synoviocytes)。在某些情况下,所述细胞是滑膜成纤维细
胞。在某些情况下,所述细胞是滑膜细胞(synovial cells和/或synoviocytes)。在某些情况下,所述细胞是软骨细胞。在某些情况下,所述细胞是滑膜巨噬细胞。
10.在某些实施方式中,所述一个或多个细胞因子和/或生长因子基因选自由il
‑
1α和il
‑
1β组成的组。
11.在某些实施方式中,所述基因编辑包括使用可编程核酸酶,所述可编程核酸酶在所述一个或多个细胞因子和/或生长因子基因处介导双链或单链断裂的产生的。
12.在某些实施方式中,所述基因编辑包含选自crispr法、tale法、锌指法及其组合的一种或多种方法。
13.在某些实施方式中,所述基因编辑包含crispr法。
14.在某些实施方式中,所述crispr法是crispr
‑
cas9法。
15.在某些实施方式中,所述基因编辑包含tale法。
16.在某些实施方式中,所述基因编辑包含锌指法。
17.在某些实施方式中,所述基因编辑使一个或多个细胞因子和/或生长因子基因包含所述关节的至少一部分细胞中的表达被沉默或降低。在某些实施方式中,所述一部分被编辑的细胞是滑膜细胞(synovial cells和/或synoviocytes)。在一种情况下,所述一部分被编辑的细胞是滑膜成纤维细胞。在某些实施方式中,所述一部分被编辑的细胞是滑膜细胞(synovial cells和/或synoviocytes)。在某些实施方式中,所述一部分被编辑的细胞是软骨细胞。在某些实施方式中所述一部分被编辑的细胞是滑膜巨噬细胞。
18.在某些实施方式中,使用腺相关病毒(aav)递送系统递送所述基因编辑系统。在某些实施方式中,所述aav递送系统被注射到关节中。
19.本发明的某些方面提供了一种用于治疗或预防关节疾病或病症的药物组合物,其包含基因编辑系统和可药用载体。在一种情况下,所述基因编辑系统包含靶向一个或多个基因座的一种或多种核酸,所述基因座选自由il
‑
1α、il
‑
1β、tnf
‑
α、il
‑
6、il
‑
8和il
‑
18组成的组。
20.一个实施方式提供了一种治疗犬跛足的方法,所述方法包括施用基因编辑组合物,其中所述组合物使在跛足关节的一部分滑膜细胞、软骨细胞、滑膜巨噬细胞或滑膜成纤维细胞中il
‑
1α和il
‑
1β的表达被沉默或降低。
21.在某些实施方式中,上述方法还包括在本文描述的任何方法和组合物中叙述的一个或多个特点。
附图说明
22.将参考附图进一步解释当前公开的实施方式。示出的附图不一定按比例绘制,而是通常将重点放在说明当前公开的实施方式的原理上。
23.图1a示出了用0.5μg spycas9(truecut
tm cas9蛋白v2,thermofisher scientific)和靶向il1a基因(#43
‑
46)和il1b基因(#47
‑
50)的200ng硫代磷酸酯修饰的单一指导(sg)rnas在体外切割的针对小鼠il1a和il1b基因设计的100ng小鼠dna(gblocks,integrated dna technologies)的琼脂糖凝胶电泳分析;图1b示出了用0.5μg saucas9(genesnipper
tm cas9,biovision)和针对il1a(#51
‑
53)和il1b(#54
‑
56)基因的200ng硫代磷酸酯修饰的指导sgrnas切割的针对小鼠il1a和il1b基因设计的100ng小鼠dna(gblocks,
integrated dna technologies)的琼脂糖凝胶电泳分析。
24.图2a
–
2d示出的图展现了与在j774.2(“j”)和nih3t3(“n”)细胞中的多种向导rna一起,spycas9和saucas9使用编辑效率;图2a:在两个细胞系nih 3t3(“n”)和j774.2(“j”)中,在两个独立的合并物(合并物1和2)中用4x sgrnas(spy cas9)编辑的il1a的体内切割;图2b:在两个细胞系nih 3t3(“n”)和j774.2(“j”)中,在两个独立的合并物(合并物1和2)中用4x sgrnas(spy cas9)编辑的il1b的体内切割;图2c:在两个细胞系nih 3t3(“n”)和j774.2(“j”)中,在两个独立的合并物(合并物1和2)中用3x sgrna(sau cas9)编辑的il1a的体内切割;图2d:在两个细胞系nih 3t3(“n”)和j774.2(“j”)中,在两个独立的合并物(合并物1和2)中用3x sgrnas(sacas9)编辑的il1b的体内切割;编辑效率使用每个合并物的sanger测序迹线(ice tool,synthego)的反卷积来确定。
25.图3示出了使用ivis系统测量的gfp表达。通量值是基于以动物的被注射的膝关节为中心的感兴趣区域。数据被呈现为每组四个样本的平均值(sd)。
26.正如在讨论中说明的,当上述被定义的附图阐述了目前公开的实施方式,其他实施方式同样也被考虑。本公开以代表而非限制的方式展现示例性方式。本领域技术人员可以设计出多种其他的落入当前公开实施方式保护范围和原则精神的修改和实施方式。
27.发明详述
28.当在本文中使用时,本发明的实施方式提供了用于改善关节功能和治疗关节疾病的组合物和方法。在特定实施方式中,提供了对滑膜成纤维细胞、滑膜细胞、软骨细胞或滑膜巨噬细胞进行基因编辑,以降低炎性细胞因子例如il
‑
1α、il
‑
1β、tnf
‑
α、il
‑
6、il
‑
8、il
‑
18、一种或多种基质金属蛋白酶(mmps)或nlrp3炎症小体的一种或多种成分的表达的组合物和方法。实施方式被用于治疗骨关节炎和其他炎性关节疾病。实施方式还可用于治疗由骨关节炎造成的犬跛足。实施方式还可用于治疗由关节疾病造成的马跛足。实施方式还可用于治疗创伤后关节炎、痛风、假性痛风和其他炎症介导或免疫介导的关节疾病。
29.定义
30.除非另有定义,否则本文中使用的所有技术和科学术语具有与本发明所属领域的技术人员通常理解的相同的含义。本文中提到的所有专利和出版物整体通过参考并入本文。
31.术语“体内”是指发生在受试者身体内的事件。
32.术语“体外”是指发生在受试者身体外的事件。体外测定法涵盖使用活细胞或死细胞的基于细胞的测定法,并且也可以涵盖不使用完整细胞的无细胞测定法。
33.术语“离体”是指涉及对已从受试者身体取出的细胞、组织和/或器官进行处理或执行程序的事件。在恰当情况下,可以在手术或治疗方法中将所述细胞、组织和/或器官返回到所述受试者的身体。
34.术语“il
‑
1”(在本文中也被称为“il1”)是指被称为白介素
‑
1的促炎性细胞因子,并包含所有形式的il
‑
1,包括il1
‑
α和il
‑
1β、人类和哺乳动物形式、保守氨基酸替换、糖型、生物类似物及其变体。il
‑
1α和il
‑
1β结合到相同的受体分子,其被称为i型il
‑
1受体(il
‑
1ri)。这种受体存在第三个配体:白介素1受体拮抗剂(il
‑
1ra),其不激活下游信号传导,因此通过与il
‑
1α和il
‑
1β竞争所述受体的结合位点而充当il
‑
1α和il
‑
1β信号传导的抑制剂。参见例如dinarello,blood 117:3720
–
32(2011)和weber等,science signaling 3(105):
cm1,doi:10.1126/scisignal.3105cm1。il
‑
1被描述,例如,在dinarello,cytokine growth factor rev.8:253
‑
65(1997)中,其公开内容通过参考并入本文。例如,所述术语il
‑
1涵盖了人类,重组形式的il
‑
1。
35.表1.白介素的氨基酸序列
36.涵盖在哺乳动物、特别是人类、犬科动物、猫科动物或马科动物中对疾病的任何治疗,并包括:(a)在可能易患所述疾病但尚未被诊断为患有所述疾病的受试者中阻止所述疾病的发生;(b)抑制所述疾病,即阻止其发展或进展;和(c)缓解所述疾病,即引起所述疾病的消退和/或缓解一种或多种疾病症状。“治疗”也意味着涵盖递送药剂以便提供药理效果,即使在不存在疾病或病症的情况下。例如,“治疗”涵盖在不存在疾病病症的情况下递送可以引发免疫应答或赋予免疫力的组合物,例如在疫苗的情况下。应该理解,本发明的组合物和方法适用于治疗所有哺乳动物,包括但不限于人类、犬科动物、猫科动物、马科动物和牛科动物受试者。
43.在用于指称核酸或蛋白质的部分时,术语“异源的”表示所述核酸或蛋白质包含两个或更多个在自然界中彼此不以相同关系存在的子序列。例如,所述核酸通常是重组产生的,具有来自于不相关基因的两个或更多个序列,它们被排列成新的功能性核酸,例如来自于一个来源的启动子和来自于另一个来源的编码区或来自于不同来源的多个编码区。类似地,异源蛋白表示所述蛋白质包含两个或更多个在自然界中彼此不以相同关系存在的子序列(例如融合蛋白)。
44.在两个或更多个核酸或多肽的情形中,术语“序列同一性”、“同一性百分比”和“序列同一性百分比”(或其同义语例如“99%同一的”)是指两个或更多个序列或子序列在最大对应的比较和比对(如有必要,引入空位)时是相同的,或具有特定百分率的核苷酸或氨基酸残基是相同的,不考虑任何保守的氨基酸替换作为序列同一性的一部分。同一性百分比可以使用序列比较软件或算法或通过目测检查来测量。可用于获得氨基酸或核苷酸序列的比对的各种不同算法和软件在本领域中是已知的。适合于确定序列同一性百分比的程序包括例如可以从美国政府的国家生物技术信息中心blast网站获得的blast程序套件。两个序列之间的比较可以使用blastn或blastp算法来进行。blastn被用于比较核酸序列,而blastp被用于比较氨基酸序列。可以从dnastar获得的align、align
‑
2(genentech,south san francisco,california)或megalign,是可用于比对序列的其他可公开获得的软件程序。clustalw和clustalx可用于产生比对,larkin等,bioinformatics 23:2947
‑
2948(2007);goujon等,nucleic acids research,38suppl:w 695
‑
9(2010);以及mcwilliam等,nucleic acids research 41(网络服务器版):w 597
‑
600(2013)。本领域技术人员可以通过特定比对软件确定用于最大比对的适合参数。在某些实施方式中,使用比对软件的默认参数。
45.当在本文中使用时,术语“变体”包括但不限于抗体或融合蛋白,其包含的氨基酸序列通过在参比抗体的氨基酸序列内或附近的某些位置中的一个或多个替换、缺失和/或添加的方法而不同于所述参比抗体的氨基酸序列。与参比抗体的氨基酸序列相比,所述变体可以在其氨基酸序列中包含一个或多个保守替换。保守替换可以包括例如带有相似电荷或不带电荷的氨基酸的替换。所述变体保留与所述参比抗体的抗原特异性结合的能力。术语变体还包括聚乙二醇化的抗体或蛋白质。
46.当在本文中使用时,“载体”或“介质”是指适合于药物施用的载体材料。在本文中有用的载体和介质包括本领域中已知的任何此类材料,例如无毒并且不以有害方式与所述组合物的其他组分相互作用的任何液体、凝胶、溶剂、液体稀释剂、增溶剂、表面活性剂等。
47.短语“可药用的”是指在健全的医学判断范围内,适合与人类和动物的组织相接触
使用而没有过度毒性、刺激性、过敏反应或与合理的利益/风险比相称的其他问题或并发症的化合物、材料、组合物和/或剂型。
48.术语“可药用载体”或“可药用赋形剂”打算包括任何和所有的溶剂、分散介质、包衣、抗细菌和抗真菌剂、等渗和吸收延迟剂以及惰性成分。此类可药用载体或可药用赋形剂用于活性药物成分在本领域中是公知的。除非任何常规的可药用载体或可药用赋形剂与所述活性药物成分不相容,否则其在本发明的治疗性组合物中的使用均可考虑。其他的活性药物成分例如其他药物,也可以并入到所描述的组合物和方法中。
49.术语“可药用赋形剂”打算包括能够与化合物共同施用以促进其目标功能的表现的介质和载体。此类介质在药物活性物质中的使用在本领域中是公知的。此类介质和载体的实例包括溶液、溶剂、分散介质、延迟剂、乳液等。适用于多结合性化合物的任何其他常规载体也在本公开的范围之内。
50.当在本文中使用时,没有具体数目的指称通常被解释为涵盖单数和复数形式两个。
51.术语“约”和“大约”意味着在值的统计上有意义的范围内。这样的范围可以在给定值或范围的一个数量级内,优选地在给定值或范围的50%以内,更优选地20%以内,更优选地10%以内,甚至更优选地5%以内。术语“约”或“大约”所涵盖的容许变化取决于所研究的特定系统,并且可以被本领域普通技术人员容易地理解。此外,当在本文中使用时,术语“约”和“大约”意味着组成、量、配方、参数、形状和其他数量和特征不是且不必是精确的,而是根据需要可以是近似的和/或更大或更小,反映出公差、换算因数、四舍五入、测量误差等以及本领域技术人员已知的其他因素。通常,维度、尺寸、配方、参数、形状或其他数量或特征是“约”或“大约”的,无论是否明确陈述。应该指出,尺寸、形状和维度非常不同的实施方式可以利用所描述的布置。
52.当在本文中使用时,术语“基本上”可以是指大部分或大多数,例如至少约50%、60%、70%、80%、90%、95%、96%、97%、98%、99%、99.5%、99.9%、99.99%或至少约99.999%或更多。
53.当在原始和修改形式的随附的权利要求书中使用时,过渡性术语“包含”、“基本上由
……
组成”和“由
……
组成”,就哪些未叙述的附加权利要求要素或步骤(如果有的话)被排除在权利要求书的范围之外定义了所述权利要求书的范围。术语“包含”打算是包含性或开放式的,不排除任何额外的、未叙述的要素、方法、步骤或材料。术语“由
……
组成”排除权利要求书中指定的之外的任何要素、步骤或材料,并且在后一种情况下,排除通常与所述指定的材料相关的杂质。术语“基本上由
……
组成”将权利要求书的范围限制到所述指定的要素、步骤或材料以及不实质性影响要求保护的发明的基本和新颖特征的那些要素、步骤或材料。在可选实施方式中,本文中描述的体现本发明的所有组合物、方法和药剂盒,均可以用任何过渡性术语“包含”、“基本上由
……
组成”和“由
……
组成”更具体地定义。
[0054]“关节疾病”被定义为关节的细胞或组织中可能使疾病的可测量的异常,例如在关节中引发解剖学和/或生理变化的代谢和分子紊乱。包括但不限于关节间隙变窄、软骨下硬化、软骨下囊肿和骨赘形成的放射学检测。
[0055]“关节病患”在人类受试者中被定义为驱使受试者寻求医疗干预的症状,例如受试者报告的疼痛、僵硬、肿胀或不能活动。对于非人类哺乳动物来说,“关节病患”被定义为例
如跛足、步态、负重、异常性疼痛或探索性行为的可观察的变化。
[0056]
当在本文中使用时,sgrna(单一向导rna)是由靶向序列和支架组成的rna,优选为合成rna。它用于在基因组工程实验中将cas9引导至特定基因组基因座。sgrna可以被施用或配制,例如作为合成rna或作为包含编码grna的序列的核酸,其然后在靶细胞中表达。
[0057]
当在本文中使用时,“cas9”是指crispr相关蛋白;cas9核酸酶是用于ii型crispr系统的活性酶。“ncas9”是指两个核酸酶结构域之一、即ruvc或hnh结构域被失活的cas9。ncas9只能切割靶dna的一条链(“切口酶”)。
[0058]
当在本文中使用时,“pam”是指前间区序列邻近基序,是cas9结合靶dna所必需的,并且紧跟在所述靶序列之后。所述cas9可以被施用或配制,例如作为蛋白质(例如重组蛋白)或作为包含编码cas9蛋白的序列的核酸,其然后在靶细胞中表达。
[0059]
通过本文中描述的任何方法或组合物治疗的受试者可以是任何年龄,并且可以是成人、婴儿或儿童。在某些情况下,所述受试者是0、1、2、3、4、5、6、7、8、9、10、11、12、13、14、15、16、17、18、19、20、21、22、23、24、25、26、27、28、29、30、31、32、33、34、35、36、37、38、39、40、41、42、43、44、45、46、47、48、49、50、51、52、53、54、55、56、57、58、59、60、61、62、63、64、65、66、67、68、69、70、71、72、73、74、75、76、77、78、79、80、81、82、83、84、85、86、87、88、89、90、91、92、93、94、95、96、97、98或99岁,或在其中的范围之内(例如但不限于2至20岁之间、20至40岁之间或40至90岁之间)。所述受试者可以是人类或非人类受试者。可以从本公开的组合物和方法获益的受试者的特定类别包括年龄超过40、50或60岁的受试者。可以从本公开的组合物和方法获益的另一类受试者是患有关节炎(例如骨关节炎)的受试者。
[0060]
可以将本文公开的任何组合物施用到非人类受试者,例如实验室或农场动物。非人类受试者的非限制性实例包括实验室或研究动物、宠物、野生或驯养动物、农场动物等,例如狗、山羊、豚鼠、仓鼠、小鼠、猪、非人类灵长动物(例如大猩猩、猿、猩猩、狐猴、狒狒等)、大鼠、绵羊、马、奶牛等。
[0061]
本发明提供了可用于治疗具有炎性成分的关节障碍的组合物。在某些情况下,所述组合物可用于在哺乳动物关节中阻止骨关节炎的进展和治疗骨关节炎。
[0062]
在某些情况下,所述药物组合物包含基因编辑系统,其中所述基因编辑系统使至少一个与关节功能相关的遗传基因座在至少一部分包括关节的细胞中的表达被沉默或降低。
[0063]
在一种情况下,所述药物组合物包含基因编辑系统,其中所述基因编辑系统靶向il
‑
1α和il
‑
1β中的一个或多个。在某些情况下,所述药物组合物包含基因编辑系统,其中所述基因编辑系统靶向tnf
‑
α、il
‑
6、il
‑
8、il
‑
18、基质金属蛋白酶(mmp)或nlrp3炎症小体的组分中的一个或多个。
[0064]
在某些情况下,所述药物组合物包含基因编辑系统,其中所述基因编辑包括使用可编程核酸酶,所述可编程核酸酶在所述至少一个与关节功能相关的基因座处介导双链或单链断裂的产生。在某些实施方式中,所述基因编辑系统降低所述靶基因座或靶位点的基因表达。在某些实施方式中,所述与关节组织相关的至少一个基因座在所述至少一部分包含关节的细胞中被沉默或降低。
[0065]
在某些情况下,所述包含所述关节的细胞是滑膜细胞。在某些情况下,所述细胞是滑膜巨噬细胞。在某些情况下,所述细胞是滑膜成纤维细胞。在某些情况下,至少一部分所
述滑膜细胞被编辑。在某些情况下,所述包含关节的细胞是软骨细胞。
[0066]
在某种情况下,所述药物组合物靶向所述一个或多个细胞因子和/或生长因子基因,其选自由il
‑
1α、il
‑
1β、tnf
‑
α、il
‑
6、il
‑
8、il
‑
18、基质金属蛋白酶(mmp)或nlrp3炎症小体的组分组成的组。在某些实施方式中,所述nlrp3炎症小体的组分包括nlrp3、asc(含有card的凋亡相关斑点样蛋白)、半胱天冬酶
‑
1及其组合。
[0067]
还提供了药物组合物,其中所述基因编辑使一个或多个细胞因子和/或生长因子基因在至少一部分包含关节的细胞中的表达被增强,所述细胞因子和/或生长因子基因选自由il
‑
1ra、timp
‑
1、timp
‑
2、timp
‑
3、timp
‑
4及其组合组成的组。
[0068]
在某些实施方式中,所述药物组合物提供基因编辑,其中所述基因编辑包括使用可编程核酸酶,所述可编程核酸酶在所述一个或多个细胞因子和/或生长因子基因处介导双链或单链断裂的产生。在某些实施方式中,所述基因编辑包括选自crispr法、tale法、锌指法及其组合的一种或多种方法。
[0069]
在一种情况下,所述基因编辑包括crispr法。在其他情况下,所述crispr法是crispr
‑
cas9法。在某些情况下,所述cas9被突变以增强功能。
[0070]
骨关节炎的动物模型
[0071]
在本领域中已知几种用于骨关节炎的动物模型。概述了示例性而非限制性的动物模型;然而应该理解,可以使用各种不同的模型。许多不同物种的动物被用于模拟oa,例如已对小鼠、大鼠、兔、豚鼠、狗、猪、马和甚至其他动物进行了研究。参见例如kuyinu等,j orthop surg res.11:19(2016)(在后文中被称为“kuyinu,2016”)。
[0072]
应该理解,用于诱导oa的各种不同方法可用于任何哺乳动物中。在小鼠中,常使用自发、化学诱导、手术诱导和非侵入性诱导。例如kuyinu,2016;bapat等,clin transl med.7:36(2018)(在后文中被称为“bapat,2018”);和poulet,curr rheumatol rep 18:40(2016)。在马中,常使用骨骼软骨碎片运动模型、化学诱导、创伤诱导和过度使用诱导。在绵羊中,手术诱导最为常见;在豚鼠中,常使用手术诱导、化学诱导和自发(durkin hartley)方法。例如bapat,2018。
[0073]
去稳定化内侧半月板(dmm)常用于在小鼠中模拟创伤后骨关节炎,例如culley等,methods mol biol.1226:143
‑
73(2015)。所述dmm模型模拟临床半月板损伤,这是人类oa发展的已知易感因素,并允许研究疾病过程中的结构和生物学变化。小鼠是有吸引力的模型生物,因为可以使用具有确定遗传背景的小鼠株系。此外,可以使用敲除或其他遗传操作过的小鼠株系来评估各种不同分子途径在对各种不同oa治疗方式和方案做出响应中的重要性。例如,str/ort小鼠具有使所述株系特别容易发生oa的特点,包括炎性细胞因子il1β的水平提高,bapat等,clin transl med.7:36(2018)。这些小鼠常常在膝、踝、肘和颞下颌关节中发展出oa,jaeger等,osteoarthritis cartilage16:607
–
614(2018)。其他有用的小鼠突变株系对专业技术人员来说是已知的,例如col9a1(
‑
/
‑
)小鼠,allen等,arthritis rheum,60:2684
–
2693(2009)。
[0074]
oa的另一种常用手术模型是前交叉韧带横断(aclt)模型。little和hunter,nat rev rheumatol.,9(8):485
–
497(2013)。所述受试者的acl被手术横断,使关节失稳。所述弯曲关节的前抽屉试验被用于确认韧带的横断已经发生。在某些情况下,可以横断其他韧带例如后交叉韧带、内侧副韧带、外侧副韧带和/或任一个半月板。与dmm模型一样,可以使用
各种不同小鼠株系来研究各种不同分子途径。
[0075]
取决于技术目标,可以选择使用尺寸不同的动物。啮齿动物是有用的,因为骨骼成熟所需的时间短,因此在手术或诱导oa的其他技术后发生oa的时间较短。大型动物对于评估治疗干预特别有用。大型动物的解剖结构与人类非常相似;例如,在狗中,软骨厚度不到人类厚度的约一半;这种惊人的相似性示例了为什么这种软骨退化和骨骼软骨缺损研究在大型动物模型中远远更加有用。例如,mccoy,vet.pathol.,52:803
‑
18(2015);和pelletier等,therapy,7:621
–
34(2010)。
[0076]
基因编辑过程
[0077]
概述:对滑膜细胞进行基因编辑的组合物
[0078]
本发明的实施方式涉及对滑膜细胞进行基因编辑的方法,所述方法包括对关节中的至少一部分所述滑膜细胞进行基因编辑的一个或多个步骤,以治疗骨关节炎或其他关节障碍。当在本文中使用时,“基因编辑”和“基因组编辑”是指一种类型的遗传修饰,其中将细胞基因组中的dna永久修饰,例如在所述细胞的基因组内进行dna插入、缺失、修饰或替换。在某些实施方式中,基因编辑使dna序列的表达被沉默(有时被称为基因敲除)或抑制/降低(有时被称为基因敲减)。在其他实施方式中,基因编辑使dna序列的表达被增强(例如通过引起过表达)。根据本发明的实施方式,基因编辑技术被用于降低促炎性基因的表达或沉默促炎性基因和/或增强再生性基因的表达。
[0079]
白介素
[0080]
根据其他实施方式,本发明的基因编辑方法可用于提高某些白介素例如il
‑
1α、il
‑
1β、il
‑
4、il
‑
6、il
‑
8、il
‑
9、il
‑
10、il
‑
13、il
‑
18和tnf
‑
α中的一个或多个的表达。已证实某些白介素在关节组织中增强炎性反应并与疾病进展有关联。
[0081]
表达构建物
[0082]
编码向导rna和/或cas9编辑酶中的一者或两个的表达构建物可以在任何有效载体,例如能够在体内将组分基因有效递送到细胞的任何制剂或组合物中施用。方法包括例如电穿孔和/或将所述基因插入到包括重组反转录病毒、腺病毒、腺相关病毒、慢病毒和单纯性疱疹病毒
‑
1在内的病毒载体或重组细菌或真核质粒中。病毒载体直接转染细胞;质粒dna可以裸露地或在例如阳离子脂质体(lipofectamine)或衍生(例如抗体偶联的)、聚赖氨酸偶联物、短杆菌肽s、人工病毒包膜或其他此类细胞内载体的帮助下递送,以及所述基因构建物的直接注射或在体内进行的capo4沉淀。
[0083]
核酸在细胞中的体内导入的优选方法是利用含有核酸例如cdna的病毒载体。用病毒载体感染细胞的优点在于大部分靶细胞可以接受所述核酸。此外,所述病毒载体内,例如由所述病毒载体中包含的cdna编码的分子,在已摄取病毒载体核酸的细胞中高效表达。
[0084]
反转录病毒载体和腺相关病毒载体可用作重组基因递送系统,用于在体内转移外源基因,特别是转移到人类中。这些载体提供基因在细胞中的高效递送。在某些情况下,被转移的核酸稳定地整合到宿主的染色体dna中。在其他情况下,特别是对于腺相关病毒载体而言,在宿主dna中的稳定整合可能是稀有事件,使所述转入基因的游离体表达和转入基因的瞬时表达。
[0085]
仅产生复制缺陷型反转录病毒的特殊细胞系(被称为“包装细胞”)的开发增加了反转录病毒在基因疗法中的应用,并且已表征了出于基因疗法目的用于基因转移的缺陷型
反转录病毒(综述参见miller,blood 76:271(1990))。复制缺陷型反转录病毒可以被包装成病毒粒子,其可以通过标准技术,通过使用辅助病毒而用于感染靶细胞。产生重组反转录病毒和使用此类病毒在体外或体内感染细胞的方案可以在ausubel等主编,《分子生物学现代方法》(current protocols in molecular biology),greene publishing associates,(1989),第9.10
‑
9.14节和其他标准实验室手册中找到。适合的反转录病毒的实例包括本领域技术人员已知的plj、pzip、pwe和pem。用于制备亲嗜性和双嗜性反转录病毒系统两个的适合的包装病毒系的实例包括ψcrip、ψcre、ψ2和ψam。反转录病毒已被用于在体外和/或体内将各种不同基因导入到包括上皮细胞在内的许多不同细胞类型中(参见例如eglitis等,(1985)science 230:1395
‑
1398;danos和mulligan,(1988)proc.natl.acad.sci.usa 85:6460
‑
6464;wilson等,(1988)proc.natl.acad.sci.usa85:3014
‑
3018;armentano等,(1990)proc.natl.acad.sci.usa87:6141
‑
6145;huber等,(1991)proc.natl.acad.sci.usa88:8039
‑
8043;ferry等,(1991)proc.natl.acad.sci.usa 88:8377
‑
8381;chowdhury等,(1991)science 254:1802
‑
1805;van beusechem等,(1992)proc.natl.acad.sci.usa 89:7640
‑
7644;kay等,(1992)human gene therapy 3:641
‑
647;dai等,(1992)proc.natl.acad.sci.usa89:10892
‑
10895;hwu等,(1993)j.immunol.150:4104
‑
4115;美国专利号4,868,116;美国专利号4,980,286;pct申请wo 89/07136;pct申请wo 89/02468;pct申请wo 89/05345;pct申请wo 92/07573,每个所述参考文献为所有目的整体通过参考并入本文)。
[0086]
在本发明中有用的另一种病毒基因递送系统利用腺病毒衍生载体。可以对腺病毒的基因组进行操作,使其编码和表达感兴趣的基因产物,但就其在正常的病毒裂解生命周期中复制的能力而言被失活。参见例如berkner等,biotechniques 6:616(1988);rosenfeld等,science252:431
‑
434(1991);和rosenfeld等,cell 68:143
‑
155(1992)。适合的腺病毒载体可以源自于任何腺病毒毒株(例如ad2、ad3、ad5或ad7等),包括本领域技术人员已知的来自于其他物种(例如小鼠、狗、人类等)的腺病毒血清型。病毒粒子相对稳定,易于纯化和浓缩,并且如上所述可以被修饰以影响感染谱。此外,引入的腺病毒dna(和其中包含的外来dna)不整合到宿主细胞的基因组中,而是保持游离状态,从而避免了作为原位插入诱变的结果可能发生的潜在问题,在后一种情况下引入的dna变得整合到宿主基因组中(例如反转录病毒dna)。此外,相对于其他基因递送载体,腺病毒基因组对外来dna的承载能力很大(高达8千碱基)(berkner等,同上;haj
‑
ahmand和graham,j.virol.57:267(1986)。
[0087]
也可以产生除了在病毒dna的每个末端处的dna复制原点以及在左侧包装信号下游的基因组的5'
‑
末端处的包装信号之外所有腺病毒序列均被缺失的辅助病毒依赖性(hdad)载体。hdad载体在具有复制能力的辅助腺病毒存在下构建和繁殖,所述辅助腺病毒提供复制所需的必要早期和晚期蛋白。
[0088]
可用于核酸递送的另一种病毒载体系统是腺相关病毒(aav)。腺相关病毒是一种天然存在的缺陷病毒,其需要另一种病毒例如腺病毒或疱疹病毒作为辅助病毒才能实现高效复制和生产性生命周期。(综述参见muzyczka等,curr.topics in micro.and immunol.158:97
‑
129(1992)。它也是可以将其dna整合到非分裂细胞中,并表现出高频稳定整合的少数几种病毒之一(参见例如flotte等,am.j.respir.cell.mol.biol.7:349
‑
356(1992);samulski等,j.virol.63:3822
‑
3828(1989);和mclaughlin等,j.virol.62:1963
‑
1973(1989))。包含少至300个碱基对的aav的载体可以被包装并且可以整合。外源dna的空间被限制到约4.5kb。如在tratschin等,mol.cell.biol.5:3251
‑
3260(1985)中描述的aav载体可用于将dna引入到细胞中。已使用aav载体将各种不同的核酸引入到不同细胞类型中(参见例如hermonat等,proc.natl.acad.sci.usa 81:6466
‑
6470(1984);tratschin等,mol.cell.biol.4:2072
‑
2081(1985);wondisford等,mol.endocrinol.2:32
‑
39(1988);tratschin等,j.virol.51:611
‑
619(1984);和flotte等,j.biol.chem.268:3781
‑
3790(1993))。可以被包装在在体内高度稳定有效、易于生产、获得fda批准并在多项临床试验中测试过的腺相关病毒(aav)载体中的金黄色葡萄球菌(sacas9)和其他更小的cas9酶的鉴定,为治疗性基因编辑铺平了新的道路。
[0089]
在某些实施方式中,将编码crispr il
‑
1α或il
‑
1β基因编辑复合体(例如cas9或grna)的核酸包裹在表面带有正电荷的脂质体(例如lipofectin)中,所述脂质体可以用针对靶细胞的细胞表面抗原的抗体标记。这些递送载体也可用于递送cas9蛋白/grna复合体。
[0090]
在临床环境中,用于编码crispr il
‑
1α或il
‑
1β基因编辑复合体的核酸的基因递送系统,可以通过各自在本领域中熟知的多种方法中的任一种引入到受试者中。例如,基因递送系统的药物制剂可以被系统性引入,例如通过静脉内注射,并且所述蛋白质在靶细胞中的特异性转导的发生主要是由于由基因递送载体提供的转染特异性,由控制受体基因的表达的转录调控序列造成的细胞类型或组织类型表达,或其组合。在其他实施方式中,编码crispr il
‑
1α或il
‑
1β基因编辑复合体的核酸的初始递送更为有限,其中在所述受试者中的引入相当局部。例如,可以将所述编码crispr il
‑
1α或il
‑
1β基因编辑复合体的核酸通过关节内注射引入到表现出关节疾病(例如骨关节炎)的关节中。在某些实施方式中,所述编码crispr il
‑
1α或il
‑
1β基因编辑复合体的核酸在手术期间或之后施用;在某些实施方式中,包含所述编码crispr il
‑
1α或il
‑
1β基因编辑复合体的核酸的受控释放水凝胶在手术结束时在闭合之前施用,以通过随时间提供编码crispr il
‑
1α或il
‑
1β基因编辑复合体的核酸的稳定剂量来防止减轻或消除骨关节炎。
[0091]
所述编码crispr il
‑
1α或il
‑
1β基因编辑复合体的核酸的药物制剂可以基本上由可接受的稀释剂中的基因递送系统(例如病毒载体)组成,或者可以包含其中包埋有基因递送载体的缓释基质。可选地,在完整的基因递送系统可以从重组细胞,例如腺病毒载体,完整产生的情况下。所述药物制剂可以包含产生所述基因递送系统的一个或多个细胞。
[0092]
优选地,所述crispr il
‑
1α或il
‑
1β编辑复合体是特异性的,即偏好性地在靶位点(il
‑
1α或il
‑
1β)处诱导基因组改变,并且不在其他位点处诱导改变,或很少在其他位点处诱导改变。在某些实施方式中,所述crispr il
‑
1α或il
‑
1β编辑复合体具有至少50%、至少60%、至少70%、至少80%、至少90%、至少95%或至少99%的编辑效率。在某些实施方式中,可以修饰向导rna(例如单一向导rna)的序列,以提高编辑效率和/或减少脱靶效应。在某些实施方式中,所述向导rna的序列可以与靶序列相差约1个碱基、约2个碱基、约3个碱基、约4个碱基、约5个碱基、约5个碱基、约6个碱基、约7个碱基、约8个碱基、约9个碱基、约10个碱基、约15个碱基或超过约15个碱基。在某些实施方式中,所述向导rna的序列可以与靶序列相差约1%、约2%、约3%、约4%、约5%、约6%、约7%、约8%、约9%、约10%、约11%、约12%、约13%、约14%、约15%、约16%、约17%、约18%、约19%、约20%或超过约20%。当在本文中使用时,与靶序列相比的变动可以是指互补性程度。
[0093]
基因编辑方法
[0094]
正如上文讨论的,本发明的实施方式提供了治疗关节障碍的组合物和方法,其中为了治疗关节障碍,通过基因编辑对一部分所述关节细胞进行遗传修饰。本发明的实施方式包括通过向滑膜细胞群体中的核苷酸插入(rna或dna)或重组蛋白插入进行遗传编辑,用于促进一种或多种蛋白质的表达和抑制一种或多种蛋白质的表达两个及其组合。本发明的实施方式还提供了用于将基因编辑组合物递送到关节细胞,特别是将基因编辑组合物递送到滑膜细胞的方法。有几种基因编辑技术可用于遗传修饰关节细胞,这些技术适合根据本发明使用。
[0095]
在某些实施方式中,遗传修饰关节细胞的方法包括稳定地并入用于产生一种或多种蛋白质的基因的步骤。在一个实施方式中,对一部分关节滑膜细胞进行遗传修饰的方法包括反转录病毒转导的步骤。在一个实施方式中,对一部分关节滑膜细胞进行遗传修饰的方法包括慢病毒转导的步骤。慢病毒转导系统在本领域中是已知的,并描述在例如levine等,proc.nat’l acad.sci.2006,103,17372
‑
77;zufferey等,nat.biotechnol.1997,15,871
‑
75;dull等,j.virology 1998,72,8463
‑
71和美国专利号6,627,442中,每个所述文献的公开内容通过参考并入本文。在一个实施方式中,对一部分关节滑膜细胞进行遗传修饰的方法包括γ
‑
反转录病毒转导的步骤。γ
‑
反转录病毒转导系统在本领域中是已知的,并描述在例如cepko和pear,cur.prot.mol.biol.1996,9.9.1
‑
9.9.16中,其公开内容通过参考并入本文。在一个实施方式中,对一部分关节滑膜细胞进行遗传修饰的方法包括转座子介导的基因转移的步骤。转座子介导的基因转移系统在本领域中是已知的,并包括其中转座酶被提供为dna表达载体,或提供为可表达的rna或蛋白质以便在转基因细胞中不发生转座酶的长期表达的系统,例如转座酶被提供为mrna(例如包含帽子结构和poly
‑
a尾的mrna)。适合的转座子介导的基因转移系统,包括鲑鱼型tel样转座酶(sb或睡美人转座酶)例如sb10、sb11和sb100x,以及具有提高的酶活性的工程化酶,被描述在例如hackett等,mol.therapy 2010,18,674
‑
83和美国专利号6,489,458中,每个所述文献的公开内容通过参考并入本文。
[0096]
在某些情况下,使用病毒载体或系统将基因编辑系统引入到包含关节的细胞中。在某些情况下,所述细胞是滑膜成纤维细胞。在某些情况下,所述病毒载体是aav载体。在某些情况下,所述aav载体包含选自下述的血清型:aav1,aav1(y705 731f t492v),aav2(y444 500 730f t491v),aav3(y705 731f),aav4,aav5,aav5(y436 693 719f),aav6,aav6(vp3变体y705f/y731f/t492v),aav
‑
7m8,aav8,aav8(y733f),aav9,aav9(vp3变体y731f),aav10(y733f),aav
‑
shh10和aav
‑
dj/8。在某些情况下,所述aav载体包含选自下述的血清型:aav1,aav5,aav6,aav6(y705f/y731f/t492v),aav8,aav9和aav9(y731f)。
[0097]
在某些情况下,所述病毒载体是慢病毒。在一种情况下,所述慢病毒选自下述组:人免疫缺陷病毒
‑
1(hiv
‑
1),人免疫缺陷病毒
‑
2(hiv
‑
2),猴免疫缺陷病毒(siv),猫免疫缺陷病毒(fiv),牛免疫缺陷病毒(biv),jembrana病病毒(jdv),马传染性贫血病毒(eiav)和山羊关节炎脑炎病毒(caev)。
[0098]
在一个实施方式中,对一部分关节滑膜细胞进行遗传修饰的方法包括稳定地并入用于一种或多种蛋白质的产生或抑制(例如沉默)的基因的步骤。在一个实施方式中,对一部分关节滑膜细胞进行遗传修饰的方法包括脂质体转染的步骤。脂质体转染方法,例如使
用阳离子脂质n
‑
[1
‑
(2,3
‑
二油烯氧基)丙基]
‑
n,n,n
‑
三甲基氯化铵(dotma)和二油酰基磷脂酰乙醇胺(dope)在过滤过的水中的1:1(w/w)脂质体配方的方法,在本领域中是已知的,并描述在rose等,biotechniques 1991,10,520
‑
525和felgner等,proc.natl.acad.sci.usa,1987,84,7413
‑
7417以及美国专利号5,279,833、5,908,635、6,056,938、6,110,490、6,534,484和7,687,070中,每个所述文献的公开内容通过参考并入本文。在一个实施方式中,对一部分关节滑膜细胞进行遗传修饰的方法包括使用在美国专利号5,766,902、6,025,337、6,410,517、6,475,994和7,189,705中描述的方法的转染步骤,每个所述专利的公开内容通过参考并入本文。
[0099]
根据一个实施方式,所述基因编辑过程可以包括使用可编程核酸酶,所述可编程核酸酶在一个或多个免疫检查点基因处介导双链或单链断裂的产生。此类可编程核酸酶能够通过在特定基因组位点处引入断裂进行精确的基因组编辑,即它们依靠基因组内特定dna序列的识别将核酸酶结构域靶向该位置,并在所述靶序列处介导双链断裂的产生。所述dna中的双链断裂随后将内源性修复机制召集到所述断裂位点,通过非同源末端连接(nhej)或同源定向修复(hdr)介导基因组编辑。因此,断裂的修复可以使破坏(例如沉默、抑制或增强)靶基因产物的插入/缺失突变的引入。
[0100]
已开发的能够进行位点特异性基因组编辑的核酸酶的主要类别包括锌指核酸酶(zfn)、转录激活子样核酸酶(talen)和crispr相关核酸酶(例如crispr
‑
cas9)。这些核酸酶系统可以根据它们的dna识别模式大致分为两类:zfns和talens通过蛋白质
‑
dna相互作用实现特异性dna结合,而crispr系统例如cas9通过直接与靶dna碱基配对的短rna指导分子并通过蛋白质
‑
dna相互作用靶向特定dna序列。参见例如cox等,nature medicine,2015,vol.21,no.2。
[0101]
可以按照本发明的方法使用的基因编辑方法的非限制性实例包括crispr法、tale法和zfn法,它们在下文中被更详细地描述。
[0102]
crispr法
[0103]
用于治疗或预防关节疾病或病症的药物组合物包含基因编辑系统,其中所述基因编辑系统靶向至少一个与关节功能相关的基因座,其中对至少一部分关节滑膜细胞的基因编辑通过crispr法(例如crispr
‑
cas9、crispr
‑
cas13a或crispr/cpf1(也被称为crispr
‑
cas12a))进行。根据特定实施方式,使用crispr法对关节滑膜细胞进行基因编辑使在至少一部分所述关节滑膜细胞中一个或多个免疫检查点基因的表达被沉默或降低。
[0104]
crispr表示“成簇规则间隔短回文重复序列”。使用crispr系统进行基因编辑的方法在本文中也被称为crispr法。存在三种类型的将rna与cas蛋白相结合并且可以根据本发明使用的crispr系统:ii、v和vi型。ii型crispr(以cas9为例)是表征最充分的系统之一。
[0105]
crispr技术改编自细菌和古菌(单细胞微生物域)的天然防御系统。这些生物使用crispr来源的rna和包括cas9在内的各种不同cas蛋白,通过切断并破坏外来入侵者的dna或rna挫败病毒和其他外来体的攻击。crispr是特殊化的dna区域,具有两个明显特征:核苷酸重复序列和间隔区的存在。核苷酸重复序列分布在整个crispr区域中,在所述重复序列之间散布有外来dna的短区段(间隔区)。在ii型crispr
‑
cas系统中,间隔区整合在crispr基因组位点内并转录和加工成短crispr rna(crrna)。这些crrnas退火到反式激活crrnas(tracrrnas)并指导病原dna被cas蛋白的序列特异性切割和沉默。cas9蛋白的靶识别需要
technologies(grand island,ny,usa)商购。适合用于本发明的tale和talen方法描述在美国专利申请出版号us 2011/0201118 a1、us 2013/0117869 a1、us 2013/0315884a1、us 2015/0203871a1和us 2016/0120906a1中,其公开内容通过参考并入本文。
[0114]
可以通过使用tale法对滑膜细胞进行永久性基因编辑而沉默或抑制的基因的非限制性实例包括il
‑
1α、il
‑
1β、il
‑
4、il
‑
9、il
‑
10、il
‑
13和tnf
‑
α。
[0115]
可以通过使用tale法对滑膜细胞进行永久性基因编辑而增强的基因的非限制性实例包括il
‑
1α、il
‑
1β、il
‑
4、il
‑
9、il
‑
10、il
‑
13和tnf
‑
α。
[0116]
可以根据本发明的实施方式使用,用于通过tale法改变靶基因序列的表达的系统、方法和组合物的实例,描述在美国专利号8,586,526中,其通过参考并入本文。
[0117]
锌指法
[0118]
用于治疗或预防关节疾病或病症的药物组合物包含基因编辑系统,其中所述基因编辑系统靶向至少一个与关节功能相关的基因座,其中所述方法还包括通过锌指或锌指核酸酶法对至少一部分关节滑膜细胞进行基因编辑。根据特定实施方式,使用锌指法靶向至少一个与关节功能相关的基因座,其中对至少一部分关节滑膜细胞进行基因编辑。可选地,在靶向至少一个与关节功能相关的基因座期间使用锌指法,其中对至少一部分关节滑膜细胞进行基因编辑使在至少一部分所述关节滑膜细胞中至少一个与关节功能基因相关的基因座的表达被增强。
[0119]
在保守的ββα构型中,单个锌指含有大约30个氨基酸。α
‑
螺旋表面上的几个氨基酸通常与dna大沟中的3bp接触,具有不同的选择性水平。锌指具有两个蛋白质结构域。第一个结构域是dna结合结构域,其包括真核转录因子并含有锌指。第二个结构域是核酸酶结构域,其包括foki限制性酶并负责dna的催化切割。
[0120]
单个zfns的dna结合结构域通常含有3至6个之间的单独的锌指重复序列,可以各自识别9至18个之间的碱基对。如果锌指结构域对它们的目标靶位点特异,那么即使是识别总共18个碱基对的一对3
‑
指zfns在理论上也可以靶向哺乳动物基因组中的单个基因座。产生新的锌指阵列的一种方法是将特异性已知的较小锌指“模块”组合。最常用的模块化组装过程包括将3个可以各自识别3个碱基对的dna序列的独立的锌指组合,以产生可以识别9个碱基对的靶位点的3
‑
指阵列。可选地,可以使用基于选择的方法例如寡聚体库工程(open)从随机文库中选择新的锌指阵列,所述方法将相邻锌指之间的背景依赖性相互作用考虑在内。工程化改造的锌指是可商购的;sangamo biosciences(richmond,ca,usa)与sigma
‑
aldrich(st.louis,mo,usa)合作开发了一种用于锌指构建的专用平台
[0121]
可以通过使用锌指法对滑膜细胞进行永久性基因编辑而沉默或抑制的基因的非限制性实例包括il
‑
1α、il
‑
1β、il
‑
4、il
‑
9、il
‑
10、il
‑
13、tnf
‑
α、il
‑
6、il
‑
8、il
‑
18、基质金属蛋白酶(mmp)或nlrp3炎症小体的组分。在某些实施方式中,所述nlrp3炎症小体的组分包含nlrp3、asc(含有card的凋亡相关斑点样蛋白)、半胱天冬酶
‑
1及其组合。
[0122]
可以通过使用锌指法对滑膜细胞进行永久性基因编辑而增强的基因的非限制性实例包括由il
‑
1ra、timp
‑
1、timp
‑
2、timp
‑
3、timp
‑
4及其组合组成的组。在一种情况下,本发明提供了用于上调抗炎性细胞因子的组合物。
[0123]
可以根据本发明的实施方式使用,用于通过锌指法改变靶基因序列的表达的系统、方法和组合物的实例,描述在美国专利号6,534,261、6,607,882、6,746,838、6,794,
136、6,824,978、6,866,997、6,933,113、6,979,539、7,013,219、7,030,215、7,220,719、7,241,573、7,241,574、7,585,849、7,595,376、6,903,185和6,479,626中,所述专利通过参考并入本文。
[0124]
在某些情况下,细胞可以离体进行基因编辑,其中所述基因编辑靶向一个或多个抗炎性细胞因子基因座。在某些情况下,所述细胞是非滑膜细胞。在某些情况下,所述细胞是间充质干细胞。在某些情况下,所述细胞是巨噬细胞。在某些情况下,本发明提供了一种用于治疗或预防关节疾病或病症的药物组合物,其包含基因编辑过的细胞的群体,其中所述基因编辑过的细胞通过靶向至少一个与关节功能相关的基因座的基因编辑系统来编辑。在一种情况下,所述基因编辑过的细胞群体被注射到滑膜关节中。
[0125]
可以根据本发明的实施方式使用,用于通过锌指法改变靶基因序列的表达的系统、方法和组合物的其他实例,描述在beane等,mol.therapy,2015,23 1380
‑
1390中,其公开内容通过参考并入本文。
[0126]
治疗骨关节炎和其他疾病的方法
[0127]
本文描述的组合物和方法可用于治疗疾病的方法中。在一个实施方式中,它们用于治疗炎性关节障碍。它们也可用于治疗在本文和下面的段落中描述的其他障碍。在一种情况下,所述组合物和方法用于治疗骨关节炎(oa)。
[0128]
在某些实施方式中,本公开提供了一种用于治疗或预防关节疾病或病症的方法,所述方法包括引入基因编辑系统,其中所述基因编辑系统靶向至少一个与关节功能相关的基因座。在某些实施方式中,所述关节疾病是骨关节炎。在一种情况下,所述方法用于治疗患有骨关节炎的犬类。在另一种情况下,所述方法用于治疗患有退行性关节疾病的哺乳动物。在某些情况下,所述方法用于治疗患有关节疾病的犬类或马类。在某些情况下,所述方法用于治疗骨关节炎、创伤后关节炎、感染后关节炎、类风湿性关节炎、痛风、假性痛风、自身免疫介导的关节炎、炎性关节炎、炎症介导和免疫介导的关节疾病。
[0129]
在某些实施方式中,所述方法还包括对一部分(所述)关节滑膜细胞进行基因编辑,以降低或沉默il
‑
1α、il
‑
1β、il
‑
4、il
‑
9、il
‑
10、il
‑
13和tnf
‑
α中的一个或多个的表达。在一种情况下,所述方法还包括对一部分(所述)关节滑膜细胞进行基因编辑,以降低或沉默il
‑
1α、il
‑
1β中的一个或多个的表达。
[0130]
在一种情况下,所述方法还包括基因编辑,其中所述基因编辑包括选自crispr法、tale法、锌指法及其组合的一种或多种方法。
[0131]
在某些情况下,所述方法还包括使用aav载体、慢病毒载体或反转录病毒载体递送所述基因编辑。在优选实施方式中,所述方法还包括使用aav1、aav1(y705 731f t492v)、aav2(y444 500 730f t491v)、aav3(y705 731f)、aav5、aav5(y436 693 719f)、aav6、aav6(vp3变体y705f/y731f/t492v)、aav
‑
7m8、aav8、aav8(y733f)、aav9、aav9(vp3变体y731f)、aav10(y733f)和aav
‑
shh10递送所述基因编辑。在某些情况下,所述aav载体包含选自下述的血清型:aav1,aav5,aav6,aav6(y705f/y731f/t492v),aav8,aav9和aav9(y731f)。
[0132]
药物组合物和施用方法
[0133]
本文描述的方法包括使用包含crispr基因(例如il
‑
1α和/或il
‑
1β)编辑复合体作为活性成分的药物组合物。
[0134]
取决于施用方法/途径,药物剂型分为几种类型。这些包括多种液体、固体和半固
体剂型。常见的药物剂型包括丸剂、片剂或胶囊、饮剂或糖浆以及天然或草药形式例如各种各样的植物或食品等以及很多其他形式。值得注意的是,用于药物递送的施用途径(roa)取决于所讨论物质的剂型。液体药物剂型是旨在用于施用或摄入的一定剂量的用作药物或医药的化学化合物的液体形式。
[0135]
在一个实施方式中,本公开的组合物可以皮下(例如关节内注射)、经皮(例如通过贴片透皮)和/或通过植入递送到受试者。示例性的药物剂型包括例如丸剂、渗透递送系统、酏剂、乳液、水凝胶、悬液、糖浆、胶囊、片剂、口服溶解片剂(odts)、凝胶胶囊、薄膜、黏附性局部贴片、棒棒糖、锭剂、口香糖、干粉吸入器(dpis)、汽化器、雾化器、定量吸入器(mdis)、软膏、透皮贴片、皮内植入物、皮下植入物和经皮植入物。
[0136]
当在本文中使用时,“经皮递送”或“经皮施用”可以是指其中将药物剂型施用到真皮(即表皮(与其一起构成皮肤)与皮下组织之间的皮肤层)或通过真皮施用的施用途径。“皮下递送”可以是指其中将药物剂型施用到皮下组织层或皮下组织层下方的施用途径。
[0137]
配制适合的药物组合物的方法在本领域中是已知的,参见例如《remington药学科学与实践》(remington:the science and practice of pharmacy),第21版,2005;以及《药物与制药科学:教科书和专著丛书》(drugs and the pharmaceutical sciences:a series of textbooks and monographs)(dekker,n.y.)系列中的书籍。例如,用于肠胃外、真皮内或皮下施用的溶液或悬液可以包含下述组分:无菌稀释剂,例如注射用水、盐水溶液、非挥发油、聚乙二醇、甘油、丙二醇或其他合成溶剂;抗细菌剂,例如苯甲醇或对羟基苯甲酸甲酯;抗氧化剂,例如抗坏血酸或硫酸氢钠;螯合剂,例如乙二胺四乙酸;缓冲剂,例如乙酸盐、柠檬酸盐或磷酸盐;以及调节渗涨度的试剂,例如氯化钠或右旋糖。ph可以用酸或碱例如盐酸或氢氧化钠来调节。肠胃外制剂可以封装在安瓿、一次性注射器或玻璃或塑料制成的多剂量小瓶中。
[0138]
适合于注射使用的药物组合物可以包括无菌水性溶液(如果是水溶性的)或分散系和用于临时制备无菌注射溶液或分散系的无菌粉剂。对于静脉内施用来说,适合的载体包括生理盐水、抑菌水、cremophor el
tm
(basf,parsippany,n.j.)或磷酸盐缓冲盐水(pbs)。在所有情况下,所述组合物必须是无菌的,并且应该是足够流动的,以存在容易的可注射性。它在制造和储存条件下应该是稳定的,并且必须被防腐以对抗微生物例如细菌和真菌的污染作用。所述载体可以是含有例如水、乙醇、多元醇(例如甘油、丙二醇和液体聚乙二醇等)及其适合的混合物的溶剂或分散介质。例如,可以通过使用包衣例如卵磷脂,在分散的情况下通过维持所需的粒度以及通过使用表面活性剂,来维持适当的流动性。可以通过各种不同的抗细菌剂和抗真菌剂例如对羟基苯甲酸酯、氯丁醇、苯酚、抗坏血酸、硫柳汞等来防止微生物的作用。在许多情况下,优选地在组合物中包含等渗剂,例如糖、多元醇例如甘露糖醇、山梨糖醇、氯化钠。可注射组合物的延长吸收可以通过在组合物中包含延迟吸收的药剂例如单硬脂酸铝和明胶来实现。
[0139]
无菌可注射溶液可以如下制备:将所需量的活性化合物并入到适合的溶剂中,所述溶剂根据需要含有上文列举的成分中的一者或其组合,然后过滤除菌。通常,分散系通过将活性化合物并入到无菌载体中来制备,所述载体含有基础分散介质和来自于上文列举的那些所需其他成分。在用于制备无菌可注射溶液的无菌粉剂的情况下,优选的制备方法是真空干燥和冷冻干燥,这产生活性成分加上来自于其先前无菌过滤溶液的任何其他所需成
分的粉剂。
[0140]
作为核酸或包括核酸的治疗性化合物可以通过适合于核酸药剂例如dna疫苗的施用的任何方法来施用。这些方法包括基因枪、生物注射器和皮肤贴片以及无针方法,例如在美国专利号6,194,389中公开的微粒dna疫苗技术和美国专利号6,168,587中公开的使用粉剂形式的疫苗的哺乳动物经皮无针疫苗接种。此外,鼻内递送是可能的,正如在尤其是hamajima等,clin.immunol.immunopathol.,88(2),205
‑
10(1998)中所描述的。也可以使用脂质体(例如在美国专利号6,472,375中所述)和微囊化。也可以使用生物可降解的可靶向微粒递送系统(例如在美国专利号6,471,996中所描述的)。
[0141]
治疗性化合物可以用保护所述治疗性化合物以免于从体内快速消除的载体来制备,例如受控释放制剂,包括植入物和微囊化递送系统。可以使用生物可降解的生物相容性聚合物,例如胶原蛋白、乙烯
‑
乙酸乙烯酯、聚酸酐(例如聚[1,3
‑
双(羧基苯氧基)丙烷
‑
共
‑
癸二酸](pcpp
‑
sa)基质、脂肪酸二聚体
‑
癸二酸(fad
‑
sa)共聚物、聚(丙交酯
‑
共
‑
乙交酯))、聚乙醇酸、胶原蛋白、聚原酸酯、聚乙二醇包被的脂质体和聚乳酸。此类制剂可以使用标准技术来制备,或者商业获得,例如从alza corporation和nova pharmaceuticals,inc。脂质体悬液(包括靶向具有针对细胞抗原的单克隆抗体的选定细胞的脂质体)也可用作可药用载体。它们可以按照本领域技术人员已知的方法来制备,例如在美国专利号4,522,811中所述。可以使用半固体、凝胶、软凝胶或其他制剂(包括受控释放制剂),例如当需要向手术部位施用时。制造此类制剂的方法在本领域中是已知的,并且可以包括使用生物可降解的生物相容性聚合物。参见例如sawyer等,yale j biol med.2006december;79(3
‑
4):141
‑
152。
[0142]
所述药物组合物可以与施用说明书一起包含在容器、药剂盒、包装或分配器中。
实施例
[0143]
现在参考下面的实施例描述本文涵盖的实施方式。提供这些实施例仅仅是出于说明的目的,并且本文涵盖的公开内容绝不应被解释为限于这些实施例,而是应该被解释为涵盖作为本文中提供的教示的结果而变得显而易见的任何和所有变化形式。
[0144]
实施例1.在骨关节炎的小鼠模型中通过crispr基因工程降低il
‑
1的表达
[0145]
选择60只c57b小鼠并分为四组,每组15只小鼠。使用dmm手术法在每只小鼠中诱导oa。一旦小鼠发生oa后,将所述小鼠如下进行治疗:
[0146]
第1组:在所述oa关节中直接注射被工程化改造以靶向il
‑
1α和il
‑
1β并沉默或降低il
‑
1蛋白的表达的crispr aav载体。
[0147]
第2组:在oa关节中直接注射用不影响il
‑
1产生的“无意”负载物工程化改造的crispr aav载体;阴性对照。
[0148]
第3组:在oa关节中直接注射被工程化改造以靶向il
‑
1ra并沉默或降低il
‑
1ra蛋白的表达的crispr aav载体。
[0149]
第4组:在oa关节中直接注射无菌缓冲盐水;注射过程的对照。
[0150]
在治疗之前和之后对所述小鼠进行监测,以评估对它们的运动和探索活动的影响。也监测机械敏感度和步态变化。还可以监测异常性疼痛和后肢握力。
[0151]
在大约8周后,将所述动物处死并评估oa关节组织的总体组织病理学,并通过ihc评估il
‑
1表达。还评估了炎症的生物标志物,例如oa关节中的mmp
‑
3表达。
[0152]
用被工程化改造以靶向il
‑
1α和il
‑
1β并沉默或降低il
‑
1蛋白的表达的crispr aav载体治疗的第1组小鼠与其他三组中的任一组相比,通过ihc显示出il
‑
1的水平降低,通过组织病理学显示出组织再生,并显示出更低水平的炎症生物标志物。第3组小鼠与其他三组中的任一组相比显示出相对较高水平的炎症生物标志物。
[0153]
实施例2.评估针对小鼠il1a和il1b的指导切割效率
[0154]
体外切割测定法
[0155]
针对il1a的外显子4和il1b的外显子4(il1a
‑
201ensmust00000028882.1和il1b
‑
201ensmust00000028881.13;对于il1a的外显子4和il1b的外显子4上的靶序列来说,参见表2)设计了crispr向导rna(硫代磷酸酯修饰的sgrna,表3)。使用c57bl/6小鼠基因组dna,通过pcr(phusion高保真dna聚合酶,neb cat#m0530s)扩增il1a和il1b的外显子4;il1a引物fwd:cattgggaggatgcttagga,il1a引物rev:ggctgctttctctccaacag,il1b引物fwd:aggaagcctgtgtctggttg,il1b引物rev:tggcatcgtgagataagctg。将扩增子进行pcr纯化(qiaquick pcr纯化试剂盒,cat#28106)。指导切割效率使用体外切割测定法来确定,所述测定法使用100ng纯化的pcr产物、200ng修饰的向导rna(sigma aldrich)和0.5μg truecut spy cas9蛋白v2(invitrogen a36498)或0.5μg gene snipper nls sau cas9(biovision cat#m1281
‑
50
‑
1)。对所述两种类型的,cas9即酿脓链球菌(s.pyogenes)cas9和金黄色葡萄球菌(s.aureus)cas9的编辑效率进行比较。使用2%琼脂糖凝胶对切割测定法进行定性读出。
[0156]
编辑细胞系
[0157]
针对il1a的外显子4和il1b的外显子4(il1a
‑
201 ensmust00000028882.1和il1b
‑
201ensmust00000028881.13)设计了crispr向导rna(硫代磷酸酯修饰的sgrna,表2)。向导rna切割效率在j774.2和nih3t3细胞的合并物中使用sanger测序和synthego ice(参见例如“从sanger迹线数据推断crispr编辑”(inference of crispr edits from sanger trace data),hsiau t,maures t,waite k,yang j等,biorxiv.2018,其为所有目的通过参考并入本文)或tide(参见例如“通过序列迹线分解对基因组编辑进行轻松定量评估”(easy quantitative assessment of genome editing by sequence trace decomposition),brinkman e,chen t,amendola m和van steensel b,nucleic acids res 2014,其为所有目的通过参考并入本文)网络工具以计算编辑百分率来确定。所述实验还比较了酿脓链球菌(s.pyogenes)cas9和金黄色葡萄球菌(s.aureus)cas9的效率。使用5μg truecut spy cas9蛋白v2(invitrogen a36498)或5μg engen sau cas9蛋白(neb m0654t)和100pmol修饰的向导rna(sigma aldrich)对所述细胞进行电穿孔(amaxa 4d nucleofector装置,lonza)。将sf nucleofector溶液和程序cm139用于j774.2细胞,并将sg nucleofector溶液和程序en158用于nih3t3细胞。在电穿孔后3天获取细胞沉淀,并从每个合并物提取gdna(qiagen,dneasy血液和组织试剂盒,69506)。通过pcr(phusion高保真dna聚合酶,neb,cat#m0530s)在适合的合并物中扩增il1a或il1b的外显子4。il1a引物fwd:tggtttcaggaaaacccaag,il1a引物rev:gcagtatggccaagaaagga,il1b引物fwd:aggaagcctgtgtctggttg,il1b引物rev:ctgggcaagaacattggatt。对扩增子进行sanger测序,并使用synthego ice或tide网络工具进行分析,以确定在每个克隆中不存在野生型序列并存在使cdna序列中的移码的插入缺失。
[0158]
表2.il1a和il1b靶序列
[0159][0160][0161]
表3.crispr向导rna
[0162][0163]
每个crna(参见例如表3)作为单一向导rna合成,其由与下方的tracrrna序列融合的上方的crna序列组成(参见例如seq id no:35
‑
36)。在某些实施方式中,使用a<>u翻转来提高向导rna活性。
[0164]
sau cas9:guuauaguacucuggaaacagaaucuacuaaaacaaggcaaaaugccguguuuaucucgucaacuuguuggcgagauuuuu(seq id no:35)
[0165]
spy cas9:guuauagagcuagaaauagcaaguuaaaauaaggcuaguccguuaucaacuugaaaaaguggcaccgagucggugcuuuuuu(seq id no:36)
[0166]
体外切割测定法
[0167]
图1a示出了用0.5μg spy cas9和200ng修饰的向导rna(对于il1a基因来说43
‑
46,对于il1b来说47
‑
50)切割的100ng小鼠dna的琼脂糖凝胶电泳分析。使用所述向导rna将dna在特定位点处用cas9切开,以与未切开的对照相比在琼脂糖凝胶上产生可预测的条带图案(不希望受到任何特定理论限制,sg8*的所述琼脂糖凝胶电泳似乎显示出失败的合成)。
[0168]
图1b示出了用0.5μg sau cas9和200ng修饰的向导rna(对于il1a基因来说51
‑
53,对于il1b来说54
‑
56)切割的100ng小鼠dna的琼脂糖凝胶电泳分析。使用所述向导rna将dna在特定位点处用cas9切开,以与未切开的对照相比在琼脂糖凝胶上产生可预测的条带图案。
[0169]
编辑细胞系
[0170]
从编辑的合并物提取基因组dna,并在适合的合并物中pcr扩增所述il1a或il1b的
外显子4。将所述pcr产物送去sanger测序,然后使用tide或synthego ice软件反卷积。synthego ice被用于反卷积spy cas9合并物。所述软件可以在向导rna序列和pam位点的基础上确定每个合并物中的编辑模式。它可以区分引起可以产生截短的功能性蛋白的框内缺失的编辑和引起产生真正敲除的移码突变的编辑。所述saucas9合并物使用tide进行分析,因为synthego ice软件不能反卷积saucas9编辑。tide分析以与ice相似的方式,通过在向导rna和pam位点的基础上确定合并物中的编辑模式而起作用。然而,它不是给出真正的敲除分值,而是给出编辑效率分值,其不能区分框内和移码编辑模式。因此,编辑效率分值可能过度代表了向导rna敲除蛋白质的能力。spycas9是在crispr基因编辑中使用的标准蛋白。然而,它是4101bp,与此相比sau cas9是3156bp。由于包装某些病毒例如aav的尺寸限制,因此决定比较saucas9和spycas9的编辑能力,以观察较小的sau cas9是否可用于为此项目设计的载体中。
[0171]
图2a
–
2d示出的图展示了在j774.2(“j”)和nih3t3(“n”)细胞中与多种向导rna一起使用的spy cas9(图2a和2b)和saucas9(图2c和2d)的编辑效率。编辑效率使用synthego ice或tide sanger反卷积软件来确定。图2a:在j774.2和nih3t3中使用向导rna 43
‑
46和spycas9时il1a的敲除效率。使用synthego ice来反卷积sanger序列迹线并确定敲除效率。图2b:在j774.2和nih3t3中使用向导rna47
‑
50和spycas9时il1b的敲除效率;不希望受到任何特定理论限制,所述sgrna8的数据似乎显示出失败的合成。使用synthego ice来反卷积sanger序列迹线并确定敲除效率。图2c:在j774.2和nih3t3中使用向导rna 51
‑
53和sacas9时il1a的敲除效率。使用tide来反卷积sanger序列迹线并确定编辑效率。图2d:在j774.2和nih3t3中使用向导rna 54
‑
56和sau cas9时il1b的敲除效率。使用tide来反卷积sanger序列迹线并确定编辑效率。
[0172]
实施例3.在小鼠尿酸模型中通过crispr基因工程降低il
‑
1β表达确定最佳预处理时间的时间过程实验
[0173]
在用尿酸激惹小鼠之前进行了预实验,以确定小鼠用病毒的最佳预处理时间。将gfp标记的aav5载体注射到小鼠的膝关节中。然后通过pcr定量病毒载量,并在感染后3、5和7天通过组织学定量病毒感染的位置。选择在关节内产生鲁棒的病毒表达的处理时间作为将病毒载体注射到小鼠中的最佳提前时间,用于在小鼠尿酸模型中确定由被工程化改造以靶向il
‑
1b并沉默或降低il
‑
1b的表达的crispr aav载体引起的il
‑
1b的降低的实验。
[0174]
在尿酸模型中确认crispr aav(aav
‑
spcas9)对ll
‑
1b表达的敲减和治疗效果的实验
[0175]
选择小鼠并将其分成三组:
[0176]
第1组:用被工程化改造以靶向il
‑
1b并沉默或降低il
‑
1蛋白表达的crispr aav载体(aav
‑
spcas9)注射的小鼠,
[0177]
第2组:用被工程化改造成具有不影响il
‑
1生产的负载物的crispr aav载体、即“乱序的”向导rna/cas9(aav
‑
spcas9)注射的小鼠,和
[0178]
第3组:用盐水注射的小鼠。
[0179]
然后在最佳预处理时间后,将所述小鼠用尿酸激惹。在用尿酸注射的24小时内,将所述动物处死,并分析所述关节组织的细胞因子表达(例如通过ihc评估il
‑
1表达)。还可以评估所述关节组织的总体组织病理学和炎症生物标志物的表达。
[0180]
用被工程化改造以靶向il
‑
1b并沉默或降低il
‑
1蛋白表达的crispr aav载体治疗的第1组小鼠与其他两组中的任一组相比,通过ihc显示出il
‑
1水平的降低并显示出炎症生物标志物的较低水平。
[0181]
实施例4.小鼠中aav的关节内注射的时间过程研究
[0182]
进行了研究以评估将aav注射到雄性c57bl/6小鼠的关节中的时间过程。
[0183]
材料和方法
[0184]
测试物鉴定和制备
‑
egfp aavprime
tm
纯化的腺相关病毒粒子:gfp标记的aav5(genecopoeia
tm
,目录号ab201,批号gc08222k1902,1.18
×
10
13
个基因组拷贝/ml)和aav6(genecopoeia
tm
,目录号ab401,批号gc09242k1905,5.47
×
10
12
个基因组拷贝/ml)由我们提供。aav粒子在干冰上运输并在收货后立即储存在
‑
80℃。在即将施用前,将所述aav粒子在磷酸盐缓冲盐水(不含钙和镁的pbs:corning,批号11419005)中重构,用于以每个膝盖10μl的剂量ia施用。对于测试物的制备、储存和操作的其他详情,参见研究方案(附录a)。
[0185]
测试系统鉴定
‑
8至10周龄的雄性c57bl/6小鼠(n=30)获自the jackson laboratory(bar harbor,me)。在研究的第0天登记时,小鼠重约24至29克(平均值为26g)。所述动物通过在尾根处描绘组和动物编号的明显标牌来识别。在随机分组后,所有笼子都用适合的颜色编码标记有方案编号、组编号和动物编号(附录a)。
[0186]
环境和饲养
‑
在抵达后,将所述动物按每笼3至5只饲养在带有木屑垫料和悬挂食物瓶和水瓶的聚碳酸酯笼中。将所述小鼠饲养在带有过滤顶的鞋盒笼(静态气流,大约70in2地板空间)或单独通风的饼笼(被动气流,大约70
‑
75in2地板空间)中。包括房间、笼子和设备卫生在内的动物护理符合《实验动物护理和使用指南》(guide,2011)和适用的bolder biopath sop中引用的指南。
[0187]
在进入研究之前,使所述动物适应环境4天。在研究的活阶段,一位主治兽医在现场或随叫随到。没有提供同期药物。
[0188]
在适应和研究期间,将所述动物饲养在温度在19℃至25℃的范围内并且相对湿度为30%至70%的实验室环境中。自动计时器提供12小时的光照和12小时的黑暗。允许动物随意取用envigo teklad 8640饮食和新鲜的市政自来水。
[0189]
实验设计
‑
在研究第0天,将小鼠按体重随机分为治疗组。在随机分组后,如表4中所示将所述动物通过关节内(ia)注射施用。如第8.5.1节中所述测量动物体重。如下文标题为“尸检样本”的部分中所述,在3个时间点(第3、5和7天)将小鼠安乐死,用于尸检和组织收集。
[0190]
表4.分组和治疗信息
[0191]
[0192]
观察、测量和样本
[0193]
体重测量
‑
在研究第0天将所述小鼠称重用于随机分组,并在第1、3、5和7天再次称重。体重测量值可以在表6中发现。
[0194]
尸检样本
‑
如表5中所示,在研究第3、5和7天将小鼠尸检。
[0195]
表5.尸检时间表
[0196]
组动物编号时间点11
‑
10第3天111
‑
20第5天121
‑
30第7天
[0197]
在尸检时,通过心脏穿刺将所述小鼠放血,然后颈椎脱位。从所有动物收获右膝和左膝。从所述关节上除去皮肤和肌肉,同时保持所述关节囊完整。将关节分别速冻在仅标有小鼠编号、收集日期和右腿或左腿的15
‑
ml锥形管中。将膝关节在
‑
80℃冷冻储存以备运输。
[0198]
动物处置
‑
根据bbp sops处置动物尸体。
[0199]
样本和原始数据储存
‑
在研究期间或完成时提交样本(右膝和左膝关节)、研究数据和报告。
[0200]
偏差对研究质量和完整性的影响的声明
‑
与研究方案没有偏差。
[0201]
结果/结论
[0202]
在研究第0天,雄性c57bl/6小鼠在右膝中接受gfp标记的aav5(5
×
109个粒子,10μl)的ia注射并在左膝中接受gfp标记的aav6(5
×
109个粒子,10μl)的ia注射。在研究第0、1、3、5和7天将所述动物称重。在研究第3天(第1
‑
10号动物)、第5天(第11
‑
20号动物)和第7天(第21
‑
30号动物)进行尸检,并收集右膝和左膝关节用于运输。这项研究的活体部分已成功完成,包括动物称重、施用和生物样品收集。所有动物存活至研究结束。
[0203]
参考文献
[0204]
《实验动物护理和使用指南》(guide for the care and use of laboratory animals)(第8版),national research council,national academy of sciences,washington,dc,2011,其为所有目的整体通过参考并入本文。
[0205]
[0206][0207]
方案
[0208]
测试系统
[0209]
动物数目:33(30 3额外)
[0210]
物种/株系或品种:c57bl/6
[0211]
供应商:jackson
[0212]
到达时的年龄/体重:8
‑
10周龄(~20克)
[0213]
性别:雄性
[0214]
研究开始时的年龄/体重范围:到研究开始时至少9周适应:抵达bbp后适应至少3天
[0215]
饲养:3
‑
5只动物/笼
[0216]
研究日历
[0217][0218]
材料
[0219][0220][0221]
测试物品和介质信息
[0222]
未配制的测试物品储存条件
‑
gfp标记的aav5(第1组):
‑
80℃;gfp标记的aav6(第1组):
‑
80℃。
[0223]
介质信息
‑
gfp标记的aav5(第1组):pbs(w/o ca&mg);gfp标记的aav6(第1组):pbs(w/o ca&mg)。
[0224]
测试物品配制说明和计算
‑
gfp标记的aav5(第1组):使用pbs将储用物稀释至适合浓度;gfp标记的aav6(第1组):使用pbs将储用物稀释至适合浓度。
[0225]
施用剂型和介质储存和稳定性
‑
gfp标记的aav5(第1组):在即将注射前稀释;gfp标记的aav6(第1组):在即将注射前稀释。
[0226]
施用后测试物品的处置
‑
gfp标记的aav5(第1组):丢弃剂型,保留储用物用于将来的研究;gfp标记的aav6(第1组):丢弃剂型,保留储用物用于将来的研究。
[0227]
活体阶段可交付成果
[0228][0229]
尸检信息
[0230]
处死时间表:第1组an 1
‑
10:第3天
[0231]
第1组an 11
‑
20:第5天
[0232]
第1组an 21
‑
30:第7天
[0233]
安乐死方法:通过心脏穿刺放血,然后颈椎脱位。
[0234]
时间点:不定时
[0235][0236][0237]
*管只标有小鼠编号、收集日期和左腿或右腿。样品在不提及它们是用aav
‑
2还是用aav
‑
5注射的情况下进行测试。仅在pcr完成后提供答案。
[0238]
样品分析
[0239]
组织样本
‑
将来自于aav注射的小鼠的后肢速冻并运输。在抵达后,将样本转移到所述
‑
80℃冰箱储存。
[0240]
靶组织中的gfp表达
‑
将后肢(成对)在室温融化并在ivis生物发光成像系统(lumina iii;perkin elmer)中成像。使用在488nm处激发和在510nm处测量发射对gfp荧光进行定量。在每个时间点(3天、5天和7天)评估总共4只小鼠。保留来自于每个时间点的剩余6只动物的组织,用于随后使用实时pcr确认病毒负荷。
[0241]
结果
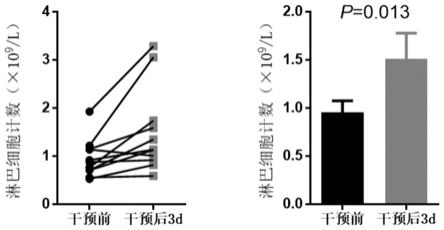
‑
正如可以在图3中看到的,在注射后3天时在注射的膝关节内存在gfp的高水平表达。在第5天病毒载量略微下降,然后再次上升至第7天。由于本试验性研究中样本量有限,因此在aav
‑
5和aav
‑
6的行为之间没有显著差异。
[0242]
讨论
‑
来自于本研究的数据支持了将aav
‑
5或aav
‑
6用于crispr
‑
cas9在小鼠膝关节中的关节内递送。从第5天到第7天两种病毒血清型的水平提高,保留了如果随访延长至2周或可能3周,它们可能进一步提高的可能性。为了证实这一点需要另外的工作,但迄今为止的数据表明在注射载体并用关节内单碘代乙酸(mia)晶体激惹之前,应该存在至少一周的时间间隔。
[0243]
背景和基本原理
‑
在本工作中出于两个原因使用单碘代乙酸(mia)诱导的oa模型。
首先,自然(自发的)oa在小鼠中极为罕见,而mia的注射产生的oa的诱导模型发作相对快,可预测,并提供与人类oa患者中看到的疾病表型包括关节内炎症、疼痛和软骨退化的良好临床相关性。其次,与手术模型例如内侧半月板失稳(dmm)和前交叉韧带横切(aclt)相比,mia模型不涉及关节囊的手术切口,使其更加贴近于患有oa的人类患者的关节囊。
[0244]
在啮齿动物中注射mia晶体重现oa样病变和功能缺损,其可以通过诸如行为测试和客观跛行评估的技术来分析和定量。mia是甘油醛
‑3‑
磷酸酶的抑制剂,引起的细胞糖酵解变化最终使包括软骨细胞在内的关节内细胞的死亡。软骨细胞死亡表现为软骨退化和蛋白聚糖染色的改变。用mia注射的小鼠通常在72小时内表现出疼痛样行为,并且在注射后4周左右表现出软骨丧失。在大鼠和小鼠中已证实在注射后2
‑
3天内il
‑
1表达提高。
[0245]
研究设计
‑
将小鼠用mia或盐水介质对照单侧注射(每只动物一个关节)。在每个组中,将一半的动物用靶向小鼠il
‑
1β基因的aav
‑
crispr
‑
cas9载体预处理,并将另一半用aav
‑
crispr
‑
cas9乱序对照注射。来自于两个组的动物在两个时间点之一退出研究:48小时的早期时间点,以允许评估疗法对滑膜液中il
‑
1水平的影响;以及4周的晚期时间点,以允许评估疗法对软骨破坏和骨关节炎的组织学证据的影响。
[0246]
方法
[0247]
实验动物
‑
在本研究中使用总共80只小鼠。实验程序由当地iacuc审查和批准。小鼠被饲养在小型隔离笼中,喂食标准实验动物饮食,并允许随意饮水。
[0248]
mia模型和抗il1疗法
‑
在研究前使小鼠适应环境为期7天。在研究的第一天,通过吸入异氟烷在氧气中的混合物将小鼠麻醉。一旦确认手术麻醉平面后,将右后肢夹住并用手术消毒剂擦洗皮肤。40只小鼠(治疗)接受靶向il
‑
1的aav
‑
crispr
‑
cas9载体的关节内注射,其余40只小鼠(对照)关节内注射aav
‑
crispr
‑
cas9乱序对照。7天后,将每组中一半的动物在同一关节中注射mia,另一半注射盐水介质。这使建立了四个研究组:
[0249]
第1组:治疗
‑
mia(20只小鼠)
[0250]
第2组:对照
‑
mia(20只小鼠)
[0251]
第3组:治疗
‑
介质(20只小鼠)
[0252]
第4组:对照
‑
介质(20只小鼠)
[0253]
在mia激惹后48小时将每组10只小鼠安乐死,以便记录膝关节中的il
‑
1水平。将剩余的动物饲养4周,以便评估疗法对疼痛行为(行为测试,包括von frey测试)、跛行(肢体使用)、关节肿胀(卡尺测量)和关节病理学(组织病理学)的影响。
[0254]
安乐死和组织收集
‑
通过放血,然后颈椎脱位杀死小鼠。将关节打开,并冲洗以用于il
‑
1测量(48小时组),或在10%福尔马林中浸泡固定用于脱钙组织病理学检查(4周组)。
[0255]
提供上述实施例是为了给本领域普通技术人员提供如何制造和使用本发明的组合物、系统和方法的实施方式的完整的公开和描述,并且不打算限制本发明人认为的发明范围。对上述用于实施本发明的方式的修改对于本领域技术人员来说是显而易见的,并打算落于下述权利要求书的范围之内。本说明书中提到的所有专利和出版物均指明了本发明所属领域的专业技术人员的技术水平。
[0256]
所有标题和章节名称仅仅出于清晰和参考的目的使用,并且不应视为以任何方式限制。例如,本领域技术人员将会认识到,根据本文描述的本发明的精神和范围适合地组合来自于不同标题和章节的各个不同方面,将是有用的。
[0257]
应该理解,本文描述的方法不限于本文中描述的特定方法、方案、受试者和测序技术,因此可以变化。还应该理解,本文中使用的术语仅仅是出于描述特定实施方式的目的,并且不打算限制本文描述的方法和组合物的范围,所述范围将仅受随附的权利要求书限制。尽管在本文中已示出并描述了本公开的某些实施方式,但对于本领域技术人员来说,显然这些实施方式仅仅作为实例提供。在不背离本公开的情况下,本领域技术人员现在将想到大量改变、变化和替换。应该理解,在实践本公开中,可以使用本文描述的本公开的实施方式的各种替代方案。下面的权利要求书旨在定义本公开的范围,并因此覆盖在这些权利要求书及其等同物的范围之内的方法和结构。
[0258]
为了说明,参考示例性应用描述了几个方面。除非另有指明,否则任何实施方式都可以与任何其他实施方式组合。应该理解,大量具体细节、关系和方法的阐述是为了提供对本文描述的特点的全面理解。然而,专业技术人员将会容易地认识到,本文描述的特点可以在没有一个或多个具体细节或使用其他方法的情况下实践。本文描述的特点不受所说明的行动或事件的顺序限制,因为某些行动可以以不同的顺序发生和/或与其他行动或事件同时发生。此外,为了实施符合本文描述的特点的方法,不是所有所说明的行动或事件都是必需的。
[0259]
尽管在本文中已示出并描述了某些实施方式,但对于本领域技术人员来说,显然这些实施方式仅仅作为实例提供。本发明不打算受限于本说明书中提供的具体实例。尽管本发明已参考上述说明书进行了描述,但本文中实施方式的描述和说明并不意味着在限制意义上解释。在不背离本发明的情况下,本领域技术人员现在将想到大量改变、变化和替换。
[0260]
此外,应该理解,本发明的所有方面不限于本文中阐述的取决于各种不同条件和变量的具体描述、配置或相对比例。应该理解,在实践本发明中,可以使用本文描述的本发明的实施方式的各种替代方案。因此,设想了本发明还应该覆盖任何此类替代、修改、变化或等同方案。下面的权利要求书旨在定义本发明的范围,并因此覆盖在这些权利要求书及其等同物的范围之内的方法和结构。
[0261]
本文中的所有出版物、专利和专利申请通过参考并入本文,其程度如同每个单独的出版物、专利或专利申请被具体且单独地指明通过参考并入本文。在本文中的术语与并入的参考文献中的术语之间发生冲突的情况下,以本文中的术语为准。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。