1.本发明属于多重荧光检测技术领域,特别是针对妇科阴道微生态检测;具体涉及一种多重荧光染色液及其制备方法和使用方法。
背景技术:
2.现有的妇科阴道微生态检测方法采用两步法对样本进行染色,即每个样本中真菌的检测要单独进行染色。每个样本需要涂两个玻片,一个玻片染真菌,采用紫外荧光模块进行检测;另一个玻片染除真菌外的微生物及其他有形成分,采用蓝光荧光模块进行检测;因此采用上述的检测方法存在操作时间长,步骤繁琐,并且需要两个荧光模块,对成像设备的配置要求高。
3.并且目前同类产品对目标物的染色清晰度不高,尤其对小目标物(如细菌,真菌等)的成像轮廓不清晰,会导致其在识别(人工和自动)过程中造成错误(遗漏和错认);目前传统的不染色方式(盐水片检测)识别的准确度,由于技术本身的限制,最高仅仅只能达到75%
‑
80%。
技术实现要素:
4.本发明针对现有妇科阴道微生态检测方法存在的上述问题,提供一种多重荧光染色液。
5.本发明采用以下技术方案:一种多重荧光染色液,包括以每一升计的以下组分:强碱105.5
‑
365mm、酸0.01
‑
50g、结合蛋白5
‑
250g、防腐剂0.01
‑
0.2l、增溶剂0.1
‑
50l、破膜剂0.001
‑
20l以及荧光染色剂0.0194
‑
180mg、余量为灭菌蒸馏水。
6.进一步限定,所述强碱包括nacl 100
‑
200mm、kcl 1
‑
5mm、na2hpo
4 0.5
‑
2mm以及kh2po
4 5
‑
158mm中的一种或多种。
7.进一步限定,所述结合蛋白以每一升计包括以下组分:鼠抗单克隆抗体2
‑
100g、羊抗单克隆抗体1
‑
50g以及兔抗单克隆抗体1
‑
50g中的一种或多种。
8.进一步限定,所述酸为乙酸。
9.进一步限定,所述防腐剂为食品用或药品用防腐剂,优选proclin300。
10.进一步限定,所述增溶剂为工业有机溶剂,优选二甲基亚砜。
11.进一步限定,所述破膜剂为调节生物膜分子流动性的表面活性剂,优选甘油、丙三醇或吐温20中的一种。
12.进一步限定,所述荧光染色剂以每一升计包括以下组分:hochest 0.01
‑
10mg、4,4
’‑
双(2
‑
苯并噁唑基)二苯乙烯0.001
‑
10mg、吖啶橙0.001
‑
10mg、羧基荧光素二醋酸盐琥珀酰亚胺酯0.001
‑
50mg、sybr green i 0.001
‑
10mg、sybr greenⅱ0.001
‑
10mg、细胞膜荧光探针0.0003
‑
40mg、异硫氰酸荧光素0.001
‑
10mg、藻红蛋白0.001
‑
10mg、多甲藻黄素
‑
叶绿素
‑
蛋白质复合物0.001
‑
10mg、碘化丙啶0.001
‑
10mg以及别藻青蛋白0.001
‑
10mg中的一种或多种的混合物。
13.本发明的有益效果为:本发明将真菌检测物和真菌以外的其他微生物检测物鳌合在一起,因此只需要一次涂抹,一次染色,且只需要一次观色即可得出检测结果,并且染色后效果更加清晰,目标物染色边界更加锐化,这样对小目标物的识别非常有好处,尤其是微生物中细菌及真菌都是形态比较小,边界清晰,锐化的荧光染色效果,有利于此类目标物的鉴定,也更加有利于实施“人工智能识别”,实现妇科阴道微生态检测的自动化,采用上述多重荧光染色液操作时间短,操作步骤简单,提高实验效率,降低了对检测设备的配置要求;
14.本发明提供的多重荧光染色液能够对所有的有型微生物及组织细胞进行荧光染色或标记,完全呈现检测环境的微生态状况,利于临床检测结果的判断。
15.本发明还公开了一种多重荧光染色液的制备方法,包括以下步骤:
16.将强碱、乙酸以及灭菌蒸馏水混合配制盐母液,搅拌20
‑
35分钟,0.22μm水系膜过滤,2
‑
5℃避光保存;
17.配制结合蛋白母液,0.22μm水系膜过滤,
‑
20~
‑
17℃分装避光保存;
18.配制荧光染色剂母液,0.22μm脂溶系膜过滤,2
‑
5℃避光保存;
19.将盐母液、结合蛋白母液、荧光染色剂母液、防腐剂、增溶剂以及破膜剂混合,以灭菌蒸馏水为稀释液,稀释得到多重荧光染色液,室温避光保存。
20.本发明的有益效果为:该制备方法简单,在常温下和只需要搅拌即可实现鳌合,并且只需要在常温下保存,保存条件友好。
21.本发明还公开了一种多重荧光染色液的使用方法,包括以下步骤:
22.用生理盐水将采样拭子的采样端淹没且搅拌1
‑
2分钟;
23.将采样拭子的采样端于载玻片上涂抹单层样本膜;
24.固化样本后加入多重荧光染色液以使样本完全被覆盖,30
‑
45秒后冲洗样本;
25.晾干冲洗的样本,且将样本置于具有蓝光荧光模块的显微镜下观察即可。
26.本发明的有益效果为:使用方法简单,可操作性强,减少了对检测结果影响的因素,因此检测结果准确性高,并且采用上述的使用方法,可以减少生理盐水的使用量。
附图说明
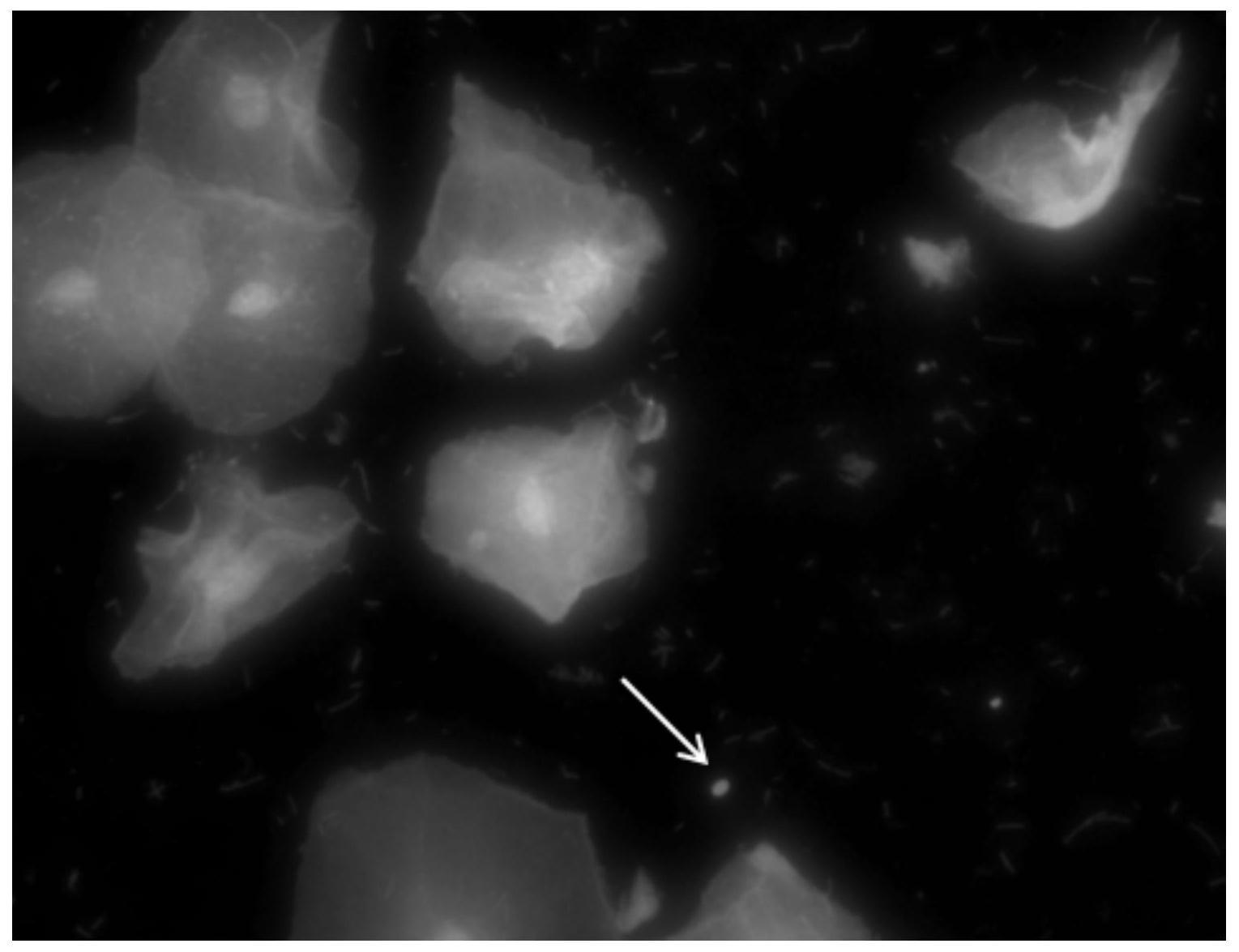
27.图1为采用实施例2制备得到的多重荧光染色液染色样本后显微镜下病原体孢子的染色图;
28.图2为采用现有荧光染色液染色样本后显微镜下病原体孢子的染色图;
29.图3为采用实施例2制备得到的多重荧光染色液染色样本后显微镜下病原体线索细胞的染色图;
30.图4为采用现有荧光染色液染色样本后显微镜下病原体线索细胞的染色图;
31.图5为采用实施例2制备得到的多重荧光染色液染色样本后显微镜下上皮细胞、白细胞以及乳杆菌的染色图;
32.图6为采用实施例2制备得到的多重荧光染色液染色样本后显微镜下加德纳菌感染的上皮细胞的染色图;
33.图7为采用实施例2制备得到的多重荧光染色液染色样本后显微镜下线索细胞真菌孢子的染色图;
34.图8为采用实施例2制备得到的多重荧光染色液染色样本后显微镜下菌丝的染色
图;
35.图9为采用实施例2制备得到的多重荧光染色液染色样本后显微镜下滴虫的染色图;
36.图10为实施例5中采用实施例2制备得到的多重荧光染色液染色样本后显微镜下图;
37.图11
‑
14为实施例5中采用实施例2制备得到的多重荧光染色液染色样本后显微镜下多个局部染色图;
38.图15
‑
18为实施例5中采用实施例2制备得到的多重荧光染色液染色样本后显微镜下病原体线索细胞的多个局部染色图;
39.图19为采用现有荧光染色液染色样本后显微镜下图;
40.图20
‑
23为采用现有荧光染色液染色样本后显微镜下病原体孢子和其他有型成分的多个局部染色图;
41.图24
‑
26为采用现有荧光染色液染色样本后显微镜下病原体线索细胞的多个局部染色图。
具体实施方式
42.实施例1
43.制备多重荧光染色液,包括以下步骤:
44.s1:称取或量取以下各物质:nacl 100mm、kcl 1mm、na2hpo
4 0.5mm、kh2po
4 5mm、鼠抗阴道加德纳单克隆抗体a/b/c 1g、兔抗白色念珠菌单克隆抗体a/b 1g、鼠抗白色奈瑟氏淋球菌单克隆抗体a/b 1g、鼠抗阴道毛滴虫单克隆抗体a/b 1g、鼠抗单纯疱疹病毒(i/ii型)单克隆抗体a/b 1g、proclin300 0.01l、dmso 0.1l、吐温20 0.001l、hochest 0.01mg、4,4
’‑
双(2
‑
苯并噁唑基)二苯乙烯0.001mg、吖啶橙0.001mg、羧基荧光素二醋酸盐琥珀酰亚胺酯0.001mg、sybr green i 0.001mg、sybr greenⅱ0.001mg、细胞膜荧光探针(dii)0.0001mg、细胞膜荧光探针(dio)0.0001mg、细胞膜荧光探针(dir)0.0001mg、异硫氰酸荧光素0.001mg、藻红蛋白0.001mg、多甲藻黄素
‑
叶绿素
‑
蛋白质复合物0.001mg、碘化丙啶0.001mg、别藻青蛋白0.001mg以及乙酸0.01g。
45.s2:制备盐母液:将nacl、kcl、na2hpo4、kh2po4、乙酸,以灭菌蒸馏水为溶剂,混合搅拌搅拌30分钟,0.22μm水系膜过滤得到100x的盐母液,4℃避光保存;
46.s3:制备结合蛋白母液:将鼠抗阴道加德纳单克隆抗体a/b/c、兔抗白色念珠菌单克隆抗体a/b、鼠抗白色奈瑟氏淋球菌单克隆抗体a/b、鼠抗阴道毛滴虫单克隆抗体a/b、鼠抗单纯疱疹病毒(i/ii型)单克隆抗体a/b,以灭菌蒸馏水为溶剂,混合搅拌30分钟,0.22μm水系膜过滤得到100x的结合蛋白母液,
‑
20℃避光保存;
47.s4:配制荧光染色剂母液:hochest,荧光增白剂,吖啶橙,cfse,sybr green i,sybr greenⅱ,细胞膜荧光探针(dii,dio,dir),异硫氰酸荧光素(fitc),藻红蛋白(pe),多甲藻黄素
‑
叶绿素
‑
蛋白质复合物(percp),碘化丙啶(pi),别藻青蛋白(apc),以dmso为溶剂混合后搅拌30分钟,0.22μm脂溶系膜过滤得到1000x荧光染色剂母液,4℃避光保存;
48.s5:将100x盐母液、100x结合蛋白母液、1000x荧光染色剂母液、proclin300,dmso,吐温20,以灭菌蒸馏水为稀释液混合后经0.22μm脂溶系膜过滤得到多重荧光染色液,室温
避光保存。
49.实施例2
50.制备多重荧光染色液,包括以下步骤:
51.s1:称取或量取以下各物质:nacl 135mm、kcl 2.7mm、na2hpo
4 1.5mm、kh2po
4 8mm、鼠抗阴道加德纳单克隆抗体a/b/c 5g、兔抗白色念珠菌单克隆抗体a/b 10g、鼠抗白色奈瑟氏淋球菌单克隆抗体a/b 7.5g、鼠抗阴道毛滴虫单克隆抗体a/b 12g、鼠抗单纯疱疹病毒(i/ii型)单克隆抗体a/b 6.7g、proclin300 0.05l、dmso 2.5l、吐温20 0.01l、hochest 0.05mg、4,4
’‑
双(2
‑
苯并噁唑基)二苯乙烯10mg、吖啶橙10mg、羧基荧光素二醋酸盐琥珀酰亚胺酯50mg、sybr green i 10mg、sybr greenⅱ10mg、细胞膜荧光探针(dii)10mg、细胞膜荧光探针(dio)10mg、细胞膜荧光探针(dir)10mg、异硫氰酸荧光素10mg、藻红蛋白10mg、多甲藻黄素
‑
叶绿素
‑
蛋白质复合物10mg、碘化丙啶10mg、别藻青蛋白10mg以及乙酸50g;
52.s2:制备盐母液:将nacl、kcl、na2hpo4、kh2po4、乙酸,以灭菌蒸馏水为溶剂,混合搅拌搅拌35分钟,0.22μm水系膜过滤得到100x的盐母液,4℃避光保存;
53.s3:制备结合蛋白母液:将鼠抗阴道加德纳单克隆抗体a/b/c、兔抗白色念珠菌单克隆抗体a/b、鼠抗白色奈瑟氏淋球菌单克隆抗体a/b、鼠抗阴道毛滴虫单克隆抗体a/b、鼠抗单纯疱疹病毒(i/ii型)单克隆抗体a/b,以灭菌蒸馏水为溶剂,混合搅拌35分钟,0.22μm水系膜过滤得到100x的结合蛋白母液,
‑
20℃避光保存;
54.s4:配制荧光染色剂母液:hochest,荧光增白剂,吖啶橙,cfse,sybr green i,sybr greenⅱ,细胞膜荧光探针(dii,dio,dir),异硫氰酸荧光素(fitc),藻红蛋白(pe),多甲藻黄素
‑
叶绿素
‑
蛋白质复合物(percp),碘化丙啶(pi),别藻青蛋白(apc),以dmso为溶剂混合后搅拌35分钟,0.22脂溶系膜过滤得到1000x荧光染色剂母液,4℃避光保存;
55.s5:将100x盐母液、100x结合蛋白母液、1000x荧光染色剂母液、proclin300,dmso,吐温20,以灭菌蒸馏水为稀释液混合后经0.22μm脂溶系膜过滤得到多重荧光染色液,室温避光保存。
56.实施例3
57.制备多重荧光染色液,包括以下步骤:
58.s1:称取或量取以下各物质:nacl 200mm、kcl 5mm、na2hpo
4 2mm、kh2po
4 158mm、鼠抗阴道加德纳单克隆抗体a/b/c 50g、兔抗白色念珠菌单克隆抗体a/b 50g、鼠抗白色奈瑟氏淋球菌单克隆抗体a/b 50g、鼠抗阴道毛滴虫单克隆抗体a/b 50g、鼠抗单纯疱疹病毒(i/ii型)单克隆抗体a/b 50g、proclin300 0.2l、dmso 50l、吐温20 20l、hochest 10mg、4,4
’‑
双(2
‑
苯并噁唑基)二苯乙烯0.02mg、吖啶橙0.02mg、羧基荧光素二醋酸盐琥珀酰亚胺酯0.05mg、sybr green i 0.01mg、sybr greenⅱ0.01mg、细胞膜荧光探针(dii)0.001mg、细胞膜荧光探针(dio)0.001mg、细胞膜荧光探针(dir)0.001mg、异硫氰酸荧光素0.01mg、藻红蛋白0.01mg、多甲藻黄素
‑
叶绿素
‑
蛋白质复合物0.01mg、碘化丙啶0.01mg、别藻青蛋白0.01mg以及乙酸0.5g;
59.s2:制备盐母液:将nacl、kcl、na2hpo4、kh2po4、乙酸,以灭菌蒸馏水为溶剂,混合搅拌搅拌20分钟,0.22μm水系膜过滤得到100x的盐母液,4℃避光保存;
60.s3:制备结合蛋白母液:将鼠抗阴道加德纳单克隆抗体a/b/c、兔抗白色念珠菌单克隆抗体a/b、鼠抗白色奈瑟氏淋球菌单克隆抗体a/b、鼠抗阴道毛滴虫单克隆抗体a/b、鼠
抗单纯疱疹病毒(i/ii型)单克隆抗体a/b,以灭菌蒸馏水为溶剂,混合搅拌20分钟,0.22μm水系膜过滤得到100x的结合蛋白母液,
‑
20℃避光保存;
61.s4:配制荧光染色剂母液:hochest,荧光增白剂,吖啶橙,cfse,sybr green i,sybr greenⅱ,细胞膜荧光探针(dii,dio,dir),异硫氰酸荧光素(fitc),藻红蛋白(pe),多甲藻黄素
‑
叶绿素
‑
蛋白质复合物(percp),碘化丙啶(pi),别藻青蛋白(apc),以dmso为溶剂混合后搅拌20分钟,0.22μm脂溶系膜过滤得到1000x荧光染色剂母液,4℃避光保存;
62.s5:将100x盐母液、100x结合蛋白母液、1000x荧光染色剂母液、proclin300,dmso,吐温20,以灭菌蒸馏水为稀释液混合后经0.22μm脂溶系膜过滤得到多重荧光染色液,室温避光保存。
63.实施例4
64.本实施例中采用前来检查的患者进行下来操作。
65.本实施例公开了一种关于实施例2制备得到的多重荧光染色液的使用方法,包括以下步骤:
66.h1:将采样拭子(如阴道采样拭子)中加入适量的生理盐水,以刚没过拭子采样端为宜,搅拌混匀,将拭子采样端轻放在玻璃载玻片上,涂抹单层样本膜;
67.h2:室温晾干或60℃烤干,固定样本(甲醇2min或火烤3
‑
4次),滴加一滴(约50μl)实施例2制备得到,用竹签调整染色液覆盖整个样本层,室温染色30s,用蒸馏水冲洗干净;
68.h3:室温晾干玻片,将玻片置于显微镜下,蓝光荧光模块下观察;染色结果如图1、图3、图5、图6、图7、图8和图9所示。
69.对比例1
70.采用现有市面上两步检测的试剂对来自实施例4中同一患者的样本进行检测,结果如图2、图4。
71.由于病原体孢子和病原体线索细胞这两种引起的疾病在妇科阴道炎症中占比90%以上,因此重点比较这两种疾病的检测效果,其中病原体孢子为真菌,病原体线索细胞为细菌感染的鳞状上皮细胞,其中细菌主要为加德纳菌。
72.由图1和图2对比可知,图1中病原体孢子被染成红色,如图1中的箭头所指,边界清晰且亮度大,易于识别和区分;图2中病原体孢子和其他有型成分都被染成绿色(图2中箭头所指),边界模糊而且亮度低,不易识别及区分;
73.由图3和图4对比可知,图3中病原体线索细胞被染成红色,亮度明显区别于背景紫杂菌,易于识别和区分;图4中病原体线索细胞被染成黄绿色,而且背景杂菌也被全部染色,不易识别及区分。
74.图5中1号箭头所指为上皮细胞,2号箭头所指为白细胞,3号箭头所指为乳杆菌;
75.图6中箭头所指为加德纳菌感染的上皮细胞;图7中箭头所指为线索细胞真菌孢子;
76.图8中箭头所指为菌丝,图9中箭头所指为滴虫。
77.实施例5
78.采用实施例4中的使用方法,用实施例1制备得到的多重荧光染色液检测健康人群和患者采取的试样,结果图10
‑
18所示,由图10(健康人样本)可知,上皮细胞、白细胞染色清晰;正常乳杆菌染成明显红色,利于临床对微生态体系的判断;背景干净,杂信号少。
79.图11
‑
14(真菌感染患者样本)为病原体孢子的染色情况,由图11
‑
14可知,病原体孢子(图中箭头指的是红色孢子,很容易识别出来)被染成红色,且亮度大十分易于识别和区分;图15
‑
18(细菌感染患者)为病原体线索细胞的染色情况,由图15
‑
18可知,病原体线索细胞被染成红色,亮度明显区别于背景杂菌十分易于识别和区分。
80.对比例2
81.采用现有市面上两步检测的试剂对来自实施例5中对应的相同患者的样本进行检测,结果如图19
‑
26所示,由图19可知,上皮细胞、白细胞、乳杆菌都被染成绿色,无颜色区分,不利于临床观察区分判断;背景杂菌也被全部染色,干扰信号强。
82.图20
‑
23为病原体孢子和其他有型成分的染色情况,由图20
‑
23可知,病原体孢子和其他有型成分都被染成绿色,而且亮度低,不易识别及区分(图中箭头指的是绿色孢子,不易识别出来)。
83.图24
‑
26为病原体线索细胞的染色情况,由图24
‑
26可知,病原体线索细胞被染成黄绿色,而且背景杂菌也被全部染色,不易识别及区分。
84.由此可知,本发明提供的多重荧光染色液不仅能够一次完成细菌和真菌的检测,而且使得真菌和细菌被染色后亮度增加,边界清晰,有利于临床判定。
85.最后应说明的是:以上所述仅为本发明的优选实施例而已,并不用于限制本发明的保护范围。凡在本发明的精神和原则之内,所作的任何修改、等同替换、改进等,均应包含在本发明的保护范围之内。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。