1.本发明涉及药物体内代谢技术领域,尤其涉及一种瓜蒌薤白半夏剂中2种入血成分的同时定量检测方法及应用。
背景技术:
2.经典名方瓜蒌薤白半夏汤出自《金匮要略》,由瓜蒌、薤白、半夏和米酒共煎制成,临床上广泛用于治疗心绞痛型冠心病、风湿性心脏病、室性心动过速、肋间神经痛、乳腺增生、慢性阻塞性肺病、创伤性气胸、老年咳喘、慢性支气管肺炎、慢性胆囊炎等。
3.目前对于瓜蒌薤白半夏汤的研究主要集中在化学成分的研究,而瓜蒌薤白半夏汤中发挥功效的药效物质基础还不是太清楚,而且有效成分在血液中的检测手段更是空白。
4.众所周知,中药有效成分在进入人体血液后才能发挥疗效,微量的有效成分如何在复杂的基质条件下进行定量检测成为难题,为了进一步深入研究瓜蒌薤白半夏剂及其有效成分在血液中的变化情况,并为瓜蒌薤白半夏剂中发挥功效的药效物质基础提供科学依据,开发一种准确、可靠的瓜蒌薤白半夏剂入血成分的定量检测方法成为目前亟待解决的技术问题。
技术实现要素:
5.针对目前没有关于瓜蒌薤白半夏剂入血成分的定量检测方法的缺陷,本发明提供一种瓜蒌薤白半夏剂中2种入血成分的同时定量检测方法及应用,该定量检测方法能够为进一步筛选经典名方瓜蒌薤白半夏剂的质量标志物和药效物质基础提供依据。
6.为达到上述发明目的,本发明实施例采用了如下的技术方案:
7.一种瓜蒌薤白半夏剂中2种入血成分的同时定量检测方法,包括如下步骤:
8.采用uplc
‑
ms/ms检测待测血浆样品中鸟苷和腺苷的含量;
9.其中,色谱条件:以硅胶颗粒为填料的反相色谱柱;流动相a:含0.1%甲酸水溶液,流动相b为乙腈;梯度洗脱的程序如下:
[0010]0‑
1.5min,95%流动相a,5%流动相b;
[0011]
1.5
‑
2.0min,95%
→
80%流动相a,5%
‑
20%流动相b;
[0012]
2.0
‑
2.5min,80%
→
50%流动相a,20%
‑
50%流动相b;
[0013]
2.5
‑
3.5min,50%
‑
95%流动相a,50%
‑
5%流动相b;
[0014]
3.5
‑
5.0min,95%流动相a,5%流动相b;
[0015]
上述百分比均为体积百分比。
[0016]
本发明通过限定uplc
‑
ms/ms方法中的分析参数,各参数之间相互配合,可同时测定瓜蒌薤白半夏剂中鸟苷和腺苷2种入血成分的含量,该瓜蒌薤白半夏剂中2种入血成分的同时定量检测方法简单快捷、可靠、灵敏度高、专属性好、准确度好、稳定性好、检测限和定量限更低,将该方法应用于药物动力学研究,通过分析多组分在体内吸收的特征,验证其对质量标准的制定与评价具有重要意义。
[0017]
其中瓜蒌薤白半夏剂包括瓜蒌薤白半夏汤、瓜蒌薤白半夏冻干粉、瓜蒌薤白半夏膏等,瓜蒌薤白半夏冻干粉和瓜蒌薤白半夏膏等剂型均由瓜蒌薤白半夏汤经常规工艺加工而成。
[0018]
可选地,所述瓜蒌薤白半夏剂的制备方法如下:
[0019]
取瓜蒌,薤白和半夏,加入米酒煎煮、过滤,按照常规工艺制得瓜蒌薤白半夏剂,如汤剂、膏剂或冻干粉。
[0020]
优选地,瓜蒌薤白半夏汤的制备方法如下:称取瓜蒌饮片10
‑
15g,薤白饮片7
‑
12g,半夏饮片10
‑
15g,加入米酒300
‑
500ml浸透约1.5
‑
3.5h,武火煎煮至沸腾,后改文火煎煮15
‑
25min,趁热3
‑
5层纱布过滤,即得。
[0021]
更优选地,瓜蒌薤白半夏汤的制备方法如下:称取瓜蒌饮片12.0g,薤白饮片9.0g,半夏饮片12.0g,加入米酒400ml浸透约2小时,武火煎煮至沸腾,后改文火煎煮20min,趁热用4层纱布过滤,即得。
[0022]
可选地,所述反相色谱柱为acquity uplc hss t3柱。
[0023]
可选地,所述色谱条件中还包括:柱温30
‑
40℃,进样量为1.5
‑
2.5μl,流速为0.2
‑
0.4ml/min。
[0024]
优选地,所述色谱条件的柱温为35℃,进样量为2.0μl,流速为0.3ml/min。
[0025]
可选地,质谱条件:离子源为esi源,毛细管电压为3.2kv,去溶剂气为氮气;去溶剂气的温度为500℃,去溶剂气的流速为600l/h,锥孔气流速为50l/h。通过限定质谱条件,可进一步提高该定量检测方法的准确度及稳定性。
[0026]
可选地,所述待测血浆样品的制备方法包括如下步骤:取血浆样品置于ep管中,加入内标溶液,涡旋混合,再加入乙腈涡旋混合,离心取上清液,即为待测血浆样品。
[0027]
可选地,所述待测血浆样品的制备方法还包括取血,然后置于肝素化离心管中,4000
‑
4500r/min离心8
‑
12min,得到血浆的步骤。
[0028]
优选地,所述血浆的制备方法如下:取血,然后置于肝素化离心管中,4500r/min离心10min,得到血浆。
[0029]
可选地,所述内标溶液中的内标物为玉米素。
[0030]
可选地,所述内标溶液中玉米素的浓度为3
‑
8μg/ml。
[0031]
可选地,所述内标溶液的配置方法如下:
[0032]
称取玉米素5.00mg于10ml容量瓶,加甲醇溶液定容至刻度,得0.5mg/ml内标储备液,经稀释,制得所述内标溶液。
[0033]
本发明还提供了上述的瓜蒌薤白半夏剂中2种入血成分的同时定量检测方法在瓜蒌薤白半夏剂在质量控制研究中的应用。
[0034]
所述质量控制研究包括但是不限于体内药代动力学研究。
[0035]
与现有技术相比,本发明通过对色谱条件、质谱条件、内标物质的选择及样品前处理条件进行合理的设置,提高了检测灵敏度,缩短了分析时间;实现了对鸟苷和腺苷两种极性比较相近的物质的同时定量分析;可用于瓜蒌薤白半夏剂口服给药后的鸟苷和腺苷的药动学研究;为瓜蒌薤白半夏剂中其它组分的同时定量分析提供技术参考。
附图说明
[0036]
图1为实施例2中专属性实验的色谱图;
[0037]
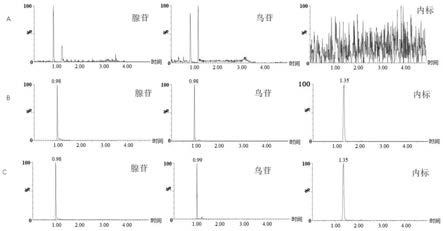
图2为实施例3中大鼠体内药代动力学研究中不同方式给药后腺苷、鸟苷的平均血药浓度-时间曲线。
[0038]
附图说明:
[0039]
附图1中,a为大鼠空白血浆的色谱图,b为含有混合对照品溶液和内标物的大鼠血浆的色谱图,c为大鼠灌胃给药后血浆样品的色谱图;
[0040]
附图2中,a为连续三天给药后大鼠体内腺苷的血药浓度
‑
时间曲线,b为连续三天给药后大鼠体内鸟苷的血药浓度
‑
时间曲线,c为单次给药后大鼠体内腺苷的血药浓度
‑
时间曲线,d为单次给药后大鼠体内鸟苷的血药浓度
‑
时间曲线。
具体实施方式
[0041]
为了使本发明的目的、技术方案及优点更加清楚明白,以下结合实施例,对本发明进行进一步详细说明。应当理解,此处所描述的具体实施例仅仅用以解释本发明,并不用于限定本发明。
[0042]
中药给药后经吸收入血且在体内有一定含量的化学成分才有可能是潜在的生物活性成分,一些中药成分尽管在复方中含量较高,但由于人体吸收程度有限或者成分代谢较快,会制约药物在体内发挥药效,而且血液样品基质复杂、样品含量低,这些因素都给血液样品的检测带来了研发难度。
[0043]
目前,对于瓜蒌薤白半夏汤的研究主要集中在化学成分的研究,而瓜蒌薤白半夏汤中发挥功效的药效物质基础还不是太清楚,有效成分在血液中的检测手段更是空白,且国内外对于瓜蒌薤白半夏汤的多成分药代动力学研究未见报道。本发明在现有鉴定的瓜蒌薤白半夏汤中的84种原型成分的基础上,选取了其中22种主要代表性成分,包括葫芦巴碱、尿嘧啶、胸苷、腺嘌呤、咖啡酸、尿苷、鸟嘌呤、鸟苷、黄嘌呤、腺苷、香草酸、5
‑
羟甲基糠醛、烟酰胺、芦丁、槲皮素、木犀草素、原儿茶酸、高三尖杉酯碱、夏佛塔苷、葫芦素b、n
‑
对香豆酰酪胺和阿魏酸,以此来确定瓜蒌薤白半夏汤的入血原型成分,并探讨瓜蒌薤白半夏汤的药效物质基础。
[0044]
本发明为了建立瓜蒌薤白半夏剂中入血成分的同时定量检测方法,在方法开发和方法验证中,为保证多成分同步检测,对色谱条件、质谱条件、血浆样品的处理方式、内标物的选择进行了不断地探索和优化实验,对上述22种成分的体内定量分析方法进行了研究,最终结果表明只有腺苷和鸟苷这两种成分在体内表现出较高的浓度,可准确定量。具体地,本发明研发得到的可同时定量检测瓜蒌薤白半夏剂中入血成分中鸟苷和腺苷的方法如下:
[0045]
内标溶液的制备:称取玉米素5.00mg于10ml容量瓶,加甲醇溶液定容至刻度,得0.5mg/ml内标储备液,经稀释,制得4μg/ml内标溶液,备用;
[0046]
待测血浆样品的制备:精密吸取50μl大鼠血浆样品置于1.5ml的ep中,精密加入10μl的上述内标溶液,涡旋1min使混合均匀,随后加入140μl乙腈溶液,涡旋5min,充分混合均匀,12000g离心10min,上清液即为待测血浆样品;
[0047]
采用uplc
‑
ms/ms同时检测待测血浆样品中鸟苷和腺苷的含量;
[0048]
其中,质谱条件:离子源为esi源,毛细管电压为3.2kv,去溶剂气为氮气;去溶剂气
的温度为500℃,去溶剂气的流速为600l/h,锥孔气流速为50l/h;采用mrm模式进行定量分析;
[0049]
色谱条件:以硅胶颗粒为填料的反相色谱柱,如acquity uplc hss t3柱;流动相a:体积百分含量为0.1%甲酸水溶液,流动相b为乙腈;洗脱方式为梯度洗脱;柱温30
‑
40℃,进样量为1.5
‑
2.5μl,流速为0.2
‑
0.4ml/min;
[0050]
梯度洗脱的程序如下:
[0051]0‑
1.5min,95%流动相a,5%流动相b;
[0052]
1.5
‑
2.0min,95%
→
80%流动相a,5%
‑
20%流动相b;
[0053]
2.0
‑
2.5min,80%
→
50%流动相a,20%
‑
50%流动相b;
[0054]
2.5
‑
3.5min,50%
‑
95%流动相a,50%
‑
5%流动相b;
[0055]
3.5
‑
5.0min,95%流动相a,5%流动相b;
[0056]
上述百分比为体积百分比。
[0057]
通过多反应监测(multi reaction monitor,mrm)正离子扫描模式、结合特定的色谱检测条件及选用玉米素作为内标物,对上述22种成分的体内定量分析方法研究,测定给药后大鼠体内22种成分的血药浓度,计算药动学参数,了解中药在体内的变化规律,为进一步筛选经典名方瓜蒌薤白半夏剂的质量标志物和药效物质基础提供依据。
[0058]
下面分多个实施例对本发明进行进一步的说明。
[0059]
以下实施例中采用的实验动物均由温州医科大学实验动物中心提供,sd雄性大鼠,体重200
±
20g,7
‑
8周龄,实验前先将大鼠置于温度为22
±
2℃、相对湿度为55
±
10%和12h光/暗循环的环境中适应性饲养一周。
[0060]
以下实施例中采用的主要实验仪器设备、药品见下表1
‑
2所示。
[0061]
表1主要实验仪器与设备
[0062]
仪器名称生产厂家型号电子天平北京赛多利斯仪器系统有限公司ab204n高速冷冻离心机eppendorf公司5920ruplc
‑
ms/ms美国waters公司 冷冻干燥机宁波新芝生物科技股份有限公司scientz
‑
10n数控超声波清洗器昆山市超声仪器有限公司hg64涡旋混合器江苏海门其林贝尔仪器制造有限公司xw
‑
80a
[0063]
表2药品及试剂
[0064]
试剂/药材厂家/产地批号瓜蒌河南安阳gl20200501薤白山东新泰sdx20191001半夏湖北钟祥bx201807091米酒米婆婆20201202腺苷中国食品药品检定研究院110879
‑
201703鸟苷中国食品药品检定研究院111977
‑
201501尿苷中国食品药品检定研究院140660
‑
202002腺嘌呤中国食品药品检定研究院110886
‑
201102
黄嘌呤中国食品药品检定研究院140662
‑
200802尿嘧啶中国食品药品检定研究院100469
‑
201302香草酸中国食品药品检定研究院110776
‑
201503葫芦巴碱中国食品药品检定研究院110883
‑
2005025
‑
羟甲基糠醛成都德思特生物技术有限公司111626
‑
200906烟酰胺中国食品药品检定研究院100115
‑
202005n
‑
对香豆酰酪胺成都德思特生物技术有限公司bp3309鸟嘌呤中国食品药品检定研究院140718
‑
202003胸苷中国食品药品检定研究院101215
‑
201401咖啡酸中国食品药品检定研究院110885
‑
201703芦丁中国食品药品检定研究院100080
‑
201811槲皮素中国食品药品检定研究院100081
‑
201610木犀草素中国食品药品检定研究院111520
‑
202006原儿茶酸中国食品药品检定研究院110809
‑
201906高三尖杉酯碱中国食品药品检定研究院111533
‑
201904夏佛塔苷中国食品药品检定研究院111912
‑
201703阿魏酸中国食品药品检定研究院110773
‑
201915葫芦素b中国食品药品检定研究院111945
‑
201301质谱级甲醇merck公司 质谱级乙腈merck公司 色谱级甲酸roe scientific公司 去离子水杭州娃哈哈集团公司 [0065]
实施例1瓜蒌薤白半夏剂入血成分含量测定方法的研究
[0066]
1.溶液的制备
[0067]
1.1混合对照品溶液的制备
[0068]
精密称取对照品葫芦巴碱、尿嘧啶、胸苷、腺嘌呤、咖啡酸、尿苷、鸟嘌呤、鸟苷、黄嘌呤、腺苷、香草酸、5
‑
羟甲基糠醛、烟酰胺、芦丁、槲皮素、木犀草素、原儿茶酸、高三尖杉酯碱、夏佛塔苷、葫芦素b、n
‑
对香豆酰酪胺和阿魏酸各5.00mg,分别置于10ml容量瓶中,加甲醇定容至刻度,得最终浓度为0.5mg/ml各对照品储备溶液;
[0069]
然后分别精密量取各对照品储备溶液,混合后用甲醇稀释,制得混合对照品溶液;该混合对照品溶液中各对照品的浓度如下:葫芦巴碱250μg/ml;尿嘧啶100μg/ml;胸苷50μg/ml;腺嘌呤50μg/ml;咖啡酸250μg/ml;尿苷50μg/ml;鸟嘌呤50μg/ml;鸟苷50μg/ml;黄嘌呤10μg/ml;腺苷50μg/ml;香草酸500μg/ml;5
‑
羟甲基糠醛250μg/ml;烟酰胺50μg/ml;芦丁100μg/ml;槲皮素100μg/ml木犀草素500μg/ml;原儿茶酸500μg/ml;高三尖杉酯碱100μg/ml;夏佛塔苷250μg/ml;葫芦素b 100μg/ml;n
‑
对香豆酰酪胺20μg/ml;阿魏酸250μg/ml。
[0070]
1.2内标储备溶液及内标溶液的制备
[0071]
精密称取玉米素5.00mg,于10ml容量瓶,加甲醇溶液定容至刻度,得最终浓度为0.5mg/ml内标储备液,然后置于4℃冰箱中保存;
[0072]
精密量取上述内标储备液,经甲醇稀释,制得4μg/ml内标溶液。
[0073]
1.3用于灌胃的瓜蒌薤白半夏冻干粉的制备
[0074]
称取瓜蒌饮片12.0g,薤白饮片9.0g,半夏饮片12.0g,加入米酒400ml浸透约2h,武火煎煮至沸腾,后改文火煎煮20min,趁热用4层纱布过滤,用冷冻干燥机将其冻干,得到瓜蒌薤白半夏冻干粉,置于
‑
80℃冰箱中密封保存。
[0075]
给大鼠灌胃时,瓜蒌薤白半夏冻干粉的用量按照每次6g/kg的剂量,每天给药1次,每次灌胃给药时,瓜蒌薤白半夏冻干粉与纯水的质量体积比为1.5g:1ml。
[0076]
1.4待测血浆样品的制备
[0077]
精密吸取50μl大鼠血浆样品置于1.5ml的ep管中,精密加入10μl内标溶液(内标储备液用稀释后得到,浓度为4μg/ml),涡旋1min使混合均匀。随后加入140μl乙腈溶液,涡旋5min,充分混合均匀,12000g离心10min,取上清液即为待测样血浆样品。
[0078]
2.检测
[0079]
精密吸取大鼠血浆样品,按照1.4项下方法制备待测血浆样品并注入uplc
‑
ms/ms进行检测。
[0080]
2.1检测条件
[0081]
质谱条件
[0082]
waters quattro api三重四级杆串联质谱仪(美国waters公司),电喷雾离子源(esi);毛细管电压为3.2kv;去溶剂气为氮气;去溶剂气温度为500℃;去溶剂气流速为600l/h;锥孔气流速为50l/h,采用mrm模式对样品进行定量分析,实验数据的采集和处理采用masslynx软件(4.1版本,waters公司)。
[0083]
各对照品的定量离子、锥孔电压及碰撞电压如下表所示。
[0084]
表3
[0085][0086][0087]
色谱条件
[0088]
色谱柱:acquity uplc hss t3 column(2.1
×
100mm,1.8μm)
[0089]
流动相:a:水(含0.1%甲酸),b:乙腈
[0090]
柱温:35℃
[0091]
进样量:2μl
[0092]
梯度洗脱条件如下表:
[0093]
表4梯度洗脱条件
[0094]
时间(min)a(%)b(%)流速(ml/min)0.09550.31.59550.32.080200.32.550500.33.59550.359550.3
[0095]
2.2最终确立的检测条件
[0096]
含氮类化合物在电喷雾离子源正负离子检测模式下均有响应,在正离子模式下响应要高于负离子模式,并且在正离子模式下能检测到明显的准分子离子峰。
[0097]
流动相对各待测物的色谱行为(峰对称性和保留时间)和质谱响应有很大的影响,在有机相的选择上,分别以甲醇和乙腈作为流动相进行考察,结果表明,乙腈作为有机相时出峰快,峰形较好,分布均匀,峰强度高,因此选择乙腈作为流动相。在水相添加剂选择上,当水相中不加酸时,待测成分的色谱峰拖尾严重,加入甲酸后,色谱行为明显该善,待测物的响应也有所升高,结果表明乙腈
‑
0.1%甲酸水为流动相能够获得良好的离子响应。
[0098]
柱温考察了35℃和40℃对色谱峰的影响,结果显示温度对色谱峰的分离影响不大,结合色谱柱本身的特性,故选择35℃。
[0099]
最终确定的瓜蒌薤白半夏剂入血成分含量测定方法与2.1项下的检测条件相同。
[0100]
实施例2瓜蒌薤白半夏冻剂入血成分含量测定方法的方法学验证
[0101]
检测限和定量限(入血原型成分确定)
[0102]
根据混合对照品溶液中各对照品的信噪比,计算所需的稀释倍数,将各对照品储备溶液进行适当稀释,得混合对照品溶液中各对照品浓度,然后按照2.1项下的检测条件进行检测,以信噪比(s/n)大于10确定定量限,以信噪比(s/n)大于3确定检测限,22种成分的检测限和定量限见表示。
[0103]
表5 22种成分在大鼠血浆内的定量限和检测限
[0104][0105][0106]
按照1.3项下的条件对12只大鼠灌胃给药0、10min、20min、30min、1h、2h、4h、8h、12h、24h、36h、48h后,抽血,置肝素化离心管中,4500r/min离心10min,得到的血浆分别按照1.4项下的条件制备待测血浆样品,然后按照2.1项下的检测条件对该待测血浆样品中22种成分的血药浓度进行含量测定。
[0107]
经检测,葫芦巴碱、胸苷、咖啡酸、香草酸、5
‑
羟甲基糠醛、芦丁、槲皮素、木犀草素、原儿茶酸、高三尖杉酯碱、夏佛塔苷、葫芦素b和阿魏酸这13种成分在血浆中未检测到。烟酰胺、n
‑
对香豆酰酪胺、尿嘧啶、腺嘌呤、鸟嘌呤、黄嘌呤和尿苷这7种成分虽在血浆中检测到,但血药浓度均低于仪器最低定量限,无法进行准确定量分析。只有腺苷和鸟苷这两种成分在血浆中含量较高,可以进行准确定量。因此,本实验选取了腺苷和鸟苷这两种成分进行后续药代动力学研究。
[0108]
专属性:比较空白大鼠血浆色谱图、加混合对照品溶液和内标溶液的血浆色谱图、大鼠灌胃给药后血浆样品色谱图,考察方法的选择性。
[0109]
其中,空白大鼠血浆样品的制备方法如下:
[0110]
精密吸取50μl大鼠血浆样品置于1.5ml的ep管中,随后加入150μl乙腈溶液,涡旋5min,充分混合均匀,12000g离心10min,取上清液即为空白大鼠血浆样品。
[0111]
加混合对照品和内标的大鼠血浆样品的制备方法如下:
[0112]
取1.2项下配置的内标溶液1ml加入14ml乙腈中,得混有内标的乙腈溶液,备用;
[0113]
将大鼠血浆在低温离心机中于4℃、4500r/min离心15min后,取50μl上清液加入1.1项下配置的混合对照品溶液10μl和上述混有内标的乙腈溶液140μl,涡旋5min后12000r/min离心10min,取上清液即为加混合对照品和内标的大鼠血浆样品。
[0114]
大鼠灌胃给药后血浆样品的制备方法如下:
[0115]
取1.2项下配置的内标溶液1ml加入14ml乙腈中,得混有内标的乙腈溶液,备用;
[0116]
大鼠灌胃给药1h后,抽血,置肝素化离心管中,4500r/min离心10min,得到的血浆,将血浆在低温离心机4℃条件下于4500r/min离心15分钟,取50μl上清加入上述混有内标的乙腈溶液150μl,涡旋5min后12000r/min离心10min,取上清液,即得。
[0117]
由于腺苷、鸟苷为内源性物质,大鼠体内有一定的本底浓度,因此无法取得空白生物样品,本发明在进行专属性研究时将空白血浆样本、加混合对照品的血浆样品与给药后1h血浆样品的色谱图进行对比,以各离子监测通道内化合物的保留时间是否有干扰作为依据,对专属性进行确定。
[0118]
如图1所示:a为大鼠空白血浆的色谱图、b为加混合对照品和内标的大鼠血浆的色谱图、c为大鼠灌胃给药后血浆样品的色谱图。由图1可知,在上述色谱条件下,其它内源性物质和代谢物不干扰样品中待测物的测定。
[0119]
线性(血浆样品标准曲线的绘制)
[0120]
精密吸取1.1项下制备的混合对照品溶液10μl、空白血浆50μl,涡旋混合1min后,随后再参照1.4项下方法处理,配置成一系列不同浓度的标准含药血浆样品,按照2.1项下的检测条件进样测试分析,以浓度(c)为横坐标,以待测物峰面积和内标物峰面积的比值为纵坐标,用加权(1/c2)最小二乘法进行回归运算,进行线性回归。鸟苷和腺苷的标准曲线及定量下限(lloq)如下表所示,
[0121]
表6血浆样品中腺苷、鸟苷的标准曲线和定量下限
[0122]
名称线性方程r2线性范(ng/ml)腺苷y=151.3x 3119.10.9990.5
‑
2500鸟苷y=9.291x 1600.50.9981
‑
1500
[0123]
由上表中的数据可知,每个分析物的标准曲线的相关系数均≥0.99,表明该uplc
‑
ms/ms分析方法灵敏度较高,线性范围好。
[0124]
精密度和准确度
[0125]
同一天内,按1.4项下的处理方法处理并制备低、中、高三个浓度的含药血浆样品,每个浓度各做6份,计算日内准确度和精密度(rsd)。
[0126]
按1.4处理方法处理并制备低、中、高三个浓度的含药血浆样品,每个浓度各做3份,连续5天内测定。根据当日标准曲线计算样品质量浓度,将质控样品的结构进行方差分析,计算日间的准确度和精密度(rsd),检测结果如下表所示。
[0127]
表7血浆样品中腺苷、鸟苷的精密度和准确度
[0128][0129]
由上表中的实验数据可知,2种成分的日内精密度、日间精密度均小于15%,准确度均在83.1%~94.4%内,说明该uplc
‑
ms/ms分析方法的精密度和准确度良好。
[0130]
基质效应和提取回收率
[0131]
精密吸取1.1项下的混合对照品溶液10μl的、空白血浆50μl,涡旋1min混匀,再参照1.4项的方法下处理血浆样品,制备含高、中、低3个浓度的质量控制样品(qc),每个浓度下至少6个样品,峰面积记为a;
[0132]
精密吸取空白血浆50μl和150μl乙腈溶液涡旋8min,充分混合均匀。以12000g,离心10min,取上清液50μl,加入到含有10μl的混合对照品溶液和10μl内标溶液(浓度为50ng/ml)的ep管中,涡旋1min。再参照1.4项下的方法下处理血浆样品,制备含高、中、低3个浓度的质量控制样品(qc),每个浓度下至少6个样品,峰面积记为b;
[0133]
精密吸取10μl的混合对照品溶液和超纯水50μl,涡旋1min混匀,再参照1.4项下处理样品,制备含高、中、低3个浓度的质量控制样品(qc),每个浓度下至少6个样品,峰面积记为c。
[0134]
提取回收率为经过提取后样品的色谱峰面积a与未经提取样品的色谱峰面积b之比(a/b)。基质效应由同一浓度两种处理方法的峰面积比值(b/c)计算出来。提取回收率和基质效应结果见下表所示。
[0135]
表8血浆样品中腺苷、鸟苷的基质效应和提取回收率
[0136][0137]
由上表中的数据可知,腺苷和鸟苷的基质效应分别为77.7%
‑
90.4%和81.9%
‑
89.9%,表明2种成分各浓度水平质控样品的基质效应均符合检测要求;质控水平下2种成分在大鼠血浆中提取回收率范围在67.2%
‑
78.6%之间且较稳定,符合生物样品测定要求。
[0138]
稳定性
[0139]
精密吸取空白血浆50μl,参照1.4项下方法操作,制备含高、中、低3个浓度的质量控制样品(qc),对待测成分进行稳定性考察。稳定性考察包括短期稳定性考察(质量控制样
品放置在室温12h)、长期稳定性考察(质量控制样品放置在
‑
80℃冰箱贮存15天)、冻融稳定性考察(质量控制样品经3次冷冻
‑
解冻循环),稳定性结果见表9所示。
[0140]
表9血浆样品中腺苷、鸟苷的稳定性
[0141][0142][0143]
由上表中的数据可知,腺苷和鸟苷的短期稳定性、长期稳定性、冻融稳定性rsd均小于15%,均符合检测要求,说明该uplc
‑
ms/ms分析方法的稳定性良好。
[0144]
实施例3大鼠体内药代动力学研究
[0145]
健康雄性sd大鼠12只,按6g/kg的剂量分别灌胃给药瓜蒌薤白半夏冻干粉(按照1.3项下操作),其中的6只给药一次后立即取血,另外6只连续给药3天,大鼠在第3天灌胃给药结束后进行取血,取血时间点分别为0min,10min,20min,30min,1h,2h,4h,8h,12h,然后分别置于肝素化离心管中,4500r/min离心10min,吸取血浆,然后按照1.4项下的方法处理,处理之后得到的待测血浆样品在
‑
20℃条件下储存以供分析。测得不同时间血药浓度,由das软件分析药代动力学参数(3.0版,上海,中国),不同方式给药后腺苷、鸟苷的主要药代动力学参数结果如下表所示,不同方式给药后腺苷、鸟苷的平均血药浓度-时间曲线见图2。
[0146]
表10给药后腺苷、鸟苷在大鼠体中的药代动力学参数(n=6)
[0147][0148][0149]
由上表中的数据结合附图2可知,单次给药后的腺苷和鸟苷的c
max
值分别为875.46
±
439.12ng/ml和1137.51
±
407.19ng/ml,连续三天给药后腺苷和鸟苷的c
max
值分别为
709.69
±
343.75ng/ml和351.26
±
85.94ng/ml,都表现出较高的血药浓度,通常认为经吸收入血且在体内有一定含量的化学成分才能发挥药效作用,因此,腺苷和鸟苷可能是瓜蒌薤白半夏剂中的的主要活性成分。此外,单次给药后腺苷和鸟苷的达峰时间(t
max
)值分别为0.63
±
0.77h和0.61
±
0.70h,表明瓜蒌薤白半夏剂进入体内后吸收较快,能很快进入血液循环中发挥疗效。
[0150]
以上所述仅为本发明的较佳实施例而已,并不用以限制本发明,凡在本发明的精神和原则之内所作的任何修改、等同替换或改进等,均应包含在本发明的保护范围之内。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。