1.本发明涉及资源回收技术领域,更具体地讲,涉及一种回收钴酸锂电池正极材料中锂和钴的方法。
背景技术:
2.目前,废旧钴酸锂电池正极材料的回收方法主要有火法和湿法。由于火法回收存在操作温度高,能耗大,对设备要求高,易产生有害气体等缺点,因此,湿法回收越来越受到人们的关注。
3.例如,公开号为cn111074075a公开了一种利用低共熔溶剂回收废旧钴酸锂电池正极材料中钴、锂的方法,通过低共熔溶剂将钴和锂浸出后,再分别将钴和锂进行沉淀处理,得到草酸锂和草酸钴。该法具有使用材料来源广、成本低,容易获得的优点,但该法是将钴和锂浸出后再分别对其进行处理,仍然存在工艺流程长的问题。
技术实现要素:
4.针对现有技术中存在的不足,本发明的目的之一在于解决上述现有技术中存在的一个或多个问题。例如,本发明的目的之一在于提供一种工艺操作简单、流程短的回收钴酸锂电池正极材料中锂和钴的方法。
5.本发明提供了一种回收钴酸锂电池正极材料中锂和钴的方法,可以包括以下步骤:将氯化胆碱、草酸与添加剂混合,得到低共熔溶剂,其中,添加剂可以为水或无水乙醇;将钴酸锂电池正极与低共熔溶剂混合后搅拌浸出,静置后分离,得到草酸锂沉淀和含钴滤液;收集草酸锂,并对含钴滤液中的钴进行回收。
6.在本发明回收钴酸锂电池正极材料中锂和钴的方法的一个示例性实施例中,氯化胆碱、草酸与添加剂的摩尔比可以为(1~3):1:(1~4)。
7.在本发明回收钴酸锂电池正极材料中锂和钴的方法的一个示例性实施例中,对含钴滤液中的钴进行回收可以包括:将去离子水与含钴滤液进行混合,搅拌后分离,得到含钴沉淀。
8.在本发明回收钴酸锂电池正极材料中锂和钴的方法的一个示例性实施例中,去离子水与含钴滤液的体积比可以为(1~3):1。
9.在本发明回收钴酸锂电池正极材料中锂和钴的方法的一个示例性实施例中,还可以包括得到草酸锂沉淀后利用低共熔溶剂对草酸锂进行清洗,干燥后收集草酸锂。
10.在本发明回收钴酸锂电池正极材料中锂和钴的方法的一个示例性实施例中,钴酸锂电池正极与低共熔溶剂的固液比可以为(5~35)g:1l。
11.在本发明回收钴酸锂电池正极材料中锂和钴的方法的一个示例性实施例中,搅拌浸出的温度可以为90℃~120℃,搅拌转速可以为300r/min~500r/min。
12.在本发明回收钴酸锂电池正极材料中锂和钴的方法的一个示例性实施例中,得到低共熔溶剂可以包括:将氯化胆碱、草酸与添加剂混合后,在60℃~80℃,200r/min~400r/
min的搅拌速度下均匀混合,得到低共熔溶剂。
13.在本发明回收钴酸锂电池正极材料中锂和钴的方法的一个示例性实施例中,搅拌浸出的时间可以为120min~360min。
14.与现有技术相比,本发明的有益效果至少包含以下中的至少一项:
15.(1)本发明方法通过一次浸出即可将锂转变为钴酸锂沉淀进行回收,工艺简单,操作方便;
16.(2)本发明方法所使用的原料价廉易得、成本低;
17.(3)本发明低共熔溶剂制备简单、黏度低、物理化学性质稳定、对金属氧化物溶解性强;
18.(4)本发明低共熔溶剂无毒可降解,可循环使用,减少了废物的排放和锂的损失,实现了清洁流程的目标,环境友好;
19.(5)本发明方法温度低、时间短,浸出过程无污染,操作环境好,易于控制和放大生产。
附图说明
20.通过下面结合附图进行的描述,本发明的上述和其他目的和特点将会变得更加清楚,其中:
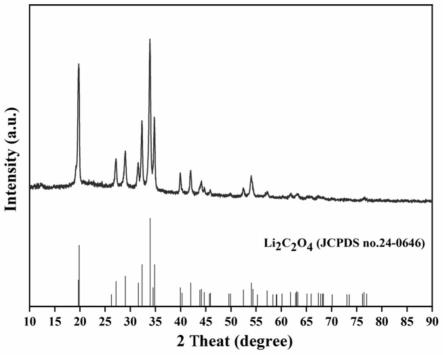
21.图1为示例1回收得到的草酸锂xrd图。
22.图2为示例1回收得到的草酸钴xrd图。
23.图3为不同浸出温度与浸出率的对应关系图。
具体实施方式
24.在下文中,将结合附图和示例性实施例详细地描述根据本发明的一种回收钴酸锂电池正极材料中锂和钴的方法。
25.本发明的一方面提供了一种回收钴酸锂电池正极材料中锂和钴的方法。在本发明的回收钴酸锂电池正极材料中锂和钴的方法的一个示例性实施例中,可以包括以下步骤:
26.s101,将氯化胆碱、草酸与添加剂混合,得到低共熔溶剂,其中,添加剂可以为水或无水乙醇;
27.s102,将钴酸锂电池正极与低共熔溶剂混合后搅拌浸出,静置后分离,得到草酸锂沉淀和含钴滤液;
28.s103,收集草酸锂,并对含钴滤液中的钴进行回收。
29.以上,本发明通过氯化胆碱、草酸与添加剂(水或无水乙醇)的相互配合,能够在浸出静置后让锂元素生成草酸锂(li2c2o4)而析出,同时让钴元素不形成草酸钴而不析出,创新性地实现了通过一次浸出将锂沉淀而不沉淀钴,完成了锂与钴的分离回收,同时也创新性的实现了先将锂沉淀出来后再回收钴的回收顺序,实现了在短流程下对锂和钴的回收。
30.具体来讲,传统湿法中,钴酸锂电池或者其它锂电池(ncm、lmo等)的回收顺序都是先将钴或其它有价金属分离出溶液,然后再将含锂溶液进行蒸发浓缩后,锂以碳酸锂形式得到,但该过程只适用于水溶液中,且蒸发浓缩耗能高,易造成空气污染。对于离子液体低共熔溶剂,其成分为有机物,蒸发浓缩不适用于在低共熔溶剂体系中锂的回收,对于采用低
共熔溶剂回收锂仍然是一个难题。而本发明创新性的实现了先将锂沉淀的顺序,不仅流程短,绿色,还将减少蒸发浓缩的步骤,耗能低,为绿色溶剂低共熔溶剂在锂离子电池回收领域提供了新的发展方向。
31.其原理是,氯化胆碱-草酸对于有价金属具有溶解度高、还原能力强、环境友好等特点,非常适用于电池回收行业,添加剂水或无水乙醇的加入降低了溶剂的黏度,使浸出过程能够实现并更加迅速,且黏度的降低使锂沉淀析出。浸出过程中,草酸首先将钴酸锂中的三价钴还原为二价钴,使钴酸锂溶解进入溶液中;其次,在溶液中草酸提供的草酸根离子与锂离子形成沉淀,而钴离子则与绿化胆碱提供的氯离子形成配位能力更强的四氯合钴配阴离子([cocl4]
2-),将钴固定在了溶液中,实现了锂元素的单独分离。
[0032]
进一步地,所述草酸可以为无水草酸。若使用二水合草酸,并不能通过浸出而静置而直接得到草酸锂沉淀。
[0033]
进一步地,氯化胆碱、草酸与添加剂的摩尔比可以为(1~3):1:(1~4)。在上述摩尔比范围内,能够让锂元素生成草酸锂而析出,同时让钴元素不形成草酸钴而不析出。对于添加剂的含量而言,若添加剂的含量过高,草酸钴会被析出,不能实现锂与钴的分离;若添加剂的含量过低,无法生成草酸锂。例如,氯化胆碱、草酸与添加剂的摩尔比可以为2:1:2或者2:1:3等。
[0034]
进一步地,对含钴滤液中的钴进行回收可以是现有的常规方法,优选地,可以是以下方法:将去离子水与含钴滤液混合,搅拌后分离,得到含钴沉淀和分离后的滤液。所述分离可以是离心分离。所述含钴沉淀可以是coc2o4·
2h2o固体,呈现淡粉红色。由于分离后的滤液中含有添加剂,可以在其重新加入氯化胆碱和草酸后形成新的低共熔溶剂对钴酸锂电池正极材料进行浸出,已实现循环利用。
[0035]
以上,优选地,去离子水与含钴滤液的体积比可以为(1~3):1在上述比例下,能够将含钴滤液中的钴尽可能的析出来。例如,去离子水与含钴滤液的体积比可以为2:1或者2.5:1。
[0036]
进一步地,由于析出后的草酸锂表面可能附着有粘度较大的浸出液,为了清除附着在表面的浸出液,可以利用上述低共熔溶剂对钴酸锂进行反复清洗,然后再用乙醇冲洗多次,干燥后即可对草酸锂进行收集。
[0037]
进一步地,钴酸锂电池正极与低共熔溶剂的固液比可以为(5~35)g:1l。不同的固液比对钴元素和锂元素的浸出有较大的影响。随着固液比的增大,钴和锂的浸出呈现先增大后减小的趋势。优选地,固液比为(10~15)g:1l,此时,钴和锂的浸出率均可以达到90%以上。
[0038]
进一步地,对于浸出温度而言,随着浸出温度的升高,锂和钴的浸出率也会相应的升高。当浸出温度低于90℃时,锂和钴也会有浸出,相比于90℃以上的浸出温度,其浸出率相对较低。当浸出温度大于90℃以后,锂和钴的浸出率开始高于80%。达到120℃以后,随着浸出温度的升高,浸出率将不再显著增加或者变化,因此,优选地,浸出温度为90℃~120℃。搅拌转速可以为300r/min~500r/min。例如,搅拌浸出的温度为80℃,搅拌转速为360r/min。再例如,搅拌浸出的温度为95℃,搅拌转速为420r/min。
[0039]
进一步地,得到低共熔溶剂可以包括:将氯化胆碱、草酸与添加剂混合后,在60℃~80℃,200r/min~400r/min的搅拌速度下均匀混合,得到低共熔溶剂。当混合后的低共熔
溶剂呈现澄清透明的溶液后即可使用。例如,将氯化胆碱、草酸与添加剂混合后,在72℃,325r/min的搅拌速度下均匀混合,得到低共熔溶剂。
[0040]
进一步地,搅拌浸出的时间可以为120min~360min。搅拌浸出的时间可以根据锂和钴的浸出程度进行确定,当锂和钴的浸出率达到预定值后即可停止对正极材料进行浸出。
[0041]
进一步地,将钴酸锂电池正极与低共熔溶剂混合后搅拌浸出,静置后的分离可以是离心分离。当然本发明的分离方式不限于此,常规的分离方式均可。离心的转速可以为7000r/min~9000r/min,离心时间可以为6min~10min。例如,离线的转速为8000r/min,时间为8min。静置的时间可以是12h~72h,例如,静置的时间可以是30h或者35h或者62h。
[0042]
进一步地,所述钴酸锂电池正极材料可以是钴酸锂电池正极拆分剥离后的钴酸锂粉末。
[0043]
为了更好地理解本发明,下面结合具体示例进一步阐明本发明的内容,但本发明的内容不仅仅局限于下面的示例。
[0044]
示例1:
[0045]
(1)将氯化胆碱、草酸与水按1:1:1混合,在温度为70℃,转速为300r/min条件下混合得到低共熔溶剂;
[0046]
(2)将0.3g废旧钴酸锂粉末加入到20ml步骤1合成的低共熔溶剂中,并在90℃、400r/min条件下搅拌浸出4h后得到浸出液,测定锂的浸出率和钴的浸出率;
[0047]
(3)将步骤2中得到的浸出液静置48h,经8000r/min离心8min后得到白色草酸锂沉淀和滤液a;
[0048]
(4)采用步骤1合成的低共熔溶剂对草酸锂沉淀反复清洗至草酸锂沉淀清洗干净后,再采用乙醇冲洗3次后收集,其草酸锂的xrd如图1所示;
[0049]
(5)将2倍去离子水加入到滤液a中,搅拌离心后得到淡粉红色草酸钴沉淀和滤液b,其草酸钴的xrd如图2所示;
[0050]
(6)将收集的草酸锂沉淀和淡粉红色草酸钴沉淀放置于鼓风干燥箱中,在60℃条件下干燥5h,分别回收得到li2c2o4和coc2o4·
2h2o固体。
[0051]
示例2~示例9与示例1相比,浸出温度进行了调整,其他条件相同,分别测量锂和钴的浸出率,如表1所示。
[0052]
示例浸出温度co浸出率(%)li浸出率(%)示例25021.320436.4418示例36038.212242.6352示例47045.301559.3446示例58067.908569.5345示例19086.386480.7378示例610094.775493.7512示例711098.247798.98示例812099.999999.9989示例913099.999999.9999
[0053]
不同浸出温度下的钴和锂浸出率对应关系如图3所示。从图3和表1可以看出,在不
同的浸出温度下,均有钴和锂元素的浸出。随着浸出温度的升高,浸出率随之升高,当达到90℃以后,锂和钴的浸出率达到了80%以上;当达到120℃以后,随着浸出温度的升高,浸出率将不变,因此,优选地,浸出温度为90℃~120℃。
[0054]
示例10:
[0055]
(1)将氯化胆碱和草酸与无水乙醇按1:1:1混合,在温度为70℃,转速为300r/min条件下混合得到低共熔溶剂;
[0056]
(2)将0.4g废旧钴酸锂粉末加入到25ml步骤1合成的低共熔溶剂中,并在90℃、400r/min条件下搅拌浸出4h后得到浸出液,锂的浸出率为95.32%,钴的浸出率为96.12%;
[0057]
(3)将步骤2中得到的浸出液静置48h,经8000r/min离心8min后得到白色沉淀和滤液a;
[0058]
(4)采用步骤1合成的低共熔溶剂对白色沉淀反复清洗至白色沉淀清洗干净后,再采用乙醇冲洗3次后收集;
[0059]
(5)将2倍去离子水加入到滤液a中,搅拌离心后得到淡粉红色沉淀和滤液b;
[0060]
(6)将收集的白色沉淀和淡粉色沉淀放置于鼓风干燥箱中,在60℃条件下干燥5h,最终分别回收得到li2c2o4和coc2o4·
2h2o固体。
[0061]
示例11:
[0062]
(1)将氯化胆碱和草酸与添加剂按2:1:2混合,在温度为70℃,转速为300r/min条件下混合得到低共熔溶剂;
[0063]
(2)将1.2g废旧钴酸锂粉末加入到50ml步骤1合成的低共熔溶剂中,并在90℃、400r/min条件下搅拌浸出4h后得到浸出液,锂的浸出率为89.43%,钴的浸出率为90.42%;
[0064]
(3)将步骤2中得到的浸出液静置48h,经8000r/min离心8min后得到白色沉淀和滤液a;
[0065]
(4)采用步骤1合成的低共熔溶剂对白色沉淀反复清洗至白色沉淀清洗干净后,再采用乙醇冲洗3次后收集;
[0066]
(5)将2倍去离子水加入到滤液a中,搅拌离心后得到淡粉红色沉淀和滤液b;
[0067]
(6)将收集的白色沉淀和淡粉色沉淀放置于鼓风干燥箱中,在60℃条件下干燥5h,最终分别回收得到li2c2o4和coc2o4·
2h2o固体。
[0068]
尽管上面已经通过结合示例性实施例描述了本发明,但是本领域技术人员应该清楚,在不脱离权利要求所限定的精神和范围的情况下,可对本发明的示例性实施例进行各种修改和改变。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。