1.本发明涉及医药领域,具体的说,本发明涉及一种芬乐胺21位代谢物及其制备和应用。
背景技术:
2.芬乐胺是番荔枝酰胺的衍生物,其化合物结构已在中国专利cn1445211(公开号)中公开,该专利记载了中国医学科学院药物研究所发明的“新的番荔枝酰胺衍生物及其制法和其药物组合物与用途”。
3.芬乐胺(化学名:反式-2-(2,5-二甲氧基苯基)-3-(4-羟基-3-甲氧基苯基)-n-(4-羟苯乙基)丙烯酰胺)分子结构式如下:
[0004][0005]
芬乐胺治疗帕金森病(parkinson's disease,pd)的药效学作用与已知阳性药左旋多巴相近,活性强于左旋多巴。芬乐胺作用机制新颖,可抗神经细胞凋亡,具有神经保护作用。但芬乐胺对于神经保护的效果并不能让人满意,因此,开发新的芬乐胺替代产品是目前亟需解决的问题。
技术实现要素:
[0006]
本发明的一个目的在于提供一种芬乐胺的21位代谢物;
[0007]
本发明的另一目的在于提供所述芬乐胺21位代谢物的制备方法;
[0008]
本发明的又一目的在于提供一种药物组合物;
[0009]
本发明的再一目的在于提供所述芬乐胺21位代谢物的应用。
[0010]
为达上述目的,一方面,本发明提供了一种芬乐胺21位代谢物,其中,所述芬乐胺21位代谢物如下式(i)所示:
[0011][0012]
另一方面,本发明还提供了所述的芬乐胺21位代谢物的制备方法,其中,所述方法
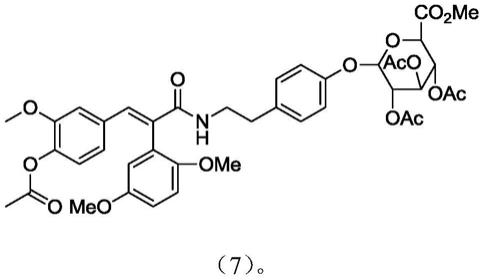
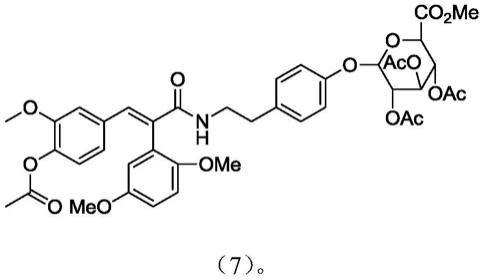
包括以式(7)化合物为原料制备式(i)所示的芬乐胺21位代谢物:
[0013][0014]
根据本发明一些具体实施方案,其中,所述方法还包括以式(6)化合物和式(3)化合物为原料制备式(7)化合物:
[0015][0016]
根据本发明一些具体实施方案,其中,所述方法还包括以式(5)化合物和式(5a)化合物为原料制备式(6)化合物:
[0017][0018]
根据本发明一些具体实施方案,其中,所述方法还包括以式(4)化合物和式(4a)化合物为原料制备式(5)化合物:
[0019][0020]
根据本发明一些具体实施方案,其中,所述方法还包括以式(2)化合物和ccl3cn为原料制备式(3)化合物:
[0021][0022]
根据本发明一些具体实施方案,其中,所述方法还包括以式(1)化合物和(nh2nh2)2coch3为原料制备式(2)化合物:
[0023][0024]
根据本发明一些具体实施方案,其中,所述方法包括如下步骤:
[0025][0026][0027]
根据本发明一些具体实施方案,其中,步骤1的溶剂选自dmf、二氯甲烷、乙腈、1,4-二氧六环、dmso和四氢呋喃中的一种或多种的混合。
[0028]
根据本发明一些具体实施方案,其中,步骤2的溶剂选自二氯甲烷、dmf、乙腈、1,4-二氧六环、dmso和四氢呋喃中的一种或多种的混合。
[0029]
根据本发明一些具体实施方案,其中,步骤3的溶剂为乙酸酐。
[0030]
根据本发明一些具体实施方案,其中,步骤4和步骤5的溶剂各自独立的选自二氯甲烷、dmf、乙腈、1,4-二氧六环、dmso和四氢呋喃中的一种或多种的混合。
[0031]
根据本发明一些具体实施方案,其中,步骤6的溶剂选自甲醇、或选自如下混合溶液中的一种:甲醇/水、乙醇/水、乙腈/水、1,4-二氧六环/水、dmf/水、四氢呋喃/水和dmso/水。
[0032]
根据本发明一些具体实施方案,其中,步骤2是在有机碱的存在下,以式(2)化合物和ccl3cn为原料制备式(3)化合物。
[0033]
根据本发明一些具体实施方案,其中,步骤3是在催化剂的存在下,以式(4)化合物和式(4a)化合物为原料制备式(5)化合物。
[0034]
根据本发明一些具体实施方案,其中,步骤4是在有机碱的存在下,以式(5)化合物和式(5a)化合物为原料制备式(6)化合物。
[0035]
根据本发明一些具体实施方案,其中,步骤5是在催化剂的存在下,以式(6)化合物和式(3)化合物为原料制备式(7)化合物。
[0036]
根据本发明一些具体实施方案,其中,步骤6当溶剂选自甲醇/水、乙醇/水、乙腈/水、1,4-二氧六环/水、dmf/水、四氢呋喃/水和dmso/水中的一种时,步骤6是在碱性物质的存在下,以式(7)化合物为原料制备式(i)化合物。
[0037]
或者,步骤6当溶剂选自甲醇时,步骤6是在甲醇/甲醇钠体系或叔丁醇钠/甲醇体系中,以式(7)化合物为原料制备式(i)化合物。
[0038]
根据本发明一些具体实施方案,其中,步骤2的有机碱选自dbu(1,8-二氮杂二环十一碳-7-烯)、三乙胺、二异丙基乙基胺和n-甲基咪唑中的一种。
[0039]
根据本发明一些具体实施方案,其中,步骤3的催化剂选自三乙胺或二异丙基乙基胺。
[0040]
根据本发明一些具体实施方案,其中,步骤4的有机碱选自三乙胺、二异丙基乙基胺、n-甲基咪唑和n甲基吗啉中的一种或多种的混合。
[0041]
根据本发明一些具体实施方案,其中,步骤5的催化剂选自bf3.et2o、tmsotf(三氟甲磺酸三甲基硅酯)和bf3.thf中的一种。
[0042]
根据本发明一些具体实施方案,其中,步骤6的碱性物质选自碳酸钠、碳酸钾和氢氧化钠中的一种或多种的混合。
[0043]
根据本发明一些具体实施方案,其中,步骤1是在10℃-30℃进行反应。
[0044]
根据本发明一些具体实施方案,其中,步骤1是在室温进行反应。
[0045]
根据本发明一些具体实施方案,其中,步骤2是在10℃-30℃进行反应。
[0046]
根据本发明一些具体实施方案,其中,步骤2是在室温进行反应。
[0047]
根据本发明一些具体实施方案,其中,步骤3是在回流下进行反应。
[0048]
根据本发明一些具体实施方案,其中,步骤4是在5℃-15℃进行反应。
[0049]
根据本发明一些具体实施方案,其中,步骤5是在-30℃至-10℃进行反应。
[0050]
根据本发明一些具体实施方案,其中,步骤5是在-20℃进行反应。
[0051]
根据本发明一些具体实施方案,其中,步骤6是在10℃-30℃进行反应。
[0052]
根据本发明一些具体实施方案,其中,步骤6是在室温进行反应。
[0053]
又一方面,本发明还提供了一种药物组合物,所述药物组合物含有本发明所述的芬乐胺21位代谢物,和一种或多种药学上可接受的载体和/或赋形剂。
[0054]
再一方面,本发明还提供了所述的芬乐胺21位代谢物在制备抗氧化药物、抗神经炎症药物和神经保护药物中的应用。
[0055]
本发明还提供了所述的芬乐胺21位代谢物在制备防治帕金森氏病、改善学习记忆障碍、治疗记忆能力减退及阿尔兹海默病的药物中的应用。
[0056]
综上所述,本发明提供了一种芬乐胺21位代谢物及其制备和应用。本发明的芬乐胺21位代谢物具有如下优点:
[0057]
本发明的芬乐胺21位代谢物具有良好的抗氧化活性、抗神经炎症及神经保护活性。
具体实施方式
[0058]
以下通过具体实施例详细说明本发明的实施过程和产生的有益效果,旨在帮助阅读者更好地理解本发明的实质和特点,不作为对本案可实施范围的限定。
[0059]
实施例1
[0060]
步骤1:
[0061]
在三口瓶中加入四乙酰葡萄糖醛酸(15.0g,39.9mmol),dmf(150ml),冰浴氮气保护下加入醋酸肼(4.4g,47.9mmol),自然回温至室温搅拌4小时,tlc显示反应完全,将体系倒入水(500ml)中,ea(丙烯酸乙酯)(300ml)萃取,有机相用水洗三次,饱和食盐水洗一次,无水硫酸钠干燥,旋干得化合物2(11g,收率83%)。
[0062]1hnmr cdcl3δ:5.61-5.55(m,2h),5.23-5.16(m,1h),4.93-4.90(m,1h),4.61-4.58(d,1h,j=10.0hz),3.74(s,3h),2.05-2.04(m,9h)。
[0063]
步骤2:
[0064]
在三口瓶中加入化合物2(12.0g,35.9mmol),二氯甲烷(150ml),冰浴氮气保护下加入三氯乙腈(25.8g,180mmol),dbu(2.18g,14.4mmol),溶液变为褐色,自然回温至室温搅拌6小时,tlc显示反应完全,加入三乙胺终止反应。直接湿法硅胶柱层析(硅胶柱先用0.5%三乙胺/石油醚洗脱液润湿)纯化(石油醚/乙酸乙酯=5:1-3:1-1:1),快速过柱得化合物3粗品(12g,收率70%)。
[0065]1hnmr cdcl3δ:8.75(s,1h),6.66-6.65(d,1h,j=2.8hz),5.67-5.62(m,1h),5.29-5.26(m,1h),5.18-5.15(m,1h),4.53-4.51(d,1h,j=10.4hz),3.77(s,3h),2.10-2.03(m,9h)。
[0066]
步骤3:
[0067]
在单口瓶中加入化合物4(20.0g,102mmol),化合物4a(15.5g,102mmol),乙醋酐(47.8g,469mmol),三乙胺(6.9g,68.4mmol),130-140℃加热回流15小时,停止反应,降温至90℃,加入水(26ml)回流1小时,减压蒸除溶剂,残留物加二氯甲烷(100ml)稀释,1n盐酸洗(50ml),用二氯甲烷(100ml)萃取水层,合并有机相,1n盐酸(50ml)洗有机相,无水硫酸钠干燥,过滤,蒸除溶剂,加甲苯回流溶解,冰箱内冷藏一夜,过滤,乙醚洗滤饼,得浅黄色化合物5(30g,收率79%)。
[0068]1hnmr d6-dmsoδ:12.50-12.46(m,1h),7.71(s,1h),7.10-6.92(m,3h),6.90-6.66
(m,2h),6.62-6.61(d,1h,j=2.8hz),3.84-3.73(m,6h),3.53(s,3h,),3.77(s,3h),2..27(s,3h)。
[0069]
步骤4:
[0070]
在三口瓶中加入化合物5(10.0g,26.9mmol),dcm(二氯甲烷)(200ml),化合物5a(3.70g,26.9mmol),hobt(1-羟基苯并三唑)(4.40g,32.3mmol),edci(1-乙基-3(3-二甲基丙胺)碳二亚胺)(7.70g,40.3mmol),三乙胺(6.80g,67.2mmol),然后在10℃搅拌7小时,tlc显示反应完全。反应体系用水洗(50ml
×
3),饱和氯化钠(50ml)洗,无水硫酸钠干燥,过滤蒸除溶剂得粗品,粗品用硅胶柱层析纯化(石油醚:乙酸乙酯=5:1)得化合物6(6.00g,收率45%)。
[0071]1hnmr cdcl3δ:7.81(s,1h),6.93-6.87(m,5h),6.79-6.72(m,3h),6.63-6.59(m,1h),5.80-5.66(m,2h),3.71(s,3h),3.62(s,3h),3.54-3.31(m,2h),3.45(s,3h),2.73-2.69(m,2h),2..28(s,3h)。
[0072]
步骤5:
[0073]
在三口瓶中加入化合物6(5.00g,10.2mmol),化合物3(9.70g,20.4mmol),4a分子筛(24.0g),无水二氯甲烷(1500ml),-20℃氮气保护下滴入bf3.et2o(2.89g,20.4mmol),-20℃搅拌2小时后,tlc显示反应完全,加入1滴三乙胺终止反应。过滤,二氯甲烷洗滤饼,有机相依次水洗(30ml),饱和氯化钠洗(30ml),无水硫酸钠干燥,过滤,蒸除溶剂,硅胶柱层析(石油醚:乙酸乙酯=6:1),得化合物7(6g,收率73%)。
[0074]1hnmr cdcl3δ:7.78(s,1h),6.99-6.97(m,2h),6.93-6.85(m,5h),6.76-6.71(m,1h),6.60-6.57(m,2h),5.60-5.57(m,1h),5.35-5.25(m,3h),5.10-5.08(d,1h,j=7.6hz),4.19-4.09(m,1h),3.78-3.69(m,6h),3.59(s,3h),3.54-3.46(m,2h),3.43(s,3h),2.74-2.67(m,2h),2..25(s,3h),2.07-2.05(m,9h)。
[0075]
步骤6:
[0076]
化合物7(6.00g,7.44mmol)溶于甲醇/水(135ml,v/v=2:1),加入na2co3(12.3g,119mmol),室温搅拌过夜。lcms监测反应完成。将反应液旋干,将用水溶解,反应液用1n盐酸调节ph=5-6,过滤,滤饼为粗品,粗品用prep-hplc纯化得化合物i(target 1,t1)(1.1g,收率23%)。
[0077]1hnmr cd3odδ:7.56(s,1h),7.03-7.05(m,4h),6.96-6.98(m,2h),6.70-6.73(m,1h),6.62-6.67(m,2h),6.44-6.48(m,2h),4.93-4.95(m,1h),3.99-4.01(d,1h),3.73(s,3h),3.61-3.67(m,4h),3.46-3.53(m,4h),3.43(s,3h),2.72-2.75(t,2h).
[0078]
lc-ms:m/z=626(m 1)。
[0079]
试验例1
[0080]
本试验例评价并比较芬乐胺(flz)及其本发明的芬乐胺21位代谢物的体外抗氧化、抗神经炎症和神经保护活性。
[0081]
1、实验方法
[0082]
1.1、脂质过氧化产物丙二醛(mda)含量的测定
[0083]
制备肝微粒体:大鼠肝组织称重后,用tris-hc1缓冲液制备10%匀浆,以差数离心法分离出肝脏微粒体。
[0084]
实验设空白组、模型组、flz组和flz 21位代谢物组,每组设置3个复孔。每管加入
pbs缓冲液、肝微粒体、半胱氨酸及受试药溶液。受试药组每管加flz或flz21位代谢物,终浓度分别为1
×
10-4
、1
×
10-5
和1
×
10-6
m,空白组、模型组每管加同体积的dmso。于37℃水浴震荡15min,模型组和加药组每管加1
×
10-2
m feso4溶液,空白组加同体积pbs缓冲液,继续于37℃水浴震荡15min。后每管加入tca溶液、tba溶液,100℃水浴10min。于8000rpm离心10min。取上清液于532nm处测吸光度(od)。
[0085][0086][0087]
1.2、抗神经炎症给药及一氧化氮(no)含量的检测
[0088]
bv2细胞于含10%胎牛血清的dmem培养基中,置于37℃,5%co2的培养箱中培养。选取对数生长期细胞分为空白组、模型组、flz组和flz 21位代谢物组,每组设置3个复孔。加入不同浓度的flz或flz 21位代谢物(终浓度1
×
10-5
,1
×
10-6
,1
×
10-7
m),空白组、模型组加同体积的dmso,1h后模型组和加药组加入500ng/ml lps孵育24h,空白组加同体积pbs缓冲液。每孔吸取100μl培养基,加入配置好的griess试剂,室温静置20min。各组于540nm处测其吸光度值(od值)。利用标准曲线将吸光度转换成no浓度值带入公式计算。
[0089]
no抑制率=[1-(c
待测化合物-c
空白
)/(c
模型-c
空白
]
×
100%
[0090]
1.3、神经保护给药及细胞存活率的测定
[0091]
sh-sy5y神经细胞培养于含10%胎牛血清的dmem培养基中,置于37℃,含5%co2的培养箱中培养。选取对数生长期细胞进行实验。将sh-sy5y细胞分为空白组、模型组、flz组和flz 21位代谢物组,各组设3个复孔。加入不同浓度的flz或flz 21位代谢物(终浓度1
×
10-5
,1
×
10-6
,1
×
10-7
m),1h后模型组和加药组加入8mm mpp
孵育24h,空白组加同体积pbs缓冲液。吸弃上清液,每孔加mtt(0.5mg/ml)100μl,继续孵育4h,于570nm波长,在酶标仪上测定吸光度值(od值)。
[0092]
有效率%=(od
待测化合物-od
模型
)/(od
空白-od
模型
)
×
100%
[0093]
2、实验结果
[0094]
2.1、flz 21位代谢物对脂质过氧化的影响
[0095]
在体外肝微粒体脂质抗氧化实验中,flz 21位代谢物t1对mda的生成有一定的抑制作用,并具有一定的剂量效应关系(表1)。
[0096]
表1.flz 21位代谢物体外抗氧化活性结果
[0097][0098]
2.2、flz及其flz 21位代谢物对no释放的影响
[0099]
lps刺激bv2小胶质细胞后,培养基中no的水平明显升高,flz及其flz 21位代谢物t1对bv2细胞释放no有一定的抑制作用,且t1对no的释放抑制作用强于flz(表2)。
[0100]
表2.flz及flz 21位代谢物体外抗神经炎活性结果
[0101][0102][0103]
2.3、flz及其flz 21位代谢物对细胞存活率的影响
[0104]
sh-sy5y细胞加入mpp
后细胞存活率明显降低,flz对细胞损伤表现出一定的保护作用,且具有剂量效应关系。t1也表现出一定保护作用,且t1效果优于flz(表3)。
[0105]
表3.flz及flz 21位代谢物体外神经保护活性结果
[0106][0107]
3、结论
[0108]
flz 21位代谢物具有一定的抗氧化、抗神经炎症及神经保护活性,其中高浓度效果较好,并且具有剂量依赖性。flz 21位代谢物在抗神经炎症及神经保护活性药效高于flz。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。