1.本发明涉及核酸体外诊断技术领域,尤其涉及将特定的基因甲基化标志物应用于子宫内膜癌早筛早检,具体是一种子宫内膜癌早期筛查诊断用标志物、引物及试剂盒。
背景技术:
2.子宫内膜癌是发生于子宫内膜的上皮性恶性肿瘤,高发年龄为50
‑
60岁,多见于绝经后妇女,近年来有年轻化趋势。据最新全球癌症数据报告显示,2020年全球女性子宫内膜癌新发病例数达42万,位列全球女性恶性肿瘤发病率第六。2020年中国女性子宫内膜癌新发病例数为8万,位列中国女性恶性肿瘤发病率第九。在美国,子宫内膜癌是继乳腺癌、肺癌和结直肠癌之后,第四大最常见的癌症。约有70%的子宫内膜样癌患者,发现时局限于子宫体。子宫内膜癌大部分是局限性病变,生存率相对较高,但常忽略早期不规则阴道流血和阴道排液等症状,失去早期诊断的机会。有数据显示,我国近年来子宫内膜癌的病死率增速超过了发病率的增速。增高的病死率可能与晚期病例的增加、高危型病理类型(如浆乳癌)、诊断时处于高龄等相关。美国监测、流行病学和结果(seer)数据显示,年轻患者、早期病例、低级别病变的患者有更好的生存率。
3.大部分的子宫内膜癌患者是散发性的,但有5%左右的患者是遗传性子宫内膜癌,其特点是这些患者发病年龄要比散发性子宫内膜癌患者平均年龄要小10~20岁。女性林奇综合征是子宫内膜癌的高危人群,发病率高达60%,建议林奇综合征患者密切监测子宫内膜。
4.依据当前子宫内膜癌的诊治指南,目前对于子宫内膜癌早期检测的方法临床上主要采用阴道超声、血清肿瘤标志物ca125、基于子宫内膜细胞采样器的细胞学检测以及最终确诊的组织病理学方法诊断性刮宫和宫腔镜下活检。文献报道,子宫内膜癌具有一定的超声特征图像。只要熟练掌握超声对子宫内膜癌的诊断技巧和图像特点,超声对诊断子宫内膜癌还是有很大价值,但是超声诊断对早期子宫内膜癌的灵敏度不算高,超声诊断子宫内膜癌的灵敏度为59.4%,特异度为81.1%,假阴性率为40.6%,假阳性率为18.9%。血清ca125的检测在早期诊断子宫内膜癌和预测预后方面具有一定的价值。但是子宫内膜癌和良性子宫病变患者血清ca125的阳性率各为24%和20%,因此血清ca125的检测对早期诊断子宫内膜癌缺乏敏感性,并且特异性也相对较差。子宫内膜细胞在月经期外不易脱落,而宫腔脱落的癌细胞容易发生溶解、变性,染色后不易辨认,因此,阴道脱落细胞学检查阳性率不高。常用子宫内膜细胞采集器结合液基细胞学制片技术进行子宫内膜癌的早期检测,诊断子宫内膜非典型增生的灵敏度为55%,特异度为82.6%,诊断子宫内膜癌的灵敏度为36.4%,特异度为99.7%。因此应用子宫内膜细胞采集器取材行液基细胞学检查,可用于筛查症状人群及高危人群子宫内膜病变,但在细胞学检查过程中的诊断技术灵敏度较差,取样具有一定的创伤性。诊断性刮宫和宫腔镜下活检是子宫内膜癌明确诊断的必要方法,鉴于子宫内膜活检可能有约10%的假阴性,如果高度怀疑子宫内膜癌或具有典型症状,子宫内膜活检阴性者,应在麻醉下再次分段诊刮、宫颈管搔刮,以减少漏诊。对有持续或者反复
的未明确内膜病变的阴道流血者,宫腔镜辅助检查有助于判断子宫内膜病变的良恶性,但对人体的伤害较大,不适用子宫内膜癌的早期筛查,只能用于最后的病理确诊。因而,需要一种客观、可重复、特异性高的检测方法来更好分辨出可能形成子宫内膜癌的可能。目前,尚缺乏有效的子宫内膜癌筛查手段,可探索无创筛查方法。目前国内子宫内膜癌的发病率呈现每年递增的趋势,新的筛查手段刻不容缓。
5.dna甲基化是表观遗传学中的一种,是在dna 5’端对胞嘧啶进行共价修饰,这种修饰通常跟基因的沉默相关。因为dna甲基化在很长的时间里都能保持相对稳定,同时在样本中(例如石蜡切片)中都存在,使dna甲基化成为人类疾病研究最有用的表观标志。在早期筛查相关的研究和应用中,甲基化标记检测是目前被普遍认可最有可行性的检测方案,因为dna甲基化标记相比mrna、蛋白质或代谢物标记有更好的稳定性,便于稳定检出;相比dna标记有更好的多样性,能反应身体内外环境变化的影响。甲基化是dna上的一种修饰,对基因转录进行精细调控,基本表现为高甲基化降低基因表达,低甲基化升高基因表达。甲基化水平和模式的改变,会导致抑癌基因的表达被关闭,或原癌基因的表达被激活,因而检测特定位点的dna甲基化水平,可用于推测个体肿瘤生长的情况,从而实现肿瘤早筛早诊的目标。
6.近年来dna甲基化引起了越来越多的基础研究和临床转化的重视。大量的通路被发现受到表观遗传的调控,基于芯片技术和二代测序技术的甲基化大数据的产生,以及众多已有研究表明体液中dna甲基化水平的改变,可用于癌症的早期诊断、预后评估和疗效评估;有部分前沿工作已经开始转化并进入了临床应用。dna甲基化在肠癌的早筛早诊方面已经应用到临床中,以美国exact sciences公司的cologuard(大肠卫士)和国内诺辉、康立明为代表。其他种类癌症的dna甲基化的肿瘤早筛早诊虽然也有国内外企业进行相关研究,但整体还处于科研阶段,能够应用于临床且有明确诊断价值的还较少,其中美国公司foundation medicine在多实体瘤(肺癌、乳腺癌、胃癌、食管癌、结直肠癌、肝癌、胆管胆囊癌、胰腺癌、胃肠道间质瘤、头颈部癌、宫颈癌、卵巢癌、子宫内膜癌、前列腺癌、膀胱癌、肾癌、黑色素瘤等)甲基化方向做了部分数据的科研研究。2016年huang等人以50例子宫内膜癌、40例子宫肌瘤、以及56例健康人的宫颈分泌物作为研究对象筛选了180个相关基因,从中发现了14个在子宫内膜癌中高甲基化的基因,其中bhlhe22、cdo1、celf4三个基因表现尤为突出,它们的灵敏度介于83.7%
‑
96%之间,特异性也能达到78.7%
‑
96.0%,同时两两进行组合检测,灵敏度能达到91.8%同时保持特异性在95.5%。2014年nicolas等人采集了148例子宫内膜癌标本以及23例良性子宫内膜标本,研究了涵盖807个基因的1500个探针,筛选出来8个潜在基因(adcyap1、ascl2、hs3st2、htr1b、mme、npy、以及sox1),可以具有区分子宫内膜良恶性的潜在能力。2013年allison等人研究了64例子宫内膜组织样本以及23例对照样本中的27,000个cpg岛的甲基化情况,发现hand2基因是在子宫内膜癌中最常见的超甲基化的基因之一,同时在后续以272名女性的研究中,hand2的作用被再次证明,该基因的甲基化是子宫内膜病变发展的重要因素之一。
7.dna甲基化主要发生在基因的启动子区域,通常与抑癌基因的表达失活紧密相关。目前应用于基因甲基化检测的方法主要有:甲基化特异性pcr(methylation
‑
specific pcr,msp)、亚硫酸氢盐测序法(bisulfite sequencing pcr,bsp)和高分辨率熔解曲线法(high resolution melting,hrm)等。甲基化特异性pcr主要依靠引物与目标模板的结合以进行pcr扩增来检测甲基化位点;亚硫酸氢盐测序法依靠测序引物进行pcr扩增,在此基础
上进行后续测序以实现对甲基化位点的检测;高分辨率溶解曲线法主要通过样本中的cg含量的变化导致的溶解温度的变化以此对甲基化与非甲基化情况进行区分。每种方法都有各自的特点,bsp法结果准确性较高,易于直观进行判读,但灵敏度较低,操作相对更为繁琐,成本高;hrm法灵敏度相对较低,同时结果分析略复杂;msp法检测灵敏度高,对样本的要求相对较低,同时检测时长较短、成本较低,结果易于判读。
8.非侵入性且成本低是癌症早期筛查的理想特征。对于子宫内膜癌的检测临床上主要采用阴超、或者基于子宫内膜采样器的细胞学检测以及诊断性刮宫等,一方面检测灵敏度低,另一方面直接采集子宫内膜细胞具有一定的侵入性。
9.有鉴于此,特提出本发明。
技术实现要素:
10.本发明的目的在于针对现有技术中的上述不足,提供一种检测准确性高、操作便捷快速、可为子宫内膜癌的临床诊断提供可靠参考依据的子宫内膜癌早期筛查诊断用标志物、引物、探针和试剂盒。可以以宫颈脱落细胞作为检测样本,不会对患者造成损伤,更易于被患者接受。
11.本发明具体技术方案详述如下:
12.第一方面,本发明提供了一组子宫内膜癌早期筛查诊断用标志物,选自目标基因cdo1、celf4、hand2和hs3st2中每个基因中以下任意至少一段甲基化区域:
13.cdo1基因:chr5:115816884
‑
115817037、chr5:115816018
‑
115816152、chr5:115815760
‑
115815872;
14.celf4基因:chr18:37566573
‑
37566662、chr18:37565524
‑
37565639、chr18:37565036
‑
37565173;
15.hand2基因:chr4:173530858
‑
173530953、chr4:173530225
‑
173530335、chr4:173528847
‑
173528958;
16.hs3st2基因:chr16:22813813
‑
22813928、chr16:22814029
‑
22814146、chr16:22814452
‑
22814557。
17.通过对子宫内膜癌相关基因种类,以及每个基因甲基化区域进行联合筛选,最终筛选出上述四个标志物基因(或称为靶基因),及其对应的功能最优甲基化区域,能够通过各标志物基因甲基化结果的互补性确定判读界值,各甲基化区域结果相互结合用于子宫内膜癌的早期检测时,结果准确性非常高,能够给临床医生提供辅助诊断参考。
18.可选或优选的,上述子宫内膜癌早期筛查诊断用标志物中,选自目标基因cdo1、celf4、hand2和hs3st2中每个基因中以下甲基化区域:
19.cdo1基因:chr5:115815760
‑
115815872;
20.celf4基因:chr18:37565524
‑
37565639;
21.hand2基因:chr4:173528847
‑
173528958;
22.hs3st2基因:chr16:22813813
‑
22813928。
23.上述组合检测效果最好。
24.第二方面,本发明还提供了一组子宫内膜癌早期筛查诊断用检测引物,用于对应检测上述标志物基因甲基化区域的甲基化状态,所述引物设计采用卡环式结构,引物核苷
酸序列的5’端增加一段5
‑
10bp长度的且与3’端互补配对的序列,这段序列不含cg位点,3’端的末端最后两个碱基为cg,引物双链结合区域tm值应与pcr反应体系中退火温度保持一致。
25.上述引物设计中,增加的一段5
‑
10bp长度的序列,不含cg位点,能够确保形成卡环时结合更加紧密。引物序列采用卡环式的设计结构,一是没有引物二聚体的产生,在退火的过程中,优先保持自身形成双链结构而不与其他的引物形成双链,因此引物二聚体不会形成。二是具有高特异性,由于引物自身具有卡环式结构,引物与甲基化的靶向序列结合自由能需要大于引物自身形成的环状自由能,因此当引物3’端存在不匹配碱基时,包含卡环式结构的引物几乎很难与非甲基化的序列进行结合,保持引物扩增具有更好的特异性。三是具有高灵敏性,因所使用的样本是宫颈脱落细胞,dna模板量少,模板中含有甲基化dna的含量较低,对于卡环式结构设计的引物只会单一地去匹配甲基化靶向序列,大大提升引物的扩增效率。引物的设计合成过程中无需增加其他额外的修饰,合成简单,只需要常用的合成仪即可完成。
26.上述引物因卡环式设计结构,保持引物扩增的高特异性,所以引物之间的扩增效率不会产生干扰,对于多重引物的扩增具有明显的优势。本发明采用的就是4个目标基因加上一个内参基因,在一个反应体系内进行扩增,不存在各基因引物之间扩增效率存在相互影响。
27.可选或优选的,上述子宫内膜癌早期筛查诊断用检测引物,所述检测引物的核苷酸序列如下所示:
28.cdo1基因中:
29.chr5:115816884
‑
115817037对应检测引物为seq id no:1~2,
30.chr5:115816018
‑
115816152对应检测引物为seq id no:4~5,
31.chr5:115815760
‑
115815872对应检测引物为seq id no:7~8;
32.celf4基因中:
33.chr18:37566573
‑
37566662对应检测引物为seq id no:10~11,
34.chr18:37565524
‑
37565639对应检测引物为seq id no:13~14,
35.chr18:37565036
‑
37565173对应检测引物为seq id no:16~17;
36.hand2基因中:
37.chr4:173530858
‑
173530953对应检测引物为seq id no:19~20,
38.chr4:173530225
‑
173530335对应检测引物为seq id no:22~23,
39.chr4:173528847
‑
173528958对应检测引物为seq id no:25~26;
40.hs3st2基因中:
41.chr16:22813813
‑
22813928对应检测引物为seq id no:28~29,
42.chr16:22814029
‑
22814146对应检测引物为seq id no:31~32,
43.chr16:22814452
‑
22814557对应检测引物为seq id no:34~35。
44.第三方面,本发明还提供了一组子宫内膜癌早期筛查诊断用检测探针,用于对应检测以上所述标志物基因,检测探针的核苷酸序列设计采用卡环式结构,核苷酸序列的5’端增加一段3
‑
6bp长度的且与靠近3’端末端3
‑
4bp区域进行互补配对的序列,这段序列不含cg位点,探针双链结合区域tm值应高于pcr反应体系中退火温度2~15℃,探针的核苷酸序
列与标志物基因序列的结合自由能高于探针自身形成的卡环结构;检测探针的5’端标记荧光基团,3’端标记淬灭基团,且同一检测体系中不同的标志物基因检测探针标记不同的荧光基团。
45.荧光基团包括但不限于:fam、rox、cy5、hex,淬灭基团包括但不限于bhq1、bhq2。
46.上述不同荧光通道标记的目标基因检测探针可放在一管中反应,保证样本中不同目标基因的扩增效率最佳,荧光曲线为标准的s型扩增曲线,与各基因单重扩增相比荧光曲线保持一致的趋势。
47.探针的设计同样采用卡环式设计结构,可以使荧光基团和淬灭基团靠近,探针形成环状结构时不会有荧光产生。同时探针序列中包含2
‑
5个cg位点,用于特异性识别甲基化序列。探针5’端增加一段3
‑
6bp序列与靠近3端末端3
‑
4bp区域形成碱基序列互补,且此互补区域不含cg位点,探针双链结合区域tm值要高于反应体系中退火温度2~5℃,随着cg位点的增加,需提高tm值5~10℃,具体需要根据探针的筛选结果而定。在设计探针的过程中,探针序列与靶序列的结合自由能要高于探针序列自身形成的卡环结构。
48.此种探针方式设计的优势有:一是因卡环式结构的形成,序列的荧光基团与淬灭基团相距较近,荧光淬灭效果更好,不会产生额外的荧光,因此荧光本底低。二是具有很高的特异性,一方面探针为卡环式设计结构,序列本身很难与非甲基化序列结合,另一方面探针上包含2
‑
5个cg位点,确保这个探针序列只会与匹配的甲基化序列相结合。三是高灵敏性,只需探针环状结构打开与甲基化序列结合在一起,荧光基团与淬灭基团分开,即可检测出荧光。四是适用于多重扩增反应,探针序列之间各形成卡环结构,相互之间很难进行互补配对结合,不会产生引物二聚体,也不会影响探针序列与靶序列的结合。
49.可选或优选的,上述子宫内膜癌早期筛查诊断用检测探针,检测探针的核苷酸序列如下所示:
50.cdo1基因检测探针:seq id no:9;
51.celf4基因检测探针:seq id no:15;
52.hand2基因检测探针:seq id no:27;
53.hs3st2基因检测探针:seq id no:30。
54.第四方面,本发明提供了一种子宫内膜癌早期筛查诊断用检测试剂盒,其包括以上任一所述的检测引物,以及任一所述的检测探针。
55.可选或优选的,上述子宫内膜癌早期筛查诊断用检测试剂盒中,还包括内参基因检测引物和探针,所述内参基因为gapdh,内参基因检测引物的核苷酸序列如seq id no:37~38所示,内参基因检测探针的核苷酸序列如seq id no:39所示,内参基因检测探针的核苷酸序列5’端标记荧光基团,3’端标记淬灭基团,同一检测体系中内参基因检测探针标记的荧光基团与标志物基因检测探针标记的荧光基团不同。
56.可选或优选的,上述子宫内膜癌早期筛查诊断用检测试剂盒中,还包括pcr反应液,和样本甲基化前处理试剂;所述样本为宫颈脱落细胞,所述样本甲基化前处理试剂包括细胞基因组dna提取试剂和dna重亚硫酸盐转化试剂。
57.样本前处理对于整个的试剂盒来说是具有重要作用的,直接关系到后续的pcr扩增效果。
58.该试剂盒特别适用于宫颈脱落细胞作为样本。目前临床上常用的取样方式为基于
子宫内膜细胞采样器收集子宫内膜样本或者通过刮宫的形式获得子宫内膜组织,这一采样方式对患者是具有侵入性的,且会给与患者一定的创伤性。上述试剂盒中采用的宫颈脱落细胞样本,检测的也是从子宫内膜区域脱落到宫颈部分的细胞,因此子宫内膜细胞的含量很低,但是对于样本来源来说更为简单无创易取。由于宫颈脱落细胞中子宫内膜细胞的含量较低,因此对应本试剂盒中包含的样本前处理试剂以及后续的pcr反应液尤为重要,决定是否能检测到子宫内膜细胞中dna甲基化的变化。
59.使用上述样本甲基化前处理试剂时,包括两个过程,一个是基因组dna的提取过程,另一个是重亚硫酸盐的转化过程,其中一个过程出现问题,其最终结果都会发生很大的变化。
60.细胞基因组dna提取试剂是以宫颈脱落细胞为样本,优选采用申请人自主开发的基因组dna提取试剂盒(核酸提取或纯化试剂(北京起源聚禾生物科技有限公司京大械备20210020号))对宫颈脱落细胞进行dna的提取,此提取/纯化试剂盒在开发过程中通过对比筛选不管是在dna的得率还是在dna的纯度方面均有很大的提升,提取2ml宫颈脱落细胞保存液,dna的总量在4μg
‑
8μg之间,od260/280在1.9
‑
2.0之间,保持较好的得率和纯度。
61.在dna提取完成之后,进行dna的重亚硫酸盐转化实验,需要用到dna重亚硫酸盐转化试剂。同样优选采用申请人自主开发的重亚硫酸盐转化试剂盒(甲基化检测样本前处理试剂盒(北京起源聚禾生物科技有限公司京大械备20200110号)),转化过程对比主要的指标:一是重亚硫酸盐的转化率,能将多少序列中的c转化成u,二是转化之后纯化效率为多少,即最后的bisdna得率是多少。使用上述dna重亚硫酸盐转化试剂时,重亚硫酸盐的转化效率为99.8%,纯化效率为99%,为后续的pcr扩增反应提供高质量的bisdna。
62.可选或优选的,上述子宫内膜癌早期筛查诊断用检测试剂盒中,所述pcr反应液每一人份由浓度1u/μl的甲基化特性的taq dna聚合酶0.5~1μl、浓度10mm的dntps 2~5μl、浓度2~5mm的mg
2
2~6μl、10
×
dna聚合酶buffer 5μl和纯化水补足15μl组成。
63.上述pcr反应体系中,重要的成分为甲基化特异性的taq聚合酶,主要具有以下优势:针对重亚硫酸盐转化之后的模板序列进行扩增,能特异性识别转化后序列,提高引物对转化后序列的扩增效率。酶量不够会使扩增效率下降,酶量过多容易引起非特异性扩增,因此对于酶量的多少能够显著影响后续pcr扩增结果。另外,体系中dntps、mg
2
、10
×
dna聚合酶buffer之间的配比也直接关系到引物和探针的组合的扩增效率。
64.该pcr反应体系是专门针对重亚硫酸盐转化之后的bis
‑
dna扩增,且包含多重引物探针,因此pcr反应液的选择尤其重要,体系中每一个基因引物探针的扩增效率需与其对应的单重扩增时类似,确保体系中的引物或者探针之间不相互干扰,充分发挥每一组引物探针的扩增效果。需要对不同的甲基化特异性的taq聚合酶以及与其他组分之间的配比进行筛选验证,确保整个多重扩增体系扩增效率最佳。
65.与现有技术相比,本发明具有如下有益效果:
66.1、本发明筛选出cdo1、celf4、hand2和hs3st2四个标志物基因(靶基因、目标基因),以及确定了各基因中最优的甲基化区域,能够相互结合用于子宫内膜癌的早期检测。所筛选出的区域不仅包括基因的启动子区域,还包括基因的编码区域,由于子宫内膜癌种类多样性,选择多基因甲基化区域联合检测,形成功能间的互补,显著提升对子宫内膜癌检出的灵敏度,但对正常及子宫内膜良性肿瘤具有很高特异性。该检测组合物通过分子表观
遗传手段,利用甲基化检测技术对妇科恶性肿瘤可能的患者提早检出,结果准确性非常高,能够给临床医生提供辅助诊断参考,提早进行预防治疗。
67.2、针对四个联合标志物基因特定甲基化位点设计检测引物和探针,均采用卡环式设计结构,对甲基化模板可以进行双重识别,显著提高检测的灵敏度、特异性,增加检测的准确性,减少检测的误差。对于以宫颈脱落细胞作为样本、dna量少,dna甲基化量更少的情况来说,提高灵敏度是非常重要的,采用本发明的引物和探针,能够以少量样本得出准确检测结果,更适合临床应用。
68.所有引物和探针构成的检测体系,还可以采用多基因多通道荧光检测手段,利用五种荧光探针标记通过特异性引物探针与甲基化序列准确识别,以及优化的特殊的甲基化dna taq聚合酶,对cdo1、celf4、hand2和hs3st2基因甲基化位点精确检测,批量完成多基因甲基化位点检测,检测方法操作简单、判读直观、8个小时内出结果,通用的荧光定量pcr仪均能满足检测需求,整套实验流程采用一站式全封闭形式,操作更简便,也避免了交叉污染的可能。
69.3、试剂盒中的样本甲基化前处理试剂和pcr反应液,分别为宫颈脱落细胞的dna提取及前处理和后续的pcr反应提供了保障。目前pcr扩增中出现非特异性扩增(产生假阳性结果)的现象较多,目前最主流的重亚硫酸盐转化技术对提取后的样本进行转化处理,受限于目前重亚硫酸盐转化技术的限制,除了会有约80%左右的目的基因组可能发生损耗外,还会有一定概率的未转化完成的模板,是存在可能造成假阳性结果的原因。本发明除了在目标基因引物探针的设计采用卡环式结构,增加扩增的灵敏度和特异性,在样本甲基化前处理(包含dna提取和重亚硫酸盐转化)方面也进行了优化以提高最终的bisdna的转化得率。
70.4、试剂盒结合特异性引物探针、样本前处理试剂、pcr反应液的dna聚合酶等,保证了试剂盒使用时保持高灵敏度,引物探针特异性好,扩增效率高,对于低浓度的模板也有非常好的检测率,对早期子宫内膜癌的检测非常灵敏。本试剂盒检测的高灵敏性适用于子宫内膜癌的早期检测。
附图说明
71.图1为cdo1、celf4、hand2和hs3st2各基因筛选甲基化区域的roc曲线;
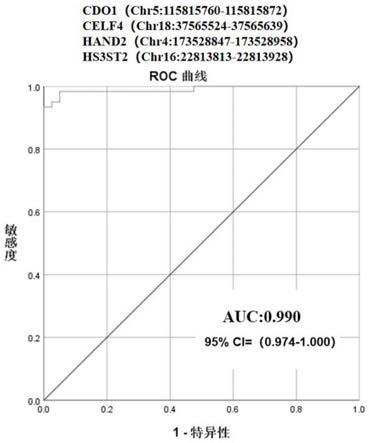
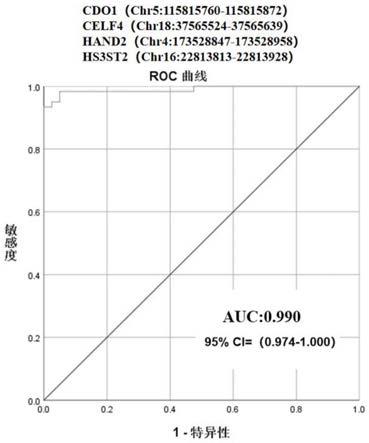
72.图2为cdo1、celf4、hand2和hs3st2联合检测的roc曲线。
具体实施方式
73.下面结合符合图较佳的具体实施例,对本发明的技术方案进行详细解释和说明,以是本领域技术人员能够更好地理解本发明并予以实施。
74.实施例1
75.检测子宫内膜癌相关基因cdo1、celf4、hand2和hs3st2甲基化试剂盒的检测试验。
76.所用引物和探针的具体核苷酸序列如下表所示:
77.[0078][0079]
注:f表示正向检测引物,r表示反向检测引物,fp表示检测探针。本表格中,所展示的探针序列已经进行了荧光基团标记和淬灭基团标记。
[0080]
无样本前处理试剂的试剂盒组分如下表:
[0081]
[0082][0083]
选取已知明确病理信息结果的60例子宫内膜癌样本:15例鉴定为子宫内膜样癌、15例子宫内膜黏液性癌、15例子宫内膜浆液性癌、15例子宫内膜透明细胞癌;40例为子宫内膜良性样本。以上样本均为宫颈脱落细胞留样获得。
[0084]
一、样本甲基化前处理
[0085]
样本甲基化前处理试剂包括细胞基因组dna提取试剂和dna重亚硫酸盐转化试剂。
[0086]
1、采用公司自主开发的基因组dna提取试剂盒(核酸提取或纯化试剂(北京起源聚禾生物科技有限公司京大械备20210020号))作为细胞基因组dna提取试剂,对上述100例子宫内膜良恶性宫颈脱落细胞样本进行基因组dna的提取,同时进行dna质量监控。dna的总量在4μg
‑
8μg之间,od260/280在1.9
‑
2.0之间,保持较好的得率和纯度。
[0087]
2、采用公司自主开发的重亚硫酸盐转化试剂盒(甲基化检测样本前处理试剂盒(北京起源聚禾生物科技有限公司京大械备20200110号))作为dna重亚硫酸盐转化试剂,对提取好的dna进行重亚硫酸盐转化,dna中未甲基化的胞嘧啶(c)转变为尿嘧啶(u),而甲基化的胞嘧啶(c)不变,得到转化后的bis
‑
dna。本实施例中重亚硫酸盐的转化效率为99.8%,高于市场上多数重亚硫酸盐转化试剂盒。
[0088]
二、bis
‑
dna进行荧光定量pcr扩增
[0089]
3、配制pcr反应液和引物探针混合液;
[0090]
pcr反应液(15μl/人份)
[0091][0092][0093]
引物探针混合液(5μl/人份)
[0094]
组分一人份加入量(μl)
cdo1/celf1/hand2/hs3st2
‑
f(100μm)0.2
‑
0.8cdo1/celf1/hand2/hs3st2
‑
r(100μm)0.2
‑
0.8cdo1/celf1/hand2/hs3st2
‑
fp(100μm)0.2
‑
0.4gapdh基因
‑
f(100μm)0.05gapdh基因
‑
r(100μm)0.05gapdh基因
‑
fp(100μm)0.05纯化水补足至5μl
[0095]
4、加样
[0096]
向上述配制的体系中分别加入5μl阴、阳性质控品和转化好的bis
‑
dna临床样本。进行pcr反应,条件为:96℃预变性5min;94℃变性15s,60℃退火延伸35s,45个循环;25℃保持10min。
[0097]
5、扩增程序如下:
[0098]
step1:96℃预变性5min;
[0099]
step2:94℃变性15s,60℃退火延伸35s,45个循环;
[0100]
step3:25℃,10min;
[0101]
信号收集,60℃收集fam、hex、rox、joe以及cy5信号。
[0102]
6、结果判读
[0103]
(1)内标通道有s型扩增曲线且ct值≤32.2为结果有效;
[0104]
(2)4个基因的δct值分别为:
[0105]
δct(cdo1)=ct(cdo1)
‑
ct(gapdh);
[0106]
δct(celf4)=ct(celf4)
‑
ct(gapdh);
[0107]
δct(hand2)=ct(hand2)
‑
ct(gapdh);
[0108]
δct(hs3st2)=ct(hs3st2)
‑
ct(gapdh)。
[0109]
(3)综合上述4个基因的δct值,根据roc曲线确定目标基因多个甲基化区域的界值和性能(包括特异性、灵敏度、阴性预测值、阳性预测值),确定最优甲基化区域,以及4个目标基因的判读方式。
[0110]
7、检测结果分析
[0111]
利用上述试剂盒反应体系检测共100例样本,其中包括子宫内膜癌样本60例,子宫内膜良性样本40例。
[0112]
对比临床病理结果,在100例宫颈脱落细胞样本中,
[0113]
cdo1(chr5:115816884
‑
115817037)在子宫内膜癌中的阳性率为58.3%(35/60),在良性样本中的特异性为82.5%(33/40),roc面积为0.728;
[0114]
cdo1(chr5:115816018
‑
115816152)在子宫内膜癌中的阳性率为50%(30/60),在良性样本中的特异性为92.5%(37/40),roc面积为0.714;
[0115]
cdo1(chr5:115815760
‑
115815872)在子宫内膜癌中的阳性率为68.3%(41/60),在良性样本中的特异性为80%(32/40),roc面积为0.767;
[0116]
celf4(chr18:37566573
‑
37566662)在子宫内膜癌中的阳性率为61.7%(37/60),在良性样本中的特异性为90%(36/40),roc面积为0.776;
[0117]
celf4(chr18:37565524
‑
37565639)在子宫内膜癌中的阳性率为73.3%(44/60),
在良性样本中的特异性为87.5%(35/40),roc面积为0.847;
[0118]
celf4(chr18:37565036
‑
37565173)在子宫内膜癌中的阳性率为86.7%(52/60),在良性样本中的特异性为62.5%(25/40),roc面积为0.792;
[0119]
hand2(chr4:173530858
‑
173530953)在子宫内膜癌中的阳性率为46.7%(28/60),在良性样本中的特异性为100%(40/40),roc面积为0.742;
[0120]
hand2(chr4:173530225
‑
173530335)在子宫内膜癌中的阳性率为60%(36/60),在良性样本中的特异性为95%(38/40),roc面积为0.811;
[0121]
hand2(chr4:173528847
‑
173528958)在子宫内膜癌中的阳性率为78.3%(47/60),在良性样本中的特异性为90%(36/40),roc面积为0.882;
[0122]
hs3st2(chr16:22813813
‑
22813928)在子宫内膜癌中的阳性率为86.7%(52/60),在良性样本中的特异性为95%(38/40),roc面积为0.915;
[0123]
hs3st2(chr16:22814029
‑
22814146)在子宫内膜癌中的阳性率为66.7%(40/60),在良性样本中的特异性为95%(38/40),roc面积为0.790;
[0124]
hs3st2(chr16:22814452
‑
22814557)在子宫内膜癌中的阳性率为91.7%(55/60),在良性样本中的特异性为65%(26/40),roc面积为0.797。
[0125]
经过cdo1、celf4、hand2和hs3st2多甲基化区域对比分析,cdo1基因选择的甲基化区域为chr5:115815760
‑
115815872,celf4基因选择的甲基化区域为chr18:37565524
‑
37565639,hand2基因选择的甲基化区域为chr4:173528847
‑
173528958,hs3st2选择的甲基化区域为chr16:22813813
‑
22813928)。
[0126]
根据cdo1、celf4、hand2和hs3st2的各最佳甲基化区域进行联合检测,可以两个基因参与判读、也可以三个或四个基因同时参与判读分析,可以得到如下表结果:
[0127]
表1两个基因联合检测性能
[0128][0129]
表2三个基因联合检测性能
[0130][0131][0132]
表3四个基因联合检测性能
[0133][0134]
从上表中我们可以得到,4个基因中任意两个同时为阳性,在子宫内膜癌中的阳性率为98.3%(59/60),在良性样本中的特异性为100%(40/40),检测得到的roc面积为0.990。
[0135]
因此通过实例1可以分析得出,cdo1、celf4、hand2、hs3st2联合检测对子宫内膜癌的检出率最高,且具有很好的特异性。通过小量样本的验证,确定了dna甲基化对于子宫内膜癌早期检测的初步应用,并且可以通过宫颈脱落细胞可以具有高检出率,并且假阳性率很低。
[0136]
实施例2
[0137]
试剂盒中其他成分与实施例1相同。实例1中进行小量单中心样本的测试,接下来收集多中心样本近1000例样本的检测,多中心分别包括北京协和医院、北京大学国际医院、解放军总医院、内蒙古自治区人民医院、河北沧州市中心医院,其中子宫内膜癌样本450例,子宫内膜良性样本650例,共1100例样本。
[0138]
对比组织病理学病理结果,使用本甲基化检测试剂盒得到的联合roc曲线面积为0.98,整体特异性为98.5%(640/650),子宫内膜癌检出灵敏度为98.9%%(445/450)。
[0139]
本发明中的试剂盒通过小量样本验证到大量样本研究,均证明dna甲基化对于子宫内膜癌早期检测具有很高的准确性,并且通过宫颈脱落细胞即可检测。本发明运用了特
殊的引物探针设计方法以及公司自主研发的样本前处理试剂盒,多基因联合检测,功能互补,显著提高对早期子宫内膜癌的检出。
[0140]
本文中应用了具体个例对发明构思进行了详细阐述,以上实施例的说明只是用于帮助理解本发明的核心思想。应当指出,对于本技术领域的普通技术人员来说,在不脱离该发明构思的前提下,所做的任何显而易见的修改、等同替换或其他改进,均应包含在本发明的保护范围之内。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。