一种(e)-3,5-二羟基-4-异丙基二苯乙烯的合成方法
技术领域
1.本发明涉及药物合成技术领域,特别涉及一种(e)-3,5-二羟基
⁃4⁃
异丙基二苯乙烯的合成方法。
背景技术:
2.本维莫德,中文化学名称为(e)
⁃
3,5
⁃
二羟基
⁃4⁃
异丙基二苯乙烯,分子式为c
17h18
o2,最早是在1981年从土壤光杆线虫共生菌代谢产物中分离出的一种天然小分子化合物,而后又在发光杆菌、异小杆线虫、大蜡螟等中发现这种化合物。随后,本维莫德被证明有多种优秀的生物活性。本维莫德由冠昊生物科技股份有限公司研制,其乳膏剂为我国拥有完整自主知识产权的国家i类新药,主要用于治疗炎症反应及自身免疫反应,还可以抑制与过敏反应相关的肥大细胞和嗜碱性细胞的脱粒作用,同时对银屑病也有较好的治疗效果。但是,对于这种化合物的化学全合成,直到2009年才陆续被报道。目前,本维莫德的化学全合成已经有几条合成路线,但多有弊端如化学废料(如氯铬酸吡啶、磷酸二乙酯等产生的废产物)多、试剂活泼(如kbh4、socl2、br2、lialh4、nbuli等)污染性大,合成路线长(合成步骤多达6步以上)等,这些缺点也是造成本维莫德合成成本居高不下的原因。
3.因此,寻找一种合成步骤少、反应绿色环保的本维莫德合成方法具有重要的意义。
技术实现要素:
4.为了解决上述现有技术中存在的问题,本发明的主要目的是提供一种(e)-3,5-二羟基
⁃4⁃
异丙基二苯乙烯的合成方法。
5.为实现上述目的,本发明提出了一种(e)-3,5-二羟基
⁃4⁃
异丙基二苯乙烯的合成方法,包括以下步骤:(1)以3,5-二甲氧基溴化苯为起始原料,在酸性条件下经异丙基化反应得到3,5-二甲氧基-4-异丙基溴化苯;(2)将所述3,5-二甲氧基-4-异丙基溴化苯在钯催化剂条件下与苯乙烯发生heck反应得到(e)
⁃
3,5
⁃
二甲氧基
⁃4⁃
异丙基二苯乙烯;(3)对所述(e)
⁃
3,5
⁃
二甲氧基
⁃4⁃
异丙基二苯乙烯进行脱甲基反应得到所述(e)-3,5-二羟基
⁃4⁃
异丙基二苯乙烯。
6.上述合成方法的合成路径如下:
本发明技术方案中提供的合成方法,以3,5-二甲氧基溴化苯为起始原料,仅需三步即可合成本维莫德,相较于现有的工艺路线,大大缩短了合成路径,具有更高的原子利用率,采用本发明的合成方法合成本维莫德的收率更高。并且,本发明提供的合成方法中,由于不需要添加如氯铬酸吡啶、磷酸二乙酯等物质,也不需要添加如kbh4、socl2、br2、lialh4、nbuli等活泼试剂,因而相较于现有的工艺路线更加绿色环保。
7.作为本发明所述合成方法的优选实施方式,所述步骤(1)包括:将3,5-二甲氧基溴化苯溶解于浓酸物质中,在加热条件下继续加入异丙醇发生异丙基化反应,反应完成后将反应液冷却至室温,后处理后得到所述3,5-二甲氧基-4-异丙基溴化苯。
8.作为本发明所述合成方法的优选实施方式,所述步骤(1)中的浓酸物质为浓硫酸,所述加热条件对应的温度为70~85oc,优选为80oc;以及以所述3,5-二甲氧基溴化苯的添加量为参照,所述异丙醇的加入量为1.1~1.5当量,优选为1.2当量,异丙基化反应时间为3~5h,优选反应时间为4h。
9.作为本发明所述合成方法的优选实施方式,所述步骤(1)中的后处理包括:将所述反应液冷却至室温后,加水稀释,后用乙酸乙酯萃取,收集乙酸乙酯层,干燥、浓缩、柱层析得到所述3,5-二甲氧基-4-异丙基溴化苯。
10.作为本发明所述合成方法的优选实施方式,所述步骤(2)包括:将所述3,5-二甲氧基-4-异丙基溴化苯、所述钯催化剂、溶剂和配体混合,继续加入苯乙烯和碱性物质,在加热条件下发生所述heck反应,后处理后得到所述(e)
⁃
3,5
⁃
二甲氧基
⁃4⁃
异丙基二苯乙烯。
11.作为本发明所述合成方法的优选实施方式,所述步骤(2)中的钯催化剂包括醋酸钯、氯化钯和(1,5-环辛二烯)二氯化钯中的至少一种,优选为(1,5-环辛二烯)二氯化钯;所述溶剂包括n-甲基吡咯烷酮、n, n-二甲基甲酰胺和乙腈中的至少一种,优选为n-甲基吡咯烷酮;所述配体包括三(邻甲苯基)膦、三苯基膦和三(二乙氨基)膦中的至少一种,优选为三(二乙氨基)膦;以及所述碱性物质包括碳酸钾、碳酸钠、碳酸铯和三乙胺中的至少一种,优选为碳酸钾。
12.作为本发明所述合成方法的优选实施方式,所述步骤(2)中的反应温度为120~
140oc,优选为120oc;以及以所述3,5-二甲氧基-4-异丙基溴化苯的添加量为参照,所述苯乙烯的加入量为1.5~2当量,优选为1.5当量。
13.作为本发明所述合成方法的优选实施方式,按照摩尔百分比计,所述步骤(2)中的钯催化剂的加入量为3,5-二甲氧基-4-异丙基溴化苯的0.05~0.1%,优选为0.1%;以及所述配体与所述钯催化剂的添加量之比为2:1。
14.作为本发明所述合成方法的优选实施方式,所述步骤(2)中的后处理方法包括:将反应液冷却到室温后,加盐酸稀溶液淬灭,用乙酸乙酯萃取,收集乙酸乙酯层,干燥、浓缩、柱层析得到所述(e)
⁃
3,5
⁃
二甲氧基
⁃4⁃
异丙基二苯乙烯。
15.作为本发明所述合成方法的优选实施方式,所述步骤(3)包括:将所述(e)
⁃
3,5
⁃
二甲氧基
⁃4⁃
异丙基二苯乙烯在低温下经三溴化硼处理,脱甲基化反应得到所述(e)
⁃
3,5
⁃
二羟基
⁃4⁃
异丙基二苯乙烯。
16.相对于现有技术,本发明的有益效果为:(1)本发明技术方案中提供的合成方法,以3,5-二甲氧基溴化苯为起始原料,仅需三步即可合成本维莫德,相较于现有的工艺路线,大大缩短了合成路径,具有更高的原子利用率,本维莫德的收率更高,且操作简单适合产业化;(2)本发明提供的合成方法中,由于不需要添加如氯铬酸吡啶、磷酸二乙酯等物质,也不需要添加如kbh4、socl2、br2、lialh4、nbuli等活泼试剂,因而相较于现有的工艺路线更加绿色环保。
附图说明
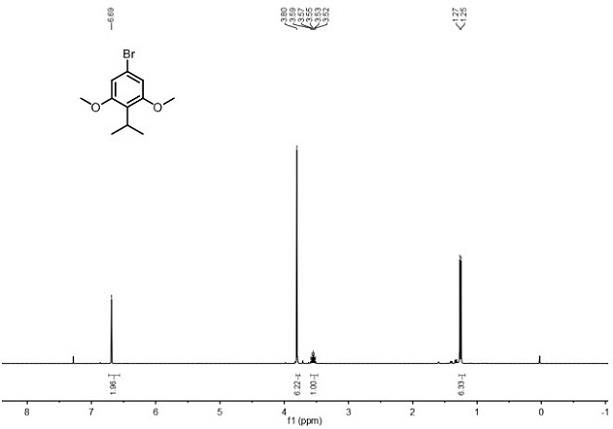
17.图1为实施例1中制备的3,5-二甲氧基-4-异丙基溴化苯的1hnmr谱图(400mhz,cdcl3);图2为实施例1中制备的3,5-二甲氧基-4-异丙基溴化苯的
13
cnmr谱图(100mhz,cdcl3);图3为实施例3中制备的(e)
⁃
3,5
⁃
二甲氧基
⁃4⁃
异丙基二苯乙烯的1hnmr谱图(400mhz,cdcl3);图4为实施例3中制备的(e)
⁃
3,5
⁃
二甲氧基
⁃4⁃
异丙基二苯乙烯的
13
cnmr谱图(100mhz,cdcl3);图5为实施例6中制备的(e)
⁃
3,5
⁃
二羟基
⁃4⁃
异丙基二苯乙烯的1hnmr谱图(400mhz,cdcl3);以及图6为实施例6中制备的(e)
⁃
3,5
⁃
二羟基
⁃4⁃
异丙基二苯乙烯的
13
cnmr谱图(100mhz,cdcl3)。
具体实施方式
18.为更好地说明本发明的目的、技术方案和优点,下面将通过具体实施例对本发明作进一步说明。
19.实施例1(3,5-二甲氧基-4-异丙基溴化苯的制备)在三口瓶中加入4.3g(20 mmol)3,5-二甲氧基溴化苯,氮气保护下,加入50ml 85%的浓硫酸,搅拌均匀后加热到80oc,接着缓慢滴加1.32 g(22 mmol)异丙醇,反应4小时后,
冷却到室温后,加入50 ml水,加入100 ml乙酸乙酯,萃取,油相旋干,用石油醚过硅胶柱,得到3.4g白色固体。
20.表征数据:1h nmr (400 mhz, chloroform-d) δ 6.69 (s, 2h), 3.80 (s, 6h), 3.55 (p, j = 7.1 hz, 1h), 1.26 (d, j = 7.1 hz, 6h);
13
c nmr (101 mhz, cdcl3) δ 158.12, 122.53, 118.56, 107.27, 55.03, 23.10, 19.56。
21.对上述白色固体进行1h nmr和
13
c nmr分析,1h nmr谱图如图1所示,
13
c nmr谱图如图2所示,确定白色固体即为3,5-二甲氧基-4-异丙基溴化苯。经计算,产率=3.4
÷
(20
×
259
×
10-3
)
×
100%,即本实施例中3,5-二甲氧基-4-异丙基溴化苯的产率为66%。
22.实施例2(3,5-二甲氧基-4-异丙基溴化苯的制备)在三口瓶中加入4.3g(20 mmol)3,5-二甲氧基溴化苯,氮气保护下,加入50ml 85%的浓硫酸,搅拌均匀后加热到80oc,接着缓慢滴加1.8 g(30mmol)异丙醇,反应4小时后,冷却到室温后,加入50 ml水,加入100 ml乙酸乙酯,萃取,油相旋干,用石油醚过硅胶柱,得到4.2g白色固体。
23.对上述白色固体进行1h nmr和
13
c nmr分析,确定白色固体即为3,5-二甲氧基-4-异丙基溴化苯。经计算,产率=4.2
÷
(20
×
259
×
10-3
)
×
100%,即本实施例中3,5-二甲氧基-4-异丙基溴化苯的产率为81%。
24.实施例3((e)
⁃
3,5
⁃
二甲氧基
⁃4⁃
异丙基二苯乙烯的制备)在三口瓶中加入2.6 g(10 mmol)3,5-二甲氧基-4-异丙基溴化苯,氮气保护下,加入30ml n-甲基吡咯烷酮,再加入0.05 % (1,5-环辛二烯)二氯化钯和0.1%三(二乙氨基)膦,然后加入1.56 g (15 mmol)苯乙烯和2.1 g(15 mmol)碳酸钾,加热到120℃反应12小时。冷却到室温后,加入10 ml 6%的盐酸,加入100 ml乙酸乙酯,萃取,油相旋干,用石油醚过硅胶柱,得到2.54g白色固体。
25.表征数据:1h nmr (400 mhz, chloroform-d) δ 7.57
–
7.49 (m, 2h), 7.38 (t, j = 7.7 hz, 2h), 7.31
–
7.24 (m, 1h), 7.08 (s, 2h), 6.72 (s, 2h), 3.88 (s, 6h), 3.64
–
3.57 (m, 1h), 1.31 (d, j = 7.1 hz, 6h);
13
c nmr (101 mhz, cdcl3) δ 158.87, 137.52, 136.03, 129.18, 128.81, 128.16, 127.64, 126.58, 124.66, 103.08, 55.93, 24.33, 20.84。
26.对上述白色固体进行1h nmr和
13
c nmr分析,1h nmr谱图如图3所示和
13
c nmr谱图如图4所示,确定白色固体即为(e)
⁃
3,5
⁃
二甲氧基
⁃4⁃
异丙基二苯乙烯。经计算,产率=2.54
÷
(10
×
282
×
10-3
)
×
100%,即本实施例中(e)
⁃
3,5
⁃
二甲氧基
⁃4⁃
异丙基二苯乙烯的产率为90%。
27.实施例4((e)
⁃
3,5
⁃
二甲氧基
⁃4⁃
异丙基二苯乙烯的制备)在三口瓶中加入2.6 g(10 mmol)3,5-二甲氧基-4-异丙基溴化苯,氮气保护下,加入30ml n, n-二甲基甲酰胺,再加入0.05 % (1,5-环辛二烯)二氯化钯和0.1%三(二乙氨基)膦,然后加入1.56 g (15 mmol)苯乙烯和2.1 g(15 mmol)碳酸钾,加热到120℃反应12小时。冷却到室温后,加入10 ml 6%的盐酸,加入100 ml乙酸乙酯,萃取,油相旋干,用石油醚过硅胶柱,得到1.41g白色固体。
28.对上述白色固体进行1h nmr和
13
c nmr分析,确定白色固体即为(e)
⁃
3,5
⁃
二甲氧基
⁃4⁃
异丙基二苯乙烯。经计算,产率=1.41
÷
(10
×
282
×
10-3
)
×
100%,即本实施例中(e)
⁃
3,5⁃
二甲氧基
⁃4⁃
异丙基二苯乙烯的产率为50%。
29.实施例5((e)
⁃
3,5
⁃
二甲氧基
⁃4⁃
异丙基二苯乙烯的制备)在三口瓶中加入2.6 g(10 mmol)3,5-二甲氧基-4-异丙基溴化苯,氮气保护下,加入30ml n-甲基吡咯烷酮,再加入0.1% (1,5-环辛二烯)二氯化钯和0.2%三(二乙氨基)膦,然后加入1.56 g (15 mmol)苯乙烯和2.8 g(20 mmol)碳酸钾,加热到120℃反应24小时。冷却到室温后,加入10 ml 6%的盐酸,加入100 ml乙酸乙酯,萃取,油相旋干,用石油醚过硅胶柱,得到2.67g白色固体。
30.对上述白色固体进行1h nmr和
13
c nmr分析,确定白色固体即为(e)
⁃
3,5
⁃
二甲氧基
⁃4⁃
异丙基二苯乙烯。经计算,产率=2.67
÷
(10
×
282
×
10-3
)
×
100%,即本实施例中(e)
⁃
3,5
⁃
二甲氧基
⁃4⁃
异丙基二苯乙烯的产率为95%。
31.实施例6((e)
⁃
3,5
⁃
二羟基
⁃4⁃
异丙基二苯乙烯的制备)在三口瓶中加入1.41 g(5 mmol)(e)
⁃
3,5
⁃
二甲氧基
⁃4⁃
异丙基二苯乙烯,氮气保护下,加入150 ml干燥二氯甲烷,冷却到-20℃,然后慢慢滴入三溴化硼溶液(8.5 g, 33.5 mmol, 30% in dcm)。搅拌慢慢回稳到室温,反应4个小时;反应结束后,倒入到装有100 ml水的烧杯中,用二氯甲烷(3x50 ml)萃取,再用饱和食盐水洗涤,最后用无水硫酸钠干燥后,旋干过柱,得到1.04g白色固体。
32.表征数据:1h nmr (400 mhz, chloroform-d) δ 7.54
–
7.43 (m, 2h), 7.37 (dd, j = 8.4, 6.8 hz, 2h), 7.32
–
7.23 (m, 1h), 6.96 (q, j = 16.3 hz, 2h), 6.52 (s, 2h), 4.85 (s, 2h), 3.48 (p, j = 7.1 hz, 1h), 1.40 (d, j = 7.1 hz, 6h);
13
c nmr (101 mhz, cdcl3) δ 155.10, 137.34, 136.42, 128.83, 127.91, 127.79, 126.64, 120.49, 109.56, 107.05, 24.79, 20.90。
33.对上述白色固体进行1h nmr和
13
c nmr分析,1h nmr谱图如图5所示和
13
c nmr谱图如图6所示,确定白色固体即为(e)
⁃
3,5
⁃
二羟基
⁃4⁃
异丙基二苯乙烯。经计算,产率=1.04
÷
(5
×
254
×
10-3
)
×
100%,即本实施例中(e)
⁃
3,5
⁃
二羟基
⁃4⁃
异丙基二苯乙烯的产率为82%。
34.采用上述实施例合成(e)
⁃
3,5
⁃
二羟基
⁃4⁃
异丙基二苯乙烯的最高收率为:81%*95%*82%=63%。
35.最后所应当说明的是,以上实施例仅用以说明本发明的技术方案而非对本发明保护范围的限制,尽管参照较佳实施例对本发明作了详细说明,本领域的普通技术人员应当理解,可以对本发明的技术方案进行修改或者等同替换,而不脱离本发明技术方案的实质和范围。
再多了解一些
本文用于创业者技术爱好者查询,仅供学习研究,如用于商业用途,请联系技术所有人。
