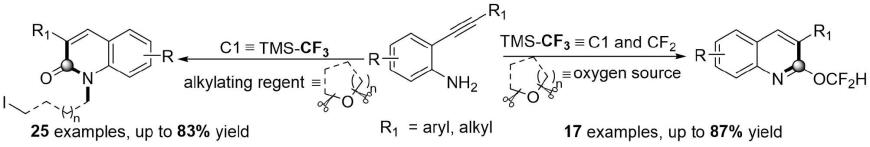
铜催化2-炔基苯胺的选择性环化生成喹啉类和喹诺酮类衍生物
【技术领域】
1.本发明涉及一种通过使用2-氨基炔烃类化合物,tmscf3和thf在氮气条件下,通过温度的控制分别生成了2-二氟甲基醚-3-取代喹啉和2-喹诺酮类化合物。tmscf3在反应中不仅作为c1源出现,更是作为cf2的原料,因此,说明tmscf3试剂是一种多功能的氟化试剂及碳源试剂。环醚在此反应中不仅是承担着溶剂的作用,同样也是目标产物的氧源和烷烃提供者。
背景技术:
2.喹啉及喹诺酮衍生物作为生物碱广泛存在于自然界,不仅具有良好的生物药理活性,在荧光和磷光探针分子领域具有重要的应用;作为高效的催化剂或配体,在手性分子合成中也扮演着重要的角色。基于喹啉及喹诺酮化合物不同领域的应用,如何高效绿色地合成具有喹啉和喹诺酮骨架的衍生物一直是有机化学家追求的目标。特别是2-烷氧基喹啉是广泛存在于生物活性医药中的基础结构,比如贝达喹啉(bedaquiline)被世卫组织认定为治疗耐多药结核病的首选药物,他非诺喹(tafenoquine)是一种喹啉类抗疟疾新药,和局部麻醉剂等。同样,2-喹诺酮也是多种医药药物中的核心骨架,比如拉喹莫德(laquinimod),是一种有效的免疫调节剂,可预防中枢神经系统的神经变性和炎症;替吡法尼(tipifarnib)是可以很好的抑制法尼基转移酶,具有潜在抗肿瘤活性。将丰富的可再生生物质转化为增值原材料,为全球对化学品和燃料日益增长的需求提供了一个潜在的可持续解决方案。四氢呋喃和四氢吡喃衍生物等环醚是重要的目标,因为它们很容易从乙酰丙酸和糠醛等生物质衍生中间体中获得。如何将环醚化合物通过一种高效,高选择性的途径转化成碳氢化合物是生物质研究中的一大挑战,其中除了通过催化加氢除氧的方式以外,通过仅仅除氧获得高附加值的化学品也是一种可行性途径。目前环醚去氧中转化中较为常见一种策略是,通过碘化钐等途径将环醚去氧生成二碘化物,也可以通过其他方式得到二氯化合物。但是,通过去氧双官能团化的途径获得高附加值化学品的过程是罕见的,是难以实现的。我组在以前的工作中实现了环醚通过脱氧与有机羧酸构建碘代烷基酯类化合物,是首次实现环醚去氧的双官能化研究。在此课题组我们使用2-氨基炔烃类化合物与环醚同样获得了双管能团的喹诺酮类目标产物,再次为环醚类去氧双官能团化反应做出了贡献,也为合成2-喹诺酮类衍生物提供了全新的合成途径。
3.由于氟原子具有最大的电负性、较小的原子半径以及含氟基团特殊的亲脂性,含氟化合物在医药、农药、材料等领域具有广泛的应用。其中二氟甲氧基作为醇羟基和硫羟基的生物电子等排体,可以更好地提高生物活性分子代谢稳定性和生物利用度,发展合成2-位含有二氟甲氧基喹啉类化合物的新方法对于药物的发现和发展有重要意义。目前合成2-二氟甲基醚喹啉类的方法鲜有人涉及,目前仅是通过2-喹诺酮或者二氢喹啉酮与氟化烷基试剂生成目标物,但底物普适性较差,一般需要多步一锅法进行,这通常会导致挂能团兼容性较差,以及较长时间的保护或基脱保护导致无法产率降低等现象,因此仍然需要直接的
策略构建此类化合物。在此,我们使用2-炔基苯胺与tmscf3直接构建多样性的2-二氟甲基醚-3-取代喹啉。目前,国内外还没有方法合成2-二氟甲氧基-3-取代喹啉和n-取代-2-喹诺酮类化合物的公开文献和专利申请。
技术实现要素:
4.本发明开发了一种以廉价铜为催化剂制备2-二氟甲氧基-3-取代喹啉和n-取代-2-喹诺酮类化合物的高效、简便的方法。反应对各种末端炔烃表现出耐受性,相应产物具有较高的化学选择性和区域选择性,且反应条件温和。该催化方案具有原料广泛、无贵金属和有害副产品等优点。并且,这些产品构成了多功能的亲电试剂,在有机合成和化学生物学中都有应用。
[0005][0006]
其中所述r1为芳香性基团(苯基等);r为取代基团(卤素、甲基等)。
【附图说明】
[0007]
附图1所示是2-二氟甲氧基-3-取代喹啉和n-取代-2-喹诺酮类化合物合成的路线图。
【具体实施方式】
[0008][0009]
其中所述r1为芳香性基团(苯基等);r为取代基团(卤素、甲基等)。
[0010]
实例1:
[0011]
向装有磁力搅拌的10ml schlenk管中添加2-((4-甲氧基苯基)乙炔基)苯胺(0.30mmol, 1.0当量)、cui(0.03mmol,0.1当量)和碘化钠(nai,0.60mmol,2.0当量)。用泵抽真空后填充氮气,三次。然后,在n2气氛下添加1.0ml超干溶剂四氢呋喃,三氟甲基三甲基硅烷(tmscf3,0.36mmol,1.2当量),去离子水(0.45mmol,1.5当量)。该混合物在50℃下搅拌12小时(恒温油浴锅)。冷却至室温后,该混合物用乙酸乙酯稀释后,加入适量水,再用乙酸乙酯萃取三次,收集有机相,并加入适量的无水na2so4脱水合并的有机层,在减压下浓缩。粗产物在硅胶上通过柱色谱分离方法,得到纯化的2-二氟甲氧基-3-取代喹啉。
[0012]
通过柱色谱法分离纯化(石油醚/乙酸乙酯=250:1),得到标题化合物,为黄色固体。收率:75.9mg,84%。1h nmr(400mhz,cdcl3)δ8.11(s,1h),7.89(d,j=8.4hz,1h),7.81(s, 1h),7.79(d,j=1.4hz,1h),7.67(m,1h),7.61
–
7.53(m,2h),7.49(m,1h),7.06
–
6.97(m,2h), 3.87(s,3h).
13
c nmr(101mhz,cdcl3)δ159.7,154.7,144.4,139.2,130.7,129.9,127.5,127.4, 127.4,126.7,125.9,125.3,116.8,114.3,114.0,111.7,55.4.
19
f nmr
(377mhz,cdcl3)δ-89.63.
[0013]
实例2:
[0014]
向装有磁力搅拌的10ml schlenk管中添加2-((4-乙氧基苯基)乙炔基)苯胺(0.30mmol, 1.0当量)、cui(0.03mmol,0.1当量)和碘化钠(nai,0.60mmol,2.0当量)。用泵抽真空后填充氮气,三次。然后,在n2气氛下添加1.0ml超干溶剂四氢呋喃,三氟甲基三甲基硅烷(tmscf3,0.36mmol,1.2当量),去离子水(0.45mmol,1.5当量)。该混合物在50℃下搅拌12小时(恒温油浴锅)。冷却至室温后,该混合物用乙酸乙酯稀释后,加入适量水,再用乙酸乙酯萃取三次,收集有机相,并加入适量的无水na2so4脱水合并的有机层,在减压下浓缩。粗产物在硅胶上通过柱色谱分离方法,得到纯化的2-二氟甲氧基-3-取代喹啉。
[0015]
实例3:
[0016]
向装有磁力搅拌的10ml schlenk管中添加2-((3-甲氧基苯基)乙炔基)苯胺(0.30mmol, 1.0当量)、cui(0.03mmol,0.1当量)和碘化钠(nai,0.60mmol,2.0当量)。用泵抽真空后填充氮气,三次。然后,在n2气氛下添加1.0ml超干溶剂四氢呋喃,三氟甲基三甲基硅烷(tmscf3,0.36mmol,1.2当量),去离子水(0.45mmol,1.5当量)。该混合物在50℃下搅拌12小时(恒温油浴锅)。冷却至室温后,该混合物用乙酸乙酯稀释后,加入适量水,再用乙酸乙酯萃取三次,收集有机相,并加入适量的无水na2so4脱水合并的有机层,在减压下浓缩。粗产物在硅胶上通过柱色谱分离方法,得到纯化的2-二氟甲氧基-3-取代喹啉。
[0017]
实例4:
[0018]
向装有磁力搅拌的10ml schlenk管中添加2-((2-甲氧基苯基)乙炔基)苯胺(0.30mmol, 1.0当量)、cui(0.03mmol,0.1当量)和碘化钠(nai,0.60mmol,2.0当量)。用泵抽真空后填充氮气,三次。然后,在n2气氛下添加1.0ml超干溶剂四氢呋喃,三氟甲基三甲基硅烷(tmscf3,0.36mmol,1.2当量),去离子水(0.45mmol,1.5当量)。该混合物在50℃下搅拌12小时(恒温油浴锅)。冷却至室温后,该混合物用乙酸乙酯稀释后,加入适量水,再用乙酸乙酯萃取三次,收集有机相,并加入适量的无水na2so4脱水合并的有机层,在减压下浓缩。粗产物在硅胶上通过柱色谱分离方法,得到纯化的2-二氟甲氧基-3-取代喹啉。
[0019]
实例5:
[0020]
向装有磁力搅拌的10ml schlenk管中添加2-((4-甲基苯基)乙炔基)苯胺(0.30mmol,1.0 当量)、cui(0.03mmol,0.1当量)和碘化钠(nai,0.60mmol,2.0当量)。用泵抽真空后填充氮气,三次。然后,在n2气氛下添加1.0ml超干溶剂四氢呋喃,三氟甲基三甲基硅烷(tmscf3,0.36mmol,1.2当量),去离子水(0.45mmol,1.5当量)。该混合物在50℃下搅拌12小时(恒温油浴锅)。冷却至室温后,该混合物用乙酸乙酯稀释后,加入适量水,再用乙酸乙酯萃取三次,收集有机相,并加入适量的无水na2so4脱水合并的有机层,在减压下浓缩。粗产物在硅胶上通过柱色谱分离方法,得到纯化的2-二氟甲氧基-3-取代喹啉。
[0021]
实例6:
[0022]
向装有磁力搅拌的10ml schlenk管中添加2-((4-乙基苯基)乙炔基)苯胺(0.30mmol,1.0 当量)、cui(0.03mmol,0.1当量)和碘化钠(nai,0.60mmol,2.0当量)。用泵抽真空后填充氮气,三次。然后,在n2气氛下添加1.0ml超干溶剂四氢呋喃,三氟甲基三甲基硅烷(tmscf3,0.36mmol,1.2当量),去离子水(0.45mmol,1.5当量)。该混合物在50℃下搅拌12小时(恒温油浴锅)。冷却至室温后,该混合物用乙酸乙酯稀释后,加入适量水,再用乙酸
乙酯萃取三次,收集有机相,并加入适量的无水na2so4脱水合并的有机层,在减压下浓缩。粗产物在硅胶上通过柱色谱分离方法,得到纯化的2-二氟甲氧基-3-取代喹啉。
[0023]
实例7:
[0024]
向装有磁力搅拌的10ml schlenk管中添加2-((3-甲基苯基)乙炔基)苯胺(0.30mmol,1.0 当量)、cui(0.03mmol,0.1当量)和碘化钠(nai,0.60mmol,2.0当量)。用泵抽真空后填充氮气,三次。然后,在n2气氛下添加1.0ml超干溶剂四氢呋喃,三氟甲基三甲基硅烷(tmscf3,0.36mmol,1.2当量),去离子水(0.45mmol,1.5当量)。该混合物在50℃下搅拌12小时(恒温油浴锅)。冷却至室温后,该混合物用乙酸乙酯稀释后,加入适量水,再用乙酸乙酯萃取三次,收集有机相,并加入适量的无水na2so4脱水合并的有机层,在减压下浓缩。粗产物在硅胶上通过柱色谱分离方法,得到纯化的2-二氟甲氧基-3-取代喹啉。
[0025]
实例8:
[0026]
向装有磁力搅拌的10ml schlenk管中添加2-((2-甲基苯基)乙炔基)苯胺(0.30mmol,1.0 当量)、cui(0.03mmol,0.1当量)和碘化钠(nai,0.60mmol,2.0当量)。用泵抽真空后填充氮气,三次。然后,在n2气氛下添加1.0ml超干溶剂四氢呋喃,三氟甲基三甲基硅烷(tmscf3,0.36mmol,1.2当量),去离子水(0.45mmol,1.5当量)。该混合物在50℃下搅拌12小时(恒温油浴锅)。冷却至室温后,该混合物用乙酸乙酯稀释后,加入适量水,再用乙酸乙酯萃取三次,收集有机相,并加入适量的无水na2so4脱水合并的有机层,在减压下浓缩。粗产物在硅胶上通过柱色谱分离方法,得到纯化的2-二氟甲氧基-3-取代喹啉。
[0027]
实例9:
[0028]
向装有磁力搅拌的10ml schlenk管中添加2-((4-取代基苯基)乙炔基)苯胺(取代基:氟、氯、苯基)(0.30mmol,1.0当量)、cui(0.03mmol,0.1当量)和碘化钠(nai,0.60mmol, 2.0当量)。用泵抽真空后填充氮气,三次。然后,在n2气氛下添加1.0ml超干溶剂四氢呋喃,三氟甲基三甲基硅烷(tmscf3,0.36mmol,1.2当量),去离子水(0.45mmol,1.5当量)。该混合物在50℃下搅拌12小时(恒温油浴锅)。冷却至室温后,该混合物用乙酸乙酯稀释后,加入适量水,再用乙酸乙酯萃取三次,收集有机相,并加入适量的无水na2so4脱水合并的有机层,在减压下浓缩。粗产物在硅胶上通过柱色谱分离方法,得到纯化的2-二氟甲氧基-3-取代喹啉。
[0029]
实例10:
[0030]
向装有磁力搅拌的10ml schlenk管中添加2-(戊-1-炔-1-基)苯胺(0.30mmol,1.0当量)、cui(0.03mmol,0.1当量)和碘化钠(nai,0.60mmol,2.0当量)。用泵抽真空后填充氮气,三次。然后,在n2气氛下添加1.0ml超干溶剂四氢呋喃,三氟甲基三甲基硅烷 (tmscf3,0.36mmol,1.2当量),去离子水(0.45mmol,1.5当量)。该混合物在50℃下搅拌12小时(恒温油浴锅)。冷却至室温后,该混合物用乙酸乙酯稀释后,加入适量水,再用乙酸乙酯萃取三次,收集有机相,并加入适量的无水na2so4脱水合并的有机层,在减压下浓缩。粗产物在硅胶上通过柱色谱分离方法,得到纯化的2-二氟甲氧基-3-取代喹啉。
[0031]
实例11:
[0032]
向装有磁力搅拌的10ml schlenk管中添加2-((2-萘基)乙炔基)苯胺(0.30mmol,1.0当量)、cui(0.03mmol,0.1当量)和碘化钠(nai,0.60mmol,2.0当量)。用泵抽真空后填充氮气,三次。然后,在n2气氛下添加1.0ml超干溶剂四氢呋喃,三氟甲基三甲基硅烷 (tmscf3,
0.36mmol,1.2当量),去离子水(0.45mmol,1.5当量)。该混合物在50℃下搅拌12小时(恒温油浴锅)。冷却至室温后,该混合物用乙酸乙酯稀释后,加入适量水,再用乙酸乙酯萃取三次,收集有机相,并加入适量的无水na2so4脱水合并的有机层,在减压下浓缩。粗产物在硅胶上通过柱色谱分离方法,得到纯化的2-二氟甲氧基-3-取代喹啉。
[0033]
实例12:
[0034]
向装有磁力搅拌的10ml schlenk管中添加2-((4-甲酯基苯基)乙炔基)苯胺(0.30mmol, 1.0当量)、cui(0.03mmol,0.1当量)和碘化钠(nai,0.60mmol,2.0当量)。用泵抽真空后填充氮气,三次。然后,在n2气氛下添加1.0ml超干溶剂四氢呋喃,三氟甲基三甲基硅烷(tmscf3,0.36mmol,1.2当量),去离子水(0.45mmol,1.5当量)。该混合物在50℃下搅拌12小时(恒温油浴锅)。冷却至室温后,该混合物用乙酸乙酯稀释后,加入适量水,再用乙酸乙酯萃取三次,收集有机相,并加入适量的无水na2so4脱水合并的有机层,在减压下浓缩。粗产物在硅胶上通过柱色谱分离方法,得到纯化的2-二氟甲氧基-3-取代喹啉。
[0035]
实例13:
[0036]
向装有磁力搅拌的10ml schlenk管中添加2-(噻吩-2-亚乙基)苯胺(0.30mmol,1.0 当量)、cui(0.03mmol,0.1当量)和碘化钠(nai,0.60mmol,2.0当量)。用泵抽真空后填充氮气,三次。然后,在n2气氛下添加1.0ml超干溶剂四氢呋喃,三氟甲基三甲基硅烷(tmscf3,0.36mmol,1.2当量),去离子水(0.45mmol,1.5当量)。该混合物在50℃下搅拌12小时(恒温油浴锅)。冷却至室温后,该混合物用乙酸乙酯稀释后,加入适量水,再用乙酸乙酯萃取三次,收集有机相,并加入适量的无水na2so4脱水合并的有机层,在减压下浓缩。粗产物在硅胶上通过柱色谱分离方法,得到纯化的2-二氟甲氧基-3-取代喹啉。
[0037]
实例14:
[0038]
向装有磁力搅拌的10ml schlenk管中添加2-((2-氯基苯基)乙炔基)苯胺(取代基:氟、氯、苯基)(0.30mmol,1.0当量)、cui(0.03mmol,0.1当量)和碘化钠(nai,0.60mmol, 2.0当量)。用泵抽真空后填充氮气,三次。然后,在n2气氛下添加1.0ml超干溶剂四氢呋喃,三氟甲基三甲基硅烷(tmscf3,0.36mmol,1.2当量),去离子水(0.45mmol,1.5当量)。该混合物在50℃下搅拌12小时(恒温油浴锅)。冷却至室温后,该混合物用乙酸乙酯稀释后,加入适量水,再用乙酸乙酯萃取三次,收集有机相,并加入适量的无水na2so4脱水合并的有机层,在减压下浓缩。粗产物在硅胶上通过柱色谱分离方法,得到纯化的2-二氟甲氧基-3-取代喹啉。
[0039]
实例15:
[0040]
向装有磁力搅拌的10ml schlenk管中添加2-((苯基)乙炔基)苯胺(0.30mmol,1.0当量)、 cui(0.03mmol,0.1当量)和碘化钠(nai,0.60mmol,2.0当量)。用泵抽真空后填充氮气,三次。然后,在n2气氛下添加1.0ml超干溶剂四氢呋喃,三氟甲基三甲基硅烷(tmscf3, 0.36mmol,1.2当量),去离子水(0.45mmol,1.5当量)。该混合物在50℃下搅拌12小时 (恒温油浴锅)。冷却至室温后,该混合物用乙酸乙酯稀释后,加入适量水,再用乙酸乙酯萃取三次,收集有机相,并加入适量的无水na2so4脱水合并的有机层,在减压下浓缩。粗产物在硅胶上通过柱色谱分离方法,得到纯化的2-二氟甲氧基-3-取代喹啉。
[0041]
实例16:
[0042]
向装有磁力搅拌的10ml schlenk管中添加2-((4-甲氧基苯基)乙炔基)苯胺
(0.30mmol, 1.0当量)、cui(0.03mmol,0.1当量)和碘化钠(nai,0.60mmol,2.0当量)。用泵抽真空后填充氮气,三次。然后,在n2气氛下添加1.0ml超干溶剂四氢呋喃,三氟甲基三甲基硅烷(tmscf3,0.36mmol,1.2当量),去离子水(0.45mmol,1.5当量)。该混合物在25℃下搅拌12小时(恒温油浴锅)。冷却至室温后,该混合物用乙酸乙酯稀释后,加入适量水,再用乙酸乙酯萃取三次,收集有机相,并加入适量的无水na2so4脱水合并的有机层,在减压下浓缩。粗产物在硅胶上通过柱色谱分离方法,得到纯化的n-取代-2-喹诺酮类化合物。
[0043]
通过柱色谱法分离纯化(石油醚/乙酸乙酯=250:1),得到标题化合物,为黄色液体。收率: 90.9mg,70%。1hnmr(400mhz,cdcl3)δ7.75(s,1h),7.70
–
7.65(m,2h),7.61
–
7.51(m,2h), 7.37(s,1h),7.22(t,j=7.5hz,1h),7.01
–
6.90(m,2h),4.37(t,j=7.3hz,2h),3.83(s,3h), 3.26(t,j=6.6hz,2h),2.04
–
1.89(m,4h).
13
c nmr(101mhz,cdcl3)δ161.5,159.6,138.4, 136.0,131.8,130.2,130.1,129.0,122.2,121.2,113.9,113.7,55.4,41.7,30.8,28.5,6.3.
[0044]
实例17:
[0045]
向装有磁力搅拌的10ml schlenk管中添加2-((4-乙氧基苯基)乙炔基)苯胺(0.30mmol, 1.0当量)、cui(0.03mmol,0.1当量)和碘化钠(nai,0.60mmol,2.0当量)。用泵抽真空后填充氮气,三次。然后,在n2气氛下添加1.0ml超干溶剂四氢呋喃,三氟甲基三甲基硅烷(tmscf3,0.36mmol,1.2当量),去离子水(0.45mmol,1.5当量)。该混合物在25℃下搅拌12小时(恒温油浴锅)。冷却至室温后,该混合物用乙酸乙酯稀释后,加入适量水,再用乙酸乙酯萃取三次,收集有机相,并加入适量的无水na2so4脱水合并的有机层,在减压下浓缩。粗产物在硅胶上通过柱色谱分离方法,得到纯化的n-取代-2-喹诺酮类化合物。
[0046]
实例18:
[0047]
向装有磁力搅拌的10ml schlenk管中添加2-((3-甲氧基苯基)乙炔基)苯胺(0.30mmol, 1.0当量)、cui(0.03mmol,0.1当量)和碘化钠(nai,0.60mmol,2.0当量)。用泵抽真空后填充氮气,三次。然后,在n2气氛下添加1.0ml超干溶剂四氢呋喃,三氟甲基三甲基硅烷(tmscf3,0.36mmol,1.2当量),去离子水(0.45mmol,1.5当量)。该混合物在25℃下搅拌12小时(恒温油浴锅)。冷却至室温后,该混合物用乙酸乙酯稀释后,加入适量水,再用乙酸乙酯萃取三次,收集有机相,并加入适量的无水na2so4脱水合并的有机层,在减压下浓缩。粗产物在硅胶上通过柱色谱分离方法,得到纯化的n-取代-2-喹诺酮类化合物。
[0048]
实例19:
[0049]
向装有磁力搅拌的10ml schlenk管中添加2-((2-甲氧基苯基)乙炔基)苯胺(0.30mmol, 1.0当量)、cui(0.03mmol,0.1当量)和碘化钠(nai,0.60mmol,2.0当量)。用泵抽真空后填充氮气,三次。然后,在n2气氛下添加1.0ml超干溶剂四氢呋喃,三氟甲基三甲基硅烷(tmscf3,0.36mmol,1.2当量),去离子水(0.45mmol,1.5当量)。该混合物在25℃下搅拌12小时(恒温油浴锅)。冷却至室温后,该混合物用乙酸乙酯稀释后,加入适量水,再用乙酸乙酯萃取三次,收集有机相,并加入适量的无水na2so4脱水合并的有机层,在减压下浓缩。粗产物在硅胶上通过柱色谱分离方法,得到纯化的n-取代-2-喹诺酮类化合物。
[0050]
实例20:
[0051]
向装有磁力搅拌的10ml schlenk管中添加2-((4-甲基苯基)乙炔基)苯胺(0.30mmol,1.0 当量)、cui(0.03mmol,0.1当量)和碘化钠(nai,0.60mmol,2.0当量)。用泵
抽真空后填充氮气,三次。然后,在n2气氛下添加1.0ml超干溶剂四氢呋喃,三氟甲基三甲基硅烷(tmscf3,0.36mmol,1.2当量),去离子水(0.45mmol,1.5当量)。该混合物在25℃下搅拌12小时(恒温油浴锅)。冷却至室温后,该混合物用乙酸乙酯稀释后,加入适量水,再用乙酸乙酯萃取三次,收集有机相,并加入适量的无水na2so4脱水合并的有机层,在减压下浓缩。粗产物在硅胶上通过柱色谱分离方法,得到纯化的n-取代-2-喹诺酮类化合物。
[0052]
实例21:
[0053]
向装有磁力搅拌的10ml schlenk管中添加2-((4-乙基苯基)乙炔基)苯胺(0.30mmol,1.0 当量)、cui(0.03mmol,0.1当量)和碘化钠(nai,0.60mmol,2.0当量)。用泵抽真空后填充氮气,三次。然后,在n2气氛下添加1.0ml超干溶剂四氢呋喃,三氟甲基三甲基硅烷(tmscf3,0.36mmol,1.2当量),去离子水(0.45mmol,1.5当量)。该混合物在25℃下搅拌12小时(恒温油浴锅)。冷却至室温后,该混合物用乙酸乙酯稀释后,加入适量水,再用乙酸乙酯萃取三次,收集有机相,并加入适量的无水na2so4脱水合并的有机层,在减压下浓缩。粗产物在硅胶上通过柱色谱分离方法,得到纯化的n-取代-2-喹诺酮类化合物。
[0054]
实例22:
[0055]
向装有磁力搅拌的10ml schlenk管中添加2-((3-甲基苯基)乙炔基)苯胺(0.30mmol,1.0 当量)、cui(0.03mmol,0.1当量)和碘化钠(nai,0.60mmol,2.0当量)。用泵抽真空后填充氮气,三次。然后,在n2气氛下添加1.0ml超干溶剂四氢呋喃,三氟甲基三甲基硅烷(tmscf3,0.36mmol,1.2当量),去离子水(0.45mmol,1.5当量)。该混合物在25℃下搅拌12小时(恒温油浴锅)。冷却至室温后,该混合物用乙酸乙酯稀释后,加入适量水,再用乙酸乙酯萃取三次,收集有机相,并加入适量的无水na2so4脱水合并的有机层,在减压下浓缩。粗产物在硅胶上通过柱色谱分离方法,得到纯化的n-取代-2-喹诺酮类化合物。
[0056]
实例23:
[0057]
向装有磁力搅拌的10ml schlenk管中添加2-((2-甲基苯基)乙炔基)苯胺(0.30mmol,1.0 当量)、cui(0.03mmol,0.1当量)和碘化钠(nai,0.60mmol,2.0当量)。用泵抽真空后填充氮气,三次。然后,在n2气氛下添加1.0ml超干溶剂四氢呋喃,三氟甲基三甲基硅烷(tmscf3,0.36mmol,1.2当量),去离子水(0.45mmol,1.5当量)。该混合物在25℃下搅拌12小时(恒温油浴锅)。冷却至室温后,该混合物用乙酸乙酯稀释后,加入适量水,再用乙酸乙酯萃取三次,收集有机相,并加入适量的无水na2so4脱水合并的有机层,在减压下浓缩。粗产物在硅胶上通过柱色谱分离方法,得到纯化的n-取代-2-喹诺酮类化合物。
[0058]
实例24:
[0059]
向装有磁力搅拌的10ml schlenk管中添加2-((4-取代基苯基)乙炔基)苯胺(取代基:氟、氯、苯基)(0.30mmol,1.0当量)、cui(0.03mmol,0.1当量)和碘化钠(nai,0.60mmol, 2.0当量)。用泵抽真空后填充氮气,三次。然后,在n2气氛下添加1.0ml超干溶剂四氢呋喃,三氟甲基三甲基硅烷(tmscf3,0.36mmol,1.2当量),去离子水(0.45mmol,1.5当量)。该混合物在25℃下搅拌12小时(恒温油浴锅)。冷却至室温后,该混合物用乙酸乙酯稀释后,加入适量水,再用乙酸乙酯萃取三次,收集有机相,并加入适量的无水na2so4脱水合并的有机层,在减压下浓缩。粗产物在硅胶上通过柱色谱分离方法,得到纯化的n-取代-2-喹诺酮类化合物。
[0060]
实例25:
[0061]
向装有磁力搅拌的10ml schlenk管中添加2-(戊-1-炔-1-基)苯胺(0.30mmol,1.0当量)、cui(0.03mmol,0.1当量)和碘化钠(nai,0.60mmol,2.0当量)。用泵抽真空后填充氮气,三次。然后,在n2气氛下添加1.0ml超干溶剂四氢呋喃,三氟甲基三甲基硅烷 (tmscf3,0.36mmol,1.2当量),去离子水(0.45mmol,1.5当量)。该混合物在25℃下搅拌12小时(恒温油浴锅)。冷却至室温后,该混合物用乙酸乙酯稀释后,加入适量水,再用乙酸乙酯萃取三次,收集有机相,并加入适量的无水na2so4脱水合并的有机层,在减压下浓缩。粗产物在硅胶上通过柱色谱分离方法,得到纯化的n-取代-2-喹诺酮类化合物。
[0062]
实例26:
[0063]
向装有磁力搅拌的10ml schlenk管中添加2-((2-萘基)乙炔基)苯胺(0.30mmol,1.0当量)、cui(0.03mmol,0.1当量)和碘化钠(nai,0.60mmol,2.0当量)。用泵抽真空后填充氮气,三次。然后,在n2气氛下添加1.0ml超干溶剂四氢呋喃,三氟甲基三甲基硅烷 (tmscf3,0.36mmol,1.2当量),去离子水(0.45mmol,1.5当量)。该混合物在25℃下搅拌12小时(恒温油浴锅)。冷却至室温后,该混合物用乙酸乙酯稀释后,加入适量水,再用乙酸乙酯萃取三次,收集有机相,并加入适量的无水na2so4脱水合并的有机层,在减压下浓缩。粗产物在硅胶上通过柱色谱分离方法,得到纯化的n-取代-2-喹诺酮类化合物。
[0064]
实例27:
[0065]
向装有磁力搅拌的10ml schlenk管中添加2-((4-甲酯基苯基)乙炔基)苯胺(0.30mmol,1.0当量)、cui(0.03mmol,0.1当量)和碘化钠(nai,0.60mmol,2.0当量)。用泵抽真空后填充氮气,三次。然后,在n2气氛下添加1.0ml超干溶剂四氢呋喃,三氟甲基三甲基硅烷(tmscf3,0.36mmol,1.2当量),去离子水(0.45mmol,1.5当量)。该混合物在25℃下搅拌12小时(恒温油浴锅)。冷却至室温后,该混合物用乙酸乙酯稀释后,加入适量水,再用乙酸乙酯萃取三次,收集有机相,并加入适量的无水na2so4脱水合并的有机层,在减压下浓缩。粗产物在硅胶上通过柱色谱分离方法,得到纯化的n-取代-2-喹诺酮类化合物。
[0066]
实例28:
[0067]
向装有磁力搅拌的10ml schlenk管中添加2-(噻吩-2-亚乙基)苯胺(0.30mmol,1.0 当量)、cui(0.03mmol,0.1当量)和碘化钠(nai,0.60mmol,2.0当量)。用泵抽真空后填充氮气,三次。然后,在n2气氛下添加1.0ml超干溶剂四氢呋喃,三氟甲基三甲基硅烷(tmscf3,0.36mmol,1.2当量),去离子水(0.45mmol,1.5当量)。该混合物在25℃下搅拌12小时(恒温油浴锅)。冷却至室温后,该混合物用乙酸乙酯稀释后,加入适量水,再用乙酸乙酯萃取三次,收集有机相,并加入适量的无水na2so4脱水合并的有机层,在减压下浓缩。粗产物在硅胶上通过柱色谱分离方法,得到纯化的n-取代-2-喹诺酮类化合物。
[0068]
实例29:
[0069]
向装有磁力搅拌的10ml schlenk管中添加2-((2-氯基苯基)乙炔基)苯胺(取代基:氟、氯、苯基)(0.30mmol,1.0当量)、cui(0.03mmol,0.1当量)和碘化钠(nai,0.60mmol, 2.0当量)。用泵抽真空后填充氮气,三次。然后,在n2气氛下添加1.0ml超干溶剂四氢呋喃,三氟甲基三甲基硅烷(tmscf3,0.36mmol,1.2当量),去离子水(0.45mmol,1.5当量)。该混合物在25℃下搅拌12小时(恒温油浴锅)。冷却至室温后,该混合物用乙酸乙酯稀释后,加入适量水,再用乙酸乙酯萃取三次,收集有机相,并加入适量的无水na2so4脱水合并的有机层,在减压下浓缩。粗产物在硅胶上通过柱色谱分离方法,得到纯化的n-取代-2-喹诺酮类化合
0.60mmol,2.0当量)。用泵抽真空后填充氮气,三次。然后,在n2气氛下添加1.0ml超干溶剂四氢呋喃,三氟甲基三甲基硅烷(tmscf3,0.36mmol,1.2当量),去离子水(0.45 mmol,1.5当量)。该混合物在25℃下搅拌12小时(恒温油浴锅)。冷却至室温后,该混合物用乙酸乙酯稀释后,加入适量水,再用乙酸乙酯萃取三次,收集有机相,并加入适量的无水na2so4脱水合并的有机层,在减压下浓缩。粗产物在硅胶上通过柱色谱分离方法,得到纯化的n-取代-2-喹诺酮类化合物。
[0080]
以上所述实施例仅表达了本发明的几种实施方式,其描述较为具体和详细,但并不能因此而理解为对本发明专利范围的限制。应当指出的是,对于本领域的普通技术人员来说,在不脱离本发明构思的前提下,还可以做出若干变形和改进,这些都属于本发明的保护范围。因此,本发明专利的保护范围应以所附权利要求为准。
再多了解一些
本文用于创业者技术爱好者查询,仅供学习研究,如用于商业用途,请联系技术所有人。