1.本发明属于医药技术领域,具体涉及一种基于水凝胶的胶质母细胞瘤类器官的构建方法、类器官模型和应用。
背景技术:
2.胶质母细胞瘤(gbm)是成人最常见的原发恶性脑肿瘤,预后较差。即使采用标准治疗,初诊的患者中位生存期仍16为至20个月。由于胶质母细胞瘤的异质性和侵袭性以及传统药物筛选方法的局限性,目前还没有开发出特别有效的抗肿瘤药物。药物筛选的经典模型是在二维平面培养肿瘤细胞系。然而,肿瘤细胞系在二维培养过程中,肿瘤内异质性较差,逐渐失去了亲代肿瘤的特征。这导致了抗肿瘤药物在前期研发过程中遇到很大的局限性。近年来,肿瘤类器官被广泛应用于药物的筛选和疗效评价,以探讨针对患者的个性化治疗策略。国外学者研究发现,患者来源的胶质母细胞瘤类器官可以保持亲代肿瘤的关键特征,包括组织学特征、细胞多样性、基因表达和突变谱,对抗肿瘤药物的前期研发以及实现患者个性化治疗有重大的前景。相关研究成果已经发表在《cell》,《natureprotocols》等权威期刊上。
3.目前国际上主流的胶质母细胞瘤类器官培养主要是将患者的肿瘤组织切成碎片,直接置于类器官培养基中进行培养。这样的胶质母细胞瘤类器官本质是肿瘤组织碎片,在剪碎肿瘤组织的过程中会丧失很多细胞外基质,缺乏细胞外基质,容易使得肿瘤组织的微环境发生改变,从而影响一系列生物学特征,如相关重要基因的表达。
4.相关技术公开了一种胶质母细胞瘤类器官模型的构建方法和应用,该技术方案是选用了胶质母细胞瘤细胞系作为样本进行了处理后构建,该种样本的选取必须经过酶处理、标记、注射进入大脑皮质类器官中进行处理获得大脑皮质类器官的模型。由于胶质母细胞瘤患者之间存在肿瘤异质性,也就是说不同的患者,肿瘤的表型不尽相同。而该技术使用的胶质母细胞瘤细胞系并不能体现患者之间的肿瘤异质性。因此,该技术构建的胶质母细胞瘤类器官,无法个性化地预测药物反应,不利于患者的个性化治疗。此外,大脑的细胞外基质中含有丰富的透明质酸,而该技术使用matrigel基质胶作为细胞外基质,但matrigel中没有透明质酸成分,无法真实模拟大脑的细胞外基质。
5.目前尚未有将水凝胶与胶质母细胞瘤组织碎片混合培养的方式对胶质母细胞瘤类器官进行的探索。
技术实现要素:
6.为了解决现有技术存在的常规使用的胶质母细胞瘤组织在预处理过程中会导致缺乏细胞外基质,进而会影响胶质母细胞瘤类器官的完整性;有的采用胶质母细胞瘤的细胞系作为样本进行处理,存在构建方法繁杂且不能体现患者间的肿瘤异质性的问题;采用matrigel基质胶作为细胞外基质,缺乏透明质酸成分,存在无法真实模拟大脑细胞外基质
的上述问题,本发明目的在于提供一种基于水凝胶的胶质母细胞瘤类器官的构建方法、类器官模型和应用。
7.本发明所采用的技术方案为:一种基于水凝胶的胶质母细胞瘤类器官的构建方法,所述构建方法包括如下步骤:
8.胶质母细胞瘤组织样本:将胶质母细胞瘤组织预处理后进行培养;
9.制备水凝胶:选取甲基丙烯酸化水凝胶和透明质酸混合;
10.构建基于水凝胶的胶质母细胞瘤类器官:重悬胶质母细胞瘤组织样本后与水凝胶混匀、交联。
11.作为优选地,所述预处理包括清洗和剪切;
12.所述清洗为采用4-5℃、无菌pbs缓冲液对胶质母细胞瘤组织进行清洗;
13.所述剪切为胶质母细胞瘤组织剪成1-2mm直径的碎片。
14.作为优选地,所述胶质母细胞瘤组织样本中的培养用培养基为:
15.所述培养基培养基配制由235ml dmem:f12培养基(thermo fisher scientific) 235ml神经基础培养基(neurobasal,thermo fisher scientific) 5ml l-谷氨酰胺添加剂(100
×
glutamax,thermo fisher scientific) 5ml青霉素/链霉素双抗(100
×
penstrep,thermo fisher scientific) 5ml n2添加剂(100
×
n2supplement,thermo fisher scientific) 10ml b27添加剂(50
×
b27 supplement,minus vitamin a) 5ml非必须氨基酸溶液(100
×
neaas,thermo fisher scientific) 125ul人胰岛素(human insulin,sigma)组成。
16.作为优选地,所述甲基丙烯酸化水凝胶和透明质酸混合质量份数比为10:0.4-0.5。
17.作为优选地,所述制备水凝胶的步骤还包括水浴加热、过滤和预热保存。
18.作为优选地,所述水浴加热为60-70℃,加热时长20-25分钟;
19.所述采用0.45-0.55um过滤器过滤水凝胶;
20.所述预热保存温度为35-37℃。
21.作为优选地,所述构建基于水凝胶的胶质母细胞瘤类器官中,重悬胶质母细胞瘤组织样本与水凝胶的混合体积比为1:1。
22.作为优选地,所述交联时采用400-405nm的紫外光进行交联处理;
23.所述交联时长20-30秒。
24.一种基于水凝胶的胶质母细胞瘤类器官模型,如所述的基于水凝胶的胶质母细胞瘤类器官的构建方法构建而成。
25.一种基于水凝胶的胶质母细胞瘤类器官模型在制备胶质母细胞瘤的药物中的应用。
26.本发明的有益效果为:
27.(一)由于现有胶质母细胞瘤类器官缺乏细胞外基质的缺点,本方案利用水凝胶作为细胞外基质与肿瘤组织碎片混合起来。水凝胶是由甲基丙烯酸化水凝胶(gelma)和透明质酸(ha)混合而成。甲基丙烯酸化水凝胶作为常用的生物工程材料,作为人工的细胞外基质具有良好的生物相容性、安全性和稳定性。透明质酸是大脑最丰富的细胞外基质成分,同时在脑肿瘤中也存在。因此甲基丙烯酸化水凝胶和透明质酸的混合可以模拟胶质母细胞瘤
的细胞外基质。
28.(二)本技术技术通过利用rna二代测序,验证得到水凝胶的胶质母细胞瘤类器官在维持神经发育相关基因表达方面有如下优点特性:第一,有水凝胶的胶质母细胞瘤类器官在相应培养天数上维持了神经发育相关基因的表达,包括胶质瘤干细胞标记基因sox2、olig2,神经前体细胞标记基因nes、hopx、fabp7、细胞增殖标记基因mki67;第二,有水凝胶的胶质母细胞瘤类器官在相应培养天数上,其hopx、fabp7、gfap、s100b、sox2、olig2的表达高于没有水凝胶的胶质母细胞瘤类器官。
附图说明
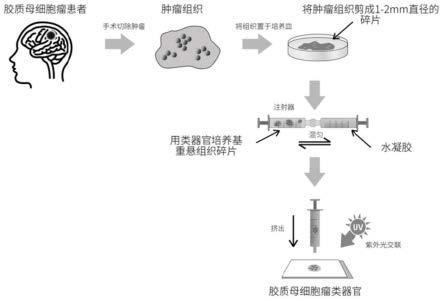
29.图1为实施例1的基于水凝胶的胶质母细胞瘤类器官的构建方法的流程示意图;
30.图2为实验例1中亲代肿瘤与第7天无水凝胶的胶质母细胞瘤类器官的对比示意图
31.图3为实验例1中亲代肿瘤与第14天无水凝胶的胶质母细胞瘤类器官的对比示意图
32.图4为实验例1中亲代肿瘤与第7天水凝胶的胶质母细胞瘤类器官的对比示意图;
33.图5为实验例1中亲代肿瘤与第14天水凝胶的胶质母细胞瘤类器官的对比示意图;
34.图6为实验例1中水凝胶胶质母细胞瘤类器官与无水凝胶的胶质母细胞瘤类器官的第7天对比示意图;
35.图7为实验例1中水凝胶胶质母细胞瘤类器官与无水凝胶的胶质母细胞瘤类器官的第14天的对比示意图;
36.图8为实验例1中有水凝胶的胶质母细胞瘤类器官紫外光交联示意图;
37.图9为实验例1中有水凝胶的胶质母细胞瘤类器官比例尺为2um的扫描电镜图;
38.图10为实验例1中有水凝胶的胶质母细胞瘤类器官比例尺为50um的扫描电镜图。
具体实施方式
39.下面结合具体实施例对本发明做进一步阐释。本领域技术人员将会理解,下列所描述的实施例是本发明一部分实施例,而不是全部的实施例,仅用于说明本发明,而不应视为限制本发明的范围。所用试剂均为可以通过市售购买获得的常规产品。
40.实施例1:如图1所示,为该基于水凝胶的胶质母细胞瘤类器官的构建方法的流程图:
41.1、样本收集:离体肿瘤组织样本来自于某医院某60岁的胶质母细胞瘤患者。将肿瘤组织在4℃无菌pbs缓冲液中冲洗后,用无菌剪将肿瘤组织剪成1-2mm直径的碎片。
42.2、配制胶质母细胞瘤类器官培养基:235ml dmem:f12培养基(thermo fisher scientific) 235ml神经基础培养基(neurobasal,thermo fisher scientific) 5ml l-谷氨酰胺添加剂(100
×
glutamax,thermo fisher scientific) 5ml青霉素/链霉素双抗(100
×
penstrep,thermo fisher scientific) 5ml n2添加剂(100
×
n2 supplement,thermo fisher scientific) 10ml b27添加剂(50
×
b27 supplement,minus vitamin a) 5ml非必须氨基酸溶液(100
×
neaas,thermo fisher scientific) 125ul人胰岛素(human insulin,sigma)。
43.3、制备水凝胶:将10%(w/v)的gelma(efl-gm-60,中国苏州)和0.5%(w/v)的ha
(efl-ha-150k,中国苏州)的混合物在70℃水浴中加热20分钟。然后立即用0.45um过滤器过滤水凝胶。水凝胶过滤后,在37℃水浴锅中预热。
44.4、制备有水凝胶的胶质母细胞瘤类器官:
45.4.1将肿瘤组织碎片用类器官培养基重悬;
46.4.2取1ml注射器,将针头取下,吸取0.4ml的重悬液,注意要把肿瘤组织碎片吸进去;
47.4.3取1ml注射器,将针头取下,吸取等体积(0.4ml)水凝胶;
48.4.4两个注射器之间连接一个螺母头,左右交替推进注射器,将水凝胶与组织碎片悬液充分混合;
49.4.5混匀后将所有液体推到一个注射器里,推进该注射器,挤出0.2ml体积的混合液,立即用波长为405nm的紫外光交联30s,使得水凝胶固化,获得水凝胶的胶质母细胞瘤类器官。
50.5、有水凝胶的胶质母细胞瘤类器官培养:用无菌6孔板培养,每孔一个类器官,培养基为4ml,每4天换一次液。置于37.0℃、5.0%co2的培养箱中培养。
51.6、无水凝胶的胶质母细胞瘤类器官培养:无水凝胶的胶质母细胞瘤类器官作为对照组,将肿瘤组织碎片直接置于类器官培养基中进行培养,用无菌6孔板培养,每孔一个类器官,培养基为4ml,每4天换一次液。置于37.0℃、5.0%co2的培养箱中培养。
52.7、验证:rna二代测序及差异分析:取亲代肿瘤以及培养7天和14天的胶质母细胞瘤类器官样本进行rna二代测序。先用gelma裂解液将水凝胶裂解,1000rpm离心5分钟,再用pbs将肿瘤组织碎片重悬,再次1000rpm离心5分钟,弃上清,保存在-80℃的冰箱,送公司进行rna二代测序。
53.8、测序完成后,我们通过edger软件,对每个样本基因的表达量进行差异分析,将差异倍数大于或等于2,且校正后的p值小于或等于0.05的基因作为有差异表达的基因,否则作为无差异表达的基因。
54.本方案选取神经发育相关基因作为评价的指标,这些基因在胶质母细胞瘤发生发展方面发挥重要作用。胶质瘤干细胞标记基因sox2、olig2、胶质细胞标记基因gfap、s100b、神经前体细胞标记基因nes、hopx、fabp7、细胞增殖标记基因mki67。
55.实验例1:以rna二代测序和差异分析法测定实验
56.神经发育相关基因在胶质母细胞瘤发生发展中发挥重要作用,当基因的表达量在胶质母细胞瘤类器官中的表达高于或者与亲代肿瘤无差异时,我们便认为胶质母细胞瘤类器官维持了该基因的表达,并且可以反映亲代肿瘤的部分生物学特性。
57.本技术技术通过利用rna二代测序,验证得到水凝胶的胶质母细胞瘤类器官在维持神经发育相关基因表达方面有如下优点特性:第一,有水凝胶的胶质母细胞瘤类器官在相应培养天数上维持了神经发育相关基因的表达,包括胶质瘤干细胞标记基因sox2、olig2,神经前体细胞标记基因nes、hopx、fabp7、细胞增殖标记基因mki67;第二,有水凝胶的胶质母细胞瘤类器官在相应培养天数上,其hopx、fabp7、gfap、s100b、sox2、olig2的表达高于没有水凝胶的胶质母细胞瘤类器官。
58.rna二代测序可以从rna水平对基因的表达进行定量。通过edger软件,可以从统计学的角度去评价一些关键基因在亲代肿瘤和胶质母细胞瘤类器官中表达的差异,使得结果
具有统计学意义,更加严谨。当基因的表达量在胶质母细胞瘤类器官中的表达高于或者与亲代肿瘤无差异时,我们便认为胶质母细胞瘤类器官维持了该基因的表达,并且可以反映亲代肿瘤的部分生物学特性。
59.实验对象:实验组选用上述实施例1的流程构建得到有水凝胶的胶质母细胞瘤类器官、对照组1以及对照组2。实验对象肿瘤组织均来源于同一位患者。
60.对照组1为亲代肿瘤组织,采用如下构建方法进行处理:
61.离体肿瘤组织样本1来自于某医院某60岁的胶质母细胞瘤患者。将肿瘤组织在4℃无菌pbs缓冲液中冲洗后,直接置于冻存管中,干冰运输至公司进行二代测序。
62.对照组2选用亲代肿瘤,采用如下构建方法进行处理:
63.1、样本收集:离体肿瘤组织样本来自于某医院某60岁的胶质母细胞瘤患者。将肿瘤组织在4℃无菌pbs缓冲液中冲洗后,用无菌剪将肿瘤组织剪成1-2mm直径的碎片。
64.2、配制胶质母细胞瘤类器官培养基:235ml dmem:f12培养基(thermo fisher scientific) 235ml神经基础培养基(neurobasal,thermo fisher scientific) 5ml l-谷氨酰胺添加剂(100
×
glutamax,thermo fisher scientific) 5ml青霉素/链霉素双抗(100
×
penstrep,thermo fisher scientific) 5ml n2添加剂(100
×
n2 supplement,thermo fisher scientific) 10ml b27添加剂(50
×
b27 supplement,minus vitamin a) 5ml非必须氨基酸溶液(100
×
neaas,thermo fisher scientific) 125ul人胰岛素(human insulin,sigma)。
65.3.将肿瘤组织碎片用类器官培养基重悬;
66.4.用无菌6孔板培养,每孔一个类器官,培养基为4ml,每4天换一次液。置于37.0℃、5.0%co2的培养箱中培养。
67.5、验证:rna二代测序及差异分析:取培养7天和14天的样本进行rna二代测序。将肿瘤组织碎片悬液1000rpm离心5分钟,弃上清,干冰运送公司进行rna二代测序。
68.如图2和3结果显示,无水凝胶的类器官:其神经前体细胞标记基因hopx、nes和fabp7在7天时表达量都是低于亲代肿瘤的,在14天时hopx仍然低于亲代肿瘤,nes与亲代肿瘤表达无差异,fabp7高于亲代肿瘤。胶质瘤干细胞标记基因sox2和olig2在7天时也是低表达,但在14天时表达也升高而且与亲代肿瘤无差异。肿瘤增殖标记基因mki67在7天时候与亲代肿瘤无差异,14天时高于亲代肿瘤。
69.结果表明,无水凝胶的胶质母细胞瘤类器官在14天时可以维持nes、fabp7、sox2、olig2、mki67的表达。
70.图2中,亲代肿瘤作为对照,箭头向上提示表达升高,箭头向下提示表达下降,没有箭头则提示表达无差异,横坐标是两样本基因表达量的"log2差异倍数",纵坐标是"-log
10
校正后的p"。
71.图3中,亲代肿瘤作为对照,箭头向上提示表达升高,箭头向下提示表达下降,没有箭头则提示表达无差异,横坐标是两样本基因表达量的"log2差异倍数",纵坐标是"-log
10
校正后的p"。
72.如图4和5结果显示,有水凝胶的胶质母细胞瘤类器官,其神经前体细胞标记基因hopx和nes的表达虽然在7天时是低表达的,但在14天时表达升高并且与亲代肿瘤无差异,fabp7在7天时与亲代肿瘤无差异,在14天时高于亲代肿瘤。胶质瘤干细胞标记基因sox2和
olig2在7天时也是低表达,但在14天时表达也升高而且大于亲代肿瘤,肿瘤增殖标记基因mki67在7天时候与亲代肿瘤无差异,14天时高于亲代肿瘤。
73.结果表明,有水凝胶的胶质母细胞瘤类器官在14天时可以维持hopx、nes、fabp7、sox2、olig2、mki67的表达。
74.图4中,亲代肿瘤作为对照,箭头向上提示表达升高,箭头向下提示表达下降,没有箭头则提示表达无差异,横坐标是两样本基因表达量的"log2差异倍数",纵坐标是"-log
10
校正后的p"。
75.图5中,亲代肿瘤作为对照,箭头向上提示表达升高,箭头向下提示表达下降,没有箭头则提示表达无差异,横坐标是两样本基因表达量的"log2差异倍数",纵坐标是"-log
10
校正后的p"。
76.如图6和7结果显示,有水凝胶的胶质母细胞瘤类器官,其神经前体细胞标记基因hopx、fabp7的表达在7天和14天均高于无水凝胶的胶质母细胞瘤类器官,星形胶质细胞标记基因gfap、s100b的表达在7天时高于无水凝胶的胶质母细胞瘤类器官,胶质瘤干细胞标记基因sox2和olig2的表达分别在7天和14天高于无水凝胶的胶质母细胞瘤类器官。在这8个用于评估的基因中,有水凝胶的胶质母细胞瘤类器官,没有一个基因的表达量低于无水凝胶的胶质母细胞瘤类器官。
77.图6中,无水凝胶的胶质母细胞瘤类器官作为对照,箭头向上提示表达升高,箭头向下提示表达下降,没有箭头则提示表达无差异,横坐标是两样本基因表达量的"log2差异倍数",纵坐标是"-log
10
校正后的p"。
78.图7中,无水凝胶的胶质母细胞瘤类器官作为对照,箭头向上提示表达升高,箭头向下提示表达下降,没有箭头则提示表达无差异,横坐标是两样本基因表达量的"log2差异倍数",纵坐标是"-log
10
校正后的p"。
79.上述所有图中箭头向上表示表达上调的基因,箭头向下表示下调的基因,没有箭头说明基因表达无变化。
80.验证的结果总结如下:两组类型的胶质母细胞瘤类器官在14天时均维持了nes、sox2、olig2、fabp7、mki67基因的表达,但是无水凝胶的胶质母细胞瘤类器官无论在7天、还是14天,都无法维持hopx的表达,而有水凝胶的胶质母细胞瘤类器官在14天时可以维持hopx的表达。
81.值得注意的是,在这8个用于评估的基因中,有水凝胶的胶质母细胞瘤类器官,没有一个基因的表达量低于无水凝胶的胶质母细胞瘤类器官,在相应培养天数上,其hopx、fabp7、gfap、s100b、sox2、olig2的表达高于没有水凝胶的胶质母细胞瘤类器官。
82.从验证的结果来看,有水凝胶的胶质母细胞瘤类器官在维持亲代肿瘤的生物学特性上,并不亚于无水凝胶的胶质母细胞瘤类器官,在维持某些基因的表达上甚至优于无水凝胶的胶质母细胞瘤类器官。
83.图8中,为有水凝胶的胶质母细胞瘤类器官紫外光交联示意图,其为紫外光交联后的基于水凝胶的胶质母细胞瘤类器官实物图。
84.图9为实验例1中有水凝胶的胶质母细胞瘤类器官比例尺为2um的扫描电镜图;
85.图10为实验例1中有水凝胶的胶质母细胞瘤类器官比例尺为50um的扫描电镜图。
86.本发明不局限于上述可选的实施方式,任何人在本发明的启示下都可得出其他各
种形式的产品,均属于本发明的保护范围。上述具体实施方式不应理解成对本发明的保护范围的限制,本领域的普通技术人员应当理解,在不背离本发明的范围下,可对前述各实施例所记载的技术方案进行修改,或对其中部分或者全部技术特征进行等同替换,与此同时这些修改或者替换,并不会使相应的技术方案的本质脱离本发明各实施例技术方案的范围。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。