用于增强的免疫疗法的系统和方法
相关申请的交叉引用
1.本技术要求2020年11月03日提交的国际申请号pct/cn2020/126186、2020年11月03日提交的国际申请号pct/cn2020/126179和2021年2月24日提交的国际申请号pct/cn2021/077658的权益,所述申请各自通过引用整体并入本文。
背景技术:
2.癌症(例如,赘生物、肿瘤)是世界范围内的主要死因,每年导致约1千万人死亡。癌症为个人、家庭、社区和国家持续带来渐增的健康、经济和感情负担。对癌症生物学(例如,具体而言癌症免疫生物学)和基因工程愈加深入的理解已经鼓励开发过继细胞疗法(例如,细胞免疫疗法),目标是治疗或控制多种不同的癌症。
技术实现要素:
3.本公开文本提供用于治疗癌症的方法和系统。本公开文本的一些方面提供工程化的免疫细胞(例如,工程化的自然杀伤(nk)细胞)及其用于癌症如例如血液学恶性肿瘤或实体瘤的治疗的使用方法。
4.在一方面,本公开文本提供一种工程化的nk细胞的群体,其中:工程化的nk细胞的所述群体的工程化的nk细胞包含异源多肽,其中所述异源多肽包括异源il-15;并且工程化的nk细胞的所述群体在基本上不含外源白介素-2(il-2)的环境中的持久性水平比nk细胞的可比较群体在包含外源il-2的对照环境中的对照持久性水平高至少约5%。
5.在另一方面,本公开文本提供一种工程化的nk细胞的群体,其中:所述群体的工程化的nk细胞包含异源分泌型il-15;并且工程化的nk细胞的所述群体展现il-15的内源下游信号传导蛋白的信号传导水平比缺乏所述异源分泌型il-15的nk细胞的对照群体的内源下游信号传导蛋白的对照信号传导水平高至少约0.1倍。
6.在另一方面,本公开文本提供一种工程化的nk细胞的群体,其中:工程化的nk细胞的所述群体的工程化的nk细胞包含包括选自pd-l2、tgf-β、cd46、cd55和cd59的一个或多个成员的至少一种异源低免疫性调节多肽;并且如与缺乏所述至少一种异源低免疫性调节多肽的nk细胞的对照群体相比,工程化的nk细胞的所述群体展现增强的针对免疫排斥的抗性。
7.在另一方面,本公开文本提供一种工程化的nk细胞的群体,其中:工程化的nk细胞的所述群体的工程化的nk细胞包含多种异源低免疫性调节多肽;并且如与缺乏所述多种异源低免疫性调节多肽中的一种或多种的nk细胞的对照群体相比,工程化的nk细胞的所述群体展现增强至少约5%的针对免疫排斥的抗性。
8.在另一方面,本公开文本提供一种工程化的nk细胞的群体,其中:工程化的nk细胞的所述群体的工程化的nk细胞包含降低的并非ptpn2的至少一种内源免疫调节多肽的表达;并且工程化的nk细胞的所述群体的持久性水平高于缺乏(i)和/或(ii)的nk细胞的对照群体的对照持久性水平。
9.在另一方面,本公开文本提供一种包含如本文所公开的工程化的nk细胞的群体的组合物。
10.在另一方面,本公开文本提供一种生成如本文所公开的工程化的nk细胞的群体的方法。在一些实施方案中,工程化的nk细胞的所述群体是从诱导多能干细胞(ipsc)生成。
11.在另一方面,本公开文本提供一种治疗有需要的受试者的方法,所述方法包括向所述受试者施用如本文所公开的工程化的nk细胞的群体。
12.从以下详细描述中,本公开文本的其他方面和优点对于本领域技术人员将变得显而易见,其中仅示出和描述了本公开文本的说明性实施方案。如将认识到的,本公开文本能够具有其他和不同的实施方案,并且其若干细节能够在各种明显的方面进行修改,所有这些都不脱离本公开文本。因此,附图和描述本质上应被视为说明性的而非限制性的。通过引用并入
13.此说明书中提到的所有出版物、专利和专利申请都通过引用并入本文,并入程度就像每个单独的出版物、专利或专利申请被明确和单独地指出以通过引用并入一样。就通过引用并入的出版物和专利或专利申请与说明书中包括的公开内容相矛盾而言,说明书旨在取代和/或优先于任何这种矛盾的材料。
附图说明
14.本发明的新颖特征在随附权利要求中具体阐述。通过参考以下详细描述,将获得对本发明的特征和优点的更好理解,该详细描述阐述了使用本发明原理的说明性实施方案和附图(本文中也称为“图”),并且附图中:
15.图1a-图1g说明包含用于增强的cd16信号传导的cd16变体的工程化的nk细胞;
16.图2a-图2g说明包含针对cd19的嵌合抗原受体的工程化的nk细胞;并且
17.图3a和图3b说明包含异源人il-15的工程化的t细胞。
18.图4a-图4e说明在wt ink和从不同hncd16-ipsc克隆分化的ink之间cd56
、nkg2a
、nkp30
、nkp44
和nkp46
的表达。(图4a)总分化细胞中cd56
细胞的百分比。(图4b)cd56
群体中nkg2a
的百分比。(图4c)cd56
群体中nkp30
的百分比。(图4d)cd56
群体中nkp44
的百分比。(图4e)cd56
群体中nkp46
细胞的百分比。
19.图5说明通过facs(荧光激活细胞分选法)用pe(藻红蛋白)缀合的抗cd16抗体检测的在hncd16(具有增强的cd16信号传导)nk-92细胞中cd16的过表达。
20.图6说明通过facs用apc(别藻蓝蛋白)缀合的抗il-15抗体检测的在从hil15-il15ra融合-1ipsc克隆分化的ink细胞中il-15的表面表达。pw15、pw18和pw23是表达膜结合il-15的克隆。
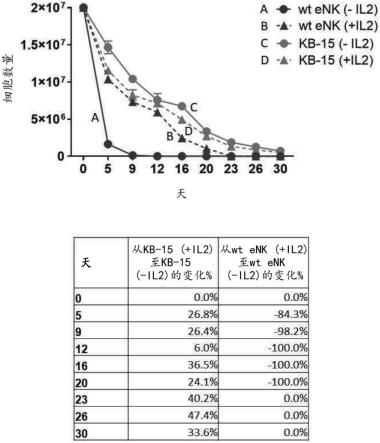
21.图7说明在存在或不存在il-2的情况下培养的从表达mbil-15的ipsc克隆分化的enk细胞(kb-15)的体外生长曲线。
22.图8a-图8e说明在wt ink和从不同mbil-15-ipsc克隆分化的ink之间cd56
、nkg2a
、nkp30
、nkp44
和nkp46
的表达。(图8a)总分化细胞中cd56
细胞的百分比。(图8b)cd56
群体中nkg2a
的百分比。(图8c)cd56
群体中nkp30
的百分比。(图8d)cd56
群体中nkp44
的百分比。(图8e)cd56
群体中nkp46
细胞的百分比。
23.图9a-图9b说明在用工程化的mbil-15enk细胞输注后8、15和22天,具有nalm-6异
种移植模型的ncg小鼠的外周血中的nk细胞浓度。(图9a)通过facs用cd56-apc抗体检测的nk细胞。(图9b)图9a的定量。qn-019表示表达acd19 car hncd16 膜结合il-15的enk。qn-001表示wt enk。
24.图10a-图10c说明从表达分泌型il-15的ipsc克隆分化的nk细胞的特性。(图10a)在wt ink细胞和从不同sil15-ipsc克隆分化的ink之间,总分化细胞中cd56
细胞的百分比。(图10b)来自wt ink细胞和从表达分泌型il-15的ipsc克隆分化的ink细胞(ka08)的培养基中il-15的浓度。(图10c)在不存在外源细胞因子的情况下,wt enk细胞和从表达分泌型il-15的ipsc克隆分化的enk细胞(oq-20)的体外生长曲线。
25.图11说明经由编辑和分化ipsc进行的针对低免疫性的测试方案。
26.图12a-图12q说明确认的编辑-1克隆至编辑-9克隆的建立。图12a说明编辑-1克隆的facs分析(用靶向b2m的预混合的核糖核蛋白[rnp]电穿孔的hipsc)。图12b说明编辑-1克隆的桑格测序(sanger sequencing)。图12c说明编辑-2克隆的桑格测序(用靶向ciita的rnp电穿孔的hipsc)。图12d说明编辑-3克隆的facs分析(用靶向b2m和ciita的两种rnp电穿孔的hipsc)。图12e说明编辑-3克隆的桑格测序。图12f说明编辑-4克隆的facs分析(用过表达pd-l1、pd-l2、tgf-β、hla-e、hla-g、cd47、il-10、ccl-21、cd46、cd55、cd59的构建体以及靶向b2m和ciita的两种rnp电穿孔的hipsc)。图12g说明编辑-4克隆的桑格测序。图12h说明编辑-5克隆的facs分析(用过表达pd-l1、hla-e、cd47、il-10、ccl-21的构建体以及靶向b2m和ciita的两种rnp电穿孔的hipsc)。图12i说明编辑-5克隆的桑格测序。图12j说明编辑-6克隆的facs分析(用过表达pd-l1、hla-e、cd47、cd46、cd55、cd59的构建体以及靶向b2m和ciita的两种rnp电穿孔的hipsc)。图12k说明编辑-6克隆的桑格测序。图12l说明编辑-7克隆的facs分析(用过表达pd-l1、hla-e、cd47、ccl-21、cd55的构建体以及靶向b2m和ciita的两种rnp电穿孔的hipsc)。图12m说明编辑-7克隆的桑格测序。图12n说明编辑-8克隆的facs分析(用过表达cd47的构建体以及靶向b2m和ciita的两种rnp电穿孔的hipsc)。图12o说明编辑-8克隆的桑格测序。图12p说明编辑-9克隆的facs分析(用过表达pd-l1、pd-l2、tgf-β、hla-e、hla-g、cd47、il-10、ccl-21、cd46、cd55、cd59的构建体、靶向b2m和ciita的两种rnp电穿孔的hipsc)。图12q说明编辑-9克隆的桑格测序。从编辑-1至编辑-9的基因编辑总结于图18中。
[0027]
图13a-图13s说明编辑-1克隆至编辑-9克隆的功能特性。(图13a)当不同编辑的ipsc克隆与人补体共孵育时的细胞裂解。(图13b)当不同编辑的ipsc克隆与脐带血来源的自然杀伤(cbnk)共孵育时的细胞裂解。(图13c)在从相应编辑的ipsc分化的不同ink之间cd56
细胞的细胞计数。ipsc克隆编号显示于括号中。(图13d)在从相应编辑的ipsc分化的不同ink之间的cd56
百分比。ipsc克隆编号显示于括号中。(图13e)在从相应编辑的ipsc分化的不同ink之间的nkg2a
百分比。ipsc克隆编号显示于括号中。(图13f)当在单一时间点与相应enk共培养时k562细胞的nk细胞介导的裂解。(图13g)当在6天中与相应enk共培养时k562细胞的nk细胞介导的裂解。(图13h)当具有不同编辑的ink与来自供体1的外周血单个核细胞(pbmc)共培养时增殖cd8
t细胞的百分比。(图13i)当具有不同编辑的ink与来自供体2的pbmc共培养时增殖cd8
t细胞的百分比。(图13j)当具有不同编辑的ink与来自供体3的pbmc共培养时增殖cd8
t细胞的百分比。(图13k)当具有不同编辑的ink与来自供体4的pbmc共培养时增殖cd8
t细胞的百分比。(图13l)当具有不同编辑的ink与来自供体5的pbmc
共培养时增殖cd8
t细胞的百分比。(图13m)当具有不同编辑的ink与来自供体6的pbmc共培养时增殖cd8
t细胞的百分比。(图13n)当具有不同编辑的ink与来自供体1的pbmc共培养时增殖cd4
t细胞的百分比。(图13o)当具有不同编辑的ink与来自供体2的pbmc共培养时增殖cd4
t细胞的百分比。(图13p)当具有不同编辑的ink与来自供体3的pbmc共培养时增殖cd4
t细胞的百分比。(图13q)当具有不同编辑的ink与来自供体4的pbmc共培养时增殖cd4
t细胞的百分比。(图13r)当具有不同编辑的ink与来自供体5的pbmc共培养时增殖cd4
t细胞的百分比。(图13s)当具有不同编辑的ink与来自供体6的pbmc共培养时增殖cd4
t细胞的百分比。
[0028]
图14a-图14c说明针对持久性对工程化的nk细胞的筛选。(图14a)设计用于nk持久性相关基因的体外筛选的方法,其比较与低或高细胞因子一起培养。(图14b)当与低或高细胞因子一起培养时,在fcer1g缺陷编辑中插入缺失(indel)的百分比。(图14c)当与低或高细胞因子一起培养时,在ptpn2缺陷编辑中插入缺失的百分比。
[0029]
图15a-图15g说明针对持久性对工程化的nk细胞的筛选。(图15a)设计用于nk持久性相关基因的体内筛选的方法,其比较体外培养和体内生长。(图15b)在小鼠肝中相比于与高细胞因子一起培养,在stat3缺陷编辑中插入缺失的百分比。(图15c)在小鼠脾中相比于与高细胞因子一起培养,在stat3缺陷编辑中插入缺失的百分比。(图15d)在小鼠骨髓(bm)中相比于与高细胞因子一起培养,在stat3缺陷编辑中插入缺失的百分比。(图15e)在小鼠肝中相比于与高细胞因子一起培养,在ptpn2缺陷编辑中插入缺失的百分比。(图15f)在小鼠脾中相比于与高细胞因子一起培养,在ptpn2缺陷编辑中插入缺失的百分比。(图15g)在小鼠骨髓(bm)中相比于与高细胞因子一起培养,在ptpn2缺陷编辑中插入缺失的百分比。
[0030]
图16a-图16b说明具有cd33-car整合的nk92细胞的特性。(图16a)cd33car结构设计的示意图。tm代表跨膜结构域;scfv代表单链可变片段。(图16b)cd33-car nk92细胞对kg1细胞的靶向细胞毒性。
[0031]
图17a-图17d说明具有bcma-car整合的nk92细胞的特性。(图17a)bcma car结构设计的示意图。tm代表跨膜结构域;scfv代表单链可变片段。(图17b)bcma-car nk92细胞对rpmi8826细胞的靶向细胞毒性。(图17c)在bcma-car nk92细胞与wt nk92细胞中,cd107a的表达的百分比。(图17d)在bcma-car nk92细胞与wt nk92细胞中,ifn-γ的表达的百分比。
[0032]
图18是从编辑-1至编辑-9的基因编辑的总结。
[0033]
图19a显示包含能够与cd19特异性结合的抗原结合部分的不同嵌合受体多肽构建体(例如,不同嵌合抗原受体构建体)。图19b和图19c显示包含图19a中所示不同嵌合受体多肽之一的nk细胞针对cd19呈递靶细胞的靶向细胞毒性。
具体实施方式
[0034]
虽然在本文中已经示出和描述了本发明的各种实施方案,但是对于本领域的技术人员来说,显然这些实施方案仅作为举例提供。在不脱离本发明的情况下,本领域技术人员可以想到许多变化、改变和替换。应当理解,可以采用在本文中描述的本发明实施方案的各种替代方案。
[0035]
除非上下文另有明确指示,如说明书和权利要求中所用,单数形式“一个/一种(a)”、“一个/一种(an)”和“所述(the)”包括复数指示物。例如,术语“嵌合跨膜受体”包括多
种嵌合跨膜受体。
[0036]
术语“约”或“大约”通常意指在如由本领域普通技术人员确定的特定值的可接受的误差范围内,这将部分取决于如何测量或确定所述值,即测量系统的局限性。例如,根据本领域的实践,“约”可以意指在1个或超过1个标准差内。可替代地,“约”可以意指给定值的至多20%、至多10%、至多5%或至多1%的范围。可替代地,特别是关于生物系统或过程,所述术语可以意指在值的一个数量级内,优选在5倍内,并且更优选在2倍内。在本技术和权利要求书中描述特定值的情况下,除非另有说明,应假设术语“约”意指在所述特定值的可接受的误差范围内。
[0037]
替代方案(例如,“或”)的使用应理解为意指替代方案中的一个、两个或它们的任何组合。术语“和/或”应理解为意指一个或两个替代方案。
[0038]
术语“细胞”通常是指生物细胞。细胞可以是活的生物体的基础的结构、功能和/或生物学单元。细胞可以源自具有一个或多个细胞的任何生物体。一些非限制性例子包括:原核细胞、真核细胞、细菌细胞、古细菌细胞、单细胞真核生物体的细胞、原生动物细胞、来自植物的细胞(例如来自植物作物、水果、蔬菜、谷类、大豆、玉米(corn)、玉米(maize)、小麦、种子、番茄、稻、木薯、甘蔗、南瓜、干草、马铃薯、棉花、大麻、烟草、有花植物、松柏植物、裸子植物、蕨类、石松、金鱼藻、苔类植物、藓类植物)、藻细胞(例如,布朗葡萄藻(botryococcus braunii)、莱茵衣藻(chlamydomonas reinhardtii)、盖蒂塔微拟球藻(nannochloropsis gaditana)、蛋白核小球藻(chlorella pyrenoidosa)、展枝马尾藻c.agardh(sargassum patens c.agardh)等)、海藻(例如昆布)、真菌细胞(例如,酵母细胞、来自蘑菇的细胞)、动物细胞、来自无脊椎动物(例如果蝇、刺胞动物、棘皮动物、线虫等)的细胞、来自脊椎动物(例如,鱼、两栖动物、爬行动物、鸟、哺乳动物)的细胞、来自哺乳动物(例如,猪、牛、山羊、绵羊、啮齿动物、大鼠、小鼠、非人灵长类动物、人等)的细胞等等。有时,细胞并非源自天然生物体(例如细胞可以是合成制备的,有时称为人工细胞)。
[0039]
如本文可互换使用的术语“重编程”、“去分化”、“增加细胞潜能”或“增加发育潜能”通常是指增加细胞潜能或将细胞去分化至更低分化状态的方法。例如,与处于非重编程状态的相同细胞相比,具有增加的细胞潜能的细胞具有更高的发育可塑性(即,可以分化为更多细胞类型)。换言之,重编程的细胞是处于比处于非重编程状态的相同细胞更低的分化状态的细胞。
[0040]
术语“分化”通常是指未特化(“未定型”)或较低特化的细胞借以获得特化细胞如例如免疫细胞的特征的过程。分化的或分化诱导的细胞是已经呈现细胞谱系内的更特化(“定型”)的位置的细胞。术语“定型的”通常是指已经在分化途径中前进至一点的细胞,在所述点,在正常情况下,其将继续分化为特定细胞类型或细胞类型的子集,并且在正常情况下无法分化为不同的细胞类型或恢复至较低分化的细胞类型。
[0041]
术语“多能”通常是指细胞形成身体或胞体(即,胚体)的所有谱系的能力。例如,胚胎干细胞是一类多能干细胞,其能够从三个胚层即外胚层、中胚层和内胚层中的每一个形成细胞。多能性可以是发育潜能的连续谱,所述发育潜能的范围为不能产生完整生物体的不完全或部分多能的细胞(例如,上胚层干细胞)至能够产生完整生物体的更原始、更多能的细胞(例如,胚胎干细胞)。
[0042]
术语“诱导多能干细胞”(ipsc)通常是指源自分化的细胞(例如,分化的成体、新生
儿或胎儿细胞)的干细胞,其已经被诱导或改变(即,重编程)为能够分化为以下所有三个胚层或皮层的组织的细胞:中胚层、内胚层和外胚层。所产生的ipsc并非是指如其在自然中被发现的那样的细胞。在一些情形中,可以将ipsc工程化以直接分化为定型的细胞(例如,自然杀伤(nk)细胞。在一些情形中,可以将ipsc工程化以首先分化为组织特异性干细胞(例如,造血干细胞(hsc)),其可以被进一步诱导以分化为定型的细胞(例如,nk细胞)。
[0043]
术语“胚胎干细胞”(esc)通常是指胚胎胚泡的内细胞团的天然存在的多能干细胞。胚胎干细胞是多能的并且在发育期间产生三个原胚层即外胚层、内胚层和中胚层的所有衍生物。在一些情形中,可以将esc工程化以直接分化为定型的细胞(例如,nk细胞)。在一些情形中,可以将esc工程化以首先分化为组织特异性干细胞(例如,hsc),其可以被进一步诱导以分化为定型的细胞(例如,nk细胞)。
[0044]
术语“分离的干细胞”通常是指从多细胞生物体分离的本文所公开的任何类型的干细胞(例如,esc、hsc、间充质干细胞(msc)等)。例如,可以从哺乳动物身体如人的身体分离hsc。在另一例子中,可以从胚胎分离胚胎干细胞。
[0045]
术语“分离的”通常是指已经与其初始环境分开的细胞或细胞群。例如,分离的细胞的新环境基本上不含如在“未分离的”参考细胞所存在的环境中发现的至少一种组分。分离的细胞可以是从如所述细胞在其自然环境中被发现的那样的一些或所有组分去除的细胞,例如,从组织或活检样品分离的细胞。所述术语还包括从如所述细胞在非天然存在的环境中被发现的那样的至少一种、一些或所有组分去除的细胞,例如,从细胞培养物或细胞悬浮液分离的细胞。因此,分离的细胞与如所述细胞在自然界中被发现的那样或者如所述细胞在非天然存在的环境中生长、储存或生存的那样的至少一种组分(包括其他物质、细胞或细胞群)部分或完全分离。
[0046]
如本文可互换使用的术语“造血干细胞和祖细胞”、“造血干细胞”、“造血祖细胞”或“造血前体细胞”通常是指定型至造血谱系但是能够进一步造血分化(例如,分化为nk细胞)的细胞,并且包括多潜能造血干细胞(成血细胞)、髓样祖细胞、巨核细胞系祖细胞、红细胞系祖细胞和淋巴样祖细胞。造血干细胞和祖细胞(hsc)是产生所有血细胞类型的多潜能干细胞,所述血细胞类型包括髓样谱系(单核细胞和巨噬细胞、嗜中性粒细胞、嗜碱性粒细胞、嗜酸性粒细胞、红细胞、巨核细胞/血小板、树突细胞)和淋巴样谱系(t细胞、b细胞、nk细胞)。在一些情形中,hsc可以是能够产生成熟髓样和淋巴样细胞类型二者(包括t细胞、nk细胞和b细胞)的cd34 造血细胞。
[0047]
术语“免疫细胞”通常是指分化的造血细胞。免疫细胞的非限制性例子可以包括nk细胞、t细胞、单核细胞、先天淋巴细胞、肿瘤浸润淋巴细胞、巨噬细胞、粒细胞等。
[0048]
术语“nk细胞”或“自然杀伤细胞”通常是指通过cd56或cd16的表达以及t细胞受体(cd3)的不存在来定义的外周血淋巴细胞的子集。在一些情形中,nk细胞的表型为cd3-和cd56 ,其表达nkg2c和cd57中的至少一种(例如,nkg2c、cd57或者以相同或不同程度表达二者),并且任选地表达cd16,但是缺乏以下中的一种或多种的表达:plzf、syk、fcerγ和eat-2。在一些情形中,cd56 nk细胞的分离的子群体可以展现以下的表达:cd16、nkg2c、cd57、nkg2d、ncr配体、nkp30、nkp40、nkp46、激活和抑制kir、nkg2a和/或dnam-1。
[0049]
如本文所用的术语“核苷酸”通常是指碱基-糖-磷酸酯组合。核苷酸可以包括合成核苷酸。核苷酸可以包括合成核苷酸类似物。核苷酸可以是核酸序列(例如脱氧核糖核酸
(dna)和核糖核酸(rna))的单体单元。术语核苷酸可以包括核糖核苷三磷酸腺苷三磷酸(atp)、尿苷三磷酸(utp)、胞嘧啶三磷酸(ctp)、鸟苷三磷酸(gtp)以及脱氧核糖核苷三磷酸如datp、dctp、ditp、dutp、dgtp、dttp或其衍生物。这样的衍生物可以包括例如[αs]datp、7-脱氮-dgtp和7-脱氮-datp,以及如下核苷酸衍生物:所述核苷酸衍生物赋予含有它们的核酸分子以核酸酶抗性。如本文所用术语核苷酸可以是指双脱氧核糖核苷三磷酸(ddntp)及其衍生物。双脱氧核糖核苷三磷酸的说明性例子可以包括但不限于ddatp、ddctp、ddgtp、dditp和ddttp。核苷酸可以是未标记的或者通过熟知技术进行可检测标记。标记也可以用量子点来进行。可检测标记可以包括例如放射性同位素、荧光标记、化学发光标记、生物发光标记和酶标记。核苷酸的荧光标记可以包括但不限于荧光素、5-羧基荧光素(fam)、2'7'-二甲氧基-4'5-二氯-6-羧基荧光素(joe)、罗丹明、6-羧基罗丹明(r6g)、n,n,n',n'-四甲基-6-羧基罗丹明(tamra)、6-羧基-x-罗丹明(rox)、4-(4'二甲基氨基苯偶氮基)苯甲酸(dabcyl)、cascade blue、oregon green、texas red、酞菁和5-(2'-氨基乙基)氨基萘-1-磺酸(edans)。荧光标记的核苷酸的具体例子可以包括:[r6g]dutp、[tamra]dutp、[r110]dctp、[r6g]dctp、[tamra]dctp、[joe]ddatp、[r6g]ddatp、[fam]ddctp、[r110]ddctp、[tamra]ddgtp、[rox]ddttp、[dr6g]ddatp、[dr110]ddctp、[dtamra]ddgtp和[drox]ddttp,可从perkin elmer(福斯特市,加利福尼亚州)获得;fluorolink脱氧核苷酸、fluorolink cy3-dctp、fluorolink cy5-dctp、fluorolink fluor x-dctp、fluorolink cy3-dutp和fluorolink cy5-dutp,可从amersham(阿灵顿高地,伊利诺伊州)获得;荧光素-15-datp、荧光素-12-dutp、四甲基-罗丹明-6-dutp、ir770-9-datp、荧光素-12-ddutp、荧光素-12-utp和荧光素-15-2'-datp,可从boehringer mannheim(印第安纳波利斯,印第安纳州)获得;以及染色体标记的核苷酸、bodipy-fl-14-utp、bodipy-fl-4-utp、bodipy-tmr-14-utp、bodipy-tmr-14-dutp、bodipy-tr-14-utp、bodipy-tr-14-dutp、cascade blue-7-utp、cascade blue-7-dutp、荧光素-12-utp、荧光素-12-dutp、oregon green 488-5-dutp、罗丹明green-5-utp、罗丹明green-5-dutp、四甲基罗丹明-6-utp、四甲基罗丹明-6-dutp、texas red-5-utp、texas red-5-dutp和texas red-12-dutp,可从molecular probes(尤金,俄勒冈州)。核苷酸也可以通过化学修饰来标记或加标。化学修饰的单一核苷酸可以是生物素-dntp。生物素化的dntp的一些非限制性例子可以包括生物素-datp(例如,bio-n6-ddatp、生物素-14-datp)、生物素-dctp(例如,生物素-11-dctp、生物素-14-dctp)和生物素-dutp(例如生物素-11-dutp、生物素-16-dutp、生物素-20-dutp)。
[0050]
如本文可互换使用的术语“多核苷酸”、“寡核苷酸”或“核酸”通常是指任何长度的核苷酸(脱氧核糖核苷酸或核糖核苷酸或其类似物)的聚合形式,其呈单链、双链或多链形式。多核苷酸可以对于细胞是外源的或内源的。多核苷酸可以存在于无细胞环境中。多核苷酸可以是基因或其片段。多核苷酸可以是dna。多核苷酸可以是rna。多核苷酸可以具有任何三维结构,并且可以执行任何功能,已知的或未知的。多核苷酸可以包含一种或多种类似物(例如改变的骨架、糖或核碱基)。如果存在对核苷酸结构的修饰,其可以在聚合物装配之前或之后被赋予。类似物的一些非限制性例子包括:5-溴尿嘧啶、肽核酸、异种核酸(xeno nucleic acid)、吗啉代、锁核酸、二醇核酸、苏阿糖核酸、双脱氧核苷酸、虫草菌素、7-脱氮-gtp、荧光团(例如与糖连接的罗丹明或荧光素)、含有硫醇的核苷酸、生物素连接的核苷酸、荧光碱基类似物、cpg岛、甲基-7-鸟苷、甲基化核苷酸、肌苷、硫脲苷、假尿苷、二氢尿苷、辫
苷和怀俄苷。多核苷酸的非限制性例子包括基因或基因片段的编码或非编码区、根据谱系分析定义的多个基因座(一个基因座)、外显子、内含子、信使rna(mrna)、转移rna(trna)、核糖体rna(rrna)、干扰短rna(sirna)、短发夹rna(shrna)、微rna(mirna)、核酶、cdna、重组多核苷酸、分支多核苷酸、质粒、载体、分离的任何序列的dna、分离的任何序列的rna、无细胞多核苷酸(包括无细胞dna(cfdna)和无细胞rna(cfrna))、核酸探针和引物。核苷酸的序列可以被非核苷酸组分中断。
[0051]
术语“基因”通常是指参与编码rna转录物的核酸(例如,dna,如基因组dna和cdna)及其相应核苷酸序列。如本文关于基因组dna所用的所述术语包括间插非编码区域以及调节区域,并且可以包括5'端和3'端。在一些使用中,所述术语涵盖转录的序列,包括5'和3'非翻译区(5'-utr和3'-utr)、外显子和内含子。在一些基因中,转录的区域将含有编码多肽的“开放阅读框”。在所述术语的一些使用中,“基因”仅包含编码多肽所需的编码序列(例如,“开放阅读框”或“编码区”)。在一些情形中,基因不编码多肽,例如,核糖体rna基因(rrna)和转移rna(trna)基因。在一些情形中,术语“基因”不仅包括转录的序列,而且另外还包括非转录区域,包括上游和下游调节区域、增强子和启动子。基因可以是指位于其在生物体基因组中的天然位置的“内源基因”或天然基因。基因可以是指“外源基因”或非天然基因。非天然基因可以是指通常并非在宿主生物体中发现而是通过基因转移被引入宿主生物体中的基因。非天然基因还可以是指并非位于其在生物体基因组中的天然位置的基因。非天然基因还可以是指包含突变、插入和/或缺失(例如,非天然序列)的天然存在的核酸或多肽序列。
[0052]
术语“表达”通常是指多核苷酸从dna模板被转录(如转录为mrna或其他rna转录物)的一个或多个过程和/或转录的mrna随后被翻译为肽、多肽或蛋白质的过程。转录物和编码的多肽可以被统称为“基因产物”。如果多核苷酸源自基因组dna,表达可以包括真核细胞中mrna的剪接。关于表达的“上调的”通常是指多核苷酸(例如,rna,如mrna)和/或多肽序列相对于其在野生型状态中的表达水平提高的表达水平,而“下调的”通常是指多核苷酸(例如,rna,如mrna)和/或多肽序列相对于其在野生性状态中的表达降低的表达水平。转染的基因的表达可以在细胞中瞬时或稳定进行。在“瞬时表达”期间,转染的基因没有在细胞分裂期间被转移至子细胞中。因为其表达被限制于转染的细胞,所以所述基因的表达随着时间而丧失。相比之下,在转染的基因与赋予对被转染细胞的选择优势的另一基因共转染时,可以发生所述基因的稳定表达。这样的选择优势可以是针对被呈递至所述细胞的某种毒素的抗性。
[0053]
如本文可互换使用的术语“肽”、“多肽”或“蛋白质”通常是指通过一个或多个肽键接合的至少两个氨基酸残基的聚合物。此术语没有表示聚合物的具体长度,其也不意图暗示或区分所述肽是使用重组技术、化学或酶合成来产生的还是天然存在的。所述术语适用于天然存在的氨基酸聚合物以及包含至少一个修饰的氨基酸的氨基酸聚合物。在一些情形中,聚合物可以被非氨基酸中断。所述术语包括任何长度的氨基酸链,包括全长蛋白质以及具有或没有二级和/或三级结构(例如,结构域)的蛋白质。所述术语还涵盖已经被修饰的氨基酸聚合物,例如,通过二硫键形成、糖基化、脂化、乙酰化、磷酸化、氧化和任何其他操作如与标记组分缀合来修饰。如本文所用术语“氨基酸(amino acid)”和“氨基酸(amino acids)”通常是指天然和非天然氨基酸,包括但不限于修饰的氨基酸和氨基酸类似物。修饰
的氨基酸可以包括天然氨基酸和非天然氨基酸,其已经被化学修饰以包括并非天然存在于所述氨基酸上的基团或化学部分。氨基酸类似物可以是指氨基酸衍生物。术语“氨基酸”包括d-氨基酸和l-氨基酸二者。
[0054]
如本文关于多肽所用术语“衍生物”、“变体”或“片段”,通常是指与野生型多肽相关的多肽,例如在氨基酸序列、结构(例如,二级和/或三级)、活性(例如,酶活性)和/或功能方面相关。与野生型多肽相比,多肽的衍生物、变体和片段可以包含一个或多个氨基酸变异(例如,突变、插入和缺失)、截短、修饰或其组合。
[0055]
如本文关于多肽分子(例如,蛋白质)所用的术语“工程化的”、“嵌合的”或“充足的”通常是指由于将基因工程化技术应用于编码多肽分子的核酸以及表达多肽分子的细胞或生物体而具有异源氨基酸序列或改变的氨基酸序列的多肽分子。如本文关于多核苷酸分子(例如,dna或rna分子)所用的术语“工程化的”或“充足的”通常是指由于应用基因工程化技术而具有异源核酸序列或改变的核酸序列的多核苷酸分子。基因工程化技术包括但不限于pcr和dna克隆技术;转染、转化和其他基因转移技术;同源重组;定点诱变;以及基因融合。在一些情形中,工程化或重组多核苷酸(例如,基因组dna序列)可以被基因编辑部分修饰或改变。
[0056]
术语“基因编辑部分”通常是指可以编辑核酸序列的部分,其对于包含所述核酸序列的细胞是外源的或内源的。在一些实施方案中,基因编辑部分通过编辑核酸序列来调节基因的表达。在一些情形中,基因编辑部分可以通过编辑基因组dna序列来调节基因的表达。在一些情形中,基因编辑部分可以通过编辑mrna模板来调节基因的表达。在一些情形中,编辑核酸序列可以改变基因表达的底层模板。
[0057]
可替代地或另外地,基因编辑部分可能能够通过以下方式来调节基因的表达或活性:特异性结合至与所述基因可操作地偶联的靶序列(或者在所述基因内的靶序列),并调节从dna(如染色体dna或cdna)产生mrna。在一些情形中,基因编辑部分可以招募或包含结合至特定dna序列的至少一种转录因子,从而控制遗传信息从dna转录为mrna的速率。基因编辑部分可以自身结合至dna并通过物理阻碍来调节转录,所述物理阻碍例如防止蛋白质如rna聚合酶和其他相关蛋白在dna模板上装配。基因编辑部分可以在翻译水平上调节基因的表达,例如,通过调节从mrna模板产生蛋白质。在一些情形中,基因编辑部分可以通过影响mrna转录物的稳定性来调节基因表达。
[0058]
术语“抗体”通常是指具有免疫球蛋白样功能的蛋白质结合分子。术语抗体包括抗体(例如,单克隆和多克隆抗体)以及其衍生物、变体和片段。抗体包括但不限于不同类别(即iga、igg、igm、igd和ige)和亚类(如igg1、igg2等)的免疫球蛋白(ig)。其衍生物、变体或片段可以是指保留相应抗体的结合特异性(例如,完全和/或部分)的功能衍生物或片段。抗体结合片段包括fab、fab'、f(ab')2、可变片段(fv)、单链可变片段(scfv)、微抗体、双抗体和单结构域抗体(“sdab”或“纳米抗体”或“骆驼科动物抗体(camelid)”)。术语抗体包括已经被优化、工程化或化学缀合的抗体和抗体的抗原结合片段。已经被优化的抗体的例子包括亲和力成熟的抗体。已经被工程化的抗体的例子包括fc优化的抗体(例如,在片段可结晶区域中被优化的抗体)和多特异性抗体(例如,双特异性抗体)。
[0059]
术语“嵌合多肽受体”通常是指包含一个或多个抗原结合部分的非天然多肽受体,每个抗原结合部分能够结合至特定抗原。嵌合多肽受体可以是单特异性的(即,能够结合至
一种类型的特定抗原)。可替代地,嵌合多肽受体可以是多特异性的(即,能够结合至两种或更多种不同类型的特定抗原)。嵌合多肽受体可以是单价的(即,包含单一抗原结合部分)。可替代地,嵌合多肽受体可以是多价的(即,包含多个抗原结合部分)。在一些情形中,嵌合多肽受体可以包含t细胞受体(tcr)融合蛋白(tfp)或嵌合抗原受体(car)。
[0060]
术语“抗原结合结构域”通常是指展现与特定靶抗原的优先结合的构建体。抗原结合结构域可以是多肽构建体,如抗体、其功能变体(例如,预设计锚蛋白重复蛋白(darpin))、其修饰、其片段或其组合。抗原结合结构域可以是如本文所公开的任何抗体或其功能变体。抗原结合结构域的非限制性例子可以包括鼠抗体、人抗体、人源化抗体、骆驼ig、鲨鱼仅有重链的抗体(vnar)、ig nar、嵌合抗体、重组抗体或其抗体片段。抗体片段的非限制性例子包括fab、fab'、f(ab)'2、f(ab)'3、fv、单链抗原结合片段(scfv)、(scfv)2、二硫键稳定的fv(dsfv)、微抗体、双抗体、三抗体、四抗体、单结构域抗原结合片段(sdab、纳米抗体)、充足的仅有重链的抗体(vhh)以及维持完整抗体的结合特异性的其他抗体片段。
[0061]
术语“预设计锚蛋白重复蛋白”或“darpin”通常是指包含一个或多个锚蛋白重复结构域的合成多肽,其中所述一个或多个锚蛋白重复结构域能够结合至一种或多种抗原。本文所述的锚蛋白重复结构域通常包含至少一个锚蛋白重复基序。在一些例子中,锚蛋白重复基序包含两个反平行α螺旋和之后的β凸起和β发夹,其含有将所述锚蛋白重复基序与相邻重复连接的环,每个重复基序具有约33个残基。包含预设计锚蛋白重复基序的重组蛋白或其结合结构域可以被称为darpin蛋白或darpin多肽。
[0062]
在一些情形中,本文所述的锚蛋白重复结构域可以包含(i)提供结构的核心支架,和(ii)结合至靶标(例如,靶抗原)的靶标结合残基。结构核心可以包含保守氨基酸残基,并且靶标结合表面可以包含根据靶标而不同的氨基酸残基。在另一例子中,锚蛋白重复基序可以包含以下序列:dxxgxtplhlaxxxgxxxvvxlllxxgadvnax(seq id no:1),其中“x”表示任何氨基酸。在另一例子中,锚蛋白重复基序可以包含以下序列:dxxgxtplhlaxxxgxxx|vxvllxxgadvnax(seq id no:2),其中“x”表示任何氨基酸。
[0063]
在一些情形中,多个锚蛋白重复结构域可以被连接(经由共价键或非共价缔合)以形成双特异性或多特异性分子(例如,双特异性或多特异性嵌合多肽受体)。
[0064]
darpin构建体的例子和细节提供于例如国际专利申请号pct/ep2001/010454中,所述申请通过引用整体并入本文。
[0065]
术语“安全开关”通常是指设计为防止细胞疗法的潜在毒性或其他不良影响的工程化的多肽构建体。当在细胞中表达时,安全开关可以诱导宿主细胞死亡,从而使宿主中(例如,受试者体内)的细胞活性失活。因此,安全开关可以是自杀部分。在一些情形中,细胞可以被编程以在其生命周期的某个阶段表达自杀部分(例如,时间编程)。在一些情形中,自杀部分在细胞中的表达可以是条件性的或诱导性的。在一些例子中,自杀部分的条件性调节(例如,表达)可以包括通过小分子介导的翻译后激活来控制以及组织特异性和/或时序转录调节。因此,安全开关可以是诱导性自杀部分。安全开关可以介导细胞凋亡的诱导、蛋白质合成的抑制、dna复制、生长停滞、转录和转录后基因调节和/或抗体介导的耗尽。在一些情形中,安全开关可以被在激活时触发细胞(例如,如本文所公开的工程化的nk细胞)的细胞凋亡和/或细胞死亡的外源分子(例如,药物或前药)激活。
[0066]
术语“免疫调节多肽”通常是指能够调节或控制免疫细胞如nk细胞的一种或多种
属性的多肽构建体(例如,蛋白质、抗体、膜结合多肽、分泌型多肽、可切割多肽、不可切割多肽等)。免疫细胞的一种或多种属性可以包括免疫细胞的分化、免疫细胞形态、多核苷酸或多肽构建体在免疫细胞内的表达或者免疫细胞的活性(例如,工程化的nk细胞针对患病细胞如癌细胞的细胞毒性活性)。免疫调节多肽可以对于宿主细胞是内源的。可替代地或另外地,免疫调节多肽可以对于宿主细胞是异源的。在一些情形中,控制免疫细胞的一种或多种属性可以通过下调免疫调节多肽的表达(例如,抑制、敲低或敲除)来介导。可替代地或另外地,控制免疫细胞的一种或多种属性可以通过上调免疫调节多肽的表达(例如,内源基因的上调或编码免疫调节多肽的异源基因的敲入)来介导。又在另一替代方案中或者另外地,控制免疫细胞的一种或多种属性可以通过维持免疫调节多肽的表达长于所述免疫调节多肽在宿主细胞中的天然或正常表达谱的时间段来介导。在一些情形中,免疫调节多肽可以包括低免疫性调节剂。在一些情形中,免疫调节多肽可以包括免疫检查点抑制剂。
[0067]
术语“低免疫性调节剂”通常是指细胞中的多肽构建体,其中细胞中低免疫性调节剂的增强的表达(例如,通过异源基因的敲入)或降低的表达(例如,通过内源基因的敲除或敲低)可以帮助细胞在施用至宿主身体后减少或避免来自宿主身体的免疫应答(例如,免疫攻击,如适应性免疫排斥)。在一些情形中,细胞(例如,如本文所公开的工程化的nk细胞)可以被修饰以展现低免疫性调节剂的增强的表达或降低的表达,使得在将所述细胞第二次或进一步输注至宿主(即,受者)后,所述细胞可以逃避宿主免疫攻击。因此,所述细胞(i)不会被宿主的免疫系统(例如,抗体介导的补体细胞毒性,或抗体依赖性细胞毒性(adcc))排斥,和/或(ii)如与没有低免疫性调节剂的增强的表达或降低的表达的对照细胞相比,会以更慢的速率被宿主的免疫系统排斥。展现低免疫性调节剂的增强的表达或降低的表达的细胞可以被称为展现“低免疫性”或者是“免疫豁免的”。例如,如本文所公开的工程化的免疫细胞的群体(例如,工程化的nk细胞的群体)的增强的低免疫性(例如,增强的针对adcc的抗性)可以在体外(例如,在人血清或人补体和抗体(例如,ssea-4抗体)的存在下)或者在体内(例如,在施用至受试者的血流后)被查明。
[0068]
在一些情形中,如本文所公开的免疫细胞(例如,nk细胞)的工程化可以将免疫细胞针对免疫排斥(例如,adcc)的抗性增强至少或多达约5%、至少或多达约10%、至少或多达约15%、至少或多达约20%、至少或多达约25%、至少或多达约30%、至少或多达约40%、至少或多达约50%、至少或多达约60%、至少或多达约70%、至少或多达约80%、至少或多达约85%、至少或多达约90%、至少或多达约95%、至少或多达约100%、至少或多达约150%、至少或多达约200%、至少或多达约300%、至少或多达约400%或者至少或多达约500%。
[0069]
在一些情形中,增强的针对免疫排斥的抗性(例如,adcc)可以在体外在包含至少或多达约5%、至少或多达约10%、至少或多达约15%、至少或多达约20%、至少或多达约25%、至少或多达约30%、至少或多达约40%、至少或多达约50%、至少或多达约60%、至少或多达约70%或者至少或多达约80%人补体的培养基中被查明。
[0070]
术语“免疫检查点抑制剂”通常是指在免疫细胞(例如,t细胞、髓样细胞、nk细胞、b细胞等)的细胞表面上呈现的分子组,其可以通过下调或抑制免疫细胞针对靶细胞如癌细胞的免疫应答(即,抗癌或抗肿瘤免疫应答)来调节所述细胞的免疫应答。靶细胞可以表达在免疫细胞的表面上呈现的免疫检查点抑制剂的受体或配体,以与免疫检查点抑制剂接合
并且下调或抑制免疫细胞针对靶细胞的免疫应答。因此,在一些情形中,下调或抑制免疫检查点抑制剂在免疫细胞中的表达可以增强或延长免疫细胞针对靶细胞的免疫应答。
[0071]
术语“免疫应答”通常是指宿主的免疫系统针对目标(例如,外来目标)的t细胞介导的和/或b细胞介导的免疫应答。免疫应答的例子包括t细胞应答,例如,细胞因子产生和细胞毒性。在一些情形中,免疫应答可以通过t细胞激活(例如,抗体产生(体液应答))和细胞因子响应细胞如巨噬细胞的激活来间接地实现。
[0072]
术语“增强的表达”、“增加的表达”或“上调的表达”通常是指目的部分(例如,多核苷酸或多肽)的产生,其水平高于所述目的部分在宿主品系(例如,宿主细胞)中的正常表达水平。所述正常表达水平可能基本上为零(或空)或高于零。目的部分可以包含宿主品系的内源基因或多肽构建体。目的部分可以包含被引入宿主品系或宿主品系中的异源基因或多肽构建体。例如,编码目的多肽的异源基因可以被敲入(ki)宿主品系的基因组中,用于所述目的多肽在所述宿主品系中的增强的表达。
[0073]
术语“增强的活性”、“增加的活性”或“上调的活性”通常是指目的部分(例如,多核苷酸或多肽)的活性,其被修改至高于所述目的部分在宿主品系(例如,宿主细胞)中的正常活性水平的水平。所述正常活性水平可能基本上为零(或空)或高于零。目的部分可以包含宿主品系的多肽构建体。目的部分可以包含被引入宿主品系或宿主品系中的异源多肽构建体。例如,编码目的多肽的异源基因可以被敲入(ki)宿主品系的基因组中,用于所述目的多肽在所述宿主品系中的增强的活性。
[0074]
术语“降低的表达”、“减少的表达”或“下调的表达”通常是指目的部分(例如,多核苷酸或多肽)的产生,其水平低于所述目的部分在宿主品系(例如,宿主细胞)中的正常表达水平。所述正常表达水平高于零。目的部分可以包含宿主品系的内源基因或多肽构建体。在一些情形中,目的部分可能在宿主品系中被敲除或敲低。在一些例子中,目的部分的降低的表达可以包括对宿主品系中这样的表达的完全抑制。
[0075]
术语“降低的活性”、“减少的活性”或“下调的活性”通常是指目的部分(例如,多核苷酸或多肽)的活性,其被修改至低于所述目的部分在宿主品系(例如,宿主细胞)中的正常活性水平的水平。所述正常活性水平高于零。目的部分可以包含宿主品系的内源基因或多肽构建体。在一些情形中,目的部分可能在宿主品系中被敲除或敲低。在一些例子中,目的部分的降低的活性可以包括对宿主品系中这样的活性的完全抑制。
[0076]
如本文可互换使用的术语“受试者”、“个体”或“患者”通常是指脊椎动物,优选地哺乳动物,如人。哺乳动物包括但不限于鼠、猿猴、人、农场动物、运动动物和宠物。还涵盖在体内获得的或在体外培养的生物实体的组织、细胞及其后代。
[0077]
术语“治疗(treatment)”或“治疗(treating)”通常是指用于获得有益或所需结果(包括但不限于治疗益处和/或预防益处)的方法。例如,治疗可以包括施用本文所公开的系统或细胞群。治疗益处意指在所治疗的一种或多种疾病、病症或症状中的任何治疗相关的改进或对所述疾病、病症或症状的效果。对于预防益处,可以将组合物施用至具有患上特定疾病、病症或症状的风险的受试者,或者施用至报告疾病的一种或多种生理学症状的受试者,即使所述疾病、病症或症状可能尚未表现。
[0078]
术语“有效量”或“治疗有效量”通常是指组合物(例如包含含有本公开文本的系统的免疫细胞如淋巴细胞(例如,t淋巴细胞和/或nk细胞)的组合物)的足以在施用至有需要
的受试者后得到所需活性的量。在本公开文本的上下文内,术语“治疗有效的”通常是指组合物的足以延迟通过本公开文本的方法治疗的障碍的表现、阻止所述障碍的进展、减轻或缓和所述障碍的至少一种症状的量。
[0079]
a.概述
[0080]
t细胞是适应性免疫系统的部分并且可以被致敏以通过识别外来细胞表面上的免疫蛋白(即,抗原)来识别特定威胁。相比之下,nk细胞是先天免疫应答的部分并且可以响应宽范围的被认为是“非自身”的目标。通常,与t细胞不同,nk细胞可以在没有敏化(即,抗原特异性致敏)的情况下攻击其靶细胞以消除外来物质。
[0081]
源自受试者(例如,源自受试者的hsc)的未修饰的nk细胞可以被离体培养和扩增,然后作为治疗被施用至所述受试者以攻击其靶细胞例如癌细胞。然而,基于nk细胞的疗法可能由于离体或体内nk细胞的短半衰期和/或较差增殖而受限。另外,未修饰的nk细胞可能在靶向更难治疗(harder-to-treat)的癌症如骨髓瘤或实体瘤中是无效的。此外,nk细胞基于血液源干细胞(例如,hsc)的离体产生可以得到用于有效过继免疫疗法的nk细胞的有限供应。
[0082]
因此,对于被采购和工程化以展现例如增强的增殖、半衰期和针对靶细胞的细胞毒性活性的nk细胞仍然存在大量需求。
[0083]
b.工程化的免疫细胞
[0084]
本公开文本描述用于免疫疗法的系统和方法。可以将免疫细胞工程化以展现如与对照细胞(例如,非工程化的免疫细胞)相比延长的半衰期。可以将免疫细胞工程化以展现如与对照细胞相比增强的增殖。可以将免疫细胞工程化以有效且特异性靶向对照细胞原本不足以或无法靶向的患病细胞(例如,癌细胞)。本文所公开的工程化的免疫细胞可以离体、在体外以及(在一些情形中)在体内被工程化。可以将离体或在体外制备的工程化的免疫细胞施用至有需要的受试者以治疗疾病(例如,骨髓瘤或实体瘤)。工程化的免疫细胞可以对于受试者是自体的。可替代地,工程化的免疫细胞可以对于受试者是同种异体的。
[0085]
在一些情形中,本文所公开的工程化的免疫细胞(例如,工程化的nk细胞)可以源自分离的干细胞(例如,分离的esc)。在一些情形中,本文所公开的工程化的免疫细胞可以源自诱导干细胞(例如,ipsc)。
[0086]
在一些情形中,本文所公开的干细胞(例如,分离的干细胞、诱导干细胞)可以是自体细胞或源自自体细胞。自体细胞可以从患有病症或怀疑患有病症的受试者获得。可替代地,自体细胞可以在受试者被发现患有病症之前从所述受试者获得。在一些情形中,自体细胞可以是具有降低的免疫原性且具有减少的免疫抑制药物的量或对免疫抑制药物无需要的同种异体细胞,例如,全能干细胞。自体细胞可以从健康供体获得。
[0087]
在一些情形中,工程化的免疫细胞(例如,工程化的nk细胞)可以是自体细胞。工程化的免疫细胞可以从患有病症或怀疑患有病症的受试者获得。可替代地,工程化的免疫细胞可以在受试者被发现患有病症之前从所述受试者获得。在一些情形中,工程化的免疫细胞可以是具有降低的免疫原性且具有减少的免疫抑制药物的量或对免疫抑制药物无需要的同种异体细胞,例如,用于通用同种异体免疫疗法。工程化的免疫细胞可以从健康供体获得。
[0088]
在一些方面,可以将t细胞工程化以展现如与对照细胞(例如,非工程化的t细胞)
相比延长的半衰期。可以将t细胞工程化以展现如与对照细胞相比增强的增殖。可以将t细胞工程化以有效且特异性靶向对照细胞原本不足以或无法靶向的患病细胞(例如,癌细胞)。本文所公开的工程化的t细胞可以离体、在体外以及(在一些情形中)在体内被工程化。可以将离体或在体外制备的工程化的t细胞施用至有需要的受试者以治疗疾病(例如,骨髓瘤或实体瘤)。工程化的t细胞可以对于受试者是自体的。可替代地,工程化的t细胞可以对于受试者是同种异体的。
[0089]
在一些方面,可以将nk细胞工程化以展现如与对照细胞(例如,非工程化的nk细胞)相比延长的半衰期。可以将nk细胞工程化以展现如与对照细胞相比增强的增殖。可以将nk细胞工程化以有效且特异性靶向对照细胞原本不足以或无法靶向的患病细胞(例如,癌细胞)。本文所公开的工程化的nk细胞可以离体、在体外以及(在一些情形中)在体内被工程化。可以将离体或在体外制备的工程化的nk细胞施用至有需要的受试者以治疗疾病(例如,骨髓瘤或实体瘤)。工程化的nk细胞可以对于受试者是自体的。可替代地,工程化的nk细胞可以对于受试者是同种异体的。
[0090]
在一方面,本公开文本提供一种工程化的免疫细胞(例如,工程化的nk细胞)。所述工程化的免疫细胞可以包含对于免疫细胞是异源的细胞因子(例如,分泌型细胞因子)。在一些情形中,所述异源细胞因子可以包含异源白介素(il)(例如,异源分泌型il-15)。工程化的免疫细胞还可以包含以下中的一种或两种:(i)用于如与对照细胞相比增强的cd16信号传导的cd16变体,以及(ii)包含能够与抗原结合的抗原结合部分的嵌合多肽受体。在一些例子中,所述抗原并非cd19。因此,所述抗原结合部分可以不展现并且无需展现与cd19的任何特异性结合,而是展现与并非cd19的抗原(例如,一种或多种抗原)的特异性结合。
[0091]
如本文所公开的工程化的免疫细胞(例如,工程化的nk细胞)可以包含作为如本文所公开的异源细胞因子的相应受体的异源受体(例如,异源il-15的异源il-15受体(il-15r,如il-15α或il-15β))。可替代地,工程化的免疫细胞可能不包含并且无需包含作为异源细胞因子的相应受体的任何异源受体。例如,包含异源il(例如,il-15)的工程化的免疫细胞缺乏异源il的异源受体(例如,il-15r)。
[0092]
在一方面,本公开文本提供一种工程化的免疫细胞(例如,工程化的nk细胞)。所述工程化的免疫细胞可以包含对于免疫细胞是异源的细胞因子(例如,分泌型细胞因子)。异源细胞因子还可以包括异源白介素(il)(例如,异源分泌型il-15)。工程化的免疫细胞可以不包含并且无需包含作为异源细胞因子的相应受体的异源受体(例如,异源il-15r)。
[0093]
如本文所公开的异源细胞因子(例如,异源il)可以属于与工程化的免疫细胞(例如,工程化的nk细胞)相同的物种。例如,异源细胞因子和工程化的免疫细胞二者可以都为人来源。可替代地,异源细胞因子可以属于与工程化的免疫细胞不同的物种。
[0094]
如本文所公开的异源细胞因子(例如,异源il)可以通过使编码异源细胞因子的异源多核苷酸与工程化的免疫细胞接触而被引入工程化的免疫细胞(例如,工程化的nk细胞)。异源多核苷酸可以被整合至工程化的免疫细胞的染色体(例如,核染色体)中。可替代地,异源多核苷酸可以不被整合至并且无需被整合至工程化的免疫细胞的染色体中。在一个例子中,编码异源细胞因子的mrna可以被引入(或插入)工程化的免疫细胞中。
[0095]
在一些情形中,如本文所公开的异源细胞因子可以是异源il。如本文所公开的异源il可以包括至少1、2、3、4、5或更多种不同类型的异源il。如本文所公开的异源il可以包
括至多5、4、3或2种不同类型的异源il。可替代地,异源il可以是单一类型的异源il。异源il的非限制性例子可以包括但不限于il-1、il-2、il-3、il-4、il-5、il-6、il-7、il-8、il-9、il-10、il-11、il-12、il-13、il-14、il-15、il-16、il-17、il-18、il-19、il-20、il-21、il-22、il-23、il-24、il-25、il-26、il-27、il-28、il-29、il-30、il-31、il-32、il-33、il-34、il-35和il-36。在一些例子中,异源il可以包含选自以下的一个或多个成员:il2、il4、il6、il7、il9、il10、il11、il12、il15、il18、il21及其功能修饰。例如,如本文所公开的工程化的免疫细胞(例如,工程化的nk细胞)可以包含异源人il-15(或其编码基因)的至少一部分。
[0096]
如本文所公开的异源细胞因子(例如,异源il)可以是分泌型细胞因子。可替代地,异源细胞因子可以不由并且无需由工程化的免疫细胞分泌。在这样的情形中,例如,异源细胞因子可以结合至工程化的免疫细胞的细胞表面。
[0097]
在一些情形中,如本文所公开的异源细胞因子(例如,异源il)可以是分泌型细胞因子。编码异源细胞因子的表达盒可以被引入工程化的免疫细胞。表达盒还可以编码另外的异源多肽,例如,异源受体。在表达盒内,编码异源细胞因子的第一多核苷酸序列和编码另外的异源多肽(例如,异源受体)的第二多核苷酸序列可以经由编码切割接头的多核苷酸接头彼此偶联。在一些例子中,异源受体可以是异源细胞因子的相应受体(例如,异源il-15的异源il-15α或il-15β)。可替代地,表达盒可以不编码并且无需编码除了异源细胞因子以外的任何另外的异源多肽。
[0098]
如本文所公开的可切割接头可以包含自切割肽,如自切割2a肽。自切割肽可以发现于微小rna病毒科(picornaviridae)病毒科的成员中,包括口蹄疫病毒如口蹄疫病毒(fmdv)、马鼻炎a病毒(erav)、明脉扁刺蛾β四体病毒(tav)和猪捷申病毒-1(ptv-i)以及心病毒如鼠脑脊髓炎病毒(例如,泰勒氏鼠脑脊髓炎)和脑心肌炎病毒。自切割2a肽的非限制性例子可以包括“f2a”、“e2a”、“p2a”、“t2a”及其功能变体。
[0099]
在一些情形中,如本文所公开的异源细胞因子(例如,异源il)可以结合至工程化的免疫细胞(例如,工程化的nk细胞)的细胞表面。在一些例子中,工程化的免疫细胞可以被遗传修饰,使得编码异源细胞因子的异源多核苷酸序列与编码工程化的免疫细胞的内源跨膜蛋白的基因偶联。在一个例子中,内源跨膜蛋白可以是异源细胞因子的相应受体(例如,异源il-15的异源il-15α或il-15β)。在一些例子中,编码包含与(ii)异源受体偶联的(i)异源细胞因子的异源融合多肽的表达盒可以被引入工程化的免疫细胞。此处,异源细胞因子可以不是并且无需是可从异源受体切割的。异源受体的非限制性例子可以包括异源细胞因子的相应受体(例如,异源il-15的异源il-15α或il-15β),或者不同受体,如共有γ链(γc)受体或其修饰。
[0100]
如本文所公开的表达盒可以通过如本文所公开的基因编辑部分的作用被整合至工程化的细胞(例如,工程化的nk细胞)的基因组中。可替代地,表达盒可以不被整合至并且无需被整合至工程化的细胞的基因组中。
[0101]
如本文所公开的工程化的免疫细胞(例如,工程化的nk细胞)可以展现内源信号传导途径的增强的信号传导,其涉及如本文所公开的异源细胞因子(例如,异源il,如异源il-15)和/或异源受体(例如,异源il受体,如异源il-15r)。如本文所公开的内源信号传导途径的增强的信号传导可以通过多种方法来查明,所述方法包括但不限于:(i)下游信号传导蛋白(例如,用于il-15/il-15r的jak3、stat3、stat5等)的磷酸化,或者(ii)通过蛋白质印迹
或聚合酶链式反应(pcr)技术确定的下游基因(例如,用于il-15/il-15r的mcl1、cdk4/6、mki67、tnf、gzmb、gzmc、ifng等)的表达。
[0102]
在一些情形中,本公开文本的工程化的免疫细胞中由异源细胞因子和/或异源受体诱导(例如,由如本文所公开的异源细胞因子和/或异源受体如il-15/il-15r诱导)的内源信号传导途径的增强的信号传导的特征可以是如与对照细胞相比,下游信号传导蛋白的磷酸化增加至少或多达约0.1倍、至少或多达约0.2倍、至少或多达约0.3倍、至少或多达约0.4倍、至少或多达约0.5倍、至少或多达约0.6倍、至少或多达约0.7倍、至少或多达约0.8倍、至少或多达约0.9倍、至少或多达约1倍、至少或多达约2倍、至少或多达约3倍、至少或多达约4倍、至少或多达约5倍、至少或多达约6倍、至少或多达约7倍、至少或多达约8倍、至少或多达约9倍、至少或多达约10倍、至少或多达约20倍、至少或多达约30倍、至少或多达约40倍、至少或多达约50倍、至少或多达约60倍、至少或多达约70倍、至少或多达约80倍、至少或多达约90倍、至少或多达约100倍、至少或多达约500倍、至少或多达约1,000倍、至少或多达约5,000倍或者至少或多达约10,000倍。
[0103]
在一些情形中,本公开文本的工程化的免疫细胞中由异源细胞因子和/或异源受体诱导(例如,由如本文所公开的异源细胞因子和/或异源受体如il-15/il-15r诱导)的内源信号传导途径的增强的信号传导的特征可以是如与对照细胞相比,下游基因的表达增加至少或多达约0.1倍、至少或多达约0.2倍、至少或多达约0.3倍、至少或多达约0.4倍、至少或多达约0.5倍、至少或多达约0.6倍、至少或多达约0.7倍、至少或多达约0.8倍、至少或多达约0.9倍、至少或多达约1倍、至少或多达约2倍、至少或多达约3倍、至少或多达约4倍、至少或多达约5倍、至少或多达约6倍、至少或多达约7倍、至少或多达约8倍、至少或多达约9倍、至少或多达约10倍、至少或多达约20倍、至少或多达约30倍、至少或多达约40倍、至少或多达约50倍、至少或多达约60倍、至少或多达约70倍、至少或多达约80倍、至少或多达约90倍、至少或多达约100倍、至少或多达约500倍、至少或多达约1,000倍、至少或多达约5,000倍或者至少或多达约10,000倍。
[0104]
如本文所公开的工程化的免疫细胞(例如,工程化的nk细胞)的增强的cd16信号传导(例如,cd16的组成型激活的信号传导)可以通过在受试细胞中具有不可切割cd16变体来实现。cd16(例如,cd16a)是免疫细胞(例如,nk细胞)表达的跨膜蛋白,其结合附接至靶细胞的单体igg以激活所述免疫细胞并促进抗体依赖性细胞介导的细胞毒性(adcc)。在非工程化的免疫细胞中,cd16与单体igg之间的结合可以诱导cd16蛋白在跨膜结构域附近的切割位点处的切割,以调节cd16在免疫细胞激活后的细胞表面密度。因此,工程化的免疫细胞的内源cd16可以被修饰以增强其信号传导。可替代地,cd16的增强的信号传导变体可以被人工引入工程化的免疫细胞。
[0105]
在一些情形中,工程化的免疫细胞的编码cd16的内源基因可以通过如本文所公开的基因编辑部分的作用在其胞外域中进行遗传修饰(例如,f176v),使得修饰的cd16展现如与天然cd16相比更高的与其靶标(例如,单体igg)的结合亲和力。在一些情形中,编码这样的修饰的cd16的异源基因可以被引入细胞。
[0106]
在一些情形中,工程化的免疫细胞的编码cd16的内源基因可以通过如本文所公开的基因编辑部分的作用进行遗传修饰,使得修饰的cd16是不可切割的并且可以诱导增强的cd16信号传导。在一些例子中,cd16的膜近端区域(位置189-212)中的切割位点(例如,位置
195-198)可以被修饰或消除(例如,作为不可切割的cd16变体的cd16s197p变体)。在一些情形中,编码这样的修饰的cd16的异源基因可以被引入细胞。
[0107]
在一些情形中,编码(i)展现与其靶标(例如,单体igg)的更高的结合亲和力并且(ii)是不可切割的异源cd16变体的异源基因可以被引入细胞(即,hncd16)。在一些例子中,异源cd16变体可以是如本文所公开的修饰的cd16,其包含例如f176v和s197p。在一些例子中,异源cd变体可以是融合受体蛋白,其包含(i)cd16中具有失活的切割位点的至少一部分,以及(ii)不同的细胞表面蛋白如糖蛋白(例如,cd64)的胞外域,其展现如与未修饰的cd16相比增强的与靶标(例如,单体igg)的结合。
[0108]
如本文所公开的异源基因可以通过如本文所公开的基因编辑部分的作用被整合至工程化的细胞(例如,工程化的nk细胞)的基因组中。可替代地,异源基因可以不被整合至并且无需被整合至工程化的细胞的基因组中。
[0109]
如本文所公开的工程化的免疫细胞(例如,工程化的nk细胞)的增强的cd16信号传导可以通过多种方法来查明,所述方法包括但不限于(i)通过蛋白质印迹确定的下游信号传导蛋白(例如,shp-1)的磷酸化,或者(ii)通过蛋白质印迹或pcr技术确定的下游基因(例如,cd25、ifn-γ、tnf等)的表达。
[0110]
在一些情形中,本公开文本的工程化的免疫细胞(例如,包含hncd16的工程化的nk细胞)的cd16信号传导可以比对照细胞的cd16信号传导大至少或多达约0.1倍、至少或多达约0.2倍、至少或多达约0.3倍、至少或多达约0.4倍、至少或多达约0.5倍、至少或多达约0.6倍、至少或多达约0.7倍、至少或多达约0.8倍、至少或多达约0.9倍、至少或多达约1倍、至少或多达约2倍、至少或多达约4倍、至少或多达约4倍、至少或多达约5倍、至少或多达约6倍、至少或多达约7倍、至少或多达约8倍、至少或多达约9倍、至少或多达约10倍、至少或多达约20倍、至少或多达约30倍、至少或多达约40倍、至少或多达约50倍、至少或多达约60倍、至少或多达约70倍、至少或多达约80倍、至少或多达约90倍、至少或多达约100倍、至少或多达约500倍、至少或多达约1,000倍、至少或多达约5,000倍或者至少或多达约10,000倍。
[0111]
在一些情形中,本公开文本的工程化的免疫细胞(例如,包含hncd16的工程化的nk细胞)的增强的cd16信号传导的特征可以是如与对照细胞相比,下游信号传导蛋白的磷酸化增加至少或多达约0.1倍、至少或多达约0.2倍、至少或多达约0.3倍、至少或多达约0.4倍、至少或多达约0.5倍、至少或多达约0.6倍、至少或多达约0.7倍、至少或多达约0.8倍、至少或多达约0.9倍、至少或多达约1倍、至少或多达约2倍、至少或多达约3倍、至少或多达约4倍、至少或多达约5倍、至少或多达约6倍、至少或多达约7倍、至少或多达约8倍、至少或多达约9倍、至少或多达约10倍、至少或多达约20倍、至少或多达约30倍、至少或多达约40倍、至少或多达约50倍、至少或多达约60倍、至少或多达约70倍、至少或多达约80倍、至少或多达约90倍、至少或多达约100倍、至少或多达约500倍、至少或多达约1,000倍、至少或多达约5,000倍或者至少或多达约10,000倍。
[0112]
在一些情形中,本公开文本的工程化的免疫细胞(例如,包含hncd16的工程化的nk细胞)的增强的cd16信号传导的特征可以是如与对照细胞相比,下游基因的表达增加至少或多达约0.1倍、至少或多达约0.2倍、至少或多达约0.3倍、至少或多达约0.4倍、至少或多达约0.5倍、至少或多达约0.6倍、至少或多达约0.7倍、至少或多达约0.8倍、至少或多达约0.9倍、至少或多达约1倍、至少或多达约2倍、至少或多达约3倍、至少或多达约4倍、至少或
多达约5倍、至少或多达约6倍、至少或多达约7倍、至少或多达约8倍、至少或多达约9倍、至少或多达约10倍、至少或多达约20倍、至少或多达约30倍、至少或多达约40倍、至少或多达约50倍、至少或多达约60倍、至少或多达约70倍、至少或多达约80倍、至少或多达约90倍、至少或多达约100倍、至少或多达约500倍、至少或多达约1,000倍、至少或多达约5,000倍或者至少或多达约10,000倍。
[0113]
在一些情形中,本公开文本的工程化的免疫细胞(例如,包含hncd16的工程化的nk细胞)的cd16信号传导可以比对照细胞的cd16信号传导更延长(例如,激活的cd16信号传导的更长持续时间)至少或多达约0.1倍、至少或多达约0.2倍、至少或多达约0.3倍、至少或多达约0.4倍、至少或多达约0.5倍、至少或多达约0.6倍、至少或多达约0.7倍、至少或多达约0.8倍、至少或多达约0.9倍、至少或多达约1倍、至少或多达约2倍、至少或多达约3倍、至少或多达约4倍、至少或多达约5倍、至少或多达约6倍、至少或多达约7倍、至少或多达约8倍、至少或多达约9倍、至少或多达约10倍、至少或多达约20倍、至少或多达约30倍、至少或多达约40倍、至少或多达约50倍、至少或多达约60倍、至少或多达约70倍、至少或多达约80倍、至少或多达约90倍、至少或多达约100倍、至少或多达约500倍、至少或多达约1,000倍、至少或多达约5,000倍或者至少或多达约10,000倍。
[0114]
在一方面,本公开文本提供一种工程化的免疫细胞(例如,工程化的nk细胞)。工程化的免疫细胞可以包含如本文所公开的异源细胞因子,其中所述异源细胞因子结合至工程化的免疫细胞的膜(例如,质膜)。在一些情形中,异源细胞因子可以包括如本文所公开的异源il(例如,异源il-15)。工程化的免疫细胞还可以包含以下中的一种、两种或全部:(a)不同的异源细胞因子(例如,如本文所公开的异源细胞因子,除了结合至受试细胞的膜的异源细胞因子以外),(b)内源免疫调节多肽的降低的表达或活性,以及(c)安全开关。在一些例子中,内源免疫调节多肽并非b2m。因此,内源免疫调节剂可以是例如除了b2m以外的多肽。
[0115]
工程化的免疫细胞(例如,工程化的nk细胞)可以包含不同的异源细胞因子以及以下中的一种或两种:(b)内源免疫调节多肽(例如,非b2m多肽)的降低的表达或活性,和(c)安全开关。工程化的免疫细胞包含内源免疫调节多肽(例如,非b2m多肽)的降低的表达或活性以及以下中的一种或两种:(a)不同的异源细胞因子,和(c)安全开关。工程化的免疫细胞包含安全开关以及以下中的一种或两种:(a)不同的异源细胞因子,和(b)内源免疫调节多肽(例如,非b2m多肽)的降低的表达或活性。工程化的免疫细胞包含(a)、(b)和(c)的全部。
[0116]
如与对照细胞相比,工程化的免疫细胞(例如,工程化的nk细胞)可以展现内源信号传导途径的增强的信号传导,其涉及异源细胞因子,如本文所公开。
[0117]
内源免疫调节多肽的表达或活性可以在工程化的免疫细胞(例如,工程化的nk细胞)中降低,例如,通过如本文所公开的基因编辑部分的作用。
[0118]
如本文所公开的工程化的免疫细胞(例如,工程化的nk细胞)中内源免疫调节多肽的降低的表达或活性可以通过多种方法来查明,所述方法包括但不限于(i)下游信号传导蛋白(例如,用于pd1/pdl1信号传导的shp2、igα/β、syk等)的磷酸化或去磷酸化,或者(ii)通过蛋白质印迹或pcr技术确定的内源免疫调节多肽(例如,pd1)的表达。
[0119]
在一些情形中,如本文所公开的工程化的免疫细胞(例如,工程化的nk细胞)中内源免疫调节多肽的降低的表达的特征可以是如与对照细胞相比,内源免疫调节多肽(例如,pd1)的表达减少至少或多达约0.1倍、至少或多达约0.2倍、至少或多达约0.3倍、至少或多
达约0.4倍、至少或多达约0.5倍、至少或多达约0.6倍、至少或多达约0.7倍、至少或多达约0.8倍、至少或多达约0.9倍、至少或多达约1倍、至少或多达约2倍、至少或多达约3倍、至少或多达约4倍、至少或多达约5倍、至少或多达约6倍、至少或多达约7倍、至少或多达约8倍、至少或多达约9倍、至少或多达约10倍、至少或多达约20倍、至少或多达约30倍、至少或多达约40倍、至少或多达约50倍、至少或多达约60倍、至少或多达约70倍、至少或多达约80倍、至少或多达约90倍、至少或多达约100倍、至少或多达约500倍、至少或多达约1,000倍、至少或多达约5,000倍或者至少或多达约10,000倍。
[0120]
在一些情形中,如本文所公开的工程化的免疫细胞(例如,工程化的nk细胞)中内源免疫调节多肽的降低的活性的特征可以是如与对照细胞相比,下游信号传导蛋白(例如,用于pd1/pdl1信号传导的shp2)的磷酸化减少至少或多达约0.1倍、至少或多达约0.2倍、至少或多达约0.3倍、至少或多达约0.4倍、至少或多达约0.5倍、至少或多达约0.6倍、至少或多达约0.7倍、至少或多达约0.8倍、至少或多达约0.9倍、至少或多达约1倍、至少或多达约2倍、至少或多达约3倍、至少或多达约4倍、至少或多达约5倍、至少或多达约6倍、至少或多达约7倍、至少或多达约8倍、至少或多达约9倍、至少或多达约10倍、至少或多达约20倍、至少或多达约30倍、至少或多达约40倍、至少或多达约50倍、至少或多达约60倍、至少或多达约70倍、至少或多达约80倍、至少或多达约90倍、至少或多达约100倍、至少或多达约500倍、至少或多达约1,000倍、至少或多达约5,000倍或者至少或多达约10,000倍。
[0121]
在一些情形中,如本文所公开的工程化的免疫细胞(例如,工程化的nk细胞)中内源免疫调节多肽的降低的活性的特征可以是如与对照细胞相比,下游靶信号传导蛋白(例如,用于pd1/pdl1信号传导的igα/β或syk)的磷酸化增加至少或多达约0.1倍、至少或多达约0.2倍、至少或多达约0.3倍、至少或多达约0.4倍、至少或多达约0.5倍、至少或多达约0.6倍、至少或多达约0.7倍、至少或多达约0.8倍、至少或多达约0.9倍、至少或多达约1倍、至少或多达约2倍、至少或多达约3倍、至少或多达约4倍、至少或多达约5倍、至少或多达约6倍、至少或多达约7倍、至少或多达约8倍、至少或多达约9倍、至少或多达约10倍、至少或多达约20倍、至少或多达约30倍、至少或多达约40倍、至少或多达约50倍、至少或多达约60倍、至少或多达约70倍、至少或多达约80倍、至少或多达约90倍、至少或多达约100倍、至少或多达约500倍、至少或多达约1,000倍、至少或多达约5,000倍或者至少或多达约10,000倍。下游靶信号传导蛋白可以是通常被内源免疫调节多肽的功能信号传导途径的作用抑制的蛋白质。
[0122]
在一方面,本公开文本提供一种工程化的免疫细胞(例如,工程化的nk细胞)。工程化的免疫细胞可以包含如本文所公开的cd16变体用于工程化的nk细胞中的增强的cd16信号传导。在一些情形中,cd16变体(例如,异源cd16变体)可以包含cd16的至少一部分和cd64的至少一部分(例如,如本文所公开的hncd16)。如与对照细胞相比,工程化的免疫细胞还可以包含内源免疫调节多肽的降低的表达或活性,如本文所公开。
[0123]
如与对照细胞相比,工程化的免疫细胞(例如,工程化的nk细胞)可以展现增强的cd16信号传导,如本文所公开。
[0124]
在一方面,本公开文本提供一种工程化的免疫细胞(例如,工程化的nk细胞)。工程化的免疫细胞可以包含内源细胞因子信号传导(例如,内源il信号传导,如内源il-17信号传导)的降低的活性。工程化的免疫细胞可以源自分离的干细胞(例如,分离的esc)。可替代地,工程化的免疫细胞可以源自诱导干细胞(例如,ipsc)。
[0125]
在一些情形中,工程化的nk细胞可以用内源细胞因子信号传导的抑制剂(例如,小分子抑制剂)来处理。在一些情形中,工程化的nk细胞可以包含内源il-17或其内源受体的降低的表达(例如,通过插入缺失或转基因突变,通过瞬时或持久抑制等)。在一些情形中,工程化的nk细胞可以包含内源il-17的降低的表达。在一些情形中,工程化的nk细胞可以包含内源il-17r的降低的表达。在一些情形中,工程化的nk细胞可以包含内源il-17和内源il-17r的降低的表达。
[0126]
在一些情形中,如本文所公开的内源细胞因子可以是内源il。如本文所公开的内源il可以包括至少1、2、3、4、5或更多种不同类型的内源il。如本文所公开的内源il可以包括至多5、4、3或2种不同类型的内源il。可替代地,内源il可以是单一类型的内源il。内源il的非限制性例子可以包括但不限于il-1、il-2、il-3、il-4、il-5、il-6、il-7、il-8、il-9、il-10、il-11、il-12、il-13、il-14、il-15、il-16、il-17、il-18、il-19、il-20、il-21、il-22、il-23、il-24、il-25、il-26、il-27、il-28、il-29、il-30、il-31、il-32、il-33、il-34、il-35和il-36。在一些例子中,内源il可以是il-17。内源il-17的非限制性例子可以包括il-17a、il-17f及其天然突变。例如,如本文所公开的工程化的免疫细胞(例如,工程化的nk细胞)可以展现il-17a或il-17f的降低的表达或活性。
[0127]
在一些情形中,如本文所公开的编码内源细胞因子(例如,内源il,如il-17)的内源基因可以通过如本文所公开的基因编辑部分的作用进行修饰。
[0128]
内源受体可以是如本文所公开的任何细胞因子的相应受体(例如,如本文所公开的任何il的相应受体)。在一些情形中,内源受体可以是il的相应受体(例如,用于il-7信号传导的il-17r)。il-17r的非限制性例子可以包括il-17ra、il-17rb、il-17rc、il-17rd、il-17re及其变体。在一个例子中,内源il-17r包含il-17ra。
[0129]
在一些情形中,如本文所公开的内源细胞因子(例如,内源il,如il-17)或其内源受体的降低的表达或活性可以通过多种方法来查明,所述方法包括但不限于(i)下游信号传导蛋白(例如,用于il-17的pi3k、act1、map3k、mek1/2、mkk3/6、mkk4/7、mkk3/6、erk、p38、jnk等)的磷酸化,或者(ii)通过蛋白质印迹或pct技术确定的下游基因的表达。在一些例子中,il细胞因子如il-17的下游基因可以包括趋化因子(例如,cxcl1、cxcl2、cxcl8、cxcl9、cxcl10、ccl2、ccl20等)、细胞因子(例如,il-6、tnfa、g-csf、gm-csf等)、急性期应答分子(例如,saa、crp、脂质运载蛋白2/24p3等)和/或酶(例如,金属蛋白酶,如mmp1、mmp3、mmp9、mmp13)。
[0130]
在一些情形中,如本文所公开的工程化的免疫细胞(例如,工程化的nk细胞)中内源细胞因子(例如,内源il,如il-17)或其内源受体的降低的表达或活性的特征可以是如与对照细胞相比,内源细胞因子的下游信号传导蛋白的磷酸化减少至少或多达约0.1倍、至少或多达约0.2倍、至少或多达约0.3倍、至少或多达约0.4倍、至少或多达约0.5倍、至少或多达约0.6倍、至少或多达约0.7倍、至少或多达约0.8倍、至少或多达约0.9倍、至少或多达约1倍、至少或多达约2倍、至少或多达约3倍、至少或多达约4倍、至少或多达约5倍、至少或多达约6倍、至少或多达约7倍、至少或多达约8倍、至少或多达约9倍、至少或多达约10倍、至少或多达约20倍、至少或多达约30倍、至少或多达约40倍、至少或多达约50倍、至少或多达约60倍、至少或多达约70倍、至少或多达约80倍、至少或多达约90倍、至少或多达约100倍、至少或多达约500倍、至少或多达约1,000倍、至少或多达约5,000倍或者至少或多达约10,000
倍。
[0131]
在一些情形中,如本文所公开的工程化的免疫细胞(例如,工程化的nk细胞)中内源细胞因子(例如,内源il,如il-17)或其内源受体的降低的表达或活性的特征可以是如与对照细胞相比,内源细胞因子的下游基因的表达减少至少或多达约0.1倍、至少或多达约0.2倍、至少或多达约0.3倍、至少或多达约0.4倍、至少或多达约0.5倍、至少或多达约0.6倍、至少或多达约0.7倍、至少或多达约0.8倍、至少或多达约0.9倍、至少或多达约1倍、至少或多达约2倍、至少或多达约3倍、至少或多达约4倍、至少或多达约5倍、至少或多达约6倍、至少或多达约7倍、至少或多达约8倍、至少或多达约9倍、至少或多达约10倍、至少或多达约20倍、至少或多达约30倍、至少或多达约40倍、至少或多达约50倍、至少或多达约60倍、至少或多达约70倍、至少或多达约80倍、至少或多达约90倍、至少或多达约100倍、至少或多达约500倍、至少或多达约1,000倍、至少或多达约5,000倍或者至少或多达约10,000倍。
[0132]
在一些情形中,如与不展现如本文所公开的内源细胞因子信号传导(例如,内源il信号传导,如内源il-17信号传导)的降低的活性的对照细胞相比,如本文所公开的工程化的免疫细胞(例如,工程化的nk细胞)可以展现用于定型的免疫细胞的特定细胞标记(例如,nk细胞标记)的增强的表达谱。例如,用于定型的nk细胞的特定细胞标记的非限制性例子可以包括cd57或杀伤免疫球蛋白样受体(kir)。kir可以包含kir2d和/或kir3d。kir2d可以包含kir2dl1、kir2dl2、kir2dl3、kir2dl4、kir2dl5a、kir2dl5b、kir2ds1、kir2ds2、kir2ds3、kir2ds4和/或kir2ds5。kir3d可以包含kir3dl1、kir3dl2、kir3dl3和/或kir3ds1。
[0133]
用于如本文所公开的定型的免疫细胞的特定细胞标记(例如,用于nk细胞的cd57或kir)的增强的表达谱可以通过多种方法来查明,所述方法包括但不限于蛋白质印迹或pcr技术。
[0134]
在一些情形中,本公开文本的工程化的免疫细胞中用于定型的免疫细胞的特定细胞标记(例如,用于nk细胞的cd57或kir)的表达可以比对照细胞中所述特定细胞标记的表达大至少或多达约0.1倍、至少或多达约0.2倍、至少或多达约0.3倍、至少或多达约0.4倍、至少或多达约0.5倍、至少或多达约0.6倍、至少或多达约0.7倍、至少或多达约0.8倍、至少或多达约0.9倍、至少或多达约1倍、至少或多达约2倍、至少或多达约4倍、至少或多达约4倍、至少或多达约5倍、至少或多达约6倍、至少或多达约7倍、至少或多达约8倍、至少或多达约9倍、至少或多达约10倍、至少或多达约20倍、至少或多达约30倍、至少或多达约40倍、至少或多达约50倍、至少或多达约60倍、至少或多达约70倍、至少或多达约80倍、至少或多达约90倍、至少或多达约100倍、至少或多达约500倍、至少或多达约1,000倍、至少或多达约5,000倍或者至少或多达约10,000倍。
[0135]
在一方面,本公开文本提供一种工程化的免疫细胞(例如,工程化的nk细胞)。工程化的免疫细胞可以包含以下中的一种或两种:(i)异源转录因子(例如,异源stat),(ii)内源细胞因子信号传导(例如,如本文所公开的内源il信号传导)的降低的活性,以及(iii)内源酶(例如,连接酶,如cbl-b)的降低的表达或活性。工程化的免疫细胞可以源自分离的干细胞(例如,分离的esc)。可替代地,工程化的免疫细胞可以源自诱导干细胞(例如,ipsc)。
[0136]
异源转录因子可以包含至少1、2、3、4、5或更多种不同类型的异源转录因子。异源转录因子可以包含至多5、4、3或2种不同类型的转录因子。可替代地,异源转录因子可以具有单一类型的转录因子。转录因子可以参与工程化的免疫细胞的免疫活性、增殖、细胞凋亡
和/或分化。在一些情形中,用于工程化的免疫细胞(例如,工程化的nk细胞)的异源转录因子可以是stat。stat的非限制性例子可以包括stat1、stat2、stat3、stat4、stat3、stat4、stat5a、stat5b、stat6及其修饰。在一个例子中,stat可以包含stat3。在另一例子中,stat可以包含stat5b。
[0137]
在一些情形中,如与没有(i)异源转录因子(例如,异源stat)或(ii)内源细胞因子信号传导(例如,内源il-17信号传导)的降低的活性的对照细胞相比,在肿瘤细胞的存在下,如本文所公开的工程化的免疫细胞(例如,工程化的nk细胞)可以展现增强的存活。在一些情形中,在肿瘤细胞的存在下,工程化的免疫细胞可以存活比对照细胞长至少或多达约0.1倍、至少或多达约0.2倍、至少或多达约0.3倍、至少或多达约0.4倍、至少或多达约0.5倍、至少或多达约0.6倍、至少或多达约0.7倍、至少或多达约0.8倍、至少或多达约0.9倍、至少或多达约1倍、至少或多达约2倍、至少或多达约3倍、至少或多达约4倍、至少或多达约5倍、至少或多达约6倍、至少或多达约7倍、至少或多达约8倍、至少或多达约9倍、至少或多达约10倍、至少或多达约20倍、至少或多达约30倍、至少或多达约40倍、至少或多达约50倍、至少或多达约60倍、至少或多达约70倍、至少或多达约80倍、至少或多达约90倍、至少或多达约100倍、至少或多达约500倍、至少或多达约1,000倍、至少或多达约5,000倍或者至少或多达约10,000倍。
[0138]
在一方面,本公开文本提供一种工程化的免疫细胞(例如,工程化的nk细胞)。如与对照细胞相比,工程化的免疫细胞可以展现用于如本文所公开的定型的免疫细胞的特定内源细胞标记(例如,nk细胞标记,如kir)的降低的表达或活性。在一些例子中,特定内源细胞标记是kir。工程化的免疫细胞还可以包含以下中的一种或多种:(a)包含能够与抗原结合的抗原结合部分的嵌合多肽受体,如本文所公开,(b)异源细胞因子(例如,异源il,如il-15),如本文所公开,(c)用于如与对照细胞相比增强的cd16信号传导的cd16变体,其中所述cd16变体对于工程化的nk细胞是异源的,如本文所公开,(d)如本文所公开的免疫调节多肽,其中所述免疫调节多肽对于工程化的免疫细胞是异源的,以及(e)内源免疫调节多肽的降低的表达或活性,如本文所公开。
[0139]
工程化的免疫细胞可以包含嵌合多肽受体以及以下中的一种或多种(例如,以下中的1、2、3或4种):(b)异源细胞因子,(c)用于增强的cd16信号传导的cd16变体,(d)异源免疫调节剂,以及(e)内源免疫调节多肽的降低的表达或活性。
[0140]
工程化的免疫细胞可以包含异源细胞因子以及以下中的一种或多种(例如,以下中的1、2、3或4种):(a)嵌合多肽受体,(c)用于增强的cd16信号传导的cd16变体,(d)异源免疫调节剂,以及(e)内源免疫调节多肽的降低的表达或活性。
[0141]
工程化的免疫细胞可以包含用于增强的cd16信号传导的cd16变体以及以下中的一种或多种(例如,以下中的1、2、3或4种):(a)嵌合多肽受体,(b)异源细胞因子,(d)异源免疫调节剂,以及(e)内源免疫调节多肽的降低的表达或活性。
[0142]
工程化的免疫细胞可以包含异源免疫调节剂以及以下中的一种或多种(例如,以下中的1、2、3或4种):(a)嵌合多肽受体,(b)异源细胞因子,(c)用于增强的cd16信号传导的cd16变体,以及(e)内源免疫调节多肽的降低的表达或活性。
[0143]
工程化的免疫细胞可以包含内源免疫调节多肽的降低的表达或活性以及以下中的一种或多种(例如,以下中的1、2、3或4种):(a)嵌合多肽受体,(b)异源细胞因子,(c)用于
增强的cd16信号传导的cd16变体,以及(d)异源免疫调节剂。
[0144]
用于如本文所公开的定型的免疫细胞的特定内源细胞标记(例如,用于nk细胞的kir)的降低的表达或活性可以通过多种方法来查明,所述方法包括但不限于蛋白质印迹或pcr技术。
[0145]
在一些情形中,本公开文本的工程化的免疫细胞中用于定型的免疫细胞的特定内源细胞标记(例如,用于nk细胞的kir)的表达可以比对照细胞中所述特定内源细胞标记的表达小至少或多达约0.1倍、至少或多达约0.2倍、至少或多达约0.3倍、至少或多达约0.4倍、至少或多达约0.5倍、至少或多达约0.6倍、至少或多达约0.7倍、至少或多达约0.8倍、至少或多达约0.9倍、至少或多达约1倍、至少或多达约2倍、至少或多达约4倍、至少或多达约4倍、至少或多达约5倍、至少或多达约6倍、至少或多达约7倍、至少或多达约8倍、至少或多达约9倍、至少或多达约10倍、至少或多达约20倍、至少或多达约30倍、至少或多达约40倍、至少或多达约50倍、至少或多达约60倍、至少或多达约70倍、至少或多达约80倍、至少或多达约90倍、至少或多达约100倍、至少或多达约500倍、至少或多达约1,000倍、至少或多达约5,000倍或者至少或多达约10,000倍。
[0146]
在一方面,本公开文本提供一种工程化的免疫细胞(例如,工程化的nk细胞)。工程化的免疫细胞可以展现一种或多种(例如,1、2、3、4、5或更多种)内源免疫检查点抑制剂(例如,cd94、cd96、tgfβ受体、ship2等)的降低的表达或活性。在一些情形中,工程化的免疫细胞可以展现以下中的一种或多种(例如,1、2、3、4、5或更多种)的降低的表达或活性:(i)内源cd94,(ii)内源cd96,(iii)内源tgfβ受体,以及(iv)内源ship(例如,ship2)。
[0147]
在一些情形中,工程化的免疫细胞可以展现内源cd94的降低的表达或活性以及以下中的一种或多种(例如,以下中的1、2或全部)的降低的表达或活性:(ii)内源cd96,(iii)内源tgfβ受体,以及(iv)内源ship(例如,ship2)。
[0148]
在一些情形中,工程化的免疫细胞可以展现内源cd96的降低的表达或活性以及以下中的一种或多种(例如,以下中的1、2或全部)的降低的表达或活性:(i)内源cd94,(iii)内源tgfβ受体,以及(iv)内源ship(例如,ship2)。
[0149]
在一些情形中,工程化的免疫细胞可以展现内源tgfβ受体的降低的表达或活性以及以下中的一种或多种(例如,以下中的1、2或全部)的降低的表达或活性:(i)内源cd94,(ii)内源cd96,以及(iv)内源ship(例如,ship2)。
[0150]
在一些情形中,工程化的免疫细胞可以展现内源ship(例如,ship2)的降低的表达或活性以及以下中的一种或多种(例如,以下中的1、2或全部)的降低的表达或活性:(i)内源cd94,(ii)内源cd96,以及(iii)内源tgfβ受体。
[0151]
在一些情形中,本公开文本的工程化的免疫细胞(例如,工程化的nk细胞)中免疫检查点抑制剂(例如,cd94、cd96、tgfβ受体、ship2等)的降低的表达或活性可以比对照细胞中所述免疫检查点抑制剂的表达小至少或多达约0.1倍、至少或多达约0.2倍、至少或多达约0.3倍、至少或多达约0.4倍、至少或多达约0.5倍、至少或多达约0.6倍、至少或多达约0.7倍、至少或多达约0.8倍、至少或多达约0.9倍、至少或多达约1倍、至少或多达约2倍、至少或多达约4倍、至少或多达约4倍、至少或多达约5倍、至少或多达约6倍、至少或多达约7倍、至少或多达约8倍、至少或多达约9倍、至少或多达约10倍、至少或多达约20倍、至少或多达约30倍、至少或多达约40倍、至少或多达约50倍、至少或多达约60倍、至少或多达约70倍、至少
或多达约80倍、至少或多达约90倍、至少或多达约100倍、至少或多达约500倍、至少或多达约1,000倍、至少或多达约5,000倍或者至少或多达约10,000倍。
[0152]
在一些情形中,本公开文本的工程化的免疫细胞(例如,工程化的nk细胞)中内源cd94的降低的表达或活性可以比对照细胞中所述内源cd94的表达小至少或多达约0.1倍、至少或多达约0.2倍、至少或多达约0.3倍、至少或多达约0.4倍、至少或多达约0.5倍、至少或多达约0.6倍、至少或多达约0.7倍、至少或多达约0.8倍、至少或多达约0.9倍、至少或多达约1倍、至少或多达约2倍、至少或多达约4倍、至少或多达约4倍、至少或多达约5倍、至少或多达约6倍、至少或多达约7倍、至少或多达约8倍、至少或多达约9倍、至少或多达约10倍、至少或多达约20倍、至少或多达约30倍、至少或多达约40倍、至少或多达约50倍、至少或多达约60倍、至少或多达约70倍、至少或多达约80倍、至少或多达约90倍、至少或多达约100倍、至少或多达约500倍、至少或多达约1,000倍、至少或多达约5,000倍或者至少或多达约10,000倍。
[0153]
在一些情形中,本公开文本的工程化的免疫细胞(例如,工程化的nk细胞)中内源cd96的降低的表达或活性可以比对照细胞中所述内源cd96的表达小至少或多达约0.1倍、至少或多达约0.2倍、至少或多达约0.3倍、至少或多达约0.4倍、至少或多达约0.5倍、至少或多达约0.6倍、至少或多达约0.7倍、至少或多达约0.8倍、至少或多达约0.9倍、至少或多达约1倍、至少或多达约2倍、至少或多达约4倍、至少或多达约4倍、至少或多达约5倍、至少或多达约6倍、至少或多达约7倍、至少或多达约8倍、至少或多达约9倍、至少或多达约10倍、至少或多达约20倍、至少或多达约30倍、至少或多达约40倍、至少或多达约50倍、至少或多达约60倍、至少或多达约70倍、至少或多达约80倍、至少或多达约90倍、至少或多达约100倍、至少或多达约500倍、至少或多达约1,000倍、至少或多达约5,000倍或者至少或多达约10,000倍。
[0154]
在一些情形中,本公开文本的工程化的免疫细胞(例如,工程化的nk细胞)中内源tgfβ受体的降低的表达或活性可以比对照细胞中所述内源tgfβ受体的表达小至少或多达约0.1倍、至少或多达约0.2倍、至少或多达约0.3倍、至少或多达约0.4倍、至少或多达约0.5倍、至少或多达约0.6倍、至少或多达约0.7倍、至少或多达约0.8倍、至少或多达约0.9倍、至少或多达约1倍、至少或多达约2倍、至少或多达约4倍、至少或多达约4倍、至少或多达约5倍、至少或多达约6倍、至少或多达约7倍、至少或多达约8倍、至少或多达约9倍、至少或多达约10倍、至少或多达约20倍、至少或多达约30倍、至少或多达约40倍、至少或多达约50倍、至少或多达约60倍、至少或多达约70倍、至少或多达约80倍、至少或多达约90倍、至少或多达约100倍、至少或多达约500倍、至少或多达约1,000倍、至少或多达约5,000倍或者至少或多达约10,000倍。
[0155]
在一些情形中,本公开文本的工程化的免疫细胞(例如,工程化的nk细胞)中内源ship(例如,ship2)的降低的表达或活性可以比对照细胞中所述内源ship的表达小至少或多达约0.1倍、至少或多达约0.2倍、至少或多达约0.3倍、至少或多达约0.4倍、至少或多达约0.5倍、至少或多达约0.6倍、至少或多达约0.7倍、至少或多达约0.8倍、至少或多达约0.9倍、至少或多达约1倍、至少或多达约2倍、至少或多达约4倍、至少或多达约4倍、至少或多达约5倍、至少或多达约6倍、至少或多达约7倍、至少或多达约8倍、至少或多达约9倍、至少或多达约10倍、至少或多达约20倍、至少或多达约30倍、至少或多达约40倍、至少或多达约50
倍、至少或多达约60倍、至少或多达约70倍、至少或多达约80倍、至少或多达约90倍、至少或多达约100倍、至少或多达约500倍、至少或多达约1,000倍、至少或多达约5,000倍或者至少或多达约10,000倍。
[0156]
在一方面,本公开文本提供一种工程化的免疫细胞(例如,工程化的nk细胞)。工程化的免疫细胞可以展现内源免疫调节多肽的降低的表达或活性,如本文所公开。在一些情形中,内源免疫调节多肽包含一种或多种(例如,1、2、3、4、5或更多种)低免疫性调节剂。在一些情形中,工程化的免疫细胞展现来自以下的一种或多种(例如,1、2、3、4、5或更多种)低免疫性调节剂的降低的表达或活性:(i)内源cd80,(ii)内源cd86,(iii)内源icosl,(iv)内源cd40l,(v)内源mica或micb,或者(vi)内源nkg2dl。工程化的免疫细胞可以源自分离的干细胞(例如,分离的esc)。可替代地,工程化的免疫细胞可以源自诱导干细胞(例如,ipsc)。
[0157]
在一些情形中,本公开文本的工程化的免疫细胞(例如,工程化的nk细胞)中内源低免疫性调节剂(例如,cd80、cd86、icosl、cd40l、mica、micb、nkg2dl等)的降低的表达或活性可以比对照细胞中所述内源低免疫性调节剂的表达小至少或多达约0.1倍、至少或多达约0.2倍、至少或多达约0.3倍、至少或多达约0.4倍、至少或多达约0.5倍、至少或多达约0.6倍、至少或多达约0.7倍、至少或多达约0.8倍、至少或多达约0.9倍、至少或多达约1倍、至少或多达约2倍、至少或多达约4倍、至少或多达约4倍、至少或多达约5倍、至少或多达约6倍、至少或多达约7倍、至少或多达约8倍、至少或多达约9倍、至少或多达约10倍、至少或多达约20倍、至少或多达约30倍、至少或多达约40倍、至少或多达约50倍、至少或多达约60倍、至少或多达约70倍、至少或多达约80倍、至少或多达约90倍、至少或多达约100倍、至少或多达约500倍、至少或多达约1,000倍、至少或多达约5,000倍或者至少或多达约10,000倍,如通过蛋白质印迹或pct技术所查明,如本文所公开。
[0158]
在一些情形中,本公开文本的工程化的免疫细胞(例如,工程化的nk细胞)中内源cd80的降低的表达或活性可以比对照细胞中所述内源cd80的表达小至少或多达约0.1倍、至少或多达约0.2倍、至少或多达约0.3倍、至少或多达约0.4倍、至少或多达约0.5倍、至少或多达约0.6倍、至少或多达约0.7倍、至少或多达约0.8倍、至少或多达约0.9倍、至少或多达约1倍、至少或多达约2倍、至少或多达约4倍、至少或多达约4倍、至少或多达约5倍、至少或多达约6倍、至少或多达约7倍、至少或多达约8倍、至少或多达约9倍、至少或多达约10倍、至少或多达约20倍、至少或多达约30倍、至少或多达约40倍、至少或多达约50倍、至少或多达约60倍、至少或多达约70倍、至少或多达约80倍、至少或多达约90倍、至少或多达约100倍、至少或多达约500倍、至少或多达约1,000倍、至少或多达约5,000倍或者至少或多达约10,000倍。
[0159]
在一些情形中,本公开文本的工程化的免疫细胞(例如,工程化的nk细胞)中内源cd86的降低的表达或活性可以比对照细胞中所述内源cd86的表达小至少或多达约0.1倍、至少或多达约0.2倍、至少或多达约0.3倍、至少或多达约0.4倍、至少或多达约0.5倍、至少或多达约0.6倍、至少或多达约0.7倍、至少或多达约0.8倍、至少或多达约0.9倍、至少或多达约1倍、至少或多达约2倍、至少或多达约4倍、至少或多达约4倍、至少或多达约5倍、至少或多达约6倍、至少或多达约7倍、至少或多达约8倍、至少或多达约9倍、至少或多达约10倍、至少或多达约20倍、至少或多达约30倍、至少或多达约40倍、至少或多达约50倍、至少或多达约60倍、至少或多达约70倍、至少或多达约80倍、至少或多达约90倍、至少或多达约100
倍、至少或多达约500倍、至少或多达约1,000倍、至少或多达约5,000倍或者至少或多达约10,000倍。
[0160]
在一些情形中,本公开文本的工程化的免疫细胞(例如,工程化的nk细胞)中内源icosl的降低的表达或活性可以比对照细胞中所述内源icosl的表达小至少或多达约0.1倍、至少或多达约0.2倍、至少或多达约0.3倍、至少或多达约0.4倍、至少或多达约0.5倍、至少或多达约0.6倍、至少或多达约0.7倍、至少或多达约0.8倍、至少或多达约0.9倍、至少或多达约1倍、至少或多达约2倍、至少或多达约4倍、至少或多达约4倍、至少或多达约5倍、至少或多达约6倍、至少或多达约7倍、至少或多达约8倍、至少或多达约9倍、至少或多达约10倍、至少或多达约20倍、至少或多达约30倍、至少或多达约40倍、至少或多达约50倍、至少或多达约60倍、至少或多达约70倍、至少或多达约80倍、至少或多达约90倍、至少或多达约100倍、至少或多达约500倍、至少或多达约1,000倍、至少或多达约5,000倍或者至少或多达约10,000倍。
[0161]
在一些情形中,本公开文本的工程化的免疫细胞(例如,工程化的nk细胞)中内源低免疫性调节剂cd40l的降低的表达或活性可以比对照细胞中所述内源低免疫性调节剂cd40l的表达小至少或多达约0.1倍、至少或多达约0.2倍、至少或多达约0.3倍、至少或多达约0.4倍、至少或多达约0.5倍、至少或多达约0.6倍、至少或多达约0.7倍、至少或多达约0.8倍、至少或多达约0.9倍、至少或多达约1倍、至少或多达约2倍、至少或多达约4倍、至少或多达约4倍、至少或多达约5倍、至少或多达约6倍、至少或多达约7倍、至少或多达约8倍、至少或多达约9倍、至少或多达约10倍、至少或多达约20倍、至少或多达约30倍、至少或多达约40倍、至少或多达约50倍、至少或多达约60倍、至少或多达约70倍、至少或多达约80倍、至少或多达约90倍、至少或多达约100倍、至少或多达约500倍、至少或多达约1,000倍、至少或多达约5,000倍或者至少或多达约10,000倍。
[0162]
在一些情形中,本公开文本的工程化的免疫细胞(例如,工程化的nk细胞)中内源mica或micb的降低的表达或活性可以比对照细胞中所述内源mica或micb的表达小至少或多达约0.1倍、至少或多达约0.2倍、至少或多达约0.3倍、至少或多达约0.4倍、至少或多达约0.5倍、至少或多达约0.6倍、至少或多达约0.7倍、至少或多达约0.8倍、至少或多达约0.9倍、至少或多达约1倍、至少或多达约2倍、至少或多达约4倍、至少或多达约4倍、至少或多达约5倍、至少或多达约6倍、至少或多达约7倍、至少或多达约8倍、至少或多达约9倍、至少或多达约10倍、至少或多达约20倍、至少或多达约30倍、至少或多达约40倍、至少或多达约50倍、至少或多达约60倍、至少或多达约70倍、至少或多达约80倍、至少或多达约90倍、至少或多达约100倍、至少或多达约500倍、至少或多达约1,000倍、至少或多达约5,000倍或者至少或多达约10,000倍。
[0163]
在一些情形中,本公开文本的工程化的免疫细胞(例如,工程化的nk细胞)中内源nkg2dl的降低的表达或活性可以比对照细胞中所述内源nkg2dl的表达小至少或多达约0.1倍、至少或多达约0.2倍、至少或多达约0.3倍、至少或多达约0.4倍、至少或多达约0.5倍、至少或多达约0.6倍、至少或多达约0.7倍、至少或多达约0.8倍、至少或多达约0.9倍、至少或多达约1倍、至少或多达约2倍、至少或多达约4倍、至少或多达约4倍、至少或多达约5倍、至少或多达约6倍、至少或多达约7倍、至少或多达约8倍、至少或多达约9倍、至少或多达约10倍、至少或多达约20倍、至少或多达约30倍、至少或多达约40倍、至少或多达约50倍、至少或
多达约60倍、至少或多达约70倍、至少或多达约80倍、至少或多达约90倍、至少或多达约100倍、至少或多达约500倍、至少或多达约1,000倍、至少或多达约5,000倍或者至少或多达约10,000倍。
[0164]
在一方面,本公开文本提供一种工程化的免疫细胞(例如,工程化的nk细胞)。工程化的免疫细胞可以展现内源免疫调节多肽的降低的表达或活性,如本文所公开。在一些情形中,内源免疫调节多肽包含低免疫性调节剂(例如,icam1)。工程化的免疫细胞还包含以下中的一种或多种:(a)包含能够与抗原结合的抗原结合部分的嵌合多肽受体,如本文所公开,(b)异源细胞因子(例如,异源il,如il-15),如本文所公开,以及(c)用于如与对照细胞相比增强的cd16信号传导的cd16变体。
[0165]
在一些情形中,工程化的免疫细胞(例如,工程化的nk细胞)包含如本文所公开的嵌合多肽受体以及以下中的一种或两种:(b)异源细胞因子(例如,异源il,如il-15),如本文所公开,以及(c)用于增强的cd16信号传导的cd16变体。
[0166]
在一些情形中,工程化的免疫细胞(例如,工程化的nk细胞)包含如本文所公开的异源细胞因子(例如,异源il,如il-15)以及以下中的一种或两种:(a)如本文所公开的嵌合多肽受体,以及(c)用于增强的cd16信号传导的cd16变体。
[0167]
在一些情形中,工程化的免疫细胞(例如,工程化的nk细胞)包含用于增强的cd16信号传导的cd16变体以及以下中的一种或两种:(a)如本文所公开的嵌合多肽受体,以及(b)异源细胞因子(例如,异源il,如il-15),如本文所公开。
[0168]
在一些情形中,本公开文本的工程化的免疫细胞(例如,工程化的nk细胞)中内源icam1的降低的表达或活性可以比对照细胞中所述内源icam1的表达小至少或多达约0.1倍、至少或多达约0.2倍、至少或多达约0.3倍、至少或多达约0.4倍、至少或多达约0.5倍、至少或多达约0.6倍、至少或多达约0.7倍、至少或多达约0.8倍、至少或多达约0.9倍、至少或多达约1倍、至少或多达约2倍、至少或多达约4倍、至少或多达约4倍、至少或多达约5倍、至少或多达约6倍、至少或多达约7倍、至少或多达约8倍、至少或多达约9倍、至少或多达约10倍、至少或多达约20倍、至少或多达约30倍、至少或多达约40倍、至少或多达约50倍、至少或多达约60倍、至少或多达约70倍、至少或多达约80倍、至少或多达约90倍、至少或多达约100倍、至少或多达约500倍、至少或多达约1,000倍、至少或多达约5,000倍或者至少或多达约10,000倍,如通过蛋白质印迹或pct技术所查明,如本文所公开。
[0169]
在一方面,本公开文本提供一种工程化的免疫细胞(例如,工程化的nk细胞)。工程化的免疫细胞可以展现内源免疫调节多肽的降低的表达或活性,如本文所公开。在一些情形中,内源免疫调节多肽包含低免疫性调节剂(例如,icam1)。工程化的免疫细胞可以源自诱导干细胞(例如,ipsc)。
[0170]
在一些情形中,本公开文本的工程化的免疫细胞(例如,工程化的nk细胞)中内源icam1的降低的表达或活性可以低于对照细胞中所述内源icam1的表达,如本文所公开。
[0171]
在一方面,本公开文本提供一种工程化的免疫细胞(例如,工程化的nk细胞)。工程化的免疫细胞可以包含如本文所公开的免疫调节多肽,其中所述免疫调节多肽对于工程化的免疫细胞是异源的。在一些情形中,免疫调节多肽包含低免疫性调节剂。低免疫性调节剂可以是pdl2。可替代地或另外地,低免疫性调节剂可以是tgf-β。
[0172]
在一方面,本公开文本提供一种工程化的免疫细胞(例如,工程化的nk细胞)。工程
化的免疫细胞可以包含如本文所公开的免疫调节多肽,其中所述免疫调节多肽对于工程化的免疫细胞是异源的。在一些情形中,免疫调节多肽包含低免疫性调节剂。低免疫性调节剂可以包含来自以下的一个或多个(例如,1、2、3、4或更多个)成员:(i)异源ccl21,(ii)异源il-10,(iii)异源cd46,(iv)异源cd55,以及(v)异源cd59。工程化的免疫细胞可以源自分离的干细胞(例如,分离的esc)。可替代地,工程化的免疫细胞可以源自诱导干细胞(例如,ipsc)。
[0173]
在一些情形中,如本文所公开的工程化的免疫细胞(例如,工程化的nk细胞)可以包含异源ccl21以及以下中的一种或多种(例如,以下中的1、2、3或全部):(ii)异源il-10,(iii)异源cd46,(iv)异源cd55,以及(v)异源cd59。
[0174]
在一些情形中,如本文所公开的工程化的免疫细胞(例如,工程化的nk细胞)可以包含异源il-10以及以下中的一种或多种(例如,以下中的1、2、3或全部):(i)异源ccl21,(iii)异源cd46,(iv)异源cd55,以及(v)异源cd59。
[0175]
在一些情形中,如本文所公开的工程化的免疫细胞(例如,工程化的nk细胞)可以包含异源cd46以及以下中的一种或多种(例如,以下中的1、2、3或全部):(i)异源ccl21,(ii)异源il-10,(iv)异源cd55,以及(v)异源cd59。
[0176]
在一些情形中,如本文所公开的工程化的免疫细胞(例如,工程化的nk细胞)可以包含异源cd55以及以下中的一种或多种(例如,以下中的1、2、3或全部):(i)异源ccl21,(ii)异源il-10,(iii)异源cd46,以及(v)异源cd59。
[0177]
在一些情形中,如本文所公开的工程化的免疫细胞(例如,工程化的nk细胞)可以包含异源cd59以及以下中的一种或多种(例如,以下中的1、2、3或全部):(i)异源ccl21,(ii)异源il-10,(iii)异源cd46,以及(iv)异源cd55。
[0178]
在一方面,本公开文本提供一种工程化的免疫细胞(例如,工程化的nk细胞)。工程化的免疫细胞可以包含并非il-15的如本文所公开的异源细胞因子(例如,异源il)。在一些例子中,异源细胞因子包括il-21或其变体。工程化的免疫细胞可以源自诱导干细胞(例如,ipsc)。
[0179]
在一些情形中,对照细胞可以是用于比较目的的细胞可以是免疫细胞,如nk细胞。在一些情形中,对照细胞可以是不包含异源细胞因子(例如,il-15)的细胞。在一些情形中,对照细胞可以是不包含用于增强的cd16信号传导的cd16变体的细胞。在一些情形中,对照细胞可以是包含能够与抗原结合的抗原结合部分的嵌合多肽受体的细胞。在一些情形中,对照细胞可以是包含异源il-15r的细胞。在一些情形中,对照细胞可以是不包含膜结合异源细胞因子(例如,il-15)的细胞。在一些情形中,对照细胞可以是不展现内源免疫调节多肽的降低的表达或活性的细胞。在一些情形中,对照细胞可以是不展现内源细胞因子(例如,il-17)或其受体(例如,il-17r)的降低的表达或活性的细胞。在一些情形中,对照细胞可以是不包含异源转录因子(例如,stat)的细胞。在一些情形中,对照细胞可以是不展现用于定型的免疫细胞的特定内源细胞标记(例如,nk细胞标记,如kir)的降低的表达或活性的细胞。在一些情形中,对照细胞可以是不包含异源免疫调节多肽的细胞。在一些情形中,对照细胞可以是不展现以下中的一种或多种(例如,1、2、3或4种)的降低的表达或活性的细胞:内源cd94、内源cd96、内源tgfβ受体或内源ship2。在一些情形中,对照细胞可以是不展现以下中的一种或多种(例如,1、2、3、4或5种)的降低的表达或活性的细胞:内源cd80、内源
cd86、内源icosl、内源cd40l、内源mica或micb或者内源nkg2dl。在一些情形中,对照细胞可以是不展现icam1的降低的表达或活性的细胞。在一些情形中,对照细胞可以是不包含异源pdl2或异源tgfβ的细胞。在一些情形中,对照细胞可以是不包含以下中的一种或多种(例如,1、2、3、4或5种)的细胞:异源ccl21、异源il-10、异源cd46、异源cd55或异源cd59。在一些情形中,对照细胞可以是不包含异源il-21的细胞。在一些情形中,对照细胞可以是并非源自细胞系的细胞。在一些情形中,对照细胞可以是并非源自分离的esc的细胞。在一些情形中,对照细胞可以是并非源自ipsc的细胞。
[0180]
在一些实施方案中,本公开文本提供包含任一种如本文所公开的工程化的免疫细胞的工程化的免疫细胞的群体(例如,包含任一种如本文所公开的工程化的nk细胞的工程化的nk细胞的群体)。免疫细胞的群体(例如,nk细胞的群体)的工程化的免疫细胞(例如,工程化的nk细胞)可以包含异源多肽,其中所述异源多肽包括异源il-15(例如,异源分泌型il-15,和/或膜结合il-15,如il15-il15受体融合物)。工程化的免疫细胞的群体在基本上不含外源白介素(例如,il-2、il-15等)的环境中的活性水平(例如,持久性水平)可以比免疫细胞的可比较群体(例如,工程化以包含如本文所公开的可比较的异源il-15)在包含外源白介素的对照环境中的对照持久性水平高至少约5%、至少约10%、至少约15%、至少约20%、至少约30%、至少约40%、至少约50%、至少约60%、至少约70%、至少约80%、至少约85%、至少约90%、至少约95%、至少约99%、至少约或更多。在免疫细胞的所述群体在所述环境中持续至少或多达约1天、至少或多达约2天、至少或多达约3天、至少或多达约4天、至少或多达约5天、至少或多达约6天、至少或多达约7天、至少或多达约8天、至少或多达约9天、至少或多达约10天、至少或多达约11天、至少或多达约12天、至少或多达约13天、至少或多达约14天、至少或多达约15天、至少或多达约16天、至少或多达约17天、至少或多达约18天、至少或多达约19天、至少或多达约20天、至少或多达约21天、至少或多达约22天、至少或多达约23天、至少或多达约24天、至少或多达约25天、至少或多达约26天、至少或多达约27天、至少或多达约28天、至少或多达约5周、至少或多达约6周或者至少或多达约8周之后,可以查明这样的持久性水平。所述环境中外源白介素(例如,il-2、il-15等)的量可以是至少或多达约1单位/毫升(u/ml)、至少或多达约5u/ml、至少或多达约10u/ml、至少或多达约15u/ml、至少或多达约20u/ml、至少或多达约30u/ml、至少或多达约40u/ml、至少或多达约50u/ml、至少或多达约60u/ml、至少或多达约80u/ml、至少或多达约100u/ml、至少或多达约150u/ml、至少或多达约200u/ml、至少或多达约300u/ml、至少或多达约400u/ml或者至少或多达约500u/ml。所述环境可以是体外的、离体的或体内的。
[0181]
在基本上不含外源白介素(例如,il-2)的环境中持续至少或多达约1天、至少或多达约2天、至少或多达约3天、至少或多达约4天、至少或多达约5天、至少或多达约6天、至少或多达约7天、至少或多达约8天、至少或多达约9天、至少或多达约10天、至少或多达约11天、至少或多达约12天、至少或多达约13天、至少或多达约14天、至少或多达约3周或者至少或多达约4周之后,如本文所公开的工程化的nk细胞的群体可以展现至少或多达约10%、至少或多达约20%、至少或多达约30%、至少或多达约40%、至少或多达约50%、至少或多达约60%、至少或多达约70%、至少或多达约80%、至少或多达约90%、至少或多达约95%或更高持久性(或存活率)。
[0182]
例如,在基本上不含外源白介素(例如,il-2)的环境中至少约5天之后,如本文所
公开的工程化的nk细胞的群体可以展现至少约50%存活(在9天之后50%,在15天之后25%)。例如,在基本上不含外源白介素(例如,il-2)的环境中至少约9天之后,如本文所公开的工程化的nk细胞的群体可以展现至少约50%存活。例如,在基本上不含外源白介素(例如,il-2)的环境中至少约15天之后,如本文所公开的工程化的nk细胞的群体可以展现至少约25%存活。
[0183]
如与缺乏包含异源il-15的异源多肽(例如,缺乏异源膜结合il-15)的nk细胞的可比较群体相比,在基本上不含外源白介素(例如,il-2、il-15等)的环境中持续至少或多达约1天、至少或多达约2天、至少或多达约3天、至少或多达约4天、至少或多达约5天、至少或多达约6天、至少或多达约7天、至少或多达约8天、至少或多达约9天、至少或多达约10天、至少或多达约11天、至少或多达约12天、至少或多达约13天、至少或多达约14天、至少或多达约2周、至少或多达约3周、至少或多达约4周、至少或多达约6周或者至少或多达约8周之后,如本文所公开的工程化的nk细胞的群体可以展现增强至少或多达约0.1倍、至少或多达约0.2倍、至少或多达约0.3倍、至少或多达约0.4倍、至少或多达约0.5倍、至少或多达约0.6倍、至少或多达约0.7倍、至少或多达约0.8倍、至少或多达约0.9倍、至少或多达约1倍、至少或多达约2倍、至少或多达约3倍、至少或多达约4倍、至少或多达约5倍、至少或多达约6倍、至少或多达约7倍、至少或多达约8倍、至少或多达约9倍、至少或多达约10倍、至少或多达约20倍、至少或多达约30倍、至少或多达约40倍、至少或多达约50倍、至少或多达约60倍、至少或多达约70倍、至少或多达约80倍、至少或多达约90倍、至少或多达约100倍、至少或多达约200倍、至少或多达约300倍、至少或多达约400倍或者至少或多达约500倍的持久性。例如,在所述环境中至少约5天之后,如与缺乏异源il-15的nk细胞的可比较群体相比,如本文所公开的工程化的nk细胞的群体可以展现增强至少约7倍的持久性。
[0184]
不希望受理论束缚,通过具有包含增强的il-15信号传导的异源多肽(例如,通过包含含有异源il-15的异源多肽)而具有这样的增强的持久性水平可以减少工程化的免疫细胞的产生所需的外源蛋白(例如,il-2)的量,增强产生工程化的免疫细胞的效率,和/或减小免疫细胞疗法的总成本。在体外查明的任何增强的持久性水平可以转化为体内(例如,在有需要的受试者的血流中)的事件。
[0185]
如本文所公开的外源白介素可以包括并非由细胞或细胞群(例如,一种或多种工程化的免疫细胞,例如如本文所公开的工程化的nk细胞)分泌的白介素,并且可以人工添加至环境。在体外环境中,外源白介素可以包括添加至培养基的重组白介素蛋白。在体内环境中(例如,在血浆中),外源白介素可以包括施用至有需要的受试者的重组白介素蛋白。
[0186]
如本文所用的术语“持久性”通常可以指代在将细胞群体引入环境(例如,在体外培养基中,在静脉内(iv)施用后在血清中等)之后,保留在环境中的细胞群体(例如,工程化的免疫细胞的群体,例如如本文所公开的工程化的nk细胞的群体)的至少一部分的存在。持久性可以通过细胞群体的至少一部分以可检测水平保留在环境中的持续时间来查明。在一些例子中,细胞群体的持久性可能与细胞群体在环境(例如,培养基、血流等)中的半衰期相关联。在一些情形中,目的细胞群体(例如,工程化的免疫细胞的群体,如工程化的nk细胞的群体)可能不随时间而生长(例如,增殖),并且如本文所公开的细胞群体的持久性水平可以通过测量细胞群体的大小随时间的降低(或其速率)来查明。例如,细胞群体在一时间段之后(例如,在至少约5天之后)在环境中的持久性水平高于(例如,高至少5%)在可比较的时
间段之后在可比较的环境中的对照细胞群体可以表明,如与所述对照细胞群体相比,所述细胞群体的大小的更大比例(例如,大至少5%)已经存活。
[0187]
c.工程化的免疫细胞的另外的方面
[0188]
在任一种本文所公开的工程化的免疫细胞(例如,工程化的nk细胞)的一些实施方案中,工程化的免疫细胞可以包含如本文所公开的异源细胞因子(例如,异源il,如il-15)。异源细胞因子可以是异源分泌型细胞因子。异源细胞因子可以是膜结合细胞因子。在一些情形中,工程化的免疫细胞(例如,工程化的nk细胞)包含作为异源细胞因子的相应受体的异源受体(例如,异源il-15r),如本文所公开。在一些情形中,异源细胞因子和相应异源受体可以作为融合蛋白(例如,il15-il15r融合物)来提供。因此,工程化的免疫细胞(例如,工程化的nk细胞)可以展现由异源细胞因子和/或异源受体诱导(例如,由异源细胞因子和/或异源受体如il-15/il-15r诱导)的内源信号传导途径的增强的信号传导,如本文所公开。
[0189]
在任一种本文所公开的工程化的免疫细胞(例如,工程化的nk细胞)的一些实施方案中,如与对照细胞相比,工程化的免疫细胞可以展现内源cd38的降低的表达或活性。这样的工程化的免疫细胞可以用于治疗患有或怀疑患有白细胞癌症如多发性骨髓瘤(mm)的受试者。
[0190]
在任一种本文所公开的工程化的免疫细胞(例如,工程化的nk细胞)的一些实施方案中,工程化的免疫细胞的内源cd38的表达或活性可以不被修饰并且无需修饰。这样的工程化的免疫细胞可以用于治疗患有或怀疑患有并非多发性骨髓瘤的疾病(例如,癌症、肿瘤)的受试者。
[0191]
在任一种本文所公开的工程化的免疫细胞(例如,工程化的nk细胞)的一些实施方案中,工程化的免疫细胞可以包含异源il-15或其片段,并且所述异源il-15或其片段可以由所述工程化的免疫细胞分泌。
[0192]
在任一种本文所公开的工程化的免疫细胞(例如,工程化的nk细胞)的一些实施方案中,工程化的免疫细胞可以包含异源il-15或其片段,并且所述异源il-15或其片段可以结合至所述工程化的免疫细胞的细胞表面膜。
[0193]
在任一种本文所公开的工程化的免疫细胞(例如,工程化的nk细胞)的一些实施方案中,工程化的免疫细胞可以包含含有能够与抗原结合的抗原结合部分的至少一种嵌合多肽受体,如本公开文本中所提供。在一些例子中,工程化的免疫细胞可以包含多种不同嵌合多肽受体以特异性结合多种不同的抗原。在一些例子中,工程化的免疫细胞可以包含含有多个抗原结合部分的至少一种嵌合多肽受体以特异性结合多种不同的抗原。
[0194]
在任一种本文所公开的工程化的免疫细胞(例如,工程化的nk细胞)的一些实施方案中,工程化的免疫细胞可以包含能够实现所述工程化的免疫细胞的死亡的安全开关。工程化的免疫细胞可以通过基因编辑部分的作用包含编码安全开关的基因(例如,整合至免疫细胞的基因组中),如本文所公开。在一些情形中,如果发生不良事件或者在不再需要适应性免疫疗法时,可以将前药引入工程化的免疫细胞(例如,施用至包含工程化的免疫细胞的受试者),并且前药可以由安全开关分子激活以杀伤受试免疫细胞。在一些情形中,安全开关可以包含选自以下的一个或多个成员:胱天蛋白酶(例如,胱天蛋白酶3、7或9)、胸苷激酶、胞嘧啶脱氨酶、修饰的egfr、b细胞cd20及其功能变体。在一些情形中,安全开关可以通过激活物(例如,小分子或蛋白质,如抗体)激活,用于受试工程化免疫细胞的死亡(或耗尽)
的翻译后、时序和/或位点特异性调节。安全开关及其激活物的非限制性例子可以包括胱天蛋白酶9(或胱天蛋白酶3或7)和ap1903;胸苷激酶(tk)和更昔洛韦(gcv);以及胞嘧啶脱氨酶(cd)和5-氟胞嘧啶(5-fc)。可替代地或另外地,含有由抗体(例如,抗egfr ab,如西妥昔单抗)识别的表位的修饰的表皮生长因子受体(egfr)可以用于在受试细胞暴露于抗体时耗尽工程化的免疫细胞。在一些情形中,如本文所公开的工程化的免疫细胞(例如,工程化的nk细胞)可以包含选自以下的安全开关蛋白:胱天蛋白酶9(胱天蛋白酶3或7)、胸苷激酶、胞嘧啶脱氨酶、修饰的egfr和b细胞cd20.3。
[0195]
在任一种本文所公开的工程化的免疫细胞(例如,工程化的nk细胞)的一些实施方案中,工程化的免疫细胞可以包含异源免疫受体多肽。免疫调节多肽可以包括选自以下的一个或多个(例如,1、2、3、4或更多个)成员:hla-e、cd47、cd113、pdl1、pdl2、a2ar、hla-g、tgf-β、ccl21、il10、cd46、cd55和cd59。
[0196]
在任一种本文所公开的工程化的免疫细胞(例如,工程化的nk细胞)的一些实施方案中,工程化的免疫细胞可以展现内源免疫调节多肽的降低的表达或活性,如本文所公开。内源免疫调节多肽包含免疫检查点抑制剂或低免疫性调节剂(或二者)。
[0197]
在一些情形中,如本文所公开的免疫检查点抑制剂可以包括选自以下的一个或多个(例如,1、2、3、4或更多个)成员:pd1、ctla-4、tim-3、kir2d、cd94、nkg2a、nkg2d、tigit、cd96、lag3、tigit、tgfβ受体和2b4。在一些情形中,免疫检查点抑制剂可以包括ship2。
[0198]
在一些情形中,如本文所公开的低免疫性调节剂可以包括选自以下的一个或多个(例如,1、2、3、4或更多个)成员:b2m、ciita、tap1、tap2、tapasin、nlrc5、rfxank、rfx5、rfxap、cd80、cd86、icosl、cd40l、icam1、mica、micb、ulbp1、hla-e、cd47、cd113、pdl1、pdl2、a2ar、hla-g、tgf-β、ccl21、il10、cd46、cd55和cd59。
[0199]
具有任一种如本文所公开的内源免疫调节多肽(例如,免疫检查点抑制剂、低免疫性调节剂)的降低的表达或活性水平可以增强如本文所公开的工程化的免疫细胞(例如,工程化的nk细胞)的一种或多种功能,例如,增强的持久性或存活、增强的针对免疫排斥的抗性(例如,adcc细胞毒性)、增强的针对靶细胞(例如,癌细胞)的细胞毒性等。
[0200]
在任一种本文所公开的工程化的免疫细胞(例如,工程化的nk细胞)的一些实施方案中,工程化的免疫细胞可以包含用于如与对照细胞相比增强的cd16信号传导的cd16变体,其中所述cd16变体对于所述工程化的免疫细胞是异源的。
[0201]
在任一种本文所公开的工程化的免疫细胞(例如,工程化的nk细胞)的一些实施方案中,工程化的免疫细胞可以展现如与对照细胞相比增强的针对靶细胞的细胞毒性。在一些情形中,如本文所公开的工程化的免疫细胞可以展现比对照细胞大至少或多达约0.1倍、至少或多达约0.2倍、至少或多达约0.3倍、至少或多达约0.4倍、至少或多达约0.5倍、至少或多达约0.6倍、至少或多达约0.7倍、至少或多达约0.8倍、至少或多达约0.9倍、至少或多达约1倍、至少或多达约2倍、至少或多达约3倍、至少或多达约4倍、至少或多达约5倍、至少或多达约6倍、至少或多达约7倍、至少或多达约8倍、至少或多达约9倍、至少或多达约10倍、至少或多达约20倍、至少或多达约30倍、至少或多达约40倍、至少或多达约50倍、至少或多达约60倍、至少或多达约70倍、至少或多达约80倍、至少或多达约90倍、至少或多达约100倍、至少或多达约500倍、至少或多达约1,000倍、至少或多达约5,000倍或者至少或多达约10,000倍的针对靶细胞或靶细胞群体的细胞毒性(例如,体外、离体或体内),如通过例如跟
踪靶细胞群体的数量的变化所查明。
[0202]
在任一种本文所公开的工程化的免疫细胞(例如,工程化的nk细胞)的一些实施方案中,如与对照细胞相比,工程化的免疫细胞可以诱导来自单独的免疫细胞(例如,体外的单独的t细胞和/或b细胞,或者在将工程化的免疫细胞施用至宿主后宿主的免疫细胞)的降低的免疫应答。在一些情形中,如与暴露于对照细胞时来自单独的免疫细胞的免疫应答相比,如本文所公开的工程化的免疫细胞可以将来自单独的免疫细胞的免疫应答降低至少或多达约0.1倍、至少或多达约0.2倍、至少或多达约0.3倍、至少或多达约0.4倍、至少或多达约0.5倍、至少或多达约0.6倍、至少或多达约0.7倍、至少或多达约0.8倍、至少或多达约0.9倍、至少或多达约1倍、至少或多达约2倍、至少或多达约3倍、至少或多达约4倍、至少或多达约5倍、至少或多达约6倍、至少或多达约7倍、至少或多达约8倍、至少或多达约9倍、至少或多达约10倍、至少或多达约20倍、至少或多达约30倍、至少或多达约40倍、至少或多达约50倍、至少或多达约60倍、至少或多达约70倍、至少或多达约80倍、至少或多达约90倍、至少或多达约100倍、至少或多达约500倍、至少或多达约1,000倍、至少或多达约5,000倍或者至少或多达约10,000倍,如通过例如测量(i)工程化的免疫细胞的初始群体的数量在暴露于单独的免疫细胞之后的变化或(ii)单独的免疫细胞的细胞因子释放在暴露于工程化的免疫细胞的初始群体之后的变化所查明。
[0203]
在任一种本文所公开的工程化的免疫细胞(例如,工程化的nk细胞)的一些实施方案中,如与对照细胞相比,工程化的免疫细胞可以在暴露于单独的免疫细胞(例如,体外的单独的t细胞和/或b细胞,或者在将工程化的免疫细胞施用至宿主后宿主的免疫细胞)之后展现延长的半衰期。在一些情形中,在暴露于单独的免疫细胞(例如,在体外或在体内)之后,工程化的免疫细胞的半衰期可以比对照细胞长至少或多达约0.1倍、至少或多达约0.2倍、至少或多达约0.3倍、至少或多达约0.4倍、至少或多达约0.5倍、至少或多达约0.6倍、至少或多达约0.7倍、至少或多达约0.8倍、至少或多达约0.9倍、至少或多达约1倍、至少或多达约2倍、至少或多达约3倍、至少或多达约4倍、至少或多达约5倍、至少或多达约6倍、至少或多达约7倍、至少或多达约8倍、至少或多达约9倍、至少或多达约10倍、至少或多达约20倍、至少或多达约30倍、至少或多达约40倍、至少或多达约50倍、至少或多达约60倍、至少或多达约70倍、至少或多达约80倍、至少或多达约90倍、至少或多达约100倍、至少或多达约500倍、至少或多达约1,000倍、至少或多达约5,000倍或者至少或多达约10,000倍,如通过随时间监测工程化的免疫细胞的数量(例如,通过facs)所查明。
[0204]
在任一种本文所公开的工程化的免疫细胞(例如,工程化的nk细胞)的一些实施方案中,如与对照细胞相比,工程化的免疫细胞可以实现受试者的身体组织的增强的功能或病理状态。在一些情形中,如与对照细胞或媒介物(即,无细胞)相比,用工程化的免疫细胞治疗可以实现增强至少或多达约0.1倍、至少或多达约0.2倍、至少或多达约0.3倍、至少或多达约0.4倍、至少或多达约0.5倍、至少或多达约0.6倍、至少或多达约0.7倍、至少或多达约0.8倍、至少或多达约0.9倍、至少或多达约1倍、至少或多达约2倍、至少或多达约3倍、至少或多达约4倍、至少或多达约5倍、至少或多达约6倍、至少或多达约7倍、至少或多达约8倍、至少或多达约9倍、至少或多达约10倍、至少或多达约20倍、至少或多达约30倍、至少或多达约40倍、至少或多达约50倍、至少或多达约60倍、至少或多达约70倍、至少或多达约80倍、至少或多达约90倍、至少或多达约100倍、至少或多达约500倍、至少或多达约1,000倍、
至少或多达约5,000倍或者至少或多达约10,000倍的受试者的身体组织的功能或病理状态。
[0205]
在任一种本文所公开的工程化的免疫细胞(例如,工程化的nk细胞)的一些实施方案中,如与对照细胞相比,工程化的免疫细胞可以实现受试者的身体组织的功能或病理状态的延迟的退化。在一些情形中,如与对照细胞或媒介物(即,无细胞)相比,用工程化的免疫细胞治疗可以实现延迟至少或多达约0.1倍、至少或多达约0.2倍、至少或多达约0.3倍、至少或多达约0.4倍、至少或多达约0.5倍、至少或多达约0.6倍、至少或多达约0.7倍、至少或多达约0.8倍、至少或多达约0.9倍、至少或多达约1倍、至少或多达约2倍、至少或多达约3倍、至少或多达约4倍、至少或多达约5倍、至少或多达约6倍、至少或多达约7倍、至少或多达约8倍、至少或多达约9倍、至少或多达约10倍、至少或多达约20倍、至少或多达约30倍、至少或多达约40倍、至少或多达约50倍、至少或多达约60倍、至少或多达约70倍、至少或多达约80倍、至少或多达约90倍、至少或多达约100倍、至少或多达约500倍、至少或多达约1,000倍、至少或多达约5,000倍或者至少或多达约10,000倍的受试者的身体组织的功能或病理状态的退化。
[0206]
在任一种本文所公开的工程化的免疫细胞(例如,工程化的nk细胞)的一些实施方案中,身体组织可以包括选自以下的一个或多个(例如,1、2、3、4或更多个)成员:血液、血浆、血清、尿、外淋巴液、粪便、唾液、精液、羊水、脑脊液、胆汁、汗、泪、痰、滑液、呕吐物、骨、心脏、胸腺、动脉、血管、肺、肌肉、胃、肠、肝、胰、脾、肾、胆囊、甲状腺、肾上腺、乳腺、卵巢、前列腺、睾丸、皮肤、脂肪、眼、脑、受感染组织、患病组织、恶性组织、钙化组织和健康组织。
[0207]
在任一种本文所公开的工程化的免疫细胞(例如,工程化的nk细胞)的一些实施方案中,工程化的免疫细胞可以诱导针对靶细胞的免疫应答。靶标可以是例如患病细胞、癌细胞、肿瘤细胞等。
[0208]
在任一种本文所公开的工程化的免疫细胞(例如,工程化的nk细胞)的一些实施方案中,异源基因可以与组成型的、诱导型的、时序的、组织特异性的和/或细胞类型特异性的启动子可操作地偶联(例如,用于敲入)。目的启动子的非限制性例子可以包括cmv、ef1a、pgk、cag和ubc。插入位点的非限制性例子可以包括aavs1、ccr5、rosa26、胶原、htrp、h11、b2m、gapdh、tcr、runx1、tap1、tap2、tapasin、nlrc5、ciita、rfxank、ciita、rfx5、rfxap、tcr a或b恒定区、nkg2a、nkg2d、cd38、cis、cbl-b、socs2、pd1、ctla4、lag3、tim3和tigit。
[0209]
在任一种本文所公开的工程化的免疫细胞(例如,工程化的nk细胞)的一些实施方案中,可以展现用于增强工程化的免疫细胞在肿瘤微环境中的功能的以下内源基因(即,肿瘤微环境基因或“tme”)中的一种或多种(例如,1、2、3、4或更多种)的降低的表达或活性。在一些情形中,具有tme的降低的表达或活性可以增强工程化的免疫细胞的针对靶细胞的免疫活性。在一些情形中,tme基因可以是免疫检查点抑制剂。tme的非限制性例子可以包括:nkg2a、nkg2d、pd1、ctla4、lag3、tim3、tigit、kir2d、cd94、cd96、tgfβ受体、2b4和ship2。
[0210]
在任一种本文所公开的工程化的免疫细胞(例如,工程化的nk细胞)的一些实施方案中,可以展现用于例如增强的功能的一种或多种(例如,1、2、3、4或更多种)异源基因(例如,敲入的):cd137、cd80、cd86、dap10(例如,具有或没有点突变)。
[0211]
在任一种本文所公开的工程化的免疫细胞(例如,工程化的nk细胞)的一些实施方案中,可以展现用于例如低免疫性的以下内源基因中的一种或多种(例如,1、2、3、4或更多
种)的降低的表达或活性:b2m、ciita、tap1、tap2、tapasin、nlrc5、rfxank、rfx5、rfxap、cd80、cd86、icosl、cd40l、icam1、mica、micb和nkg2dl(例如,ulbp1)。
[0212]
在任一种本文所公开的工程化的免疫细胞(例如,工程化的nk细胞)的一些实施方案中,可以展现用于例如低免疫性的一种或多种(例如,1、2、3、4或更多种)异源基因(例如,敲入的):hla-e、cd47、cd113、pdl1、pdl2、a2ar、hla-g、tgf-β、ccl21、il10、cd46、cd55和cd59。
[0213]
在任一种本文所公开的工程化的免疫细胞(例如,工程化的nk细胞)的一些实施方案中,可以展现一种或多种(例如,1、2、3、4或更多种)异源基因(例如,敲入的):cd3、cd4、cd80、41bbl和cd131。
[0214]
d.嵌合抗原受体
[0215]
本公开文本的工程化的免疫细胞(例如,工程化的nk细胞)可以包含如本文所公开的嵌合多肽受体(例如,至少1、2、3、4、5或更多种不同类型的嵌合多肽受体)。可以将工程化的免疫细胞工程化以瞬时地或永久地表达嵌合多肽受体。在一些情形中,重组嵌合多肽受体可以经由例如脂质体被递送至工程化的免疫细胞,并且可以通过膜融合被掺入工程化的免疫细胞中。在一些情形中,可以将编码嵌合多肽受体的异源多核苷酸构建体(例如,dna或rna)递送至工程化的免疫细胞。编码异源多核苷酸构建体的异源多核苷酸构建体(即,基因)可以被掺入工程化的免疫细胞的染色体中(即,染色体基因),或者可替代地,可以不被整合至或无需被整合至如本文所公开的工程化的免疫细胞的染色体中。
[0216]
嵌合多肽受体可以包含t细胞受体融合蛋白(tfp)。术语“t细胞受体融合蛋白”或“tfp”通常是指重组多肽构建体,其包含(i)一个或多个抗原结合部分(例如,单特异性或多特异性),(ii)tcr细胞外结构域的至少一部分,(iii)tcr跨膜结构域的至少一部分,以及(iv)tcr细胞内结构域的至少一部分。
[0217]
在一些情形中,可以使本公开文本的工程化的免疫细胞(例如,工程化的nk细胞)的内源t细胞受体(tcr)失活。在一些例子中,工程化的免疫细胞的内源tcr的功能可以被抑制剂抑制。在一些例子中,可以使编码内源tcr的亚基的基因失活(例如,通过如本文所公开的基因编辑部分的作用进行编辑),使得所述内源tcr失活。编码内源tcr的亚基的基因可以是以下中的一种或多种:tcrα、tcrβ、cd3ε、cd3δ、cd3γ和cd3ζ。
[0218]
嵌合多肽受体可以包含嵌合抗原受体(car)。术语“嵌合抗原受体”或“car”通常是指重组多肽构建体,其包含至少细胞外抗原结合结构域、跨膜结构域以及包括源自刺激分子的功能信号传导结构域的胞质信号传导结构域(本文中也称为“细胞内或内在信号传导结构域”)。在一些情形中,刺激分子可以是与t细胞受体复合物相关的ζ链。在一些情形中,细胞内信号传导结构域还包括源自至少一种共刺激分子的一个或多个功能信号传导结构域。在一些情形中,共刺激分子可以包括4-1bb(即,cd137)、cd27和/或cd28。在一方面,car包含在car融合蛋白的氨基末端(n-ter)的可选前导序列。在一方面,car还包含在细胞外抗原识别结构域的n末端的前导序列,其中在细胞加工和car定位至细胞膜期间,所述前导序列任选地从抗原识别结构域(例如,scfv、darpin等)切割。
[0219]
car可以是第一代、第二代、第三代或第四代car系统、其功能变体或其任何组合。第一代car(例如,cd19r或cd19car)包括具有对特定抗原的特异性的抗原结合结构域(例如,抗体或其抗原结合片段,如darpin、scfv、fab片段、vhh结构域或仅有重链的抗体的vh结
构域)、源自适应性免疫受体的跨膜结构域(例如,来自cd28受体的跨膜结构域)以及源自适应性免疫受体的信号传导结构域(例如,源自cd3ζ受体或fcεriγ的细胞内区域的一个或多个(例如,三个)itam结构域)。第二代car通过将共刺激结构域添加至car的细胞内信号传导结构域部分(例如,源自与t细胞受体共同作用的共刺激受体,如cd28、cd137/4-1bb和cd134/ox40)来改良第一代car,从而消除了对与第一代car共同施用辅因子(例如,il-2)的需要。第三代car将多个共刺激结构域添加至car的细胞内信号传导结构域部分(例如,cd3ζ-cd28-ox40或cd3ζ-cd28-41bb)。第四代car通过将激活细胞因子(例如,il-12、il-23或il-27)添加至car的细胞内信号传导部分(例如,在一个或多个共刺激结构域与cd3ζitam结构域之间)或处于car诱导的启动子(例如,nfat/il-2最小启动子)的控制下来改良第二代或第三代car。在一些情形中,car可以是如本文所公开的与第一代、第二代、第三代或第四代car系统不同的新一代car系统。
[0220]
如本文所公开的工程化的免疫细胞(例如,工程化的nk细胞)中car的铰链结构域(例如,细胞外抗原结合结构域与跨膜结构域之间的接头)可以包含cd3d、cd3e、cd3g、cd3c cd4、cd8、cd8a、cd8b、cd27、cd28、cd40、cd84、cd166、4-1bb、ox40、icos、icam-1、ctla-4、pd-1、lag-3、2b4、btla、cd16、il7、il12、il15、kir2dl4、kir2ds1、nkp30、nkp44、nkp46、nkg2c、nkg2d或t细胞受体多肽的天然或修饰的跨膜区域的全长或至少一部分。
[0221]
如本文所公开的工程化的免疫细胞(例如,工程化的nk细胞)中car的跨膜结构域可以包含cd3d、cd3e、cd3g、cd3c cd4、cd8、cd8a、cd8b、cd27、cd28、cd40、cd84、cd166、4-1bb、ox40、icos、icam-1、ctla-4、pd-1、lag-3、2b4、btla、cd16、il7、il12、il15、kir2dl4、kir2ds1、nkp30、nkp44、nkp46、nkg2c、nkg2d或t细胞受体多肽的天然或修饰的跨膜区域的全长或至少一部分。
[0222]
如本文所公开的car的铰链结构域和跨膜结构域(例如,对于工程化的免疫细胞,如工程化的nk细胞)可以源自相同蛋白质(例如,cd8)。可替代地,如本文所公开的car的铰链结构域和跨膜结构域可以源自不同蛋白质。
[0223]
car的信号传导结构域可以包含至少或多达约1个信号传导结构域、至少或多达约2个信号传导结构域、至少或多达约3个信号传导结构域、至少或多达约4个信号传导结构域、至少或多达约5个信号传导结构域、至少或多达约6个信号传导结构域、至少或多达约7个信号传导结构域、至少或多达约8个信号传导结构域、至少或多达约9个信号传导结构域或者至少或多达约10个信号传导结构域。
[0224]
如本文所公开的工程化的免疫细胞(例如,工程化的nk细胞)中car的信号传导结构域(例如,细胞内信号传导结构域的信号传导肽)可以包含cd3ζ、2b4、dap10、dap12、dnam1、cd137(41bb)、il21、il7、il12、il15、nkp30、nkp44、nkp46、nkg2c、nkg2d或其任何组合的多肽的全长或至少一部分。
[0225]
可替代地或者除了(即,共刺激结构域)外,如本文所公开的工程化的免疫细胞(例如,工程化的nk细胞)中的信号传导结构域car可以包含cd27、cd28、4-1bb、ox40、icos、pd-1、lag-3、2b4、btla、dap10、dap12、ctla-4或nkg2d或其任何组合的多肽的全长或至少一部分。
[0226]
在一些情形中,如本文所公开的工程化的免疫细胞(例如,工程化的nk细胞)包含嵌合多肽受体(例如,car),所述嵌合多肽受体包含至少cd8跨膜结构域以及以下中的一种
或多种:(i)2b4信号传导结构域和(ii)dap10信号传导结构域。在一些情形中,如本文所公开的工程化的细胞(例如,工程化的nk细胞)包含嵌合多肽受体(例如,tfp或car),所述嵌合多肽受体包含至少(i)cd8跨膜结构域,(ii)2b4信号传导结构域,以及(iii)dap10信号传导结构域。2b4信号传导结构域的侧翼可以是cd8跨膜结构域和dap10信号传导结构域。可替代地,dap10信号传导结构域的侧翼可以是cd8跨膜结构域和2b4信号传导结构域。在一些情形中,如本文所公开的嵌合多肽受体还可以包含源自cd3ζ的又另外的信号传导结构域。
[0227]
如本文所公开的嵌合多肽受体(例如,tfp或car)的抗原结合部分的抗原(即,靶抗原)可以是细胞表面标记、分泌型标记或细胞内标记。
[0228]
如本文所公开的嵌合多肽受体(例如,tfp或car)的抗原结合部分的抗原(即,靶抗原)的非限制性例子可以包括adgre2、碳酸酐酶ix(ca1x)、ccri、ccr4、癌胚抗原(cea)、cd3ζ、cd5、cd8、cd10、cd19、cd20、cd22、cd30、cd33、cd34、cd38、cd41、cd44、cd44v6、cd49f、cd56、cd70、cd74、cd99、cd123、cd133、cd138、cd269(bcma)、cd s、clec12a、巨细胞病毒(cmv)感染的细胞的抗原(例如,细胞表面抗原)、上皮糖蛋白2(egp 2)、上皮糖蛋白-40(egp-40)、上皮细胞粘附分子(epcam)、egfrviii、受体酪氨酸蛋白激酶erb-b2,3,4、egfir、egfr-viii、erbb叶酸结合蛋白(fbp)、胎儿乙酰胆碱受体(achr)、叶酸受体-a、神经节苷脂g2(gd2)、神经节苷脂g3(gd3)、gp100、人表皮生长因子受体2(her-2)、人端粒酶逆转录酶(htert)、icam-1、整合素b7、白介素-13受体亚基α-2(il-13rα2)、κ轻链、激酶插入结构域受体(kdr)、κ、lewis a(ca19.9)、lewis y(ley)、l1细胞粘附分子(l1-cam)、lilrb2、mart-1、黑色素瘤抗原家族a1(mage-a1)、mica/b、黏蛋白1(muc-1)、黏蛋白16(muc-16)、间皮素(msln)、nkcsi、nkg2d配体、c-met、癌症-睾丸抗原ny-eso-1、ny-eso-2、癌胚胎抗原(h5t4)、praivie、前列腺干细胞抗原(psca)、prame前列腺特异性膜抗原(psma)、ror1、肿瘤相关糖蛋白72(tag-72)、tim-3、trbci、trbc2、血管内皮生长因子r2(vegf-r2)、肾母细胞瘤蛋白(wt-1)以及各种病原体抗原(例如,源自能够引起疾病的病毒、细菌、真菌、寄生虫和原生动物的病原体抗原)。在一些例子中,病原体抗原源自hiv、hbv、ebv、hpv、lasse病毒、流感病毒或冠状病毒。
[0229]
如本文所公开的嵌合多肽受体的抗原结合部分的抗原的另外的例子可以包括1-40-β-淀粉样蛋白、4-1bb、5ac、5t4、激活素受体样激酶1、acvr2b、腺癌抗原、ags-22m6、甲胎蛋白、血管生成素2、血管生成素3、炭疽毒素、aoc3(vap-1)、b7-h3、炭疽杆菌(bacillus anthracis)炭疽、baff、β-淀粉样蛋白、b淋巴瘤细胞、c242抗原、c5、ca-125、家犬(canis lupus familiaris)il31、碳酸酐酶9(ca-ix)、心肌肌球蛋白、ccl11(嗜酸性粒细胞趋化因子-1)、ccr4、ccr5、cd11、cd18、cd125、cd140a、cd147(basigin)、cd15、cd152、cd154(cd40l)、cd19、cd2、cd20、cd200、cd22、cd221、cd23(ige受体)、cd25(il-2受体的α链)、cd27、cd274、cd28、cd3、cd3ε、cd30、cd33、cd37、cd38、cd4、cd40、cd40配体、cd41、cd44 v6、cd5、cd51、cd52、cd56、cd6、cd70、cd74、cd79b、cd80、cea、cea相关抗原、cfd、ch4d5、cldn18.2、艰难梭菌(clostridium difficile)、凝集因子a、csf1r、csf2、ctla-4、c—x—c趋化因子受体类型4、巨细胞病毒、巨细胞病毒糖蛋白b、达比加群、dll4、dpp4、dr5、大肠杆菌(e.coli)志贺毒素类型1、大肠杆菌志贺毒素类型2、egfl7、egfr、内毒素、epcam、表唾液酸蛋白(episialin)、erbb3、大肠杆菌(escherichia coli)、呼吸道合胞病毒的f蛋白、fap、纤维蛋白iiβ链、纤连蛋白额外结构域b、叶酸水解酶、叶酸受体1、叶酸受体α、卷曲受体、神
经节苷脂gd2、gd2、gd3神经节苷脂、磷脂酰肌醇蛋白聚糖3、gmcsf受体α链、gpnmb、生长分化因子8、gucy2c、血凝素、乙型肝炎表面抗原、乙型肝炎病毒、her1、her2/neu、her3、hgf、hhgfr、组蛋白复合物、hiv-1、hla-dr、hngf、hsp90、人散射因子受体激酶、人tnf、人β-淀粉样蛋白、icam-1(cd54)、ifn-α、ifn-γ、ige、ige fc区、igf-1受体、igf-1、ighe、il17a、il17f、il20、il-12、il-13、il-17、il-1β、il-22、il-23、il-31ra、il-4、il-5、il-6、il-6受体、il-9、ilgf2、甲型流感血凝素、甲型流感病毒血凝素、胰岛素样生长因子i受体、整合素α4β7、整合素α4、整合素α5β1、整合素α7β7、整合素αiibβ3、整合素αvβ3、干扰素α/β受体、干扰素γ诱导蛋白、itga2、itgb2(cd18)、kir2d、lewis-y抗原、lfa-1(cd11a)、lingo-1、脂磷壁酸、loxl2、l-选择素(cd62l)、lta、mcp-1、间皮素、mif、ms4a1、msln、muc1、黏蛋白canag、髓磷脂相关糖蛋白、肌生成抑制蛋白、nca-90(粒细胞抗原)、神经细胞凋亡调节蛋白酶1、ngf、n-羟乙酰神经氨酸、nogo-a、notch受体、nrp1、穴兔(oryctolagus cuniculus)、ox-40、oxldl、pcsk9、pd-1、pdcd1、pdgf-rα、磷酸钠协同转运蛋白、磷脂酰丝氨酸、源自血小板的生长因子受体β、前列腺癌细胞、铜绿假单胞菌(pseudomonas aeruginosa)、狂犬病毒糖蛋白、rankl、呼吸道合胞病毒、rhd、恒河猴因子、ron、rtn4、硬化蛋白、sdc1、选择素p、slamf7、sost、鞘氨醇-1-磷酸、金黄色葡萄球菌(staphylococcus aureus)、steap1、tag-72、t细胞受体、tem1、生腱蛋白c、tfpi、tgf-β1、tgf-β2、tgf-β、tnf-α、trail-r1、trail-r2、肿瘤抗原ctaa16.88、muc1的肿瘤特异性糖基化、肿瘤相关的钙信号转导蛋白2、tweak受体、tyrp1(糖蛋白75)、vegfa、vegfr1、vegfr2、波形蛋白和vwf。
[0230]
如本文所公开的嵌合多肽受体的抗原结合部分的抗原的另外的例子可以包括707-ap、生物素化的分子、a-辅肌动蛋白-4、abl-bcr alb-b3(b2a2)、abl-bcr alb-b4(b3a2)、脂肪分化相关蛋白(adipophilin)、afp、aim-2、膜联蛋白ii、art-4、bage、b-连环素、bcr-abl、bcr-abl p190(e1a2)、bcr-abl p210(b2a2)、bcr-abl p210(b3a2)、bing-4、cag-3、caix、camel、胱天蛋白酶-8、cd171、cd19、cd20、cd22、cd23、cd24、cd30、cd33、cd38、cd44v7/8、cdc27、cdk-4、cea、clca2、cyp-b、dam-10、dam-6、dek-can、egfrviii、egp-2、egp-40、elf2、ep-cam、epha2、epha3、erb-b2、erb-b3、erb-b4、es-eso-1a、etv6/aml、fbp、胎儿乙酰胆碱受体、fgf-5、fn、g250、gage-1、gage-2、gage-3、gage-4、gage-5、gage-6、gage-7b、gage-8、gd2、gd3、gnt-v、gp100、gp75、her-2、hla-a*0201-r170i、hmw-maa、hsp70-2 m、hst-2(fgf6)、hst-2/neu、htert、ice、il-11rα、il-13rα2、kdr、kiaa0205、k-ras、l1-细胞粘附分子、lage-1、ldlr/fut、lewis y、mage-1、mage-10、mage-12、mage-2、mage-3、mage-4、mage-6、mage-a1、mage-a2、mage-a3、mage-a6、mage-b1、mage-b2、苹果酸酶、乳腺珠蛋白-a、mart-1/黑色素-a、mart-2、mc1r、m-csf、间皮素、muc1、muc16、muc2、mum-1、mum-2、mum-3、肌球蛋白、na88-a、neo-pap、nkg2d、npm/alk、n-ras、ny-eso-1、oa1、ogt、癌胚胎抗原(h5t4)、os-9、p多肽、p15、p53、prame、psa、psca、psma、ptprk、rage、ror1、ru1、ru2、sart-1、sart-2、sart-3、sox10、ssx-2、存活蛋白、存活蛋白-2b、syt/ssx、tag-72、tel/aml1、tgfarii、tgfbrii、tp1、trag-3、trg、trp-1、trp-2、trp-2/int2、trp-2-6b、酪氨酸酶、vegf-r2、wt1、α-叶酸受体和κ轻链。
[0231]
如本文所公开的嵌合多肽受体的抗原结合部分的抗原的另外的例子可以包括抗体、其片段或其变体。这样的抗体可以是天然抗体(例如,由受试者的免疫细胞如b细胞天然分泌的)、合成抗体或修饰的抗体。在一些情形中,如本文所公开的嵌合多肽受体的抗原结
enhanze)(达雷木单抗)、darleukin、德屈库单抗(dectrekumab)、登赛珠单抗(demcizumab)、地妥珠单抗莫福汀(denintuzumab mafodotin)、地诺单抗(denosumab)、迪妥昔珠单抗(depatuxizumab)、迪妥昔珠单抗莫福汀(depatuxizumab mafodotin)、德鲁妥昔单抗生物素(derlotuximab biotin)、地莫单抗(detumomab)、di-b4、地努妥昔单抗(dinutuximab)、地利伏单抗(diridavumab)、dkn-01、dmot4039a、阿托度单抗(dorlimomab aritox)、德罗妥单抗(drozitumab)、ds-1123、ds-8895、杜利妥单抗(duligotumab)、度皮鲁单抗(dupilumab)、度伐鲁单抗(durvalumab)、度司妥单抗(dusigitumab)、依美昔单抗(ecromeximab)、依库珠单抗(eculizumab)、埃巴单抗(edobacomab)、依决洛单抗(edrecolomab)、依法利珠单抗(efalizumab)、依芬古单抗(efungumab)、埃德鲁单抗(eldelumab)、依更妥单抗(elgemtumab)、埃罗妥珠单抗(elotuzumab)、艾西莫单抗(elsilimomab)、艾马妥珠单抗(emactuzumab)、依玛妥珠单抗(emibetuzumab)、依那妥珠单抗(enavatuzumab)、恩诺单抗维多汀(enfortumab vedotin)、恩莫单抗培戈(enlimomab pegol)、依诺妥珠单抗(enoblituzumab)、恩诺珠单抗(enokizumab)、恩诺库单抗(enoticumab)、恩妥昔单抗(ensituximab)、依匹莫单抗西妥昔坦(epitumomab cituxetan)、依帕珠单抗(epratuzumab)、厄利珠单抗(erlizumab)、厄妥索单抗(ertumaxomab)、埃达珠单抗(etaracizumab)、依曲利单抗(etrolizumab)、依维苏单抗(evinacumab)、依洛尤单抗(evolocumab)、艾韦单抗(exbivirumab)、法索单抗(fanolesomab)、法拉莫单抗(faralimomab)、法妥珠单抗(farletuzumab)、法辛单抗(fasinumab)、fbta05、泛维珠单抗(felvizumab)、非扎奴单抗(fezakinumab)、ff-21101、fgfr2抗体-药物缀合物、fibromun、非克拉珠单抗(ficlatuzumab)、芬妥木单抗(figitumumab)、非利伏单抗(firivumab)、法兰妥单抗(flanvotumab)、夫来库单抗(fletikumab)、芳妥珠单抗(fontolizumab)、福雷芦单抗(foralumab)、福拉韦单抗(foravirumab)、fpa144、非苏木单抗(fresolimumab)、fs102、富兰奴单抗(fulranumab)、伏妥昔单抗(futuximab)、加利昔单抗(galiximab)、加尼妥单抗(ganitumab)、甘特珠单抗(gantenerumab)、加维莫单抗(gavilimomab)、吉妥珠单抗奥佐米星(gemtuzumab ozogamicin)、戈丽珠单抗(gerilimzumab)、吉伏珠单抗(gevokizumab)、吉妥昔单抗(girentuximab)、格巴妥木单抗维多汀(glembatumumab vedotin)、gnr-006、gnr-011、戈利木单抗(golimumab)、戈米利昔单抗(gomiliximab)、gsk2849330、gsk2857916、gsk3174998、gsk3359609、古塞库单抗(guselkumab)、hu14.18k322a mab、hu3s193、hu8f4、hul2g7、humab-5b1、伊巴珠单抗(ibalizumab)、替伊莫单抗替西坦(ibritumomab tiuxetan)、伊克鲁单抗(icrucumab)、依达赛珠单抗(idarucizumab)、ign002、ign523、伊戈伏单抗(igovomab)、imab362、imab362(克劳地昔单抗(claudiximab))、伊玛鲁单抗(imalumab)、imc-cs4、imc-d11、伊西罗单抗(imciromab)、伊加妥珠单抗(imgatuzumab)、imgn529、immu-102(钇y-90依帕珠单抗泰坦(epratuzumab tetraxetan))、immu-114、immutune imp701拮抗剂抗体、incagn1876、恩库拉单抗(inclacumab)、incshr1210、英达妥昔单抗拉坦辛(indatuximab ravtansine)、吲哚妥单抗维多汀(indusatumab vedotin)、英夫利昔单抗(infliximab)、伊诺莫单抗(inolimomab)、奥英妥珠单抗(inotuzumab ozogamicin)、英特木单抗(intetumumab)、伊帕西普(ipafricept)、iph4102、伊匹单抗(ipilimumab)、达妥木单抗(iratumumab)、伊沙妥昔单抗(isatuximab)、艾司妥单抗(istiratumab)、伊托珠单抗
(itolizumab)、依奇珠单抗(ixekizumab)、jnj-56022473、jnj-61610588、凯利昔单抗(keliximab)、ktn3379、l19il2/l19tnf、拉贝妥珠单抗(labetuzumab)、拉贝妥珠单抗戈维替康(labetuzumab govitecan)、lag525、兰博利珠单抗(lambrolizumab)、兰帕利珠单抗(lampalizumab)、l-dos47、来瑞珠单抗(lebrikizumab)、来马索单抗(lemalesomab)、伦齐鲁单抗(lenzilumab)、乐地单抗(lerdelimumab)、鲁库妥昔单抗(leukotuximab)、来沙木单抗(lexatumumab)、利韦单抗(libivirumab)、利法珠单抗维多汀(lifastuzumab vedotin)、利格珠单抗(ligelizumab)、利洛托单抗沙司坦(lilotomab satetraxetan)、林妥珠单抗(lintuzumab)、利瑞鲁单抗(lirilumab)、lkz145、洛迪赛珠单抗(lodelcizumab)、洛吉维单抗(lokivetmab)、洛沃妥珠单抗美坦辛(lorvotuzumab mertansine)、鲁卡木单抗(lucatumumab)、培戈-鲁利珠单抗(lulizumab pegol)、鲁昔单抗(lumiliximab)、鲁妥珠单抗(lumretuzumab)、ly3164530、马帕木单抗(mapatumumab)、玛格妥昔单抗(margetuximab)、马司莫单抗(maslimomab)、马妥珠单抗(matuzumab)、玛弗利木单抗(mavrilimumab)、mb311、mcs-110、medi0562、medi-0639、medi0680、medi-3617、medi-551(伊奈利珠单抗(inebilizumab))、medi-565、medi6469、美泊珠单抗(mepolizumab)、美替木单抗(metelimumab)、mgb453、mgd006/s80880、mgd007、mgd009、mgd011、米拉妥珠单抗(milatuzumab)、米拉妥珠单抗-sn-38、明瑞莫单抗(minretumomab)、索星-米妥昔单抗(mirvetuximab soravtansine)、米妥莫单抗(mitumomab)、mk-4166、mm-111、mm-151、mm-302、莫格利珠单抗(mogamulizumab)、mor202、mor208、morab-066、莫洛木单抗(morolimumab)、莫维珠单抗(motavizumab)、莫妥昔单抗帕索多(moxetumomab pasudotox)、莫罗单抗-cd3(muromonab-cd3)、纳可洛单抗他非那妥(nacolomab tafenatox)、纳米鲁单抗(namilumab)、那普妥莫单抗依他芬妥司(naptumomab estafenatox)、那呐妥单抗(narnatumab)、那他珠单抗(natalizumab)、奈巴库单抗(nebacumab)、耐昔妥珠单抗(necitumumab)、奈莫利珠单抗(nemolizumab)、奈瑞莫单抗(nerelimomab)、奈伐苏单抗(nesvacumab)、尼妥珠单抗(nimotuzumab)、纳武单抗(nivolumab)、巯诺莫单抗(nofetumomab merpentan)、nov-10、奥比妥昔单抗(obiltoxaximab)、奥滨尤妥珠单抗(obinutuzumab)、奥卡妥珠单抗(ocaratuzumab)、奥瑞珠单抗(ocrelizumab)、奥度莫单抗(odulimomab)、奥法木单抗(ofatumumab)、奥拉木单抗(olaratumab)、奥洛珠单抗(olokizumab)、奥马珠单抗(omalizumab)、omp-131r10、omp-305b83、奥那妥珠单抗(onartuzumab)、昂妥昔珠单抗(ontuxizumab)、奥匹西单抗(opicinumab)、莫妥珠单抗莫纳妥昔(oportuzumab monatox)、奥戈伏单抗(oregovomab)、奥替苏单抗(orticumab)、奥昔珠单抗(otelixizumab)、奥妥珠单抗(otlertuzumab)、ox002/men1309、奥塞芦单抗(oxelumab)、奥扎尼珠单抗(ozanezumab)、奥丽珠单抗(ozoralizumab)、帕吉昔单抗(pagibaximab)、帕利珠单抗(palivizumab)、帕尼单抗(panitumumab)、潘科单抗(pankomab)、潘科单抗-gex、帕巴库单抗(panobacumab)、帕萨妥珠单抗(parsatuzumab)、帕考珠单抗(pascolizumab)、帕妥昔珠单抗(pasotuxizumab)、帕替利单抗(pateclizumab)、帕曲妥单抗(patritumab)、pat-sc1、pat-sm6、派姆单抗(pembrolizumab)、喷妥莫单抗(pemtumomab)、培拉凯珠单抗(perakizumab)、帕妥珠单抗(pertuzumab)、培珠单抗(pexelizumab)、pf-05082566(乌托米单抗(utomilumab))、pf-06647263、pf-06671008、pf-06801591、匹地利珠单抗(pidilizumab)、匹那妥珠单抗维多汀
(pinatuzumab vedotin)、平妥单抗(pintumomab)、普拉库鲁单抗(placulumab)、泊洛妥珠单抗维多汀(polatuzumab vedotin)、泊奈珠单抗(ponezumab)、普立昔单抗(priliximab)、普妥昔单抗(pritoxaximab)、普托木单抗(pritumumab)、pro 140、proxinium、psma adc、奎利珠单抗(quilizumab)、雷妥莫单抗(racotumomab)、雷曲妥单抗(radretumab)、雷韦单抗(rafivirumab)、雷泮赛珠单抗(ralpancizumab)、雷莫芦单抗(ramucirumab)、雷珠单抗(ranibizumab)、瑞西巴库单抗(raxibacumab)、瑞法尼单抗(refanezumab)、瑞加韦单抗(regavirumab)、regn1400、regn2810/sar439684、瑞替珠单抗(reslizumab)、rfm-203、rg7356、rg7386、rg7802、rg7813、rg7841、rg7876、rg7888、rg7986、利妥木单抗(rilotumumab)、雷努库单抗(rinucumab)、利妥昔单抗(rituximab)、rm-1929、ro7009789、罗妥木单抗(robatumumab)、罗勒度单抗(roledumab)、罗莫唑单抗(romosozumab)、罗塔利珠单抗(rontalizumab)、罗维珠单抗(rovelizumab)、卢利珠单抗(ruplizumab)、赛妥珠单抗戈维替康(sacituzumab govitecan)、沙马珠单抗(samalizumab)、sar408701、sar566658、沙利鲁单抗(sarilumab)、sat 012、沙妥莫单抗喷地肽(satumomab pendetide)、sct200、sct400、sea-cd40、苏金单抗(secukinumab)、司利班单抗(seribantumab)、司妥沙昔单抗(setoxaximab)、赛韦鲁单抗(sevirumab)、sgn-cd19a、sgn-cd19b、sgn-cd33a、sgn-cd70a、sgn-liv1a、西罗珠单抗(sibrotuzumab)、西法木单抗(sifalimumab)、司妥昔单抗(siltuximab)、辛妥珠单抗(simtuzumab)、西利珠单抗(siplizumab)、西鲁库单抗(sirukumab)、索非妥珠单抗维多汀(sofituzumab vedotin)、索拉珠单抗(solanezumab)、索利妥单抗(solitomab)、索耐珠单抗(sonepcizumab)、索土珠单抗(sontuzumab)、司他芦单抗(stamulumab)、硫索单抗(sulesomab)、舒维珠单抗(suvizumab)、syd985、sym004(伏妥昔单抗(futuximab)和扎妥昔单抗(modotuximab))、sym015、tab08、他巴鲁单抗(tabalumab)、他卡珠单抗泰坦(tacatuzumab tetraxetan)、他多昔珠单抗(tadocizumab)、他利珠单抗(talizumab)、塔尼珠单抗(tanezumab)、他尼单抗(tanibirumab)、塔利托莫单抗帕妥昔(taplitumomab paptox)、他瑞妥单抗(tarextumab)、tb-403、替非珠单抗(tefibazumab)、teleukin、替利莫单抗阿瑞妥昔(telimomab aritox)、替那莫单抗(tenatumomab)、替奈昔单抗(teneliximab)、替利珠单抗(teplizumab)、替普鲁木单抗(teprotumumab)、特度鲁单抗(tesidolumab)、替妥洛单抗(tetulomab)、tg-1303、tgn1412、钍-227-依帕珠单抗(epratuzumab)缀合物、伊匹木单抗(ticilimumab)、替加珠单抗(tigatuzumab)、替拉珠单抗(tildrakizumab)、替索托单抗维多汀(tisotumab vedotin)、tnx-650、托珠单抗(tocilizumab)、托拉珠单抗(toralizumab)、托沙妥昔单抗(tosatoxumab)、托西莫单抗(tositumomab)、托维妥单抗(tovetumab)、曲罗芦单抗(tralokinumab)、曲妥珠单抗(trastuzumab)、曲妥珠单抗恩坦辛(trastuzumab emtansine)、trbs07、trc105、曲加珠单抗(tregalizumab)、曲美木单抗(tremelimumab)、曲弗单抗(trevogrumab)、trph 011、trx518、tsr-042、tti-200.7、托妥珠单抗西莫白介素(tucotuzumab celmoleukin)、妥韦单抗(tuvirumab)、u3-1565、u3-1784、乌利妥昔单抗(ublituximab)、乌洛鲁单抗(ulocuplumab)、乌瑞芦单抗(urelumab)、乌妥珠单抗(urtoxazumab)、乌司奴单抗(ustekinumab)、瓦达妥昔单抗塔利林(vadastuximab talirine)、凡多珠单抗维多汀(vandortuzumab vedotin)、维迪西妥单抗(vantictumab)、伐努赛珠单抗(vanucizumab)、伐帕利昔单抗(vapaliximab)、伐立鲁单抗(varlilumab)、瓦
替珠单抗(vatelizumab)、vb6-845、维多珠单抗(vedolizumab)、维妥珠单抗(veltuzumab)、维帕利莫单抗(vepalimomab)、维森库单抗(vesencumab)、维西珠单抗(visilizumab)、伏洛昔单抗(volociximab)、沃瑟妥珠单抗莫福汀(vorsetuzumab mafodotin)、伏木单抗(votumumab)、yyb-101、扎芦木单抗(zalutumumab)、扎诺木单抗(zanolimumab)、扎妥昔单抗(zatuximab)、齐拉木单抗(ziralimumab)和唑莫单抗阿瑞妥昔(zolimomab aritox)。
[0232]
在一些情形中,如本文所公开的工程化的免疫细胞(例如,工程化的nk细胞)可以包含含有抗原结合结构域的嵌合多肽受体(例如,tfp或car),并且所述抗原结合结构域可能能够特异性地且优先地结合至包括选自以下的一个或多个(例如,1、2、3、4或更多个)成员的抗原:bcma、cd20、cd22、cd30、cd33、cd38、cd70、cd123、κ、lewis y、nkg2d配体、ror1、ny-eso-1、ny-eso-2、mart-1和gp100。nkg2d配体的非限制性例子包括选自以下的一个或多个(例如,1、2、3、4或更多个)成员:mica、micb、ulbp1、ulbp2、ulbp3、ulbp4、ulbp5和ulbp6。
[0233]
在一些情形中,如本文所公开的工程化的免疫细胞(例如,工程化的nk细胞)可以包含含有抗原结合结构域的嵌合多肽受体(例如,tfp或car),所述抗原结合结构域能够特异性结合靶细胞的抗原,并且工程化的免疫细胞可以展现编码嵌合多肽受体的相同抗原的内源基因的降低的表达或活性。因此,工程化的免疫细胞的群体可以避免彼此靶向和杀伤,例如,在施用至有需要的受试者之后。
[0234]
在一些情形中,如本文所公开的工程化的免疫细胞(例如,工程化的nk细胞)可以包含含有抗原结合结构域的嵌合多肽受体(例如,tfp或car),并且所述抗原结合结构域可能能够特异性地且优先地结合至cd23。在一些情形中,工程化的免疫细胞的编码cd23的内源基因可以被修饰以实现内源cd23的降低的表达或活性。
[0235]
在一些情形中,如本文所公开的工程化的免疫细胞(例如,工程化的nk细胞)可以包含含有抗原结合结构域的嵌合多肽受体(例如,tfp或car),并且所述抗原结合结构域可能能够特异性地且优先地结合至cd123。在一些情形中,工程化的免疫细胞的编码cd123的内源基因可以被修饰以实现内源cd123的降低的表达或活性。
[0236]
在一些情形中,如本文所公开的工程化的免疫细胞(例如,工程化的nk细胞)可以包含含有抗原结合结构域的嵌合多肽受体(例如,tfp或car),并且所述抗原结合结构域可能能够特异性地且优先地结合至cd38。在一些情形中,工程化的免疫细胞的编码cd38的内源基因可以被修饰以实现内源cd38的降低的表达或活性。在一些情形中,包含针对cd38的嵌合多肽受体的受试工程化免疫细胞可能能够靶向浆细胞并实现浆细胞的死亡(或降解)。
[0237]
在一些情形中,如本文所公开的工程化的免疫细胞(例如,工程化的nk细胞)可以包含含有抗原结合结构域的嵌合多肽受体(例如,tfp或car),并且所述抗原结合结构域可能能够特异性地且优先地结合至cd38。在一些例子中,工程化的免疫细胞是源自分离的esc或诱导干细胞(例如,ipsc)的工程化的nk细胞。在一些情形中,工程化的免疫细胞的编码cd38的内源基因可以被修饰以实现内源cd38的降低的表达或活性。
[0238]
在一些情形中,如本文所公开的工程化的免疫细胞(例如,工程化的nk细胞)可以包含含有抗原结合结构域的嵌合多肽受体(例如,tfp或car),并且所述抗原结合结构域可能能够特异性地且优先地结合至cd7。在一些情形中,工程化的免疫细胞的编码cd7的内源基因可以被修饰以实现内源cd7的降低的表达或活性。
[0239]
e.干细胞
[0240]
任一种本文所公开的工程化的免疫细胞(例如,工程化的nk细胞)可以源自分离的干细胞(例如,esc)或诱导干细胞(ipsc)。分离的干细胞或诱导干细胞可以被修饰(例如,遗传修饰)以生成工程化的免疫细胞。
[0241]
在一些情形中,干细胞(例如,esc或ipsc)的多能性可以部分通过评估细胞的多能性特征来确定。多能性特征可以包括但不限于:(i)多能干细胞形态;(ii)无限自我更新的潜力;(iii)包括但不限于ssea1(仅小鼠)、ssea3/4、ssea5、tra1-60/81、tra1-85、tra2-54、gctm-2、tg343、tg30、cd9、cd29、cd133/prominin、cd140a、cd56、cd73、cd90、cd105、oct4、nanog、sox2、cd30和/或cd50的多能干细胞标记的表达;(iv)分化为所有三个体细胞谱系(外胚层、中胚层和内胚层)的能力;(v)由三个体细胞谱系组成的畸胎瘤形成;以及(vi)由来自三个体细胞谱系的细胞组成的胚状体的形成。
[0242]
在一些情形中,干细胞(例如,esc或ipsc)可以被遗传修饰以生成(例如,诱导分化为)cd34 造血干细胞。干细胞可以被遗传修饰以在诱导的造血干细胞分化之前、之后或期间表达任一种如本文所公开的异源多肽(例如,细胞因子、受体等)。干细胞可以被遗传修饰以在诱导的造血干细胞分化之前、之后或期间降低任一种如本文所公开的内源基因或多肽(例如,细胞因子、受体等)的表达或活性。在一些情形中,这样的遗传修饰的cd34 造血干细胞是任一种本公开文本的工程化的免疫细胞或是其来源。
[0243]
在一些例子中,如本文所公开的干细胞可以在apel培养基中培养以分化为cd34 造血干细胞,所述apel培养基含有rocki(y-27632)(例如,约10微摩尔(μm))、scf(例如,约40纳克/毫升(ng/ml)培养基)、vegf(例如,约20ng/ml培养基)以及bmp-4(例如,约20ng/ml培养基)。
[0244]
在一些情形中,cd34 造血干细胞(例如,遗传修饰具有任一种本公开文本的工程化的免疫细胞的一种或多种特征)可以被诱导以分化为定型的免疫细胞,如t细胞或nk细胞。因此,在一些情形中,诱导的分化过程生成任一种本公开文本的工程化的nk细胞。
[0245]
在一些例子中,在il-3(例如,约5ng/ml)、il-7(例如,约20ng/ml)、il-15(例如,约10ng/ml)、scf(例如,约20ng/ml)以及flt3l(例如,约10ng/ml)的存在下培养遗传修饰的cd34 造血干细胞以分化为cd45 nk细胞。
[0246]
在一些情形中,可以使用透气性快速扩增(g-rex)平台在培养中,例如,在包含il-2、mbil-21aapc的培养基中扩增cd45 nk细胞。
[0247]
在一些情形中,如本文所公开的源自ipsc的nk细胞可以与包括il-2、il-15或il-21的一种或多种异源细胞因子一起培养。在一些情形中,如本文所公开的源自ipsc的nk细胞可以与选自il-2、il-15和il-21的一种或多种异源细胞因子一起培养(例如,用于细胞扩增)。在一些情形中,如本文所公开的源自ipsc的nk细胞可以与选自il-2、il-15和il-21的两种或更多种异源细胞因子(例如,il-2和il-15、il-2和il-21或者il-15和il-21)同时或以任何顺序依序一起培养。在一些情形中,如本文所公开的源自ipsc的nk细胞可以与il-2、il-15和il-21中的全部同时或以任何顺序依序一起培养。
[0248]
f.基因编辑或遗传物质递送
[0249]
如本文所公开的基因编辑部分可以包括crispr相关多肽(cas)、锌指核酸酶(zfn)、锌指相关基因调节多肽、转录激活物样效应子核酸酶(talen)、转录激活物样效应子相关基因调节多肽、兆核酸酶、天然主转录因子、表观遗传修饰酶、重组酶、翻转酶、转座酶、
rna结合蛋白(rbp)、argonaute蛋白、其任何衍生物、其任何变体或其任何片段。在一些实施方案中,致动器部分包含cas蛋白,并且系统还包含与cas蛋白复合的指导rna(grna)。在一些实施方案中,致动器部分包含与grna复合的rbp,所述grna能够与cas蛋白形成复合物。在一些实施方案中,grna包含展现与靶多核苷酸的至少80%序列同一性的靶向区段。在一些实施方案中,cas蛋白基本上缺乏dna切割活性。
[0250]
在一些情形中,合适的基因编辑部分包括crispr相关(cas)蛋白或cas核酸酶,包括i型crispr相关(cas)多肽、ii型crispr相关(cas)多肽、iii型crispr相关(cas)多肽、iv型crispr相关(cas)多肽、v型crispr相关(cas)多肽和vi型crispr相关(cas)多肽;锌指核酸酶(zfn);转录激活物样效应子核酸酶(talen);兆核酸酶;rna结合蛋白(rbp);crispr相关rna结合蛋白;重组酶;翻转酶;转座酶;argonaute(ago)蛋白(例如,原核argonaute(pago)、古细菌argonaute(aago)和真核argonaute(eago));其任何衍生物、其任何变体;及其任何片段。
[0251]
cas蛋白的非限制性例子包括c2c1、c2c2、c2c3、cas1、cas1b、cas2、cas3、cas4、cas5、cas5e(casd)、cas6、cas6e、cas6f、cas7、cas8a、cas8a1、cas8a2、cas8b、cas8c、cas9(csn1或csx12)、cas10、cas10d、cas1o、cas1od、casf、casg、cash、cpf1、csy1、csy2、csy3、cse1(casa)、cse2(casb)、cse3(case)、cse4(casc)、csc1、csc2、csa5、csn2、csm2、csm3、csm4、csm5、csm6、cmr1、cmr3、cmr4、cmr5、cmr6、csb1、csb2、csb3、csx17、csx14、csx1o、csx16、csax、csx3、csx1、csx15、csf1、csf2、csf3、csf4和cul966,以及其同系物或修饰形式。
[0252]
在一些情形中,如本文所公开的基因编辑部分可以与另外的功能部分融合(例如,以形成融合部分),并且另外的功能部分的功能的非限制性例子可以包括甲基转移酶活性、去甲基化酶活性、歧化酶活性、烷基化活性、脱嘌呤活性、氧化活性、嘧啶二聚体形成活性、整合酶活性、转座酶活性、重组酶活性、聚合酶活性、连接酶活性、解旋酶活性、光裂合酶活性或糖苷酶活性、乙酰转移酶活性、脱乙酰酶活性、激酶活性、磷酸酶活性、泛素连接酶活性、脱泛素化活性、腺苷酸化活性、脱腺苷酸化活性、sumo化活性、脱sumo化活性、核糖基化活性、脱核糖基化活性、豆蔻酰化活性、重塑活性、蛋白酶活性、氧化还原酶活性、转移酶活性、水解酶活性、裂解酶活性、异构酶活性、合酶活性、合成酶活性和脱豆蔻酰化活性。例如,融合蛋白可以是cas蛋白以及效应子或阻遏蛋白功能部分中的融合物。
[0253]
可替代地或另外地,异源遗传物质的基因编辑(例如,敲入)或递送可以通过其他基于病毒和非病毒的基因转移方法来实现,所述方法可以用于在宿主细胞(例如,如本文所公开的干细胞、造血干细胞等)中引入核酸。这样的方法可以用于将编码本公开文本的多肽分子的核酸施用至培养中(或宿主生物体中)的细胞。病毒载体递送系统可以包括dna和rna病毒,其可以在递送至细胞后具有附加的或整合的基因组。非病毒载体递送系统可以包括dna质粒、rna(例如本文所述载体的转录物)、裸核酸以及与递送媒介物如脂质体复合的核酸。
[0254]
基于rna或dna病毒的系统可以用于靶向特定细胞并且将病毒有效载荷运输至细胞核。病毒载体可以用于在体外处理细胞,并且可以任选地施用(离体)修饰的细胞。可替代地,可以将病毒载体直接(在体内)施用至受试者。基于病毒的系统可以包括用于基因转移的逆转录病毒、慢病毒、腺病毒、腺相关病毒和单纯疱疹病毒载体。在宿主基因组中的整合
可以用逆转录病毒、慢病毒和腺相关病毒基因转移方法来进行,所述方法可以导致所插入基因的长期表达。
[0255]
核酸的非病毒递送方法可以包括脂转染、核转染、显微注射、基因枪、病毒体、脂质体、免疫脂质体、聚阳离子或脂质:核酸缀合物、裸dna、人工病毒粒子以及dna的药剂增强摄取。可以使用适合于多核苷酸的有效受体识别脂转染的阳离子和中性脂质。
[0256]
可替代地或另外地,反义寡核苷酸可以用于抑制或沉默靶基因表达。反义寡核苷酸的非限制性例子可以包括短发夹rna(shrna)、微rna(mirna)和小干扰rna(sirna)。
[0257]
g.共疗法
[0258]
本公开文本的工程化的免疫细胞(例如,工程化的nk细胞)可以与共治疗剂组合以治疗有需要的受试者。在一些情形中,可以在将共治疗剂施用至受试者之前、同时或之后将工程化的免疫细胞施用至受试者。
[0259]
在一方面,本公开文本提供一种组合物,其包含(a)任一种本文所公开的工程化的免疫细胞(例如,工程化的nk细胞)和(b)共治疗剂(即,单独治疗剂)(例如,抗体,如抗cd20抗体或抗pd1抗体)。在一些情形中,工程化的免疫细胞可以包含以下中的一种或多种:(i)如本文所公开的异源细胞因子(例如,异源il,如il-15),(ii)如本文所公开的用于增强的cd16信号传导的cd16变体,以及(iii)如本文所公开的包含能够与抗原结合的抗原结合部分的嵌合多肽受体。在一些例子中,共治疗剂包括抗cd20抗体。
[0260]
在一些情形中,工程化的免疫细胞可以包含如本文所公开的异源细胞因子(例如,il-15)以及以下中的一种或两种:(ii)用于增强的cd16信号传导的cd16变体,以及(iii)包含抗原结合部分的嵌合多肽受体。
[0261]
在一些情形中,工程化的免疫细胞可以包含用于增强的cd16信号传导的cd16变体以及以下中的一种或两种:(i)异源细胞因子(例如,il-15),和(iii)包含抗原结合部分的嵌合多肽受体。
[0262]
在一些情形中,工程化的免疫细胞可以包含含有抗原结合部分的嵌合多肽受体以及以下中的一种或两种:(i)异源细胞因子(例如,il-15),和(ii)用于增强的cd16信号传导的cd16变体。
[0263]
共治疗剂的非限制性例子可以包括细胞毒性剂、化学治疗剂、生长抑制剂、用于放射疗法的药剂、抗血管发生剂、凋亡剂、抗微管蛋白剂以及用于治疗癌症的其他药剂,例如,抗cd20抗体、抗pd1抗体(例如,派姆单抗)、源自血小板的生长因子抑制剂(例如,gleevec
tm
(甲磺酸伊马替尼))、cox-2抑制剂(例如,塞来昔布)、干扰素、细胞因子、与以下靶标pdgfr-β、blys、april、一种或多种bcma受体中的一种或多种结合的拮抗剂(例如,中和抗体)、trail/apo2、其他生物活性剂和有机化学剂等。
[0264]
术语“细胞毒性剂”通常是指抑制或阻止细胞功能和/或引起对细胞的破坏的物质。细胞毒性剂的非限制性例子可以包括放射性同位素(例如,at211、i131、i125、y90、re186、re188、sm153、bi212、p32以及lu的放射性同位素)、化学治疗剂(例如,氨甲蝶呤、亚德里亚霉素、长春花生物碱(长春花新碱、长春花碱、依托泊苷)、多柔比星、美法仑、丝裂霉素c、苯丁酸氮芥、道诺霉素或其他嵌入剂)、酶及其片段如溶核酶、抗生素,以及细菌、真菌、植物或动物来源的毒素,如小分子毒素或酶活性毒素。
[0265]
化学治疗剂的非限制性例子可以包括烷基化剂,如噻替派(thiotepa)和
propionate)、表硫雄醇(epitiostanol)、美雄烷(mepitiostane)、睾内酯;抗肾上腺,如氨鲁米特(aminoglutethimide)、米托坦(mitotane)、曲洛司坦(trilostane);叶酸补充剂,如亚叶酸;乙酰葡醛酯;醛磷酰胺糖苷;氨基乙酰丙酸(aminolevulinic acid);恩尿嘧啶(eniluracil);安吖啶(amsacrine);阿莫司汀(bestrabucil);比生群(bisantrene);依达曲沙(edatraxate);去氧胺(defofamine);地美可辛(demecolcine);地吖醌(diaziquone);依氟尼丁(elfornithine);依利醋铵(elliptinium acetate);埃博霉素(epothilone);依托格鲁(etoglucid);硝酸镓;羟基脲;香菇多糖(lentinan);氯尼达明(lonidainine);类美登素,如美登素(maytansine)和安丝菌素(ansamitocin);米托胍腙(mitoguazone);米托蒽醌(mitoxantrone);莫坦莫尔(mopidanmol);耐曲瑞(nitraerine);喷司他汀(pentostatin);蛋氨氮芥(phenamet);吡柔比星(pirarubicin);洛索蒽醌(losoxantrone);2-乙基酰肼;甲基苄肼(procarbazine);多糖复合物(美国俄勒冈州尤金市的jhs natural products);雷佐生(razoxane);根霉菌素(rhizoxin);西索菲兰(sizofiran);锗螺胺(spirogermanium);细交链孢菌酮酸(tenuazonic acid);三亚胺醌(triaziquone);2,2',2
”‑
三氯三乙胺;单端孢霉烯族毒素(尤其是t-2毒素、维拉库林a(verracurin a)、漆斑菌素a(roridin a)和蛇形菌素(anguidine));尿烷;长春地辛(vindesine);达卡巴嗪(dacarbazine);甘露醇氮芥(mannomustine);二溴甘露醇(mitobronitol);二溴卫矛醇(mitolactol);哌泊溴烷(pipobroman);加司特新(gacytosine);阿糖胞苷(“ara-c”);噻替派(thiotepa);类紫杉醇(taxoid),例如紫杉烷,包括太平洋紫杉醇(新泽西州普林斯顿市的bristol-myers squibb oncology)、abraxane
tm
不含聚氧乙烯蓖麻油的太平洋紫杉醇的经白蛋白工程化的纳米颗粒配制品(伊利诺伊州康堡市的american pharmaceutical partners)和多西他赛(docetaxel)(法国安东尼市的 rorer);苯丁酸氮芥(chloranbucil);吉西他滨(gemcitabine)();6-硫鸟嘌呤;巯基嘌呤;甲氨蝶呤;铂类似物,如顺铂和卡铂;长春花碱();铂;依托泊苷(vp-16);异环磷酰胺;米托蒽醌;长春新碱();奥沙利铂(oxaliplatin);亚叶酸;长春瑞滨(vinorelbine)();盐酸米托恩醌(novantrone);依达曲沙(edatrexate);道诺霉素(daunomycin);氨基蝶呤(aminopterin);伊班膦酸盐(ibandronate);拓扑异构酶抑制剂rfs 2000;二氟甲基鸟氨酸(dmfo);类视黄醇,如视黄酸;卡培他滨(capecitabine)();以上任一种药物的药学上可接受的盐、酸或衍生物;以及上述两种或多种的组合,如chop,其为环磷酰胺、多柔比星、长春新碱和泼尼松龙(prednisolone)的组合疗法的缩写,和folfox,其为使用奥沙利铂(eloxatin
tm
)与5-fu和醛氢叶酸的组合的治疗方案的缩写。另外的化学治疗剂包括用作抗体药物缀合物的细胞毒性剂,例如,如类美登素(例如,dm1)和奥瑞他汀mmae和mmaf。
[0266]
化学治疗剂的例子还可以包括“抗激素剂”或“内分泌治疗剂”,其作用以调节、降低、阻断或抑制可以促进肿瘤生长的激素的作用,并且通常呈系统或全身治疗的形式。它们可以是激素本身。例子包括抗雌激素和选择性雌激素受体调节剂(serm),包括例如他莫昔芬(tamoxifen)(包括他莫昔芬)、雷洛昔芬(raloxifene)、屈洛昔芬(droloxifene)、4-羟基他莫昔芬、曲沃昔芬(trioxifene)、凯奥昔芬(keoxifene)、ly117018、奥那司酮(onapristone)和托瑞米芬(toremifene);抗黄体酮;雌
激素受体下调剂(erd);用于抑制或关闭卵巢的药剂,例如促黄体生成激素释放激素(lhrh)激动剂,如和eligard乙酸亮丙瑞林(leuprolide acetate)、乙酸戈舍瑞林(goserelin acetate)、乙酸布舍瑞林(buserelin acetate)和曲普瑞林(tripterelin);其他抗雄激素,如氟他胺(flutamide)、尼鲁米特(nilutamide)和比卡鲁胺(bicalutamide);以及抑制调节肾上腺中雌激素产生的酶芳香酶的芳香酶抑制剂,如例如4(5)-咪唑、氨鲁米特(aminoglutethimide)、乙酸甲地孕酮(megestrol acetate)、依西美坦(exemestane)、福美司坦(formestane)、法曲唑(fadrozole)、伏氯唑(vorozole)、来曲唑(letrozole)以及阿那曲唑(anastrozole)。另外,这样定义的化学治疗剂包括双膦酸盐,如氯膦酸盐(clodronate)(例如,或)、依替膦酸盐(etidronate)、ne-58095、唑来膦酸(zoledronic acid)/唑来膦酸盐(zoledronate)、阿仑膦酸盐(alendronate)、帕米膦酸盐(pamidronate)、帕米膦酸盐(pamidronate)、替洛膦酸盐(tiludronate)或利塞膦酸盐(risedronate);以及曲沙他滨(troxacitabine)(1,3-二氧戊环核苷胞嘧啶类似物);反义寡核苷酸,特别是抑制参与异常细胞增殖的信号传导路径中的基因表达的反义寡核苷酸,如例如pkc-α、raf、h-ras和表皮生长因子受体(egfr);疫苗,如疫苗和基因治疗疫苗,例如疫苗、疫苗和疫苗;拓扑异构酶1抑制剂; rmrh;拉帕替尼二甲苯磺酸盐(erbb-2和egfr双酪氨酸激酶小分子抑制剂,也称为gw572016);以及上述任一种药物的药学上可接受的盐、酸或衍生物。
[0267]
化学治疗剂的例子还可以包括抗体,如阿仑单抗(campath)、贝伐珠单抗(,genentech);西妥昔单抗(,imclone);帕尼单抗(,amgen)、利妥昔单抗(,genentech/biogen idec)、帕妥珠单抗(,2c4,genentech)、曲妥珠单抗(,genentech)、托西莫单抗(bexxar、corixia)以及抗体药物缀合物、吉妥珠单抗奥佐米星(,wyeth)。作为与本发明的化合物组合的药剂具有治疗潜力的另外的人源化单克隆抗体包括:阿泊珠单抗、阿塞珠单抗、阿特利珠单抗、巴匹珠单抗、比伐珠单抗美坦辛、坎妥珠单抗美坦辛、西利珠单抗、培塞利珠单抗、西非妥珠单抗(cidfusituzumab)、西妥珠单抗(cidtuzumab)、达克珠单抗、依库珠单抗、依法利珠单抗、依帕珠单抗、厄利珠单抗、非姆珠单抗(femzumab)、芳妥珠单抗、吉妥珠单抗奥佐米星、奥英妥珠单抗、伊匹单抗、拉贝妥珠单抗、林妥珠单抗、马妥珠单抗、美泊珠单抗、莫维珠单抗、莫托维珠单抗(motovizumab)、那他珠单抗、尼妥珠单抗、诺维珠单抗(nolovizumab)、努马维珠单抗(numavizumab)、奥瑞珠单抗、奥马珠单抗、帕利珠单抗、帕考珠单抗、培妥珠单抗(pecfusituzumab)、派妥珠单抗(pectuzumab)、培珠单抗、雷维珠单抗(ralivizumab)、雷珠单抗、瑞珠单抗(reslivizumab)、瑞替珠单抗、瑞西单抗(resyvizumab)、罗维珠单抗、卢利珠单抗、西罗珠单抗、西利珠单抗、索土珠单抗、他卡珠单抗泰坦、他多昔珠单抗、他利珠单抗、替非珠单抗、托珠单抗、托拉珠单抗、托妥珠单抗西莫白介素、图库西珠单抗(tucusituzumab)、乌玛珠单抗(umavizumab)、乌妥珠单抗、乌司奴单抗、维西珠单抗,以及抗白介素-12(abt-874/j695,wyeth research and abbott laboratories,其为被遗传修饰以识别白介素-12p40蛋白的重组的仅人序列的全长igg1λ抗体)。
[0268]
化学治疗剂的例子还可以包括“酪氨酸激酶抑制剂”,如egfr靶向剂(例如,小分子、抗体等);小分子her2酪氨酸激酶抑制剂,如可从takeda获得的tak165;cp-724,714,一种erbb2受体酪氨酸激酶的口服选择性抑制剂(pfizer和osi);双重her抑制剂,如优先结合egfr但抑制her2和egfr过表达细胞二者的ekb-569(可从wyeth获得);拉帕替尼(gsk572016;可从glaxo-smithkline获得),一种口服her2和egfr酪氨酸激酶抑制剂;pki-166(可从novartis获得);泛her抑制剂,如卡拉替尼(ci-1033;pharmacia);raf-1抑制剂,如可从isis pharmaceuticals获得的抑制raf-1信号传导的反义剂isis-5132;非her靶向的tk抑制剂,如甲磺酸伊马替尼(,可从glaxo smithkline获得);多靶向酪氨酸激酶抑制剂,如舒尼替尼(,可从pfizer获得);vegf受体酪氨酸激酶抑制剂,如瓦特拉尼(ptk787/zk222584,可从novartis/schering ag获得);mapk细胞外调节的激酶i抑制剂ci-1040(可从pharmacia获得);喹唑啉,如pd 153035,4-(3-氯代苯胺基)喹唑啉;吡啶并嘧啶;嘧啶并嘧啶;吡咯并嘧啶,如cgp 59326、cgp 60261和cgp 62706;吡唑并嘧啶,4-(苯胺基)-7h-吡咯并[2,3-d]嘧啶;姜黄素(二阿魏酰基甲烷,4,5-双(4-氟苯胺基)邻苯二甲酰亚胺);含有硝基噻吩部分的酪磷汀;pd-0183805(warner-lamber);反义分子(例如,结合至her编码核酸的那些);喹噁啉(美国专利号5,804,396);酪磷蛋白(tryphostin)(美国专利号5,804,396);zd6474(astra zeneca);ptk-787(novartis/schering ag);泛her抑制剂,如ci-1033(pfizer);affinitac(isis 3521;isis/lilly);甲磺酸伊马替尼();pki 166(novartis);gw2016(glaxo smithkline);ci-1033(pfizer);ekb-569(wyeth);司马沙尼(pfizer);zd6474(astrazeneca);ptk-787(novartis/schering ag);inc-1c11(imclone);以及雷帕霉素(西罗莫司,)。
[0269]
化学治疗剂的例子还可以包括地塞米松、干扰素、秋水仙素、氯苯氨啶(metoprine)、环孢菌素、两性霉素、甲硝唑、阿仑单抗、阿利维a酸、别嘌呤醇、氨磷汀、三氧化二砷、天冬酰胺酶、活bcg、贝伐单抗(bevacuzimab)、贝沙罗汀、克拉屈滨、氯法拉滨、达依泊汀α、地尼白介素、右雷佐生、阿法依泊汀、埃罗替尼、非格司亭、醋酸组氨瑞林、替伊莫单抗(ibritumomab)、干扰素α-2a、干扰素α-2b、来那度胺、左旋咪唑、美司钠、甲氧沙林、苯丙酸诺龙、奈拉滨、诺菲单抗(nofetumomab)、奥普瑞白介素、帕利夫明、帕玛二磷酸、培加酶(pegademase)、培门冬酶、培非司亭、培美曲塞二钠、普卡霉素、卟吩姆钠、奎那克林、拉布立酶、沙格司亭、替莫唑胺、vm-26、6-tg、托瑞米芬、维甲酸、atra、戊柔比星、唑来膦酸酯和唑来膦酸及其药学上可接受的盐。
[0270]
化学治疗剂的例子还可以包括氢化可的松(hydrocortisone)、醋酸氢化可的松(hydrocortisoneacetate)、醋酸可的松(cortisone acetate)、替可的松匹伐酯(tixocortol pivalate)、曲安奈德(triamcinolone acetonide)、曲安西龙醇(triamcinolone alcohol)、莫米松(mometasone)、安西奈德(amcinonide)、布地奈德(budesonide)、地奈德(desonide)、醋酸氟轻松(fluocinonide)、氟轻松(fluocinolone acetonide)、倍他米松(betamethasone)、倍他米松磷酸钠(betamethasone sodium phosphate)、地塞米松(dexamethasone)、地塞米松磷酸钠(dexamethasone sodium phosphate)、氟可龙(fluocortolone)、氢化可的松-17-丁酸盐(hydrocortisone-17-butyrate)、氢化可的松-17-戊酸盐(hydrocortisone-17-valerate)、二丙酸氯米松(aclometasone dipropionate)、戊酸倍他米松(betamethasone valerate)、二丙酸倍他米
8-(羟基乙酰基)-1-甲氧基-5,12-萘并萘二酮)、表柔比星、道诺霉素、依托泊苷和博来霉素。停滞g1的那些药剂也溢出至s期停滞中,例如,dna烷化剂,如他莫昔芬、泼尼松、达卡巴嗪、氮芥、顺铂、氨甲蝶呤、5-氟尿嘧啶和ara-c。紫杉烷(紫杉醇和多西他赛)都是源自紫杉树的抗癌药。源自欧洲紫衫的多西他赛(,rhone-poulenc rorer公司)是紫杉醇(,bristol-myers squibb公司)的半合成类似物。紫杉醇和多西他赛促进从微管蛋白二聚体组装呈微管并且通过防止解聚来稳定微管,从而导致抑制细胞的有丝分裂。
[0272]
h.使用方法
[0273]
本公开文本的工程化的免疫细胞(例如,工程化的nk细胞)可以使用(例如,施用)以治疗有需要的受试者。受试者可能患有或者可能怀疑患有病症,如疾病(例如,癌症、肿瘤、组织变性、纤维化等)。细胞(例如,干细胞或定型成体细胞)可以从受试者获得,并且可以将这样的细胞离体培养并遗传修饰以生成如本文所公开的任何受试工程化免疫细胞(例如,任何工程化的nk细胞)。随后,可以将工程化的免疫细胞施用至受试者用于适应性免疫疗法。
[0274]
受试者可以用本公开文本的工程化的免疫细胞(例如,工程化的nk细胞)的群体进行治疗(例如,施用)持续至少或多达约1个剂量、至少或多达约2个剂量、至少或多达约3个剂量、至少或多达约4个剂量、至少或多达约5个剂量、至少或多达约6个剂量、至少或多达约7个剂量、至少或多达约8个剂量、至少或多达约9个剂量或者至少或多达约10个剂量。
[0275]
在一方面,本公开文本提供一种包括以下的方法:(a)从受试者获得细胞;以及(b)从所述细胞生成任一种本文所公开的工程化的免疫细胞(例如,工程化的nk细胞)。在一些情形中,从受试者获得的细胞是esc。在一些情形中,将从受试者获得的细胞(例如,成纤维细胞,如成体皮肤成纤维细胞)修饰并转化为ipsc。
[0276]
在一方面,本公开文本提供一种方法,其包括向有需要的受试者施用包含任一种本文所公开的工程化的免疫细胞(例如,工程化的nk细胞)的nk细胞的群体。在一些情形中,所述方法还可以包括向所述受试者施用共治疗剂(例如,化学治疗剂、抗cd20抗体等)。
[0277]
在一方面,本公开文本提供一种方法,其包括向有需要的受试者施用任一种本文所公开的组合物。在一些情形中,所述组合物可以包含(i)任一种本文所公开的工程化的免疫细胞(例如,工程化的nk细胞)以及(ii)共治疗剂(例如,化学治疗剂、抗cd20抗体等)。
[0278]
任一种本文所公开的方法可以用于治疗受试者的靶细胞、靶组织、靶病症或靶疾病。
[0279]
靶疾病可以是病毒、细菌和/或寄生虫感染;炎性和/或自身免疫性疾病;或者赘生物,如癌症和/或肿瘤。
[0280]
靶细胞可以是患病细胞。患病细胞可以具有改变的代谢、基因表达和/或形态学特征。患病细胞可以是癌细胞、糖尿病细胞和凋亡细胞。患病细胞可以是来自患病受试者的细胞。示例性疾病可以包括血液障碍、癌症、代谢障碍、眼部障碍、器官障碍、肌肉骨骼障碍、心脏病等。
[0281]
可以使用任一种本文所公开的工程化的免疫细胞(例如,工程化的nk细胞)杀伤多种靶细胞。靶细胞可以包括众多种细胞类型。靶细胞可以是体外的。靶细胞可以是体内的。靶细胞可以是离体的。靶细胞可以是分离的细胞。靶细胞可以使生物体内部的细胞。靶细胞可以是生物体。靶细胞可以是细胞培养中的细胞。靶细胞可以是细胞集合中的一种。靶细胞
可以是哺乳动物细胞或源自哺乳动物细胞。靶细胞可以是啮齿动物细胞或源自啮齿动物细胞。靶细胞可以是人细胞或源自人细胞。靶细胞可以是原核细胞或源自原核细胞。靶细胞可以是细菌细胞或可以源自细菌细胞。靶细胞可以是古细菌细胞或源自古细菌细胞。靶细胞可以是真核细胞或源自真核细胞。靶细胞可以是多能干细胞。靶细胞可以是植物细胞或源自植物细胞。靶细胞可以是动物细胞或源自动物细胞。靶细胞可以是无脊椎动物细胞或源自无脊椎动物细胞。靶细胞可以是脊椎动物细胞或源自脊椎动物细胞。靶细胞可以是微生物细胞或源自微生物细胞。靶细胞可以是真菌细胞或源自真菌细胞。靶细胞可以来自特定器官或组织。
[0282]
靶细胞可以是干细胞或祖细胞。靶细胞可以包括干细胞(例如,成体干细胞、胚胎干细胞、诱导多能干(ips)细胞)和祖细胞(例如,心脏祖细胞、神经祖细胞等)。靶细胞可以包括哺乳动物干细胞和祖细胞,包括啮齿动物干细胞、啮齿动物祖细胞、人干细胞、人祖细胞等。克隆细胞可以包括细胞的后代。靶细胞可以包含靶核酸。靶细胞可以在活的生物体中。靶细胞可以是遗传修饰的细胞。靶细胞可以是宿主细胞。
[0283]
靶细胞可以是全能干细胞,然而,在本公开文本的一些实施方案中,可以使用术语“细胞”,但可能不是指全能干细胞。靶细胞可以是植物细胞,但是在本公开文本的一些实施方案中,可以使用术语“细胞”,但可能不是指植物细胞。靶细胞可以是多能细胞。例如,靶细胞可以是多能造血细胞,其可以分化为造血细胞谱系中的其他细胞,但是可能不能分化为任何其他非造血细胞。靶细胞可能能够发育为完整生物体。靶细胞可能能够或者可能不能发育为完整生物体。靶细胞可以是完整生物体。
[0284]
靶细胞可以是原代细胞。例如,可以将原代细胞的培养物传代0次、1次、2次、4次、5次、10次、15次或更多次。细胞可以是单细胞生物体。细胞可以在培养中生长。
[0285]
靶细胞可以是患病细胞。患病细胞可以具有改变的代谢、基因表达和/或形态学特征。患病细胞可以是癌细胞、糖尿病细胞和凋亡细胞。患病细胞可以是来自患病受试者的细胞。示例性疾病可以包括血液障碍、癌症、代谢障碍、眼部障碍、器官障碍、肌肉骨骼障碍、心脏病等。
[0286]
如果靶细胞是原代细胞,那么可以通过任何方法从个体收获它们。例如,白细胞可以通过单采术、白细胞单采术、密度梯度分离等来收获。来自诸如皮肤、肌肉、骨髓、脾、肝、胰腺、肺、肠、胃等组织的细胞可以通过活检来收获。可以使用适当的溶液用于所收获细胞的分散或悬浮。这样的溶液通常可以是平衡盐溶液,(例如生理盐水、磷酸盐缓冲盐水(pbs)、汉克平衡盐溶液等),便捷地补充有胎牛血清或其他天然存在的因子,与可接受的缓冲液以低浓度结合。缓冲液可以包括hepes、磷酸盐缓冲液、乳酸盐缓冲液等。可以立即使用细胞,或者可以将其储存(例如,通过冷冻)。可以使冷冻的细胞解冻,并且可能能够被再次使用。可以在dmso、血清、培养基缓冲液(例如,10%dmso、50%血清、40%缓冲培养基)和/或用于在冷冻温度下保存细胞的一些其他这样的常用溶液中冷冻细胞。
[0287]
可以作为靶细胞的细胞的非限制性例子包括但不限于淋巴样细胞,如b细胞、t细胞(细胞毒性t细胞、自然杀伤t细胞、调节t细胞、t辅助细胞)、自然杀伤细胞、细胞因子诱导的杀伤(cik)细胞(参见例如us20080241194);髓样细胞,如粒细胞(嗜碱性粒细胞、嗜酸性粒细胞、嗜中性粒细胞/多分叶核嗜中性粒细胞)、单核细胞/巨噬细胞、红细胞(网织红细胞)、肥大细胞、血小板/巨核细胞、树突细胞;来自内分泌系统的细胞,包括甲状腺(甲状腺
上皮细胞、滤泡旁细胞)、甲状旁腺(甲状旁腺主细胞、甲状旁腺嗜酸细胞)、肾上腺(嗜铬细胞)、松果体(松果体细胞)细胞;神经系统的细胞,包括神经胶质细胞(星形胶质细胞、小胶质细胞)、大细胞神经分泌细胞、星形细胞、伯特歇尔细胞和垂体(促性腺激素细胞、促皮质激素细胞、促甲状腺素细胞、促体素细胞、促乳素细胞);呼吸系统的细胞,包括肺细胞(i型肺细胞、ii型肺细胞)、克拉拉细胞、杯形细胞、尘细胞;循环系统的细胞,包括心肌细胞、周细胞;消化系统的细胞,包括胃(胃主细胞、周缘细胞)、杯形细胞、帕内特细胞、g细胞、d细胞、ecl细胞、i细胞、k细胞、s细胞;肠内分泌细胞,包括肠嗜铬细胞、apud细胞、肝(肝细胞、肝巨噬细胞)、软骨/骨/肌肉;骨细胞,包括成骨细胞、骨细胞、破骨细胞、牙(成牙骨质细胞、成釉质细胞);软骨细胞,包括成软骨细胞、软骨细胞;皮肤细胞,包括毛细胞、角质形成细胞、黑色素细胞(痣细胞);肌肉细胞,包括肌细胞;泌尿系统细胞,包括足细胞、球旁细胞、球内系膜细胞/球外系膜细胞、肾近端小管刷状缘细胞、致密斑细胞;繁殖系统细胞,包括精子、支持细胞、睾丸间质细胞、卵子;以及其他细胞,包括脂肪细胞、成纤维细胞、腱细胞、表皮角质形成细胞(分化表皮细胞)、表皮基细胞(干细胞)、指甲和趾甲的角质形成细胞、甲床基细胞(干细胞)、髓毛干细胞、皮质毛干细胞、角质层毛干细胞、角质层毛根鞘细胞、赫胥黎层的毛根鞘细胞、亨勒层的毛根鞘细胞、外毛根鞘细胞、毛母质细胞(干细胞)、湿分层屏障上皮细胞、角膜、舌、口腔、食道、肛管、远端尿道和阴道的复层扁平上皮的表面上皮细胞、角膜、舌、口腔、食道、肛管、远端尿道和阴道的上皮的基细胞(干细胞)、尿道上皮细胞(衬层膀胱和尿管)、外分泌分泌型上皮细胞、唾液腺粘液细胞(富含多糖的分泌)、唾液腺浆液细胞(富含糖蛋白酶的分泌)、舌中的冯
·
埃布纳腺细胞(清洗味蕾)、乳腺细胞(乳汁分泌)、泪腺细胞(泪液分泌)、耳中的耵聍腺细胞(蜡分泌)、外泌汗腺暗细胞(糖蛋白分泌)、外泌汗腺透明细胞(小分子分泌)。顶泌汗腺细胞(有气味的分泌、性激素敏感的)、眼睑中的莫尔腺细胞(特化的汗腺)、皮脂腺细胞(富含脂质的皮脂分泌)、鼻中的鲍曼腺细胞(清洗嗅上皮)、十二指肠中的布伦纳腺细胞(酶和碱性粘液)、精囊细胞(分泌精液组分,包括用于游动精子的果糖)、前列腺细胞(分泌精液组分)、尿道球腺细胞(粘液分泌)、巴氏腺细胞(阴道润滑物分泌)、利特雷腺细胞(粘液分泌)、子宫内膜细胞(碳水化合物分泌)、呼吸道和消化道的分离的杯形细胞(粘液分泌)、胃粘膜粘液细胞(粘液分泌)、胃腺胃酶细胞(胃蛋白酶原分泌)、胃腺壁细胞(盐酸分泌)、胰腺腺泡细胞(碳酸氢盐和消化酶分泌)、小肠的帕内特细胞(溶菌酶分泌)、肺的ii型肺细胞(表面活性剂分泌)、肺的克拉拉细胞、激素分泌细胞、垂体前叶细胞、促体素细胞、促乳素细胞、促甲状腺素细胞、促性腺激素细胞、促皮质激素细胞、垂体中叶细胞、大细胞神经分泌细胞、肠道和呼吸道细胞、甲状腺细胞、甲状腺上皮细胞、滤泡旁细胞、甲状旁腺细胞、甲状旁腺主细胞、甲状旁腺嗜酸细胞、肾上腺细胞、嗜铬细胞、睾丸的莱迪希细胞、卵泡的内膜细胞、破裂卵泡的黄体细胞、颗粒黄体细胞、卵泡膜黄体细胞、球旁细胞(肾素分泌)、肾的致密斑细胞、代谢和储存细胞、屏障功能细胞(肺、肠、外分泌腺和泌尿生殖道)、肾、i型肺细胞(肺的内衬气腔)、胰管细胞(泡心细胞)、无横纹管细胞(汗腺、唾液腺、乳腺等的)、管细胞(精囊、前列腺等的)、上皮细胞衬层封闭的内部体腔、具有推进功能的纤毛细胞、细胞外基质分泌细胞、收缩细胞;骨骼肌细胞、干细胞、心肌细胞、血液和免疫系统细胞、红细胞(红血球)、巨核细胞(血小板前体)、单核细胞、结缔组织巨噬细胞(各种类型)、表皮朗格汉斯细胞、破骨细胞(骨中)、树突细胞(淋巴组织中)、小神经胶质细胞(中枢神经系统中)、嗜中性粒细胞、嗜酸性粒细胞、嗜碱性粒细胞、肥大细胞、辅助t细胞、抑制t细
胞、细胞毒性t细胞、自然杀伤t细胞、b细胞、自然杀伤细胞、网织红细胞、血液和免疫系统的干细胞和定型祖细胞(各种类型)、多能干细胞、全能干细胞、诱导多能干细胞、成体干细胞、感觉传感器细胞、自主神经元细胞、感觉器官和周围神经元支持细胞、中枢神经系统神经元和神经胶质细胞、晶状体细胞、色素细胞、黑色素细胞、视网膜色素上皮细胞、生殖细胞、藏卵器/卵母细胞、精子细胞、精母细胞、精原细胞(精母细胞的干细胞)、精子、胸腺抚育细胞、卵泡细胞、支持细胞(睾丸中)、胸腺上皮细胞、间质细胞以及间质肾细胞。
[0288]
特别关注癌细胞。在一些实施方案中,靶细胞是癌细胞。癌细胞的非限制性例子包括癌症的细胞,所述癌症包括棘皮瘤、腺泡细胞癌、听神经瘤、肢端黑色素瘤、顶端螺旋瘤、急性嗜酸性粒细胞白血病、急性淋巴母细胞性白血病、急性巨核母细胞白血病、急性单核细胞白血病、伴随成熟的急性髓母细胞白血病、急性髓系树突细胞白血病、急性髓样白血病、急性早幼粒细胞白血病、釉质瘤、腺癌、腺样囊性癌、腺瘤、牙源性腺瘤样瘤、肾上腺皮质癌、成人t细胞白血病、侵袭性nk细胞白血病、aids相关癌症、aids相关淋巴瘤、软组织腺泡状肉瘤、成釉细胞纤维瘤、直肠癌、间变性大细胞淋巴瘤、未分化甲状腺癌、血管免疫母细胞性t细胞淋巴瘤、血管肌脂瘤、血管肉瘤、阑尾肿瘤、星形细胞瘤、非典型畸胎样横纹肌样瘤、基底细胞癌、基底样癌、b细胞白血病、b细胞淋巴瘤、贝里尼导管癌、胆道癌、膀胱癌、母细胞瘤、骨癌、骨瘤、脑干神经胶质瘤、脑瘤、乳腺癌、brenner瘤、支气管肿瘤、细支气管肺泡癌、棕色瘤、伯基特淋巴瘤、部位不明的转移癌、类癌瘤、上皮癌、原位癌、阴茎癌、原发灶不明癌、癌肉瘤、卡斯尔曼病、中枢神经系统胚胎瘤、小脑星形细胞瘤、大脑星形细胞瘤、宫颈癌、胆管上皮癌、软骨瘤、软骨肉瘤、脊索瘤、绒毛膜癌、脉络膜丛乳头状瘤、慢性淋巴细胞白血病、慢性单核细胞白血病、慢性髓性白血病、慢性骨髓增生病、慢性嗜中性白细胞白血病、透明细胞瘤、结肠癌、结直肠癌、颅咽管癌、皮肤t细胞淋巴瘤、德戈斯病、隆突性皮肤纤维肉瘤、皮样囊肿、结缔组织增生性小圆细胞肿瘤、弥漫性大b细胞淋巴瘤、胚胎发育不良性神经上皮肿瘤、胚胎性癌、内胚层窦瘤、子宫内膜癌、子宫内膜子宫癌、卵巢子宫内膜样瘤、肠病相关t细胞淋巴瘤、室管膜母细胞瘤、室管膜瘤、上皮样肉瘤、红白血病、食管癌、鼻腔神经胶质瘤、尤因肿瘤家族、尤因家族肉瘤、尤因肉瘤、颅外生殖细胞肿瘤、性腺外生殖细胞肿瘤、肝外胆管癌、乳腺外佩吉特病、输卵管癌、胎中胎、纤维瘤、纤维肉瘤、滤泡淋巴瘤、滤泡甲状腺癌、胆囊癌、胆囊癌、神经节神经胶质瘤、神经节瘤、胃癌、胃淋巴瘤、胃肠癌、胃肠类癌瘤、胃肠道间质瘤、胃肠道间质瘤、胚细胞瘤、生殖细胞瘤、妊娠性绒毛膜癌、妊娠滋养细胞肿瘤、骨巨细胞瘤、多形性胶质母细胞瘤、神经胶质瘤、大脑神经胶质瘤病、血管球瘤、胰高血糖素瘤、性腺母细胞瘤、粒层细胞瘤、多毛细胞白血病、多毛细胞白血病、头颈癌、头颈癌、心脏癌症、血管母细胞瘤、血管外皮细胞瘤、血管肉瘤、骨髓恶性肿瘤、肝细胞癌、肝脾t细胞淋巴瘤、遗传性乳腺癌卵巢癌综合征、霍奇金淋巴瘤、霍奇金淋巴瘤、下咽癌、下丘脑神经胶质瘤、炎性乳腺癌、眼球内黑色素瘤、胰岛细胞癌、胰岛细胞瘤、幼年型骨髓单核细胞性白血病、卡波西肉瘤、卡波西肉瘤、肾癌、klatskin瘤、krukenberg瘤、喉癌、喉癌、恶性雀斑样黑素瘤、白血病、白血病、唇和口腔癌、脂肪肉瘤、肺癌、黄体瘤、淋巴管瘤、淋巴管肉瘤、淋巴上皮瘤、淋巴样白血病、淋巴瘤、巨球蛋白血症、恶性纤维组织细胞瘤、恶性纤维组织细胞瘤、骨恶性纤维组织细胞瘤、恶性神经胶质瘤、恶性间皮瘤、恶性周围神经鞘瘤、恶性横纹肌杨瘤、恶性蝾螈瘤、malt淋巴瘤、套细胞淋巴瘤、肥大细胞白血病、纵隔生殖细胞瘤、纵隔肿瘤、甲状腺髓样癌、髓母细胞瘤、髓母细胞瘤、髓上皮瘤、黑色素瘤、黑色素瘤、脑膜瘤、merkel细
胞癌、间皮瘤、间皮瘤、转移性鳞状颈部癌症伴隐匿原发、转移性尿路上皮癌、苗勒型混合瘤、单核细胞性白血病、口腔癌、粘液性瘤、多发性内分泌肿瘤综合征、多发性骨髓瘤、多发性骨髓瘤、蕈样真菌病、蕈样真菌病、骨髓增生异常疾病、骨髓增生异常综合征、髓样白血病、髓样肉瘤、骨髓增殖性疾病、粘液瘤、鼻腔癌、鼻咽癌、鼻咽癌、肿瘤、神经鞘瘤、神经母细胞瘤、神经母细胞瘤、神经纤维瘤、神经瘤、结节性黑色素瘤、非霍奇金淋巴瘤、非霍奇金淋巴瘤、非黑色素瘤皮肤癌、非小细胞肺癌、眼部肿瘤、少突星形细胞瘤、少突神经胶质瘤、嗜酸粒细胞腺瘤、视神经鞘脑膜瘤、口癌、口癌、口咽癌、骨肉瘤、骨肉瘤、卵巢癌、卵巢癌、卵巢上皮癌、卵巢生殖细胞肿瘤、卵巢低恶性潜能肿瘤、乳房佩吉特病、肺上沟瘤、胰腺癌、胰腺癌、乳头状甲状腺癌、乳头状瘤病、副神经节瘤、鼻旁窦癌、甲状旁腺癌、阴茎癌、血管周上皮样细胞瘤、咽癌、嗜铬细胞瘤、中间分化的松果体实质瘤、松果体母细胞瘤、垂体细胞瘤、垂体腺瘤、垂体瘤、浆细胞瘤、胸膜肺母细胞瘤、多胚瘤、前体t淋巴母细胞淋巴瘤、原发性中枢神经系统淋巴瘤、原发性渗出性淋巴瘤、原发性肝细胞癌、原发性肝癌、原发性腹膜癌、原发性神经外胚层瘤、前列腺癌、腹膜假粘液瘤、直肠癌、肾细胞癌、涉及染色体15上的nut基因的呼吸道癌、视网膜母细胞瘤、横纹肌瘤、横纹肌肉瘤、里希特转化、骶尾部畸胎瘤、涎腺癌、肉瘤、施万细胞瘤病、皮脂腺癌、继发性肿瘤、精原细胞瘤、浆液性肿瘤、塞尔托利-莱迪希细胞瘤、性索间质瘤、sezary综合征、印戒细胞癌、皮肤癌、小蓝圆细胞瘤、小细胞癌、小细胞肺癌、小细胞淋巴瘤、小肠癌、软组织肉瘤、生长抑素瘤、煤烟疣、脊髓瘤、脊柱肿瘤、脾边缘带淋巴瘤、鳞状细胞癌、胃癌、浅表扩散性黑色素瘤、幕上原发性神经外胚层瘤、表面上皮间质瘤、滑膜肉瘤、t细胞急性淋巴母细胞性白血病、t细胞大颗粒淋巴细胞白血病、t细胞白血病、t细胞淋巴瘤、t细胞幼淋巴细胞白血病、畸胎瘤、终末淋巴癌、睾丸癌、泡膜细胞瘤、喉癌、胸腺癌、胸腺瘤、甲状腺癌、肾盂和输尿管移行细胞癌、移行细胞癌、脐尿管癌、尿道癌、泌尿生殖肿瘤、子宫肉瘤、葡萄膜黑色素瘤、阴道癌、弗纳-莫里森综合征、疣状癌、视觉通路神经胶质瘤、外阴癌、沃尔登斯特伦巨球蛋白血症、沃辛瘤、肾母细胞瘤及其组合。在一些实施方案中,所靶向的癌细胞表示癌细胞群体内的子群体,如癌症干细胞。在一些实施方案中,癌症属于造血谱系,如淋巴瘤。抗原可以是肿瘤相关抗原。
[0289]
在一些情形中,如本文所公开的靶细胞(例如,b细胞)与自身免疫性疾病相关或怀疑与其相关。用任一种本公开文本的工程化的免疫细胞(例如,工程化的nk细胞)治疗的受试者可能患有或者可能怀疑患有自身免疫性疾病。
[0290]
自身免疫性疾病的非限制性例子可以包括急性播散性脑脊髓炎(adem)、急性坏死性出血性白质脑炎、艾迪生病、无丙种球蛋白血症、过敏性哮喘、过敏性鼻炎、斑秃、淀粉样变性、强直性脊柱炎、抗体介导的移植排斥、抗gbm/抗tbm肾炎、抗磷脂综合征(aps)、自身免疫性血管性水肿、自身免疫性再生障碍性贫血、自身免疫性自主神经机能异常、自身免疫性肝炎、自身免疫性高脂血症、自身免疫性免疫缺陷、自身免疫性内耳疾病(aied)、自身免疫性心肌炎、自身免疫性胰腺炎、自身免疫性视网膜病变、自身免疫性血小板减少性紫癜(atp)、自身免疫性甲状腺疾病、自身免疫性荨麻疹、轴突和神经元神经病、巴洛病、贝切特氏病、大泡性类天泡疮、心肌病、卡斯尔曼病、乳糜泻、美洲锥虫病、慢性疲劳综合征、慢性炎性脱髓鞘性多发性神经病(cidp)、慢性复发性多病灶性骨髓炎(crmo)、变应性肉芽肿性血管炎、瘢痕性类天疱疮/良性粘膜类天疱疮、克罗恩病、cogan综合征、冷凝激素疾病、先天性心脏传导阻滞、柯萨奇病毒性心肌炎、crest疾病、特发性混合性冷球蛋白血症、脱髓鞘性神
经病、疱疹样皮炎、皮肌炎、德维克病(视神经脊髓炎)、盘状狼疮、心肌梗死后综合征、子宫内膜异位症、嗜酸细胞性筋膜炎、瓜藤缠、实验性过敏性脑脊髓炎、伊文思综合征、纤维肌痛、纤维化肺泡炎、巨细胞性动脉炎(颞动脉炎)、肾小球肾炎、肺出血肾炎综合征、肉芽肿性多血管炎(gpa)、格雷夫斯病、急性炎症性脱髓鞘性多发性神经病、桥本脑炎、桥本甲状腺炎、溶血性贫血、过敏性紫癜、妊娠疱疹、低丙球蛋白血症、高丙球蛋白血症、特发性血小板减少性紫癜(itp)、iga肾病、igg4相关硬化性疾病、免疫调节脂蛋白、包涵体肌炎、炎性肠病、胰岛素依赖型糖尿病(1型)、间质性膀胱炎、幼年型关节炎、幼年型糖尿病、川崎综合征、兰伯特-伊顿综合征、白细胞分裂性血管炎、扁平苔藓、硬化性苔藓、木样结膜炎、线性iga病(lad)、狼疮(sle)、莱姆病、梅尼埃病、显微镜下多血管炎、混合性结缔组织病(mctd)、未定性的单克隆丙球蛋白病(mgus)、蚕蚀性角膜溃疡、mucha-habermann病、多发性硬化症、重症肌无力、肌炎、发作性睡病、视神经脊髓炎(devic's)、中性粒细胞减少、眼部瘢痕性类天疱疮、视神经炎、复发性风湿病、pandas(与链球菌相关的小儿自身免疫性神经精神障碍)、副肿瘤性小脑变性、阵发性睡眠性血红蛋白尿(pnh)、帕-罗二氏综合征、parsonnage-turner综合征、睫状体扁平部炎(中间葡萄膜炎)、天疱疮、周围神经病、静脉周脑脊髓炎、恶性贫血、poems综合征、结节性多动脉炎、i型、ii型和iii型自身免疫性多内分泌腺综合征、风湿性多肌痛、多肌炎、心肌梗死后综合征、心包切开术后综合征、孕激素皮肤炎、原发性胆汁性肝硬化、原发性硬化性胆管炎、银屑病、银屑病关节炎、特发性肺纤维化、化脓性关节炎-坏疽性脓皮病-痤疮综合征、纯红细胞再生障碍、雷诺现象、反射性交感神经营养障碍、莱特尔综合征、复发性多软骨炎、下肢不宁综合征、腹膜后纤维化、风湿热、类风湿性关节炎、结节病、施密特综合征、巩膜炎、硬皮病、舍格伦综合征、精子和睾丸自身免疫、僵人综合征、亚急性细菌性心内膜炎(sbe)、susac综合征、交感性眼炎、大动脉炎、颞动脉炎/巨细胞性动脉炎、血小板减少性紫癜(ttp)、托洛萨-亨特综合征、横贯性脊髓炎、溃疡性结肠炎、未分化结缔组织病(uctd)、葡萄膜炎、血管炎、水泡大疱性皮肤病、白癜风、沃尔登斯特伦巨球蛋白血症(wm)以及韦氏肉芽肿病(肉芽肿性多血管炎(gpa))。
[0291]
在一些情形中,自身免疫性疾病包括选自以下的一个或多个成员:类风湿性关节炎、1型糖尿病、系统性红斑狼疮(狼疮或sle)、重症肌无力、多发性硬化症、硬皮病、艾迪生病、大疱性类天疱疮、寻常型天疱疮、吉兰-巴雷综合征、舍格伦综合征、皮肌炎、血栓性血小板减少性紫癜、高丙球蛋白血症、未定性的单克隆丙球蛋白病(mgus)、沃尔登斯特伦巨球蛋白血症(wm)、慢性炎性脱髓鞘多神经病(cidp)、桥本脑病(he)、桥本甲状腺炎、格雷夫斯病、韦氏肉芽肿病以及抗体介导的移植排斥(例如,对于组织移植物如肾移植物)。在例子中,自身免疫性疾病可以是1型糖尿病、狼疮或类风湿性关节炎。
[0292]
在一些情形中,靶疾病是t细胞白血病(tcl),如t细胞急性淋巴母细胞性白血病(t-all)。例如,可以将任一种本文所公开的工程化的免疫细胞(例如,工程化的nk细胞)施用至有需要的受试者以治疗tcl,所述免疫细胞包含以下中的一种或多种:(i)如本文所公开的包含能够与cd7结合的抗原结合结构域的嵌合多肽受体,(ii)如本文所公开的异源细胞因子(例如,il-15),以及(iii)编码与异源细胞因子相同的细胞因子(例如,内源cd7)的内源基因的降低的表达或活性。
[0293]
在一些情形中,靶疾病是急性髓样白血病(aml)。例如,可以将任一种本文所公开的工程化的免疫细胞(例如,工程化的nk细胞)施用至有需要的受试者以治疗aml,所述免疫
细胞包含以下中的一种或多种:(i)如本文所公开的包含能够与抗原(例如,cd33和/或cd123)结合的抗原结合结构域的嵌合多肽受体,(ii)如本文所公开的异源细胞因子(例如,il-15),以及(iii)如本文所公开的用于增强的cd16信号传导的cd16变体。
[0294]
在一些情形中,靶疾病是非霍奇金淋巴瘤(nhl)。
[0295]
在一些情形中,靶疾病是慢性淋巴细胞白血病(cll)。
[0296]
在一些情形中,靶疾病是b细胞白血病(bcl)。例如,可以将任一种本文所公开的工程化的免疫细胞(例如,工程化的nk细胞)施用至有需要的受试者以治疗bcl,所述免疫细胞包含以下中的一种或多种:(i)如本文所公开的包含能够与cd19结合的抗原结合结构域的嵌合多肽受体,(ii)如本文所公开的异源细胞因子(例如,il-15),以及(iii)如本文所公开的用于增强的cd16信号传导的cd16变体。
[0297]
在一些情形中,靶疾病是非小细胞肺癌(nsclc)。
[0298]
在一些情形中,靶细胞形成肿瘤(即,实体瘤)。用本文方法治疗的肿瘤可以导致稳定的肿瘤生长(例如,一个或多个肿瘤的大小增加不超过1%、5%、10%、15%或20%,和/或不转移)。在一些情形中,使肿瘤稳定至少约1、2、3、4、5、6、7、8、9、10、11、12或更多周。在一些情形中,使肿瘤稳定至少约1、2、3、4、5、6、7、8、9、10、11、12或更多个月。在一些情形中,使肿瘤稳定至少约1、2、3、4、5、6、7、8、9、10或更多年。在一些情形中,肿瘤的大小或肿瘤细胞的数量降低至少约5%、10%、15%、20%、25%、30%、35%、40%、45%、50%、55%、60%、65%、70%、75%、80%、85%、90%、95%或更多。在一些情形中,肿瘤被完全消除,或者减小至低于检测水平。在一些情形中,受试者在治疗后保持无肿瘤(例如在缓解中)至少约1、2、3、4、5、6、7、8、9、10、11、12或更多周。在一些情形中,受试者在治疗后保持无肿瘤至少约1、2、3、4、5、6、7、8、9、10、11、12或更多个月。在一些情形中,受试者在治疗后保持无肿瘤至少约1、2、3、4、5、6、7、8、9、10或更多年。实施例
[0299]
实施例1:工程化的nk细胞
[0300]
表1说明具有或不具有遗传修饰的工程化的nk细胞的实施例,以及可能的功能和治疗适应症。治疗适应症的例子可以包括急性髓样白血病(aml)、多发性骨髓瘤(mm)、骨髓增生异常综合征(mds)、b细胞白血病、t细胞白血病、实体瘤和血癌。
[0301]
如本文所公开的nk细胞可以通过工程化源自受试者的nk细胞来生成。可替代地,如本文所公开的nk细胞可以源自干细胞,如分离的干细胞(例如,胚胎干细胞)或诱导干细胞(例如,ipsc)。对于源自干细胞的nk细胞,如本文所公开的一个或多个遗传修饰可以在以下状态引入:(a)干细胞状态,(b)造血干细胞状态,和/或(c)nk细胞状态。又在另一替代方案中,如本文所公开的nk细胞可以是nk细胞系。表1
[0302]
实施例2:在肿瘤微环境(tme)中增强的功能
[0303]
对于在肿瘤微环境中改进的功能(例如,增殖、持久性、低免疫性、抗肿瘤活性等),可以将目的细胞工程化以携带(i)一种或多种增强的或引入的基因(例如,引入的转基因)和/或(ii)内源基因的一个或多个降低的表达水平(例如,目的基因的功能丧失)。内源基因的降低的表达水平可以通过例如crispp/cas和一种或多种指导核酸分子来诱导,如表3中提供的非限制性示例性指导rna序列。目的细胞可以是干细胞,如分离的干细胞(例如,胚胎干细胞)或诱导干细胞(例如,ipsc)。目的细胞可以是免疫细胞(例如,nk细胞)。这样的免疫细胞可以源自如本文所公开的干细胞。可替代地,这样的免疫可以是免疫细胞系(例如,nk细胞系)。
[0304]
例如,对于在肿瘤微环境中的改进的功能,可以将nk细胞工程化以携带某些转基因和/或目的基因的功能丧失,如表3中所示。表3:用于在肿瘤微环境中的增强的功能的指导rna序列
[0305]
klrd1的优化的转基因序列(seq id no.15):
[0306]
atggcggtgttcaaaacaacgctgtggcggctcatctctggcaccttgggcataatatgcttgtcccttatgtctactctcggcattctgctcaaaaatagcttcacgaagctgtctatagaacctgcgtttacccccggacccaacatcgagttgcagaaagactccgactgctgttcctgtcaagaaaaatgggtcggataccgatgcaactgttactttatttcctctgagcagaaaacctggaatgagagccgacatctgtgtgcaagtcagaagtctagccttttgcaattgcaaaacaccgacgagcttgacttcatgtcctcttcccaacaattctattggatcgggcttagctattccgaagagcacaccgcatggctttgggagaatgggagcgcactgagccaatacctgtttccttcattcgaaacctttaacactaagaattgtatcgcttacaatcctaatggtaatgctctggatgaaagttgcgaggataaaaatcgctatatttgtaagcagcaattgatttaa
[0307]
cd96的优化的转基因序列(seq id no.16):
[0308]
atggaaaaaaagtggaaatactgcgccgtgtactacataatacagattcactttgtcaaaggagtatgggagaaaacagtgaacacagaagagaacgtatatgcaacattgggatctgatgtgaatctcacgtgccagacgcagaccgtaggctttttcgttcaaatgcaatggtccaaagtaacgaataaaatagacctcatcgccgtatatcatccgcaatatggtttctattgcgcgtacggcagaccatgcgagagcctcgtcaccttcaccgagactccggagaatggcagcaag
tggacgcttcacctgcggaatatgagctgtagcgtgtccggaagatatgaatgcatgttggtgctgtatcccgagggtatacagactaagatctacaatctgctcattcaaacgcacgtaactgctgacgaatggaactcaaatcacaccattgaaatagagatcaatcagactctggagataccttgttttcaaaattcctccagcaaaataagttcagagtttacttatgcctggagtgtggaggacaatggcacacaagaaaccttgatttctcaaaaccacctcatttcaaactccaccttgttgaaggaccgggtaaagttgggaacggactacagactgcatctgtcccccgtgcaaatatttgacgacggcaggaagttctcctgtcacataagagtaggacctaacaagattctcagatcttcaactaccgtaaaagtgtttgctaagcccgagatccccgtaatcgtggagaacaattccacagacgtactcgtcgagcgcagattcacctgtttgttgaaaaacgtttttcccaaagccaatatcacgtggtttatcgatgggtccttccttcacgatgagaaggagggcatctatattacaaacgaggaaaggaaggggaaagatggatttcttgaactcaaatccgttctgactcgcgtccactccaataagccagcacaaagcgataatttgactatctggtgcatggcgttgtcccccgtgccgggcaacaaggtttggaacatctcttccgaaaaaataaccttcctcttgggctccgagatttcatctaccgaccctccattgtccgtaaccgagtctacactcgacactcagccgtcccctgcctcttccgtgagtcctgcacgctaccccgcgactagctctgtgacactggttgacgtatcagcattgaggcctaacactactcctcaaccatcaaattcatctatgacaacccggggtttcaattatccatggacttcctccggcacggacacaaaaaaatcagtctcacgaattccttccgaaacatactcatccagcccaagcggcgcgggttccacattgcatgataacgtatttaccagtactgcacgggccttcagcgaagtacctacaactgcgaacggatctacaaaaaccaatcatgttcacataactggcatcgttgtgaataaacccaaagacggcatgtcatggccagtgatagttgccgcattgctcttctgctgcatgatcctgtttggcctgggagtccgcaaatggtgtcagtatcagaaagagataatggagcgaccgcctcctttcaaaccccctccacctcccataaagtacacgtgtattcaggaacctaatgaaagcgaccttccctaccatgagatggagactctttag
[0309]
cd244的优化的转基因序列(seq id no.17):
[0310]
atgcttggtcaagttgtaactcttatcctgttgttgctgctcaaagtgtaccaaggcaaaggctgtcaaggctctgctgaccatgtcgtttcaataagcggtgttcccttgcaactccaacccaattccatacaaaccaaggtcgatagtatcgcttggaagaagctcctgccgtcccaaaatgggtttcatcacatattgaaatgggaaaacggttcccttccatcaaacacgtccaacgacagattctcctttatcgtaaaaaacctcagtctgctcatcaaagctgctcaacagcaagattcagggctttattgcctggaagttactagcatttctggcaaggtccagaccgccacctttcaagtgttcgtgtttgataaggtcgagaagccgcggctccaaggacagggaaaaattctggaccgagggagatgccaggtcgcgctgagttgcctcgtgagccgcgatggaaatgtatcttacgcttggtaccggggcagcaagttgatccagaccgcgggcaatctgacataccttgacgaggaggtcgacatcaacggcacacatacttacacttgcaatgtgagtaaccctgtatcctgggagtcccatacgctgaatctgacacaagactgccaaaacgcccatcaagagttccgattttggccctttctggttatcatcgtaatattgagtgctttgttccttggtacattggcctgtttctgtgtctggcgacggaaacgcaaggaaaagcagagcgagacaagccctaaagagtttttgaccatatacgaggatgtcaaggacctgaaaacaagaaggaatcatgaacaagagcagactttccccggcggaggttctaccatatattctatgattcaaagtcaaagcagcgcgcccacctcacaagagcctgcgtatactttgtattcccttattcaaccttcacggaaaagcgggtccaggaagaggaatcatagcccgtcctttaattcaactatctatgaagtcattggaaagagtcagcctaaggcacaaaatcctgcgaggctctcccggaaggaattggaaaactttgacgtatactcctag
[0311]
ccr4的优化的转基因序列(seq id no.18):
[0312]
atgaaccctacggacattgcggatactaccctcgatgagtcaatttatagcaattattacctttatgaatcaatccccaagccgtgcaccaaggaaggcattaaagcctttggtgaactctttcttccacctctgtattcacttgtgtttgtttttggactgctcggcaactcagttgtggtgctggtactctttaaatacaaaagactccgcagcatgaccg
atgtgtacctcttgaatctggcaatatctgacctcctgtttgtattctccctccccttttggggatattacgctgctgatcaatgggtttttgggttgggcctctgcaaaatgatcagctggatgtacctcgtgggattttactccgggattttctttgtcatgctcatgtccatcgaccgataccttgccatagttcatgcggtcttttctttgcgggcccgaaccctgacatacggcgttatcacgagcctggctacgtggagcgtggctgttttcgcgagcctccctggctttctcttttcaacctgctacacggagcgcaaccatacctattgcaaaactaaatactcacttaactccactacttggaaggtgctctccagtttggaaatcaatattttgggcctggttatccctctgggcataatgttgttttgctattccatgatcataagaacattgcaacactgcaagaacgagaaaaaaaataaggccgtaaaaatgatatttgcagtagttgtcctttttcttggtttttggacgccctataacatagtactgttcttggaaactttggtagaactggaggtgctccaagattgtacattcgaaagatatttggactatgccattcaagctaccgaaactctcgctttcgtgcattgctgtctgaaccccataatatactttttcctcggcgaaaaattccgaaaatacatactccagctcttcaaaacctgccggggcctctttgtactgtgccaatactgtggcttgctccaaatatatagcgcggacacaccatcttcctcctacacacaaagtactatggaccatgaccttcacgatgcgttgtag
[0313]
ccr9的优化的转基因序列(seq id no.19):
[0314]
atgacccccacggactttacttccccgattccaaatatggcggacgactatggcagcgaatccacgagctccatggaggactatgtgaatttcaatttcaccgatttctattgcgagaagaacaatgttcgacagttcgcctcccacttcctgccaccactgtactggctggtattcatcgtgggggcgctgggaaattccctggtcatacttgtatattggtactgtacccgcgtaaaaactatgacggatatgtttctcctcaaccttgcgatagctgatctgctttttttggtcacgctgcccttctgggcaatcgcagcggcagatcagtggaaattccaaacctttatgtgcaaagtcgtgaattccatgtataagatgaatttttattcatgcgtgcttctcataatgtgcattagtgttgatcggtatatagccatcgcccaggcgatgagggctcatacctggcgcgagaaacgactcctgtactccaaaatggtatgtttcaccatctgggtacttgccgctgcactttgcatacctgaaattttgtactcccaaattaaagaggagtccgggattgcaatttgcacaatggtctaccctagcgatgaatcaactaaacttaaatctgcggtgcttactctcaaagttatactcgggttctttcttccctttgtcgtcatggcctgctgctatactattataatacatacgttgatacaggcaaagaaatccagcaaacataaggcgttgaaagtcactatcacagtgttgactgtgttcgtgttgtctcaatttccatacaattgtatattgctggttcaaacaatagacgcctatgcaatgttcatctccaattgtgcggtttctactaacatcgacatttgcttccaagtcacccaaactatcgcattcttccattcatgcttgaatccggtactttatgtatttgtcggcgagaggtttcgcagagatttggtcaaaaccctcaagaaccttgggtgcatcagccaagcgcaatgggtatcatttacgcgccgggaggggtcactgaaactcagtagtatgcttctggaaactactagtggggcgctctccctgtga
[0315]
cxcr6的优化的转基因序列(seq id no.20):
[0316]
atggcggaacacgattaccacgaggattatggctttagcagctttaacgattccagccaggaggaacatcaggactttctgcaattctccaaagtatttttgccatgcatgtatctggtggtgtttgtgtgtggcctcgttggaaatagtctcgttctcgtaatatccatattttaccacaaactgcaatctctcaccgatgtgttccttgtaaacctgccccttgccgatctcgtctttgtatgtacactgccgttttgggcatatgctggcatacacgaatgggtatttgggcaggttatgtgcaaatcacttcttggaatctatacgataaacttctatacaagcatgcttattctcacttgcattaccgtggacagattcatagtggtggtgaaggcgaccaaagcgtataaccaacaagctaaacgaatgacttgggggaaggtcaccagccttttgatctgggttatctcacttcttgtgtctcttccacaaataatctatgggaacgtctttaatcttgacaaattgatttgcggataccatgacgaagcgatcagtactgtagtattggcgacacagatgacgcttggattctttctcccgcttctgacgatgatcgtttgttattccgttatcattaaaaccctgctgcatgctggcgggtttcaaaaacacagatctctcaagataattttccttgtgatggccgtgttcctccttacccaaatgccgttcaatcttatgaagtttatacgc
tcaactcattgggagtattacgctatgacctcttttcattacacaatcatggtgactgaagccattgcgtatcttcgcgcttgtctcaacccggttctctatgcattcgtgtccctgaaatttagaaagaacttctggaagttggtcaaagacattggctgtttgccttatctgggagtcagccatcaatggaagagtagtgaggataacagcaaaacgttttccgcctcccataacgttgaggcaacatcaatgtttcaactctag
[0317]
ccr2的优化的转基因序列(seq id no.21):
[0318]
atgcttagtaccagccgaagtagatttataagaaacacaaacgagtctggggaggaggtgacgactttttttgattatgattatggcgcgccgtgccataaatttgacgttaaacaaataggagcccaactgctccctccattgtattccctggtgttcatattcggcttcgtgggaaacatgctggtggtgcttatattgatcaactgtaaaaagctcaaatgtcttaccgatatttatctccttaatctcgcaataagcgatttgcttttcttgatcactctccccctttgggcccattccgctgctaacgaatgggttttcggcaacgcgatgtgtaaacttttcaccggcttgtaccatatcggctacttcggcggcatattctttataatacttttgactatcgaccgctacctcgctatcgtccacgcggtctttgctcttaaggcaaggacggtaacctttggagtcgttacctccgttatcacttggctggtggccgtgtttgcctccgttcccggcataatttttacaaaatgccagaaagaggattcagtatatgtctgtgggccctatttcccccggggatggaataatttccatacaatcatgcgaaatatactgggactcgtacttccacttcttataatggttatatgctactccggaatcttgaaaacacttctcagatgtcggaatgagaagaagcgccatcgagccgtgcgagtgatttttaccatcatgatcgtatacttcttgttctggacaccgtacaacatcgtcatattgctgaatactttccaagaattttttggcctttccaactgcgaaagcacctctcaactggatcaagcgactcaggtgacagaaaccttggggatgactcactgctgcattaacccgataatttacgcgttcgtgggcgagaagtttcgacgatatttgagcgtgttcttccggaagcacatcaccaaaagattttgcaagcaatgcccagtcttttatcgagaaaccgtagatggagttacgagtacgaacactccatccactggcgagcaagaagtgtcagcaggactttaa
[0319]
cxcr2的优化的转基因序列(seq id no.22):
[0320]
atggaggattttaacatggagagtgactcctttgaagatttctggaaaggggaggacctcagtaattactcatactcttctaccctcccgccattcttgctcgacgcggcaccctgcgagcccgagagtcttgagataaacaaatattttgtagtgataatttacgcccttgtgttcttgctttccttgttgggcaatagcttggtgatgctggtcatcctgtactcacgggtgggacggtccgttaccgacgtgtacctcctgaatctggccctcgcggacttgctttttgccctgactttgccaatatgggcagctagcaaagtcaatggctggatatttggaacctttctgtgtaaggtcgtgtcactgttgaaagaagtaaacttctacagtggcatactgttgcttgcctgtatatctgtcgatcggtacctcgctatagtacacgccacacggacgctcacacaaaaacgctatttggtgaaattcatatgcttgagcatatggggcctttcccttttgcttgctttgccggtcctccttttccgacggactgtctactcctctaatgtgtccccggcttgttatgaggacatggggaacaacaccgctaactggcgcatgctcctgaggatactcccacaaagttttggcttcatcgtcccgctccttataatgctcttttgctacggtttcaccttgcgaactctttttaaggctcatatgggccagaagcacagagctatgcgcgtgattttcgccgtggtccttatcttcttgttgtgctggctcccttacaatttggttctgctggcggatactctgatgcgaacgcaagttattcaggagacttgcgagcggcgaaatcatatagatagggcacttgacgccactgagatcttggggatactccattcctgtctcaacccgctcatatatgcgttcattggccaaaagttccgacatggtctgctcaagattctcgcgattcacggacttatcagtaaagacagtctgccaaaagattcacgcccctcatttgttggatcttcctccggacatacatcaactacgctttaa
[0321]
cx3cr1的优化的转基因序列(seq id no.23):
[0322]
atggatcaattccccgaaagcgtcaccgaaaattttgagtatgacgatttggctgaagcgtgttatataggcgacatagttgtgttcggcactgttttcttgtccatcttttactccgttattttcgccattggacttgtgggcaa
tctgcttgtggtgttcgcacttaccaatagcaagaagccaaagagcgtcacggatatttatttgctgaatctggctttgtctgatctgcttttcgtggctactctccccttttggacgcattacctgatcaatgaaaaggggctgcataacgctatgtgcaaatttaccacagcgttttttttcatcggtttttttggctcaatctttttcataaccgttattagcattgatcgctaccttgcgattgtacttgccgctaatagtatgaacaatcgcacggtgcaacacggagttacaatatcattgggagtatgggcggctgcaattctcgtcgccgcgccacaatttatgttcaccaaacaaaaagagaacgagtgcttgggggattatcccgaggtcctccaggagatctggcctgttctgaggaacgtggaaacaaatttcctcggatttctgctccccctccttatcatgtcatactgctattttcgcattatccaaacattgttttcttgtaaaaatcacaagaaagccaaggcgatcaagctgattctgcttgttgtgatcgtctttttcctcttttggaccccttataatgtaatgatttttttggaaacactcaaactctacgacttctttccatcctgcgatatgcggaaggatctgcggctggcgctctccgtaaccgaaactgtagcttttagtcattgttgtttgaatcctttgatctatgcgtttgccggggaaaagtttagaagatacctgtatcacctctatggaaagtgtttggccgttttgtgtggtcgatctgtccacgttgatttctcctcctcagagtcccaacgcagcagacacgggtctgtactctcctcaaacttcacatatcatacgagcgacggagatgcattgctgcttttgtga
[0323]
klrc2的优化的转基因序列(seq id no.24):
[0324]
atgaataaacaaagaggaacattctccgaggtatctctggctcaggaccctaaaagacagcaacgcaaacctaaaggaaataaatcaagcatcagtggcacagaacaggaaatatttcaagtggaattgaatctgcagaatccctccttgaaccaccagggcatcgacaaaatttatgattgtcaggggctcctgccgccgcccgaaaagttgacagccgaggtgctgggcatcatctgtatagtcttgatggcgacggttcttaagacaattgtccttataccctttctggagcaaaacaatttttcacccaatactcgaacccaaaaagctcggcactgcggccactgtcccgaggagtggataacatactcaaactcttgctattatatcggcaaagaaagaagaacttgggaggagagtttgctcgcttgtacgagcaaaaatagcagtctcctttccatcgataacgaagaggagatgaaattccttgcgtcaatactgcctagttcttggattggcgtctttcggaactcctcacaccacccttgggtaactataaacggcctcgcattcaagcataagatcaaggactctgacaacgcggagcttaattgtgcggttctgcaagtgaaccggttgaagagtgcccagtgcggatcatccatgatataccactgtaaacacaagctgtag
[0325]
tgfbr2的的优化的转基因序列(seq id no.25):
[0326]
atgggtagagggctgctgcgcggtttgtggccgctccatatcgttctttggacgaggattgcatccactatccctccgcatgtgcaaaagtccgtaaacaacgacatgatcgtcacagacaataatggcgcggtaaagtttcctcaactctgtaaattttgtgacgtgaggtttagcacctgcgataaccagaagagctgcatgtcaaattgttctattacctccatatgcgaaaaaccccaggaggtctgcgtcgcagtgtggagaaagaacgacgagaacataaccttggaaactgtttgccatgatccgaaattgccgtatcatgactttattctcgaggacgcggccagtccaaaatgcattatgaaggaaaaaaagaagcctggcgagactttctttatgtgctcatgttcaagcgatgagtgtaatgataatataattttcagcgaggaatacaacacgagcaaccctgaccttctcttggtcatcttccaggtcactggcatatccctcctgccgccgttgggggttgcgattagtgtaattattatattttattgctacagagtgtag
[0327]
kir2ds1的优化的转基因序列(seq id no.26):
[0328]
atgtccctcacggttgtttcaatggcctgtgtaggcttcttcctcctccaaggcgcctggccccatgagggagtgcatagaaagccttccctcttggcacatcccggtcgccttgttaaatccgaggagactgttattcttcaatgttggtctgatgtcatgttcgagcacttccttttgcaccgggaaggcatgttcaacgatacgttgcgcttgatcggagagcatcatgatggtgttagtaaagccaacttttctatttcacggatgaaacaagacctggctgggacatacagatgctacggatccgtcacacattctccgtatcaattgtctgctccttctgaccctttggacatagtaataatcggcctttatgaaaagccgtccttgtctgctcaacctgggccaactgtactggccggagaaaacgtgaccctctcatgctcctccc
gctcctcttacgacatgtaccatctctcccgggagggggaagcccacgaacgacggcttccggcgggcactaaagtaaatggcacgtttcaagcgaatttcccgctcggtcccgccacccacggcggaacctatcggtgctttggctccttccgagacagcccttatgagtggagcaagtcaagcgatccgctgctcgtgtctgttactggcaatccaagcaactcatggccgagccccacggaaccgagtagcgaaacaggcaatcccagacacctccatgtcctcattgggacgtccgtcgtcaagattccatttacaattttgttgttcttcttgttgcaccgatggtgttcagacaaaaagaacgctgctgtaatggatcaagaacctgcgggcaatcgcactgttaactccgaggatagcgacgaacaagatcatcaagaggtgtcttatgcgtga
[0329]
kir2ds2的优化的转基因序列(seq id no.27):
[0330]
atgagcttgatggtagtgtctatggcgtgtgtaggatttttcctgcttcaaggcgcttggccgcatgaaggcgtgcatagaaagccctccctgctcgcccatcctgggccgctggtaaaaagcgaggagacagttattcttcaatgttggagtgatgttagattcgaacattttttgctgcaccgggaggggaaatacaaggatacgctccaccttatcggagagcatcatgacggagtcagtaaagcaaacttctctatcggccctatgatgcaggacttggcgggcacgtaccgatgctacggttctgtgacccattccccctatcaactgtccgccccctccgaccctctggacatcgtcatcactggactctacgaaaaaccatccttgtctgctcaacccggccccactgtgctcgccggggagagtgtcacgcttagctgttcctctcgatcctcctatgacatgtaccatctttctcgcgaaggagaagcacatgaaagacgattcagtgccggtccgaaagtgaatggcacattccaggccgactttccgctgggacctgccacgcacgggggcacgtaccgatgttttgggagttttcgggatagcccatatgagtggagtaattcaagcgacccgctcttggtgtctgtgactgggaaccccagcaactcctggccgagccccaccgaaccttctagcaagactggcaacccccgacacttgcacgtgctcatcggaacgagtgtcgtcaaaatcccttttaccattcttctctttttcttgcttcatcgatggtgttcaaataaaaagaacgccgcagtgatggatcaagaaccggcaggcaatcggaccgtaaactccgaggactccgacgaacaggaccatcaagaggtgagttacgcatga
[0331]
kir2ds3的优化的转基因序列(seq id no.28):
[0332]
atgtctctgatggttatcagcatggcctgtgtgggattcttctggctccaaggcgcgtggccgcacgagggattccgaagaaaaccctctctcctggcccaccccggcagattggtaaagagcgaggaaactgtaatacttcagtgctggagtgatgtcatgttcgaacactttcttttgcatcgggaagggacatttaacgatactttgagactgatcggagagcatattgacggagtgagcaaggcgaatttctcaatcggaaggatgcgccaggatctggcaggcacatacagatgctatggttctgttcctcattcaccgtaccaattcagcgctccatccgatcctctcgacattgtaataactggtctttatgagaaaccgtcactctccgcccaacctggcccaaccgtgttggcgggcgagagtgtcactctgtcctgctcatcttggagttcatacgacatgtatcatttgtctactgaaggggaagcccacgagaggcggttctccgccgggccaaaagttaatggaacctttcaggctgacttccctctcggacctgctacccaaggaggaacctacagatgtttcggatcttttcacgactctccctatgagtggagcaagagctccgatcccttgctcgtatccgttacgggcaatccgtccaactcctggccttctccgacggaaccctcatcaaaaaccggcaaccctcgacacctgcatgtcttgatcggaactagtgtcgtcaagctcccattcaccatacttctcttctttttgctgcatcggtggtgttccgataaaaaaaacgctagtgttatggatcaaggccccgccggtaaccggactgtgaatcgagaagattcagatgaacaggaccatcaagaggtcagctatgcctga
[0333]
kir2ds4的优化的转基因序列(seq id no.29):
[0334]
atgagtctcatggtaataatcatggcttgtgtcgggtttttcctgcttcagggggcttggccgcaggagggagttcacagaaagccctctttcctggcgctccccggtcatcttgtaaaatctgaagaaactgtaatactgcagtgttggagcgacgtgatgtttgaacattttctccttcatcgggaagggaagttcaataataccctgcacctgatcggcgaacaccatgatggagttagtaaagcaaacttcagcataggcccgatgatgccggttcttgcgggaacctataggtgttacgggagtgttccgcactctccttaccaactctccgcaccaagcgatcctctcgatatggtgattatcggtctttacgaaaaaccgagcctgtcagctcaacctggaccgacggtccaagcaggggaaaatgtaactctcagttgctccagcc
gctcctcctatgatatgtaccatttgagtcgggagggagaagcacacgaacggcgcctgcctgccgtacggtctataaacggcacctttcaagcggacttccctctcggccccgcaactcatggcgggacgtacagatgctttggatccttccgggacgcgccatatgagtggagcaattccagcgatccactgctcgtgtccgttaccggaaatccaagcaactcctggccgagccctactgaaccaagttctaagactggcaacccgagacacctgcatgtgcttattggcacctcagtagtgaagatcccgtttactatcttgctcttctttcttcttcatcgctggtgtagcgataaaaagaatgcggccgtgatggatcaagagccagcaggtaaccggacagtaaacagcgaagattccgacgagcaagatcaccaggaagtttcttatgcatga
[0335]
kir2ds5的优化的转基因序列(seq id no.30):
[0336]
atgagtcttatggtgatttccatggcctgtgttgcttttttcctcctgcagggtgcttggcctcacgaagggttccgcaggaagccatctctccttgcccaccctggtcctcttgtaaagtcagaggaaacggttatcttgcaatgttggagcgatgtgatgtttgagcatttcctgctccaccgggagggaacatttaaccataccctccgcctcatcggagaacatatcgacggcgtgagcaagggaaacttttcaatagggaggatgacccaggatttggccgggacatatcgctgttatggctcagtcactcactcaccatatcaactcagtgctccgagcgatccacttgacattgtgattaccggcctctatgagaaacctagtctctccgctcaacctggtccgaccgttttggccggcgaatccgtcaccctttcctgctcttcccgctcctcctatgacatgtaccatctgagtagagagggcgaggcgcatgagcggagacttccagccggtccaaaagttaatcgcacctttcaggccgatttcccgctggaccctgcgacccacggcgggacgtaccgctgtttcggatcatttcgggactcaccttatgagtggagtaaaagttcagatcctttgcttgtctccgttacgggcaattcaagcaactcctggccctctcccacggaaccctctagtgaaaccggaaatccccgccatctccatgtgttgattggaacctccgtcgtaaagttgcctttcacgatcctgctgttcttccttttgcatcggtggtgctctaataaaaagaacgcttccgtgatggatcaaggcccggccggtaaccgcacggtcaatagagaagatagtgacgaacaagaccaccaagaagtgagctacgcgtga
[0337]
kir2dl1的优化的转基因序列(seq id no.31):
[0338]
atgagcttgctcgtcgtgtcaatggcctgcgtcggtttcttccttctccagggtgcatggcctcacgagggagtgcaccgaaaaccaagtttgctggctcaccctggcccgttggtgaagtcagaggaaacggtcatattgcaatgttggagcgatgtaatgtttgaacatttcctcctgcaccgagagggcatgttcaatgacacgctgcggcttattggggagcaccacgacggcgtgtctaaggcgaacttctcaatctcccggatgacgcaagaccttgccgggacttatagatgctacgggagtgtcacgcattccccttatcaagtgtctgccccttccgaccccctggacatagtcatcataggcctgtatgaaaaaccgtccttgagtgctcaaccgggtcccacagtcctcgctggcgagaatgttactttgagttgctcctcacgctcttcctatgacatgtatcacctgagccgggagggggaggctcacgagcggcgactgccagcagggccaaaggtaaacggaacttttcaagcagattttccgctcggccccgcaacccacggcggcacatatcggtgttttggatccttccacgactccccctacgaatggtccaagtcatctgatcctctgcttgtctccgtcaccggcaacccgtcaaattcctggccttcacccaccgaaccctcctcaaaaaccggcaacccgaggcatttgcatatccttattggcacaagcgtagttatcatcctcttcattttgctgttttttttgcttcaccgctggtgctccaataagaaaaatgcagcagttatggatcaggagagtgcagggaaccgcaccgcaaacagcgaggattccgatgaacaagacccgcaagaggtgacctacacacagcttaaccactgcgttttcacgcaaaggaagatcacccgaccatcccaacgacccaagaccccgcccaccgatataattgtatataccgagctcccaaacgctgagtctcgatcaaaagttgtctcctgcccatga
[0339]
kir2dl2的优化的转基因序列(seq id no.32):
[0340]
atgtcattgatggtggtttctatggcctgcgtgggtttttttcttctgcaaggagcttggccccacgaaggagttcatagaaagcctagcctccttgcgcatcctggccgcttggtgaaaagcgaagaaaccgtgatacttcagtgttggtctgatgttcggtttgaacacttcttgttgcatcgggagggcaaattcaaggacacacttcacctgattggggaacatcacgatggagtatcaaaagctaacttctctatcggaccgatgatgcaagatctcgccggcacctatcggtgt
tatgggagtgtgactcactctccgtatcaattgtctgcaccaagcgacccactggatattgtgataaccggcttgtatgagaagccaagtttgtccgctcaacccggtccaaccgttcttgccggcgagagcgtgactctttcctgctcctcccgaagcagttatgatatgtaccacctttcccgggagggcgaggctcacgagtgtagattctctgccggccctaaagtcaacgggaccttccaagcagactttccgctgggaccggctactcacggtggcacttatcgctgctttggttcttttcgcgactccccatacgagtggagcaacagctctgacccgctccttgtgtccgtcatcgggaacccttctaattcatggccctcacccaccgagccgtcatctaagaccgggaacccacgccatcttcatattcttattggcacatccgttgtgattatacttttcattcttctttttttcctccttcatcggtggtgttcaaacaagaaaaacgccgcggtcatggaccaggaaagtgctggcaatcgaacagccaatagcgaggactcagacgaacaggacccacaggaggttacgtacactcaactgaaccactgtgttttcacccaacggaagatcactcgcccctcccaaagaccgaaaacgccccctaccgatataattgtatatgctgaactgccaaatgccgaaagtagatccaaggtagtttcttgtccttga
[0341]
kir2dl3的优化的转基因序列(seq id no.33):
[0342]
atgtctctcatggtagtctctatggtttgcgtgggcttctttctccttcaaggcgcttggccacacgagggagtccaccgaaaaccgtcactcttggcgcatccgggccccttggtaaaaagcgaagaaacggttatccttcaatgctggtccgatgtaagatttcagcacttcctcctccatcgggaaggcaaatttaaggataccctccatctgatcggagagcatcatgacggggtatctaaggcgaacttctctatcgggcccatgatgcaggacctcgctggaacgtatcgatgctacggatctgtaacgcactcaccttaccaactcagtgctccttccgacccattggacattgttataaccggactctatgaaaaaccctcactgagcgcacaaccgggccccaccgtgctcgcgggggagtccgtgacgttgagttgctcttcacggtcctcttacgacatgtaccacctgtctcgagagggggaagctcacgaacggagattttcagcaggcccaaaggtcaatggcacattccaagcagatttcccgcttggccccgctacccatgggggcacgtataggtgttttggttcatttcgggactctccgtatgaatggtccaatagcagtgatccgttgctcgtttctgtaaccggaaatcccagtaatagctggcctagtccgactgagcctagttctgaaaccggcaaccctcgacaccttcatgtactgatcggcacctctgtagtgataattctcttcattctcctccttttttttctgctccaccgctggtgctgcaacaagaagaacgctgtcgtgatggatcaggaacccgctggcaacagaacagttaatcgggaggatagtgatgagcaagacccccaagaggtgacatatgcacaactcaaccattgcgtgttcactcaacggaaaataactcggccatctcaacggccgaaaacccctcccactgacataatcgtatacaccgaattgccaaatgctgagccatga
[0343]
kir2dl4的优化的转基因序列(seq id no.34):
[0344]
atgtcaatgtccccgacggtaattatccttgcatgtcttggattctttctcgatcaaagcgtatgggcacatgtcggtggacaagacaagcctttctgctccgcttggccatccgccgtcgtcccgcaggggggccacgtcacacttcgctgccactatcggagaggtttcaatatattcactctctacaaaaaggatggggtccccgtgccggaactgtataatagaatattctggaactcttttttgatttcacccgtgacgcccgctcacgcgggcacatatagatgcaggggatttcatccgcactcaccaacggagtggagcgccccgagcaacccgttggttattatggtgaccggactttacgaaaaaccctcattgacggctaggccagggcccacagttcgggcgggcgaaaacgtaacgctgtcttgctcttcccaatcctctttcgacatctaccatttgtcacgagagggcgaggctcatgaactcaggctcccagccgtgccatcaattaacgggaccttccaggcagattttccgttgggtcctgcaactcatggagaaacctaccggtgttttggaagcttccacggttccccctatgaatggtccgatccgtctgatccattgcccgtatccgttactgggaacccgtcatccagctggccttctcctacggaacctagttttaagacgggaatagcccgccacctgcatgccgttattagatacagtgttgctatcattttgtttaccatccttcccttctttctgcttcatcggtggtgttcaaaaaagaaagatgctgcggttatgaatcaggaaccagcgggacatcgcacagttaatagggaagattcagacgaacaagacccgcaggaggtcacatatgcacagttggatcattgtatttttacacaaagaaagattacaggaccatcccagcgctccaaacgaccgtcaaccgatacatcagtttgcatt
gaactgccgaacgcggagccgcgggcgctgtcccctgcacatgagcaccatagtcaggcgctgatgggcagctcacgcgaaacgacggccctttctcaaactcaactggcgagttctaatgtcccagcggctggcatttga
[0345]
kir2dl5a的优化的转基因序列(seq id no.35):
[0346]
atgtctctcatggtcatttcaatggcttgtgtgggtttttttcttctgcagggcgcttggactcacgaaggggggcaagataagccccttctctccgcatggccgagtgcggtcgtcccgcgaggcgggcatgtgacgcttctttgtcgctcccggttggggtttaccattttttccttgtataaggaggacggagtccctgttccggagctgtataataagatattctggaagtccatacttatggggccagtaacgcccgcccacgccggcacctaccgctgccggggctcccacccgagatccccgatagagtggagcgccccgtctaatcctttggttatcgttgttactgggttgttcggaaagcctagtctgtctgcccaacccggccctacggtccggactggcgaaaacgtcacccttagctgttccagtcggtcaagtttcgatatgtatcatttgagtagagaaggccgggcgcacgaaccaagactgcctgccgtgccctctgttaatggaacattccaggctgacttccctcttggaccggctactcatggaggcacttacacttgctttggatcactgcatgattcaccttacgaatggagtgacccgtccgaccctttgcttgtgtctgtaaccggcaactcctcttcttcctcctcttcaccaactgaaccgagttccaaaactgggataagaaggcaccttcacatactcatcgggacctcagttgcaattatcctctttatcatcctcttcttcttcctgctgcattgctgctgctccaataagaaaaatgcggcggtaatggaccaagagcccgcaggggataggaccgtcaatagggaggactctgacgatcaagacccccaagaagttacctatgctcaattggatcattgtgtctttactcaaacaaagatcacttctccttcccaacgcccaaagactcctccaaccgacaccactatgtatatggagctgcctaacgctaagcctcggagcctctctccggctcacaagcaccactcacaagcactgcgaggatcatcacgagaaactaccgcattgagccaaaatagagtggcgtccagccatgttcccgccgccggaatatga
[0347]
kir2dl5b的优化的转基因序列(seq id no.36):
[0348]
atgtcactgatggtggtgtccatggcgtgcgttggcttctttctcctgcagggggcatggacgcatgagggcggtcaggacaagcctctgttgtccgcgtggcctagtgcggttgttccccggggcggtcacgtcacccttttgtgtcggagcagactgggattcacaatcttctccctttataaagaagatggggtccccgtacccgagctctacaacaagatcttttggaagtcaatactcatggggcccgtaacacccgcacatgccgggacgtaccgctgccggggaagtcacccccgaagccctattgaatggagtgcaccctccaacccgctcgtcattgtggtgactggcctgttcgggaagccctcactcagcgctcaacccggacccaccgtccgaaccggggagaacgtgactctctcttgctcctcccggagtagctttgacatgtatcacctttcccgagaggggcgggcacatgaacctagactgccagcggttccttccgtggatggcacttttcaggccgactttcccctgggacctgctactcacggggggacttacacatgtttttcatccttgcacgactcaccctacgagtggagcgacccctccgatccccttttggtatccgtcaccggaaacagttcctcaagctcctccagtccgacagaaccctcttccaagaccgggatacgccgccacctgcacattctcatcggaacttcagttgcgattatcttgttcatcatactgttcttcttcctgttgcattgctgttgctccaataaaaagaatgcagcagtaatggatcaagagcccgcgggagacaggacagtcaaccgagaggactccgacgatcaagaccctcaagaggtcacatatgcacaactggaccactgtgtctttacgcaaacgaaaataaccagcccgtcccaacgaccaaagactccacccacggacacgacaatgtatatggagcttccaaacgctaagccgagatcattgagtcctgctcacaaacatcattcccaggccctgcgggggtccagtagggaaacaacggcgctgtcccaaaaccgcgttgctagttcacatgtccccgccgccggaatttga
[0349]
mir21的优化的转基因序列(seq id no.37):
[0350]
ccagttttcttgccgttctgtaagtgttttattcttagtgtgatttttttccattgggatgtttttgattgaacttgttcattttgttttgcttgggaggaaaataaacaattttacttttttcctttaggagcattatgagcattatgtcagaatagaatagaattggggttcgatcttaacaggccagaaatgcctgggtttttttggtttgtttttgtttttgtttttttatcaaatcctgcctgactgtctgcttgttttgcctaccatcgtgacatctccatggctgtaccacct
tgtcgggtagcttatcagactgatgttgactgttgaatctcatggcaacaccagtcgatgggctgtctgacattttggtatctttcatctgaccatccatatccaatgttctcatttaaacattacccagcatcattgtttataatcagaaactctggtccttctgtctggtggcacttagagtcttttgtgccataatgcagcagtatggagggaggattttatggagaaatggggatagtcttcatgaccacaaataaataaaggaaaactaagctgcattgtgggttttgaaaaggttattatacttcttaacaattctttttttcagggacttttctagctgtatgactgttacttgaccttctttga
[0351]
mir181b1的优化的转基因序列(seq id no.38):
[0352]
cttatttgtcttcttttgtagtcttttgaaatggcataaaaatgcataaaatatatgactaaaggtactgttgtttctgtctcccatccccttcagatacttacagatactgtaaagtgagtagaattctgagttttgaggttgcttcagtgaacattcaacgctgtcggtgagtttggaattaaaatcaaaaccatcgaccgttgattgtaccctatggctaaccatcatctactccatggtgctcagaattcgctgaagacaggaaaccaaaggtggacacaccaggactttctcttccctgtgcagagattattttttaaaaggtcacaatcaacattcattgctgtcggtgggttgaactgtgtggacaagctcactgaacaatgaatgcaactgtggccccgctttttgctgtcacaatcaacagatattccatctttgaaagatgtgttcaaaatagtactattgttctttaagttttccaattcgtcagcatcttctggtttatttattcaatttatatcatgtgatgagatttcaatgaaaaagactctggtttaaacaagaataatgcttctctatcttttgtatgctataaacagagcatgttttagaaaaggcaaaactattttgtccatcaaacgtacagtatcatcatctaggttagctcaccttcctactgttgtagtgtgagtgaaaaaaagaca
[0353]
mir181a1的优化的转基因序列(seq id no.39):
[0354]
taccacaaagtactttgaataacaaattgtccctgtctttaacagtgagataattccatctctggaactagcccaatatcggccatgtttttgcttaatgaaaccgatccttttctctcatacaatgtgatgtggaggtttgccaaactctttgttggaagaatcatgcttcttatttgtcttcttttgtagtcttttgaaatggcataaaaatgcataaaatatatgactaaaggtactgttgtttctgtctcccatccccttcagatacttacagatactgtaaagtgagtagaattctgagttttgaggttgcttcagtgaacattcaacgctgtcggtgagtttggaattaaaatcaaaaccatcgaccgttgattgtaccctatggctaaccatcatctactccatggtgctcagaattcgctgaagacaggaaaccaaaggtggacacaccaggactttctcttccctgtgcagagattattttttaaaaggtcacaatcaacattcattgctgtcggtgggttgaactgtgtggacaagctcactgaacaatgaatgcaactgtggccccgctttttgctgtcacaatcaacagatattccatctttgaaagatgtgttcaaaatagtactattgttctttaagttttccaattcgtcagcatcttctggtttatttattcaatttatatcatgtgatgagat
[0355]
mir144的优化的转基因序列(seq id no.40):
[0356]
ctgggtctgtctgcctgtctgcttgttagtgtgaccaaagggaaccttctgcatcattacgccatctctggcttgtttaacactggccctgggtccctatgagatcttaacagaccctagctccagtccccttcccataacccacctgggctgtgcctgaccacagaatcaaggagacgctggcctgcgagggagctgtagagcagggagcaggaagctgtgtgtgtccagccctgacctgtcctgttctgcccccagcccctcacagtgcttttcaagccatgcttcctgtgcccccagtggggccctggctgggatatcatcatatactgtaagtttgcgatgagacactacagtatagatgatgtactagtccgggcacccccagctctggagcctgacaaggaggacaggagagatgctgcaagcccaagaagctctctgctcagcctgtcacaacctactgactgccagggcacttgggaatggcaaggaaaccgttaccattactgagtttagtaatggtaatggttctcttgctatacccagaaaacgtgccaggaagagaactcaggaccctgaagcagactactggaagggagactccagctcaaacaaggcaggggtgggggcgtgggattgggggtaggggagggaatagatacattttctctttcctgttgtaa
[0357]
mir150的优化的转基因序列(seq id no.41):
[0358]
gggagggggccgcaacctcctattcccctctgggtctccgtcccctccctctggagtccacactccctctttgccccttgctggttctctactgcccccagcatagggtggagtgggtgtgcagtttctgcgactcagggtggcgtccccccaacctgtccctgccccttcctgccctctttgatgcggccccacttcctctggcaggaacccccgccctccctggacctgggtataaggcagggactgggcccacggggaggcagcgtccccgaggcagcagcggcagcggcggctcctctccccatggccctgtctcccaacccttgtaccagtgctgggctcagaccctggtacaggcctgggggacagggacctggggaccccggcaccggcaggccccaaggggtgaggtgagcgggcattgggacctcccctccctgtactcccatctctgctgcggcttttatgcgtctctccccttcgggtcccacatatcctctggtgcgctcctgcctcaccgcccccaccccatgcctgtcgtccccacctctgtgtgatgcgcaaagtacacctgtttctattgtacctgcctctcgcggtggtctgtgctctccccagctctgcaaaacccctcctccccatgtgccacaaccctgggccaccgtgtgtcctgtcctgttc
[0359]
实施例3:增强的cd16信号传导
[0360]
对于改进的细胞疗法(例如,干细胞疗法、适应性免疫疗法等),可以将目的细胞工程化以展现增强的cd16信号传导(例如,增强的内源cd16信号传导、引入的包含cd16的转基因等)。目的细胞可以是干细胞,如分离的干细胞(例如,胚胎干细胞)或诱导干细胞(例如,ipsc)。目的细胞可以是免疫细胞(例如,nk细胞)。这样的免疫细胞可以源自如本文所公开的干细胞。可替代地,这样的免疫细胞可以是免疫细胞系(例如,nk细胞系)。
[0361]
例如,对于改进的适应性免疫疗法,可以将nk细胞工程化以展现增强的cd16信号传导。
[0362]
hncd16氨基酸序列(seq id no.1):
[0363]
mwflttlllwvpvdgqvdttkavitlqppwvsvfqeetvtlhcevlhlpgssstqwflngtatqtstpsyritsasvndsgeyrcqrglsgrsdpiqleihrgwlllqvssrvftegeplalrchawkdklvynvlyyrngkafkffhwnsnltilktnishngtyhcsgmgkhrytsagisvtvkelfpapvlnasvtspllegnlvtlscetklllqrpglqlyfsfymgsktlrgrntsseyqiltarredsglywceaatedgnvlkrspelelqvlglqlptpvwfhvsfclvmvllfavdtglyfsvktnirsstrdwkdhkfkwrkdpqdk
[0364]
工程化的nk细胞:
[0365]
将nk-92细胞工程化以展现增强的cd16信号传导。对工程化的nk-92细胞进行修饰以表达cd64/cd16a融合蛋白(即,hncd16)(seq id no.1)。
[0366]
通过使用荧光激活细胞分选法(facs)鉴定cd16(例如,通过抗cd16-pe抗体)和cd64(例如,通过抗cd64-apc/af700抗体)二者的增强的表达来验证所得hncd16nk-92细胞,如图1a中所示。使用野生型(wt)nk-92细胞作为对照。
[0367]
hncd16构建体序列可以包含“fhvs”(seq id no.2)。hncd16构建体序列可以包含“wfhvs”(seq id no.3)。hncd16构建体序列可以包含“fhvsf”(seqid no.4)。hncd16构建体序列可以包含“wfhvsf”(seq id no.5)。hncd16构建体序列可以包含“vwfhvsfc”(seq id no.6)。hncd16构建体序列可以包含“pvwfhvsfcl”(seq id no.7)。hncd16构建体序列可以包含“tpvwfhvsfclv”(seq id no.8)。
[0368]
增强的靶向:
[0369]
将hncd16 nk-92细胞单独培养(未刺激的,对照)或者在能够激活nk细胞的k562细胞(k562)或佛波醇12-肉豆蔻酸酯13-乙酸酯(pma)的存在下进行培养以激活cd16并诱导其切割。数据揭示,如与作为对照的外周血(pb)nk细胞相比,hncd16 nk-92细胞对激活诱导的cd16a的切割具有高抗性(图1b)。例如,对于hncd16 nk-92细胞,用pma处理将cd16 细胞的
百分比从92%略微减少至85%,而相同处理将cd16 细胞从96%减少至25%(图1b)。还通过使用抗cd64抗体确认hncd16在hncd16 nk-92细胞中的持久性(图1c)。另外,观察到在刺激(例如,k652或pma)后,hncd16 nk-92细胞没有下调内源cd16表达(图1d和图1e)。
[0370]
增强的共抗体疗法
[0371]
将靶细胞(raji细胞)用以下处理:(i)hncd16 nk-92细胞和(ii)作为对照的抗cd20抗体或higg。数据揭示,如与对照(例如,具有抗cd20抗体的野生型nk92细胞,或具有higg的hncd16 nk-92细胞)相比,与抗cd20抗体组合的hncd16 nk-92细胞诱导增强的靶细胞死亡(例如,至少部分adcc介导的死亡)(图1f和图1g)。
[0372]
分化为ink的表达hncd16的ipsc
[0373]
使如本文所公开的工程化的ipsc(例如,工程化而具有增强的或引入的cd16信号传导(例如,hncd16,一种cd16变体)的ipsc)经历分化为nk细胞(例如,ink细胞)。在一些情形中,收集ink细胞(例如,约5x105个含有细胞的培养物)并用于染色(例如,针对nk特异性标记进行染色),例如,用nkg2a-pe、nkp30-pe、nkp44-pe、nkp46-pe和/或cd56-apc抗体染色。分别如图4a-图4e中所示,在经由hncd16表达增强的cd16信号传导的三个例示的克隆pu02、pu06和pu24之间,在分化的细胞中检测到cd56
细胞,并且在cd56
群体中检测到nkg2a
、nkp30
、nkp44
和/或nkp46
细胞。因此,证实表达增强的或引入的cd17信号传导的ipsc能够分化为ink细胞。
[0374]
nk细胞中增强的cd16信号传导
[0375]
如图5中所描绘,在与对照野生型(wt)nk-92细胞和anb-iso相比时,通过facs用pe缀合的抗cd16抗体检测到在nk细胞(例如,野生型ink细胞或具有增强的cd16信号传导的ink克隆,如pu02、pu06和pu24克隆)中增强的cd16信号传导(例如,cd16如hncd16的过表达)的丰度更高。因此,在hncd16 nk-92细胞中hncd16实际上过表达。
[0376]
nk细胞与抗体的组合
[0377]
如本文所公开的nk细胞(例如,nk92细胞系、源自干细胞如ipsc的nk细胞)可以与单独剂量的抗体一起用于针对靶细胞(例如,癌细胞)的细胞毒性的增强。例如,被工程化以表达增强的cd16信号传导(例如,hncd16、cd16-cd64融合蛋白等)的nk细胞可以在体外用某种抗体(例如,抗cd20 mab)的组合在某些靶细胞(例如,raji细胞)中诱导细胞裂解,并且在组合治疗中裂解的靶细胞的百分比高于单独的nk细胞或抗体。
[0378]
实施例4:nk细胞的增强的存活和持久性
[0379]
对于改进的细胞疗法(例如,干细胞疗法、适应性免疫疗法等),可以将目的细胞工程化以展现(i)至少一种内源基因(例如,一种或多种免疫调节多肽)的降低的表达和/或(ii)至少一种另外的基因(例如,一种或多种另外的免疫调节多肽)的增强的或引入的表达。如本文所公开的包含(i)和/或(ii)的细胞可以展现增强的功能,如持久性水平(或存活水平)。在一些情形中,如与具有单独的(i)和(ii)之一、或(i)与(ii)的单独作用的组合、或不具有二者相比,具有(i)与(ii)的组合可以协同改进细胞的功能。目的细胞可以是干细胞,如分离的干细胞(例如,胚胎干细胞)或诱导干细胞(例如,ipsc)。目的细胞可以是免疫细胞(例如,nk细胞)。这样的免疫细胞可以源自如本文所公开的干细胞。可替代地,这样的免疫细胞可以是免疫细胞系(例如,nk细胞系)。
[0380]
工程化的nk细胞的生成:
[0381]
例如,对于适应性免疫疗法的增强的持久性,可以将nk细胞工程化以包含至少(i)异源转录因子(例如,stat)和(ii)内源细胞因子受体(例如,内源il受体,如il-17r)的降低的表达或活性。如与具有单独的(i)和(ii)之一或不具有二者相比,在工程化的nk细胞中具有(i)与(ii)的组合可以协同改进工程化的nk细胞的持久性。
[0382]
nk细胞是从分离的esc或ipsc生成。将nk细胞工程化以表达异源stat(例如,stat3和/或stat5b)。通过病毒转导或通过如本文所公开的基因编辑部分的作用将编码异源stat的基因掺入nk细胞的基因组中。还将nk细胞工程化以展现内源il-17r(即,stat3
il-17r-nk细胞)的降低的表达或活性。使用具有(i)异源stat和(ii)il-17r的降低的表达或活性中的一种的nk细胞或非工程化的nk细胞作为对照。
[0383]
体外存活和持久性:
[0384]
可以将工程化的stat3
il-17r-nk细胞在体外培养以评估工程化的stat3
il-17r-nk细胞在不存在外源细胞因子的情况下的活力和生长(或增殖能力)。将nk细胞在没有添加外源细胞因子的培养基中培养3-6周。如与对照细胞相比,工程化的stat3
il-17r-nk细胞展现显著更高数量的nk细胞,表明工程化的stat3
il-17r-nk细胞在体外增强的存活和持久性。
[0385]
体内药代动力学(pk):
[0386]
可以在具有raji异种移植模型的ncg小鼠中施用工程化的stat3
il-17r-nk细胞。ncg小鼠是三重免疫缺陷的并且缺乏功能/成熟t细胞、b细胞和nk细胞,并且具有降低的巨噬细胞和树突细胞功能以作为异种移植模型的宿主。通过静脉内(iv)尾静脉注射以约1
×
106个细胞/动物的剂量将工程化的stat3
il-17r-nk细胞和对照细胞各自施用至相应的raji异种移植模型小鼠中。用工程化的stat3
il-17r-nk细胞注射的小鼠在输注后约7天至约28天展现外周血中更高的nk细胞浓度,证实了工程化的stat3
il-17r-nk细胞在体内增强的存活和持久性。
[0387]
其他工程化的nk细胞的生成:
[0388]
可以将目的细胞(例如,干细胞、免疫细胞,如nk细胞等)工程化而具有(i)至少一种内源基因的降低的表达(例如,一种或多种免疫调节多肽的功能丧失)和/或(ii)至少一种另外的基因(例如,编码一种或多种另外的免疫调节多肽的至少一种转基因)的增强的或引入的表达。例如,nk细胞(例如,脐带血nk(cbnk)细胞、源自ipsc的nk细胞等)可以具有以下编辑:bcl3转录辅激活物(bcl3)的功能丧失;cbl原癌基因b(cblb)的功能丧失;细胞周期蛋白依赖性激酶8(cdk8)的功能丧失;ige受体ig的fc片段(fcer1g)的功能丧失;白介素17a(il17a)的功能丧失;白介素17f(il17f)的功能丧失;肌醇多磷酸-5-磷酸酶d(inpp5d/ship1)的功能丧失;细胞因子信号传导抑制剂1(socs1)的功能丧失;细胞因子信号传导抑制剂2(socs2)的功能丧失;细胞因子信号传导抑制剂3(socs3)的功能丧失;信号转导蛋白和转录激活物3(stat3)的功能丧失;tet甲基胞嘧啶双加氧酶2(tet2)的功能丧失;蛋白酪氨酸磷酸酶非受体2型(ptpn2)的功能丧失;蛋白酪氨酸磷酸酶非受体6型(ptpn6)的功能丧失;cd70分子(cd70)的功能丧失;cd38分子(cd38)的功能丧失;细胞因子诱导性含sh2蛋白(cish)的功能丧失;和/或杀伤细胞凝集素样受体c2(klrc2/nkg2c)的转基因。
[0389]
在一些情形中,功能丧失基因编辑可以通过如本文所公开的一种或多种基因编辑部分如cripsr/cas9系统来实现。简言之,将nk细胞(例如,cbnk细胞)从深低温保藏恢复并
使用培养基(例如,淋巴细胞无血清培养基kbm 581(corning)、10%人男性ab血清、1%mem非必需氨基酸溶液(100x,gibco)、1%l-谷氨酰胺(200mm)(gibco)、0.02%维生素c、200u/ml il-2)进行培养。对于每种编辑,分离细胞(例如,约1x107个细胞)并用指导rna/cas9蛋白复合物(rnp)转染(例如,使用lonza nucleofector4d和p3 primary cell 4d-nucleofectortm x试剂盒l)。指导rna和cas9例如以2:1的比率进行转染(指导rna 75皮摩尔(pmol)、cas9蛋白150pmol)。
[0390]
在下游测定之前回收转染的细胞(例如,使用具有加倍人男性ab血清(20%)的培养基)。通过片段分析或ngs来分析编辑效率。
[0391]
指导rna和用于编辑效率评价的引物的序列列于下表4和表5中。表4:用于具有增强的存活和持久性的nk细胞的指导rna的序列靶标名称grna序列grna位置链bcl3ttgaccagccggtgcacagcchr19:44756266-44756288-cblbaaattctcggaggatgctccchr3:105659009-105659031 cdk8cttgctccaagaagtagttcchr13:26385300-26385322-cishagtccacgtcggccaccagachr3:50607666-50607688 fcer1gcttcagtcgacagtagaggachr1:161218055-161218077-il17atggtattggtattccggttachr6:52187728-52187750-inpp5dcaacatcacccgctccaaggchr2:233060502-233060524 socs1tccgttcgcacgccgattacchr16:11255284-11255306-socs2cttgagccctccgggaatggchr12:93572913-93572935 socs3cagcaggttcgcctcgccgcchr17:78358919-78358941 stat3taagacccagatccagtccgchr17:42322471-42322493-tet2caggactcacacgactattcchr4:105234149-105234171-ptpn2tagaggaaagtcctgtacatchr18:12802004-12802026 ptpn6tcggcccagtcgcaagaaccchr12:6951687-6951709 il17fgtacttgctgctgtcgatatchr6:52238923-52238945-cd38tatcagccactaatgaagttchr4:15816593-15816612 cd70gcccgcaggacgcacccatachr19:6590941-6590960 表5:用于编辑效率评价的引物序列
[0392]
杀伤细胞凝集素样受体c2(klrc2/nkg2c)的转基因的优化序列(seq id no.42):
[0393]
atgaataaacaaagaggaacattctccgaggtatctctggctcaggaccctaaaagacagcaacgcaaacctaaaggaaataaatcaagcatcagtggcacagaacaggaaatatttcaagtggaattgaatctgcagaatccctccttgaaccaccagggcatcgacaaaatttatgattgtcaggggctcctgccgccgcccgaaaagttgacagccgaggtgctgggcatcatctgtatagtcttgatggcgacggttcttaagacaattgtccttataccctttctggagcaaaacaatttttcacccaatactcgaacccaaaaagctcggcactgcggccactgtcccgaggagtggataacatactcaaactcttgctattatatcggcaaagaaagaagaacttgggaggagagtttgctcgcttgtacgagcaaaaatagcagtctcctttccatcgataacgaagaggagatgaaattccttgcgtcaatactgcctagttcttggattggcgtctttcggaactcctcacaccacccttgggtaactataaacggcctcgcattcaagcataagatcaaggactctgacaacgcggagcttaattgtgcggttctgcaagtgaaccggttgaagagtgcccagtgcggatcatccatgatataccactgtaaacacaagctgtag
[0394]
针对细胞持久性(例如,nk细胞持久性)相关基因的体外筛选
[0395]
nk细胞可以用作模型细胞群体以检查增强持久性的基因编辑。可以将nk细胞群体工程化以包含(i)包括选自bcl3、cblb、cdk8、fcer1g、il17a、il17f、ship1、socs1、socs2、socs3、stat3、tet3、ptpn6和cd70的一个或多个成员的至少一种内源免疫调节多肽的降低的表达,和/或(ii)nkg2c的增强的或引入的表达。在包含工程化的nk细胞的这样的群体和不含(i)和/或(ii)的其他细胞(例如,其他nk细胞)的细胞混合物中,这样的混合物中的工程化的nk细胞的所述群体的持久性水平的特征可以是(i)所述混合物内的工程化的nk细胞的所述群体在次优环境中的富集水平高于(ii)所述混合物内的工程化的nk细胞的所述群体在最优环境中的富集水平。次优环境可以包含更低量(或浓度)的外源细胞因子(例如,外源il,如il-2)。例如,次优环境可以包含比最优环境中低至少约1%、至少约5%、至少约10%、至少约20%、至少约30%、至少约40%、至少约50%、至少约60%、至少约70%、至少约80%、至少约90%或更多的量的外源细胞因子。次优环境可以是体外培养基,并且最优环境可以是体外培养基。次优环境可以是体内环境(例如,受试者的血流),并且最优环境可以是体外培养基。这样的混合物内的工程化的nk细胞的所述群体的富集水平可以通过鉴定展现以下的细胞的量(或比例)来查明:(i)包括选自bcl3、cblb、cdk8、fcer1g、il17a、il17f、
ship1、socs1、socs2、socs3、stat3、tet3、ptpn6和cd70的一个或多个成员的至少一种内源免疫调节多肽的降低的表达,和/或(ii)nkg2c的增强的或引入的表达。
[0396]
不希望受理论束缚,具有目的基因的降低的表达或活性水平(例如,fcer1g的功能丧失)的nk细胞可以在次优环境(例如,低细胞因子)中存活或持续存在更长时间。在更优环境(例如,高细胞因子)中,nk细胞可以展现高存活率或持久性,不管nk细胞是否包含这样的目的基因(例如,fcer1g)的降低的表达或活性水平。因此,在具有不同细胞类型的混合物中在次优(或更有挑战性)的环境中展现更高富集(例如,插入缺失%)可以表明,这样的功能丧失基因可以诱导细胞的增强的存活或持久性。
[0397]
例如,为了发现与nk持久性相关的基因,将工程化的nk细胞的一种或多种这样的群体(例如,十八种基因编辑的nk细胞,如基因编辑的cbnk细胞)在如本文所公开的混合物中混合,并使用高细胞因子(200u/ml il-2)或低细胞因子(10u/ml il-2)进行培养。在8天培养后通过ngs分析每种基因的编辑百分比(插入缺失%)。使用每种基因的两次单独电穿孔来制备两种混合物,对于每种培养条件设置三次重复。显示方法设计的流程图描绘于图14a中。
[0398]
具有低或高细胞因子(或者在次优环境或更优环境中)的持久性
[0399]
通过比较低细胞因子培养的nk细胞与高细胞因子培养的nk细胞的编辑百分比,fcer1g缺陷编辑在用低细胞因子培养时显示增加的百分比,这表明fcer1g缺陷性nk细胞在低细胞因子条件中具有更高持久性,而ptpn2在相同测定中没有显著差异,分别如在图14b和图14c中所说明。
[0400]
因此,在细胞(例如,干细胞、免疫细胞,如nk细胞等)中具有并非ptpn2的免疫调节多肽(例如,fcer1g)的降低的表达或活性水平可以在所述细胞中诱导增强的持久性或存活率。
[0401]
nk持久性相关基因的体内筛选
[0402]
与细胞持久性的体外筛选类似,将工程化的nk细胞的一种或多种这样的群体(例如,十八种基因编辑的nk细胞,如基因编辑的cbnk细胞)在如本文所公开的混合物中混合,并且使用高细胞因子(200u/ml il-2)(更优环境)培养或将其注射至hil-15-ncg小鼠中(次优环境),将每种混合的nk细胞以一定量(例如,1x107个nk细胞/小鼠的量)注射至5只小鼠。随时间流逝(例如,在8天后),收获体外培养的nk细胞或小鼠组织以提取基因组。通过ngs分析每种基因的编辑百分比(插入缺失%)。使用每种基因的两次单独电穿孔制备两种混合物,对于体外培养设置三次重复,对于每种混合的nk细胞注射使用五只小鼠。显示方法设计的流程图描绘于图15a中。
[0403]
体内持久性
[0404]
如图15b-图15g中所示,通过比较小鼠组织中的nk细胞与高细胞因子培养的nk细胞的编辑百分比,与使用高细胞因子培养相比,stat3缺陷编辑在小鼠组织中显示增加的百分比,这表明stat3缺陷性nk细胞在体内具有更好的存活和持久性,而ptpn2在相同测定中没有显著差异。
[0405]
因此,在细胞(例如,干细胞、免疫细胞,如nk细胞等)中具有并非ptpn2的免疫调节多肽(例如,stat3)的降低的表达或活性水平可以在所述细胞中诱导增强的持久性或存活率。
[0406]
实施例5:工程化的car nk细胞
[0407]
对于改进的细胞疗法(例如,适应性免疫疗法等),可以将目的细胞工程化以包含含有针对靶细胞(例如,癌症或肿瘤细胞)的特定抗体的抗原结合部分的异源嵌合多肽(例如,嵌合抗原受体),以展现针对这样的靶细胞的增强的细胞毒性。目的细胞可以是免疫细胞(例如,nk细胞)。这样的免疫细胞可以源自如本文所公开的干细胞。例如,对于源自干细胞的nk细胞,如本文所公开的一个或多个遗传修饰可以在以下状态引入:(a)干细胞状态(例如,ipsc状态),(b)造血干细胞状态,和/或(c)nk细胞状态。可替代地,这样的免疫细胞可以是免疫细胞系(例如,nk细胞系)。
[0408]
工程化的抗cd19 nk细胞
[0409]
将nk细胞(例如,nk-92细胞)工程化以表达抗cd19 car,然后在cd19 raji细胞的存在下进行培养以评估工程化的抗cd19 nk细胞对raji细胞的靶向。使用野生型(wt)nk-92细胞作为对照。如与对照相比,抗cd19 car nk细胞展现针对raji细胞的增强的细胞毒性(如通过减少的活raji细胞的数量所查明)(图2a和图2b)。另外,当在raji细胞的存在下培养时,如与对照相比,抗cd19 car nk细胞展现内源cd107a的增强的表达(指示细胞毒性颗粒释放)(图2c和图2d)。此外,当在raji细胞的存在下培养时,如与对照相比,抗cd19 car nk细胞展现增强的细胞因子产生(例如,ifn-γ和/或tnf-α产生)(图2e-图2g)。
[0410]
表达cd33-car的nk细胞
[0411]
生成表达包含能够与cd33特异性结合的抗原结合部分的嵌合多肽受体的nk细胞。cd33 car结构设计的示意图显示于图16a中。以1:1的e/t(效应子/靶标)比率测试具有cd33-car整合的nk92细胞对kg1细胞(一种具有cd33的高表达的肿瘤细胞系)的靶向细胞毒性。使用wt-nk92细胞作为未修饰的对照。如图16b中所示,cd33-car对kg1细胞的靶向细胞毒性与对照相比有显著改进。
[0412]
表达bcma-car的nk细胞
[0413]
生成表达包含能够与bcma特异性结合的抗原结合部分的嵌合多肽受体的nk细胞。bcma car结构设计的示意图显示于图17a中。具有bcma-car整合的nk92细胞对rpmi8826细胞(一种具有bcma的高表达的肿瘤细胞系)的靶向细胞毒性、cd107a和inf-r表达显示于图17b-图17d中。所用e/t(效应子/靶标)比率为1:1、1:5和1:10。使用wt-nk92细胞作为未修饰的对照。
[0414]
不同嵌合多肽受体设计构建体
[0415]
图19a说明不同嵌合多肽受体(例如,car)构建体。图19a上图示意性地说明cd19 car(2b4)结构设计。tm是跨膜结构域的缩写;scfv是单链可变片段的缩写。图19a中图示意性地说明cd19 car(4-1-bb)结构设计。tm是跨膜结构域的缩写;scfv是单链可变片段的缩写。图19a下图示意性地说明cd19 car(cd28)结构设计。tm是跨膜结构域的缩写;scfv是单链可变片段的缩写。
[0416]
图19b和图19c显示表达图19a中所示嵌合多肽受体设计之一的nk细胞针对靶细胞的靶向细胞毒性。参见图19b,各种cd19-car nk92对cd19-k562细胞的靶向细胞毒性(e/t(效应子/靶标)等于5:1;1:1和0.5:1)证实,表达具有4-1-bb信号传导结构域、2b4信号传导结构域和/或cd28信号传导结构域的car构建体的nk细胞展现针对cd19呈递k562靶细胞的靶向细胞毒性。使用wt-nk92细胞作为未修饰的对照,cd19-k562是被工程化而具有高表达
的cd19的k562。参见图19c,cd19-car nk92对没有工程化而以高水平表达cd19的k562细胞的非特异性细胞毒性(e/t(效应子/靶标)等于5:1;1:1和0.5:1)显示更低程度的细胞毒性,表明4-1-bb、2b4和/或cd28细胞内信号传导结构域可用于设计各种car构建体,例如,用于免疫疗法,如nk细胞疗法。
[0417]
实施例6:工程化的hil15 nk细胞
[0418]
对于改进的细胞疗法(例如,干细胞疗法、适应性免疫疗法等),可以将目的细胞工程化以展现增强的细胞因子信号传导(例如,通过增强的或引入的il-15,如异源分泌型il-15、异源膜结合il-15、异源il-15细胞因子-il15受体融合物等实现的增强的il-15信号传导)。目的细胞可以是干细胞,如分离的干细胞(例如,胚胎干细胞)或诱导干细胞(例如,ipsc)。目的细胞可以是免疫细胞(例如,nk细胞)。这样的免疫细胞可以源自如本文所公开的干细胞。可替代地,这样的免疫细胞可以是免疫细胞系(例如,nk细胞系)。
[0419]
工程化的nk细胞:
[0420]
将nk-92细胞工程化而具有(i)hil-15敲入或(ii)hil-15-hil15r融合多肽敲入。测试hil-15-hil15r融合多肽的两种变体。第一变体(即,hil15-il15ra融合-1或“fus1”)设计为具有在hil-15与hil15r之间的接头,所述接头包含一个或多个(例如,至少1、2、3、4、5、6、7、8或更多个重复)的“ggggs”(seq id no.9),例如,“ggggsggggsggggsggggsggggsggggs”(seq id no.10)。第二遍体(即,hil15-il15ra融合-2或“fus2”)设计为具有hil-15与hil15r之间的接头,所述接头包含一个或多个(例如,至少1、2、3、4、5、6、7、8或更多个重复)的“ggggs”(seq id no.9)和一个或多个(例如,至少1、2、3、4、5、6、7、8或更多个重复)的“egkssgsgseskst”(seq id no.11),例如,“egkssgsgseskstegkssgsgseskstggggs”(seq id no.12)。具有敲入的任一种hil-15-hil15r融合多肽变体的nk-92细胞对hil-15呈阳性(图3a)。
[0421]
另外,如与工程化以表达分泌形式的il-15的对照nk-92细胞相比,表达用于增强的il-15信号传导的hil-15-hil15r融合多肽的任一变体的工程化的nk-92细胞展现更长的持久性。蛋白质印迹分析揭示如与分泌型il-15(il15)相比,在表达hil15-il15ra融合-1(fus1)或hil15-il15ra融合-2(fus2)的nk-92细胞中,il-15刺激的stat5的增加的磷酸化(图3b)。
[0422]
hil15-il15ra融合-1序列(seq id no.13):
[0423]
mriskphlrsisiqcylclllnshflteagihvfilgcfsaglpkteanwvnvisdlkkiedliqsmhidatlytesdvhpsckvtamkcfllelqvislesgdasihdtvenliilannslssngnvtesgckeceeleeknikeflqsfvhivqmfintsggggsggggsggggsggggsggggsggggsgitcpppmsvehadiwvksyslysreryicnsgfkrkagtssltecvlnkatnvahwttpslkcirdpalvhqrpappstvttagvtpqpeslspsgkepaasspssnntaattaaivpgsqlmpskspstgtteisshesshgtpsqttaknweltasashqppgvypqghsdttvaiststvllcglsavsllacylksrqtpplasvemeamealpvtwgtssrdedlencshhl
[0424]
hil15-il15ra融合-2序列(seq id no.14):mriskphlrsisiqcylclllnshflteagihvfilgcfsaglpkteanwvnvisdlkkiedliqsmhidatlytesdvhpsckvtamkcfllelqvislesgdasihdtvenliilannslssngnvtesgckeceeleeknikeflqsfvhivqmfintsegkssgsgseskstegkssgsgseskstggggsgitcpppmsvehadiwvksyslysreryicnsgfkrkagtssltecvlnkatnvahwttpslkcirdpalvhqrpappstvttagvtpqpeslspsgkepaassp
15编辑的ipsc分化的enk细胞(qn-019)。类似地,施用从wt ipsc分化的enk细胞(qn-001)作为对照。如图9a-图9b中所示,在输注后8、15和22天通过facs用cd56-apc抗体检测外周血中的nk细胞浓度。在输注至异种移植模型中之后,cd56 qn-019细胞的增殖显著快于qn-001细胞,这证实了qn-019细胞中优选的药代动力学概况。
[0435]
分化为ink的表达分泌型il-15的ipsc
[0436]
使工程化的ipsc经历ink分化。测试表达分泌型il-15的三个克隆px27、px33和px39。具体而言,收集1x105个含有细胞的培养物并将其用于用cd56-apc抗体染色。具有总分化细胞中cd56
细胞的百分比的图10a说明,表达分泌型il-15的ipsc可以分化为ink。
[0437]
在培养基中对分泌型il-15的验证
[0438]
将1x106个从表达分泌型il-15、acd19 car和用于增强的cd16信号传导的变体的ipsc克隆分化的ink细胞(ka08)在不更换培养基的情况下培养2天,并且收集上清液并将其稀释10倍以用人il-15elisa试剂盒测量人il-15。显示ink培养基中的il-15浓度的图10b证实,已针对将人il-15分泌至培养基中来验证ink细胞。
[0439]
表达分泌型il-15的enk细胞的体外生长
[0440]
图10c显示5x106个从表达分泌型il-15、acd19 car和用于增强的cd16信号传导的变体的ipsc克隆分化的enk细胞(oq-20)的体外生长曲线。每4天收集培养的细胞并计数,并且同时在不存在外源细胞因子的情况下用相应培养基更换培养基。记录16天内细胞的生长并绘制为曲线。因此,已经证实,表达分泌型il-15的enk细胞在没有外源细胞因子的情况下促进体外生长。
[0441]
实施例7:免疫调节多肽基因编辑
[0442]
对于改进的细胞疗法(例如,干细胞疗法、适应性免疫疗法等),可以将目的细胞工程化以展现(i)一种或多种免疫调节多肽(例如,一种或多种内源免疫调节多肽)的降低的表达和/或(ii)一种或多种另外的免疫调节多肽(例如,一种或多种异源免疫调节多肽)的增强的或引入的表达。如本文所公开的包含(i)和/或(ii)的细胞可以展现增强的功能,如持久性水平(或存活水平)、低免疫性(例如,针对免疫排斥或细胞毒性的抗性)、生长速率、针对靶细胞(例如,肿瘤细胞)的细胞毒性等。
[0443]
在一些情形中,如与具有单独的(i)和(ii)之一、或(i)与(ii)的单独作用的组合、或不具有二者相比,具有(i)与(ii)的组合可以协同改进细胞的功能。在一些情形中,如与具有两种或更多种免疫调节多肽的降低的表达的单独成员或者这样的单独成员的单独作用的组合相比,具有两种或更多种免疫调节多肽的降低的表达可以协同改进细胞的功能。在一些情形中,如与具有两种或更多种另外的免疫调节多肽的增强的/引入的表达的单独成员或者这样的单独成员的单独作用的组合相比,具有两种或更多种另外的免疫调节多肽的增强的/引入的表达可以协同改进细胞的功能。
[0444]
目的细胞可以是干细胞,如分离的干细胞(例如,胚胎干细胞)或诱导干细胞(例如,ipsc)。目的细胞可以是免疫细胞(例如,nk细胞)。这样的免疫细胞可以源自如本文所公开的干细胞。可替代地,这样的免疫细胞可以是免疫细胞系(例如,nk细胞系)。
[0445]
工程化的细胞:
[0446]
表2说明多种免疫调节多肽的修饰的表达或活性的示例性组合。可以将来自表2的多种免疫调节多肽的修饰的表达或活性的组合引入细胞(例如,工程化的nk细胞)中以例如
减少或避免在将所述细胞施用至宿主身体后来自宿主身体的免疫应答(例如,免疫攻击,如适应性免疫排斥)。来自表2的多种免疫调节多肽的修饰的表达或活性的组合可以包括(i)一种或多种第一免疫调节多肽的降低的表达或活性(第2栏)和(ii)一种或多种第二免疫调节多肽的增强的表达或活性(第3栏)。在一些情形中,来自表2的多种免疫调节多肽的修饰的表达或活性的组合可以包括(i)一种或多种内源免疫调节多肽基因的敲除(第2栏)和(ii)一种或多种异源免疫调节多肽基因的敲入(第3栏)。表2
[0447]
修饰的nk细胞的生成
[0448]
对于实现低免疫性,可以将nk细胞工程化以携带某些转基因和/或目的基因的功能丧失,如非限制性示例性指导rna序列显示于下表6中。表6:用于生成具有低免疫性的工程化的nk细胞的指导rna序列靶标名称指导rna序列指导rna位置nlrc5ttgccgagctggaggccaacchr16:57020719-57020741:-nlrc5atcttggcgttcagccattcchr16:57020785-57020807:-nlrc5atgtccagggttcggacaccchr16:57020897-57020919: rfxankgatgaggtcttctgcaggctchr19:19193957-19193979:-rfxankgttcaggattcacaggctcachr19:19194084-19194106:-rfxankgaaacactggcatccggttcchr19:19194100-19194122:-rfxapccgttaggtacctgtgcgaachr13:36819566-36819588: rfxapggcggacctgttagacacttchr13:36819624-36819646: rfxaptggccaagcagcgcaaaccgchr13:36819815-36819837: cd80atggtccggttcttgtactcchr3:119544693-119544715: cd80gaaattgaggtatggacactchr3:119557672-119557694: cd80ttgaggtatggacacttggachr3:119557676-119557698: cd7cggaaccgtctgtccgtagtchr17:82316810-82316832: cd7cgctggctcgcggcctgcctchr17:82317430-82317452:-cd7cgcgagccagcgccagaagcchr17:82317441-82317463: tap2tcaagactttgttgttcaccchr6:32837822-32837844: tap2catagtcctggcagcccttgchr6:32838118-32838140: tap2gactgtctccctgagagcccchr6:32837987-32838009:-tap1cttgtagaatccagtcagtgchr6:32852449-32852471: tap1gtagaatccagtcagtgaggchr6:32852452-32852474: tap1ttacgggccgcctcactgacchr6:32852459-32852481:-tapbpgaaccaacactcgatcaccgchr6:33313815-33313837: tapbpggtgatcgagtgttggttcgchr6:33313811-33313833:-tapbpgatcgagtgttggttcgtggchr6:33313808-33313830:-[0449]
nectin3/cd113的的优化的转基因序列(seq id no.42)
[0450]
atggcgagaactctgcggccaagtccactttgccctgggggaggaaaggctcaactgtcttccgccagcctccttggggccgggctgttgctccagccacccacaccgccgcccctgctgctcttgctttttcctctgttgctcttttcaaggctgtgcggtgctctcgcggggccgattatcgtagaaccccatgtaactgcagtatggggaaagaacgtgtccttgaagtgccttattgaggtaaatgagacaatcacgcaaattagttgggagaagattcatggaaaaagtagccaaacagtagctgtccaccatccacagtatgggttctcagtacagggggagtaccaggggcgggtactttttaaaaatta
ctcccttaacgatgcgactatcaccctgcacaatattggtttctcagatagcggcaaatacatttgtaaggctgtgacattcccacttggaaacgctcaatcctcaacgacggttactgttctcgttgagcctactgtatccctcataaagggtccggactctttgattgatggtggtaacgagactgtcgcagccatctgtatagcagcgactgggaagcctgtagcgcatattgattgggagggggatttgggggagatggagtctacaaccaccagtttccccaatgagacagctacaatcatttcacaatacaagttgtttccaacgcggttcgcccggggacgccgaataacctgtgtagttaagcacccggcattggagaaggacattcggtactccttcattctggatattcagtatgctcctgaagtaagtgtgacaggttacgatgggaactggtttgtcggacggaagggtgttaatttgaagtgcaacgcggatgcaaacccacccccttttaagtctgtctggtctcgattggacggacaatggcccgacgggttgttggcgtcagataatactcttcattttgttcatcccctgacttttaattatagcggtgtctacatctgcaaagtcaccaactcccttggtcagcgatccgaccagaaggtgatttatatatccgatcctccaactacgacaactttgcaacccacgattcagtggcacccgtcaaccgctgacatagaggacttggcgactgaaccaaaaaaacttccttttccgttgagtacactcgcaacgataaaagatgataccattgccactataattgcttccgtcgttgggggggctctgtttatcgttcttgtgtccgtgttggctggaatattctgctaccggcgccggcgaaccttccgcggcgattacttcgccaagaattacattcctccctctgacatgcaaaaggaatcacaaatagacgtgttgcaacaggacgagcttgatagttatcctgactctgttaagaaggaaaataagaatccagtgaataatcttatacgaaaggactatctggaagagcccgaaaaaacacaatggaacaatgtggagaatttgaaccgatttgagcgacccatggattactatgaggatcttaagatgggaatgaagttcgtttcagatgagcattatgatgagaatgaagatgaccttgtcagccacgtggacggttctgtcatcagcagaagggaatggtatgtctag
[0451]
adora2a/a2ar的优化的转基因序列(seq id no.43)
[0452]
atgcccattatgggctcatccgtctatataacagtggagctcgctattgccgtgcttgcaattctcggcaacgtattggtctgttgggctgtttggcttaactccaaccttcagaacgtgactaattattttgtagtatcacttgctgcagccgatatagctgtgggggtgctcgctattccttttgcgattacaatatccacgggcttttgtgcagcatgtcacgggtgtctcttcatagcctgcttcgtactggtgttgacacagtcatccatttttagccttcttgccatcgctatagatcgctatattgcgattcgaatccccttgcgctataacgggctggtaactggcacaagggccaaaggtattattgctatatgttgggtcctctcatttgctattggattgactccgatgctggggtggaataattgtggacagccgaaggagggcaaaaaccattcacaaggctgtggggaaggacaggtagcctgcctttttgaggatgtggtacccatgaactatatggtctatttcaatttctttgcatgcgtccttgtaccgcttttgctcatgctgggggtttacctcaggatatttcttgccgcccgaaggcaacttaaacagatggaatctcaaccgctcccaggggagcgcgccagaagtacactgcaaaaggaagtgcatgccgccaaaagcctcgcgatcatagttggcttgtttgccttgtgttggcttcccctccacatcataaattgttttacttttttttgtcccgactgttcacacgcgccattgtggctcatgtaccttgcgattgtgctcagccacacaaactcagtagttaatcctttcatctacgcttatagaattcgagaatttcgccagacgtttagaaagattatacggtctcacgtattgcggcagcaggaaccttttaaggctgctggcacttctgctcgggtgctcgcggcacatggatcagacggcgagcaggtctcactcagactgaacggccatccaccaggagtttgggcgaacggctctgctccccaccctgaacgacggcctaatggttacgctcttggcctggtgtctggcggtagcgcccaggaatcacaagggaatacgggtttgccagatgtcgagctgcttagccacgaacttaaaggggtttgtccagagccgccaggcctcgatgatcctcttgctcaggacggagctggcgtgtcatga
[0453]
生成具有基因敲入的工程化的nk细胞
[0454]
可以通过敲入基因编辑如hla-e、cd47、pdl2、hla-g、tgf-β、ccl21、il10、cd46、cd55和/或cd59将人ipsc细胞工程化。这样的工程化的ipsc细胞可以分化为nk细胞。可替代地,可以用aav系统将人外周血(pb)-nk细胞工程化。用于针对低免疫性测试工程化的nk细
胞的可能的功能性读出包括混合淋巴细胞反应(mlr)、t细胞激活测定、体外nk细胞诱导的杀伤测定以及补体依赖性细胞毒性。
[0455]
通过编辑和分化ipsc实现的低免疫性
[0456]
针对低免疫性用于生成源自ipsc细胞的nk细胞或内皮细胞(ec)的测试方案显示于图11中。简言之,可以用不同的敲入和敲除来编辑ipsc。随后,可以使这些编辑的ipsc经历分化为ink,所述ink可以进一步扩增为enk。ink细胞可以用于t细胞增殖测定,并且enk可以用于nk细胞毒性测试和低免疫性测试。可替代地,编辑的ipsc细胞可以分化为iec细胞(例如,源自ipsc的内皮细胞),所述iec细胞可以用于nk敏感性测定。
[0457]
生成工程化的ipsc的方法
[0458]
几种方法可以用于将ipsc工程化用于具有低免疫性的nk细胞。示例性方法显示于表7中。表7:用于生成工程化的ipsc的方法ko基因ko方法sgrna序列b2mrnpgagtagcgcgagcacagctaciitarnpaggcccggatggcatcctagicam1rnp micaabeggcaggcttgcattccctccmicbabeaggggccatggggctgggcculbp1abeactcaccgacccatcctgcc
[0459]
简言之,rnp方法是用含有cas9和sgrna的预混合的核糖核蛋白(rnp)对靶细胞进行电穿孔的方法。在递送至细胞之后,rnp编辑与sgrna配对的基因组区域。腺嘌呤碱基编辑器(abe)方法是其中cas蛋白可以与能够使dna核苷脱氨的酶融合的方法。
[0460]
编辑-1克隆的确认
[0461]
几种编辑-1克隆(即克隆05、07、08、104、111、112)是通过用靶向b2m的rnp对人ipsc进行电穿孔来衍生的。通过针对mhc-i的facs分析(参见图12a)和通过桑格测序(图12b)确认编辑-1克隆是b2m敲除的。简言之,对克隆05进行测序以具有一个核苷酸在两个b2m等位基因中的插入,并且对克隆07进行测序以具有一个核苷酸在一个b2m等位基因中的插入以及两个核苷酸在另一个等位基因中的缺失。
[0462]
编辑-2克隆的确认
[0463]
类似地,几种编辑-2克隆(即克隆03和06)是通过用靶向ciita的rnp对人ipsc进行电穿孔,之后针对单细胞进行facs分选来衍生的。通过桑格测序确认编辑-2克隆是ciita ko的。如图12c中所示,对克隆03进行测序以具有一个核苷酸在两个ciita等位基因中的插入,并且对克隆06进行测序以具有一个核苷酸在一个ciita等位基因中的插入以及十六个核苷酸在另一个等位基因中的缺失。
[0464]
编辑-3克隆的确认
[0465]
几种编辑-3克隆(即克隆04、20、25、48和16)是通过用分别靶向b2m和ciita的两种rnp对hipsc进行电穿孔来衍生的。通过针对mhc-i的facs分析确认编辑-3克隆是b2m敲除的(参见图12d),并且使用桑格测序在基因组水平上确认b2m和ciita的敲除(参见图12e)。
[0466]
编辑-4克隆的确认
[0467]
几种编辑-4克隆(即克隆02和30)是通过用过表达pd-l1、pd-l2、tgf-β、hla-e、hla-g、cd47、il-10、ccl-21、cd46、cd55、cd59的构建体以及分别靶向b2m和ciita的两种rnp对hipsc进行电穿孔,之后针对b2m-;pdl1
;cd47
单细胞进行facs分选来衍生的。通过针对mhc-i以及pdl1 、pd2 、cd47 、cd46 、cd55 和cd59 的facs分析确认编辑-4克隆是b2m-的(参见图12f),并且使用桑格测序在基因组水平上确认b2m和ciita的敲除。对于ciita,确认仅1个等位基因被敲除(参见图12g)。
[0468]
编辑-5克隆的确认
[0469]
几种编辑-5克隆(即克隆01、02和26)是通过用过表达pd-l1、hla-e、cd47、il-10、ccl-21的构建体以及分别靶向b2m和ciita的两种rnp对hipsc进行电穿孔,之后针对b2m-;pdl1 ;cd47 单细胞进行facs分选来衍生的。通过针对mhc-i以及pdl1 、cd47 的facs分析确认编辑-5克隆是b2m-的(参见图12h),并且使用桑格测序在基因组水平上确认b2m和ciita的ko(参见图12i)。
[0470]
编辑-6克隆的确认
[0471]
几种编辑-6克隆(即克隆08、13、15和31)是通过用过表达pd-l1、hla-e、cd47、cd46、cd55、cd59的构建体以及分别靶向b2m和ciita的两种rnp对hipsc进行电穿孔,之后针对b2m-;pdl1 ;cd47 单细胞进行facs分选来衍生的。通过针对mhc-i以及pdl1 、cd47 、cd46 、cd55 、cd59 的facs分析确认编辑-6克隆是b2m-的(参见图12j),并使用桑格测序在基因组水平上确认b2m和ciita的ko(参见图12k)。
[0472]
编辑-7克隆的确认
[0473]
几种编辑-7克隆(即克隆32、33、39和42)是通过用过表达pd-l1、hla-e、cd47、ccl-21、cd55的构建体以及分别靶向b2m和ciita的两种rnp对hipsc进行电穿孔,之后针对b2m-;pdl1 ;cd47 单细胞进行facs分选来衍生的。通过针对mhc-i以及pdl1 、cd47 、hla-e 、cd55 的facs分析确认编辑-7克隆是b2m-的(参见图12l),并使用桑格测序在基因组水平上确认b2m和ciita的ko(参见图12m)。
[0474]
编辑-8克隆的确认
[0475]
几种编辑-8克隆(即克隆15、36、40和42)是通过用过表达cd47的构建体以及分别靶向b2m和ciita的两种rnp对hipsc进行电穿孔,之后针对b2m-;cd47 单细胞进行facs分选来衍生的。通过针对mhc-i以及cd47 的facs分析确认编辑-8克隆是b2m-的(参见图12n),并使用桑格测序在基因组水平上确认b2m和ciita的ko(参见图12o)。
[0476]
编辑-9克隆的确认
[0477]
几种编辑-9克隆(即克隆03、10、22、27、34、36、37和63)是通过用过表达pd-l1、pd-l2、tgf-β、hla-e、hla-g、cd47、il-10、ccl-21、cd46、cd55、cd59的构建体、靶向b2m和ciita的两种rnp以及过表达靶向mica、micb和ulbp1的sgrna的1个碱基编辑器质粒对hipsc进行电穿孔,之后针对b2m-;pdl1 ;cd47 单细胞进行facs分选来衍生的。通过针对mhc-i以及cd47 、b2m 、hla-e 、pdl1 、cd55 、cd46 和cd59 的facs分析确认编辑-9克隆是b2m-的(参见图12p),并使用桑格测序在基因组水平上确认b2m和ciita的ko。使用下一代测序来确认mica/micb/ulbp1的ko。符号√表示基因被顺利敲除(参见图12q)。
[0478]
对抗体介导的补体细胞毒性的抗性
[0479]
如图13a中所示,将不同编辑的ipsc克隆用ssea-4抗体预标记,之后与范围为0%
~50%的不同浓度的人补体共孵育45min。结果证实,具有编辑-4而非编辑-5或编辑-8的ipsc具有对抗体介导的补体细胞毒性的抗性。
[0480]
不希望受理论束缚,增强的对抗体介导的补体细胞毒性的抗性可以归因于具有以下免疫调节多肽中的一种或多种的增强的或引入的表达:pd-l2、tgf-β、cd46、cd55、cd59和hla-g(例如,pd-l2、tgf-β、cd46、cd55和cd59中的至少一种或多种)。因此,不希望受理论束缚,如与具有编辑-5或编辑-8的细胞相比,包含编辑-9的细胞(参见图18)也可以展现增强的对抗体介导的补体细胞毒性的抗性。
[0481]
不希望受理论束缚,如与具有编辑-5或编辑-9的ipsc相比,具有编辑-4或编辑-9的ipsc可以在体外或体内展现增强的对抗体介导的补体细胞毒性的抗性。不希望受理论束缚,如与源自具有编辑-5或编辑-9的ipsc的可比较的分化的细胞相比,源自包含编辑-4或编辑-9的ipsc的分化的细胞(例如,内皮细胞、免疫细胞等)可以在体外或体内展现增强的对抗体介导的补体细胞毒性的抗性。不希望受理论束缚,如与源自具有编辑-5或编辑-9的ipsc的免疫细胞相比,源自包含编辑-4或编辑-9的ipsc的免疫细胞可以在体外或体内展现增强的对抗体介导的补体细胞毒性的抗性。不希望受理论束缚,如与源自具有编辑-5或编辑-9的ipsc的nk细胞相比,源自包含编辑-4或编辑-9的ipsc的nk细胞可以在体外或体内展现增强的对抗体介导的补体细胞毒性的抗性。
[0482]
cbnk细胞毒性
[0483]
将从相应ipsc分化的靶向的细胞iec用cfse预标记,然后以5:1的效应子:靶标比率与cbnk共培养4h。在4h后,添加pi用于染色死细胞。使用facs检测死细胞的百分比。将没有与cbnk共培养的iec视为自发的靶细胞死亡。为了计算特定nk细胞介导的靶细胞裂解的百分比,使用下式:nk介导的特异性裂解(%)=(共培养中的pi阳性靶细胞%-自发细胞死亡中的pi阳性靶细胞%)/(100-自发细胞死亡中的pi阳性靶细胞%)。定量显示于图13b中,其表明从具有编辑-4而非编辑-5或编辑-8的相应ipsc分化的iec具有对cbnk细胞毒性的抗性。
[0484]
从ipsc分化的效率
[0485]
使工程化的ipsc经历ink分化。收集200ul含有细胞的培养物并将其用于cd56和nkg2a染色。在染色后,将细胞重悬于100ul facs缓冲液(pbs 1%bsa)中。收集80ul细胞悬浮液用于分析。如下计算cd56 细胞数量的收率:(通过facs收集的绝对cd56 细胞)*18ml/(200ul*0.8)=(通过facs收集的绝对cd56 细胞)*112.5(参见图13c);cd56 和nkg2a 百分比分别显示于图13d和图13e中。从上文图中表明,具有不同编辑的ipsc可能都分化为ink,收率和效率有所不同。
[0486]
具有低免疫性的nk细胞的功能特性
[0487]
图13f显示针对k562的单次杀伤。将相应enk与cfse预标记的k562细胞以e:t=3:1或1:1的比率共培养。在4h后,添加pi用于染色死细胞。使用facs检测死细胞的百分比。将没有与enk共培养的k562视为自发靶细胞死亡。为了计算特定nk细胞介导的靶细胞裂解的百分比,使用下式:nk介导的特异性裂解(%)=(共培养中的pi阳性靶细胞%-自发细胞死亡中的pi阳性靶细胞%)/(100-自发细胞死亡中的pi阳性靶细胞%)。
[0488]
图13g显示针对k562的连续杀伤。将相应enk与k562-egfp细胞以e:t=3:1的比率共培养,所述共培养在incucyte中进行。通过以每3h的频率成像来监测k562-egfp细胞。每
天添加k562持续6天。将仅k562-gfp的样品设为对照。
[0489]
图13f和图13g表明,b2m/ciita双重敲除的enk没有显示针对k562细胞的任何低反应性表型,并且在针对k562细胞测试时,具有转基因的大多数enk具有与wt enk可比较的细胞毒性。不希望受理论束缚,针对其他靶细胞的低反应性或细胞毒性可能是不同的。
[0490]
为了测试具有不同编辑的ink是否会刺激pbmc中的cd8 t细胞的增殖,将相应enk与cfse标记的pbmc共培养。使用pbs作为阴性对照,而使用pha作为阳性对照。在5天后,针对cd3、cd4和cd8对共培养的细胞进行染色。将cd3
cd8
cfse
低
视为增殖cd8
t细胞。在图13h-图13m中测试来自不同供体的pbmc。数据显示,具有或不具有转基因的b2m/ciita双重敲除的nk没有刺激cd8 t细胞增殖。
[0491]
类似地,将相应enk与cfse标记的pbmc共培养。使用pbs作为阴性对照,而使用pha作为阳性对照。在5天后,针对cd3、cd4和cd8对共培养的细胞进行染色。将cd3
cd4
cfse
低
视为增殖cd4
t细胞。在图13n-图13s中测试来自不同供体的pbmc。数据显示,具有或不具有转基因的b2m/ciita双重敲除的nk没有刺激cd4 t细胞增殖。实施方案
[0492]
以下非限制性实施方案提供本发明的说明性实施例,但是不限制本发明的范围。
[0493]
实施方案1.一种工程化的nk细胞,其包含:对于所述工程化的nk细胞是异源的分泌型il-15;以及以下中的一种或多种:(i)用于如与对照细胞相比增强的cd16信号传导的cd16变体,其中所述cd16变体对于所述细胞是异源的,或者(ii)包含能够与抗原结合的抗原结合部分的嵌合多肽受体,其中所述抗原不是cd19,其中所述工程化的细胞缺乏异源il-15r,任选地其中:(1)所述工程化的nk细胞还包含所述cd16变体;和/或(2)所述工程化的nk细胞还包含所述嵌合多肽受体;和/或(3)所述工程化的nk细胞包含(i);和/或(4)所述工程化的nk细胞包含(ii);和/或(5)所述工程化的nk细胞包含(i)和(ii)二者;和/或(6)所述工程化的nk细胞还包含编码所述分泌型il-15的异源多核苷酸;和/或(7)所述抗原包括选自以下的一个或多个成员:bcma、cd20、cd22、cd30、cd33、cd38、cd70、κ、lewis y、nkg2d配体、ror1、ny-eso-1、ny-eso-2、mart-1和gp100;和/或(8)所述抗原包括选自以下的nkg2d配体:mica、micb、ulbp1、ulbp2、ulbp3、ulbp4、ulbp5和ulbp6;和/或(9)所述工程化的nk细胞源自分离的干细胞或诱导干细胞。
[0494]
实施方案2.一种源自分离的干细胞或诱导干细胞的工程化的nk细胞,其包含对于所述工程化的nk细胞是异源的分泌型il-15,其中所述工程化的细胞缺乏异源il-15r,任选地其中所述工程化的nk细胞还包含编码所述分泌型il-15的异源多核苷酸。
[0495]
实施方案3.一种工程化的nk细胞,其包含:
对于所述工程化的nk细胞是异源的膜结合il-15,其中所述工程化的nk细胞还包含以下中的一种或多种:(a)并非il-15的异源细胞因子,(b)内源免疫调节多肽的降低的表达或活性,其中所述内源免疫调节多肽不是b2m,或者(c)安全开关,任选地其中:(1)所述工程化的nk细胞包含并非il-15的所述异源细胞因子;和/或(2)所述工程化的nk细胞包含所述内源免疫调节多肽的降低的表达或活性,其中所述内源免疫调节多肽不是b2m;和/或(3)所述工程化的nk细胞包含所述安全开关,任选地其中所述安全开关包含诱导性细胞死亡部分;和/或(4)所述工程化的nk细胞包含(a)-(c)中的两种或更多种;和/或(5)所述工程化的nk细胞包含(a)、(b)和(c);和/或(6)所述工程化的nk细胞源自分离的干细胞或诱导干细胞;和/或(7)所述膜结合il-15是包含il-15和il-15r的至少一部分的嵌合膜受体的一部分;和/或(8)所述嵌合膜受体包含选自以下的序列:(i)seq id no.9的四个或更多个相邻重复,(ii)seq id no.10,(iii)seq id no.11,(iv)seq id no.9与seq id no.11的组合,(v)seq id no.12,(vi)seq id no.13,以及(vii)seq id no.14。
[0496]
实施方案4.一种工程化的nk细胞,其包含:用于所述工程化的nk细胞中增强的cd16信号传导的cd16变体,所述cd16变体包含cd16的至少一部分和cd64的至少一部分,其中所述工程化的nk细胞展现内源免疫调节多肽的降低的表达或活性,任选地其中:(1)所述工程化的nk细胞还包含异源il-15或其片段;和/或(2)所述工程化的nk细胞还包含含有异源il-15r或其片段的受体;和/或(3)所述工程化的nk细胞源自分离的干细胞或诱导干细胞。
[0497]
实施方案5.一种工程化的nk细胞,其包含内源il-17信号传导的降低的活性,其中所述工程化的nk细胞源自分离的干细胞或诱导干细胞,任选地其中:(1)所述工程化的nk细胞包含内源il-17或内源il-17r的降低的表达;和/或(2)所述工程化的nk细胞包含内源il-17和内源il-17r的降低的表达;和/或(3)所述内源il-17是il-17a;和/或(4)所述内源il-17是il-17f;和/或(5)所述内源il-17r包含il-17ra、il-17rb、il-17rc、il-17rd或il-17re;和/或(6)所述内源il-17r包含il-17ra;和/或(7)所述工程化的nk细胞还包含异源il-15或其片段;和/或(8)所述工程化的nk细胞还包含含有异源il-15r或其片段的受体;和/或
(9)所述工程化的nk细胞源自分离的干细胞或诱导干细胞;和/或(10)如与不具有内源il-17的降低的表达或活性的对照细胞相比,所述工程化的nk细胞展现nk细胞标记的增强的表达谱;和/或(11)所述nk细胞标记包含人cd57或杀伤免疫球蛋白样受体(kir);和/或(12)在肿瘤细胞的存在下,如与不具有内源il-17信号传导的降低的活性的对照细胞相比,所述工程化的nk细胞展现增强的存活。
[0498]
实施方案6.一种工程化的nk细胞,其包含异源stat,其中所述工程化的nk细胞源自分离的干细胞或诱导干细胞,任选地其中:(1)在肿瘤细胞的存在下,如与不具有所述异源stat的对照细胞相比,所述工程化的nk细胞展现增强的存活;和/或(2)所述异源stat包含stat1、stat2、stat3、stat4、stat3、stat4、stat5a、stat5b或stat6;和/或(3)所述异源stat包含stat3;和/或(4)所述异源stat包含stat5b;和/或(5)所述工程化的nk细胞还包含异源il-15或其片段;和/或(6)所述工程化的nk细胞还包含含有异源il-15r或其片段的受体。
[0499]
实施方案7.一种工程化的nk细胞,其包含:内源杀伤细胞免疫球蛋白样受体(kir)的降低的表达或活性,其中所述工程化的nk细胞还包含以下中的一种或多种:(a)包含能够与抗原结合的抗原结合部分的嵌合多肽受体,(b)异源细胞因子,(c)用于如与对照细胞相比增强的cd16信号传导的cd16变体,其中所述cd16变体对于工程化的nk细胞是异源的,(d)异源免疫调节多肽,和/或(e)内源免疫调节多肽的降低的表达或活性,任选地其中:(1)所述工程化的nk细胞包含所述嵌合多肽受体;和/或(2)所述工程化的nk细胞包含所述异源细胞因子;和/或(3)所述工程化的nk细胞包含所述cd16变体;和/或(4)所述工程化的nk细胞包含所述异源免疫调节多肽;和/或(5)所述工程化的nk细胞包含内源免疫调节多肽的降低的表达或活性;和/或(6)所述工程化的nk细胞包含(a)-(e)中的两种或更多种;和/或(7)所述工程化的nk细胞包含(a)-(e)中的三种或更多种;和/或(8)所述工程化的nk细胞包含(a)-(e)中的四种或更多种;和/或(9)所述工程化的nk细胞包含(a)-(e)的全部;和/或(10)所述kir包含kir2d;和/或(11)所述kir2d包含kir2dl1、kir2dl2、kir2dl3、kir2dl4、kir2dl5a、kir2dl5b、kir2ds1、kir2ds2、kir2ds3、kir2ds4或kir2ds5;和/或
(12)所述kir包含kir3d;和/或(13)所述kir3d包含kir3dl1、kir3dl2、kir3dl3或kir3ds1;和/或(14)所述工程化的nk细胞还包含异源il-15或其片段;和/或(15)所述工程化的nk细胞还包含含有异源il-15r或其片段的受体;和/或(16)所述工程化的nk细胞源自分离的干细胞或诱导干细胞。
[0500]
实施方案8.一种工程化的nk细胞,其包含:以下中的一种或多种的降低的表达或活性:(i)内源cd94,(ii)内源cd96,(iii)内源tgfβ受体,和/或(iv)内源ship2,其中所述工程化的细胞源自分离的干细胞或诱导干细胞,任选地其中:(1)所述工程化的nk细胞包含所述内源cd94的降低的表达或活性;和/或(2)所述工程化的nk细胞包含所述内源cd96的降低的表达或活性;和/或(3)所述工程化的nk细胞包含所述内源tgfβ受体的降低的表达或活性;和/或(4)所述工程化的nk细胞包含所述内源ship2的降低的表达或活性;和/或(5)所述工程化的nk细胞包含(i)-(iv)中的两种或更多种的降低的表达或活性;和/或(6)所述工程化的nk细胞包含(i)-(iv)中的三种或更多种的降低的表达或活性;和/或(7)所述工程化的nk细胞包含(i)-(iv)的降低的表达或活性;和/或(8)所述工程化的nk细胞还包含异源il-15或其片段;和/或(9)所述工程化的nk细胞还包含含有异源il-15r或其片段的受体;和/或(10)所述工程化的nk细胞源自分离的干细胞或诱导干细胞。
[0501]
实施方案9.一种工程化的nk细胞,其包含:以下中的一种或多种的降低的表达或活性:(i)内源cd80,(ii)内源cd86,(iii)内源icosl,(iv)内源cd40l,(v)内源mica或micb,和/或(vi)内源nkg2dl,其中所述工程化的细胞源自分离的干细胞或诱导干细胞,任选地其中:(1)所述工程化的nk细胞包含内源cd80的降低的表达或活性;和/或(2)所述工程化的nk细胞包含内源cd86的降低的表达或活性;和/或(3)所述工程化的nk细胞包含内源icosl的降低的表达或活性;和/或(4)所述工程化的nk细胞包含内源cd40l的降低的表达或活性;和/或
(5)所述工程化的nk细胞包含内源mica或micb的降低的表达或活性;和/或(6)所述工程化的nk细胞包含内源nkg2d的降低的表达或活性;和/或(7)所述工程化的nk细胞包含(i)-(vi)中的两种或更多种的降低的表达或活性;和/或(8)所述工程化的nk细胞包含(i)-(vi)中的三种或更多种的降低的表达或活性;和/或(9)所述工程化的nk细胞包含(i)-(vi)中的四种或更多种的降低的表达或活性;和/或(10)所述工程化的nk细胞包含(i)-(vi)中的五种或更多种的降低的表达或活性;和/或(11)所述工程化的nk细胞包含(i)-(vi)的降低的表达或活性;和/或(12)所述工程化的nk细胞还包含异源il-15或其片段;和/或(13)所述工程化的nk细胞还包含含有异源il-15r或其片段的受体。
[0502]
实施方案10.一种工程化的nk细胞,其包含:内源icam1的降低的表达或活性,其中所述工程化的细胞还包含以下中的一种或多种:(a)包含能够与抗原结合的抗原结合部分的嵌合多肽受体,(b)异源细胞因子,和/或(c)用于如与对照细胞相比增强的cd16信号传导的cd16变体,其中所述cd16变体对于工程化的nk细胞是异源的,任选地其中:(1)所述工程化的nk细胞包含所述嵌合多肽受体;和/或(2)所述工程化的nk细胞包含所述异源细胞因子;和/或(3)所述工程化的nk细胞包含所述cd16变体;和/或(4)所述工程化的nk细胞包含(a)-(c)中的两种或更多种;和/或(5)所述工程化的nk细胞包含(a)-(c)中的全部;和/或(6)所述工程化的nk细胞还包含异源il-15或其片段;和/或(7)所述工程化的nk细胞还包含含有异源il-15r或其片段的受体;和/或(8)所述工程化的nk细胞源自分离的干细胞或诱导干细胞。
[0503]
实施方案11.一种工程化的nk细胞,其包含内源icam1的降低的表达或活性,其中所述工程化的细胞源自诱导干细胞。任选地其中:(1)所述工程化的nk细胞还包含异源il-15或其片段;和/或(2)所述工程化的nk细胞还包含含有异源il-15r或其片段的受体;和/或(3)所述工程化的nk细胞源自分离的干细胞或诱导干细胞。
[0504]
实施方案12.一种工程化的nk细胞,其包含以下中的一种或多种:(i)异源pd-l2或(ii)异源tgf-β,任选地其中:(1)所述工程化的nk细胞包含所述异源pd-l2;和/或
(2)所述工程化的nk细胞包含所述异源tgf-β;和/或(3)所述工程化的nk细胞包含(i)所述异源pd-l2和(ii)所述异源tgf-β;和/或(4)所述工程化的nk细胞还包含异源il-15或其片段;和/或(5)所述工程化的nk细胞还包含含有异源il-15r或其片段的受体;和/或(6)所述工程化的nk细胞源自分离的干细胞或诱导干细胞。
[0505]
实施方案13.一种工程化的nk细胞,其包含以下中的一种或多种:(i)异源ccl21,(ii)异源il-10,(iii)异源cd46,(iv)异源cd55,和/或(v)异源cd59,其中所述工程化的细胞源自分离的干细胞或诱导干细胞,任选地其中:(1)所述工程化的nk细胞包含所述异源ccl21;和/或(2)所述工程化的nk细胞包含所述异源il-10;和/或(3)所述工程化的nk细胞包含所述异源cd46;和/或(4)所述工程化的nk细胞包含所述异源cd55;和/或(5)所述工程化的nk细胞包含所述异源cd59;和/或(6)所述工程化的nk细胞包含(i)-(v)中的两种或更多种;和/或(7)所述工程化的nk细胞包含(i)-(v)中的三种或更多种;和/或(8)所述工程化的nk细胞包含(i)-(v)中的四种或更多种;和/或(9)所述工程化的nk细胞包含(i)-(v)中的全部;和/或(10)所述工程化的nk细胞还包含异源il-15或其片段;和/或(11)所述工程化的nk细胞还包含含有异源il-15r或其片段的受体。
[0506]
实施方案14.一种源自诱导干细胞的工程化的nk细胞,其包含并非il-15的异源细胞因子,任选地其中并非il-15的所述异源细胞因子包含il-21。
[0507]
实施方案15.一种源自诱导干细胞的工程化的nk细胞,其包含异源il-21,任选地其中:(1)所述工程化的nk细胞还包含异源il-15或其片段;和/或(2)所述工程化的nk细胞还包含含有异源il-15r或其片段的受体。
[0508]
实施方案16.一种工程化的nk细胞,其包含:包含能够与cd38特异性结合的抗原结合部分的嵌合多肽受体,其中所述工程化的nk细胞源自分离的胚胎干细胞或诱导干细胞,任选地其中:(1)所述工程化的nk细胞还包含异源il-15或其片段;和/或(2)所述工程化的nk细胞还包含含有异源il-15r或其片段的受体。
[0509]
实施方案17.一种工程化的nk细胞,其包含:嵌合多肽受体,所述嵌合多肽受体包含cd8跨膜结构域以及(i)2b4信号传导结构
域和(ii)dap10信号传导结构域中的一个或多个,任选地其中:(1)所述嵌合多肽受体包含2b4信号传导结构域;和/或(2)所述嵌合多肽受体包含dap10信号传导结构域;和/或(3)所述嵌合多肽受体包含(i)2b4信号传导结构域和(ii)dap10信号传导结构域;和/或(4)所述工程化的nk细胞还包含异源il-15或其片段;和/或(5)所述工程化的nk细胞还包含含有异源il-15r或其片段的受体;和/或(6)所述工程化的nk细胞源自分离的干细胞或诱导干细胞。
[0510]
实施方案18.一种源自分离的干细胞或诱导干细胞的工程化的nk细胞,所述工程化的nk细胞包含:包含以下中的一个或多个的嵌合多肽受体:(i)cd8跨膜结构域,(ii)2b4信号传导结构域,或(iii)dap10信号传导结构域,任选地其中:(1)所述嵌合多肽受体包含cd8跨膜结构域;和/或(2)所述嵌合多肽受体包含2b4信号传导结构域;和/或(3)所述嵌合多肽受体包含dap10信号传导结构域;和/或(4)所述嵌合多肽受体包含(i)-(iii)中的两个或更多个;和/或(5)所述嵌合多肽受体包含(i)-(iii)中的全部;和/或(6)所述工程化的nk细胞还包含异源il-15或其片段;和/或(7)所述工程化的nk细胞还包含含有异源il-15r或其片段的受体。
[0511]
实施方案19.一种工程化的nk细胞,其包含:包含能够与cd23特异性结合的抗原结合部分的嵌合多肽受体,任选地其中:(1)所述工程化的nk细胞还包含异源il-15或其片段;和/或(2)所述工程化的nk细胞还包含含有异源il-15r或其片段的受体;和/或(3)所述工程化的nk细胞源自分离的干细胞或诱导干细胞。
[0512]
实施方案20.一种工程化的nk细胞,其包含:包含能够与cd123特异性结合的抗原结合部分的嵌合多肽受体,其中所述工程化的nk细胞源自分离的干细胞或诱导干细胞,任选地其中:(1)所述工程化的nk细胞还包含异源il-15或其片段;和/或(2)所述工程化的nk细胞还包含含有异源il-15r或其片段的受体。
[0513]
实施方案21.一种工程化的nk细胞,其包含:包含能够与cd7特异性结合的抗原结合部分的嵌合多肽受体,其中所述工程化的nk细胞展现内源cd7的降低的表达或活性,任选地其中:(1)tcr的表达或活性在所述工程化的nk细胞中未被修饰;和/或(2)所述工程化的nk细胞还包含异源il-15或其片段;和/或
(3)所述工程化的nk细胞还包含含有异源il-15r或其片段的受体;和/或(4)所述工程化的nk细胞源自分离的干细胞或诱导干细胞。
[0514]
实施方案22.一种工程化的nk细胞,其包含表2中标识的多种免疫调节多肽的修饰的表达或活性的组合,其中所述多种免疫调节多肽的修饰的表达或活性的组合包含(i)一种或多种第一免疫调节多肽的降低的表达或活性,和(ii)一种或多种第二免疫调节多肽的增强的表达或活性,任选地其中:(1)所述一种或多种第一免疫调节多肽对于所述工程化的nk细胞是内源的;和/或(2)所述一种或多种第二免疫调节多肽对于所述工程化的nk细胞是异源的;和/或(3)所述工程化的nk细胞还包含含有能够与抗原结合的抗原结合部分的嵌合多肽受体;和/或(4)所述工程化的nk细胞还包含异源细胞因子;和/或(5)所述工程化的nk细胞还包含内源细胞因子的降低的表达或活性;(6)所述工程化的nk细胞还包含用于所述工程化的nk细胞中增强的cd16信号传导的cd16变体;和/或(7)所述工程化的nk细胞还包含安全开关;和/或(8)如与对照细胞相比,所述工程化的nk细胞展现增强的针对靶细胞的细胞毒性;和/或(9)如与对照细胞相比,所述工程化的nk细胞在宿主细胞中诱导降低的免疫应答,任选地其中所述宿主细胞是免疫细胞;和/或(10)所述工程化的nk细胞源自分离的干细胞,任选地其中:(a)所述分离的干细胞包含胚胎干细胞;和/或(b)所述诱导干细胞包含诱导多能干细胞。
[0515]
实施方案23.根据前述实施方案1-22中任一项所述的工程化的nk细胞,任选地其中:(1)所述工程化的nk细胞展现内源cd38的降低的表达或活性;和/或(2)所述工程化的nk细胞的内源cd38的表达或活性未被修饰;和/或(3)所述异源il-15或其片段由所述工程化的nk细胞分泌;和/或(4)所述异源il-15或其片段是膜结合的;和/或(5)所述工程化的nk细胞还包含含有能够与抗原结合的抗原结合部分的嵌合多肽受体;和/或(6)所述工程化的nk细胞还包含含有能够与不同抗原结合的抗原结合部分的另外的嵌合多肽受体;和/或(7)所述嵌合多肽受体的抗原结合部分是能够与不同的两种或更多种抗原特异性结合的多特异性结合部分;和/或(8)所述抗原包括选自以下的一个或多个成员:bcma、cd19、cd20、cd22、cd30、cd33、cd38、cd70、κ、lewis y、nkg2d配体、ror1、ny-eso-1、ny-eso-2、mart-1和gp100;和/或
(9)所述抗原包括选自以下的nkg2d配体:mica、micb、ulbp1、ulbp2、ulbp3、ulbp4、ulbp5和ulbp6;和/或(10)所述工程化的nk细胞还包含能够实现所述工程化的nk细胞的死亡的安全开关;和/或(11)所述安全开关包括选自以下的一个或多个成员:胱天蛋白酶(例如,胱天蛋白酶3、7或9)、胸苷激酶、胞嘧啶脱氨酶、修饰的egfr和b细胞cd20;和/或(12)所述工程化的nk细胞还包含异源细胞因子;和/或(13)所述异源细胞因子包括选自以下的一个或多个成员:il6、il7、il9、il10、il11、il12、il15、il18和il21;和/或(14)所述工程化的nk细胞还包含异源免疫调节多肽;和/或(15)所述异源免疫调节多肽包括选自以下的一个或多个成员:hla-e、cd47、cd113、pdl1、pdl2、a2ar、hla-g、tgf-β、ccl21、il10、cd46、cd55和cd59;和/或(16)所述工程化的nk细胞展现内源免疫调节多肽的降低的表达或活性;和/或(17)所述内源免疫调节多肽包含免疫检查点抑制剂或低免疫性调节剂;和/或(18)所述免疫检查点抑制剂包括选自以下的一个或多个成员:pd1、ctla-4、tim-3、kir2d、cd94、nkg2a、nkg2d、it、cd96、lag3、tigit、tgfβ受体和2b4;和/或(19)所述免疫检查点抑制剂包含ship2;(20)所述低免疫性调节剂包括选自以下的一个或多个成员:b2m、ciita、tap1、tap2、tapasin、nlrc5、rfxank、rfx5、rfxap、cd80、cd86、icosl、cd40l、icam1、mica、micb、ulbp1、hla-e、cd47、cd113、pdl1、pdl2、a2ar、hla-g、tgf-β、ccl21、il10、cd46、cd55和cd59;和/或(21)包含用于如与对照细胞相比增强的cd16信号传导的cd16变体,其中所述cd16变体对于工程化的nk细胞是异源的;和/或(22)所述cd16变体包含选自以下的序列:seq id no.1-8;(23)如与对照细胞相比,所述工程化的nk细胞展现增强的针对靶细胞的细胞毒性;和/或(24)如与对照细胞相比,所述工程化的nk细胞在宿主细胞中诱导降低的免疫应答;和/或(25)所述宿主细胞是免疫细胞;和/或(26)所述分离的干细胞包含胚胎干细胞;和/或(27)所述诱导干细胞包含诱导多能干细胞。
[0516]
实施方案24.根据前述实施方案1-23中任一项所述的工程化的nk细胞,任选地其中:(1)所述工程化的nk细胞用于诱导靶细胞死亡的方法中,任选地其中所述靶细胞是癌细胞或肿瘤细胞;和/或(2)所述工程化的nk细胞用于治疗有需要的受试者的方法中,其中所述受试者患有或怀疑患有病症,任选地其中所述病症是癌症或肿瘤,任选地其中所述工程化的nk细胞对于所述受试者是自体的或同种异体的;(3)所述工程化的nk细胞用于制造用于诱导靶细胞死亡的药物,任选地其中所述
靶细胞是癌细胞或肿瘤细胞;和/或(4)所述工程化的nk细胞用于制造用于治疗有需要的受试者的药物,其中所述受试者患有或怀疑患有病症,任选地其中所述病症是癌症或肿瘤,任选地其中所述工程化的nk细胞对于所述受试者是自体的或同种异体的。
[0517]
实施方案25.一种方法,其包括:从受试者获得细胞;以及从所述细胞生成根据前述实施方案1-24中任一项所述的工程化的nk细胞。
[0518]
实施方案26.一种方法,其包括:向有需要的受试者施用包含根据前述实施方案1-24中任一项所述的工程化的nk细胞的nk细胞群体,任选地其中所述方法还包括向所述受试者施用单独治疗剂,进一步任选地其中所述单独治疗剂是化学治疗剂。
[0519]
实施方案27.一种组合物,所述组合物包含:根据前述实施方案1-24中任一项所述的工程化的nk细胞,以及能够与cd20结合的单独治疗剂。
[0520]
实施方案28.一种组合物,所述组合物包含:包括一个或多个成员的工程化的免疫细胞,其包含:(i)异源il-15或其片段,(ii)用于如与对照细胞相比增强的cd16信号传导的cd16变体,其中所述cd16变体对于所述工程化的免疫细胞是异源的,和或(iii)包含能够与抗原结合的抗原结合部分的嵌合多肽受体;以及能够与cd20结合的单独治疗剂;任选地其中:(1)所述工程化的免疫细胞包含所述异源il-15;和/或(2)所述异源il-15或其片段由所述工程化的免疫细胞分泌;和/或(3)所述异源il-15或其片段是膜结合的;和/或(4)所述工程化的免疫细胞包含所述cd16变体;和/或(5)所述cd16变体包含选自以下的序列:seq id no.1-8;和/或(6)所述工程化的免疫细胞包含所述嵌合多肽受体;和/或(7)所述工程化的免疫细胞包含(i)-(iii)中的两种或更多种;和/或(8)所述工程化的免疫细胞包含(i)-(iii);和/或(9)所述工程化的免疫细胞包含工程化的nk细胞;和/或(10)所述工程化的免疫细胞包含工程化的t细胞;和/或(11)所述工程化的细胞展现内源cd38的降低的表达或活性;和/或(12)所述工程化的细胞的内源cd38的表达或活性未被修饰;(13)所述嵌合多肽受体的抗原结合部分是能够与不同的两种或更多种抗原特异性结合的多特异性结合部分;和/或(14)所述抗原包括选自以下的一个或多个成员:bcma、cd19、cd20、cd22、cd30、cd33、cd38、cd70、κ、lewis y、nkg2d配体、ror1、ny-eso-1、ny-eso-2、mart-1和gp100;和/或
(15)所述抗原包含选自以下的nkg2d配体:mica、micb、ulbp1、ulbp2、ulbp3、ulbp4、ulbp5和ulbp6;和/或(16)所述工程化的免疫细胞还包含能够实现所述工程化的免疫细胞的死亡的安全开关;和/或(17)所述安全开关包括选自以下的一个或多个成员:胱天蛋白酶(例如,胱天蛋白酶3、7或9)、胸苷激酶、胞嘧啶脱氨酶、修饰的egfr和b细胞cd20;和/或(18)所述工程化的免疫细胞还包含异源细胞因子;和/或(19)所述异源细胞因子包括选自以下的一个或多个成员:il6、il7、il9、il10、il11、il12、il15、il18和il21;和/或(20)所述工程化的免疫细胞还包含异源免疫调节多肽;和/或(21)所述异源免疫调节多肽包括选自以下的一个或多个成员:hla-e、cd47、cd113、pdl1、pdl2、a2ar、hla-g、tgf-β、ccl21、il10、cd46、cd55和cd59;和/或(22)所述工程化的免疫细胞展现内源免疫调节多肽的降低的表达或活性;和/或(23)所述内源免疫调节多肽包含免疫检查点抑制剂或低免疫性调节剂;和/或(24)所述免疫检查点抑制剂包括选自以下的一个或多个成员:pd1、ctla-4、tim-3、kir2d、cd94、nkg2a、nkg2d、it、cd96、lag3、tigit、tgfβ受体和2b4;和/或(25)所述免疫检查点抑制剂包含ship2;和/或(26)所述低免疫性调节剂包括选自以下的一个或多个成员:b2m、ciita、tap1、tap2、tapasin、nlrc5、rfxank、rfx5、rfxap、cd80、cd86、icosl、cd40l、icam1、mica、micb、ulbp1、hla-e、cd47、cd113、pdl1、pdl2、a2ar、hla-g、tgf-β、ccl21、il10、cd46、cd55和cd59;和/或(27)如与对照细胞相比,所述工程化的nk细胞展现增强的针对靶细胞的细胞毒性;和/或(28)如与对照细胞相比,所述工程化的nk细胞在宿主细胞中诱导降低的免疫应答;和/或(29)所述宿主细胞是免疫细胞;和/或(30)所述工程化的nk细胞还包含含有异源il-15r或其片段的受体;和/或(31)所述工程化的nk细胞源自分离的干细胞或诱导干细胞;和/或(32)所述分离的干细胞包含胚胎干细胞;和/或(33)所述诱导干细胞包含诱导多能干细胞。
[0521]
实施方案29.一种方法,其包括向有需要的受试者施用根据实施方案27或实施方案28所述的组合物,任选地其中所述单独治疗剂是化学治疗剂。
[0522]
实施方案30.一种工程化的nk细胞的群体,其中:工程化的nk细胞的所述群体的工程化的nk细胞包含异源多肽,其中所述异源多肽包括异源il-15,并且工程化的nk细胞的所述群体在基本上不含外源白介素-2(il-2)的环境中的持久性水平比nk细胞的可比较群体在包含外源il-2的对照环境中的对照持久性水平高至少约5%,
任选地其中:(1)所述异源il-15是膜结合il-15,任选地其中所述异源多肽是包含所述异源il-15和il-15受体的至少一部分的融合多肽;和/或(2)所述异源il-15是分泌型il-15;和/或(3)所述持久性水平比所述对照持久性水平高至少约10%;和/或(4)所述持久性水平比所述对照持久性水平高至少约20%;和/或(5)所述持久性水平比所述对照持久性水平高至少约30%;和/或(6)所述持久性水平和所述对照持久性水平分别是在所述环境和所述对照环境中至少约5天后观察到的;和/或(7)所述持久性水平和所述对照持久性水平分别是在所述环境和所述对照环境中至少约15天后观察到的;和/或(8)所述持久性水平和所述对照持久性水平分别是在所述环境和所述对照环境中至少约21天后观察到的;和/或(9)所述外源白介素在所述环境中的量在约10单位/毫升(u/ml)与约500u/ml之间;和/或(10)所述环境在体外;和/或(11)所述持久性水平是在将工程化的nk细胞的所述群体施用至有需要的受试者的身体中之后查明的;和/或(12)所述工程化的nk细胞包含编码所述异源多肽的异源多核苷酸序列;和/或(13)所述工程化的nk细胞还包含用于增强的cd16信号传导的异源cd16变体;和/或(14)所述工程化的nk细胞还包含含有能够与抗原结合的抗原结合部分的嵌合多肽受体;和/或(15)所述工程化的nk细胞包含编码所述抗原的内源基因的降低的表达或活性水平;和/或(16)所述工程化的nk细胞包含内源cd38的降低的表达或活性水平;和/或(17)所述工程化的nk细胞源自分离的干细胞或诱导干细胞。
[0523]
实施方案31.一种工程化的nk细胞的群体,其中:所述群体的工程化的nk细胞包含异源分泌型il-15,并且工程化的nk细胞的所述群体展现至少约0的il-15的内源下游信号传导蛋白的信号传导水平;和/或比缺乏所述异源分泌型il-15的nk细胞的对照群体的内源下游信号传导蛋白的对照信号传导水平高1倍,任选地其中:(1)所述信号传导水平是所述内源下游信号传导蛋白的磷酸化水平;和/或(2)所述信号传导水平比所述对照信号传导水平高至少0.5倍;和/或(3)所述信号传导水平比所述对照信号传导水平高至少1倍;和/或(4)所述信号传导水平比所述对照信号传导水平高至少5倍;和/或(5)所述内源下游信号传导蛋白包含stat;和/或
(6)所述内源下游信号传导蛋白包含stat5;和/或(7)所述信号传导水平是在基本上不含外源白介素的环境中观察到的;和/或(8)所述外源白介素包括il-2和/或il-15;和/或(9)所述工程化的nk细胞不含异源il-15受体;和/或(10所述工程化的nk细胞还包含编码所述异源分泌型il-15的异源多核苷酸序列;和/或(11)所述工程化的nk细胞还包含用于增强的cd16信号传导的异源cd16变体;和/或(12)所述工程化的nk细胞还包含含有能够与抗原结合的抗原结合部分的嵌合多肽受体;和/或(13)所述工程化的nk细胞包含编码所述抗原的内源基因的降低的表达或活性水平;和/或(14)所述工程化的nk细胞包含内源cd38的降低的表达或活性水平;和/或(15)所述工程化的nk细胞源自分离的干细胞或诱导干细胞。
[0524]
实施方案32.一种工程化的nk细胞的群体,其中:工程化的nk细胞的所述群体的工程化的nk细胞包含包括选自pd-l2、tgf-β、cd46、cd55和cd59的一个或多个成员的至少一种异源低免疫性调节多肽,并且如与缺乏所述至少一种异源低免疫性调节多肽的nk细胞的对照群体相比,工程化的nk细胞的所述群体展现增强的针对免疫排斥的抗性,任选地其中:(1)所述增强的针对免疫排斥的抗性是至少约5%;和/或(2)所述增强的针对免疫排斥的抗性是至少约10%;和/或(3)所述增强的针对免疫排斥的抗性是至少约20%;和/或(4)所述增强的针对免疫排斥的抗性是至少约50%;和/或(5)所述增强的针对免疫排斥的抗性是在体外在包含至少约10%人补体的培养基中查明的;和/或(6)所述增强的针对免疫排斥的抗性是在体外在包含至少约20%人补体的培养基中查明的;和/或(7)所述增强的针对免疫排斥的抗性是在体外在包含至少约40%人补体的培养基中查明的;和/或(8)所述增强的针对免疫排斥的抗性是在将工程化的nk细胞的所述群体施用至有需要的受试者的身体中之后查明的;和/或(9)所述工程化的nk细胞包含编码所述至少一种异源低免疫性调节多肽的异源多核苷酸序列;和/或(10)所述至少一种异源低免疫性调节多肽包含pd-l2;和/或(11)所述至少一种异源低免疫性调节多肽包含tgf-β;和/或(12)所述至少一种异源低免疫性调节多肽包含cd46;和/或(13)所述至少一种异源低免疫性调节多肽包含cd55;和/或(14)所述至少一种异源低免疫性调节多肽包含cd59;和/或
(15)所述至少一种异源低免疫性调节多肽包括选自以下的两个或更多个成员:pd-l2、tgf-β、cd46、cd55和cd59;和/或(16)所述工程化的nk细胞还包含包括选自以下的一个或多个成员的至少另外的异源低免疫性调节多肽:hla-g、pd-l1、hla-e、cd47、il-10、ccl-21和cd59;和/或(17)所述工程化的nk细胞还包含包括hla-g的至少另外的异源低免疫性调节多肽;和/或(18)所述工程化的nk细胞还包含包括pd-l1的至少另外的异源低免疫性调节多肽;和/或(19)所述工程化的nk细胞还包含包括hla-e的至少另外的异源低免疫性调节多肽;和/或(20)所述工程化的nk细胞还包含包括cd47的至少另外的异源低免疫性调节多肽;和/或(21)所述工程化的nk细胞还包含包括il-10的至少另外的异源低免疫性调节多肽;和/或(22)所述工程化的nk细胞还包含包括ccl-21的至少另外的异源低免疫性调节多肽;和/或(23)所述工程化的nk细胞还包含包括cd59的至少另外的异源低免疫性调节多肽;和/或(24)所述工程化的nk细胞还包含包括选自以下的一个或多个成员的至少一种内源免疫调节多肽的降低的表达或活性:mica、micb、ulbp1、b2m、ciita和icam-1;和/或(25)所述工程化的nk细胞还包含包括选自以下的一个或多个成员的至少一种内源免疫调节多肽的降低的表达或活性:mica、micb和ulbp1;和/或(26)所述工程化的nk细胞还包含包括mica的至少一种内源免疫调节多肽的降低的表达或活性;和/或(27)所述工程化的nk细胞还包含包括micb的至少一种内源免疫调节多肽的降低的表达或活性;和/或(28)所述工程化的nk细胞还包含包括ulbp1的至少一种内源免疫调节多肽的降低的表达或活性;和/或(29)所述工程化的nk细胞还包含包括选自以下的一个或多个成员的至少一种内源免疫调节多肽的降低的表达或活性:b2m和ciita;和/或(30)所述工程化的nk细胞还包含包括icam-1的至少一种内源免疫调节多肽的降低的表达或活性;和/或(31)所述工程化的nk细胞还包含异源il-15;和/或(32)所述工程化的nk细胞还包含用于增强的cd16信号传导的异源cd16变体;和/或(33)所述工程化的nk细胞还包含含有能够与抗原结合的抗原结合部分的嵌合多肽受体;和/或(34)所述工程化的nk细胞包含编码所述抗原的内源基因的降低的表达或活性水平;和/或
(35)所述工程化的nk细胞包含内源cd38的降低的表达或活性水平;和/或(36)所述工程化的nk细胞源自分离的干细胞或诱导干细胞。
[0525]
实施方案33.一种工程化的nk细胞的群体,其中:工程化的nk细胞的所述群体的工程化的nk细胞包含多种异源低免疫性调节多肽,并且如与缺乏所述多种异源低免疫性调节多肽中的一种或多种的nk细胞的对照群体相比,工程化的nk细胞的所述群体展现增强至少约5%的针对免疫排斥的抗性,任选地其中:(1)所述增强的针对免疫排斥的抗性是至少约5%;和/或(2)所述增强的针对免疫排斥的抗性是至少约10%;和/或(3)所述增强的针对免疫排斥的抗性是至少约20%;和/或(4)所述增强的针对免疫排斥的抗性是至少约50%;和/或(5)所述增强的针对免疫排斥的抗性是在体外在包含至少约10%人补体的培养基中查明的;和/或(6)所述增强的针对免疫排斥的抗性是在体外在包含至少约20%人补体的培养基中查明的;和/或(7)所述增强的针对免疫排斥的抗性是在体外在包含至少约40%人补体的培养基中查明的;和/或(8)所述工程化的nk细胞包含编码所述多种异源低免疫性调节多肽的至少一种异源多核苷酸序列;和/或(9)所述多种异源低免疫性调节多肽包括选自以下的两个或更多个成员:pd-l2、tgf-β、cd46、cd55、cd59、hla-g、pd-l1、hla-e、cd47、il-10、ccl-21和cd59;和/或(10)所述多种异源低免疫性调节多肽包括选自以下的三个或更多个成员:pd-l2、tgf-β、cd46、cd55、cd59、hla-g、pd-l1、hla-e、cd47、il-10、ccl-21和cd59;和/或(11)所述多种异源低免疫性调节多肽包括选自以下的四个或更多个成员:pd-l2、tgf-β、cd46、cd55、cd59、hla-g、pd-l1、hla-e、cd47、il-10、ccl-21和cd59;和/或(12)所述多种异源低免疫性调节多肽包括选自以下的五个或更多个成员:pd-l2、tgf-β、cd46、cd55、cd59、hla-g、pd-l1、hla-e、cd47、il-10、ccl-21和cd59;和/或(13)所述多种异源低免疫性调节多肽包括选自以下的两个或更多个成员:pd-l2、tgf-β、cd46、cd55、cd59和hla-g;和/或(14)所述多种异源低免疫性调节多肽包括pd-l2;和/或(15)所述多种异源低免疫性调节多肽包括tgf-β;和/或(16)所述多种异源低免疫性调节多肽包括cd46;和/或(17)所述多种异源低免疫性调节多肽包括cd55;和/或(18)所述多种异源低免疫性调节多肽包括cd59;和/或(19)所述多种异源低免疫性调节多肽包括hla-g;和/或(20)所述多种异源低免疫性调节多肽包括pd-l1;和/或(21)所述多种异源低免疫性调节多肽包括hla-e;和/或(22)所述多种异源低免疫性调节多肽包括cd47;和/或
(23)所述多种异源低免疫性调节多肽包括il-10;和/或(24)所述多种异源低免疫性调节多肽包括ccl-21;和/或(25)所述多种异源低免疫性调节多肽包括cd59;和/或(26)所述工程化的nk细胞还包含包括选自以下的一个或多个成员的内源免疫调节多肽的降低的表达或活性:mica、micb、ulbp1、b2m、ciita和icam-1;和/或(27)所述工程化的nk细胞还包含包括选自以下的一个或多个成员的所述内源免疫调节多肽的降低的表达或活性:mica、micb和ulbp1;和/或(28)所述工程化的nk细胞还包含包括mica的所述内源免疫调节多肽的降低的表达或活性;和/或(29)所述工程化的nk细胞还包含包括micb的所述内源免疫调节多肽的降低的表达或活性;和/或(30)所述工程化的nk细胞还包含包括ulbp1的所述内源免疫调节多肽的降低的表达或活性;和/或(31)所述工程化的nk细胞还包含包括选自以下的一个或多个成员的所述内源免疫调节多肽的降低的表达或活性:b2m和ciita1;和/或(32)所述工程化的nk细胞还包含包括icam-1的所述内源免疫调节多肽的降低的表达或活性;和/或(33)所述工程化的nk细胞还包含异源il-15;和/或(34)所述工程化的nk细胞还包含用于增强的cd16信号传导的异源cd16变体;和/或(35)所述工程化的nk细胞还包含含有能够与抗原结合的抗原结合部分的嵌合多肽受体;和/或(36)所述工程化的nk细胞包含编码所述抗原的内源基因的降低的表达或活性水平;和/或(37)所述工程化的nk细胞包含内源cd38的降低的表达或活性水平;和/或(38)所述工程化的nk细胞源自分离的干细胞或诱导干细胞。
[0526]
实施方案34.一种工程化的nk细胞的群体,其中:工程化的nk细胞的所述群体的工程化的nk细胞包含(i)并非ptpn2的至少一种内源免疫调节多肽的降低的表达,和/或(ii)nkg2c的增强的或引入的表达,并且工程化的nk细胞的所述群体的持久性水平高于缺乏(i)和/或(ii)的nk细胞的对照群体的对照持久性水平,任选地其中:(1)nk细胞的所述对照群体包含内源ptpn2的降低的表达;和/或(2)所述持久性水平比所述对照持久性水平高至少约10%;和/或(3)所述持久性水平比所述对照持久性水平高至少约20%;和/或(4)所述持久性水平比所述对照持久性水平高至少约50%;和/或(5)所述持久性水平比所述对照持久性水平高至少约100%;和/或(6)所述工程化的nk细胞包含包括选自以下的一个或多个成员的所述至少一种内源免疫调节多肽的降低的表达:bcl3、cblb、cdk8、fcer1g、il17a、il17f、ship1、socs1、
socs2、socs3、stat3、tet3、ptpn6和cd70;和/或(7)所述工程化的nk细胞包含包括选自以下的两个或更多个成员的至少一种内源免疫调节多肽的降低的表达:bcl3、cblb、cdk8、fcer1g、il17a、il17f、ship1、socs1、socs2、socs3、stat3、tet3、ptpn6和cd70;和/或(8)所述至少一种内源免疫调节多肽包括bcl3;和/或(9)所述至少一种内源免疫调节多肽包括cblb;和/或(10)所述至少一种内源免疫调节多肽包括cdk8;和/或(11)所述至少一种内源免疫调节多肽包括fcer1g;和/或(12)所述至少一种内源免疫调节多肽包括il17a;和/或(13)所述至少一种内源免疫调节多肽包括il17f;和/或(14)所述至少一种内源免疫调节多肽包括ship1;和/或(15)所述至少一种内源免疫调节多肽包括socs1;和/或(16)所述至少一种内源免疫调节多肽包括socs2;和/或(17)所述至少一种内源免疫调节多肽包括socs3;和/或(18)所述至少一种内源免疫调节多肽包括stat3;和/或(19)所述至少一种内源免疫调节多肽包括tet3;和/或(20)所述至少一种内源免疫调节多肽包括ptpn6;和/或(21)所述至少一种内源免疫调节多肽包括cd70;和/或(22)所述工程化的nk细胞包含nkg2c的增强的或引入的表达;和/或(23)所述工程化的nk细胞包含内源nkg2c的增强的表达;和/或(24)所述工程化的nk细胞包含异源nkg2c;和/或(25)所述工程化的nk细胞包含包括选自以下的一个或多个成员的所述至少一种内源免疫调节多肽的降低的表达:nlrc5、rfxank、rfxap、cd80、cd7、tap2、tap1、tapbp;和/或(26)所述工程化的nk细胞包含包括选自以下的两个或更多个成员的至少一种内源免疫调节多肽的降低的表达:nlrc5、rfxank、rfxap、cd80、cd7、tap2、tap1、tapbp;和/或(27)所述工程化的nk细胞包含包括选自以下的三个或更多个成员的所述至少一种内源免疫调节多肽的降低的表达:nlrc5、rfxank、rfxap、cd80、cd7、tap2、tap1、tapbp;和/或(28)所述工程化的nk细胞包含包括选自以下的四个或更多个成员的所述至少一种内源免疫调节多肽的降低的表达:nlrc5、rfxank、rfxap、cd80、cd7、tap2、tap1、tapbp;和/或(29)所述工程化的nk细胞包含包括nlrc5的所述至少一种内源免疫调节多肽的降低的表达;和/或(30)所述工程化的nk细胞包含包括rfxank的所述至少一种内源免疫调节多肽的降低的表达;和/或(31)所述工程化的nk细胞包含包括rfxap的所述至少一种内源免疫调节多肽的降低的表达;和/或(32)所述工程化的nk细胞包含包括cd80的所述至少一种内源免疫调节多肽的降
低的表达;和/或(33)所述工程化的nk细胞包含包括cd7的所述至少一种内源免疫调节多肽的降低的表达;和/或(34)所述工程化的nk细胞包含包括tap2的所述至少一种内源免疫调节多肽的降低的表达;和/或(35)所述工程化的nk细胞包含包括tap1的所述至少一种内源免疫调节多肽的降低的表达;和/或(36)所述工程化的nk细胞包含包括tapbp的所述至少一种内源免疫调节多肽的降低的表达;和/或(37)所述工程化的nk细胞包含(i),并且nk细胞的所述对照群体缺乏(i);和/或(38)所述工程化的nk细胞包含(ii),并且nk细胞的所述对照群体缺乏(ii);和/或(39)所述工程化的nk细胞还包含异源il-15;和/或(40)所述工程化的nk细胞还包含用于增强的cd16信号传导的异源cd16变体;和/或(41)所述工程化的nk细胞还包含含有能够与抗原结合的抗原结合部分的嵌合多肽受体;和/或(42)所述工程化的nk细胞包含编码所述抗原的内源基因的降低的表达或活性水平;和/或(43)所述工程化的nk细胞包含内源cd38的降低的表达或活性水平;和/或(44)所述工程化的nk细胞源自分离的干细胞或诱导干细胞;和/或(45)所述至少一种内源免疫调节多肽不含socs1、socs2和/或socs3;和/或(46)所述工程化的nk细胞不含nkg2c的增强的或引入的表达。
[0527]
实施方案35.根据前述实施方案30-34中任一项所述的工程化的nk细胞的群体,任选地其中:(1)所述嵌合多肽受体是能够与不同的两种或更多种抗原特异性结合的多特异性结合部分;和/或(2)所述抗原包括选自以下的一个或多个成员:bcma、cd19、cd20、cd22、cd30、cd33、cd38、cd70、κ、lewis y、nkg2d配体、ror1、ny-eso-1、ny-eso-2、mart-1和gp100;和/或(3)所述抗原包括选自以下的nkg2d配体:mica、micb、ulbp1、ulbp2、ulbp3、ulbp4、ulbp5和ulbp6;和/或(4)所述工程化的免疫细胞还包含能够实现所述工程化的免疫细胞的死亡的安全开关;和/或(5)所述安全开关包括选自以下的一个或多个成员:胱天蛋白酶(e;和/或g;和/或,胱天蛋白酶3、7或9)、胸苷激酶、胞嘧啶脱氨酶、修饰的egfr和b细胞cd20。
[0528]
实施方案36.根据前述实施方案30-35中任一项所述的工程化的nk细胞的群体,任选地其中:(1)工程化的nk细胞的所述群体用于诱导靶细胞死亡的方法中,任选地其中所述靶细胞是癌细胞或肿瘤细胞;和/或(2)工程化的nk细胞的所述群体用于治疗有需要的受试者,其中所述受试者患有
或怀疑患有病症,任选地其中所述病症是癌症或肿瘤,进一步任选地其中所述工程化的nk细胞对于所述受试者是自体的或同种异体的;和/或(3)工程化的nk细胞的所述群体用于制造用于诱导靶细胞死亡的药物,任选地其中所述靶细胞是癌细胞或肿瘤细胞;和/或(4)工程化的nk细胞的所述群体用于制造用于治疗有需要的受试者的药物,其中所述受试者患有或怀疑患有病症,任选地其中所述病症是癌症或肿瘤,进一步任选地其中所述工程化的nk细胞对于所述受试者是自体的或同种异体的。
[0529]
实施方案37.一种组合物,其包含根据前述实施方案30-35中任一项所述的工程化的nk细胞的群体,任选地其中所述组合物还包含单独治疗剂,进一步任选地其中所述治疗剂是化学治疗剂。
[0530]
实施方案38.一种方法,其包括:从受试者获得一种或多种细胞;以及从所述一种或多种细胞生成根据前述实施方案30-35中任一项所述的工程化的nk细胞的群体,任选地其中所述一种或多种细胞是nk细胞、造血干细胞或成纤维细胞。
[0531]
实施方案39.一种方法,其包括将一种或多种诱导多能干细胞工程化以生成根据前述实施方案30-35中任一项所述的工程化的nk细胞的群体。
[0532]
实施方案40.一种方法,其包括向有需要的受试者施用根据前述实施方案30-35中任一项所述的工程化的nk细胞的群体,任选地其中所述方法还包括向所述受试者施用单独治疗剂,进一步任选地其中所述单独治疗剂是化学治疗剂。
[0533]
应理解,本发明的不同方面可以单独地、共同地或彼此组合地来了解。本文所述的本发明的各个方面可以应用于本文所公开的任何特定应用。包括本公开文本的工程化的免疫细胞的物质组合物可以用于方法章节中,包括本文所公开的使用和产生方法,或反之亦然。
[0534]
虽然在本文中已经示出和描述了本发明的优选实施方案,但是对于本领域的技术人员来说,显然这些实施方案仅作为举例提供。本发明不受说明书中提供的具体例子的限制。虽然已经参考前述说明书描述了本发明,但是这里对实施方案的描述和图示并不意味着限制。在不脱离本发明的情况下,本领域技术人员将会想到许多变化、改变和替换。此外,应当理解,本发明的所有方面不限于这里根据各种条件和变量阐述的具体描述、配置或相对比例。应当理解,在实践本发明时,可以采用在本文中描述的本发明实施方案的各种替代方案。因此,预期本发明也将覆盖任何这样的替换、修改、变化或等同物。下面的权利要求旨在限定本发明的范围,从而覆盖在这些权利要求及其等同物的范围内的方法和结构。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。