1.本发明涉及医药技术领域,特别是涉及一种木脂素苷类化合物及其制备方法和应用。
背景技术:
2.现代社会人们生活节奏加快,工作压力越来越大,疲劳作为一种慢性疾病,在逐渐侵蚀着现代社会人们的健康。疲劳是一种主观的不适感,主要表现为疲劳感、倦怠感,在进行长时间劳动、剧烈运动或长时间精神压力下会察觉到,这是一种正常的生理性保护反应,提示机体应该通过休息使机能恢复,从而避免对身体的进一步伤害。长期处于疲劳状态,会损害人体的体力、体能,身体失衡,使人难以从事或完成某些消耗体力较大或动作细腻、精巧的工作,从而使工作效率下降;另一方面,长期疲劳还会使人皮肤松弛,面色无华,呈现出未老先衰的征兆长期疲劳得不到恢复,使人体免疫系统功能失调,甚至造成免疫低下,机体抵抗疾病的屏障被打破,使人们患病的几率增加。
3.产生疲劳的原因很多,主要是能源物质耗竭,代谢产物积累,神经递质失衡和自由基产生加剧等。脑力和体力疲劳发生的同时,也会伴随诸多生理生化指标的改变。运动性疲劳恢复需要快速修复体内发生的损伤或促进运动中积累的代谢产物清除。基于此,需要找到抗疲劳物质来延缓长时间劳动、剧烈运动或过度精神压力下造成的疲劳发生,或使疲劳状态尽快恢复到正常状态,以期使人们亚健康状态恢复正常或对疲劳综合征产生疗效。
技术实现要素:
4.基于此,有必要针对上述问题,提供一种木脂素苷类化合物及其制备方法和应用,本发明的木脂素苷类化合物能显著提高乳酸率,降低基体乳酸含量,降低运动后机体血清bun与ck水平,从而达到缓解和治疗疲劳的效果。
5.本发明提供一种木脂素苷类化合物,所述木脂素苷类化合物是以刺五加茎为原料,经过溶剂提取、分离得到。
6.本发明还提供一种木脂素苷类化合物,所述木脂素苷类化合物具有式(ⅰ)-(ⅳ)任一所示结构:
7.[0008][0009]
本发明还提供一种木脂素苷类化合物,其选自式(ⅳ)所示化合物。
[0010]
本发明另一方面还提供一种上述木脂素苷类化合物的制备方法,包括以下步骤:
[0011]
s1、取刺五加茎,在醇溶液中浸泡,超声提取,浓缩提取液,加醇,混合均匀后静置,待析出沉淀,分离沉淀和溶液,保留沉淀,将沉淀干燥,得刺五加提取物;
[0012]
s2、用流动相对刺五加提取物进行梯度洗脱,分别收集各洗脱液,浓缩,分离鉴定,即得木脂素苷类化合物。
[0013]
在其中一个实施例中,所述步骤s1具体为:取干燥、粉碎的刺五加茎,加入4~6倍体积的40~60%乙醇浸泡0.5~1.5小时,利用微波超声波协同法提取0.5~1.5小时,提取2~3次,合并提取液,用旋转蒸发仪浓缩提取液至0.2~0.4倍体积,冷却后,加入2~4倍体积的乙醇,搅拌,10~15℃静置20~28小时,待析出沉淀,分离沉淀,加热干燥去除溶剂,即得刺五加提取物。
[0014]
在其中一个实施例中,所述步骤s2具体为:利用羟丙基葡聚糖凝胶对刺五加提取物进行分离,以甲醇与水的体积比为0:10、1:9、2:8、3:7、4:6、5:5、6:4、7:3、8:2、9:1、10:0的流动相进行梯度洗脱,分别收集各洗脱液,浓缩,分别得到组分1至组分11,对组分1至组分11进行分离鉴定,即得木脂素苷类化合物。
[0015]
在其中一个实施例中,所述步骤s2中,分离组分3的具体步骤为:取组分3,经半制备反相高效液相色谱法,使用c18柱,利用14~16%乙醇溶液为流动相,等度洗脱55~65min,得到结构为式(ⅰ)和式(ⅱ)的化合物。
[0016]
在其中一个实施例中,所述步骤s2中,分离组分4的具体步骤为:取组分4,经半制备反相高效液相色谱法,使用c18柱,利用16~18%至20~22%乙醇溶液为流动相,梯度洗脱65~75min,得到结构为式(ⅲ)和式(ⅳ)的化合物。
[0017]
本发明另一方面还提供一种药物组合物,所述药物组合物包含上述任一种木脂素苷类化合物,以及药学上可以接受的辅料、稀释剂或载体。
[0018]“药学上可以接受的”是指这样一些化合物、原料、组合物和/或剂型,它们在合理医学判断的范围内,适用于与患者组织接触而无过度毒性、刺激性、变态反应或与合理的利益/风险比相对称的其他问题和并发症,并有效用于既定用途。
[0019]
该药物组合物可优选为:包含结构为式(ⅰ)-(ⅳ)任一所示化合物,以及药学上可以接受的辅料、稀释剂或载体。还可优选为:包含结构为式(ⅰ)和式(ⅱ)的化合物,以及药学上可以接受的辅料、稀释剂或载体。更优选为:包含结构为式(ⅲ)和式(ⅳ)的化合物,以及药学上可以接受的辅料、稀释剂或载体。
[0020]
本方明另一方面还提供一种上述木脂素苷类化合物或上述药物组合物在制备用于缓解或治疗疲劳药物中的应用。
[0021]
与现有技术相比,本发明具有以下有益效果:
[0022]
本发明的木脂素苷类化合物能显著提高乳酸率,降低基体乳酸含量,降低运动后机体血清bun与ck水平,从而达到缓解和治疗疲劳的效果。
附图说明
[0023]
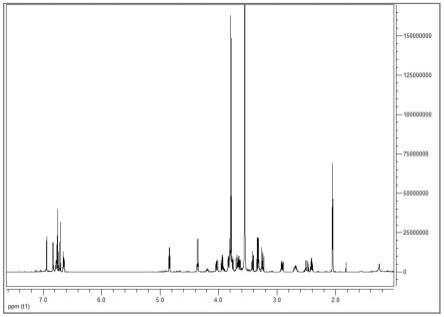
图1为化合物1的1h-nmr光谱图;
[0024]
图2为化合物1在 7.2ppm到 4.2ppm范围间的1h-nmr光谱图;
[0025]
图3为化合物1在 4.3ppm到 2.1ppm范围间的1h-nmr光谱图;
[0026]
图4为化合物1的
13
c-nmr光谱图;
[0027]
图5为化合物1的hmbc光谱图;
[0028]
图6为化合物1的noe光谱图;
[0029]
图7为化合物2的1h-nmr光谱图;
[0030]
图8为化合物2在 7.5ppm到 4.4ppm范围间的1h-nmr光谱图;
[0031]
图9为化合物2在 4.4ppm到 1.4ppm范围间的1h-nmr光谱图;
[0032]
图10为化合物2的
13
c-nmr光谱图;
[0033]
图11为化合物2的hmbc光谱图;
[0034]
图12为化合物2的noe光谱图;
[0035]
图13为化合物3的1h-nmr光谱图;
[0036]
图14为化合物3在 7.2ppm到 4.7ppm范围间的1h-nmr光谱图;
[0037]
图15为化合物3在 4.4ppm到 1.9ppm范围间的1h-nmr光谱图;
[0038]
图16为化合物3的
13
c-nmr光谱图;
[0039]
图17为化合物3的hmbc光谱图;
[0040]
图18为化合物3的noe光谱图;
[0041]
图19为化合物4的1h-nmr光谱图;
[0042]
图20为化合物4在 7.3ppm到 4.3ppm范围间的1h-nmr光谱图;
[0043]
图21为化合物4在 5.0ppm到 1.5ppm范围间的1h-nmr光谱图;
[0044]
图22为化合物4的
13
c-nmr光谱图;
[0045]
图23为化合物4的hmbc光谱图;
[0046]
图24为化合物4的noe光谱图。
具体实施方式
[0047]
为了便于理解本发明,以下将给出较佳实施例对本发明进行更全面的描述。但是,本发明可以以许多不同的形式来实现,并不限于本文所描述的实施例。相反地,提供这些实施例的目的是使对本发明的公开内容的理解更加透彻全面。
[0048]
除非另有定义,本文所使用的所有的技术和科学术语与属于本发明的技术领域的技术人员通常理解的含义相同。本文中在本发明的说明书中所使用的术语只是为了描述具体的实施例的目的,不是旨在于限制本发明。
[0049]
为方便表述,将本发明中式(ⅰ)-(ⅳ)所示的化合物分别命名为化合物1、化合物2、化合物3、化合物4。
[0050]
实施例1
[0051]
组分1-11的提取分离方法。
[0052]
称取干燥、粉碎的刺五加茎1.0kg,加入5.0l的50%乙醇浸泡1小时,利用微波超声波协同法提取1小时,提取2次。合并提取液,用旋转蒸发仪浓缩至1/5体积,放凉,加入3倍量乙醇并搅拌,低温静置24小时,析出沉淀,过滤或离心取沉淀,沉淀物置于表面皿中加热,除去乙醇和水,直至无醇味,即得刺五加提取物(357.0g)。将刺五加提取物利用羟丙基葡聚糖凝胶(lh-20)进行分离,以甲醇:水体积比为0:10,1:9,2:8,3:7,4:6,5:5,6:4,7:3,8:2,9:1,10:0的流动相进行梯度洗脱,各洗脱500ml,收集不同梯度洗脱液500ml,并浓缩,分别得到组分1至组分11。
[0053]
实施例2
[0054]
组分1-11的乳酸清除率试验。
[0055]
取健康清洁级的昆明种雄性小鼠130只,基础饲料平衡喂养7d后,筛选出体重为20-25g的小鼠70只,随机分组成空白组,实验组分1-11组,央科藏域牌红天胶囊对照组。从实验开始到结束,实验组分1-11组灌胃(600mg/kg);央科藏域牌红天胶囊对照组(600mg/kg);空白组、模型组灌胃等体积生理盐水,连续灌胃20d。末次给药1h后,将各小鼠置于高50cm,直径50cm,水深30cm的有机玻璃缸中游泳10min,水温25
±
1℃。各小鼠在游泳前,游泳后即刻、休息20min后,各用尾静脉针刺采血,测定血乳酸值。通过各个时间点的血乳酸值计算血乳酸曲线下面积。实验结果见表1。
[0056]
表1小鼠抗疲劳试验乳酸曲线下面积结果
[0057][0058][0059]
实验结果表明:与空白组相比,实验组分1-7组血乳酸曲线下面积均有所降低。其
中,实验组分3-4组与阳性对照组相比血乳酸曲线下面积显著降低。选择在组分3和组分4进行分离、鉴定和试验。
[0060]
实施例3
[0061]
(1)化合物1-4分离方法。
[0062]
组分3(3.5g)经半制备反相高效液相色谱法,使用c18柱(10mm
×
250mm,5μm),利用15%乙醇为流动相,等度洗脱60min,得到化合物1(1.3g)和2(0.8g)。
[0063]
组分4(4.3g)经半制备反相高效液相色谱法,使用c18柱(10mm
×
250mm,5μm),利用17%至21%乙醇为流动相,梯度洗脱70min,得到化合物3(1.1g)和4(0.9g)。
[0064]
(2)化合物1-4光谱数据及结构式。
[0065]
化合物1,白色粉末;旋光度-11.2(c 0.01,meoh);ms m/z 522.2106[m]
(calcd for c
26h34o11
,522.2101);uv(meoh)λ
max
(logε):228(3.96),279(3.28)nm;ir(kbr)ν
max
:3419,1599,1514,1267,1053;1h(500mhz,acetone-d6)和
13
c-nmr(125mhz,acetone-d6),hmbc和noe图谱见附图1-6;化学结构式如下。
[0066][0067]
化合物2,白色粉末;旋光度-7.2(c 0.01,meoh);ms m/z 522.2105[m]
(calcd for c
26h34o11
,522.2103);uv(meoh)λ
max
(logε):226(3.12),287(3.08)nm;ir(kbr)ν
max
:3415,1596,1512,1259,1049;1h(500mhz,acetone-d6)和
13
c-nmr(125mhz,acetone-d6),hmbc和noe图谱见附图7-12;化学结构式如下。
[0068][0069]
化合物3,白色粉末;旋光度-15.2(c 0.01,meoh);ms m/z 522.2104[m]
(calcd for c
26h34o11
,522.2101);uv(meoh)λ
max
(logε):233(2.96),273(2.37)nm;ir(kbr)ν
max
:3417,1585,1519,1253,1041;1h(500mhz,acetone-d6)和
13
c-nmr(125mhz,acetone-d6),hmbc和noe图谱见附图13-18;化学结构式如下。
[0070][0071]
化合物4,白色粉末;旋光度-1.2(c 0.01,meoh);ms m/z 522.2109[m]
(calcd for c
26h34o11
,522.2102);uv(meoh)λ
max
(logε):225(3.61),284(3.11)nm;ir(kbr)ν
max
:3431,1590,1517,1232,1046;1h(500mhz,acetone-d6)和
13
c-nmr(125mhz,acetone-d6),hmbc和noe图谱见附图19-24;化学结构式如下。
[0072][0073]
实施例4
[0074]
化合物1-4的乳酸清除率试验。
[0075]
取健康清洁级的昆明种雄性小鼠100只,基础饲料平衡喂养7d后,随机分组成空白组,化合物1-4组,央科藏域牌红天胶囊对照组。从实验开始到结束,化合物1-4组灌胃(40mg/kg,80mg/kg);央科藏域牌红天胶囊对照组(600mg/kg);空白组灌胃等体积生理盐水,连续灌胃20d。末次给药1h后,将各小鼠置于高50cm,直径50cm,水深30cm的有机玻璃缸中游泳10min,水温25
±
1℃。各小鼠在游泳前,游泳后即刻、休息20min后,各用尾静脉针刺采血,测定血乳酸值。通过各个时间点的血乳酸值计算血乳酸曲线下面积。实验结果见表2。
[0076]
表2小鼠抗疲劳试验乳酸曲线下面积结果
[0077]
[0078][0079]
实验结果表明:与空白组相比,化合物1-4组随着剂量的增加血乳酸曲线下面积均有显著降低。化合物2-4组在80mg/kg剂量下与阳性对照组相比血乳酸曲线下面积显著降低(p<0.5)。
[0080]
实施例5
[0081]
化合物1-4的运动后血清中尿素氮(bun)和肌酸激酶(ck)含量试验。
[0082]
取健康清洁级的昆明种雄性小鼠60只,基础饲料平衡喂养7d后,随机分组成空白组,化合物1-4组,央科藏域牌红天胶囊对照组。从实验开始到结束,化合物1-4组灌胃(80mg/kg);央科藏域牌红天胶囊对照组(600mg/kg);空白组灌胃等体积生理盐水,连续灌胃20d。末次给药1h后,将各小鼠置于高50cm,直径50cm,水深30cm的有机玻璃缸中游泳,水温25
±
1℃。各小鼠游泳90min,休息60min后,摘眼球取血,通过血液生化仪测定血清尿素氮(bun)和肌酸激酶(ck)。实验结果见表3。
[0083]
表3小鼠血液中bun和ck结果
[0084][0085]
实验结果表明:化合物1-4组在80mg/kg剂量下血清bun和ck均显著低于空白对照组。其中化合物3-4组的效果最显著。
[0086]
实施例6
[0087]
化合物1-4组的负重游泳试验。
[0088]
取健康清洁级的昆明种雄性小鼠60只,基础饲料平衡喂养7d后,随机分组成空白组,化合物1-4组,央科藏域牌红天胶囊对照组。从实验开始到结束,化合物1-4组灌胃(80mg/kg);央科藏域牌红天胶囊对照组(600mg/kg);空白组灌胃等体积生理盐水,连续灌胃20d。末次给药1h后,将各组各小鼠置于高50cm,直径50cm,水深30cm的有机玻璃缸中游泳,水温25
±
1℃,小鼠尾根部负载5%体重的铅丝。以小鼠沉入水底8s内不再浮出水面视为力竭标准。记录每只小鼠从游泳开始到力竭的时间即为小鼠游泳时间。实验结果见表4。
[0089]
表4小鼠抗疲劳试验力竭时间结果
[0090][0091]
实验结果表明:各给药组在80mg/kg剂量下力竭时间均显著高于空白对照组。
[0092]
以上实施例结果表明:刺五加中筛选的组分3-4均能显著地降低机体乳酸值,显著提高乳酸清除率;化合物1-4均能够在80mg/kg剂量下显著降低机体乳酸值,显著提高乳酸清除率,显著降低运动后机体血清bun与ck水平,显著增加力竭时间。
[0093]
以上所述实施例的各技术特征可以进行任意的组合,为使描述简洁,未对上述实施例中的各个技术特征所有可能的组合都进行描述,然而,只要这些技术特征的组合不存在矛盾,都应当认为是本说明书记载的范围。
[0094]
以上所述实施例仅表达了本发明的几种实施方式,其描述较为具体和详细,但并不能因此而理解为对发明专利范围的限制。应当指出的是,对于本领域的普通技术人员来说,在不脱离本发明构思的前提下,还可以做出若干变形和改进,这些都属于本发明的保护范围。因此,本发明专利的保护范围应以所附权利要求为准。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。