1.本发明涉及化妆品原料制备技术领域,特别涉及一种具有保湿作用的海参肽及其制备方法。
背景技术:
2.目前化妆品中所用的保湿成分主要为化学品,包括甘油、矿物油、多元醇等。此类化学成分保湿效果良好,但是肤感比较厚重,特别对油性皮肤,长期使用容易堵塞毛孔,诱发皮肤过敏、出痘等不良反应。
3.海参素有"海中人参"之称,是一种具有极高的营养价值和药用价值海参的海洋无脊椎动物,含有多肽、海参多糖、海参皂苷等多种具有重要生物活性的营养物质,已经被证明具有提高免疫力、美容等功效。海参体壁富含蛋白质,占干重的90%以上,其中又有80%以上为胶原蛋白,具有亲肤性好,轻薄透气,能够明显改善矿物油类成分给油性皮肤带来的不适。但相关制备技术中而得的海参肽保湿能力较差,导致其广泛推广应用于化妆品存在一定障碍。
技术实现要素:
4.本发明的主要目的是提供一种具有保湿作用的海参肽及其制备方法,旨在提高制备海参肽的保湿能力。
5.为实现上述目的,本发明提出的具有保湿作用的海参肽的制备方法,包括:
6.原材料处理:提供海参,将所述海参去除内脏,将其绞碎;
7.定向酶解:向绞碎后的所述海参中加入纯水和预设蛋白酶,混合均匀后在ph值6.8-7.5、温度40℃-50℃条件下酶解1h-2h得第一海参原液;
8.升温灭酶:将第一海参原液升温至90℃以上,保温保压10min-15min得第二海参原液;
9.硫酸铵沉淀:向第二海参原液加入硫酸铵,搅拌均匀后在温度4℃-6℃的环境下静置8h-12h,提取上清液;
10.离心沉淀:使用截留分子量为500da-2kda的超滤膜过滤所述上清液,对过滤后的所述上清液进行脱盐处理,得到浓缩液和超滤膜透过液;
11.干燥制粉:将所述浓缩液进行冷冻干燥处理,得海参肽粉末。
12.可选地,所述预设蛋白酶为胰蛋白酶、中性蛋白酶、木瓜蛋白酶中的一种。
13.可选地,所述定向酶解具体包括:
14.向绞碎后的所述海参中加入纯水和胰蛋白酶,所述胰蛋白酶加入量占混合溶液总质量的0.2%,将所述混合溶液搅拌均匀后在ph值6.8-7.5、温度45℃条件下酶解2h得第一海参原液。
15.可选地,向绞碎后的所述海参中加入纯水和中性蛋白酶,所述中性蛋白酶加入量占混合溶液总质量的0.2%,将所述混合溶液搅拌均匀后在ph值6.8-7.5、温度45℃条件下
酶解1h得第一海参原液。
16.可选地,向绞碎后的所述海参中加入纯水和木瓜蛋白酶,所述木瓜蛋白酶加入量占混合溶液总质量的0.2%,将所述混合溶液搅拌均匀后在ph值6.8-7.5、温度45℃条件下酶解2h得第一海参原液。
17.可选地,所述硫酸铵沉淀步骤具体包括:
18.对所述第二海参原液进行离心去渣处理,向所述第二海参原液加入硫酸铵至最终浓度为30%-60%,搅拌均匀后在温度4℃-6℃的环境下静置8h-12h,提取上清液。
19.可选地,在所述定向酶解步骤中,所述纯水的加入量与所述海参的质量之比为5:1。
20.可选地,在所述离心沉淀步骤中:
21.采用截留分子量为500da的纳滤膜过滤所述超滤膜透过液,将过滤后的所述超滤膜透过液经过真空浓缩和80℃热风干燥后循环使用至所述硫酸铵沉淀步骤。
22.可选地,所述原材料处理步骤具体包括:
23.提供干海参,将所述干海参去除内脏,在4℃-10℃的温度下泡发24h,得到海参,洗净所述海参表面污物和盐分,采用匀浆机将所述海参绞碎。
24.本发明还提出一种具有保湿作用的海参肽,该具有保湿作用的海参肽根据以上所述的制备方法制得。
25.与现有技术相比,本发明通过采用预设蛋白酶对海参进行定向酶解,将其中的海参肽水解成分子片段较为明确的寡肽;采用硫酸铵沉淀法,去除疏水性较强的肽段和分子量过大的肽段,最大程度地保留寡肽中高亲水性和分子量适宜的肽段;然后采用超过滤膜过滤脱除硫酸铵分子,冷冻干燥获得具有良好保湿作用的海参肽。
附图说明
26.本发明目的的实现、功能特点及优点将结合实施例,参照附图做进一步说明。
27.图1是本发明的一个实施例的具有保湿作用的海参肽的制备方法的流程示意图;
28.图2是本发明的一个实施例的具有保湿作用的海参肽的制备方法中各类型的蛋白酶水解后所获得的海参肽的表面疏水性指数;
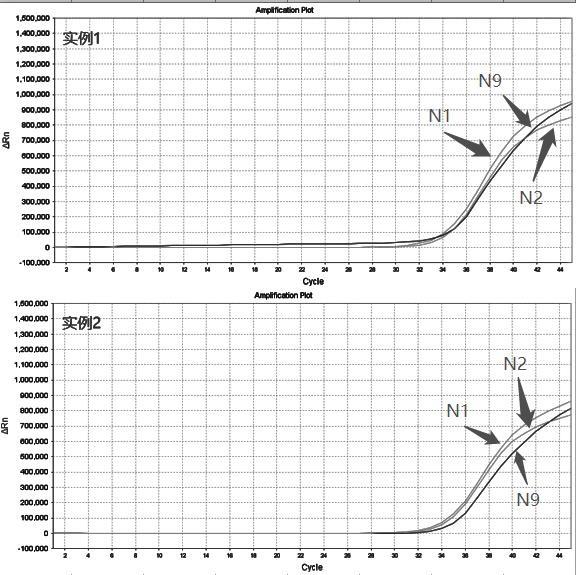
29.图3是本发明的一个实施例的具有保湿作用的海参肽的制备方法中胰蛋白酶应用于海参肽酶解正交实验结果的效应曲线图;
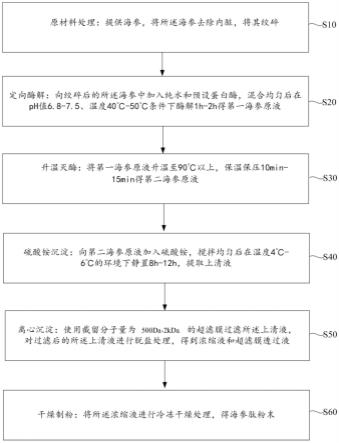
30.图4是本发明的一个实施例的具有保湿作用的海参肽的制备方法中中性蛋白酶应用于海参肽酶解正交实验结果的效应曲线图;
31.图5是本发明的一个实施例的具有保湿作用的海参肽的制备方法中木瓜蛋白酶应用于海参肽酶解正交实验结果的效应曲线图;
32.图6是本发明的一个实施例的具有保湿作用的海参肽的制备方法中各类型的蛋白酶水解后加入不同浓度的硫酸铵所获得的海参肽的表面疏水性指数。
具体实施方式
33.本文中术语第一、第二、第三等用于描述各种部分、成分、区域、层和/或段,但这些部分、成分、区域、层和/或段不应该被这些术语限制。这些术语仅用于区分某一部分、成分、
区域、层和/或段与另一部分、成分、区域、层和/或段。因此,在不脱离本发明的范围内,以下描述的第一部分、成分、区域、层和/或段也可以描述为第二部分、成分、区域、层和/或段。
34.本文所使用的术语只是出于描述特定实施例而不意在限制本发明。除非上下文中另给出明显相反的含义,否则本文所使用的单数形式也意在包含复数形式。还应该理解的是,术语“包含”具体指某一特性、领域、整数、步骤、动作、要素及/或成分,但是并不排除其他特性、领域、整数、步骤、动作、要素、成分及/或组的存在或附加。
35.虽然没有另作定义,但本文使用的所有术语(包含技术术语和科学术语)的含义与所属领域的技术人员通常理解的意思相同。对于辞典里面有定义的术语,应该被解释为具有与相关技术文献和本文中公开的内容一致的意思,而不应该以理想化或过于正式的含义来解释它们的意思。
36.下面将结合本发明实施例中的附图,对本发明实施例中的技术方案进行清楚、完整地描述,显然,所描述的实施例仅仅是本发明的一部分实施例,而不是全部的实施例。基于本发明中的实施例,本领域普通技术人员在没有作出创造性劳动前提下所获得的所有其他实施例,都属于本发明保护的范围。
37.图1示意性地示出了根据本发明的一个实施例的具有保湿作用的海参肽的制备方法的流程图。图1的具有保湿作用的海参肽的制备方法的流程图只是用于例示本发明,本发明不限于此。因此,可以对具有保湿作用的海参肽的制备方法作出各种变形。
38.如图1所示,具有保湿作用的海参肽的制备方法包含:s10原材料处理:提供海参,将所述海参去除内脏,将其绞碎;s20定向酶解:向绞碎后的所述海参中加入纯水和预设蛋白酶,混合均匀后在ph值6.8-7.5、温度40℃-50℃条件下酶解1h-2h得第一海参原液;s30升温灭酶:将第一海参原液升温至90℃以上,保温保压10min-15min得第二海参原液;s40硫酸铵沉淀:向第二海参原液加入硫酸铵,搅拌均匀后在温度4℃-6℃的环境下静置8h-12h,提取上清液;s50离心沉淀:使用截留分子量为500da-2kda的超滤膜过滤所述上清液,对过滤后的所述上清液进行脱盐处理,得到浓缩液和超滤膜透过液;s60干燥制粉:将所述浓缩液进行冷冻干燥处理,得海参肽粉末。除此之外,根据需要,具有保湿作用的海参肽的制备方法还可包含其他步骤。
39.首先,在s10原材料处理:提供海参,将所述海参去除内脏,将其绞碎;在此,海参可以选用新鲜海参或是干海参,为方便规模化生产,本发明中优选干海参。具体而言,将干海参预先去除内脏,使用纯净水在4℃-10℃的温度下对其进行低温泡发,泡发时间24h。采用低温泡可以最大程度地保留海参中的海参肽,提高海参肽的产出量。将低温泡发后海参用清水洗净其表面污物和盐分后,采用匀浆机将海参绞碎备用。
40.接下来,在s20定向酶解的步骤中:向绞碎后的海参中加入纯水和预设蛋白酶,混合均匀后在ph值6.8-7.5、温度40℃-50℃条件下酶解1h-2h得第一海参原液。期间,应每半小时检测一次溶液ph值,通过向其中加入适量的盐酸、硫酸、氢氧化钠碳酸氢钠、磷酸氢二钠等试剂将溶液ph值维持在6.8~7.5之间。
41.另外,在本发明中,预设蛋白酶优选为胰蛋白酶、中性蛋白酶、木瓜蛋白酶中的一种。本发明通过筛选实验选取最佳的预设蛋白酶种类。具体而言,本发明中选择《gb 2760食品添加剂使用标准》中所列允许在食品中使用的菠萝蛋白酶、胰蛋白酶、中性蛋白酶(枯草芽孢杆菌蛋白酶)、木瓜蛋白酶、胃蛋白酶、无花果蛋白酶等,在各酶的最适ph和最适温度
下,以料液比1:5,即100g海参加入500ml纯水;加酶量0.5%,即加酶的质量为混合后海参溶液质量的0.5%,如100g海参混合溶液加酶量为0.5g;酶解4h,以90℃的温度灭酶5min,等溶液冷却后离心去渣,取上清液进行冷冻干燥处理后获得海参肽粉末。以样品的表面疏水性为指标,选择能够获得较佳亲水性海参肽的定向酶解用酶。
42.图2示意性地示出了根据本发明的一个实施例的具有保湿作用的海参肽的制备方法的中各类型的蛋白酶水解后所获得的海参肽的表面疏水性指数。由图2可见,胰蛋白酶、中性蛋白酶、木瓜蛋白酶3种蛋白酶定向酶解海参后所获得的海参肽样品其表面疏水性较低,也即获得的海参肽样品具有较好的亲水性,具有良好的吸湿或保湿作用。因此,采用正交实验的方法,对3种酶的最佳水解条件进行进一步筛选,以期进一步降低定向酶解后获得海参肽的表面疏水性。
43.此外,以加酶量,酶解时间,酶解温度3个因素为主要因素,以加酶量0.2%,0.5%,0.8%;酶解时间1h,2h,4h;酶解温度45℃,50℃,55℃为水平,设计正交实验,以表面疏水性指数为指标,对胰蛋白酶、中性蛋白酶、木瓜蛋白酶3种酶分别进行实验,实验步骤参照上述筛选实验的步骤,在此不做多余赘述。实验结果及分析如表1至表3所示,效应曲线图请参见图3至图5。
44.表1海参肽酶解正交实验结果(胰蛋白酶)
[0045][0046]
表2海参肽酶解正交实验结果(中性蛋白酶)
[0047][0048][0049]
表3海参肽酶解正交实验结果(木瓜蛋白酶)
[0050][0051]
由表1至表3以及图3至图5可知,选定的三种酶对水解海参肽疏水性的影响基本一
致。三个因素中,加酶量为主要因素,随着加酶量的增加,海参肽的疏水性逐渐增加;酶解时间为次要因素,除中性蛋白酶外,其它2种酶水解生成海参肽的疏水性随时间延长先下降后升高;酶解温度为第三因素,随着温度的升高,定向酶解生成海参肽的疏水性先升高后趋于稳定。由此,可以确定胰蛋白酶的最佳酶解条件为:加酶量0.2%,酶解时间2h,酶解温度45℃,;中性蛋白酶的最佳酶解条件为:加酶量0.2%,酶解时间1h,酶解温度45℃,;木瓜蛋白酶的最佳酶解条件为:加酶量0.2%,酶解时间2h,酶解温度45℃。
[0052]
请再次参见图3至图5,需要说明的是,本技术中海参肽表面疏水性测定的具体方法包括,采用ans(1-苯胺基萘-8-磺酸荧光探针法测定样品表面疏水性。将样品用0.01mol/l pbs(ph 7.0)的磷酸缓冲液稀释至蛋白浓度为25、50、75、100、125、150μg/ml 6个不同的梯度,再用缓冲液配制8mmol/l的ans溶液。取4ml不同蛋白质浓度样品,分别加入20μl ans溶液,振荡混匀后,室温下避光反应3min。设定荧光分光光度计激发波长λex=390nm,λem=470nm,检测样品的荧光强度。以样品浓度为横坐标,样品的荧光强度为纵坐标作图,图中的线性回归斜率即为表面疏水性指数。
[0053]
在定向酶解获得第一海参原液后,接下来进行s30升温灭酶:将第一海参原液升温至90℃以上,保温保压10min-15min得第二海参原液。
[0054]
接下在s40硫酸铵沉淀步骤中:向第二海参原液加入硫酸铵,搅拌均匀后在温度4℃-6℃的环境下静置8h-12h,提取上清液。可以理解的是,本发明中定向酶解步骤后虽然暴露的亲水氨基酸有所增加,但是也暴露了大量的疏水氨基酸,从而使得海参肽表面疏水性的提高有限,为进一步提高海参肽的吸湿保湿能力,以定向酶解后的海参肽样品为原料,本发明对硫酸铵沉淀所需的浓度进行了优化。
[0055]
图6示意性地示出了根据本发明的一个实施例的具有保湿作用的海参肽的制备方法的中各类型的蛋白酶水解后加入不同浓度的硫酸铵所获得的海参肽的表面疏水性指数。具体而言,采用胰蛋白酶、中性蛋白酶、木瓜蛋白酶定向酶解后,经过90℃的温度灭酶10min,溶液冷却后低温离心去渣,取上清液进行冷冻干燥处理后获得的海参肽作为样品进行测定。3种海参肽样品分别加水溶解,配制成5%的溶液,加入终浓度分别为30%,40%,50%和60%硫酸铵,充分搅拌后在4℃-6℃的温度下静置沉淀8h,低温离心取上清液,使用截留分子量为500da-2kda的超滤膜浓缩对上清液进行过滤得到浓缩液和超滤膜透过液,对浓缩液加水脱盐直至浓缩液取样滴加bacl2无沉淀后,再将浓缩液冷冻干燥,获得硫酸铵沉淀的海参肽样品。对3种样品的表面疏水性进行检测,确定能够获得较佳亲水性海参肽的硫酸铵沉淀浓度。
[0056]
由图6可以看到,3种蛋白酶水解所得海参肽表面疏水性的变化规律基本一致。随着硫酸铵终浓度的不断升高,样品的表面疏水性不断下降。当硫酸铵终浓度高于50%后,所得样品的表面疏水性趋于稳定,提示样品中的疏水性肽随着硫酸铵终浓度的增加而不断沉淀,到浓度为50%时基本沉淀完全。因此,本技术中通过向第二海参原液加入硫酸铵至最终浓度为30%-60%较大程度地平衡了沉淀效率和制造成本,优选50%的终浓度作为加入硫酸铵形成沉淀的最优条件。
[0057]
接下来在s50离心沉淀:使用截留分子量为500da-2kda的超滤膜过滤所述上清液,过滤后上清液的浓度可以根据实际情况具体设定。本技术中,优选过滤后的上清液的质量与步骤s10中的海参质量比为2:1,即100g海参通过超滤膜过滤后的上清液为200ml。对过滤
后上清液采用蒸发法或是膜处理技术对其进行加水脱盐处理,得到浓缩液和超滤膜透过液。浓缩液以滴加bacl2无沉淀为标准。
[0058]
可以理解的是上清液中的盐离子在蛋白或肽溶液中可与其竞争水分子,从而破坏其表面的水化膜,降低其溶解度,使之从溶液中沉淀出来。各种肽片段的亲水性和分子量不同,亲水性越高,分子量越小,越不容易在高盐溶液中沉淀出来。本发明中,通过采用加水脱盐处理,即利用不同浓度的盐溶液来沉淀具有不同亲水性及不同分子量的肽片段,通过对目标肽片段进行纯化,去除疏水性较强的肽段和分子量过大的肽段,获得到亲水性较强和分子量适宜的肽段,从而进一步提高制备后海参肽的保湿能力。
[0059]
在本该步骤中还包括采用截留分子量为500da-2kda的纳滤膜过滤超滤膜透过液,将过滤后的超滤膜透过液经过真空浓缩和80℃热风干燥后循环使用至所述硫酸铵沉淀步骤。本发明中通过500da-2kda的纳滤膜过滤截留超滤膜透过液中的杂质肽段,通过真空浓缩和热风干燥后其中的硫酸铵又可以重新用于下一次沉淀。硫酸铵循环利用,既可降低制备成本,又能减少对环境的污染。
[0060]
而后在s60干燥制粉:将所述浓缩液进行冷冻干燥处理,得海参肽粉末。
[0061]
需要说明的是,肽段的保湿作用主要与其氨基酸组成和分子量相关。氨基酸可分为亲水和疏水两种类型,在海参肽体壁胶原蛋白的主要组成氨基酸中,含量最多(约30%)的甘氨酸和含量次多(约10%)的羟脯氨酸均为亲水性氨基酸,此外,还有大量天冬氨酸、谷氨酸等、精氨酸、赖氨酸等亲水性氨基酸。因此,从整体来看,海参肽对水具有较好的结合能力。但是,除了上述亲水性氨基酸,海参肽中同样含量有脯氨酸(约5%)、丙氨酸(约5%)、苯丙氨酸等疏水性氨基酸,这些氨基酸酸的存在,会影响肽段对水的结合能力,减弱肽段的保湿作用。此外,相同氨基酸组成的情况下,分子量越大,对水的结合能力越好。
[0062]
基于以上原理,本发明通过采用预设蛋白酶对海参进行定向酶解,将其中的海参肽水解成分子片段较为明确的寡肽,采用硫酸铵沉淀法,去除疏水性较强的肽段和分子量过大的肽片段,最大程度地保留寡肽中高亲水性和分子量适宜的肽段;然后采用超过滤膜过滤脱除硫酸铵分子,最终冷冻干燥获得具有良好保湿作用的海参肽粉末。
[0063]
下面通过实验例更详细地说明本发明。下述实验例只是用于例示本发明,本发明不限于下述实验例。
[0064]
实施例1:
[0065]
提供去除内脏的干海参100g,加水于4℃环境下泡发24h,取出海参,用纯水冲洗净表面污物和盐分,用匀浆机绞碎。加入500ml纯水中,加入胰蛋白酶0.2g,调节ph6.8~7.5,保持温度在45℃,酶解2h得第一海参原液;定向酶解完成后,升温至90℃以上灭酶10min得第二海参溶液。将第二海参溶液离心去渣后加入硫酸铵至最终浓度为30%,搅拌均匀后在温度为4℃的环境下静置8h。低温离心分离沉淀,提取上清液,该上清液用截留分子量为500da的超滤膜浓缩至200ml。加水脱盐处理得浓缩液和超滤膜透过液,浓缩液冷冻干燥,获得海参肽样品a。将超滤膜透过液用截留分子量为500da的纳滤膜脱除肽片段,而后依次经过真空浓缩和80℃热风干燥后循环用于硫酸铵沉淀。
[0066]
实施例2:
[0067]
提供去除内脏的干海参200g,加水于6℃的环境下泡发24h,取出海参,用纯水冲洗净表面污物和盐分,用匀浆机绞碎。加入1000ml纯水中,加入中性蛋白酶0.4g,调节ph6.8~
7.5,保持温度在45℃,酶解1h得第一海参原液;定向酶解完成后,升温至90℃以上灭酶12min得第二海参溶液。将第二海参溶液离心去渣后加入硫酸铵至最终浓度为50%,搅拌均匀后在温度为5℃的环境下静置10h。低温离心分离沉淀,提取上清液,该上清液用截留分子量为1kda的超滤膜浓缩至400ml,加水脱盐处理得浓缩液和超滤膜透过液,浓缩液冷冻干燥,获得海参肽样品b。将超滤膜透过液用截留分子量为1kda的纳滤膜脱除肽片段,而后依次经过真空浓缩和80℃热风干燥后循环用于硫酸铵沉淀。
[0068]
实施例3:
[0069]
提供去除内脏的干海参500g,加水于10℃的环境下泡发24h,取出海参,用纯水冲洗净表面污物和盐分,用匀浆机绞碎。加入2500ml纯水中,加入胰蛋白酶1.0g,调节ph6.8~7.5,保持温度在45℃,酶解2h得第一海参原液;定向酶解完成后,升温至90℃以上灭酶15min得第二海参溶液。将第二海参溶液离心去渣后加入硫酸铵至最终浓度为60%,搅拌均匀后在温度为6℃的环境下静置12h。低温离心分离沉淀,提取上清液,该上清液用截留分子量为2kda的超滤膜浓缩至1000ml,加水脱盐处理得浓缩液和超滤膜透过液,浓缩液冷冻干燥,获得海参肽样品c。将超滤膜透过液用截留分子量为2kda的纳滤膜脱除肽片段,而后依次经过真空浓缩和80℃热风干燥后循环用于硫酸铵沉淀。
[0070]
将实施例1-3获得的海参肽样品配成2%溶液,进行吸湿和保湿能力测定,并与2%和5%的甘油溶液对比,结果示于表4和表5:
[0071]
表4海参肽吸湿能力
[0072][0073]
表5海参肽保湿能力
[0074][0075]
由表4和表5可知,2%的浓度下,本发明制备所得的海参肽的吸湿性和保湿性与2%甘油相当,两者没有显著性差异,p》0.05。即数据表明,本发明的技术方案获得的海参肽具有良好的吸湿、保湿性能,应用在化妆品中能起到良好的保湿效果。
[0076]
需要说明的是,本发明吸湿能力的测定方法具体包括如下步骤:
[0077]
取样品500毫克,置于饱和硫酸铵溶液控制相对湿度(rh)为81%的干燥器内72个小时,每6小时测量一次样本的重量,吸湿能力的计算公式具体如下:
[0078]
吸湿能力=(样品吸湿后重量-样品吸湿前重量)/样品吸湿前重量
×
100%
[0079]
本发明保湿能力测定方法具体包括如下步骤:
[0080]
取50毫克样品,用10毫升去离子水溶解。将样品溶液存储在由饱和碳酸钾溶液控制相对湿度(rh)为43%的干燥器内72个小时,每6小时测量一次样本的重量,保湿能力的计
算公式具体如下:
[0081]
保湿能力=(样品保湿后重量/样品保湿前重量)
×
100%
[0082]
本发明能以各种不同方式实施并不局限于所述的实施例,所属领域的普通技术人员可以理解在不变更本发明的技术思想或必要特征的情况下通过其他具体方式能够实施本发明。因此,应该理解以上所述的实施例是示例性的,而并非用来限制本发明。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。