2-甲基-4-氨基苯酚的制备方法、2-甲基-4-(boc-氨基)-苯酚的制备方法
技术领域
1.本发明属于药物合成技术领域,具体涉及2-甲基-4-氨基苯酚的制备方法、2-甲基-4-(boc-氨基)-苯酚的制备方法。
背景技术:
2.冠心病、冠状动脉病和脑中风等疾病与血栓形成具有紧密联系,血栓类疾病每年会导致约1500万的死亡病例,极大地威胁人类健康。纤维蛋白原受体拮抗剂能阻止通过各种途径激活的血小板的聚集,从而有效地抑制血栓的形成。纤维蛋白原受体拮抗剂按其结构类型可分为:单克隆抗体、肽类化合物和非肽类化合物。由于单克隆抗体和肽类化合物具有分子极性大、不易穿过生物屏障、不利于口服吸收、易代谢及制造成本高等缺点,目前纤维蛋白原受体拮抗剂的研究热点主要集中在非肽类化合物。
3.4-羟基-3-甲基苯基氨基甲酸叔丁酯(c
12h17
no3,又名2-甲基-4-(boc-氨基)-苯酚)是一种制备非肽类纤维蛋白原受体拮抗剂的重要中间体。现有的4-羟基-3-甲基苯基氨基甲酸叔丁酯的制备方法操作复杂不适于大规模生产。例如文献(a novel can-sio
2-mediated one-pot oxidation of 1-keto-1,2,3,4-tetrahydrocarbazoles to carbazoloquinones:efficient syntheses of murrayaquinone a and koeniginequinone a,cheminform,2011,7,26,第30期26卷)以2-甲基苯酚为原料,在亚硝酸钠和盐酸的作用下进行亚硝化反应得到2-甲基-4-亚硝基苯酚,再利用h2s和nh3还原硝基得到2-甲基-2-氨基苯酚,最后与boc酸酐进行酰胺化反应得到2-甲基-4-(boc-氨基)-苯酚。该文献公开的2-甲基-4-(boc-氨基)-苯酚合成路线的原理和操作较为复杂不适用于工业化生产。
技术实现要素:
4.有鉴于此,本发明提供了一种2-甲基-4-氨基苯酚的制备方法、2-甲基-4-(boc-氨基)-苯酚的制备方法,本发明提供的制备方法操作简单,适合工业化生产。
5.为了解决上述技术问题,本发明提供了一种2-甲基-4-氨基苯酚的制备方法,包括以下步骤:
6.将对氨基苯磺酸盐和重氮化剂混合,进行重氮化反应,得到苯磺酸重氮盐;
7.将所述苯磺酸重氮盐、邻甲苯酚和强碱水溶液混合,进行friedel-crafts反应,得到偶氮化合物;
8.将所述偶氮化合物与还原剂混合,进行还原反应,得到2-甲基-4-氨基苯酚。
9.优选的,所述对氨基苯磺酸盐和重氮化剂的摩尔比为1:(1~3)。
10.优选的,所述重氮化反应的温度为10~20℃,时间为1~3h。
11.优选的,所述强碱水溶液包括碱金属氢氧化物水溶液;
12.所述强碱水溶液的摩尔浓度为0.2~0.7mol/l。
13.优选的,所述苯磺酸重氮盐和邻甲苯酚的摩尔比为1:(1~3)。
14.优选的,所述friedel-crafts反应的温度为0~15℃,时间为3~8h。
15.优选的,所述还原剂包括连二亚硫酸钠、亚硫酸钠、锌和醋酸的混合物、氢气或铁;
16.所述苯磺酸重氮盐和还原剂的摩尔比为1:(3~6)。
17.优选的,所述还原反应的应温度为60~80℃,时间为10~30min。
18.本发明提供了一种2-甲基-4-(boc-氨基)-苯酚的制备方法,包括以下步骤:
19.将2-甲基-4-氨基苯酚、boc酸酐溶解于有机溶剂,进行酰胺化反应,得到2-甲基-4-(boc-氨基)-苯酚;所述2-甲基-4-氨基苯酚为按照上述技术方案所述制备方法制备得到的2-甲基-4-氨基苯酚。
20.优选的,所述2-甲基-4-氨基苯酚和boc酸酐的摩尔比为1:(0.9~2);所述酰胺化反应的温度为25~40℃,时间为1~3h。
21.本发明提供了一种2-甲基-4-氨基苯酚的制备方法,包括以下步骤:将对氨基苯磺酸盐和重氮化剂混合,进行重氮化反应,得到苯磺酸重氮盐;将所述苯磺酸重氮盐、邻甲苯酚和强碱水溶液混合,进行friedel-crafts反应,得到偶氮化合物;将所述偶氮化合物与还原剂混合,进行还原反应,得到2-甲基-4-氨基苯酚。本发明提供了一种2-甲基-4-(boc-氨基)-苯酚的制备方法,包括以下步骤:将2-甲基-4-氨基苯酚、boc酸酐溶解于有机溶剂,进行酰胺化反应,得到2-甲基-4-(boc-氨基)-苯酚;所述2-甲基-4-氨基苯酚为按照上述技术方案所述制备方法制备得到的。本发明提供的2-甲基-4-(boc-氨基)-苯酚的制备方法以对氨基苯磺酸盐和邻甲苯酚为原料,进行重氮化反应、friedel-crafts反应、还原反应和酰胺化反应制备得到2-甲基-4-(boc-氨基)-苯酚。本发明提供的制备方法操作简单、副产物少、产品纯化容易,适合工业化生产。按照本发明提供的制备方法制备得到的2-甲基-4-(boc-氨基)-苯酚的产率为81%以上,纯度为97%以上。
附图说明
22.图1为实施例1制备得到的2-甲基-4-(boc-氨基)-苯酚的1h-nmr谱图。
具体实施方式
23.本发明提供了一种2-甲基-4-氨基苯酚的制备方法的制备方法,包括以下步骤:
24.将对氨基苯磺酸盐和重氮化剂混合,进行重氮化反应,得到苯磺酸重氮盐;
25.将所述苯磺酸重氮盐、邻甲苯酚和强碱水溶液混合,进行friedel-crafts反应,得到偶氮化合物;
26.将所述偶氮化合物与还原剂混合,进行还原反应,得到2-甲基-4-氨基苯酚。
27.本发明将对氨基苯磺酸盐和重氮化剂混合,进行重氮化反应,得到苯磺酸重氮盐。在本发明中,所述对氨基苯磺酸盐优选按照以下方法制备得到:
28.将对氨基苯磺酸溶解于碱性水性溶液,进行中和反应,得到所述对氨基苯磺酸盐。
29.在本发明中,所述碱性水溶液优选包括碳酸钠水溶液、碳酸钾水溶液、碳酸氢钠水溶液、氢氧化钠水溶液或氢氧化钾水溶液,更优选为碳酸钠水溶液、碳酸钾水溶液或碳酸氢钠水溶液。在本发明中,所述碱性水溶液的摩尔浓度优选为0.2~1.5mol/l,更优选为0.3~1.3mol/l,更进一步优选为0.4~0.9mol/l。在本发明中,所述对氨基苯磺酸与碱性水溶液
中碱性物质的摩尔比优选为1:(0.3~1.25),更优选为1:(0.4~1),更进一步优选为1:(0.48~0.91)。
30.在本发明中,所述中和反应的温度优选为室温,所述室温的温度优选为20~35℃,更优选为25~30℃;所述中和反应的时间优选为10~40min,更优选为15~30min。
31.本发明优选将中和反应后的体系直接和重氮化剂混合。
32.在本发明中,所述重氮化剂优选包括亚硝酸或亚硝酸钠和酸溶液的混合溶液,更优选为亚硝酸钠和酸溶液的混合溶液;所述酸溶液优选包括盐酸溶液、硫酸溶液、过氯酸溶液或氟硼酸溶液,更优选为盐酸溶液或硫酸溶液;所述酸溶液的摩尔浓度优选为1~5mol/l,更优选为3~4mol/l。在本发明中所述亚硝酸钠和酸溶液中酸的摩尔比优选为1:0.3~1.1,更优选为1:0.4~0.6。在本发明中,当重氮化剂为亚硝酸钠和酸溶液的混合溶液时所述混合优选包括以下步骤:
33.将中和反应后的体系和亚硝酸钠水溶液第一混合,重氮化反应后和酸性溶液、冰第二混合,得到苯磺酸重氮盐。
34.在本发明中,所述亚硝酸水溶液的质量浓度优选为0.2~0.6g/ml,更优选为0.3~0.5g/ml。在本发明中,所述对氨基苯磺酸盐和亚硝酸钠的摩尔比优选为1:(0.5~3),更优选为1:(0.6~1.5)。
35.在本发明中,所述冰的质量和酸溶液的体积比优选为1g:(0.1~0.5)ml,更优选为1g:(0.1~0.2)ml。
36.在本发明中,所述第一混合前优选将中和反应后体系冷却,所述冷却后温度优选为-5~5℃,更优选为-3~3℃。本发明对所述冷却的方式无特殊限定,只要能够达到所需的温度即可。
37.在本发明中,重氮化反应后体系和酸性溶液、冰第二混合后会有黄色固体析出。
38.本发明对所述第一混合和第二混合的方式无特殊要求,只要能够混合均匀即可。
39.在本发明中,所述重氮化反应的温度优选为10~20℃,更优选为12~18℃;所述重氮反应的时间优选为1~3h,更优选为1.5~2h。
40.在本发明中,所述第二混合后优选还包括后处理,所述后处理优选包括:将第二混合后体系依次进行固液分离和洗涤,得到苯磺酸重氮盐。在本发明中所述固液分离优选为过滤,本发明对所述过滤无特殊要求,采用本领域常规的方式即可。在本发明中,所述洗涤用洗涤剂优选包括水,所述水优选为去离子水。在本发明中,所述过滤得到的固体的质量和洗涤剂的体积比优选为1g:(2~3)ml,更优选为1g:(2.2~2.8)ml。
41.得到苯磺酸重氮盐后,本发明将所述苯磺酸重氮盐、邻甲苯酚和强碱水溶液混合,进行friedel-crafts反应,得到偶氮化合物。在本发明中,所述混合优选包括以下步骤:
42.将邻甲苯酚和强碱水溶液第三混合,得到初级混合液;
43.将所述混合液和苯磺酸重氮盐第四混合,得到待反应溶液。
44.本发明将邻甲苯酚和强碱水溶液第三混合,得到初级混合液。在本发明中,所述强碱水溶液优选包括碱金属氢氧化物的水溶液,所述碱金属氢氧化物水溶液优选包括氢氧化钠水溶液、氢氧化钾水溶液、氢氧化锂水溶液、氢氧化铷水溶液或氢氧化铯水溶液水溶液,更优选为氢氧化钠水溶液或氢氧化钾水溶液;所述强碱水溶液的摩尔浓度优选为0.2~0.7mol/l,更优选为0.3~0.5mol/l。在本发明中,所述邻甲苯酚和强碱水溶液中的强碱的
摩尔比优选为1:(0.2~1),更优选为1:(0.4~0.6)。本发明对所述第三混合的方式无特殊要求只要能够混合均匀即可。
45.本发明在邻甲苯酚和强碱水溶液共同作用下形成苯酚负离子,以提高friedel-crafts反应活性。
46.得到初级混合液后,本发明将所述混合液和苯磺酸重氮盐第四混合,得到待反应溶液。本发明在进行第四混合前优选将所述初级混合液冷却,所述冷却后溶液的温度优选为0~5℃,更优选为1~3℃。本发明对所述冷却的方式无特殊要求只要能够达到所需的温度即可。
47.在本发明中,所述苯磺酸重氮盐和邻甲苯酚的摩尔比优选为1:(1~3),更优选为1:(1~2)。本发明对所述第四混合的方式无特殊要求只要能够混合均匀即可。
48.在本发明中,所述friedel-crafts反应的温度优选为0~15℃,更优选为5~10℃;所述friedel-crafts反应的时间优选为3~8h,更优选为4~7h。在本发明中,所述friedel-crafts反应优选伴随搅拌,所述搅拌的转速优选为800~1000r/min,更优选为850~950r/min。
49.得到偶氮化合物后,本发明将所述偶氮化合物与还原剂混合,进行还原反应,得到2-甲基-4-氨基苯酚。在本发明中,所述还原剂优选包括连二亚硫酸钠、亚硫酸钠、锌和醋酸的混合物、氢气或铁,更优选为连二亚硫酸钠、亚硫酸钠或铁。在本发明中,当还原剂为锌和醋酸的混合物时,锌和醋酸会反应生成氢气,生成的氢气为还原剂。在本发明中,所述苯磺酸重氮盐和还原剂的摩尔比优选为1:(3~6),更优选为1:(4~5)。本发明对所述混合的方式无特殊要求只要能够混合均匀即可。在本发明中,所述还原反应的应温度优选为60~80℃,更优选为65~70℃;所述还原反应的时间优选为10~30min,更优选为20~25min。在本发明中,所述还原反应优选伴随搅拌,所述搅拌的转速优选为800~1000r/min,更优选为850~950r/min。
50.在本发明中,所述还原反应优选还包括:
51.将还原反应后体系冷却后调节ph值;
52.将调节ph值后的体系进行过滤,得到粗品;
53.将所述粗品进行重结晶后依次进行过滤和干燥,得到2-甲基-4-氨基苯酚。
54.本发明将还原反应后体系冷却后调节ph值。在本发明中,所述冷却后体系的温度优选为0~4℃,更优选为1~3℃。本发明对所述冷却的方式无特殊限定,只要能够达到所需的温度即可。在本发明中,调节ph值后溶液的ph值优选为6.5~7.5,更优选为6.8~7.2。在本发明中,所述调节ph值的ph值调节剂优选包括碳酸氢钠水溶液,所述碳酸氢钠水溶液优选为碳酸氢钠的饱和水溶液。本发明对所述ph值调节剂的用量无特殊限定,只要能够达到所需的ph值即可。在本发明中,调节ph值后溶液会析出固体。
55.调节ph值后,本发明将调节ph值后的体系进行过滤,得到粗品。本发明对所述过滤无特殊要求,采用本领域常规的方式即可。
56.得到粗品后,本发明将所述粗品进行重结晶后依次进行过滤和干燥,得到2-甲基-4-氨基苯酚。在本发明中,所述重结晶用溶剂优选包括石油醚。在本发明中,所述粗品的质量和石油醚的体积比优选为1g:(0.5~1)ml,更优选为1g:(0.6~0.8)ml。本发明对所述过滤无特殊要求,采用本领域常规的方式即可。在本发明中,所述干燥优选为旋蒸,所述旋蒸
的温度优选为35~45℃,更优选为37~40℃。本发明对所述旋蒸的时间无特殊要求,只要能够除去过滤得到的固体表面的石油醚即可。
57.本发明还提供了一种2-甲基-4-(boc-氨基)-苯酚的制备方法,包括以下步骤:
58.将2-甲基-4-氨基苯酚、boc酸酐溶解于有机溶剂,进行酰胺化反应,得到2-甲基-4-(boc-氨基)-苯酚;所述2-甲基-4-氨基苯酚为按照上述技术方案所述制备方法制备得到的2-甲基-4-氨基苯酚。
59.在本发明中,所述溶解优选包括以下步骤:
60.将2-甲基-4-氨基苯酚第一溶解于有机溶剂,得到第一溶液;
61.将boc酸酐溶解于第一溶液,得到待反应溶液。
62.在本发明中,所述有机溶剂优选包括二氯甲烷、氯仿、乙腈或四氢呋喃,更优选为二氯甲烷或四氢呋喃。在本发明中,所述2-甲基-4-氨基苯酚的质量和有机溶剂的体积比优选为1g:(10~17)ml,更优选为1g:(12~15)ml。在本发明中,所述2-甲基-4-氨基苯酚和boc酸酐的摩尔比优选为1:(0.9~2),更优选为1:(1~1.5)。在本发明中,所述第一溶解和第二溶解独立的优选在冰浴条件下进行。本发明对所述第一溶解和第二溶解无特殊限定,只要能够充分溶解即可。
63.在本发明中,所述酰胺化反应的温度优选为25~40℃,更优选为30~38℃;所述酰胺化反应的时间优选为1~3h,更优选为1.5~2h。
64.在本发明中,所述酰胺化反应后优选还包括:
65.将所述酰胺化反应后的体系浓缩后进行萃取,得到有机相;
66.将所述有机相脱水后结晶,得到粗品;
67.将所述粗品进行重结晶后依次进行过滤和干燥,得到所述2-甲基-4-(boc-氨基)-苯酚。
68.本发明将所述酰胺化反应后的体系浓缩后进行萃取,得到有机相。在本发明中,所述浓缩优选在旋蒸的条件下进行,所述旋蒸的温度优选为35~45℃,更优选为38~40℃;所述旋蒸的时间优选为10~30min,更优选为15~20min。在本发明中,所述旋蒸后得到的液体为红色液体。在本发明中,所述萃取用萃取剂优选包括乙酸乙酯,所述有机相和萃取剂的体积比优选为1:(2~4),更优选为1:(2.5~3)。
69.得到有机相后,本发明将所述有机相脱水后结晶,得到粗品。本发明在脱水前优选还包括:将有机相进行洗涤,所述洗涤用溶剂优选包括盐酸水溶液和碳酸氢钠水溶液的混合溶液,所述盐酸水溶液的质量浓度优选为10~20%,更优选为13~18%;所述碳酸氢钠水溶液优选为饱和溶液。在本发明中,所述盐酸水溶液和碳酸氢钠水溶液的体积比优选为1:1。在本发明中,所述洗涤为将有机相、盐酸水溶液和碳酸氢钠水溶液混合后将有机相分离出来。在本发明中,所述脱水用脱水剂优选为无水硫酸钠,所述无水硫酸钠的质量和溶液的体积比优选为(0.5~1)g:1ml,更优选为(0.6~0.8)g:1ml。在本发明中,脱水后优选包括过滤。本发明对所述过滤无特殊限定,采用本领域常规的过滤方式即可。本发明经过过滤除去脱水剂。在本发明中,所述结晶优选为冷却结晶,所述冷却结晶的温度优选为0~4℃,所述冷却结晶的时间优选为5~7h,更优选为6h。
70.得到粗品后,本发明将所述粗品进行重结晶后依次进行过滤和干燥,得到所述2-甲基-4-(boc-氨基)-苯酚。在本发明中,所述重结晶用溶剂优选包括石油醚,所述粗品的质
量和石油醚的体积比优选为1g:(0.5~1)ml,更优选为1g:(0.6~0.8)ml。本发明对所述过滤无特殊限定,采用本领域常规的过滤方式即可。在本发明中,所述干燥优选为旋蒸,所述旋蒸的温度优选为35~45℃,更优选为35~40℃。本发明对所述旋蒸的时间没有特殊要求,只要将过滤得到的固体表面的石油醚去除即可。在本发明中,所述2-甲基-4-(boc-氨基)-苯酚为白色晶体。
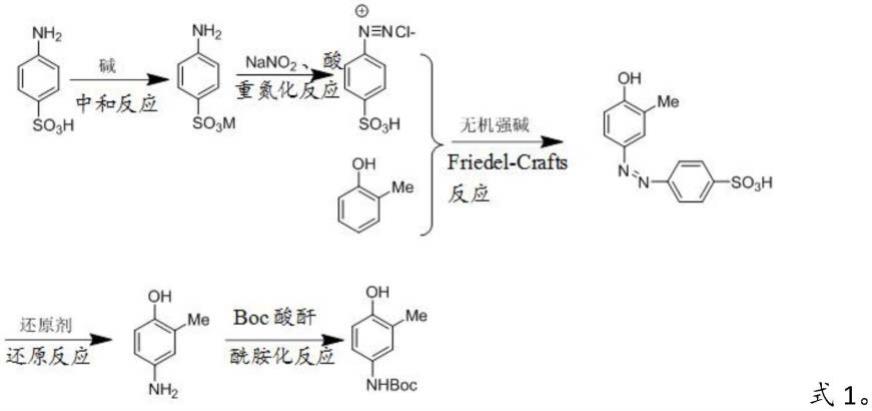
71.在本发明中,制备2-甲基-4-(boc-氨基)-苯酚的反应方程式如式1所示:
[0072][0073]
本发明提供的制备方法操作简单,反应条件温和,副反应少,产品纯化容易;按照本发明的方法制备得到的2-甲基-4-(boc-氨基)-苯酚具有较高的纯度和收率;本发明提供的制备方法原料易得、合成路径短,适合工业化生产。
[0074]
为了进一步说明本发明,下面结合实施例对本发明提供的技术方案进行详细地描述,但不能将它们理解为对本发明保护范围的限定。
[0075]
实施例1
[0076]
将4.5g碳酸钠溶解于100ml水,得到摩尔浓度为0.4mol/l的碳酸钠水溶液;将15g(0.087mol)对氨基苯磺酸溶解于所述碳酸钠水溶液中,25℃中和反应10min后冷却至0℃;将冷却后溶液和15ml质量浓度为0.41g/ml的亚硝酸钠水溶液混合,15℃重氮化反应1h后和100g冰、12ml摩尔浓度为3mol/l的盐酸水溶液混合后过滤,利用去离子水将过滤得到的固体进行洗涤(过滤得到的固体的质量和洗涤剂的体积比为1g:2.5ml),得到苯磺酸重氮盐;
[0077]
将1.5g氢氧化钠溶解于100ml水,得到质量浓度为0.375mol/l的氢氧化钠水溶液中;将9.1g(0.08mol)邻甲苯酚溶解于所述氢氧化钠水溶液后冷却至0℃,和8.5g苯磺酸重氮盐混合,10℃进行friedel-crafts反应(伴随转速为800r/min的搅拌)4h,得到偶氮化合物;
[0078]
将所述偶氮化合物和33g连二亚硫酸钠混合,60℃还原反应(伴随转速为800r/min的搅拌)20min后冷却至0℃后和利用饱和nahco3溶液调ph值为7,过滤,将过滤得到的固体溶解于5ml石油醚进行重结晶,将重结晶得到的固体35℃旋蒸,得到2-甲基-4-氨基苯酚;
[0079]
在冰浴条件下,将2.3g 2-甲基-4-氨基苯酚(0.019mol)溶解于30ml四氢呋喃,得到第一溶液;将5.4g boc酸酐(0.025mol)溶解于第一溶液,35℃酰胺化反应1h后35℃旋蒸20min,将旋蒸后红色液体和20ml乙酸乙酯混合进行萃取,得到有机相;分别利用10ml质量浓度为13%的盐酸溶液和10ml饱和nahco3溶液对所述有机相洗涤,分离得到有机相;用20g
无水硫酸钠对得到的有机相进行脱水后过滤;将过滤得到的滤液冷却至0℃结晶6h,得到粗品;将所述粗品溶解于15ml石油醚进行重结晶,将重结晶得到的固体35℃旋蒸,得到2-甲基-4-(boc-氨基)-苯酚。
[0080]
实施例2
[0081]
将10g碳酸钾溶解于200ml水,得到摩尔浓度为0.35mol/l的碳酸钾水溶液;将33g(0.19mol)对氨基苯磺酸溶解于所述碳酸钾水溶液中,25℃中和反应20min后冷却至3℃;将冷却后溶液和35ml质量浓度为0.39g/ml的亚硝酸钠水溶液混合,10℃重氮化反应1.5h后和200g冰、30ml摩尔浓度为4mol/l的硫酸水溶液混合后过滤,利用去离子水将过滤得到的固体进行洗涤(过滤得到的固体的质量和洗涤剂的体积比为1g:2.5ml),得到苯磺酸重氮盐;
[0082]
将2.5g氢氧化钾溶解于200ml水,得到质量浓度为0.22mol/l的氢氧化钾水溶液中;将20g(0.185mol)邻甲苯酚溶解于所述氢氧化钾水溶液后冷却至3℃,和18g苯磺酸重氮盐混合,5℃进行friedel-crafts反应(伴随转速为850r/min的搅拌)5h,得到偶氮化合物;
[0083]
将所述偶氮化合物和75g亚硫酸钠混合,70℃还原反应(伴随转速为850r/min的搅拌)30min后冷却至4℃后和利用饱和nahco3溶液调ph值为6.5,过滤,将过滤得到的固体溶解于15ml石油醚进行重结晶,将重结晶得到的固体37℃旋蒸,得到2-甲基-4-氨基苯酚;
[0084]
在冰浴条件下,将5g 2-甲基-4-氨基苯酚(0.04mol)溶解于60ml二氯甲烷,得到第一溶液;将12g boc酸酐(0.055mol)溶解于第一溶液,35℃酰胺化反应1h后40℃旋蒸10min,将旋蒸后红色液体和20ml乙酸乙酯混合进行萃取,得到有机相;分别利用10ml质量浓度为15%的盐酸溶液和10ml饱和nahco3溶液对所述有机相洗涤,分离得到有机相;用20g无水硫酸钠对得到的有机相进行脱水后过滤;将过滤得到的滤液冷却至0℃结晶6h,得到粗品;将所述粗品溶解于15ml石油醚进行重结晶,将重结晶得到的固体35℃旋蒸,得到2-甲基-4-(boc-氨基)-苯酚。
[0085]
实施例3
[0086]
将0.6g碳酸氢钠溶解于10ml水,得到摩尔浓度为0.71mol/l的碳酸氢钠水溶液;将1.5g(0.0087mol)对氨基苯磺酸溶解于所述碳酸氢钠水溶液中,25℃中和反应10min后冷却至0℃;将冷却后溶液和2ml质量浓度为0.4g/ml的亚硝酸钠水溶液混合,12℃重氮化反应1h后和10g冰、2ml摩尔浓度为2mol/l的过氯酸水溶液混合后过滤,利用去离子水将过滤得到的固体进行洗涤(过滤得到的固体的质量和洗涤剂的体积比为1g:2.5ml),得到苯磺酸重氮盐;
[0087]
将0.3g氢氧化钾溶解于10ml水,得到质量浓度为0.54mol/l的氢氧化钾水溶液中;将1g(0.0093mol)邻甲苯酚溶解于所述氢氧化钾水溶液后冷却至5℃,和0.7g苯磺酸重氮盐混合,8℃进行friedel-crafts反应(伴随转速为900r/min的搅拌)3h,得到偶氮化合物;
[0088]
将所述偶氮化合物和2g锌粉和5ml醋酸混合,65℃还原反应(伴随转速为900r/min的搅拌)20min后冷却至0℃后和利用饱和nahco3溶液调ph值为6.8,过滤,将过滤得到的固体溶解于2ml石油醚进行重结晶,将重结晶得到的固体35℃旋蒸,得到2-甲基-4-氨基苯酚;
[0089]
在冰浴条件下,将0.3g 2-甲基-4-氨基苯酚(0.0025mol)溶解于5ml氯仿,得到第一溶液;将0.5g boc酸酐(0.0023mol)溶解于第一溶液,38℃酰胺化反应1.5h后40℃旋蒸10min,将旋蒸后红色液体和2ml乙酸乙酯混合进行萃取,得到有机相;分别利用2ml质量浓度为18%的盐酸溶液和2ml饱和nahco3溶液对所述有机相洗涤,分离得到有机相;用3g无水
硫酸钠对得到的有机相进行脱水后过滤;将过滤得到的滤液冷却至4℃结晶6h,得到粗品;将所述粗品溶解于2ml石油醚进行重结晶,将重结晶得到的固体35℃旋蒸,得到2-甲基-4-(boc-氨基)-苯酚。
[0090]
实施例4
[0091]
将2.5g氢氧化钠溶解于50ml水,得到摩尔浓度为1.25mol/l的氢氧化钠水溶液;将8g(0.05mol)对氨基苯磺酸溶解于所述氢氧化钠水溶液中,25℃中和反应15min后冷却至-3℃;将冷却后溶液和8ml质量浓度为0.25g/ml的亚硝酸钠水溶液混合,18℃重氮化反应2h后和50g冰、6ml摩尔浓度为5mol/l的氟硼酸水溶液混合后过滤,利用去离子水将过滤得到的固体进行洗涤(过滤得到的固体的质量和洗涤剂的体积比为1g:2.5ml),得到苯磺酸重氮盐;
[0092]
将0.8g氢氧化钠溶解于50ml水,得到质量浓度为0.4mol/l的氢氧化钠水溶液中;将5g(0.046mol)邻甲苯酚溶解于所述氢氧化钠水溶液后冷却至0℃,和4.5g苯磺酸重氮盐混合,15℃进行friedel-crafts反应(伴随转速为950r/min的搅拌)6h,得到偶氮化合物;
[0093]
将所述偶氮化合物和25g铁混合,80℃还原反应(伴随转速为950r/min的搅拌)25min后冷却至0℃后和利用饱和nahco3溶液调ph值为7.2,过滤,将过滤得到的固体溶解于3ml石油醚进行重结晶,将重结晶得到的固体40℃旋蒸,得到2-甲基-4-氨基苯酚;
[0094]
在冰浴条件下,将1.5g 2-甲基-4-氨基苯酚(0.012mol)溶解于15ml四氢呋喃,得到第一溶液;将3g boc酸酐(0.014mol)溶解于第一溶液,35℃酰胺化反应2h后38℃旋蒸30min,将旋蒸后红色液体和20ml乙酸乙酯混合进行萃取,得到有机相;分别利用5ml质量浓度为20%的盐酸溶液和5ml饱和nahco3溶液对所述有机相洗涤,分离得到有机相;用15g无水硫酸钠对得到的有机相进行脱水后过滤;将过滤得到的滤液冷却至0℃结晶6h,得到粗品;将所述粗品溶解于8ml石油醚进行重结晶,将重结晶得到的固体35℃旋蒸,得到2-甲基-4-(boc-氨基)-苯酚。
[0095]
实施例5
[0096]
将5.5g碳酸钠溶解于500ml水,得到摩尔浓度为0.42mol/l的碳酸钠水溶液;将75g(0.433mol)对氨基苯磺酸溶解于所述碳酸钠水溶液中,25℃中和反应30min后冷却至0℃;将冷却后溶液和75ml质量浓度为0.41g/ml的亚硝酸钠水溶液混合,15℃重氮化反应3h后和500g冰、60ml摩尔浓度为4mol/l的盐酸水溶液混合后过滤,利用去离子水将过滤得到的固体进行洗涤(过滤得到的固体的质量和洗涤剂的体积比为1g:2.5ml),得到苯磺酸重氮盐;
[0097]
将7.5g氢氧化钠溶解于500ml水,得到质量浓度为0.375mol/l的氢氧化钠水溶液中;将45g(0.42mol)邻甲苯酚溶解于所述氢氧化钠水溶液后冷却至0℃,和43g苯磺酸重氮盐混合,10℃进行friedel-crafts反应(伴随转速为1000r/min的搅拌)7h,得到偶氮化合物;
[0098]
将所述偶氮化合物和16g连二亚硫酸钠混合,60℃还原反应(伴随转速为1000r/min的搅拌)30min后冷却至0℃后和利用饱和nahco3溶液调ph值为7,过滤,将过滤得到的固体溶解于25ml石油醚进行重结晶,将重结晶得到的固体35℃旋蒸,得到2-甲基-4-氨基苯酚;
[0099]
在冰浴条件下,将12g 2-甲基-4-氨基苯酚(0.097mol)溶解于150ml四氢呋喃,得到第一溶液;将30g boc酸酐(0.14mol)溶解于第一溶液,35℃酰胺化反应1h后35℃旋蒸
30min,将旋蒸后红色液体和100ml乙酸乙酯混合进行萃取,得到有机相;分别利用50ml质量浓度为15%的盐酸溶液和50ml饱和nahco3溶液对所述有机相洗涤,分离得到有机相;用100g无水硫酸钠对得到的有机相进行脱水后过滤;将过滤得到的滤液冷却至0℃结晶8h,得到粗品;将所述粗品溶解于70ml石油醚进行重结晶,将重结晶得到的固体35℃旋蒸,得到2-甲基-4-(boc-氨基)-苯酚。
[0100]
实施例6
[0101]
将5g氢氧化钾溶解于100ml水,得到摩尔浓度为0.089mol/l的氢氧化钾水溶液;将17g(0.098mol)对氨基苯磺酸溶解于所述氢氧化钾水溶液中,25℃中和反应15min后冷却至0℃;将冷却后溶液和15ml质量浓度为0.53g/ml的亚硝酸钠水溶液混合,15℃重氮化反应1h后和100g冰、14ml摩尔浓度为3mol/l的盐酸水溶液混合后过滤,利用去离子水将过滤得到的固体进行洗涤(过滤得到的固体的质量和洗涤剂的体积比为1g:2.5ml),得到苯磺酸重氮盐;
[0102]
将2g氢氧化钠溶解于100ml水,得到质量浓度为0.5mol/l的氢氧化钠水溶液中;将11g(0.1mol)邻甲苯酚溶解于所述氢氧化钠水溶液后冷却至0℃,和9g苯磺酸重氮盐混合,10℃进行friedel-crafts反应(伴随转速为900r/min的搅拌)4h,得到偶氮化合物;
[0103]
将所述偶氮化合物和40g连二亚硫酸钠混合,80℃还原反应(伴随转速为900r/min的搅拌)20min后冷却至0℃后和利用饱和nahco3溶液调ph值为7.5,过滤,将过滤得到的固体溶解于5ml石油醚进行重结晶,将重结晶得到的固体35℃旋蒸,得到2-甲基-4-氨基苯酚;
[0104]
在冰浴条件下,将2.5g 2-甲基-4-氨基苯酚(0.02mol)溶解于30ml四氢呋喃,得到第一溶液;将6g boc酸酐(0.027mol)溶解于第一溶液,35℃酰胺化反应2h后40℃旋蒸20min,将旋蒸后红色液体和20ml乙酸乙酯混合进行萃取,得到有机相;分别利用10ml质量浓度为17%的盐酸溶液和10ml饱和nahco3溶液对所述有机相洗涤,分离得到有机相;用20g无水硫酸钠对得到的有机相进行脱水后过滤;将过滤得到的滤液冷却至0℃结晶6h,得到粗品;将所述粗品溶解于15ml石油醚进行重结晶,将重结晶得到的固体35℃旋蒸,得到2-甲基-4-(boc-氨基)-苯酚。
[0105]
利用核磁仪对实施例1制备得到的2-甲基-4-(boc-氨基)-苯酚进行检测,得到2-甲基-4-(boc-氨基)-苯酚的1h-nmr谱图,如图1所示。由图1可知,按照本发明制备得到的产品为2-甲基-4-(boc-氨基)-苯酚。
[0106]
利用液相色谱检测实施例1~6制备得到的苯磺酸重氮盐、2-甲基-4-氨基苯酚和2-甲基-4-(boc-氨基)-苯酚的产率和纯度,其结果列于表1中。
[0107]
表1实施1~6制备得到的产物的产率和纯度
[0108][0109][0110]
由表1可知,按照本发明提供的制备方法制备得到的2-甲基-4-(boc-氨基)-苯酚具有较高的产率和纯度。
[0111]
尽管上述实施例对本发明做出了详尽的描述,但它仅仅是本发明一部分实施例,而不是全部实施例,人们还可以根据本实施例在不经创造性前提下获得其他实施例,这些实施例都属于本发明保护范围。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。